一种高性能CO氧化和NOx消除储氧材料的制备方法与流程
本发明属于复合纳米材料技术领域,具体涉及一种高性能的CO氧化和NOx消除储氧材料的制备方法。
背景技术:
具有介孔结构的Cu-Mn-O复合氧化物催化剂对一氧化碳和氮氧化物有着比较好的催化消除特性,MnOx和含Mn材料由于其独特的储氧性能及高孔洞率,被广泛用于汽车尾气三效催化、水煤气的催化变换和CO、苯甲醇等的催化氧化等。在催化材料领域扮演着极为重要的角色。
过渡元素锰的外层电子结构为3d54s2,有+4、+3和+2三种化学价态,而且其标准还原电位较低,易实现各化学价态离子间的相互转换,储存或释放氧。但纯MnOx氧化物由于其微观结构极其不稳定且储放氧主要依赖其表面进行,在高温下易烧结造成其比表面积迅速减小,从而导致储氧能力下降。
氧化铜和氧化锰的混合物是良好的氧化还原反应催化剂,CuO具有比较高的热稳定性,同时因其是一个CO、NOx等气体催化消除中的活性组分,在氧化锰中加入氧化铜可形成尖晶石型氧化物,从而增加表面氧的稳定性以及催化剂的吸氧能力和供氧能力,有利于氧化反应的进行,从而制备得到一种高性能的CO氧化和NOx消除储氧材料。
公开于该背景技术部分的信息仅仅旨在增加对本发明的总体背景的理解,而不应当被视为承认或以任何形式暗示该信息构成已为本领域一般技术人员所公知的现有技术。
技术实现要素:
本发明针对上述技术问题,发明一种高性能CO氧化和NOx消除储氧材料的制备方法,本发明方法成本低,操作简便安全,反应周期短,产品重复性好。
为实现上述目的,本发明提供的技术方案如下:
一种高性能CO氧化和NOx消除储氧材料的制备方法,包含以下操作步骤:
(1)硝酸锰溶液和柠檬酸溶液混合,得到混合溶液A;
(2)向步骤(1)所得混合溶液A中滴加高锰酸钾溶液,滴加完后,分别再加入硝酸铜溶液、脲溶液,加入的各反应物中脲与反应物中来自高锰酸钾和硝酸锰中的锰摩尔比为脲:锰(Mn)=1.2~1.5:1,即n脲:n锰=1.2~1.5:1(n锰=n高锰酸钾+n硝酸锰);
(3)调节步骤(2)所得溶液pH值,搅拌后进行水热反应;
(4)将步骤(3)水热反应后所得物质离心分离,取所得沉淀物依次进行烘干、粉碎、焙烧,即得黑色的Cu-Mn复合氧化物(CuyMn-O),即为产品。
优选的是,步骤(1)中所述的硝酸锰溶液为硝酸锰(Mn(NO3)2)溶于水,形成质量浓度为50%的硝酸锰溶液;所述的柠檬酸溶液为柠檬酸(C6H8O7)溶于水形成浓度为3mol/L的柠檬酸溶液。
优选的是,步骤(2)中高锰酸钾溶于水形成浓度为0.3mol/L的水溶液;所述的硝酸铜溶液为硝酸铜(Cu(NO3)2)溶于水形成浓度为3mol/L的硝酸铜溶液;所述的脲溶液为脲溶于水形成浓度为3mol/L的脲溶液。
优选的是,所述的高锰酸钾、硝酸锰、柠檬酸、脲之间的摩尔比为高锰酸钾:硝酸锰:柠檬酸:脲=2:1:3.6~4.5:3.6~4.5。
优选的是,所述的高锰酸钾、硝酸锰、柠檬酸、脲之间的摩尔比为高锰酸钾:硝酸锰:柠檬酸:脲=2:1:4.5:4.5。
优选的是,步骤(2)中加入的硝酸铜与混合溶液A中的高锰酸钾和硝酸锰反应后得到的锰氧化物(MnOx)成摩尔比0~0.2:1,即Cu:Mn(高锰酸钾+硝酸锰)=0~0.2:1。
优选的是,步骤(3)中用质量浓度为25%的氨水调节步骤(2)所得溶液pH值为6~7。
优选的是,步骤(3)中搅拌4h,在180℃下进行水热反应12h。
优选的是,步骤(4)中所得沉淀物80℃下烘干12h后粉碎,然后在350℃下焙烧4h。
与现有技术相比,本发明具有如下有益效果:
本发明高性能CO氧化和NOx消除储氧材料的制备方法操作简便安全,反应周期短,重复性好,操作工艺参数易控,所得产品采用的材料成本低,活性高,热稳定性高,能够在较低温度下催化还原一氧化碳和氮氧化物,在材料研究、一氧化碳催化氧化以及氮氧化物催化还原中应用良好。
附图说明
图1为本发明所得产品对CO催化转化率的曲线图。
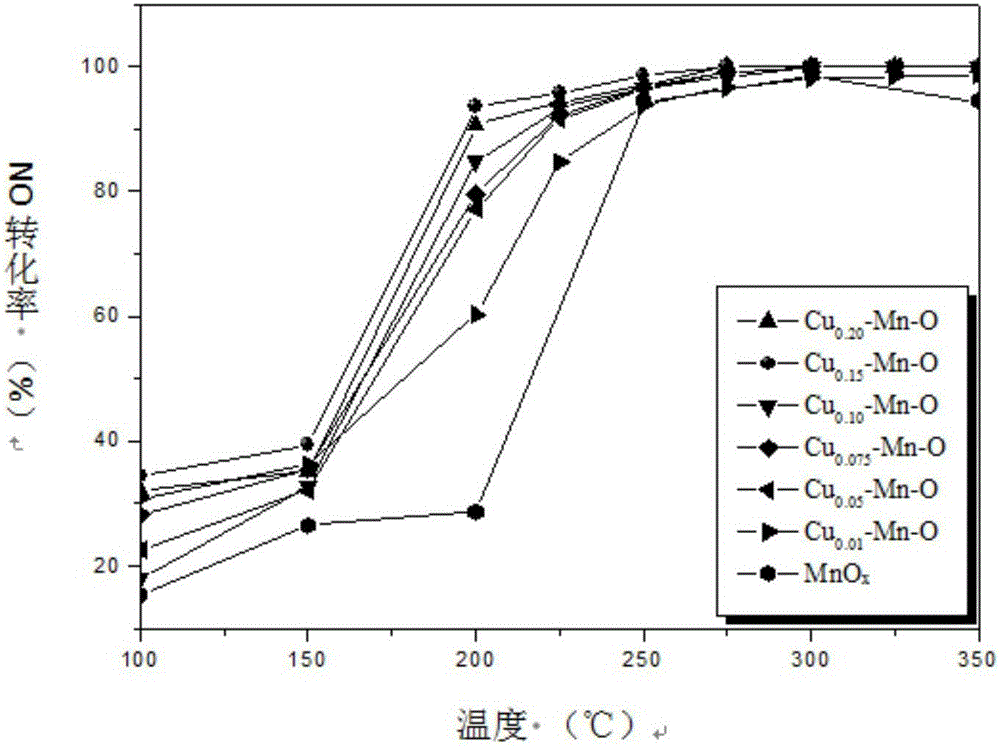
图2为本发明所得产品对NO催化转化率的曲线图。
图3为本发明所得产品对NO催化选择性的曲线图。
图4为本发明所得产品的XRD谱图。
具体实施方式
下面结合附图具体实施方式进行详细描述,但应当理解本发明的保护范围并不受具体实施方式的限制。基于本发明中的实施例,本领域普通技术人员在没有作出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。实施例中所用到的各原料,皆为市售所得,其中硝酸铜采用的是三水硝酸铜,柠檬酸采用的是一水柠檬酸。
实施例1
称取各反应物配备:称取1.8964g的高锰酸钾固体于烧杯X中,并溶于40mL去离子水中,得到0.3mol/L高锰酸钾溶液;称取硝酸锰溶于去离子水,形成质量浓度为50%的硝酸锰溶液,备用;称取5.6738g的一水柠檬酸溶于去离子水中,形成浓度为3mol/L的柠檬酸溶液,备用;称取1.6216g的脲溶于去离子水中,形成浓度为3mol/L的脲溶液,备用;高锰酸钾、硝酸锰、一水柠檬酸、脲之间的摩尔比为高锰酸钾:硝酸锰:一水柠檬酸:脲=2:1:4.5:4.5。
称取2.1474g上述备用的硝酸锰溶液和上述备用的全部柠檬酸溶液(硝酸锰:一水柠檬酸摩尔比例为1:4.5),于烧杯A中混合,得到混合溶液A;边搅拌边向烧杯A中逐渐滴加烧杯X中的高锰酸钾溶液,滴加完毕后,持续搅拌;称取上述备用的全部脲溶液,然后向烧杯A所得溶液中加入称取所得脲溶液;加入的硝酸铜与混合溶液A中的高锰酸钾和硝酸锰反应后得到的锰氧化物(MnOx)成摩尔比0:1,即Cu:Mn(高锰酸钾+硝酸锰)=0:1;加入的各反应物中脲与反应物中来自高锰酸钾和硝酸锰中的锰摩尔比为脲:锰(Mn)=1.5:1,即n脲:n锰=1.5:1(n锰=n高锰酸钾+n硝酸锰)。烧杯A中所得反应液搅拌下以质量浓度为25%的氨水调反应液pH值至6~7,常温下搅拌4h,然后在180℃烘箱中进行水热反应12h,反应结束后,所得物质离心,取离心后所得沉淀物在80℃烘干12h后粉碎,350℃马弗炉中煅烧4h,即可得到黑色的MnOx复合氧化物。
实施例2
称取各反应物配备:称取1.8964g的高锰酸钾固体于烧杯X中,并溶于40mL去离子水中,得到0.3mol/L高锰酸钾溶液;称取硝酸锰溶于去离子水,形成质量浓度为50%的硝酸锰溶液,备用;称取5.6738g的一水柠檬酸溶于去离子水中,形成浓度为3mol/L的柠檬酸溶液,备用;称取0.0435g的三水硝酸铜溶于去离子水中,形成浓度为3mol/L的硝酸铜溶液,备用;称取1.6216g的脲溶于去离子水中,形成浓度为3mol/L的脲溶液,备用;高锰酸钾、硝酸锰、一水柠檬酸、脲之间的摩尔比为高锰酸钾:硝酸锰:一水柠檬酸:脲=2:1:4.5:4.5。
称取2.1474g上述备用的硝酸锰溶液,同时称取上述备用的全部柠檬酸溶液(硝酸锰:一水柠檬酸摩尔比例为1:4.5),于烧杯A中混合,得到混合溶液A;边搅拌边向烧杯A中逐渐滴加烧杯X中的高锰酸钾溶液,滴加完毕后,持续搅拌;称取上述备用的全部硝酸铜溶液和上述备用的全部脲溶液,然后向烧杯A所得溶液中加入称取所得硝酸铜溶液,再加入脲溶液;加入的硝酸铜与混合溶液A中的高锰酸钾和硝酸锰反应后得到的锰氧化物(MnOx)成摩尔比0.01:1,即Cu:Mn(高锰酸钾+硝酸锰)=0.01:1;加入的各反应物中脲与反应物中来自高锰酸钾和硝酸锰中的锰摩尔比为脲:锰(Mn)=1.5:1,即n脲:n锰=1.5:1(n锰=n高锰酸钾+n硝酸锰)。烧杯A中所得反应液搅拌下以质量浓度为25%的氨水调反应液pH值至6~7,常温下搅拌4h,然后在180℃烘箱中进行水热反应12h,反应结束后,所得物质离心,取离心后所得沉淀物在80℃烘干12h后粉碎,350℃马弗炉中煅烧4h,即可得到产品——黑色的Cu-Mn复合氧化物。
实施例3
称取各反应物配备:称取1.8964g的高锰酸钾固体于烧杯X中,并溶于40mL去离子水中,得到0.3mol/L高锰酸钾溶液;称取硝酸锰溶于去离子水,形成质量浓度为50%的硝酸锰溶液,备用;称取5.6738g的一水柠檬酸溶于去离子水中,形成浓度为3mol/L的柠檬酸溶液,备用;称取0.2135g的三水硝酸铜溶于去离子水中,形成浓度为3mol/L的硝酸铜溶液,备用;称取1.6216g的脲溶于去离子水中,形成浓度为3mol/L的脲溶液,备用;高锰酸钾、硝酸锰、一水柠檬酸、脲之间的摩尔比为高锰酸钾:硝酸锰:一水柠檬酸:脲=2:1:4.5:4.5。
称取2.1474g上述备用的硝酸锰溶液和上述备用的全部柠檬酸溶液(硝酸锰:一水柠檬酸摩尔比例为1:4.5),于烧杯A中混合,得到混合溶液A;边搅拌边向烧杯A中逐渐滴加烧杯X中的高锰酸钾溶液,滴加完毕后,持续搅拌;称取上述备用的全部硝酸铜溶液和上述备用的全部脲溶液,然后向烧杯A所得溶液中加入称取所得硝酸铜溶液,再加入脲溶液;加入的硝酸铜与混合溶液A中的高锰酸钾和硝酸锰反应后得到的锰氧化物(MnOx)成摩尔比0.05:1,即Cu:Mn(高锰酸钾+硝酸锰)=0.05:1;加入的各反应物中脲与反应物中来自高锰酸钾和硝酸锰中的锰摩尔比为脲:锰(Mn)=1.5:1,即n脲:n锰=1.5:1(n锰=n高锰酸钾+n硝酸锰)。烧杯A中所得反应液搅拌下以质量浓度为25%的氨水调反应液pH值至6~7,常温下搅拌4h,然后在180℃烘箱中进行水热反应12h,反应结束后,所得物质离心,取离心后所得沉淀物在80℃烘干12h后粉碎,350℃马弗炉中煅烧4h,即可得到产品——黑色的Cu-Mn复合氧化物。
实施例4
称取各反应物配备:称取1.8964g的高锰酸钾固体于烧杯X中,并溶于40mL去离子水中,得到0.3mol/L高锰酸钾溶液;称取硝酸锰溶于去离子水,形成质量浓度为50%的硝酸锰溶液,备用;称取5.6738g的一水柠檬酸溶于去离子水中,形成浓度为3mol/L的柠檬酸溶液,备用;称取0.3262g的三水硝酸铜溶于去离子水中,形成浓度为3mol/L的硝酸铜溶液,备用;称取1.6216g的脲溶于去离子水中,形成浓度为3mol/L的脲溶液,备用;高锰酸钾、硝酸锰、一水柠檬酸、脲之间的摩尔比为高锰酸钾:硝酸锰:一水柠檬酸:脲=2:1:4.5:4.5。
称取2.1474g上述备用的硝酸锰溶液和上述备用的全部柠檬酸溶液(硝酸锰:一水柠檬酸摩尔比例为1:4.5),于烧杯A中混合,得到混合溶液A;边搅拌边向烧杯A中逐渐滴加烧杯X中的高锰酸钾溶液,滴加完毕后,持续搅拌;称取上述备用的全部硝酸铜溶液和上述备用的全部脲溶液,然后向烧杯A所得溶液中加入称取所得硝酸铜溶液,再加入脲溶液;加入的硝酸铜与混合溶液A中的高锰酸钾和硝酸锰反应后得到的锰氧化物(MnOx)成摩尔比0.075:1,即Cu:Mn(高锰酸钾+硝酸锰)=0.075:1;加入的各反应物中脲与反应物中来自高锰酸钾和硝酸锰中的锰摩尔比为脲:锰(Mn)=1.5:1,即n脲:n锰=1.5:1(n锰=n高锰酸钾+n硝酸锰)。烧杯A中所得反应液搅拌下以质量浓度为25%的氨水调反应液pH值至6~7,常温下搅拌4h,然后在180℃烘箱中进行水热反应12h,反应结束后,所得物质离心,取离心后所得沉淀物在80℃烘干12h后粉碎,350℃马弗炉中煅烧4h,即可得到产品——黑色的Cu-Mn复合氧化物。
实施例5
称取各反应物配备:称取1.8964g的高锰酸钾固体于烧杯X中,并溶于40mL去离子水中,得到0.3mol/L高锰酸钾溶液;称取硝酸锰溶于去离子水,形成质量浓度为50%的硝酸锰溶液,备用;称取5.6738g的一水柠檬酸溶于去离子水中,形成浓度为3mol/L的柠檬酸溶液,备用;称取0.4350g的三水硝酸铜溶于去离子水中,形成浓度为3mol/L的硝酸铜溶液,备用;称取1.6216g的脲溶于去离子水中,形成浓度为3mol/L的脲溶液,备用;高锰酸钾、硝酸锰、一水柠檬酸、脲之间的摩尔比为高锰酸钾:硝酸锰:一水柠檬酸:脲=2:1:4.5:4.5。
称取2.1474g上述备用的硝酸锰溶液和上述备用的全部柠檬酸溶液(硝酸锰:一水柠檬酸摩尔比例为1:4.5),于烧杯A中混合,得到混合溶液A;边搅拌边向烧杯A中逐渐滴加烧杯X中的高锰酸钾溶液,滴加完毕后,持续搅拌;称取上述备用的全部硝酸铜溶液和上述备用的全部脲溶液,然后向烧杯A所得溶液中加入称取所得硝酸铜溶液,再加入脲溶液;加入的硝酸铜与混合溶液A中的高锰酸钾和硝酸锰反应后得到的锰氧化物(MnOx)成摩尔比0.1:1,即Cu:Mn(高锰酸钾+硝酸锰)=0.1:1;加入的各反应物中脲与反应物中来自高锰酸钾和硝酸锰中的锰摩尔比为脲:锰(Mn)=1.5:1,即n脲:n锰=1.5:1(n锰=n高锰酸钾+n硝酸锰)。烧杯A中所得反应液搅拌下以质量浓度为25%的氨水调反应液pH值至6~7,常温下搅拌4h,然后在180℃烘箱中进行水热反应12h,反应结束后,所得物质离心,取离心后所得沉淀物在80℃烘干12h后粉碎,350℃马弗炉中煅烧4h,即可得到产品——黑色的Cu-Mn复合氧化物。
实施例6
称取各反应物配备:称取1.8964g的高锰酸钾固体于烧杯X中,并溶于40mL去离子水中,得到0.3mol/L高锰酸钾溶液;称取硝酸锰溶于去离子水,形成质量浓度为50%的硝酸锰溶液,备用;称取5.6738g的一水柠檬酸溶于去离子水中,形成浓度为3mol/L的柠檬酸溶液,备用;称取0.6525g的三水硝酸铜溶于去离子水中,形成浓度为3mol/L的硝酸铜溶液,备用;称取1.6216g的脲溶于去离子水中,形成浓度为3mol/L的脲溶液,备用;高锰酸钾、硝酸锰、一水柠檬酸、脲之间的摩尔比为高锰酸钾:硝酸锰:一水柠檬酸:脲=2:1:4.5:4.5。
称取2.1474g上述备用的硝酸锰溶液和上述备用的全部柠檬酸溶液(硝酸锰:一水柠檬酸摩尔比例为1:4.5),于烧杯A中混合,得到混合溶液A;边搅拌边向烧杯A中逐渐滴加烧杯X中的高锰酸钾溶液,滴加完毕后,持续搅拌;称取上述备用的全部硝酸铜溶液和上述备用的全部脲溶液,然后向烧杯A所得溶液中加入称取所得硝酸铜溶液,再加入脲溶液;加入的硝酸铜与混合溶液A中的高锰酸钾和硝酸锰反应后得到的锰氧化物(MnOx)成摩尔比0.15:1,即Cu:Mn(高锰酸钾+硝酸锰)=0.15:1;加入的各反应物中脲与反应物中来自高锰酸钾和硝酸锰中的锰摩尔比为脲:锰(Mn)=1.5:1,即n脲:n锰=1.5:1(n锰=n高锰酸钾+n硝酸锰)。烧杯A中所得反应液搅拌下以质量浓度为25%的氨水调反应液pH值至6~7,常温下搅拌4h,然后在180℃烘箱中进行水热反应12h,反应结束后,所得物质离心,取离心后所得沉淀物在80℃烘干12h后粉碎,350℃马弗炉中煅烧4h,即可得到产品——黑色的Cu-Mn复合氧化物。
实施例7
称取各反应物配备:称取1.8964g的高锰酸钾固体于烧杯X中,并溶于40mL去离子水中,得到0.3mol/L高锰酸钾溶液;称取硝酸锰溶于去离子水,形成质量浓度为50%的硝酸锰溶液,备用;称取5.6738g的一水柠檬酸溶于去离子水中,形成浓度为3mol/L的柠檬酸溶液,备用;称取0.8700g的三水硝酸铜溶于去离子水中,形成浓度为3mol/L的硝酸铜溶液,备用;称取1.6216g的脲溶于去离子水中,形成浓度为3mol/L的脲溶液,备用;高锰酸钾、硝酸锰、一水柠檬酸、脲之间的摩尔比为高锰酸钾:硝酸锰:一水柠檬酸:脲=2:1:4.5:4.5。
称取2.1474g上述备用的硝酸锰溶液和上述备用的全部柠檬酸溶液(硝酸锰:一水柠檬酸摩尔比例为1:4.5),于烧杯A中混合,得到混合溶液A;边搅拌边向烧杯A中逐渐滴加烧杯X中的高锰酸钾溶液,滴加完毕后,持续搅拌;称取上述备用的全部硝酸铜溶液和上述备用的全部脲溶液,然后向烧杯A所得溶液中加入称取所得硝酸铜溶液,再加入脲溶液;加入的硝酸铜与混合溶液A中的高锰酸钾和硝酸锰反应后得到的锰氧化物(MnOx)成摩尔比0.2:1,即Cu:Mn(高锰酸钾+硝酸锰)=0.2:1;加入的各反应物中脲与反应物中来自高锰酸钾和硝酸锰中的锰摩尔比为脲:锰(Mn)=1.5:1,即n脲:n锰=1.5:1(n锰=n高锰酸钾+n硝酸锰)。烧杯A中所得反应液搅拌下以质量浓度为25%的氨水调反应液pH值至6~7,常温下搅拌4h,然后在180℃烘箱中进行水热反应12h,反应结束后,所得物质离心,取离心后所得沉淀物在80℃烘干12h后粉碎,350℃马弗炉中煅烧4h,即可得到产品——黑色的Cu-Mn复合氧化物。
实施例8
称取各反应物配备:称取1.8964g的高锰酸钾固体于烧杯X中,并溶于40mL去离子水中,得到0.3mol/L高锰酸钾溶液;称取硝酸锰溶于去离子水,形成质量浓度为50%的硝酸锰溶液,备用;称取4.5390g的一水柠檬酸溶于去离子水中,形成浓度为3mol/L的柠檬酸溶液,备用;称取0.0435g的三水硝酸铜溶于去离子水中,形成浓度为3mol/L的硝酸铜溶液,备用;称取1.12973g的脲溶于去离子水中,形成浓度为3mol/L的脲溶液,备用;高锰酸钾、硝酸锰、一水柠檬酸、脲之间的摩尔比为高锰酸钾:硝酸锰:一水柠檬酸:脲=2:1:3.6:3.6。
称取2.1474g上述备用的硝酸锰溶液和上述备用的全部柠檬酸溶液(硝酸锰:一水柠檬酸摩尔比例为1:4.5),于烧杯A中混合,得到混合溶液A;边搅拌边向烧杯A中逐渐滴加烧杯X中的高锰酸钾溶液,滴加完毕后,持续搅拌;称取上述备用的全部硝酸铜溶液和上述备用的全部脲溶液,然后向烧杯A所得溶液中加入称取所得硝酸铜溶液,再加入脲溶液,加入的各反应物中脲与反应物中来自高锰酸钾和硝酸锰中的锰摩尔比为脲:锰(Mn)=1.2:1,即n脲:n锰=1.2:1(n锰=n高锰酸钾+n硝酸锰)。烧杯A中所得反应液搅拌下以质量浓度为25%的氨水调反应液pH值至6~7,常温下搅拌4h,然后在180℃烘箱中进行水热反应12h,反应结束后,所得物质离心,取离心后所得沉淀物在80℃烘干12h后粉碎,350℃马弗炉中煅烧4h,即可得到产品——黑色的Cu-Mn复合氧化物。
实施例9
称取各反应物配备:称取1.8964g的高锰酸钾固体于烧杯X中,并溶于40mL去离子水中,得到0.3mol/L高锰酸钾溶液;称取硝酸锰溶于去离子水,形成质量浓度为50%的硝酸锰溶液,备用;称取4.9173g的一水柠檬酸溶于去离子水中,形成浓度为3mol/L的柠檬酸溶液,备用;称取0.0435g的三水硝酸铜溶于去离子水中,形成浓度为3mol/L的硝酸铜溶液,备用;称取1.4054g的脲溶于去离子水中,形成浓度为3mol/L的脲溶液,备用;高锰酸钾、硝酸锰、一水柠檬酸、脲之间的摩尔比为高锰酸钾:硝酸锰:一水柠檬酸:脲=2:1:3.9:3.9。
称取2.1474g上述备用的硝酸锰溶液和上述备用的全部柠檬酸溶液(硝酸锰:一水柠檬酸摩尔比例为1:4.5),于烧杯A中混合,得到混合溶液A;边搅拌边向烧杯A中逐渐滴加烧杯X中的高锰酸钾溶液,滴加完毕后,持续搅拌;称取上述备用的全部硝酸铜溶液和上述备用的全部脲溶液,然后向烧杯A所得溶液中加入称取所得硝酸铜溶液,再加入脲溶液,加入的各反应物中脲与反应物中来自高锰酸钾和硝酸锰中的锰摩尔比为脲:锰(Mn)=1.3:1,即n脲:n锰=1.3:1(n锰=n高锰酸钾+n硝酸锰)。烧杯A中所得反应液搅拌下以质量浓度为25%的氨水调反应液pH值至6~7,常温下搅拌4h,然后在180℃烘箱中进行水热反应12h,反应结束后,所得物质离心,取离心后所得沉淀物在80℃烘干12h后粉碎,350℃马弗炉中煅烧4h,即可得到产品——黑色的Cu-Mn复合氧化物。
对由实施例1~实施例7得到的Cu-Mn复合氧化物催化剂进行分析,得出表1。
表1
表1为铜锰复合氧化物材料CuyMn-O(y=0~0.2)相应比例下的比表面积和孔径大小,由表1中可以看出,在复合氧化物材料CuyMnO(y=0~0.2)中,铜的掺杂对产品的比表面积和孔径的大小有着显著的影响。综合比较得出比表面积和孔径都比较大的材料,相对应的材料的CO催化氧化性能比较好;但是,样品的比表面积和孔径的大小与其NO催化消除性能关系不大。
检测
将本发明实施例1~7所得产品,分别对CO气体进行催化氧化性能测试实验,其中,以CO气体的流量为10.4mL/min(2vol%CO,氮气作为平衡气)和干燥空气流量为8.2mL/min建立微型反应系统,得出图1中数据。由图1可以看出,当铜锰摩尔比例为0.075时,即Cu0.075Mn-O样品的CO转化率最佳,其在65℃下便可以将CO气体催化完全氧化。
将本发明实施例1~7所得产品,分别进行NO+CO催化反应性能测试实验,其中,以5vol%NO(流量为10mL/min,氦气作为平衡气)和10vol%CO(流量为10mL/min,氦气作为平衡气)建立微型反应系统,得出图2、图3中数据。由图2、3可以看出,当铜锰摩尔比例为0.15时,即Cu0.15Mn-O样品的NO转化率和N2选择性最佳,其在275℃下便可获得100%的NO转化率和93%N2选择性。
将本发明实施例1~7所得产品,分别在PANalytical公司的X’pert PRO型号XRD衍射仪进行X射线粉末衍射(XRD)实验,得出图4中数据。由图4可以看出,催化剂样品主要由β-MnO2晶相和无定形非晶相所构成,而铜的掺杂导致了样品中形成了Cu1.5Mn1.5O4立方尖晶石结构,明显改变了催化剂样品的微观结构,对材料的CO催化氧化性能和NO催化消除性能均有显著的提升。
前述对本发明的具体示例性实施方案的描述是为了说明和例证的目的。这些描述并非想将本发明限定为所公开的精确形式,并且很显然,根据上述教导,可以进行很多改变和变化。对示例性实施例进行选择和描述的目的在于解释本发明的特定原理及其实际应用,从而使得本领域的技术人员能够实现并利用本发明的各种不同的示例性实施方案以及各种不同的选择和改变。本发明的范围意在由权利要求书及其等同形式所限定。
- 还没有人留言评论。精彩留言会获得点赞!