一种微流控芯片及其制备方法与流程
本发明涉及一种微流控芯片及其制备方法,属于芯片检测技术领域。
背景技术:
在正常人体内,有三种血红蛋白:hba、hbf、hba2,而成人红细胞中主要含有hba。在用层析法分离血红蛋白时,可洗脱出3种含糖成分即:hba1a、hba1b、hba1c,合称为糖化血红蛋白。hba1c是葡萄糖化血红蛋白,另两种是其他糖形成的糖化红蛋白。其中hbalc的量最大,反映血糖水平时一般用hbalc表示,hbalc由hba在代谢过程中与葡萄糖结合形成,因而它可准确地反映血中葡萄糖水平。
血糖和血红蛋白的结合生成糖化血红蛋白是不可逆反应,并与血糖浓度成正比,且保持120天左右,所以可以观测到120天之前的血糖浓度。糖化血红蛋白测试通常可以反映患者近8~12周的血糖控制情况。
检测糖化血红蛋白的意义在于,其反映糖尿病患者血糖总体控制情况的指标;糖化血红蛋白正常值为4-6%,<6%控制偏低,易出现低血糖;6-7%控制理想;7-8%可以接受;8-9%为控制不好;>9%为控制差,是慢性并发症的发生、发展的危险因素,并可能发生酮症酸中毒等急性合并症,所以当其>8%就应该加强血糖的控制。
现有技术对糖化血红蛋白的诊断方法具有灵敏度低、重复性差、受干扰明显,以及现有糖化血红蛋白检测配套仪器昂贵、检测流程复杂、检测时间长的问题。
技术实现要素:
为了克服现有技术的不足,本发明的第一个目的在于提供一种微流控芯片,该微流控芯片以透射比浊法为基础,通过微流控芯片技术实现样本中待测成分含量的快速定量检测,具有容易操作、高灵敏度、结果准确的特点。
本发明的第二个目的在于提供一种上述微流控芯片的制备方法。
实现本发明的第一个目的可以通过采取如下技术方案达到:一种微流控芯片,包括基板、取样件和底盖;底盖盖设在基板的下方;基板上设有进样腔、预处理区、检测腔和反应区;取样件以可拆卸的方式嵌设在进样腔中;取样件包括进样口、样本容置腔和出样口;进样口、出样口分别和样本容置腔连通;预处理区包括预处理试剂腔、预处理腔和气腔;预处理试剂腔通过第一预处理区流道与进样腔连通,进样腔通过第二预处理区流道和预处理腔相对应;取样件嵌设在进样腔时,第一预处理区流道的出口与进样口相对应,第二预处理区流道的入口与出样口相对应;预处理腔通过流道与检测腔相连通;气腔通过气道与预处理腔连通;反应区包括反应试剂腔和反应腔;检测腔通过流道与反应腔相连通;反应试剂腔通过流道与反应腔连通;预处理试剂腔、气腔、反应试剂腔和反应腔上均设有弹性腔壁;检测腔的上表面设有透光面板,下表面设有透光底板;透光面板和透光底板相对应;底盖的底面设有与透光底板相对应的通孔。
进一步地,预处理试剂腔包括第一预处理试剂腔和第二预处理试剂腔,第一预处理试剂腔通过第一预处理区流道与进样腔连通;第二预处理试剂腔通过流道与预处理腔连通。
进一步地,第一预处理试剂腔中注有溶血剂;第二预处理试剂腔中注有胶乳粒子悬浊液。
进一步地,胶乳粒子悬浊液通过以下步骤制备得到:
预处理:在甘氨酸缓冲液中加入粒径200-400nm的聚苯乙烯微球和1-乙基-(3-二甲基氨基丙基)碳二亚胺盐酸盐,在20-25℃的条件下反应2-3h,然后离心、混匀,反复离心和混匀操作,最后一次离心操作后弃上清,得到沉淀的聚苯乙烯微球;
制备悬浊液:将经预处理的聚苯乙烯微球分散于含有血红蛋白吸附剂的溶液中,用甘氨酸缓冲液调整溶液的ph=8,然后在20-25℃的条件下避光封闭至少24h,得到聚苯乙烯微球悬浊液。
进一步地,聚苯乙烯微球悬浊液中,聚苯乙烯微球的质量百分比为3%。
进一步地,反应试剂腔包括第一反应试剂腔和第二反应试剂腔;第一反应试剂腔和第二反应试剂腔分别通过流道与反应腔连通。
进一步地,第一反应试剂腔中注有第一反应试剂;第一反应试剂含有鼠抗hba1c单抗;第二反应试剂腔中注有第二反应试剂;第二反应试剂含有羊抗鼠igg抗体。
进一步地,底盖和基板之间设有废液腔;检测腔通过流道与废液腔连通。为了在检测时,待测溶液充满检测腔,以使得入射光线能够穿射待测溶液,准确测出吸光度,则待测溶液充满检测腔时,可将多余的待测溶液压进废液腔中,也可推出检测腔中的气泡。
实现本发明的第二个目的可以通过采取如下技术方案达到:一种如上所述的微流控芯片的制备方法,包括以下步骤:
制备试剂:分别制备预处理试剂和反应试剂;
组装芯片:将预处理试剂注入预处理试剂腔,反应试剂注入反应试剂腔,密封基板,安装底板,完成组装。
进一步地,组装芯片步骤中,使用胶带密封基板。
本发明的配方设计原理如下:以透射比浊法为基础,将样本中的待测成分和能够与之反应而产生悬浮物的试剂进行反应,使得溶液混浊,混浊程度与形成的悬浮物数量成正比,也与待测成分含量成正比;测定其悬浊液的吸光度,可求出样本中待测成分的含量。
相比现有技术,本发明的有益效果在于:
1、本发明的微流控芯片以透射比浊法为基础,通过微流控芯片技术实现样本中待测成分的快速定量检测,能够针对性地设置能够与待测成分产生悬浮颗粒的试剂,在检测腔中设置透光面板和透光底板,可检测入射光和出射光的强度,计算待测成分的含量,具有容易操作,自动扣除了空白干扰,具有背景影响低、高灵敏度、结果准确的特点;
2、本发明的微流控芯片技术,把样本预处理、混合、反应、分离和检测集成在芯片上,并把反应所需的所有试剂组分集成到芯片上;操作简便,可完成整套检测,检测效率大大提高。
附图说明
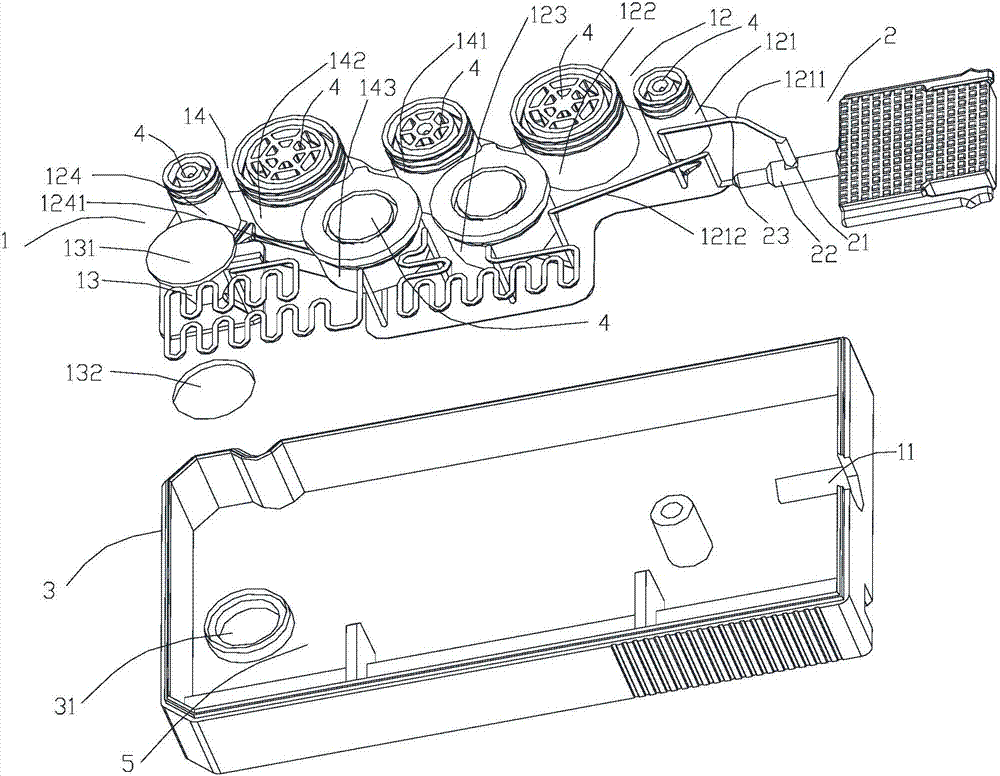
图1为本发明微流控芯片的结构示意图;
图中,1、基板;11、进样腔;12、预处理区;121、第一预处理试剂腔;1211、第一预处理区流道;1212、第二预处理区流道;122、第二预处理试剂腔;123、预处理腔;124、气腔;1241、气道;13、检测腔;131、透光面板;132、透光底板;14、反应区;141、第一反应试剂腔;142、第二反应试剂腔;143、反应腔;2、取样件;21、进样口;22、样本容置腔;23、出样口;3、底盖;31、通孔;4、弹性腔壁;5、废液腔。
具体实施方式
下面,结合附图以及具体实施方式,对本发明做进一步描述:
实施例1:
微流控芯片的制备及用于测定hba1c。
一、芯片结构:
参照图1,一种微流控芯片,包括基板1、取样件2和底盖3;底盖3盖设在基板1的下方;基板1上设有进样腔11、预处理区12、检测腔13和反应区14;取样件2以可拆卸的方式嵌设在进样腔11中;取样件2包括进样口21、样本容置腔22和出样口23;进样口21、出样口23分别和样本容置腔22连通;预处理区12包括第一预处理试剂腔121、第二预处理试剂腔122、预处理腔123和气腔124;第一预处理试剂腔121通过第一预处理区流道1211与进样腔11连通,进样腔11通过第二预处理区流道1212和预处理腔123相对应,第二预处理试剂腔122通过流道与预处理腔123连通;取样件2嵌设在进样腔11时,第一预处理区流道1211的出口与进样口21相对应,第二预处理区流道1212的入口与出样口23相对应;预处理腔123通过流道与检测腔13相连通;气腔124通过气道1241与预处理腔123连通;反应区14包括第一反应试剂腔141、第二反应试剂腔142和反应腔143;检测腔13通过流道与反应腔143相连通;第一反应试剂腔141和第二反应试剂腔142分别通过流道与反应腔143连通;第一预处理试剂腔121、第二预处理试剂腔122、气腔124、第一反应试剂腔141、第二反应试剂腔142和反应腔143上均设有弹性腔壁4;检测腔13的上表面设有透光面板131,下表面设有透光底板132;透光面板131和透光底板132相对应;底盖3的底面设有与透光底板132相对应的通孔31;底盖3和基板1之间设有废液腔5;检测腔13通过流道与废液腔5连通。
上述中的流道、第一预处理区流道和第二预处理区流道均为常规技术中的芯片流道,作用为连通两个腔室,是试剂从一个腔室流至另一个腔室的通道;气道为常规技术中供气体通过的通道,连通气腔和预处理腔。
二、注入试剂:
作为检测糖化血红蛋白,需要在第一预处理试剂腔、第二预处理试剂腔、第一反应试剂腔、第二反应试剂腔注入相应的试剂:
第一预处理试剂腔中注有溶血剂;溶血剂包括:nacl、十四烷基三甲基溴化铵(ttab)表面活性剂和稳定剂;溶血剂用于破碎血细胞,释放血细胞中的血红蛋白和糖化血红蛋白;
第二预处理试剂腔中注有胶乳粒子悬浊液;
胶乳粒子悬浊液为聚苯乙烯微球悬浊液,通过以下步骤制备得到:
预处理:在浓度为100mmol/l的甘氨酸缓冲液中加入粒径200-400nm的聚苯乙烯微球,聚苯乙烯微球的质量百分比为3%,和浓度为0.5mg/ml的1-乙基-(3-二甲基氨基丙基)碳二亚胺盐酸盐,在23℃的条件下反应2.5h,然后转速10000rmp的条件下离心15min、混匀,反复离心和混匀操作,最后一次在转速15000rmp的条件下离心25min操作后弃上清,得到沉淀的聚苯乙烯微球;
制备悬浊液:将经预处理的聚苯乙烯微球分散于含有血红蛋白吸附剂的溶液中,溶液中聚苯乙烯微球的质量百分比为3%,甘氨酸缓冲液调整溶液的ph=8,然后在23℃的条件下避光封闭24h,得到聚苯乙烯微球悬浊液。
第一反应试剂腔中注有第一反应试剂;第一反应试剂含有鼠抗hba1c单抗;
第一反应试剂通过以下步骤制备得到:在浓度为50mmol/l的甘氨酸缓冲液中加入鼠抗hba1c单抗,配置鼠抗hba1c单抗试剂,试剂中抗体的终浓度大于0.5mg/ml;
第二反应试剂腔中注有第二反应试剂;第二反应试剂含有羊抗鼠igg抗体;
第二反应试剂通过以下步骤制备得到:在浓度为50mmol/l的甘氨酸缓冲液中加入羊抗鼠igg抗体,配置成试剂羊抗鼠igg抗体试剂,试剂中抗体的终浓度大于0.5mg/ml。
三、芯片的制备:
微流控芯片的制备方法,其特征在于包括以下步骤:
制备试剂:分别溶血剂、聚苯乙烯微球悬浊液、鼠抗hba1c单抗试剂和羊抗鼠igg抗体试剂;
组装芯片:将预处理试剂注入预处理试剂腔,反应试剂注入反应试剂腔,使用胶带密封基板,安装底板,完成组装。
四、使用方法:
1、芯片的原理如下:以免疫透射比浊法为基础,将样本中hb和hba1c与有相同的非特异性吸附的胶乳粒子进行固相化,然后加入hba1c的特异性单克隆抗体后形成:胶乳粒子-hba1c-鼠抗人hba1c单克隆抗体的复合物,此复合物和羊抗鼠igg抗体作用形成凝集,凝集量因乳胶表面固相化的hba1c量的不同而不同;通过测定其吸光度并与hba1c百分浓度的标准曲线比较后,可求出样本中hba1c占总hb的百分含量。
2、制作标准曲线:
对样本进行检测前,以纯化水或生理盐水为零点,制备不同浓度水平的校准品溶液,利用芯片重复检测过程,绘制标准曲线。
3、使用步骤包括:
加样:取全血,以肝素或edta抗凝血,静置3h以上或2000rpm经2min离心,然后从红细胞层中精确取10μl作为样本,将取样件取出,从取样件的进样口加入至样本容置腔中,然后将取样件插入至基板的进样腔中;
预处理:挤压第一预处理试剂腔的弹性腔壁,则溶血剂从第一预处理区流道至进样口,并冲洗样本容置腔,样本与溶血剂混合并通过第二预处理区流道流至预处理腔;挤压第二预处理试剂腔的弹性腔壁,将聚苯乙烯微球悬浊液压进预处理腔与样本混合,样本中总hb和hba1c与聚苯乙烯微球产生非特异性吸附而固相化,得到预处理溶液;
空白检测:挤压气腔的弹性腔壁,气腔中的气体将预处理溶液推进检测腔,溶液充满检测腔时进行空白检测,预处理溶液在气体的作用下通过检测腔,随通道流至反应腔;
反应:挤压第一反应试剂腔和第二反应试剂腔的弹性腔壁,将鼠抗hba1c单抗试剂和羊抗鼠igg抗体试剂压进反应腔进行反应,形成聚苯乙烯微球-hba1c-鼠抗人hba1c单克隆抗体的复合物,此复合物和羊抗鼠igg抗体作用形成凝集,凝集量因聚苯乙烯微球表面固相化的hba1c量的不同而不同,得到待测溶液:
检测:反应后,挤压反应腔的腔壁,待测溶液回流至检测腔中,待测溶液填充检测腔,从透光面板射入入射光,透光底板检测出射光,入射光采用660nm单色光作为主波长,800nm单色光作为副波长,实测出的吸光度值a与hba1c百分浓度的标准曲线比较,计算出样本中的hba1c百分含量。
4、线性范围测试
高低值标本制备:高值样本(1#):样本含有的待分析物浓度为16%,为高出微流控芯片检测限值的14%。低值标本(2#):样本含有的待分析物浓度为1.5%。
中间5个浓度标本制备:将1#和2#样本分别按5:1、4:2、3:3、2:4、1:5体积比混匀配置成3#、4#、5#、6#、7#线性样本。
随机顺序将1-7#样本重复测试3次。
结果表明,其线性范围为2-14%,r≥0.9900,且批内重复性均较好,在样本hba1c质量百分比为4.8%处,其标准差为0.075%,变异系数为1.56%,在样本hba1c%质量百分比为10.6%处,其标准差为0.11%,变异系数为1.1%,结果符合临床需求,可为糖尿病患者诊断提供参考。
本发明采用抗原抗体特异性结合的原理,抗体(ab)与可溶性抗原(ag)反应,形成一定结构的免疫复合物,成为悬浮于反应溶液中的微粒。在反应中形成的复合物微粒具有特殊的光学性质,可用仪器检测,提高了检测的速度、灵敏度和易操作性。
对于本领域的技术人员来说,可根据以上描述的技术方案以及构思,做出其它各种相应的改变以及变形,而所有的这些改变以及变形都应该属于本发明权利要求的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!