萃取盐的方法和温度再生的萃取组合物与流程
本发明涉及盐的离子萃取的技术,尤其涉及适用于处理工业或天然盐水的亲水性盐的离子萃取技术。
背景技术:
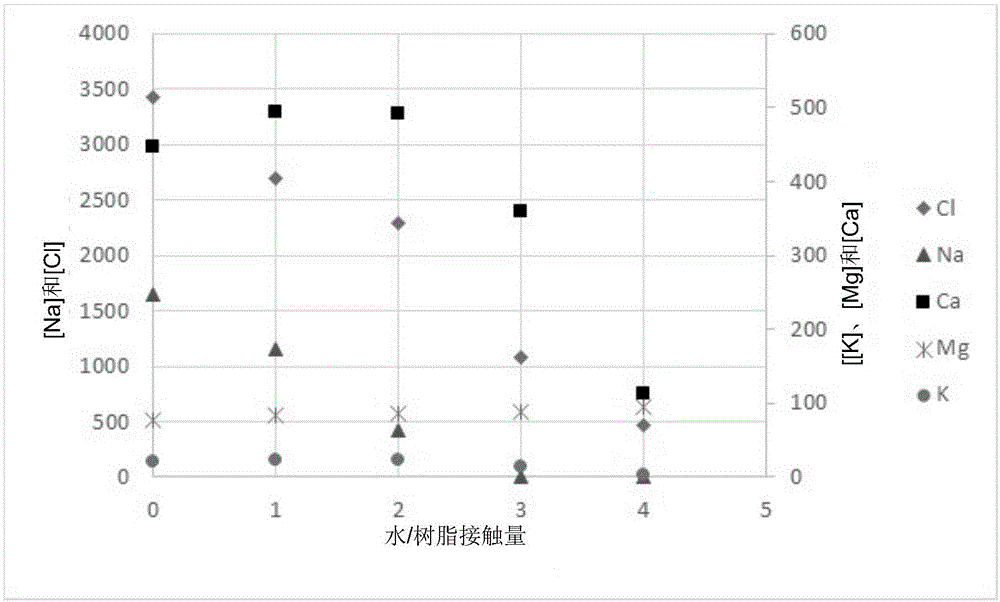
:采矿、石油或工业活动可能产生含盐量高、结垢严重和/或有毒的金属污染废水,这些废水在排入环境之前,甚至在工业过程中再利用之前,都需要加以处理。在这两种情况下,现在的制造商只有非常昂贵的解决方案,这些解决方案不是很好就是不适合他们特定的环境。也有一些情况,特别是对于含有大量碱土阳离子和/或含有微量金属的高度结垢的盐水,目前没有技术对这些水进行可持续和/或经济的处理,从而不得不在等待解决方法时将这些水储存在沉淀池中。对于由不同泉水或结垢严重的水组成的水混合物,设备通常会结垢,这是由于低水溶性的盐的沉淀,例如某些碳酸盐(mgco3、caco3、srco3、baco3、cdco3、coco3、mnco3、pbco3、nico3、feco3、znco3…),硫酸盐(caso4、srso4、baso4、pbso4…),氟盐(mgf2、caf2、srf2、baf2、cdf2、fef2、pbf2…),金属氢氧化物盐(mg(oh)2、ca(oh)2、cd(oh)2、co(oh)2、fe(oh)2、ni(oh)2、zn(oh)2…)以及可能大量存在的许多其他盐的沉淀。此外,如果所使用的技术与水的热蒸发有关,那么使用的温度通常大于80℃,这会降低某些盐(例如,诸如caco3的碳酸盐通过二氧化碳蒸发)以及具有逆溶解度的盐(例如caso4)的沉淀阙值,这会限制盐水的最大萃取水平,甚至产生更大量的需要处理的固体废物。为了萃取溶解于工业或天然水中的离子或盐,一般方法在于利用化学方法,例如通过添加试剂,如允许不溶于水的金属氢氧化物沉淀的碱(naoh…)来确保其沉淀。这种方法对沉淀的金属是非选择性的,并且对应于阳离子(这里为na+vs.金属)或阳离子的交换,并且导致其他缺点,例如增加了新的需要在下游处理的污染物,以及伴随目标化合物浓度减少的效率降低。另一种通过溶剂萃取的方法被称为湿法冶金法,其可以在用来捕获更高浓度中的镍、钴等金属时被采用,通过阳离子mn+/nh+的交换。这些方法使用溶解在溶剂中的阳离子萃取剂,以实施酸碱化学过程或萃取,并且溶剂的再生发生在ph差异几个数量级时。因此,这种方法使用昂贵的碱(naoh…)和酸(h2so4…),导致需要在下游处理的新的与盐(na2so4…)共同产生的相关污染物增加。另一种被实施了50多年的方法在于使用选择性的电渗析膜,其通常可渗透阳离子或阴离子,但不可渗透水和中性分子。在这种情况下,消耗的电能与移动的盐成正比,从而限制了其在盐水处理的情况下的高附加值应用。这种技术对于具有相同电荷的离子没有选择性,因此对于待萃取的金属或阴离子没有选择性,同时也存在膜污染的风险。其他例如离子交换法,其选择性取决于离子交换,且受经过处理的离子浓度的限制,并且由于树脂的化学再生还会产生一定量的新的污染物。最近,申请人在申请wo2010/086575中公开了氟化物在直接接触式交换器中的应用,所述直接接触式交换器包含与离子交换剂相关的液体和疏水性氟化相。但是,本申请中描述的液体有机氟化相描述了离子和非离子有机氟化物的使用,该有机氟化物与一种不太适合获得高的水脱盐率或盐的选择性脱盐的方法有关,尤其是由于再生过程的不充分需要除垢。美国专利申请us2008/179568a1描述了一种用于液-液萃取低浓度的铯和锶的方法,其使用两种分子类型的阳离子萃取剂,所述阳离子萃取剂选自中等浓度的冠醚族和浓度非常低(0.0025至0.025mol/l)的杯芳烃以及至少一种溶解于稀释剂中的改性剂,例如c12-c15异链烷烃。所述改性剂可以是乙醇,三辛胺(toa),磷酸三正丁酯(tbp)或其混合物。这种化合物旨在提高阳离子萃取剂的容量和/或其在实施过程中处于溶解状态的容量。美国专利申请us2008/0014133描述了一种在低浓度下液-液萃取铯和锶的方法,其通过使用阳离子萃取剂分子,所述阳离子萃取剂分子选自低浓度(0.04至0.095mol/l)的冠醚族和高比例的氟化醇(即氟庚醇n3)(体积>80%)和乙二醇醚。美国专利us6566561b1描述了一种在低浓度下液-液萃取铯的方法,其通过使用溶剂化剂和碱性中等稳定性苯氧氟醇型相改进剂,在有由低浓度(0.001至0.20mol/l,优选地0.01mol/l)的选自杯芳烃-冠醚族的阳离子萃取剂分子存在的情况下实施。在本领域中存在许多文献,包括t.g.levitskaia等人在《分析化学》2003,75,405-412中的文章,其论证了使用冠醚型钠中性萃取剂和可去质子的亲脂性弱酸可以从水溶液中萃取苏打(naoh),以形成疏水性醇钠。该文章还示出了在盐度为1m时,先将浓度为0.02m的dc18c6混合,然后将其与浓度为0.04m的七种弱酸(来自醇族)混合,其全部溶解在硝基苯中,由此来萃取naf、nacl、nabr、nano3和naclo4。其中两个醇是氟化芳香醇,其pka为8.8。疏水性离子(例如苦味酸盐)的盐萃取率相当高。但是,疏水性阴离子(例如氯离子cl-)的重新计算的盐萃取率的范围在0.06%至0.16%之间,这证实了从水中萃取疏水性nacl的难度很大,以及醇在该浓度下对萃取性能的影响很小。因此,当前,业界貌似在等待一种处理盐水的解决方案,无论是否被金属污染,其对于萃取各种盐度的盐均是有效的,并且在投资和实施方面花费更少。其最好能够分离结垢离子混合物,去除或减少特定盐的存在,尤其是由这些水引起装置结垢的盐和/或评价这些水中存在的无机化合物的一部分,从而支持这种处理的全部或部分。因此,本专利申请的目的在于描述一种新的用于处理盐水和被金属污染的水的技术,该技术能够选择性地或大规模地从水中萃取对于工业或天然盐水的处理具有或多或少高经济价值的盐。该技术将能够得到广泛的应用,以允许在尊重生态系统的同时将这些水排入环境中,作为工艺用水进行推广,在采矿或石油作业范围内提供一种新的或附加的经济价值或高附加价值的盐和/或金属阳离子的再循环。由于离子是从水中以无电荷化合物的盐的形式萃取的,然后通过热和非化学方式实现萃取剂的再生,从萃取溶剂中反萃取出无电荷化合物的盐,因此该技术的优点还包括不会产生新的污染物。技术实现要素:为了从水介质中萃取盐,本申请提供一种通过液液萃取法去除水中离子的方法,该方法使用液体疏水性有机相通过热再生来实施,所述液体疏水性有机相包含或基本上包含或由以下组成:-至少一种电子中性的、有机的以及疏水性化合物,其能够萃取(例如,溶剂化、复合或螯合)从水相中萃取的盐的阳离子,被称为阳离子萃取分子(cem);-至少一种第二电中性的、有机的以及疏水性化合物,其能够溶剂化从水介质中萃取的盐的阴离子,被称为阴离子溶剂化分子(asm);并且,可选择地,一流化剂,其优选地为疏水性的。出人意料的是,根据本发明所述的asm和cem的结合允许协同萃取由亲水性阳离子和阴离子组成的中性盐,这些中性盐尤其难以转移到有机相中。术语“疏水性”是指在25℃下的化合物或化合物混合物在水中的溶解度小于0.1mol/l。优选地,疏水性化合物在25℃水中的溶解度小于0.1mol/l,优选地小于0.0001mol/l,并且有利地选择了小于1x10-5mol/l。化合物的疏水性或在水中的溶解性可以通过标准方法测量,特别是通过uv/可见光谱法。cem在本申请中描述的cem化合物,其混合物以及在从含有阳离子种类的水中萃取所述阳离子种类的方法中的应用也是本发明的一部分,所述方法如通过液液萃取法利用热再生来去除水中的离子,以萃取至少一种二价阳离子种类和至少一种互补阴离子。所述允许萃取至少一种阳离子的cem可以有利地选自具有良好萃取碱土金属离子能力的分子,所述碱土金属离子例如为钙离子、锶离子或钡离子或其他二价阳离子,这取决于分离的需要。该萃取是可能的,由于通过萃取组合物溶解阳离子和阴离子替代了通过水溶解阳离子和阴离子,从而允许与cem和asm相互作用。相互作用的本质涵盖离子偶极相互作用等现象,伴随着氢键和静电相互作用,甚至范德华键的产生。优选地,cem是一种化合物,其允许络合,尤其允许螯合阳离子。所述“螯合”与简单的“络合”的不同在于阳离子通过至少两个键/相互作用连接至螯合配体。与一价碱金属阳离子相比,考虑用于选择性萃取二价阳离子的cem是来自间环芳(mcp)族的大环,其具有n酚类芳环描述的疏水腔。大环的大小为24至32个原子,特别是碳原子。优选地,大环的大小为24至28个碳原子。这些酚类芳环可以直接地或通过1-碳亚甲基桥(-ch2-)或通过2-碳桥(-ch2ch2-)或通过3-碳桥(-ch2ch2ch2-)在羟基官能团的邻位彼此连接。如果键仅是直接连接的,则这些大环的通用名称为[0n]-型球状配体。如果仅通过1-碳亚甲基桥(-ch2-)连接,则这些大环的通用名称为[1n]-型杯芳烃。如果仅通过2-碳桥(-ch2ch2-)连接,则这些大环的通用名称为[2n]-型全同杯芳烃。桥的大小也可以在相同大环中变化,也可以在0至3碳原子中变化。命名法通过命名它们来指定这种多样性,例如,对于一个具有4个芳环的大环,4个芳环在邻位中通过一个亚甲基桥,然后通过一个3-碳桥,再然后通过一个亚甲基桥,最后通过一个3-碳桥彼此相继地邻接以成环,则其被称之为[1.3.1.3]mcp或[1.3]2mcp。然后用非氢化酰胺基团对所关注的大环进行官能化,以选择性地萃取碱土,而选择性地不萃取二价过渡金属。因此,cem是一个大环,其允许实现选择性萃取非碱性阳离子,尤其是二价阳离子,相对于碱性阳离子,特别是一价阳离子,cem的环由24至32个碳原子形成,且通过酰胺基团官能化,并且具有以下通式(i)或(ii):其中,-n是5至8之间的整数,-p是1或2,-m是3或4,-q和t完全相同或不同,为0,1或2,-r是叔丁基、叔戊基、叔辛基、o-甲基、o-乙基、o-丙基、o-异丙基、o-丁基、o-异丁基、o-戊基、o-己基、o-庚基、o-辛基、och2苯基或氢原子,-r’和r”完全相同或不同,选自由甲基、乙基、丙基、异丙基、丁基、异丁基、戊基、己基、庚基和辛基组成的组,或r’和r”一起形成吡咯环、哌啶环或吗啉环。因此,对于通式(i)所示的化合物,整数n和p应选择使得24≤(3+p)×n≤32。对于通式(ii)所示的化合物,整数m、q和t应选择使得24≤(7+q+t)×m≤32。这类分子属于间环芳族。(来自[16]-型的杯[6]芳烃族),其中,r、r’和r”如上述通式(i)和(ii)中所限定的。当r’和r”均是乙基时,尤其是当基团r是叔丁基、och2ph、h或o-甲基时,二价阳离子的选择性萃取尤其强。有利的是,cem具有一种分子式:(来自[25]-型的全同杯[5]芳烃族),其中,r、r’和r”如同上述通式(i)和(ii)中所限定的。有利的是,cem具有一种分子式:(来自[26]-型的全同杯[6]芳烃族),其中,r、r’和r”如同上述通式(i)和(ii)中所限定的。有利的是,crm是下式的分子:(来自[17]-型的杯[7]芳烃族),其中,r、r’和r”如同上述通式(i)和(ii)中所限定的。有利的是,crm是下式的分子:(来自[18]-型的杯[8]芳烃族),其中,r、r’和r”如同上述通式(i)和(ii)中所限定的。当r’和r”均是乙基时,二价阳离子的选择性萃取尤其令人关注,特别是当基团r是叔丁基、och2苯基、h或o-甲基时。有利的是,crm是下式的分子:([2.1.2.1.2.1]mcp或[2.1]3mcp-型),其中,r、r’和r”如同上述通式(i)和(ii)中所限定的。有利的是,crm是下式的分子:([3.1.3.1.3.1]mcp或[3.1]3mcp-型),其中,r、r’和r”如同上述通式(i)和(ii)中所限定的。有利的是,crm是下式的分子:([2.0.2.0.2.0]mcp或[2.0]3mcp-型),其中,r、r’和r”如同上述通式(i)和(ii)中所限定的。有利的是,crm是下式的分子:([3.0.3.0.3.0]mcp或[3.0]3mcp-型),其中,r、r’和r”如同上述通式(i)和(ii)中所限定的。有利的是,crm是下式的分子:([1.0.1.0.1.0.1.0]mcp或[1.0]4mcp-型),其中,r、r’和r”如同上述通式(i)和(ii)中所限定的。有利的是,crm是下式的分子:([2.0.2.0.2.0.2.0]mcp或[2.0]4mcp-型)、其中,r、r’和r”如同上述通式(i)和(ii)中所限定的。在通式(i)和(ii)中:尤其有利的是,基团r是叔丁基。尤其有利的是,基团r’和r”均是乙基。尤其有利的是,基团r是叔丁基或氢原子。尤其有利的是,cem是下式的化合物:(来自[16]-型的杯[6]芳烃族,cas号:111786-95-9)。根据本发明,当该cem2在液液萃取过程中利用树脂的热再生与至少一种asm以及选择性地与一种流化剂结合时,该cem2对从水溶液中选择性萃取亲水性碱土盐尤其有效,特别是氯化物盐。属于这些通式(i)族的分子已经通过cas编号标识,特别地它们是下列阳离子萃取分子:根据本发明所述的组合物也可包含一种以上的能够萃取至少一种阳离子的cem化合物,其可以有利地选自本申请中描述的化合物。本发明的另一目的涉及这些cem化合物在从水介质中萃取盐和/或离子中的应用。特别地,这些化合物可以单独地或混合地在根据本申请所述的发明的组合物或方法中应用。本发明的另一目的涉及环大小在16至22个原子(尤其是碳原子)之间的大环型cem化合物的使用,其通过酰胺基团官能化,以萃取盐,尤其是亲水性阴离子盐,例如氯化物盐。特别地,这些化合物与根据本发明所述的asm相关联以允许从含有这类盐的混合物溶液中大量萃取,所述这类盐例如为氯化物盐,其包括不同的具有55pm至180pm离子半径的阳离子,有利地具有70pm至167pm,更有利地具有75pm至167pm。这类阳离子尤其是锂、钠、钾、铷或铯阳离子,其是一价的,或钙、锶或钡阳离子,其是二价的,甚至是过渡金属阳离子。应当理解的是,具有离子半径为72pm的二价阳离子镁是一个例外,并且不认为是可充分萃取的,因此这些cem可用于工业上以从水中萃取镁。这些化合物是通式(iii)和(iv)所示的化合物:(iii)(iv)其中,-n是4或5,-p是1或2,-m是2或3,-q和t完全相同或不同,是0、1或2,-r是叔丁基、叔戊基、叔辛基、o-甲基、o-乙基、o-丙基、o-异丙基、o-丁基、o-异丁基、o-戊基、o-己基、o-庚基、o-辛基、och2苯基或氢原子,-r’和r”完全相同或不同,选自由甲基、乙基、丙基、异丙基、丁基、异丁基、戊基、己基、庚基和辛基组成的组或r’和r”一起形成吡咯环、哌啶环或吗啉环。因此,对于通式(iii)所示的化合物,整数n和p应选择使得16≤(3+p)×n≤22。对于通式(iv)所示的化合物,整数m、q和t应选择使得16≤(7+q+t)×m≤32。特别是,在n=4,r=叔丁基,r’和r”=乙基的通式(iii)中的以及cas#114155-16-7的圆锥形构造的大环cem1,当其与至少一种asm以及可选择地与一种流化剂结合时,在通过利用根据本发明的液态树脂热再生进行液液萃取过程中对于从水溶液中大量或总体萃取亲水性盐尤其是氯化物盐非常有效。属于这些通式(iii)和(iv)族的分子已经通过cas编号标识,特别地它们是下列cem:对于杯芳烃,应选择圆锥形甚至部分圆锥形环构造,而不是交替的1、2-型或交替的1、3-型构造,但不排除这些交替的构造。其他20-碳间环芳型环被标识如下:在本发明的一个优选的方面,通式(iii)和(iv)的cem所萃取的阳离子种类在25℃的甲醇中的络合常数logk高于3且小于11、优选地高于5且小于9。这些酰胺型cem尤其能够很好地适应通过根据本发明的温差来进行的液液萃取法。本发明的另一目的涉及利用酯基或酮基官能化的cem化合物的使用,以选择性萃取碱性阳离子,相对于碱土阳离子,而选择性不萃取一价过渡金属(银ag+)。特别地,这些化合物可以在根据如本申请中所述的发明的组合物或方法中单独地或混合地使用。本发明的另一目的涉及环大小在16至24原子之间的大环形cem化合物的应用,其由酯基或酮基官能化,以选择性萃取碱性盐,尤其地亲水性阴离子碱性盐,例如氯化物盐。特别地,这些化合物与根据本发明的asm相关联以允许从含有这类盐的混合物溶液中选择性萃取一种或多种碱性盐,所述这类盐例如为氯化物盐,其包括不同的离子半径为55pm至180pm的阳离子,有利地为70pm至167pm。这类阳离子尤其是锂、钠、钾、铷和铯阳离子,其是一价的,或钙、锶、钡阳离子,其是二价的,甚至是过渡金属阳离子。这些化合物是通式(v)和(vi)所示的化合物:(v)(vi)其中,-n是4、5或6,-p是1或2,-m是2或3,-q和t完全相同或不同,是0、1或2,-r是叔丁基、叔戊基、叔辛基或氢原子,-r’选自由甲基、乙基、丙基、异丙基、丁基、异丁基、戊基、己基、庚基和辛基组成的组,以形成酮类键合基团,或r’选自由o-甲基、o-乙基、o-丙基、o-异丙基、o-丁基、o-异丁基、o-戊基、o-己基、o-庚基、o-辛基、och2苯基组成的组,以形成酯类键合基团。因此,对于通式(v)所示的化合物,整数n和p应选择使得16≤(3+p)×n≤24。对于通式(vi)所示的化合物,整数m、q和t应选择使得16≤(7+q+t)×m≤24。特别是,在n=4,r=叔丁基,r’=o-乙基的通式(v)中的以及cas#97600-39-0的圆锥形构造的大环cem10,当其与至少一种asm以及可选择地与一种流化剂结合时,在通过利用根据本发明的液态树脂热再生进行液液萃取方法中对于从水溶液中选择性萃取钠盐、尤其是氯化钠盐是非常有效的。特别是,在n=5,r=叔丁基,r’=o-乙基的通式(v)中的以及cas#152495-34-6的大环cem11,以及n=6,r=叔丁基,r”=o-乙基的通式(v)中的以及cas#97600-45-8的cem12,当cem11和cem12与至少一种asm以及可选择地与一种流化剂结合时,在通过利用根据本发明的液态树脂热再生进行液液萃取方法中对于从水溶液中选择性萃取碱土盐的碱性盐,尤其是碱性氯化物盐是非常有效的。cem11适于更全面地萃取碱性氯化物盐(除了锂),而cem112,对于较大的环直径为24,具有萃取碱的能力,所述碱优选具有较大直径(铯、铷甚至钾)。属于这些通式(v)和(vi)族的分子已通过cas编号标识,具体地,它们是下列cem:对于杯芳烃来说,应当选择圆锥形甚至是部分圆锥形环构造而不是交替的1、2-型或交替的1、3-型构造,尽管如此,但不是排他性的。根据一个优选的实施例,所述组合物不包含允许萃取钙离子的通式(v)或(vi)所示的cem,也就是说,钙离子的络合常数logk(ca++)在25℃的甲醇中大于3。在本发明的一个优选的方面,通式(v)或(vi)所示的cem待萃取的阳离子种类在25℃的甲醇中的络合常数logk大于3且小于11,优选地大于5且小于9。此外,在cem选择性萃取碱性阳离子种类的情况下,其logk在25℃的甲醇中可以小于5,对于所述碱土阳离子,尤其是钙来说优选小于3。这些通式(v)或(vi)所示的酯类或酮类cem尤其适合通过根据本发明的温差来进行的液液萃取法。asm化合物asm可以是一种包含6至50个碳原子,有利地7至30个碳原子,尤其是8至20个碳原子的化合物,并且包括至少一个芳香环和至少一个卤素原子或一吸电子基团,尤其是一氟化物。有利地,asm是通式b所示的化合物:其中,完全相同的或不同的基团ra、rb、rc、rd和re中的至少任一个是卤素原子或一吸电子基,特别是一卤代基团,选自以下组:-f、cl、br,-cmf2m+1且m≤4,其中m为非零整数,-cf2cf2cph2p+1且p≤4,其中,p为整数,-cf2cph2p+1且p≤4,其中p为整数,-ch2cpf2p+1且p≤4,其中p为整数,-och2cf3,-c(=o)cf3,-cmhnfpclqbrs且m≤4,其中n、p、q、s为整数,其中p、q或s非零,-c(=o)ocmh2m+1且m≤4,其中m为整数,和-c(=o)cmh2m+1且m≤4,其中m为整数,从下列非吸电子基团中选择一个或多个剩余的完全相同的不同的基团ra、rb、rc、rd和re:-h,-ch3,-ch2ch3,-ch2ch2cpf2p+1且p≤4,其中p为整数,-cmh2m-1且3≤m≤10,其中m为整数,和-cmh2m+1且3≤m≤10,其中m为整数;其中,只有一个ra至re的基团可以是上述最后两个基团cmh2m-1和cmh2m+1中的一个;其中,x选自下列基团:-oh,-nh-r’,----其中,完全相同或不同的r’和r”选自下列基团:-h,-cnh2n-1且3≤n≤4,其中n为整数,-cnh2n+1且n≤4,其中n为非零整数,-ch2ch2cpf2p+1且p≤2,其中p为整数,-ch2cpf2p+1且p≤2,其中p为整数,-和通式b的芳基:其中,完全相同或不同的ra、rb、rc、rd和re如在上述通式b中所定义的;其中,r”’选自下列基团:-cmh2m+1且m≤20,优选地≤15,其中m为整数,-cmh2m-1且3≤m≤20,其中m为整数,-cmhnfpclqbrs且m≤10,其中n、p、q、s为整数,其中至少p、q或s非零,-ch2ch2cpf2p+1且p≤4,其中p为整数,-ch2cpf2p+1且p≤4,其中p为整数,-cf2cph2p+1且p≤4,其中p为整数,-cf2cf2cph2p+1且p≤4,其中p为整数,-cmf2m+1且m≤4,其中m为非零整数,-和通式b的芳基:-其中,完全相同或不同的ra、rb、rc、rd和re如上述通式b所定义的。一种asm化合物-乙醇这类化合物有利地选自具有醇官能团的氟芳烃化合物及其衍生物。例如,该化合物可以是衍生自甲醇苯基的醇,例如3-(三氟甲基)苯甲醇(cas#:349-75-7)。优选地,该第一化合物是一甲醇苯基化合物,其有利地包含多于3个氟原子。有利地,该化合物包括至少两个–cf3基团。根据本发明的一个实施例,该第一asm化合物如通式b中的基团x:其与通式a的化合物相对应:其中,r1、r2、r3、r4和r5完全相同或不同,但是其中r1、r2和r3中的任一个是氟化基团,选自下列基团:-h,-f,-cmf2m+1且m≤4,其中m为非零整数,-cf2cf2cph2p+1且p≤4,其中p为整数,和-cf2cph2p+1且p≤4,其中p为整数;其中,完全相同或不同的r’和r”选自下列基团:-h-cnh2n-1且3≤n≤4,其中n为整数,-cnh2n+1且n≤4,其中n为非零整数,-ch2cpf2p+1且p≤2,其中p为整数,-ch2ch2cpf2p+1且p≤2,其中p为整数,-和通式a的芳基:其中,完全相同或不同的r1、r2、r3、r4和r5选自组:-h-f-cmf2m+1且m≤4,-cf2cf2cph2p+1且p≤4,其中p为整数,-cf2cph2p+1且p≤4,其中p为整数。多种asm化合物-乙醇有利地,所述第一化合物选自下表i中所示的化合物:表i:根据本发明的一个方面,疏水性有机液体组合物包含至少一种允许溶解至少一种阴离子的化合物。优选地,这些化合物选自如本申请中所描述的asm-类化合物。特别地,根据本发明所述的液体化合物可以包含固体形式的asm,例如[3,5-二(三氟甲基)苯基]甲醇(cas#:32707-89-4),还有流化剂或疏水性液体稀释剂。可选地,根据本发明的液体组合物可以包含固体asm(工作温度下),例如[3,5-二(三氟甲基)苯基]甲醇(cas#:32707-89-4),和液体asm(工作温度下),例如[(三氟甲基)苯基]甲醇(cas#:349-75-7)。在这种情况下,液体形式的asm1发挥双重功能,作为asm和流化剂/稀释剂。这些化合物彼此之间的相对体积比例可以变化,但有利地在30/70至60/40v/v范围内。优选地,该比例约为40/60v/v,特别是对于组合asm1/asm2。多种asm化合物-酰胺这种化合物有利地选自具有酰胺功能的氟芳烃及其衍生物。通式b的asm化合物还可以是一酰胺化合物。在这种情况下,通式b中的基团x为:其中,r”’如上所述。优选地,所述酰胺具有通式:(c):或(d):其中,r”’选自下列基团:-cmh2m+1且m≤20,优选地≤15,其中m为整数,-cmh2m-1且3≤m≤20,其中m为整数,-和通式b的芳基:其中,完全相同的或不同的ra、rb、rc、rd和re中的至少任一个是卤素原子或吸电子基,尤其是一卤化基团,选自下列组:-f、cl、br,-cmf2m+1且m≤4,其中m为非零整数,-cf2cf2cph2p+1且p≤4,其中p为整数,-cf2cph2p+1且p≤4,其中p为整数,-ch2cpf2p+1且p≤4,其中p为整数,-och2cf3,-c(=o)cf3,-cmhnfpclqbrs且m≤4,其中n、p、q、s为整数,其中至少p、q或s不是零,-c(=o)ocmh2m+1且m≤4,其中m为整数,和-c(=o)cmh2m+1且m≤4,其中m为整数,一种或多种剩下的完全相同或不同的基团ra、rb、rc、rd和re选自下列非吸电子基团:-h,-ch3,-ch2ch3,-ch2ch2cpf2p+1且p≤4,其中p为整数,-cmh2m-1且3≤m≤10,其中m为整数,和-cmh2m+1且3≤m≤10,其中,m为整数;其中,基团ra至re中只有一个可以是上述最后两个基团cmh2m-1和cmh2m+1中的一个。优选地,基团r”’是线性或非线性烷基链,特别地是基团n-c7h15、n-c9h19、n-c11h23或n-c13h27。这些酰胺类化合物尤其适合于液液萃取法,利用根据本发明的热再生。其他这种类型的化合物,可以用作用于萃取根据本发明的化合物的asm的例如:n-[3,5-二(三氟甲基)苯基]乙酰胺(cas#16143-84-3),n-[3,5-二(三氟甲基)苯基]-2-氯乙酰胺(cas#790-75-0),n-[3,5-二(三氟甲基)苯基]-2-溴乙酰胺(cas#99468-72-1),n-[3,5-二(三氟甲基)苯基]-2-溴乙酰胺(cas#56661-47-3),n-[3,5-二(三氟甲基)苯基]-4-氯苯甲酰胺(cas#56661-30-4),n-[3,5-二(三氟甲基)苯基]-4-溴苯甲酰胺(cas#56661-31-5),n-[3,5-二氯苯基]乙酰胺(cas#31592-84-4),n-[4-甲基-3,5-二氯苯基]乙酰胺(cas#39182-94-0),n-[3-氟-5-(三氟甲基)苯基]乙酰胺(cas#402-02-8),n-[2-氟-5-(三氟甲基)苯基]乙酰胺(cas#349-27-9),n-[4-氯-3-(三氟甲基)苯基]乙酰胺(cas#348-90-3),n-[4-溴-3-(三氟甲基)苯基]乙酰胺(cas#41513-05-7),n-[2,5-二氟-3-(三氟甲基)苯基]乙酰胺(cas#1994-23-6),n-[3-(三氟甲基)苯基]乙酰胺(cas#351-36-0),n-[2-甲基-3-(三氟甲基)苯基]乙酰胺(cas#546434-38-2),n-[2-氨基-3-(三氟甲基)苯基]乙酰胺(cas#1579-89-1),n-[3-(三氟甲基)苯基]-2,2,2-三氟乙酰胺(cas#2946-73-8),n-[3-(三氟甲基)苯基]-2,2-二氯乙酰胺(cas#2837-61-8),n-[3-(三氯甲基)苯基]-2,2,2-三氯乙酰胺(cas#1939-29-3),n-[4-氯-3-(三氟甲基)苯基]-2,2,2-三氯乙酰胺(cas#13692-04-1),n-[3-(三氟甲基)苯基]-2-溴乙酰胺(cas#25625-57-4),n-[3-(三氟甲基)苯基]丙酰胺(cas#2300-88-1),n-[2-氯-5-(三氟甲基)苯基]丙酰胺(cas#721-57-3),n-[3-(三氟甲基)苯基](2,2-二甲基-丙酰胺)(cas#1939-19-1),n-[2-甲基-3-(三氟甲基)苯基](2,2-二甲基-丙酰胺)(cas#150783-50-9),n-[4-氯-2-甲基-3-(三氟甲基)苯基](2,2-二甲基-丙酰胺)(cas#112641-23-3),n-[3-(三氟甲基)苯基](2-氯-丙酰胺)(cas#36040-85-4),n-[3-(三氟甲基)苯基]丁酰胺(cas#2339-19-7),n-[3-(三氟甲基)苯基]异丁酰胺(cas#1939-27-1),n-[3-(三氟甲基)苯基]环戊烷酰胺(cas#13691-84-4),n-[3-(三氟甲基)苯基](2-甲基-戊酰胺)(cas#1939-26-0),n-[3-(三氟甲基)苯基](2,2-二甲基-戊酰胺)(cas#2300-87-0),n-[3-(三氟甲基)苯基](2-(4-溴苯基)-乙酰胺)(cas#349420-02-6),n-[3-(三氟甲基)苯基]-1-金刚烷酰胺(cas#42600-84-0),n-[2-氯-5-(三氟甲基)苯基]辛酰胺(cas#4456-59-1)。这些用作asm的分子,通过将其整合于含有至少一个cem和可选地一流化剂的配方中,允许从水中萃取离子种类,尤其是亲水性的盐至萃取有机相。一种尤其能够用于根据本发明的萃取法中的asm是下列分子式:其中,r=n-c7h15,n-c9h19,n-c11h23或n-c13h27,即分别为asm9、asm10、asm11和asm12。“亲水性盐”指可溶于水,在20℃下浓度大于1g/l,尤其在20℃下大于20g/l,有利地在20℃下大于100g/l。流化剂一些cem和asm在萃取过程中在操作温度下是固体或粘性化合物,因此使用流化剂是有利的。鉴于根据本发明所述的方法特别允许萃取较高浓度的盐,因此流化剂应累积能够溶解至少0.1mol/l的cem和asm。实际上,传统的溶剂,例如丙酮、乙酸乙酯、庚烷、二甲基甲酰胺、硝基甲烷、甲醇、乙醇、乙醚或乙腈,无法溶解这些浓度水平下的许多已知的cem,特别是上述描述的具有16至32个原子环的大环。但是,溶剂或稀释剂,如二氯甲烷,以及更具体地极性芳族溶剂表现为适合作为本申请的增溶剂的候选物。这可以用asm的类似性质来解释,asm本身通常就是芳族化合物。例如,1,3-二(三氟甲基)苯(cas#:402-31-3)以及更优选地由两个芳香环组成的苯甲酸苄酯(cas#:120-51-4)满足该说明配方的溶解标准。至少一个存在于芳环上或2个芳环上的三氟甲基或氯化物型吸电子基允许获得特别有利的流化的化合物。二氯苯类化合物(例如,1,2-二氯苯(cas#:95-50-1)和二氯甲苯类化合物(例如,2,4-二氯甲苯(cas#:95-73-8))的衍生物和混合物是稀释剂,其特别适于稀释根据本发明所述的cem。“衍生物”指用上述三氟甲基替代的芳香族化合物,例如具有混合基团的溶剂,例如2,4-二氯-(三氟甲基)苯(cas#:320-60-5),但也是二芳香族化合物,例如二苯醚(cas#:101-84-8)。也可以选择一种asm,以使其具有结合作为asm和cem和/或asm的稀释剂作用。根据本发明的一个优选的方面,所述组合物仅包含asm和cem化合物,可选地与流化化合物相结合,从而组成含有asm、cem和流化化合物的组合物。本发明的另一方面涉及这些asm化合物的应用,尤其是用于从水介质中萃取盐和/或离子的酰胺asm。特别地,这些化合物可单独地或混合在一起用于根据如本申请所述的发明的组合物或方法中。在有机液体组合物中的asm浓度根据本发明的一个优选的方面,在根据本发明的组合物中的一种asm(或asm化合物混合物)的体积摩尔浓度至少等于0.1m。优选地,该组合物的摩尔浓度更高,且至少为1m以允许更优的萃取,尤其萃取亲水性阴离子。根据所选择的adm的阴离子溶剂的效率的不同,其也可以至少为2m,有利地至少为3m,例如至少为4m。所保留的asm浓度取决于作为阴离子溶剂的asm的效率。不提高萃取性能的过量的asm是没有意义的。由于高asm浓度导致的萃取组合物流动性缺乏也不是最佳的。在本发明的某些变形例中,asm或asm混合物可以以纯液体(摩尔浓度为7.32m的[(三氟甲基)苯基]甲醇(cas#:349-75-7)或摩尔浓度为6.41m的(3,5-二(三氟甲基)苯胺(cas#:328-74-5))的形式使用。最终所保留的asm浓度取决于本申请的目的并且取决于asm和流化剂之间的相关成本,从而实现最佳的用于去除水中离子的技术/经济解决方案。密度、溶解度和黏度根据本发明的一个有利的方面,允许在有机液体组合物中,尤其是在萃取的有机液体组合物中溶解阴离子,至少一个阴离子的asm在水中的溶解度,在其游离或络合形式下,小于0.1mol/l,优选地小于0.01mol/l,优选地小于0.0001mol/l,更特别地小于1×10-5mol/l。根据本发明的另一有利的方面,萃取至少一种阴离子的asm密度高于1kg/l,有利地高于1.1kg/l,理想地高于1.2kg/l。这种选择设计与流化剂的选择密切相关,通过较高的密度,可以补偿asm的密度缺乏。根据本发明的另一有利的方面,液体asm或asm+流化剂混合物在25℃下具有小于100mpa.s的黏度,优选小于50mpa.s,例如小于20mpa.s。asm和cem在有机液体组合物中的相对浓度为了确保最大化萃取离子种类,所选择的asm和cem的浓度取决于待萃取的离子种类在水溶液中的浓度。“水溶液”指的是含有大于mol%水的液体。因此,在等量盐水和萃取配方下,cem化合物的浓度有利地等于或高于要萃取的阳离子的浓度。大约超过两倍的浓度通常会构成一个极限,超过该极限,阳离子萃取不会得到实质性的提高。实际保留的cem化合物的浓度主要受cem仅在asm中或在asm+流化剂混合物中溶解能力,和/或所得总体配方黏度和/或总体技术/经济评估最佳化的限制。出人意料的是,可能需要远高于待萃取的阴离子的浓度的asm的浓度,以允许萃取的最佳化。因此,可能需要待萃取的阴离子浓度的至少两倍,优选三倍,甚至四倍、五倍或六倍甚至更多,以获得令人满意的结果,特别是当阴离子是氯阴离子时。实际所保留的asm的浓度主要受到asm在cem+流化剂混合物中的溶解能力的限制,和/或得到的总体配方黏度,和/或总体技术/经济评估最佳化的限制。因此,根据本发明的组合物以萃取由一种阴离子和一个阳离子组成的盐的asm/cem的相对摩尔比,有利地大于或等于1、2、3、4、5或6。所保留的用于工业应用的asm/cem的相对摩尔比的选择取决于这些化合物的相关成本,取决于项目的技术/经济数据,取决于所选择的asm的阴离子的溶解活度。优选地,对于乙醇asm该比至少等4,对于酰胺asm,该比在1和4之间。示例中给出的cem浓度涉及asm+流化剂混合物的容积,因此没有考虑到由大分子例如这些cem的稀释引起的总体配方的容积的增加。因此,实际的cem浓度通常减少10%至25%,但是不限制该范围。根据本发明的组合物的应用根据本发明的组合物可以有利地用于从液相中萃取亲水性离子(阳离子、阴离子)。应当注意的是,该离子的萃取不是通过化学上的离子或其他物质的从有机相到液相(或相反地)的转移来补偿的。该组合物尤其适合通过选择性的方式从液体溶液中萃取离子种类,所述液体溶液包括几种盐和/或离子种类。因此,其尤其适合从液体盐溶液中选择性萃取至少一种非碱性阳离子种类。所萃取阴离子和阳离子包含于根据本发明的组合物中的cem和asm是允许萃取及溶解至少两种,优选地几种离子种类的化合物。两种离子种类可以特别地组成一种或多种亲水性盐。根据本发明的目的,选择的cem和asm能够从含有其的盐溶液中萃取大于一种的盐,优选地几种盐。优选地,这些盐包括或是氯盐。根据本发明的另一目的,这些离子是例如一种或多种碱土盐以及一些金属盐,例如镉cd2+、铅pb2+或银ag+盐的组合。“盐”指由阳离子和阴离子构成的形成中性产物的化合物,并且没有静电荷。这些离子可以是无机的(氯化物cl-、钙ca++…),和有机的(乙酸盐ch3-coo-、铵r3nh+…),单原子的(氟化物f-、镁mg2+…)以及多原子的(硝酸盐no3-、碳酸氢盐hco3-、硫酸盐so42-…)。特别优选地,根据本发明含有cem和asm混合物的组合物,无论有或没有流化剂,均可以从含有下列成分的溶液中萃取:至少一种碱金属阳离子种类,至少一种非碱性阳离子种类,尤其一二价的,和至少一种补充性的阴离子种类,所述的非碱性阳离子种类的量多于碱金属阳离子种类。可选地或另外地,通过该组合物萃取的碱金属阳离子种类的量非常低。“大得多的相对量”及“非常低的萃取”指的是需萃取的一个或多个阳离子(摩尔百分比)至少是所处理的水溶液的碱性阳离子的两倍。有利地该比例可以至少是5,或甚至大于10。根据本发明的一些组合物在需萃取的阳离子和无需萃取的阳离子之间的初始浓度相同的情况下,或萃取需萃取的全部离子(例如ca)而几乎不萃取碱性阳离子(例如na),尤其是当大量碱性阳离子存在时,允许实现萃取比为13。需萃取的一个或多个阳离子优选地选自碱土金属基团,更特别地,选自钙、锶和/或钡。这种二价阳离子,尤其是水中最常见的阳离子的萃取,可以通过将其与特定阴离子的结合以避免结垢现象。碱性金属是一种来自元素周期表第一栏(第一族,氢除外)的化学元素。锂、钠、钾、铷、铯和钫是碱性金属。他们有一个正电荷。碱土金属阳离子盐的萃取是通过络合用于萃取该阳离子的cem,以及阴离子从水相“跟随”到有机相来进行的,从而确保中和正负电荷。通过asm溶剂化的“跟随”的阴离子主要是最不亲水的阴离子,即具有最高水合自由能的阴离子。因此,从水相至根据本发明的有机配方的阴离子的优选萃取顺序是:bf4-、i-、br-、no3-、cl-、hco3-、ch3coo-、f-、so42-、co32-。因此,在碱土盐的情况下,优先萃取碘化物、溴化物、硝酸盐和/或氯化物盐。这些盐即使是在高水温(cacl2在水中的溶解度大于40wt%)下也极易溶于水,他们可在溶剂热再生步骤中变成浓缩盐水。因此,根据本发明萃取的碱土或金属盐允许将阳离子从引起结垢的阴离子中分离出来,从而能够构造结垢盐以将其驱动成两种不同的水性废水。因此,根据本发明的部分去离子的水是由最亲水的阴离子,即氟化物、硫酸盐和碳酸盐、和未萃取的碱性阳离子构成。因此,该水已失去了所有的结垢能力。顺便说一下,对于根据本发明的热再生的方法产生的水也是如此,所述水主要由碱土和金属氯化物盐组成。因此,本发明的目的在于通过避免阳离子和阴离子在同一废水中的同时存在来去除许多工业应用中的结垢层,所述阳离子和阴离子为当其结合时水溶于水或难溶于水。因此,待需分离的盐主要是碳酸盐(mgco3、caco3、srco3、baco3、cdco3、coco3、mnco3、pbco3、nico3、feco3、znco3…)、硫酸盐(caso4、srso4、baso4、pbso4…)和氟化物盐(mgf2、caf2、srf2、baf2、cdf2、fef2、pbf2…)。通过调整水的ph或通过将萃取的二价阳离子释放到具有中性ph、或甚至轻微的酸性ph的水中,可以控制金属氢氧化盐(mg(oh)2、ca(oh)2、cd(oh)2、co(oh)2、fe(oh)2、ni(oh)2、zn(oh)2…)的沉淀。优选地,根据本发明萃取的阳离子为ca2+、sr2+、ba2+、pb2+、cd2+和银ag+。就过渡金属而言,上述所列并不详尽。同样地,根据本发明的组合物可以用于根据本发明用以萃取有机相中的ca++、sr++和/或ba++的方法中。对于更加疏水的阴离子来说,例如高氯酸盐clo4-、高锰酸盐mno4-、苦味酸盐,低浓度的asm通过与萃取至少一个阳离子的cem相结合,足以实现将其转化为有机相。因此,根据本发明的组合物尤其能够用于如本申请中所述的萃取方法中,特别地,用于通过利用热再生进行的液液萃取法以去除水中离子的方法中。根据一个优选的实施例,组合物不包括允许萃取氯化钠的cem,即cem络合钠的常数logk(na+)在25℃甲醇中大于3。根据本发明的一个特别的方面,不能或难以萃取氯化镁,这是由于cem在25℃的甲醇中络合镁的常数logk(mg2+)小于3。液液萃取法本发明还涉及从液体盐水溶液中萃取非碱性阳离子种类的液液萃取法,所述液体盐水溶液包括至少一个非碱性阳离子种类,一个碱金属阳离子种类和一个互补阴离子种类,所述方法包括以下步骤:a)将液体疏水性有机相和所述液体盐水溶液在第一温度下混合于第一反应器中,以随后获得经处理的液体水溶液和带有所述非碱性阳离子种类和所述互补阴离子种类的液体疏水性有机相,所述液体疏水性有机相包括萃取所述非碱性阳离子种类的分子,溶解所述互补阴离子种类的分子,以及可选地一流化剂;b)一方面分离所述经处理的液体水溶液,另一方面分离带有所述非碱性阳离子种类和所述互补阴离子种类的所述液体有机相;所述方法的特征在于,萃取非碱性阳离子种类的分子是如上所述的cem,以及溶解所述互补阴离子种类的分子有利地是如上所述的asm,尤其是酰胺类asm。优选地,执行随后的步骤c),其包括:在第二温度(优选大于第一温度)下,将带有所述非碱性阳离子种类和所述互补阴离子种类的液体有机相以液相的形式混合于具有再生液体水溶液的第二反应器中,以随后获得再生的液体有机相和带有所述非碱性阳离子种类和所述互补阴离子种类的再生液体水溶液,所述第一和第二温度之间的不同在于温度在30℃至150℃范围内变化,优选地在50℃至100℃范围内变化。术语“非碱性阳离子”或“非碱性阳离子种类”指的是除源自碱金属的阳离子之外的阳离子。优选地,非碱性阳离子种类是二价阳离子,例如碱土阳离子。根据本发明的方法尤其适应于萃取下列阳离子中的一个:钙、锶和钡。所述方法也可以适用于萃取一价金属阳离子,例如银ag+、或二价金属阳离子,例如铅pb2+和镉cd2+。根据本发明的一个优选的方面,碱金属阳离子种类是钠离子na+。有利地,所述钠离子难以或不能从盐水溶液中萃取。非碱性阳离子盐包括前述的阳离子和互补阴离子种类或阴离子。短语“互补阴离子”指的定带有一个或多个阴离子种类与阳离子种类的相对应,并且允许将其中和,从而构成中性盐。cem和asm以及可选择的流化剂如上所述。可选地,asm也可以是疏水性化合物,优选地为质子疏水性化合物,其在25℃的水中的pka至少为9,优选地至少为10.5,并且优选地低于水在25℃下的pka,或在25℃下至少低于15。cem也可以是有机的疏水性化合物,其具有待萃取非碱性阳离子种类的络合常数,logk在25℃下的甲醇中大于3小于11,优选地在大于5小于9。而且,在cem选择性萃取非碱性阳离子种类的情况下,对于碱性阳离子,尤其对于钠,其在25℃的甲醇中的对数k值可以小于5,优选小于3。限定pka(或酸度常数)为pka=-log10ka,其中ka是酸离解常数,其通过标准方法测量以获得这类pka。推荐用于强碱pka的标准测量方法最好是由popov等人在pureappl.chem.、vol.78、no3、pp663_675、2006中发布的用于确定高及低pka的国际理论和应用化学联合会(iupac)-guidelinesfornmrmeasurements中所描述的。k是在25℃下甲醇中cem和非碱性阳离子的络合常数,其根据等温量热滴定标准方法测量。根据本发明的一个特定方面,非碱性阳离子种类是针对碱金属阳离子种类被选择性地萃取的。这种选择性可以实现如上所述的水平。不像许多已知的离子萃取方法,根据本发明的该方法不是基于ph的变化来允许吸收或释放捕获的离子,而是特别通过氢离子h+酸碱迁移率。因此,在本发明的一个优选的方面,该方法不包括使再生液体水溶液的ph值发生显著变化的步骤,即超过要处理的水的ph值变化+/-2的步骤,例如相对于待处理的水的±1。根据本发明的优选方面,所述方法在萃取离子的溶剂的再生步骤中不包括添加剂、用于改变再生液体水溶液的ph值的化合物的使用或存在,例如酸或碱,尤其是无机酸,例如硫酸、盐酸或硝酸或碱,例如苏打或钾碱。而且,有利地该方法允许从待处理的水中萃取至少一中碱土阳离子种类,及阴离子种类,例如br-orcl-离子。应当注意的是,这种阴离子种类是亲水性的,并且尤其难以从水介质中萃取。根据本发明的方法的一个尤其有利的方面是,其允许从水相中萃取阳离子,尤其是ca++-类阳离子,及阴离子,尤其是cl—类阴离子,同时萃取的盐浓度可能超过0.1mol/l。步骤a)液体盐水溶液和疏水性有机相的混合步骤a)可以通过搅拌两种液相来实施,例如通过机器或轨道搅拌,当这两个相的密度不同时通过产生高湍流和/或通过垂直渗透(静态或搅拌重力柱)。与作为本发明主题的方法的实施相关的技术取决于与该方法相关的转移动力学和所考虑的操作温度。也许重复这些混合步骤a)是必要的从而实现想要的盐的萃取性能。在这种情况下,待处理的盐水溶液以及有机相的流动可以在混合反应器中逆流,以获得最大的去离子性能。还优选的是,混合步骤a)不发生以下几种情况:产生微乳液或稳定乳液,以及所选择的asm不具有表面活性剂活性的任何情况。步骤b)分离水和有机相的步骤b)有利地可以是有机相和液体液相的简单重力倾析。该倾析可以在制备混合物的反应器中进行。可选地,分离可以通过外部装置来实现,例如离心分离,可选地离心分离机单元,其与液相和有机相混合的反应器不同。由于固定的有机相体积,因此两个相的倾析时间是该方法的重要参数。类似地,优选不相溶的液相之间的密度差大于0.1kg/l,甚至大于0.2kg/l。因此,有利地选择密度大于待处理水、已处理的水和再生盐水的密度的有机相。有利地,选择密度低于待理的水、已处理的水的密度的有机相。在这两个情况下,允许有效倾析两个相的密度差(当使用此类混合物时)应当是足够的。在这两个情况下,如果该方法中实施的不相溶液体液相之间的密度差小于0.1kg/l,则可以考虑实施能够分离密度差只有0.05kg/l的液相的离心分离类型的倾析系统。步骤c)一旦相被分离,则带有离子种类的液体有机相有利地被引入一个或一系列第二反应器中,所述第二反应器在加热后,在第二温度下与液体水或再生水接触,其中所述第二温度高于第一温度。利用有机相的“热”水进行再生,可以反萃步骤a)中吸收的盐,因为再生水是热的,所以这种方法更有效。因此,这允许降低再生水的体积和/或提高液体有机相的生产率和/或减少已实施的解吸反应器的数量和/或产生带有高浓度反萃取盐的再生水。除了温度外,允许反萃取盐的混合步骤c)可在与混合步骤a)中所描述的允许萃取盐的相同操作条件下进行。但是,一些条件,例如压力可以改变以避免例如水或流化剂的沸腾。此外,在较高温度下对萃取组合物进行再生的这一步骤会对流体动力学产生影响,降低有机相粘度,从而促进相的倾析以及盐在相之间转移的动力学,这可能导致选择另一种技术,而不是步骤a)中实施的技术。选择水或再生液体水溶液以使其与反萃取盐相容,尤其以避免任何结垢问题,尤其是用于冷却由此步骤产生的热水的热交换问题。温度根据本发明的一个有利的方面,步骤a)在室温下执行。不对盐水溶液进行初步加热或冷却也是有利的。可选地,也可以实施初步加热或冷却。在这种情况下,优选地,加热或冷却液体盐水溶液不超过待处理的液体盐水溶液5℃,有利地不超过2℃。根据本发明的另一个有利的方面,第一温度低于50℃或高于0℃。该温度有利地可以在10℃至40℃范围内选择,优选地15℃至30℃,尤其是19至26℃(例如25℃)。“温度在10℃至50℃之间”指的是温度为10℃、11℃、12℃、13℃、14℃、15℃、16℃、17℃、18℃、19℃、20℃、21℃、22℃、23℃、24℃、25℃、26℃、27℃、28℃、29℃、30℃、31℃、32℃、33℃、34℃、35℃、36℃、37℃、38℃、39℃、40℃、41℃、42℃、43℃、44℃、45℃、46℃、47℃、48℃、49℃或50℃。根据本发明的另一个尤其有利的方面,所述第二温度高于60℃,优选地高于85℃。该温度可以在60℃至150℃之间选择,优选地85℃至125℃,尤其在90℃至120℃(例如95℃)之间。“在60℃至150℃之间的温度范围”指的是温度为60℃、61℃、62℃、63℃、64℃、65℃、66℃、67℃、68℃、69℃、70℃、71℃、72℃、73℃、74℃、75℃、76℃、77℃、78℃、79℃、80℃、81℃、82℃、83℃、84℃、85℃、86℃、87℃、88℃、89℃、90℃、91℃、92℃、93℃、94℃、95℃、96℃、97℃、98℃、99℃、100℃、101℃、102℃、103℃、104℃、105℃、106℃、107℃、108℃、109℃、110℃、111℃、112℃、113℃、114℃、115℃、116℃、117℃、118℃、119℃、120℃、122℃、124℃、125℃、126℃、127℃、128℃、129℃、130℃、131℃、132℃、133℃、134℃、135℃、136℃、137℃、138℃、139℃、140℃、141℃、142℃、143℃、144℃、145℃、146℃、147℃、148℃、149℃或150℃。有必要选择所述第一和第二温度使得混合物在操作压力下保持在液体状态下,并且使本发明的技术/经济性能最大化。尤其有利的是这两个温度之间的差异δt选自30℃至150℃的范围内,优选地在50℃至100℃范围内。“在50℃至100℃之间的δt”指的是δt为50℃、51℃、52℃、53℃、54℃、55℃、56℃、57℃、58℃、59℃、60℃、61℃、62℃、63℃、64℃、65℃、66℃、67℃、68℃、69℃、70℃、71℃、72℃、73℃、74℃、75℃、76℃、77℃、78℃、79℃、80℃、81℃、82℃、83℃、84℃、85℃、86℃、87℃、88℃、89℃、90℃、91℃、92℃、93℃、94℃、95℃、96℃、97℃、98℃、99℃或100℃。类似地,如果第一温度是0℃,则第二温度将高于50℃,有利地高于70℃,例如80℃。因此,本发明的方法可以包括第一步骤a):允许特定的离子(优选地为互补)物质在室温下从待处理的液体盐水溶液转移至有机相,接下来是步骤c):允许带有离子种类(优选地为互补)的有机相的再生,并且发生在高于室温的温度下,但并不特别高,以从地热、太阳能或其他可再生能源(例如低于150℃)产生。根据本方法的一个优选的方面,其包括以下步骤:c)分离所述再生液体有机相和水,或带有所述离子种类(优选为互补)的再生液体水溶液,d)使其间接热接触,例如通过热交换器,使所述带有离子种类的液体有机相和所述再生液体有机相间接热接触。根据本发明的一个特别的方面,有利的是该方法包括加热和/或冷却步骤:-带有离子种类的有机相,-不带有离子种类的有机相,尤其是再生的有机相,-再生水或水溶液,和-带有放电离子种类的再生水或水溶液;之后将这些不同的相或水引入第一和第二反应器中。上述加热步骤可全部或部分地通过上述各相中的至少两个相之间的热交换(即带电有机相之间,尤其是再生有机相,不带电离子种类之间,或液相之间,即水、再生水溶液之间,或水和带有放电离子种类的再生水溶液之间)来进行。尤其地,根据本发明的该方法包括加热再生水或水溶液的步骤,其在步骤c)之前执行,和/或包括加热带有离子种类的有机相的步骤,其在步骤c)之前执行。在本方法中,萃取组合物的热再生例如允许在其再循环之前将所需再生步骤的数量2减少两倍。当实施具有高cem容量(即高盐容量)的树脂时,这种优点似乎更为显著。提高再生温度允许减少用于接触蒸馏水或再生水的步骤的数量,同时允许每次更多的盐的反萃取。压力增加混合步骤a)和/或c)有利地在海平面约1atm大气压下进行,或者除了反应器中存在的液体重量之外,不施加压力其他压力装置。如果施加压力,则该压力可以是正的或负的。此类压力可以在0.8atm至80atm范围内变,优选地在1至10atm范围内。经处理的水的应用有利地,用于步骤c)中的再生液态水或水溶液产生自经处理的盐水溶液,所述盐水溶液在步骤a)的最后在互补处理之后得到,所述互补处理允许在步骤c)、d)或e)中避免任何结垢的风险。可选地,其可以来自外部资源。组合物所述有机相包括或主要由或由根据本发明的组合物组成,所述组合物如在本申请中所述。该组合物尤其对于实现所述方法尤其有效。尤其适于贯彻根据本发明的方法的组合物包括将与至少一个如上所述的cem类化合物结合的酰胺asm与流化剂结合的组合物。在本发明的说明中,该组合物也可以被称为“溶剂”或“液体树脂”。设备本发明还涉及用于萃取至少一种非碱性阳离子种类和至少一种互补阴离子的设备,所述非碱性阳离子种类和互补阴离子存在于液态盐水溶液中,所述设备包括:-一第一反应器,含有一液体疏水性有机相或根据如本申请中所述的发明的组合物。该设备可以有利地包括:-一第一反应器,含有所述疏水性液体有机组合物和选择性地盐水溶液,以及在液体状态下,作为随后的产物的经处理的盐水溶液和液体疏水性有机相并带有所述非碱性阳离子种类和所述互补阴离子种类;所述第一反应器还包括第一混合装置和第一装置,一方面用于分离所述经处理的液体盐水溶液,另一方面用于分离所述带电的液体有机相,-一第二反应器,含有带有至少所述非碱性阳离子种类的液体疏水性有机相,和至少一种中和其电荷的互补阴离子,以及再生水或再生水溶液,以随后获得带有所述离子种类和再生有机相的再生液体水溶液;所述第二反应器还包括第二混合装置和第二装置,一方面用于分离所述带有离子种类的再生盐水溶液,另一方面用于分离所述再生有机相;-选择性装置,用于控制所述第二反应器中的温度;-连接装置,允许在第一反应器和第二反应器之间转移:-所述再生液态水溶液,其可以从所述第一反应器中萃取-所述带电荷的液体疏水性有机相,其从所第一反应器中萃取-所述再生液态疏水性有机相,其从所述第二反应器中萃取;-所述再生液态水带有来自所述第二反应器的盐;和-热交换器,将萃取于所述第一反应器中的所述带电荷的液体疏水性有机相,和萃取于所述第二反应器中的所述再生的液体疏水性有机相聚集在一起;和可选择地,-热交换器,将所述再生液态水或水溶液与带有反萃取的互补离子种类的所述再生液态水聚集在一起。根据本发明的一个特别的方面,所述反应器,尤其是那些无法移动的部分的反应器是由不锈钢制成的。根据本发明的另一个特别的方面,所述第一反应器和/或第一反应器不包括加热(加热器)或冷却(冷却器)装置。根据本发明的又另一个特别的方面,存在于所述设备中的有机相包括,主要包括或由根据如本申请中所述发明的组合物构成。根据本发明的设备可以有利地串联安装,以使处理待处理水的步骤能够连续,从而减少水中的离子种类的浓度直到得到纯水和/或从待萃取的离子种类提纯的水。同样地,根据本发明的所述设备可以有利地串联安装,以使带有盐的再生液体疏水性有机相的步骤能够连续,从而减少树脂中的离子种类浓度直到得到从萃取的离子种类中充分提纯的树脂。这种设备也包括在本发明的中。本发明还涉及液液萃取法,萃取由至少一种亲水性阴离子例如氯化物(参见实施例1和2)组成的盐或盐混合物。所述萃取的阳离子还具有55pm至180pm的离子半径,有利地70pm至167pm。这种阳离子尤其是锂、钠、钾、铷或钙、锶或钡阳离子,这些都是二价阳离子,或甚至是过渡金属阳离子。该方法包括以下步骤:i)在第一温度下,在第一反应器中混合液体疏水性有机相和所述液态盐水溶液,以随后得到经处理的液态水溶液和带有所述阳离子种类和所述互补阴离子种类的液体疏水性有机相,所述液体疏水性有机相包括萃取所述如上所述的阳离子种类的分子,溶解所述互补阴离子种类的分子,以及可选择地一流化剂;ii)一方面,分离经处理的液体水溶液,另一方面,分离所述液体疏水性有机相,其带有所述阳离子种类和所述互补阴离子种类;所述方法的特征在于所述萃阳离子种类的分子是如上所述的cem,所述cem是具有16至22个原子(尤其是碳原子)的大环;以及在于所述溶解互补阴离子种类的分子有利地是如上所述的asm。有利地,所述方法接下来包括再生疏水性有机相的步骤,所述疏水性有机相的类型可以和上述相同。有利地,再生渐度在60℃至150℃之间,优选地在90℃至120℃。所述方法的化合物和的其他条件可以有利地参考萃取非碱性阳离子种类的方法中所描述的化合物和条件。同样地,本发明涉及允许实施该方法的装置,所述装置大质或完全与上述装置相同。附图说明通过阅读附图,能够更好地理解本发明,所述附图以示例的方式提供并且本质上不是限制性的。图1示出了如实施例2所述,盐水(初始浓度为180g/l)中五种离子na+,k+,mg2+,ca2+和cl-与含有0.4mol/l的cem1和1.2mol/l的asm9先后接触4次后全部溶解在根据本发明的1,2-二氯苯中的浓度(mmol/l)变化,其中在进行下一步骤前,每个步骤中均将实现萃取平衡。图2示出了如实施例3中所述在室温下,7种从盐水(初始浓度为0.1mol/l)中通过利用含有0.1mol/l的cem2和3.5mol/l的asm2的组合物萃取出来的盐licl,nacl,kcl,mgcl2,cacl2,srcl2和bacl2的萃取率(摩尔%),所述含有cem2和asm2的组合物均溶解于根据本发明的二氯苯中,所述licl,nacl,kcl,mgcl2,cacl2,srcl2和bacl2根据阳离子的离子半径表达。图3示出了如实施例4中所述含有全部溶解于根据本发明的1,2-二氯苯中的0.1mol/l的cem2和1mol/l的asm9组分的cacl2在室温下以及80℃下的吸收等温线图。图4示出了如实施例5所述含有全部溶解于根据本发明的1,2-二氯苯中的0.1mol/l的cem2和1mol/l的asm9组分的两个再生相在20℃和80℃下的比较图,其中所述组合物在用蒸馏水开始几个连续的反萃取阶段之前加入高达80mmol/l的cacl2。图5示出了如部分实施例1和3所述在室温下,7种从盐水(初始浓度0.1mol/l)中通过利用含有0.1mol/l的cem1至cem8和3.5mol/l的用于cem1和cem2的asm2或者1mol/l用于cem3至cem8的asm9的全部溶解于根据本发明的用于cem1和cem2的二氯甲烷或用于cem3至cem8的1,2-二氯苯中的组合物单独萃取出来的licl,nacl,kcl,mgcl2,cacl2,srcl2和bacl2盐的萃取率(摩尔%),根据阳离子离子半径表达。图6示出了asm11化合物的nmr光谱。具体实施方式用于实施本发明的cem的描述阐述了根据本发明的不同离子萃取组合物。用于这些组合物的12个cem如下所示:所有这些cem都是固体的,并且完全不能溶解于水中。所阐述的实施例的总体说明萃取组合物萃取组合物通过将大量cem和asm溶解于选择的流化剂,二氯甲烷ch2cl2、二氯苯或二氯甲苯或其他任何能够很好的溶解cem/asm混合物的流化剂来得到,以在将cem和asm溶解于至少3毫升的流化剂后获得想要的最终浓度。如果所选择的流化剂也是asm化合物,则所选择的asm体积至少是3毫升。给定的asm2和asm9的浓度涉及添加的流化剂体积,给定的cem浓度涉及添加的流化剂+asm体积。为了促进有机化合物的溶解,通过加热枪(温度约为50至60℃)稍微加热几秒(10至30秒)有机萃取组合物直到获得清液。因此将化合物在室温下静置24小时以确保获得的制剂是稳定的。然后将蒸馏过两次的与这些密封的制剂的容积相等的水加入到制剂中,后以500转数/分轨道搅拌两个小时,从而允许将所有的制剂水饱和度和ph值控制在进口和出口处(ph接近7或至少在与饱和水接触后保持不变)。因此,将萃取组合物留作倾析。所有的成分都是稳定的,并且在两个不同的相中快速(最多几分钟)倾析。盐水-尤其含有待萃取的盐的盐水从蒸馏过两次的水中制备一种或多种所考虑的氯化物盐(nacl或其他)的水溶液。所用的氯化物盐有:licl,nacl,kcl,mgcl2,cacl2,srcl2和bacl2。萃取-反萃取然后从倾析的两相混合物的下相中取出3ml制备的有机萃取组合物,并将其转移到具有含有一种或多种所考虑的氯化物盐(nacl或其他)的3ml水的小瓶中,后将小瓶密封并在室温下(rt,即20至25℃之间)轨道搅拌(500转数/分)2小时。考虑到在更高温度尤其是60℃或80℃下进行萃取或反萃取分析,因此在加热板上的金属模具中通过间接恒温控制加热来进行2个小时的磁搅拌(500转数/分)。进行验证以确保在这些搅拌期间确实存在1-2mm的液滴,从而确保在搅拌结束时所考虑的氯化物盐(nacl或其他)能够在两个液相之间实现平衡分布。有机相和水相方面是透明的,无色的或略微混浊的。一旦进行完2小时搅拌,则停止搅拌,所有剩下的用于在分析温度下倾析约10分钟,至少到两个相完全分离为止。然后,取出上层液相后搅拌并稀释,以通过离子色谱法(包括适合被搜索的盐的离子和浓度的阳离子分析柱和阴离子分析柱的metrohmtm装置)分析其盐度。同样地,通过该离子色谱法来分析氯化物盐(nacl或其他)的初始水溶液,以确定其萃取前的阳离子和氯化物的相对摩尔浓度。所有的萃取和分析都是重复的。实施例1:在室温下用cem1萃取单盐盐溶液在本实施例中,使用的cem是4-叔丁基-杯[4]芳烃四(n,n-二乙基乙酰胺)(cem1的cas#:114155-16-7)。根据出版物《杯芳烃酰胺选择性络合碱和碱土阳离子,新j.chem,1991,15,33-37》中所描述的的合成程序,其是从4-叔丁基杯[4]芳烃分子式c44h56o4中合成的,cas#为60705-62-6,购买于tcichemicals公司。使用的asm为asm2,cas#32707-89-4,c9h6f6o,mw=244.13g/mol,一种白色固体,可从几家经销商处购得。其特征在于:参数值单位密度(1.433)kg/l黏度-mpa.sbp255℃mp55℃fp97℃logp3.0(预估)-溶解度2.29mmol/lpka14.7+/-1-所考虑的萃取组合物包括在二氯甲烷ch2cl2中的0.1mol/l的cem1和3.52mol/l的asm2,所述cem和asm通过如上所述获得。无论所考虑的水中的盐是licl,nacl,kcl,mgcl2,cacl2,srcl2或bacl2,其初始浓度都是0.1mol/l。在进行完这7种特定盐的萃取(重复的)之后,在室温和同等体积的水/萃取制剂下,萃取的阳离子在萃取之前和萃取之后的相对摩尔百分比的量如表i所示:从仅含一种碱或碱土氯化物的盐水中萃取阳离子,根据阳离子的不同其萃取率在5.4%至85.8%之间变化。在这种单盐溶液中,对于该cem1来说,盐萃取水平非常好,除了镁,所述镁由于其离子半径为76-pm和高亲水性,因此不适于该16个原子大环的萃取包膜,所述16个原子的大环仍然太大。因此,该制剂看起来很适合用于大规模的盐水的脱盐,甚至是海水(一种水,其盐度高于50g/l)的脱盐。实施例2:通过使用cem1从海水中萃取盐萃取组合物如下:0.4mol/l的cem1(参考实施例1,cas#:114155-16-7),和1.2mol/l的asm9配合,通式为:其中,r为庚基基团:n-c7h15。通过下列实施例9中所述的方法合成该化合物。使用的溶解这两个化合物的流化剂是1,2-二氯苯,cas#95-50-1,其购于tci-chemicals公司,并且通过首字母缩写12clph来标识。海水是一种具有高盐度的水,浓度为180g/l(即5.6mol/l),由钠、钾、钙、镁和氯离子组成,其比例如下表ii中所示。为了接近操作条件,将待处理的盐水与三倍相对体积的该萃取组合物接触。在下表ii中示出了在室温(rt)下进行的四个萃取步骤中的每一个之前和之后的每种离子在水中的浓度(mmol/l)。表ii通过图1阐述该数据。很明显,第一步萃取的盐是氯化钠,然后从第三萃取步骤开始萃取氯化钠和氯化钾,同时nacl继续降低其在水中的浓度。不令人惊奇的是,无法萃取镁。最后,在液相之间的4次接触和混合阶段之后,水的总盐度从180g/l转变为23.7g/l。第5次萃取能够实现完全的脱盐,除了mgcl2。实施例3:在室温下用cem2萃取单盐盐水溶液在与实施例1相同条件下执行本实施例3,除了将cem1换成cem2。所使用的cem是4-叔丁基-杯[6]芳烃苯丙锡(n,n-二乙基乙酰胺(cem2的cas#:111786-95-9))。根据出版物《selectivecomplexationandmembranetransportofguanidiniumsaltsbycalix[6]areneamides,israelj.chem,1992,32,79-87》中所描述的的合成程序,其是从4-叔丁基杯[6]芳烃分子式c66h84o6中合成的,cas#为78092-53-2,购买于tcichemicals公司。使用的asm为asm2,cas#32707-89-4,c9h6f6o,mw=244.13g/mol,一种白色固体,可从几家经销商处购得。在进行完这7种特定盐的萃取(重复的)之后,在室温和同等体积的水/萃取制剂下,萃取的阳离子在萃取之前和萃取之后的相对摩尔百分比的量如表iii所示:表iii因此,从仅含一种碱或碱土氯化物的海水中萃取阳离子,根据阳离子的不同其萃取率在13.5%至63.8%之间变化。在这种单盐溶液中,所萃取的是二价阳离子(除了镁离子),其量是一价阳离子的两倍或三倍,所述镁离子更加亲水并且更小,并且其萃取难度如实施例2所示。因此,根据本发明的组合物证实了该制剂对许多工业应用来说尤其值得关注的特异性,在这些特异性中,尽管钙比钠((δg°hyd=-1515kj/molversus-406kj/mol))更加亲水(尽管他们的离子半径非常接近(102pm和100pm)),但是从水中萃取的钙和钠分别比他们各自的氯化物形式多2.54倍。实施例4:含有cem2的萃取组合物用于萃取cacl2的特征本系列实施例的目的在于建立含有0.1mol/l的cem2和1mol/l的asm9的萃取组合物(全部溶解于1,2-二氯苯)在cacl2为20℃和80℃时的两个萃取等温线。在实施了7个特定盐的萃取(重复)后,在室温下和在水/萃取制剂等体积条件下所萃取的阳离子在萃取前和萃取后的量的相对摩尔百分比如下表iv所示:表iv之后在80℃下进行相同系列的萃取并给出如下表v:表v萃取温度对萃取性能有很大影响。从这些研究中以前收集的数据中,如图3所示点绘这些吸收的等温线作为浓度函数(单位为mol/l)是可能的。横坐标示出了nacl在水中的浓度,纵坐标示出了吸收平衡时有机相nacl的浓度。根据本发明的盐的液液萃取法在吸收时放热,在再生时吸热,这允许用热水对萃取有机组合物进行热再生。实施例5:包括热再生含有cem2的萃取组合物的萃取方法以及对cacl2解吸的影响在室温下,使20℃下具有最高cacl2含量的实施例4的萃取组合物的两个样品与cacl2为1mol/l的盐水接触,以增加溶解的cem2阳离子萃取分子的盐带电水平,从而靠近他们的盐饱和度水平(0.1mol/l)。然后,使这两个样品在20℃下与等体积的蒸馏水接触并蒸馏。然后,将两个二相的样品中的一个加热至80℃并保持蒸馏状态。对初始盐电带水平进行评估为80mmol/l,稍后表现出下降,从80℃下的第一再生步骤下降至15.27mmol/l,然而,在20℃的再生期间,盐的剩余浓度为29.3mmol/l。图4阐述了在带有盐的疏水性有机液相与等体积的蒸馏水接触的几个连续步骤之后获得的结果。由于实现相同cacl2总反萃取率的必要再生步骤的数量减少了2倍,因此所述萃取组合物的热再生更有效。在使用中,当实施具有高cem含量并因此具有高盐含量的树脂时,该优点更显著。提高再生温度能够减少接触等体积的蒸馏水的连续步骤的数量,同时允许每次更多的盐的反萃取。由于使用了较少的再生水量,因此提高再生温度还允许通过更高浓度的反萃取盐接触再生水。实施例6:对照例:在室温下从二元混合物nacl/cacl2盐中选择性萃取阳离子如上所述制备含有等摩尔0.05mol/l的nacl和cacl2的混合物盐的海水,并使其与两个根据本发明的萃取组合物接触。这些组合物的不同之处仅在于cem化合物,所述cem化合物还是来自二取代的一级酰胺族,但其大环尺寸发生了变化,分别是16个碳原子(cem1)和24个碳原子(cem2)。如上所述根据本发明的方法获得这些组合物。每个萃取组合物包括0.1mol/l的cem和2.4mol/l的asm9和1,2-二氯苯。1,2-二氯苯(cas#:95-50-1),具有大于99%的纯度,其来自tcichemicals公司。从所述混合物中萃取的阳离子的量(摩尔百分比)如表vi所示:表vicem1/cem2阳离子na+ca++4-叔丁基杯[4]ch2c(=o)net2%e88.0%10.0%4-叔丁基杯[6]ch2c(=o)net2%e4.0%56.0%取决于所选择的cem,在混合物盐中,这些阳离子的萃取会具有更高的选择性,其中作为纯物质被萃取最多的阳离子,大部分为以盐的混合物形式被萃取出来。在这里,共吸收有利于萃取,并且所述萃取在在最初时最好。特别地,含有cem2(其碳环具有24个单元)的制剂在等浓度阳离子混合物中钙-钠萃取率比仅含有一种盐(参考实施例1和3)的溶液的萃取率高14倍,其中仅含有一种盐的溶液的萃取率是2.54。这种萃取能力在去除水结垢中有许多工业应用。实施例7:在室温下从含有nacl和cacl2(具有不同初始浓度)盐的二元混合物中选择性萃取阳离子如上所述制备含有nacl和cacl2混合物的海水,以获得下列混合物中的初始盐水浓度:0.2mol/lnacl和0.03mol/l的cacl2。萃取树脂是由0.1mol/l的cem2和3.52mol/l的asm2和液态asm1补充剂组成,所述液态asm1补充剂也用于流化剂。从混合物中所萃取的阳离子的量(摩尔百分比)如下表vii所示:表viicem2阳离子na+ca++4-叔丁基杯[6]ch2c(=o)net2%e5.0%88.0%在这里,ca/na萃取率之比显示为17.6,这证明了本发明的一个目的,因为在共同阴离子存在的情况下,改善了萃取多盐过程中的差异。实施例8:在室温下,从四种nacl、cacl2、srcl2和bacl2盐混合物中选择性萃取阳离子如上所述制备含有nacl、cacl2、srcl2和bacl2混合物的海水。溶解的盐浓度如表viii中所示(单位为mmol/l)。在改变二价盐浓度的情况下,进行第二次萃取。溶解的盐浓度如表ix中所示(单位为mmol/l)。萃取组合物含有0.1mol/l的cem2和两种asm混合物。该混合物由asm2和asm1组成,所述asm2通常指[3,5-二(三氟甲基)苯甲醇](35tfmbnoh),cas#:32707-89-4,含量高达60%,所述asm1指[3-(三氟甲基)苯甲醇](3tfmbnoh),分子式为c8h7f3o,mw=176,14g/mol,cas#:349-75-7含量高达40%,所述asm2和asm1均被当作流化剂和液体形式的asm。如实施例1中所述进行萃取,并且在室温下进行。所萃取的阳离子的量(摩尔百分比)如表vii和ix所示,所述表viii和ix示出了各自的初始和最终离子浓度(单位为mmol/l)。表viii表ix在这里,其示出了可以实现100%选择性萃取与这些结垢二价阳离子有关的高浓度钠。选择性萃取二价阳离子证实了根据本发明的这些组合物的有效对抗结垢以及纯化水的能力,这是因为选择性萃取了钙ca++、锶和钡。实施例9:合成asm9、asm10、asmc11和asm12化合物合成图=n-c7h15(asm9),n-c9h19(asm10),n-c11h23(asm11),n-c13h27(asm12).协议在搅拌状态下,将酸性氯化物(56.29mmol、1.0等当量)滴入到3,5-二(三氟甲基)苯胺(8.79ml,56.29mmol,1.0等当量)、二氯甲烷(40ml)和三乙胺(8.63ml,61.92mmol,1.1等当量)构成的浓液中。在加入的过程中控制温度,并且不使之超过38℃(二氯甲烷的沸点)。室温下搅拌反应混合物5个小时。加入1m的hcl(50ml)溶液,然后洗涤有机相。用1m的hcl溶液(50ml)和饱和的nacl溶液(50ml)连续洗涤。经na2so4干燥有机相并过滤,然后在降低的压力下蒸发溶剂。用石油醚(冷温或室温下)回收固体残余物,并洗涤,过滤,然后在真空下干燥,以得到想要的酰胺。所使用的石油醚是碳氢化合物,主要由来自vwr的n-戊烷、2-甲基戊烷组成,cas#64742-49-0,其以石油醚40-60℃fprrectrapur的名义售卖。获得的所述化合物的特征如表x所示。化合物asm9、asm10、asmc11和asmc12各自具有国际理论和应用化学联合会(iupac)名:n-[3,5-二(三氟甲基)苯基]辛酰胺、n-[3,5-二(三氟甲基)苯基]癸酰胺、n-[3,5-二(三氟甲基)苯基]十二酰胺、n-[3,5-二(三氟甲基)苯基]十四酰胺,并且进一步由nmr光谱限定。图6示出了asm11化合物的nmr光谱(cdcl3,300mhz),其峰值如下所示:1hnmr(cdcl3,300mhz):δ(ppm)=0.87(t,3j=7.0hz,3h),1.20-1.35(m,20h),1.73(quint.,3j=7.0hz,2h),2.40(t,3j=7.0hz,2h),7.58(s,1h),7.77(bs,1h),8.04(s,2h)。实施例10:在室温下,用cem10萃取单盐盐水溶液在和实施例1和3除了cem为cem10外的相同的条件下进行本实施例10。所使用的cem是4-叔丁基-杯[4]芳烃酸四乙酯(cem10的cas#:97600-39-0)。其是从4-叔丁基杯[4]芳烃,分子式为c44h56o4,cas#为60705-62-6以及溴乙酸乙酯,cas#105-36-2(购自sigma-aldrich的产品)中内部合成的,通过在thf/dmf(体积比为5/1)混合物中对乙醇进行常规添加程序。所使用的asm是asm2,cas#32707-89-4,c9h6f6o,mw=244.13g/mol,白色固体,可从几家经销商处购得。在对7种特定盐进行萃取(重复)后,在室温和等体积的水/萃取制剂下,萃取的阳离子的量在萃取前和萃取后的摩尔百分比如表xi所示:表xi因此,从仅由一个碱性或碱土氯化物组成的海水中萃取阳离子的萃取率根据阳离子的不同在3.7%和66.2%之间变化。在这些单盐溶液中,其表明在碱性阳离子中cem10对于氯化钠是有选择性的,并且二价阳离子的萃取率较差,na/ca的选择性为14。因此,根据本发明的化合物证明了该制剂对于与氯化学相关的工业应用的特性尤其值得关注,即可以从海水中或盐水中以选择性的方式萃取nacl,以供应用于生产naoh、hcl、或甚至cl2的电解槽。实施例11:室温下用cem12萃取单盐盐水溶液除了cem在讨论中为cem12之外,在与实施例1、3和10相同条件下执行本实施例11。所使用的cem是4-叔丁基-杯[6]芳烃酸六乙酯(cem12的cas#:92003-62-8)。其是从4-叔丁基杯[6]芳烃,分子式为c66h84o6,cas#为78092-53-2以及溴乙酸乙酯,cas#105-36-2(购自sigma-aldrich的产品)中内部合成的,通过在thf/dmf(体积比为5/1)混合物中对乙醇进行常规添加程序。所使用的asm是asm2,cas#32707-89-4,c9h6f6o,mw=244.13g/mol,白色固体,可从几家经销商处购得。在对7种特定盐进行萃取(重复)后,在室温和等体积的水/萃取制剂下,萃取的阳离子的量在萃取前和萃取后的摩尔百分比如表xii所示:表xii因此,从仅由一个碱性或碱土氯化物组成的海水中萃取阳离子的萃取率根据阳离子的不同在4.6%和55.7%之间变化。在这些单盐溶液中,其表明cem12对于具有较大直径的碱性阳离子盐具有选择性,并且对二价阳离子的萃取率较差,k/ca的选择性为10.2,但是这一定比rb+和cs+的选择性好,因为该cem12已知是一种良好的铯离子载体。本发明不限于所提出的实施例,并且对于本领域技术人员来说其他实施例将变得显而易见。特别地,在萃取制剂中结合多种cem,以允许与各自cem的特性相关联,从而获得最佳的总体性能,这是可能的。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1