两组胰腺癌血浆诊断标志物谱及其应用的制作方法
本发明涉及生物医学领域中两组胰腺癌血浆诊断标志物谱及其应用。
背景技术:
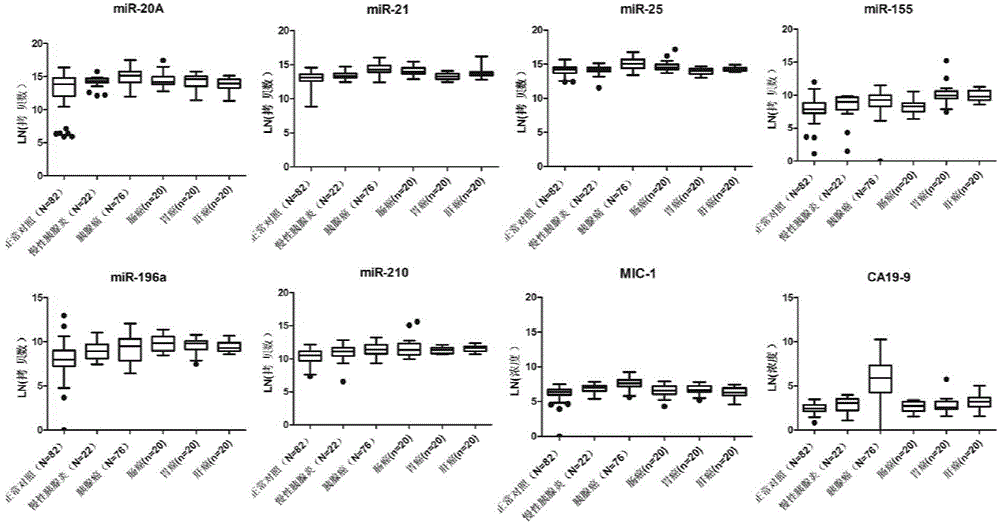
:胰腺癌是目前恶性程度最高的肿瘤之一,患者平均生存期仅2-3月。胰腺癌患者起病隐匿,早期诊断困难,手术切除是目前唯一有望根治胰腺癌的治疗方式。但是80%以上的患者在诊断时已经处于进展期,无法通过手术切除治愈,其5年生存率小于10%。有资料显示少部分接受手术的早期胰腺癌患者术后5年生存率可提高至15-40%。因此早期诊断和早期手术治疗可以显著提高胰腺癌患者的生存率。与传统诊断方式相比,从患者外周血中定量检测肿瘤标志物具有操作简单、能动态监测、易普及筛查等优点,已经成为肿瘤早期诊断和疗效监测的首选方法。目前反应性抗原决定簇1116-NS-19-9(CA19-9,碳水化合物抗原19.9)是FDA和CFDA已经批准上市的主要用于胰腺癌早期诊断的标志物,也是国际上被普遍认可和广泛使用的胰腺癌血清肿瘤标志物。临床实践证明CA19-9对胰腺癌病程和疗效的监测有较高的价值,肿瘤切除后CA19-9可明显降低,当肿瘤复发转移时可再度升高;但CA19-9对诊断胰腺癌敏感性较低,根椐临床研究报道CA19-9诊断胰腺癌的敏感性为59.4-78.2%、特异性为72.5-80%,而早期胰腺癌(<2cm)CA19-9水平升高者低于50.0%。另外CA19-9阳性预测值低,在筛查高危无症状人群发现CA19-9升高者中最终只有低于1%的人被确诊为胰腺癌。其它胰腺癌诊断标志物包括CA242、CA50、Span-1、DuPAN-2、elastase-1也存在灵敏度或特异性差的问题。肿瘤发生是一个涉及多个基因多条通路的复杂过程,单一标志物的诊断效能往往不高,因此发现新的胰腺癌诊断标志物或工具迫在眉睫。技术实现要素:本发明所要解决的技术问题是如何筛查或辅助诊断胰腺癌。为解决上述技术问题,本发明首先提供了下述1)-3)中任一用途:1)M1或M2在制备筛查或辅助诊断胰腺癌产品中的应用;2)所述M1或所述M2在制备胰腺癌预后产品中的应用;3)所述M1或所述M2在制备胰腺癌疗效监测产品中的应用;所述M1包括检测miR-21、MIC-1和反应性抗原决定簇1116-NS-19-9(CA19-9,碳水化合物抗原19.9)表达量的系统;所述M2包括检测miR-25、MIC-1和CA19-9表达量的系统。上述用途中,所述miR-21为序列表中SEQIDNo.1所示的RNA;所述MIC-1为序列表中SEQIDNo.3所示的蛋白质;所述miR-25为序列表中SEQIDNo.2所示的RNA。上述用途中,所述检测miR-21、MIC-1和表达量的系统由检测miR-21表达量的系统、检测MIC-1表达量的系统和检测CA19-9表达量的系统组成;所述检测miR-25、MIC-1和CA19-9表达量的系统由检测miR-25表达量的系统、所述检测MIC-1表达量的系统和所述检测CA19-9表达量的系统组成。所述系统可包括试剂和/或试剂盒和/或仪器。上述用途中,所述检测miR-21表达量的系统为利用定量PCR检测miR-21表达量的系统;所述检测MIC-1表达量的系统为利用酶联免疫反应检测MIC-1表达量的系统;所述检测CA19-9表达量的系统为利用电化学发光免疫分析法检测CA19-9表达量的系统;所述检测miR-25表达量的系统为利用定量PCR检测miR-25表达量的系统。上述用途中,所述检测miR-21表达量的系统可包括检测miR-21表达量的试剂和/或试剂盒和/或仪器,如通过定量PCR反应检测miR-21表达量所需的试剂、试剂盒和仪器。具体来说,检测miR-21表达量的系统可包括扩增miR-21全长或片段的PCR引物对、检测miR-21表达量的试剂盒和进行定量PCR反应所需要的其它试剂和仪器,当然,上述检测miR-21表达量的系统可只由扩增miR-21全长或片段的PCR引物对组成,也可只由检测miR-21表达量的试剂盒组成。所述扩增miR-21全长或片段的PCR引物对和进行定量PCR反应所需要的其它试剂均可独立包装。所述检测miR-25表达量的系统可包括检测miR-25表达量的试剂和/或试剂盒和/或仪器,如通过定量PCR反应检测miR-25表达量所需的试剂、试剂盒和仪器。具体来说,检测miR-25表达量的系统可包括扩增miR-25全长或片段的PCR引物对、检测miR-25表达量的试剂盒和进行定量PCR反应所需要的其它试剂和仪器,当然,上述检测miR-25表达量的系统可只由扩增miR-25全长或片段的PCR引物对组成,也可只由检测miR-25表达量的试剂盒组成。所述扩增miR-25全长或片段的PCR引物对和进行定量PCR反应所需要的其它试剂均可独立包装。上述用途中,所述扩增miR-21全长或片段的PCR引物对可为德国QIAGEN公司产品,货号为MS00009079;所述扩增miR-25全长或片段的PCR引物对可为德国QIAGEN公司产品,货号为MS00003227。所述检测miR-21表达量的系统和所述检测miR-25表达量的系统中,所述进行定量PCR反应所需要的其它试剂可为miScriptSYBRGreenPCRKit(1000)(德国QIAGEN产品,货号为218075)中的10×miScriptUniversalPrimer和/或2×QuantiTectSYBRGreenPCRMasterMix。所述检测miR-21表达量的试剂盒具体可为miScriptSYBRGreenPCRKit(1000)(德国QIAGEN产品,货号为218075)。所述检测miR-25表达量的试剂盒具体可为miScriptSYBRGreenPCRKit(1000)(德国QIAGEN产品,货号为218075)。进行定量PCR反应所需要的仪器均可为定量PCR仪。所述定量PCR仪 具体可为罗氏LightCycler480定量PCR仪。上述用途中,所述检测MIC-1表达量的系统可包括检测MIC-1表达量的试剂和/或试剂盒和/或仪器,如通过酶联免疫反应检测MIC-1表达量所需的试剂、试剂盒和仪器。具体来说,检测MIC-1表达量的系统可包括MIC-1、MIC-1抗体、检测MIC-1表达量的试剂盒和进行酶联免疫吸附实验(ELISA)所需要的其它试剂和仪器,当然,上述检测MIC-1表达量的系统可只由MIC-1和MIC-1抗体组成,也可只由MIC-1组成,也可只由MIC-1抗体组成,也可只由检测MIC-1表达量的试剂盒组成。所述MIC-1、所述MIC-1抗体和进行酶联免疫吸附实验所需要的其它试剂均可独立包装。所述检测CA19-9表达量的系统可包括检测CA19-9表达量的试剂和/或试剂盒和/或仪器,如通过电化学发光免疫分析法检测CA19-9表达量所需的试剂、试剂盒和仪器。具体来说,检测CA19-9表达量的系统可包括CA19-9、CA19-9抗体、检测CA19-9表达量的试剂盒和进行电化学发光免疫分析所需要的其它试剂和仪器,当然,上述检测CA19-9表达量的系统可只由CA19-9和CA19-9抗体组成,也可只由CA19-9组成,也可只由CA19-9抗体组成,也可只由检测CA19-9表达量的试剂盒组成。所述CA19-9、所述CA19-9抗体和进行电化学发光免疫分析所需要的其它试剂均可独立包装。上述用途中,所述MIC-1抗体可为MIC-1单克隆抗体和/或MIC-1多克隆抗体;所述CA19-9抗体可为CA19-9单克隆抗体和/或CA19-9多克隆抗体。上述用途中,所述MIC-1可为标记物标记的MIC-1;所述CA19-9可为标记物标记的CA19-9。上述用途中,所述MIC-1抗体可为用生物素标记的MIC-1抗体;所述CA19-9抗体可为用生物素标记的CA19-9抗体。上述用途中,所述MIC-1抗体可识别氨基酸序列是序列表中SEQIDNo.3的蛋白质;所述CA19-9抗体可识别所述CA19-9。上述用途中,所述MIC-1和所述MIC-1抗体均可为美国R&D生产的货号为DY957的试剂盒中的试剂;所述CA19-9和所述CA19-9抗体均可为美国Roche生产的货号为11776193122的试剂盒中的试剂。上述用途中,所述检测MIC-1表达量的试剂盒具体可为美国R&D产品,货号为DY957。所述检测CA19-9表达量的试剂盒具体可为美国Roche产品,货号为11776193122。上述用途中,所述M1还包括数据处理装置1,所述数据处理装置1用于将来自待测对象的miR-21、MIC-1和CA19-9的表达量转换为所述待测对象的诊断值,根据所述待测对象的诊断值确定所述待测对象是否为胰腺癌患者;所述M2还包括数据处理装置2,所述数据处理装置2用于将来自待测对象的miR-25、MIC-1和CA19-9的表达量转 换为所述待测对象的诊断值,根据所述待测对象的诊断值确定所述待测对象是否为胰腺癌患者。上述用途中,所述将来自待测对象的miR-21、MIC-1和CA19-9的表达量转换为所述待测对象的诊断值包括将所述来自待测对象的miR-21、MIC-1和CA19-9的表达量代入公式1得到所述待测对象的诊断值;所述公式1为:Index1=1.971×ln(MIC-1)+1.795×ln(miR-21)+1.020×ln(CA19-9)-42.305;公式1中miR-21、MIC-1和CA19-9分别表示miR-21、MIC-1和CA19-9在所述待测对象血浆中的表达量,Index1为待测对象的诊断值;所述将来自待测对象的miR-25、MIC-1和CA19-9的表达量转换为所述待测对象的诊断值包括将所述来自待测对象的miR-25、MIC-1和CA19-9的表达量代入公式2得到所述待测对象的诊断值;所述公式2为:Index2=2.138×ln(MIC-1)+1.772×ln(miR-25)+1.125×ln(CA19-9)-45.006;公式2中miR-25、MIC-1和CA19-9分别表示miR-21、MIC-1和CA19-9在所述待测对象血浆中的表达量,Index2为待测对象的诊断值。上述用途中,所述M1可为所述检测miR-21、MIC-1和表达量的系统;所述M2可为所述检测miR-25、MIC-1和CA19-9表达量的系统。上述用途中,所述检测miR-21表达量具体可为检测人血清或血浆中的miR-21浓度;所述检测miR-25表达量具体可为检测人血清或血浆中的miR-25浓度;所述检测MIC-1表达量具体可为检测人血清或血浆中的MIC-1浓度;所述检测CA19-9表达量具体可为检测人血清或血浆中的CA19-9浓度。上述用途中,当用所述M1筛查胰腺癌患者时,如果待测对象的Index1大于0,该待测对象为疑似胰腺癌患者;如果待测对象的Index1小于或等于0,该待测对象为非疑似胰腺癌患者;当用所述M2筛查胰腺癌患者时,如果待测对象的Index2大于0,该待测对象为疑似胰腺癌患者;如果待测对象的Index2小于或等于0,该待测对象为非疑似胰腺癌患者。为解决上述技术问题,本发明还提供了以miR-21、MIC-1和CA19-9作为胰腺癌标志物的筛查或辅助诊断胰腺癌的系统在制备筛查或辅助诊断胰腺癌产品中的应用。上述应用中,所述筛查或辅助诊断胰腺癌的系统为所述M1。为解决上述技术问题,本发明还提供了以miR-25、MIC-1和CA19-9作为胰腺癌标志物的筛查或辅助诊断胰腺癌的系统在制备筛查或辅助诊断胰腺癌产品中的应用。上述应用中,所述筛查或辅助诊断胰腺癌的系统为所述M2。为解决上述技术问题,本发明还提供了筛查或辅助诊断胰腺癌产品。本发明所提供的筛查或辅助诊断胰腺癌产品,为所述M1或所述M2。实验证明,当以正常对照组、慢性胰腺炎对照组、胃癌对照组、肠癌对照组和肝癌对照组为对照组,在实验1中对胰腺癌病例组的Index1进行分析时,曲线下面积AUC=0.968,灵敏度为89.5%,特异度为90.9%,准确性为90.4%;在实验1中对胰腺癌病例组的Index2进行分析时,曲线下面积AUC=0.967,灵敏度为89.5%,特异度为91.5%,准确性为90.8%;在实验2中对胰腺癌病例组的Index1进行分析时,曲线下面积AUC=0.933,灵敏度为89.2%,特异度为91.2%,准确性为90.6%;在实验2中对胰腺癌病例组的Index2进行分析时,曲线下面积AUC=0.921,灵敏度为83.8%,特异度为92.1%,准确性为89.7%。标志物谱Index1和Index2均比miR-21、miR-25、MIC-1和CA19-9标志物作为单一指标具有较好的灵敏度、特异性、准确性和AUC。实验证明,本发明的M1和M2的系统以及标志物谱Index1和Index2可用来筛查或辅助诊断胰腺癌。附图说明图1为实验1中胰腺癌标志物在各血浆标本中的表达量。其中,LN表示ln。图2为实验2中胰腺癌标志物在各血浆标本中的表达量。其中,LN表示ln。图3为Index1和Index2在实验1和实验2中的ROC曲线和分布图。A中方程1表示Index1,方程2表示Index2;B中非胰腺癌表示正常对照组、胃癌对照组、肠癌对照组、肝癌对照组和慢性胰腺炎对照组的血浆标本。具体实施方式下面结合具体实施方式对本发明进行进一步的详细描述,给出的实施例仅为了阐明本发明,而不是为了限制本发明的范围。下述实施例中的实验方法,如无特殊说明,均为常规方法。下述实施例中所用的材料、试剂等,如无特殊说明,均可从商业途径得到。受试者工作特征曲线(receiveroperatingcharacteristiccurve,简称ROC曲线):是根据一系列不同的二分类方式(分界值或决定阈),以灵敏度(真阳性率,%)为纵坐标,100-特异度(%)为横坐标绘制的曲线。ROC曲线下面积是重要的试验准确度指标,ROC曲线下面积越大,试验的诊断价值越大。灵敏度(真阳性率):实际有病而按试验标准被正确判断为有病的百分率,灵敏度越大越好,理想灵敏度为100%。特异度(真阴性率):实际无病而按试验标准被正确判断为无病的百分率,特异度越大越好,理想特异度为100%。实施例1、血浆中用于筛查胰腺癌的标志物的表达量的检测本实施例涉及357个人血浆标本,其中包括胰腺癌病例组血浆标本113个,慢 性胰腺炎对照组血浆标本32个,肠癌对照组血浆标本30个,胃癌对照组血浆标本30个,肝癌对照组血浆标本30个及正常对照组的正常健康人(该正常健康人为CT、超声及肿瘤标志物检查无异常的健康人)的血浆标本122个。各组别的基本信息见表1,胰腺癌病例组病人和正常对照组中人的性别、年龄与身体质量指数(BodyMassIndex,BMI)均无显著性差异。表1、各组别的基本信息注:性别(男/女)行中,“/”左边的数字表示男性的个体数,“/”右边的数字表示女性的个体数;“—”表示无该数据。将以上每个组别中的人群分为两组,分别进行实验1和实验2,实验1用于建立标志物谱,每个实验用到的每个组别的标本数见表2。表2、实验1和实验2中的各标本数(个)一、血浆中用于筛查胰腺癌的标志物的表达量的检测本实施例涉及了八种胰腺癌的标志物,包括六种microRNA和两种蛋白质,分别为miR-20A、miR-21、miR-25、miR-155、miR-196A和miR-210以及巨噬细胞抑制因子-1(MIC-1)和CA19-9。将由利用定量PCR检测miR-21表达量的系统、利用 酶联免疫反应检测MIC-1表达量的系统和利用电化学发光免疫分析法检测CA19-9表达量的系统组成的系统命名为M1,将由利用定量PCR检测miR-25表达量的系统、利用酶联免疫反应检测MIC-1表达量的系统和利用电化学发光免疫分析法检测CA19-9表达量的系统组成的系统命名为M2。首先按照下述操作步骤制备血浆标本:(1)利用BD抗凝管取新鲜血液后,冰上放置并于2小时内转移至实验室;(2)4℃2000rpm离心10分钟(离心后血液分离为三层,上层清液为血浆,中间为白细胞,下层为红细胞。);(3)小心吸取上层血浆至一个新的1.5mlEppendorf管中,并吸取中层白细胞保存;(4)上层血浆液4℃12000rpm再次离心10分钟(离心后可看到最下次有少许沉淀);(5)吸取上清并按0.5ml/管分装至新的1.5mlEppendorf管中,与白细胞一起于-80℃冰箱保存待用。注:标本处理和保存过程所用的枪头及1.5mlEppendorf管均为无RNase-free。1、microRNA表达水平的检测使用miRNeasySerum/PlasmaKit(50)(德国QIAGEN产品,货号为217184)提取血浆总RNA,并利用miScriptIIRTKit(50)(德国QIAGEN产品,货号为218161)进行反转录,得到各血浆标本cDNA。利用定量PCR检测miR-20A、miR-21、miR-25、miR-155、miR-196A和miR-210在各血浆标本中的表达量,外参为miR-39,用到的试剂盒为miScriptSYBRGreenPCRKit(1000)(德国QIAGEN产品,货号为218075)。具体检测方法如下:1)冰上融化2×QuantiTectSYBRGreenPCRMasterMix、10×miScriptUniversalPrimer、10×miScriptPrimerAssay、血浆标本cDNA及RNase-free水后,各自混匀备用;2)根据表3中的组分和体积配制每孔20μl的反应体系,加至96孔反应板中,每种反应各设三个重复和一个空白对照;每个反应板均扩增浓度分别为101、102、103、104、105和106拷贝/μl的miR-39。表3、20μl反应体系的组分和体积组分体积(μl)2×QuantiTectSYBRGreenPCRMasterMix1010×miScriptUniversalPrimer(通用引物)210×miScriptPrimerAssay(miRNA特异性引物)2RNase-free水5血浆标本cDNA(最后一步加入)1总体积20注:血浆标本cDNA在反应体系中的浓度为1-3ng/20μl。其中,检测外参miR-39表达量用到的10×miScriptPrimerAssay(miRNA特异性引物)为德国QIAGEN产品,货号为MS00019789;检测miR-20A表达量用到的10×miScriptPrimerAssay(miRNA特异性引物)为德国QIAGEN公司产品,货号为MS00003199;检测miR-21用到的10×miScriptPrimerAssay(miRNA特异性引物)为德国QIAGEN公司产品,货号为MS00009079;检测miR-25用到的10×miScriptPrimerAssay(miRNA特异性引物)为德国QIAGEN公司产品,货号为MS00003227;检测miR-155用到的10×miScriptPrimerAssay(miRNA特异性引物)为德国QIAGEN公司产品,货号为MS00031486;检测miR-196A用到的10×miScriptPrimerAssay(miRNA特异性引物)为德国QIAGEN公司产品,货号为MS00031563;检测miR-210用到的10×miScriptPrimerAssay(miRNA特异性引物)为德国QIAGEN公司产品,货号为MS00003801。3)将96孔反应板放入罗氏LightCycler480定量PCR仪中,选择AbsoluteQuantification,并按以下Real-timePCR的循环条件设置程序并进行PCR反应:4)数据分析编辑每个反应孔的信息,包括标本号及检测的基因等,重点编辑标准曲线孔的信息,选择AbsQuant/2ndDerivativeMax分析程序,分析结果呈现为根据标准曲线计算得出的每个检测孔的表达值及Ct值,记录每个孔的Ct值(阈值循环,即PCR过程中检测荧光强度达到设置阈值强度时所经历的PCR循环数)。同一样品的3个重复孔中的Ct值标准偏差必须小于0.387,否则数据不可靠,重复相应实验。取3孔的平均Ct值为样品的结果Ct值。若标准曲线各浓度复孔平均Ct值有意义,则反应板中各孔的表达量值有意义,根据内参miR-39的表达量及原始加入的量计算各样本的提取效率及对应检测基因的表达量。2、巨噬细胞抑制因子-1(MIC-1)表达量的检测利用ELISA检测巨噬细胞抑制因子-1(MIC-1)在各血浆标本中的表达量,用到的试剂盒为美国R&DGDF-15ELISAsystem,货号为DY957,其中,捕获抗体、检测抗体和标准品均为该试剂盒中试剂。2.1实验前准备:(1)将PBS、ELISAWashingBuffer、ReagentDiluent于常温放置待用。(2)在捕获抗体干粉中加入1mlPBS,混匀得到浓度为360μg/ml的捕获抗体储存液,分装后-80℃保存待用。(3)在检测抗体干粉中加入1mlReagentDiluent,混匀得到浓度为9μg/ml的检测抗体储存液,分装后-80℃保存待用;用ReagentDiluent将检测抗体储存液稀释180倍后得到浓度为50ng/ml的检测抗体工作液。(4)在标准品干粉中加入0.5mlReagentDiluent,混匀得到浓度为120ng/ml的标准品储存液,分装后-80℃保存,利用ReagentDiluent稀释120倍后得到浓度为1ng/ml(即1000pg/ml)的标准品工作液,将标准品工作液按照2倍梯度稀释后得到不同浓度梯度的标准品工作液(即浓度分别为500pg/ml、250pg/ml、125pg/ml、62.5pg/ml、31.25pg/ml和15.625pg/ml的标准品工作液)。(5)利用ReagentDiluent将Streptavidin-HRP储存液稀释200倍后得到Streptavidin-HRP工作液。(6)用ReagentDiluent将各血浆样本稀释5倍(血浆原液与ReagentDiluent的体积比为1:4),得到稀释的血浆样本。2.2利用ELISA方法检测血浆标本中蛋白质的表达量(1)用PBS将捕获抗体储存液稀释180倍后得到浓度为2.0μg/ml的捕获抗体工作液,向96孔酶标板的每孔中加入100μl的捕获抗体工作液,室温过夜;(2)弃去酶标板中的捕获抗体工作液,向酶标板的每孔中加入300μl的WashingBuffer,轻晃振匀后弃WashingBuffer以清洗酶标板的每个孔,重复上述清洗3次,用吸水纸吸干酶标板的每个孔中的残液;(3)向酶标板的每孔中加入300μlReagentDiluent,室温孵育1小时进行封闭;(4)弃去酶标板中的液体,向酶标板的每孔中加入300μl的WashingBuffer,轻晃振匀后弃WashingBuffer以清洗酶标板的每个孔,重复上述清洗3次;(5)向酶标板的每孔中加入100μl稀释的血浆标本或不同浓度梯度的标准品工作液(每孔一个血浆标本或一种浓度的标准品工作液),室温静置2小时;同时设置空白对照孔,每个稀释的血浆标本、每种浓度的标准品工作液和空白对照均设置3个复孔;(6)弃去酶标板中的液体,向酶标板的每孔加入300μlWashingBuffer清洗孔板,重复3次,用吸水纸吸干酶标板的每个孔中的残液;(7)向酶标板的每孔中加入100μl的检测抗体工作液,室温静置2小时;(8)弃去酶标板中的液体,向酶标板的每孔加入300μlWashingBuffer清 洗孔板,重复3次,用吸水纸吸干酶标板的每个孔中的残液;(9)向酶标板的每孔中加入每孔加入100μl的Streptavidin-HRP工作液,室温避光静置20分钟;(10)弃去酶标板中的液体,向酶标板的每孔加入300μlWashingBuffer清洗孔板,重复3次,用吸水纸吸干酶标板的每个孔中的残液;(11)将显色液A和显色液B按1:1混匀得到工作显色液,向酶标板的每孔加入100μl工作显色液,室温避光静置20分钟;(12)向酶标板的每孔加入50μl终止液,轻摇孔板一遍反应完全终止;(13)利用酶标仪检测450nm激发光下的吸光度;(14)数据处理:首先利用SD值分析检测每个稀释的血浆标本3个复孔的一致性,SD<0.3为一致性较好,然后计算每个稀释的血浆标本3个复孔吸光度的均值。计算不同浓度的标准品的三个复孔吸光度的均值和空白对照的三个复孔吸光度的均值,根据标准品的浓度和各浓度标准品的吸光度均值绘制标准曲线,列出标准品方程,计算R方(R方>0.99为佳)。将每个稀释的血浆标本的吸光度的均值代入标准品方程,计算各稀释的血浆标本中蛋白质的浓度,乘以稀释倍数,得到每个血浆标本中蛋白质的表达量。3、CA19-9表达量的检测利用电化学发光免疫分析法检测血浆标本中CA19-9的表达量,用到的仪器和试剂为Roche(罗氏,德国)cobasE601全自动电化学发光免疫分析仪和该仪器配套的糖类抗原19-9定量测定试剂盒(电化学发光法)(德国罗氏诊断有限公司产品,货号为11776193122)。检测原理如下:夹心法,总检测时间:18分钟第一次孵育:10μl标本、生物素化的CA19-9单克隆特异性抗体和钌(Ru)a标记的CA19-9单克隆抗体一起孵育,形成抗原抗体夹心复合物,第二次孵育:添加包被链霉亲和素的磁珠微粒进行孵育,复合体与磁珠通过生物素和链霉亲和素的作用结合。将反应液吸入测量池中,通过电磁作用将磁珠吸附在电极表面。未与磁珠结合的物质通过ProCell被去除。给电极加以一定的电压,使复合体化学发光,并通过光电倍增器测量发光强度。仪器自动通过2点校正的定标曲线计算得到检测结果。二、用于筛查胰腺癌的标志物谱的建立1、实验1中筛选胰腺癌特异的血浆标志物及标志物谱的建立实验1中的用到的各血浆标本如表2所示,由于microRNA的表达水平数量级 较大,数据分布部分不呈正态分布,所有表达水平的实际数值均以LOG(e)处理,各组中miR-20A、miR-21、miR-25、miR-155、miR-196A与miR-210以及MIC-1与CA19-9的表达量以ln(即LOG(e))处理后的数据见图1与图2。(1)筛选胰腺癌高表达的标志物:以T检验统计分析比较胰腺癌病例组与正常对照组两组间、胰腺癌病例组与慢性胰腺炎对照组两组间、胰腺癌病例组与正常对照组加慢性胰腺炎对照组之间的miR-20A、miR-21、miR-25、miR-155、miR-196A、miR-210、MIC-1和CA19-9表达量的差异(图1)。实验结果显示,与正常对照组相比,胰腺癌病例组的miR-20A、miR-21、miR-25、miR-155、miR-196A、miR-210、MIC-1和CA19-9均高表达且有统计学意义(P<0.000);与慢性胰腺炎对照组相比,胰腺癌病例组的miR-20A、miR-21、miR-25、MIC-1和CA19-9有统计学意义的高表达;与正常对照组加慢性胰腺炎对照组相比,胰腺癌病例组的miR-20A、miR-21、miR-25、miR-155、miR-196A、miR-210、MIC-1和CA19-9均高表达且有统计学意义。结果表明miR-20A、miR-21、miR-25、MIC-1和CA19-9不仅可以作为在正常健康人中筛选胰腺癌患者的标志物,还能作为从慢性胰腺炎患者中筛选胰腺癌患者的标志物(图2)。(2)筛选胰腺癌特异高表达的标志物:为鉴别候选标志物的组织特异性,以T检验统计分析比较胰腺癌病例组与其他消化道肿瘤对照组(胃癌对照组、肠癌对照组和肝癌对照组)间的miR-20A、miR-21、miR-25、miR-155、miR-196A、miR-210、MIC-1和CA19-9表达量的差异。实验结果显示,与其他消化道肿瘤对照组(胃癌对照组、肠癌对照组和肝癌对照组)相比,胰腺癌病例组中的miR-20A、miR-21、miR-25、MIC-1和CA19-9高表达且有统计学意义(P<0.05)。而胰腺癌病例组中的miR-155、miR-196A和miR-210仅在与正常对照组相比时有差异。结果表明,miR-20A、miR-21、miR-25、MIC-1和CA19-9在胰腺癌患者中特异性地高表达,均可以用来能区别胰腺癌患者与正常健康人、慢性胰腺炎患者及其他消化道肿瘤患者的标志物。(3)胰腺癌血浆诊断标志物谱的建立:基于上述候选标志物在胰腺癌患者和正常健康人、慢性胰腺炎患者及其他消化道肿瘤患者血浆标本中的表达量,利用单因素和多因素LOGISTIC回归分析候选标志物的诊断价值,结果见表4。表4、利用单因素和多因素LOGISTIC回归分析候选标志物的结果注:“—”表示无该数据。实验结果显示,miR-20A、miR-21、miR-25、MIC-1和临床诊断指标CA19-9的OR值在胰腺癌病例组与正常对照组、胰腺癌病例组与慢性胰腺炎对照组、胰腺癌病例组与其他消化道肿瘤(胃癌、肠癌和肝癌)对照组间均大于1且95%CI值的下限也大于1,表明miR-20A、miR-21、miR-25、MIC-1和临床诊断指标CA19-9均能区别胰腺癌患者与正常健康人、胰腺癌患者与慢性胰腺炎患者、胰腺癌患者与其他消化道肿瘤(胃癌、肠癌和肝癌)患者;而miR-155、miR-196A和miR-210的OR值仅在胰腺癌病例组与正常对照组间大于1且95%CI值的下限也大于1,表明miR-155、miR-196A和miR-210仅能区别胰腺癌患者与正常健康人。多因素Logistic回归分析发现,可将miR-21、MIC-1和CA19-9组合到一起进行联合分析诊断胰腺癌患者,将进行联合分析的标志物谱命名为Index1(即诊断值);可将miR-25、MIC-1和CA19-9组合到一起进行联合分析诊断胰腺癌患者,将进行联合分析的标志物谱命名为Index2(即诊断值)。标志物谱的诊断方程分别为:Index1=1.971×ln(MIC-1)+1.795×ln(miR-21)+1.020×ln(CA19-9)-42.305;Index2=2.138×ln(MIC-1)+1.772×ln(miR-25)+1.125×ln(CA19-9)-45.006。其中,miR-21、miR-25、MIC-1和CA19-9分别表示miR-21、miR-25、MIC-1和CA19-9在血浆标本中的表达量。2、标志物谱诊断胰腺癌患者的诊断效能分析实验2中的用到的各血浆标本如表2所示。根据实验1和实验2中的ln(即LOG(e))处理后的miR-21、miR-25、MIC-1和CA19-9的表达量以及步骤1中的诊断方程计算各血浆标本的Index1和Index2数值。根据实验1和实验2的结果分析miR-21、miR-25、MIC-1、CA19-9、Index1和Index2的诊断灵敏度、特异性、准确性和ROC的曲线下面积(图3),并分别与miR-21、miR-25、MIC-1和CA19-9标志物作为单一指标的诊断效能(灵敏度、特异性、准确性和ROC的曲线下面积)进行比较,结果见表5。表5、实验1和实验2中的不同标志物和标志物谱的诊断效能注:表5中,指标列中的miR-21行表示用miR-21在血浆中的表达量这一单一指标进行胰腺癌诊断的诊断效能;指标列中的miR-21行表示用miR-21在血浆中的表达量这一单一指标进行胰腺癌诊断的诊断效能;指标列中的miR-25行表示用miR-25在血浆中的表达量这一单一指标进行胰腺癌诊断的诊断效能;指标列中的MIC-1行表示用MIC-1在血浆中的表达量这一单一指标进行胰腺癌诊断的诊断效能;指标列中的CA19-9行表示用CA19-9在血浆中的表达量这一单一指标进行胰腺癌诊断的诊断效能;指标列中的Index1(miR-21,MIC-1,CA199)行表示用miR-21、MIC-1和CA19-9在血浆中的表达量得到的Index1进行胰腺癌诊断的诊断效能;指标列中的Index2(miR-25,MIC-1,CA199)行表示用miR-25、MIC-1和CA19-9在血浆中的表达量得到的Index2进行胰腺癌诊断的诊断效能。结果显示,当以正常对照组、慢性胰腺炎对照组、胃癌对照组、肠癌对照组和肝癌对照组为对照组,在实验1中对胰腺癌病例组的Index1进行分析时,曲线下面积AUC=0.968,灵敏度为89.5%,特异度为90.9%,准确性为90.4%,该方法判定为胰 腺癌患者的阈值为0,即当Index1大于0时,待测对象为疑似胰腺癌患者,当Index1小于或等于0时,待测对象为非疑似胰腺癌患者;在实验1中对胰腺癌病例组的Index2进行分析时,曲线下面积AUC=0.967,灵敏度为89.5%,特异度为91.5%,准确性为90.8%,该方法判定为胰腺癌患者的阈值为0,即当Index2大于0时,待测对象为疑似胰腺癌患者,当Index2小于或等于0时,待测对象为非疑似胰腺癌患者;在实验2中对胰腺癌病例组的Index1进行分析时,曲线下面积AUC=0.933,灵敏度为89.2%,特异度为91.2%,准确性为90.6%,该方法判定为胰腺癌患者的阈值为0,即当Index1大于0时,待测对象为疑似胰腺癌患者,当Index1小于或等于0时,待测对象为非疑似胰腺癌患者;在实验2中对胰腺癌病例组的Index2进行分析时,曲线下面积AUC=0.921,灵敏度为83.8%,特异度为92.1%,准确性为89.7%,该方法判定为胰腺癌患者的阈值为0,即当Index2大于0时,待测对象为疑似胰腺癌患者,当Index2小于或等于0时,待测对象为非疑似胰腺癌患者。实验结果显示,不管是在实验1中还是在实验2中,标志物谱Index1和Index2均比miR-21、miR-25、MIC-1和CA19-9标志物作为单一指标具有较好的灵敏度、特异性、准确性和AUC。实验结果表明,本发明的标志物谱Index1和Index2均可用来筛查或辅助诊断胰腺癌。当前第1页1 2 3
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1