一种癌胚抗原浓度的检测方法与流程
本发明涉及一种癌胚抗原(CEA)浓度的检测方法,尤其涉及一种CEA抗体—CEA—CEA适配体/金纳米棒三层夹心式结构的构建及其用于CEA浓度的检测方法;属于生物传感技术领域。
背景技术:
癌胚抗原是一个广谱性肿瘤标志物,它能向人们反映出多种肿瘤的存在,对大肠癌、乳腺癌和肺癌的疗效判断、病情发展、监测和预后估计是一个较好的肿瘤标志物。97%的健康成人血清CEA浓度在2.5g/L以下,原发性结肠癌患者CEA增高占45~80%。除原发性结肠癌以外,胰腺癌、胆管癌、胃癌、食管癌、腺癌、肺癌、乳腺癌和泌尿系统的肿瘤阳性率也很高,一般在50~70%。因此该指标检测对于诊断某些疾病具有较大意义。
传统的测定CEA的方法有荧光免疫分析、放射免疫法,酶联免疫检测法等。这些检测方法虽然在一定程度上灵敏有效,但对技术要求高,耗时耗力,且对仪器有一定的要求,各自具有一定的局限性。相比以上方法,电化学检测法具有仪器简单、操作方便以及灵敏度高等优点。
技术实现要素:
针对现有的检测CEA方法存在的不足,本发明的目的是在于提供一种选择性好、灵敏度高、检测限低、检测范围宽的检测CEA浓度的方法。
为了实现上述技术目的,本发明提供了一种CEA浓度的检测方法,该方法包括以下步骤:
1)在金纳米棒载体上修饰CEA适配体,得到CEA适配体/金纳米棒复合物;
2)将CEA抗体修饰到氧化石墨烯表面后,将所述氧化石墨烯固定到电极表面,再采用牛血清白蛋白对所述电极表面进行封闭,得到CEA抗体修饰电极;
3)取一系列不同浓度的标准CEA溶液分别滴加至所述CEA抗体修饰电极的表面进行CEA与CEA抗体之间的特异性结合反应,得到一系列CEA抗体—CEA修饰电极;
4)将所述CEA适配体/金纳米棒复合物滴加至各CEA抗体—CEA修饰电极表面进行CEA与CEA适配体之间的特异性结合反应,得到一系列含CEA抗体—CEA—CEA适配体/金纳米棒复合物三层夹心式结构的电极;
5)向各含CEA抗体—CEA—CEA适配体/金纳米棒复合物三层夹心式结构的电极表面分别滴加钼酸钠溶液进行反应后,采用方波伏安法进行测定,得到一系列方波伏安曲线;
6)将各方波伏安曲线中的峰电流值与对应的CEA浓度做标准曲线;
7)取待测CEA溶液替换标准CEA溶液按3)、4)和5)的步骤进行操作,得到相应峰电流值,依据标准曲线,即得待测CEA溶液的浓度。
优选的方案,在金纳米棒载体溶液中加入含末端巯基修饰的CEA适配体的溶液,在室温下反应,即得CEA适配体/金纳米棒复合物。
较优选的方案,所述金纳米棒载体通过如下方法制备得到:先采用NaBH4还原HAuCl4,得到纳米金种子溶液,所述纳米金种子溶液加入到含十六烷基三甲基溴化铵、HAuCl4、AgNO3和抗坏血酸的溶液中反应,得到金纳米棒载体。更优选的方案,含十六烷基三甲基溴化铵、HAuCl4、AgNO3和抗坏血酸的溶液由45~55mL浓度为0.05~0.15M的十六烷基三甲基溴化铵溶液,0.8~1.4mL质量百分比浓度为0.5~1.5%的HAuCl4溶液,0.2~0.6mL浓度为5~15mM的AgNO3溶液和0.25~0.35mL浓度为0.05~0.15M的抗坏血酸组成。
优选的方案,氧化石墨烯溶液采用(1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐)和N-N-羟基琥珀酰亚胺溶液活化后,与CEA抗体进行反应,得到CEA抗体修饰氧化石墨烯,所述CEA抗体修饰氧化石墨烯滴加到电极表面,得到CEA抗体修饰电极。
优选的方案,将浓度分别为1pg/mL、5pg/mL、10pg/mL、100pg/mL、1ng/mL和10ng/mL的一系列标准CEA溶液分别滴加到CEA抗体修饰电极的表面,进行特异性结合反应。
较优选的方案,所述特异性结合反应的条件为:温度为36~37℃,时间为1~2h。
优选的方案,步骤4)中的特异性结合反应的条件为:温度为36~37℃,时间为1~2h。
优选的方案,所述钼酸钠溶液的浓度为1~5mmol/L。
优选的方案,所述方波伏安法的测定条件为:以0.3~0.7mol/L的硫酸溶液为电解液,在0~0.5V电压范围内,频率为10~20Hz。
本发明的技术方案中,含CEA抗体—CEA—CEA适配体/金纳米棒复合物三层夹心式结构与钼酸钠溶液反应生成磷钼酸盐沉淀。CEA适配体上的磷酸根与钼酸钠反应生成电化学活性的磷钼酸钠盐沉淀,产生氧化还原电流通过方波伏安法进行测定。
本发明的技术方案中,在金纳米棒载体溶液中加入末端巯基修饰的适配体,在25~37℃温度下反应2~3h,即得CEA适配体/金纳米棒复合物。巯基的作用是通过巯基和金之间的共价键作用将CEA适配体固定到金纳米棒载体上。
本发明的技术方案中,末端修饰巯基的CEA适配体序列为SH-ATACCAGC TTATTCAATT。可直接购买于上海生工生物工程有限公司。
本发明的技术方案中,氧化石墨烯溶液与1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐和N-N-羟基琥珀酰亚胺溶液在25~37℃混合反应1~3h,将石墨烯表面活化,将活化石墨烯分离,与CEA抗体反应,即得CEA抗体修饰氧化石墨烯。将CEA抗体修饰氧化石墨烯直接滴加到电极表面得到CEA抗体修饰电极。其中,CEA抗体与活化石墨烯的反应比例为以浓度为10μg/mL的CEA抗体溶液与浓度为1mg/mL的活化石墨烯溶液反应,反应得到CEA抗体修饰氧化石墨烯,将CEA抗体修饰氧化石墨烯分离,洗涤2次。
本发明的技术方案中,所述金纳米棒载体通过如下方法制备得到:首先通过NaBH4还原HAuCl4得到纳米金种子溶液;往50mL 0.1M的十六烷基三甲基溴化铵溶液中加入1.1mL HAuCl4(1%w/w),0.4mL AgNO3(10mM)和0.29mL抗坏血酸(0.1M),得到混合溶液;往上述混合溶液中加入合成的纳米金种子溶液,持续反应24小时,即得到金纳米棒载体。
本发明的技术方案中,将CEA抗体修饰石墨烯溶液直接滴加在电极表面,得到CEA抗体修饰电极;CEA抗体修饰石墨烯溶液的体积为3~8μL,浓度为0.5~1.5mg/mL。
本发明的技术方案中,采用的电极为玻碳电极。
本发明的技术方案中,步骤5)中的反应条件为:在36~38℃温度下反应15~25min。
本发明的检测CEA浓度的方法是基于构建的CEA抗体—CEA—CEA适配体/金纳米棒复合物三层夹心式结构实现,该三层夹心式结构用于检测CEA浓度,具有选择性好、灵敏度高、检测限低,且检测范围宽等优点。本发明的技术方案,首先进行金纳米棒载体的合成,将带巯基的CEA适配体结合到金纳米棒载体表面;将CEA抗体修饰氧化石墨烯固定到电极表面,用牛血清白蛋白对电极表面进行封闭,防止在电极表面发生非特异性吸附;然后在电极表面滴加CEA进行反应,电极上抗体能与CEA进行特异性识别并结合;往电极上加入CEA适配体/金纳米棒复合物,被抗体捕获的CEA能与金纳米棒上的适配体发生特异性结合;在电极上滴加钼酸钠反应生成磷钼酸钠盐沉淀;以0.5mol/L的硫酸溶液为电解液,在0-0.5V电压范围内,进行测定方波伏安曲线,曲线峰电流与CEA浓度在一定范围内呈线性关系,从而实现CEA溶液浓度的检测。而在传统的适配体传感器中,需要在适配体上修饰信号分子,实现信号检测。而在本发明中采用适配体同时作为CEA捕获分子和信号分子,简化了传感器制备和检测步骤。通过加入不同浓度CEA经电化学测量处理后得到标准曲线,该标准曲线为一条直线(如图4),CEA浓度越大电流值越大;再加入未知浓度CEA测得电流值,将该电流值与标准曲线进行比较得到未知浓度CEA的浓度。本发明的技术方案利用金纳米棒纳米粒子大的比表面积,能结合大量适配体分子,促进信号放大,增强了灵敏度,降低了检测限。
与现有技术相比,本发明技术方案的优点在于:
(1)本发明的技术方案以金纳米棒为载体构建CEA抗体—CEA—CEA适配体/金纳米棒复合物三层夹心式结构,金纳米棒大的比表面积增加了适配体负载量,且与CEA之间通过特异性结合,促进信号放大,进而提高检测灵敏度,降低检测限,检测范围广。
(2)本发明的技术方案可测浓度为0.1pg/mL~10ng/mL的CEA,而人类正常血清中CEA的浓度为2.5ng/mL,当患相关肿瘤时,CEA浓度可异常增高。因此,通过本发明的技术方案对经过稀释后患者血清具有足够的检测灵敏度。
(3)本发明同时采用CEA适配体作为捕获分子和信号分子,大大简化了CEA适配体传感器制备和检测步骤。本发明技术基于CEA抗体—CEA—CEA适配体/金纳米棒复合物三层夹心式结构检测CEA的方法检测范围宽,无需借助精密仪器设备,并且可推广至其他传感器,用于对不同蛋白或小分子的浓度进行检测。
附图说明
【图1】为本发明的检测方法的原理示意图;
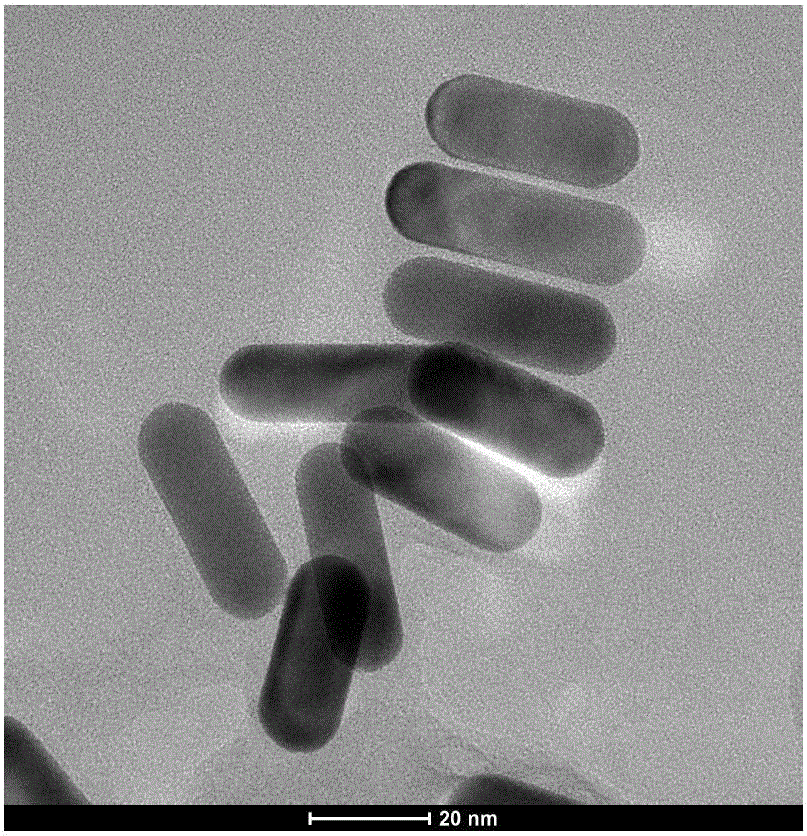
【图2】为金纳米棒载体的TEM示图;
【图3】A为实施例1中CEA适配体修饰电极与钼酸钠反应后的循环伏安图,B为电极检测空白和10ng/mLCEA的方波伏安图;
【图4】为实施例1中不同浓度CEA对应的方波伏安曲线以及测的CEA的标准曲线图。
具体实施方式
为了便于理解本发明,下文将结合说明书附图和较佳的实施例对本发明作更全面、细致地描述,但本发明的保护范围并不限于以下具体的实施例。
除非另有定义,下文中所使用的所有专业术语与本领域技术人员通常理解的含义相同。本文中所使用的专业术语只是为了描述具体实施例的目的,并不是旨在限制本发明的保护范围。
除非另有特别说明,本发明中用到的各种原材料、试剂、仪器和设备等均可通过市场购买得到或者可通过现有方法制备得到。
实施例1
本发明CEA的检测方法的一种实施例,其原理示意图如图1所示。该检测方法具体包括以下步骤:
(1)金纳米棒载体的合成:首先通过过量NaBH4在30℃还原浓度为1~2%的HAuCl4溶液得到纳米金种子溶液。然后,往50mL 0.1M的十六烷基三甲基溴化铵溶液中加入1.1mL HAuCl4(1%w/w),0.4mL AgNO3(10mM)和0.29mL抗坏血酸(0.1M)。最后往上述溶液中加入0.06mL合成的纳米金种子溶液。混合溶液持续反应24小时即得到金纳米棒载体。
(2)对金纳米棒载体修饰CEA适配体:将合成的金纳米棒载体分散在10 M CEA适配体溶液中室温下反应2h,离心洗涤去掉未反应的CEA适配体,得到CEA适配体/金纳米棒复合物。
(3)在电极表面固定CEA抗体:先将氧化石墨烯溶液(浓度为1~2mg/mL)与1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐和N-N-羟基琥珀酰亚胺溶液(浓度为50~100mM)在25~37℃混合反应2h,石墨烯分离后,再将CEA抗体与反应后的氧化石墨烯溶液反应,即得CEA抗体修饰氧化石墨烯。将5LCEA抗体修饰氧化石墨烯直接滴加到玻碳电极表面得到CEA抗体修饰电极。
(4)不同浓度CEA特异性结合:将浓度为1pg/mL、5pg/mL、10pg/mL、100pg/mL、1ng/mL和10ng/mL的人CEA溶液分别加到CEA抗体修饰电极表面,37℃水浴反应1h,缓冲溶液冲洗电极表面3次除去未结合上的CEA,得到结合了不同浓度CEA的CEA抗体—CEA修饰电极。
(5)CEA与金纳米棒载体特异性结合:将5μLCEA适配体/金纳米棒复合物滴加到CEA抗体—CEA修饰电极表面,在37℃水浴条件下反应1h,用缓冲溶液冲洗电极表面3次,除去未反应掉的金纳米棒复合物,得到CEA抗体—CEA—EA适配体/金纳米棒三层夹心式结构。
(6)CEA适配体与钼酸钠反应:向形成三层夹心式结构的电极表面滴加1mM钼酸钠溶液25℃反应20min。
(7)方波伏安法检测:以0.5mol/L的硫酸溶液为电解液,在0-0.5V电压范围内,以15Hz的频率进行测定,得到各电极的峰电流值,然后将各电极的峰电流值与对应的CEA浓度作标准曲线,得到测量CEA浓度的标准曲线。
(8)实际样品的测量:取5pg/mL、500pg/mL、1ng/mL、10ng/mLCEA的血清溶液,滴加到修饰有CEA抗体的电极表面,反应完冲洗电极后,然后将5μLCEA适配体/金纳米棒复合物滴加到电极表面,在37℃水浴条件下反应1h,用缓冲溶液冲洗电极表面3次除去未结合上的CEA,得到含CEA抗体—CEA—CEA适配体/金纳米棒三层夹心式结构的电极,在该电极表面滴加1mM钼酸钠溶液25℃反应20min,用方波伏安法测峰电流值,与标准曲线比对得到测量浓度值,测量浓度值与ELISA结果相比有很好的一致性,相关系数为0.993。
以上所述仅为本发明的优选实施例而已,并不用于限制本发明,对于本领域的技术人员来说,本发明可以有各种更改和变化。凡在本发明的精神和原则之内,所作的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!