龙桂参杞酒指纹图谱的检测方法与流程
龙桂参杞酒指纹图谱的检测方法
1.技术领域
2.本发明涉及一种中药配制酒的检测方法,具体涉及龙桂参杞酒指纹图谱的检测方法。
背景技术:
3.酒为百草之最,配以活血化瘀祛风散寒的食药材,酒助药性,药借酒力,扶正固本,人参甘温益气补中,增强整体免疫力,散寒理气;桂圆和枸杞补益心肝脾肾,使身体营养充分饱满,改善代谢障碍,散寒利湿,活血通络;薏苡仁、茯苓和橘皮散燥祛湿健脾;肉桂和干姜温中散寒补火助阳,温经通脉;甘草清热解毒促进血管末梢血液循环,青果抗炎止痛,山楂行气散瘀,合用后全面调理祛除体内风、寒、湿、热、毒,散寒逐湿,通经止痛,舒筋除痹,促进血液循环,除祛风寒和风湿。
4.龙桂参杞酒气血双补,散寒祛风,补火回阳,舒筋活血,温中止痛。适用于手臂麻木不仁,腰膝酸痛,行步脚弱,屈伸挛急,四肢不温,肌肉关节酸痛。能改善患者的免疫状态,长期服用,能增加脾胃运作机能,促进全身血液循环,具有祛风湿、清湿热、通经络、消肿止痛的作用。
5.目前关于龙桂参杞酒的质量检测方法较少。本发明采用高效液相色谱法建立龙桂参杞酒的指纹图谱检测方法,为龙桂参杞酒的成分鉴别、质量评价以及质量标准的制定具有重要的意义。
技术实现要素:
6.发明目的:本发明的目的是解决现有技术的不足,提供一种龙桂参杞酒的指纹图谱检测方法,该检测方法可以客观、全面、准确的评价龙桂参杞酒的质量,对控制龙桂参杞酒的质量和保证临床疗效具有重要意义。
7.技术方案:为了实现上述目的,本发明采取的技术方案为:一种龙桂参杞酒指纹图谱的检测方法,其特征在于,包括以下步骤:步骤1,龙桂参杞酒供试品溶液的制备:分别精密称取不同批次的龙桂参杞酒样品各10ml,过0.22μm微孔滤膜,得供试品溶液;步骤2,混合对照品溶液的制备:精密称定甘草苷、甘草酸铵对照品,置于容量瓶中,用甲醇定容至刻度,摇匀,制成混合对照品溶液;步骤3,分别精密吸取步骤1供试品溶液和步骤2对照品溶液,注入高效液相色谱仪,记录色谱图;步骤4,将步骤3中获得的龙桂参杞酒供试品溶液的指纹图谱导出,并导入中药色
谱指纹图谱相似度评价系统2004a;选择不同批次龙桂参杞酒的色谱图中均存在的色谱峰作为共有峰;用平均值计算法生成龙桂参杞酒的对照指纹图谱,计算各共有峰的相对保留时间和相对峰面积;并根据混合对照品溶液色谱图的保留时间标注对照指纹图谱中峰的化学成分;步骤5,将步骤3中获得的龙桂参杞酒指纹图谱和混合标准品图谱进行比对,指认出龙桂参杞酒中6号峰为甘草苷、11号峰为甘草酸铵。
8.作为优选方案,以上所述的龙桂参杞酒指纹图谱的检测方法,步骤1龙桂参杞酒供试品溶液制备方法为:取8批次的龙桂参杞酒样品各10ml,过0.22μm微孔滤膜,即得供试品溶液。
9.作为优选方案,以上所述的龙桂参杞酒指纹图谱的检测方法,步骤2混合对照品溶液的制备:取精密称定甘草苷、甘草酸铵对照品,置于容量瓶中,用甲醇定容至刻度,摇匀,制成含0.1167mg/ml甘草苷、0.1002mg/ml甘草酸铵组成的混合对照品溶液。作为优选方案,以上所述的龙桂参杞酒指纹图谱的检测方法,步骤3中,液相色谱条件为:色谱柱:ymc-pack ods-a,流动相:乙腈和0.1%磷酸水,梯度洗脱,二极管阵列检测器,检测波长:230nm,柱温40℃,流速0.8ml/min,进样体积:10μl,梯度洗脱程序如下表:程序时间(min)乙腈体积(%)105255325154351657536695100
10.作为优选方案,以上所述的龙桂参杞酒指纹图谱的检测方法,指纹谱图中共有峰14个,其保留时间分别为1号峰17.011min、2号峰21.538min、3号峰31.126min、4号峰34.785min、5号峰43.175min、6号峰46.623min、7号峰47.881min、8号峰50.433min、9号峰52.047min、10号峰55.397min、11号峰76.625min、12号峰83.208min、13号峰86.266min、14号峰91.777min,其中6号峰为甘草苷、11号峰为甘草酸铵。
11.作为优选方案,以上所述的龙桂参杞酒指纹图谱的检测方法,龙桂参杞酒的药味组成和配比为:肉桂、人参、薏苡仁、茯苓、大枣、青果、干姜、桂圆、枸杞、橘皮、甘草、山楂。
[0012] 作为优选方案,以上所述的龙桂参杞酒指纹图谱的检测方法,龙桂参杞酒的药味组成和配比为:肉桂4份、 人参2份 薏苡仁7份、茯苓6份、大枣2 份、青果2份、 干姜2 份、桂圆8份、 枸杞8 份、橘皮3 份、甘草2 份、山楂4份。
[0013]
作为优选方案,以上所述的龙桂参杞酒指纹图谱的检测方法,龙桂参杞酒的制备方法为:取肉桂、人参、薏苡仁、茯苓、大枣、青果、干姜、桂圆、枸杞、橘皮、甘草和山楂,加入总药材10~100倍体积量的食用乙醇或蒸馏酒(40-65%),浸泡15-20天、多层纱布和脱脂棉粗滤,压榨合并滤液(滤渣用纯水清洗),沉淀后过滤、用食用酒精(或纯水)和糖粉调配(35度)、沉淀澄清、上清液离心后膜过滤、灌装既得。
[0014]
指纹图谱检测条件的优化:
1、在样品溶液的制备优化方面本发明通过对不同制备方法(0.22μm微孔滤膜过滤、甲醇萃取、正丁醇萃取)进行实验比较,结果发现0.22μm微孔滤膜过滤所得的谱图差成分比较全面,方法简便,分离度良好,故采用滤膜过滤的方法。
[0015]
2、在色谱条件进行优化方面本发明采用二极管阵列检测器对检测波长进行考察,提取205nm、230nm、254nm、280nm处的色谱图,发现检测波长为230nm时,色谱图所包含的信息量最全面且基线平稳,故选230nm为检测波长;本发明对流速(1ml/min、0.9ml/min、0.8ml/min、0.6ml/min)进行筛选,因龙桂参杞酒中的成分中多存在同分异构体及其它极性极为相似的成分,高流速下无法将其分开,在低流速下分离效果较好,最终选择在流速为0.8ml/min梯度条件下将极性相似的物质分开。
[0016]
本发明对柱温(30
°
c、34
°
c、38
°
c、40
°
c、42
°
c)进行筛选。结果发现40
°
c柱温下色谱图响应强度较高,故最终选择柱温40
°
c。
[0017]
本发明比较了甲醇-水,乙腈-水,乙腈-0.1%甲酸,乙腈和0.05%磷酸水,乙腈-0.1%磷酸水5个不同洗脱系统在不同梯度下的洗脱效果。结果发现以乙腈和0.1%磷酸水为流动相时,龙桂参杞酒中各成分分离效果较好,故最终选定以乙腈和0.1%磷酸水为流动相。
[0018]
在确定最佳流动性组成后,本发明通过大量实验筛选最佳的梯度洗脱程序,实验发现,当采用0~5min 乙腈体积5%;5~25min 乙腈体积5%~15%;25~35min 乙腈体积15%~16%;35~75min 乙腈体积16%~36%;75~95min 乙腈体积36%~100%时,可实现指纹图谱中各色谱峰的良好分离度。
[0019]
有益效果:1、本发明根据龙桂参杞酒中所含的活性成分的结构性质特点,通过大量实验筛选出最佳的流动相组成,梯度洗脱程序、流速,检测波长、色谱柱,柱温等分析条件,经多次实验验证表明,本发明提供的龙桂参杞酒指纹图谱检测方法,可以全面、客观、准确的检测和评价龙桂参杞酒的质量,为保证临床龙桂参杞酒疗效具有重要意义。
[0020]
2、用本发明所提供的方法所建立的龙桂参杞酒指纹图谱,能有效地表征龙桂参杞酒的质量,能客观体现各个构成指纹特征峰的前后顺序和相互关系,注重整体面貌特征,既可避免因测定个别化学成分而判定龙桂参杞酒质量的片面性,又可减少为质量达标而人为处理的可能性。
[0021]
3、本发明提供的龙桂参杞酒指纹图谱的检测方法,具有方法简便、稳定性好、精密度高、重现性好等优点。
附图说明
[0022]
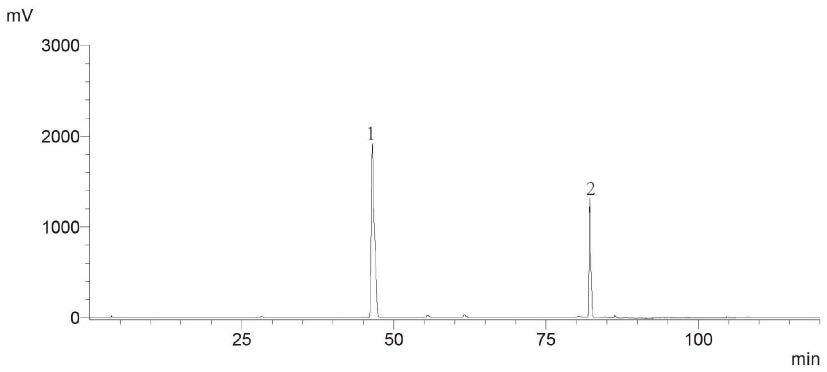
图1为本发明混合对照品的色谱图。
[0023]
图2为本发明的龙桂参杞酒样品的对照指纹图谱。
[0024]
图3为本发明龙桂参杞酒样品的8批次供试品指纹图谱。
具体实施方式
[0025]
下面将结合实施例对本发明的实施方案进行详细描述,实施例中未注明具体条件者,按照常规条件或制造商建议的条件进行。所用试剂或仪器未注明生产厂商者,均为可以通过市购获得的常规产品。
[0026]
以下实施例用到的仪器与试剂如下:实验器材1.1仪器日本岛津公司全波段扫描(200-800nm)高液相色谱系统,包括全自动在线脱气系统,全自动进样系统prominence sil-20a,二极管阵列检测器spd-m20a和自动温控柱温箱cto-20a。
[0027]
1.2药品与试剂龙桂参杞酒样品来自江苏海昇药业有限公司(制备方法为:取肉桂4g、人参2g、薏苡仁7g、茯苓6g、大枣2 g、青果2g、干姜2 g、桂圆8g、枸杞8 g、橘皮3 g、甘草2 g和山楂4g,加入总药材50倍体积量的食用乙醇,浸泡15天、多层纱布和脱脂棉粗滤,压榨合并滤液(滤渣用纯水清洗),沉淀后过滤、用食用酒精或纯水和糖粉调配35度、沉淀澄清、上清液离心后膜过滤、灌装既得);甘草苷对照品(批号111610-201607)购自中国药品生物制品检定所;甘草酸铵对照品(批号110731-201720)购自中国药品生物制品检定所;甲醇(分析纯);磷酸(分析纯);乙腈(色谱纯);水(超纯水)。
[0028]
实施例1 一种龙桂参杞酒指纹图谱的检测方法,包括以下步骤:步骤1,龙桂参杞酒供试品溶液的制备:取8批次的龙桂参杞酒样品(江苏海昇药业有限公司生产)10ml,过0.22μm微孔滤膜,得供试品溶液;步骤2,混合对照品溶液的制备:取精密称定甘草苷、甘草酸铵对照品,置于容量瓶中,用甲醇定容至刻度,摇匀,制成含0.1167mg/ml甘草苷、0.1002mg/ml甘草酸铵组成的混合对照品溶液。
[0029]
步骤3,分别精密吸取8批龙桂参杞酒供试品溶液和混合对照品溶液,注入高效液相色谱仪,记录色谱图;液相色谱条件为:色谱柱:ymc-pack ods-a,流动相:乙腈和0.1%磷酸水,梯度洗脱,二极管阵列检测器,检测波长:230nm,柱温40℃,流速0.8ml/min,进样体积:10μl,梯度洗脱程序如下表:程序时间(min)乙腈体积(%)105255325154351657536695100步骤4,将步骤3中获得的8批龙桂参杞酒供试品溶液的指纹图谱导出,并导入中药色谱指纹图谱相似度评价系统2004a;选择8批次龙桂参杞酒的色谱图中均存在的色谱峰作
为共有峰;用平均值计算法生成1批次龙桂参杞酒的对照指纹图谱,计算各共有峰的相对保留时间和相对峰面积;结果1批生品龙桂参杞酒中有14个共有峰,对照指纹图谱见图2,8批次供试品的指纹图谱如图3所示。甘草苷保留时间为46.623min,甘草酸铵保留时间为76.625min。
[0030]
步骤5,步骤3中获得的龙桂参杞酒指纹图谱和混合标准品图谱(图1)进行比对,指认主要成分,对比出龙桂参杞酒中6、11号色谱峰分别为:甘草苷(保留时间46.623min)、甘草酸铵(保留时间76.625min)。
[0031]
同时本发明使用自动生成的对照hplc指纹图谱r来生成共有色谱峰模式,分析计算获得江苏海昇药业厂家的8批龙桂参杞酒中药共有色谱峰之间具有相对很好的相似性,说明该方法建立的龙桂参杞酒中药建立的指纹图谱能够很好的检测江苏海昇药业多批次龙桂参杞酒的质量,结果如表1。
[0032]
表1各批次样品与共有模式间的相似度 s1s2s3s4s5s6s7s8rs110.8770.8990.9050.9220.9010.9440.9190.926s20.87710.8480.9980.9350.9660.9170.940.913s30.8990.84810.9550.9620.9050.9110.910.95s40.9050.9980.95510.8970.9020.9430.9270.963s50.9220.9350.9620.89710.9670.9110.9980.989s60.9010.9660.9050.9020.96710.9660.9750.979s70.9440.9170.9110.9430.9110.96610.9980.969s80.9190.940.910.9270.9980.9750.99810.95r0.9260.9130.950.9630.9890.9790.9690.951
[0033]
实施例2指纹图谱检测的方法学研究:1、方法学考察1.1精密度考察 取龙桂参杞酒样品(江苏海昇药业有限公司)10ml,按照上述实施例1的供试品制备方法,制备得到供试品溶液,连续进样6次,每次进样量10μl,按上述实施例1色谱条件检测,测定其hplc色谱图,对色谱图中14个共有指纹峰进行考察,结果表明,共有指纹峰的保留时间rsd均小于0.6%,共有峰峰面积rsd均小于1.5%,说明仪器精密度较好。
[0034]
1.2稳定性考察取龙桂参杞酒样品10ml,按照上述实施例1的供试品制备方法制备供试品溶液,按上述实施例1中的色谱条件分别于0,2,4,8,12,24h进样,记录色谱图,对色谱图中14个共有指纹峰进行考察,结果表明,共有指纹峰的保留时间rsd均小于0.9%,共有峰峰面积rsd均小于2.8%,说明供试品溶液在24h内稳定性较好。
[0035]
1.3重复性考察取龙桂参杞酒样品6份,按照上述实施例1供试品制备方法制备供试品溶液,分别测定,记录色谱图,对色谱图中14个共有指纹峰进行考察,结果表明,共有指纹峰的保留时间rsd均小于0.4%,共有峰峰面积rsd均小于1.9%,说明该方法重复性良好。
[0036]
以上实验结果表明,本发明提供的龙桂参杞酒指纹图谱检测方法,稳定性好,精密度高,重复性好,能全面客观评价龙桂参杞酒的质量,为保证临床疗效具有重要的意义。
[0037]
以上实施例仅为本发明的示例性实施例,不用于限制本发明,本发明的保护范围由权利要求书限定。本领域技术人员可以在本发明的实质和保护范围内,对本发明做出各种修改或等同替换,这种修改或等同替换也应视为落在本发明的保护范围内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1