利用锡矿尾矿硫酸浸出液制备锂离子电池用Fe3O4/C复合电极材料的方法与流程
本发明属于锂离子电池负极材料的技术领域,具体涉及一种利用锡矿尾矿硫酸浸出液制备锂离子电池用fe3o4/c复合电极材料的方法。
背景技术:
矿产资源的开发利用为社会的经济发展和建设做出了重要贡献,与此同时也给环境带来了巨大挑战。尾矿的堆积不仅侵占了大量的土地资源,而且很容易产生二次污染。尾矿的化学成分以铁、硅、铝、钙的氧化物为主,有非常高的回收价值,这使开发利用尾矿具有巨大的环境和经济双重效益。锡矿尾矿是尾矿中的一种,其中的铁氧化物约占20%,但其中的铁仍达不到炼铁要求。锡矿尾矿中锡、铁等有价金属的回收主要采用浮选、重选或浮选-重选联合工艺,但这些工艺较复杂,金属回收率不足60%,且产品附加值低。对尾矿进行浸出,再从浸出液中回收有价金属是尾矿资源化利用的一种重要方法,但有关锡矿尾矿的相关研究却鲜有报道。纳米fe3o4作为锂离子电池负极材料具有高达926mahg-1的理论比容量,相比其他过渡金属氧化物电子导电性好,同时fe3o4还具有原料丰富、价格低廉、绿色环保等优点而备受青睐。但是,fe3o4作为锂离子电池负极材料在充、放电过程中会发生巨大的体积变化和严重的粒子团聚,导致其电荷和锂离子传输及扩散性能较差,从而使其倍率性能不高以及循环衰减较快。人们研究发现,与碳材料复合和形貌调控是改善fe3o4储锂性能的两种重要方法。为此,本发明提出一种以锡矿尾矿硫酸浸出液为铁源、以柠檬酸铵为形貌调控剂和碳源,制备高性能锂离子电池用fe3o4/c复合电极材料的方法。
技术实现要素:
本发明的目的在于提供一种利用锡矿尾矿硫酸浸出液制备锂离子电池用fe3o4/c复合电极材料的方法。
具体步骤为:
(1)测定锡矿尾矿硫酸浸出液中总的铁离子的物质的量浓度和溶液的ph值,根据测定结果调节溶液中总的铁离子的物质的量浓度为0.15mol/l,并调节溶液的ph值为1。
(2)量取步骤(1)所得的溶液130ml放入500ml烧杯中,在25℃以350转/分钟的搅拌速度磁力搅拌下向烧杯中滴加浓度为1mol/l的碳酸钠溶液直至溶液的ph值为4;滴加完成以后,继续搅拌3小时,然后静置陈化12小时,最后进行过滤、洗涤、冷冻干燥,获得前驱体粉体。
(3)按步骤(2)所得的前驱体粉体和柠檬酸铵的质量比为1:1~3的比例称取并混合,向所得混合物中加入去离子水超声分散使柠檬酸铵完全溶解,然后将其置于管式炉中在氩气气氛下从室温加热至300℃并保温2小时,再继续升温至800℃并保温2小时,随炉冷却后即制得锂离子电池用fe3o4/c复合电极材料。
本发明的优点:本发明充分利用了锡矿尾矿硫酸浸出液中的铁资源制备了具有高附加值的fe3o4/c复合电极材料,这不仅可以缓解锡矿尾矿长期堆存产生的生态环境问题,而且有效提高了锡矿尾矿资源化利用率。同时,本发明制备方法简单、原料易得、成本低、条件易于控制、能大规模制备,制备的fe3o4/c复合电极材料作为锂离子电池负极材料具有较好的循环稳定性和倍率性能。
附图说明
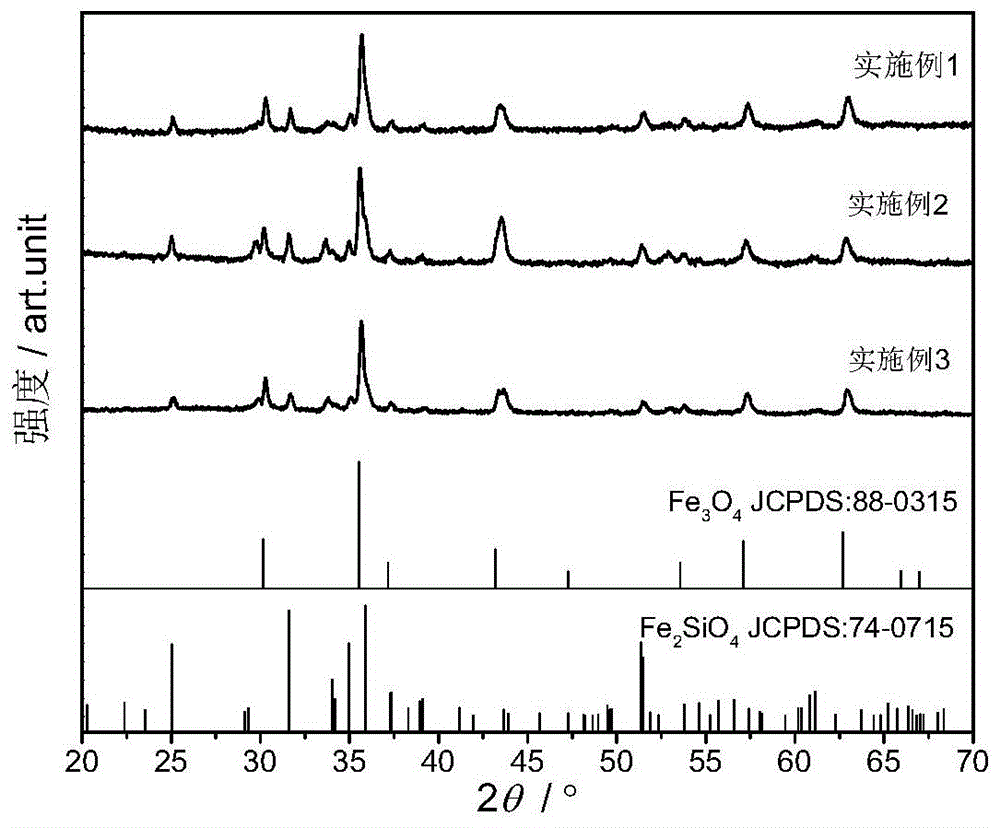
图1为实施例1~3制备的锂离子电池用fe3o4/c复合电极材料的xrd图谱。
图2为实施例1~3制备的锂离子电池用fe3o4/c复合电极材料的热重曲线。
图3为实施例1~3制备的锂离子电池用fe3o4/c复合电极材料的fesem图。
图4为实施例1~3制备的锂离子电池用fe3o4/c复合电极材料的循环性能图。
图5为实施例1~3制备的锂离子电池用fe3o4/c复合电极材料的倍率性能图。
具体实施方式
下面结合具体实施例对本发明作进一步的说明,需要指出的是以下实施例是为了本领域的技术人员更好地理解本发明,而不是对本发明保护范围的限制,该领域的技术人员可以根据上述内容做出一些非本质的改进和调整。
实施例1:
(1)调节锡矿尾矿硫酸浸出液中总的铁离子的物质量浓度为0.15mol/l,并调节溶液的ph值为1。
(2)量取步骤(1)所得的锡矿尾矿硫酸浸出液130ml放入500ml烧杯中,在25℃磁力搅拌(磁力搅拌速度350转/分钟)条件下向烧杯中缓慢滴加浓度为1mol/l的碳酸钠溶液直至溶液的ph值为4;滴加完成以后,继续搅拌3小时,然后静置陈化12小时,最后进行过滤、洗涤、冷冻干燥,获得前驱体粉体。
(3)按步骤(2)所得的前驱体粉体和柠檬酸铵的质量比为1:1的比例称取0.4g前驱体粉体和0.4g柠檬酸铵并进行混合,向混合物中加入5ml去离子水超声分散使柠檬酸铵完全溶解,然后将其置于管式炉中在氩气气氛下从室温加热至300℃并保温2小时,再继续升温至800℃并保温2小时,随炉冷却后即制得锂离子电池用fe3o4/c复合电极材料。
实施例2:
(1)调节锡矿尾矿硫酸浸出液中总的铁离子的物质量浓度为0.15mol/l,并调节溶液的ph值为1。
(2)量取步骤(1)所得的锡矿尾矿硫酸浸出液130ml放入500ml烧杯中,在25℃磁力搅拌(磁力搅拌速度350转/分钟)条件下向烧杯中缓慢滴加浓度为1mol/l的碳酸钠溶液直至溶液的ph值为4;滴加完成以后,继续搅拌3小时,然后静置陈化12小时,最后进行过滤、洗涤、冷冻干燥,获得前驱体粉体。
(3)按步骤(2)所得的前驱体粉体和柠檬酸铵的质量比为1:2的比例称取0.4g前驱体粉体和0.8g柠檬酸铵并进行混合,向混合物中加入5ml去离子水超声分散使柠檬酸铵完全溶解,然后将其置于管式炉中在氩气气氛下从室温加热至300℃并保温2小时,再继续升温至800℃并保温2小时,随炉冷却后即制得锂离子电池用fe3o4/c复合电极材料。
实施例3:
(1)调节锡矿尾矿硫酸浸出液中总的铁离子的物质量浓度为0.15mol/l,并调节溶液的ph值为1。
(2)量取步骤(1)所得的锡矿尾矿硫酸浸出液130ml放入500ml烧杯中,在25℃磁力搅拌(磁力搅拌速度350转/分钟)条件下向烧杯中缓慢滴加浓度为1mol/l的碳酸钠溶液直至溶液的ph值为4。碳酸钠滴加完成以后,继续搅拌3小时,然后静置陈化12小时,最后进行过滤、洗涤、冷冻干燥,获得前驱体粉体。
(3)按步骤(2)所得的前驱体粉体和柠檬酸铵的质量比为1:3的比例称取0.4g前驱体粉体和1.2g柠檬酸铵并进行混合,向混合物中加入5ml去离子水超声分散使柠檬酸铵完全溶解,然后将其置于管式炉中在氩气气氛下从室温加热至300℃并保温2小时,再继续升温至800℃并保温2小时,随炉冷却后即制得锂离子电池用fe3o4/c复合电极材料。
实施例1~3所采用的锡矿尾矿硫酸浸出液仅是举例,为了使本领域的技术人员能够更好地理解本发明,但并不对本发明作任何限制。
电极制备及电池组装:将实施例1~3制备的锂离子电池用fe3o4/c复合材料、导电炭黑(superp)和聚偏氟乙烯(pvdf)按质量比7:2:1的比例混合研磨均匀,向其中加入适量的n-甲基吡咯烷酮(nmp),搅拌至均匀的浆料后均匀涂覆在铜箔上,并在80℃下真空干燥12小时,冲裁后制得直径为16mmfe3o4/c电极片。以fe3o4/c电极片为工作电极,金属锂片为对电极,聚丙烯多孔膜(celgard2400)为隔膜,1mol/llipf6的碳酸乙烯酯(ec)、碳酸二甲酯(dmc)和碳酸二乙酯(dec)的混合液(体积比,v(ec):v(dmc):v(dec)=1:1:1)为电解液,在充满氩气的手套箱中组装成cr2016型扣式电池。
电化学性能测试:采用深圳新威公司的bts-5v/10ma型多通道充放电测试仪测试电池的恒流充放电性能,充放电电压范围为0.01~3.0v,循环性能测试先在0.2ag-1电流密度下循环10圈,然后在0.5ag-1电流密度循环90圈。倍率性能测试的电流密度分别为0.2ag-1、0.5ag-1、1ag-1、2ag-1、3ag-1、4ag-1。
如图1所示,为实施例1~3制备的锂离子电池用fe3o4/c复合电极材料的xrd图谱。从图中可以看出,本发明制备的材料主要物相为fe3o4,且其中含有少量的fe2sio4杂质。
如图2所示,为实施例1~3制备的锂离子电池用fe3o4/c复合电极材料的热重曲线。从图中可以看出,本发明制备的材料中含有c,是fe3o4/c复合电极材料。
如图3所示,为实施例1~3制备的锂离子电池用fe3o4/c复合材料的fesem图。从图中可以看出,本发明制备的fe3o4/c复合材料是由纳米级fe3o4颗粒镶嵌在多孔碳(c)框架里。
如图4所示,为实施例1~3制备的锂离子电池用fe3o4/c复合材料在0.2ag-1电流密度下循环10圈后再在0.5ag-1电流密度下循环90圈的循环性能曲线。从图中可以看出,实施例2制备的fe3o4/c复合材料的循环性能相对最好。实施例2制备的材料电极在0.2ag-1电流密度下循环10圈后再在0.5ag-1电流密度下循环10圈后,放电/充电比容量分别为510和506mahg-1,循环90圈后放电/充电比容量分别为438和426mahg-1,放电/充电容量保持率分别为86%和84%。
如图5所示,为实施例1~3制备的锂离子电池用fe3o4/c复合材料在不同电流密度(0.2、0.5、1、2、3、4ag-1)下的倍率性能曲线。从图中可以看出,实施例1~3制备的锂离子电池用fe3o4/c复合材料均具有较好的倍率性能。实施例2制备的fe3o4/c复合材料在0.2、0.5、1、2、3、4ag-1电流密度下,放电/充电比容量分别为592/572、507/501、460/457、405/403、368/365和344/340mahg-1。
- 还没有人留言评论。精彩留言会获得点赞!