一种三联益生菌微胶囊的制备系统的制作方法
本实用新型涉及微生态制剂领域技术领域,具体而言,是涉及一种三联益生菌微胶囊的制备系统。
背景技术:
益生菌(probiotic)通常是指摄入一定数量,能以活菌状态到达胃肠道,通过调节肠道菌群组成,进而发挥对人体或动物健康起促进作用的单一或特定微生物的混合物,益生菌及益生菌制剂对机体健康的积极作用已被公认。但是,目前的益生菌制剂及其制备技术,尤其是多联益生菌制剂及其制备技术,至少存在着如下技术缺点:
(1)益生菌制剂在加工、运输、贮存过程中容易失去活性,降低生物活性作用;
(2)益生菌制剂进入消化道后,在胃酸、胆汁酸等的破坏作用下,很难有足够的数量到达肠道或定居肠道发挥作用;
(3)益生菌制剂进入肠道后繁殖速度慢,难以在微生物竞争中处于优势地位,形成优势菌群;
(4)益生菌制剂的功能单一,应用范围受限;
(5)益生菌制剂的微胶囊产品的储存时间较短;
(6)益生菌制剂的微胶囊产品大小不均匀,微胶囊易于粘连,机械强度较小;
(7)制备方法工艺复杂,制备周期长,且设备昂贵,难以大规模、工业化生产等。
因此,目前的益生菌制剂及其制备技术,尤其是多联益生菌制剂及其制备技术,有待进一步改进。
技术实现要素:
本实用新型的目的在于提供一种三联益生菌微胶囊的制备系统,以解决例如上述现有技术问题。
本实用新型公开了一种三联益生菌微胶囊的制备系统,该制备系统所制备的三联益生菌微胶囊包括:嗜酸乳杆菌、粪肠球菌以及酿酒酵母,该制备系统包括:
培养基制备系统(100);
菌种接种与培养系统(200);
菌乳剂制备系统(300):所述菌乳剂制备系统包括:混匀设备(310)和均质设备(320);
微胶囊制备系统(400):所述微胶囊制备系统包括喷洒设备(410)、清洗设备(420)、搅拌设备(430);以及
干燥系统(500):所述干燥系统包括恒温箱(510)和干燥机(520)。
根据本实用新型的三联益生菌微胶囊的制备系统,其有益效果至少如下所述:
1、根据本实用新型的三联益生菌微胶囊的制备系统,益生菌菌体与组合培养基充分接触,满足菌体的生长需要,加快益生菌生长速度。另外,酿酒酵母摇床培养可以得到菌丝聚集球,能更有效地发挥其作用。
2、根据本实用新型的三联益生菌微胶囊的制备系统,使黄芪多糖与菌液充分混合制成均质液体,使海藻酸钠与第一菌乳剂充分混合,达到“水包油、油包水”的效果,为后期微胶囊制备提高包被率打好基础。
3、根据本实用新型的三联益生菌微胶囊的制备系统,制备的微胶囊在低转速下进行固化,既能使第二菌乳剂充分与CaCl2进行反应,又可防止过高转速使微胶囊成型过程中出现拉丝现象。
4、根据本实用新型的三联益生菌微胶囊的制备系统,使固化的微胶囊在壳聚糖溶液中成膜,构成海藻酸钠-壳聚糖复合体系,从而使制得的微胶囊具备一定的耐酸能力,更好的保护益生菌安全通过胃环境。另外,壳聚糖是一种带正电荷的聚合物,能与带负电荷的肠道上皮细胞互相结合,因此具有良好的肠道吸附性。
可选的,所述混匀设备的温度、转速、时间均可调节;
所述均质设备的温度、压力、转速、时间均可调节;
所述喷洒设备装配有多个喷嘴(411),且所述喷嘴的直径大小、喷射频率、喷射速度以及喷射角度均可调节;以及
所述喷洒设备还包括:喷射泵(412)和控制器(413),所述喷射泵与所述喷嘴连接,并且所述控制器与所述喷射泵连接,以使所述控制器能够控制所述喷射泵的喷射频率和喷射速度。
由此,其有益作用有五点:(1)可以选择最佳的菌乳剂的制备条件参数,获得最佳的菌乳剂;(2)可以选择最佳的微胶囊的制备条件参数;(3)使得喷洒的效率相同,制备的微胶囊大小均匀一致,从而有利于规模化、工业化生产;(4)使制备的微胶囊粒径可控、机械强度大、圆形,且不粘连;(5)制备微胶囊的速度更快,大幅度节省原料,显著提供了生产效率,进而利于规模化、工业化生产。
可选的,所述喷洒设备还包括:喷射泵(412)和控制器(413);
所述喷射泵与所述喷嘴连接,并且所述控制器与所述喷射泵连接,以使所述控制器能够控制所述喷射泵的喷射频率和喷射速度。由此,可以根据实际需要,选择相应的喷射泵的喷射频率和喷射速度,进而可以有效控制生产效率,适用范围更广泛。
可选的,所述培养基制备系统设置有PH检测设备。由此,可以为益生菌的生长提供最佳的生长环境。
可选的,所述菌种接种与培养系统设置有菌属鉴定设备与生物学特性分析设备。由此,可以选择最佳益生菌培养条件,进而有利于确保益生菌活性保持最强。
可选的,所述菌种接种与培养系统包括:培养箱和摇床。由此,使菌体与培养基充分接触,满足菌体的生长需要,加快益生菌生长速度。另外,酿酒酵母摇床培养可以得到菌丝聚集球,能更有效地发挥其作用。
可选的,所述菌种接种与培养系统设置有离心设备。由此,可以有效去除杂质,制备最佳菌乳剂。
可选的,所述菌种接种与培养系统设置有菌落数测定设备。由此,可以选择最佳的益生菌。
可选的,所述制备系统还包括:形态测定系统、包埋率测定系统、耐受性测定系统以及稳定性测定设备。由此,利用形态测定系统可以对微胶囊的外观检测、粒径与截面进行检测;利用包埋率测定系统可以对微胶囊的包埋率进行检测;利用耐受性测定系统可以对微胶囊的耐酸性和肠溶性进行检测;利用稳定性测定设备可以对微胶囊的稳定性进行检测。
可选的,所述形态测定系统包括:扫描电子显微镜与背散射电子衍射仪。由此,利用扫描电子显微镜可以对微胶囊的外观检测与粒径进行检测,利用背散射电子衍射仪可以对微胶囊的截面进行检测。
根据本实用新型的实施例,利用本实用新型的制备系统制备微胶囊时,其制备方法的可选技术方案如下所述,
其中,制备方法包括如下步骤:
S100、培养基的制备:在MRS肉汤培养基中加入黄芪多糖,以使黄芪多糖的含量为0.2mg/mL,且PH 5.7±0.2,以获得组合培养基;
S200、菌种的接种与培养:将活化后的嗜酸乳杆菌、粪肠球菌以及酿酒酵母接种到所述组合培养基中,然后置于培养箱中培养;
S300、菌乳剂的制备:洗下菌苔获得菌悬液,菌悬液中加入黄芪多糖,以使黄芪多糖的含量为2mg/mL,以获得第一菌乳剂,以及
在所述第一菌乳剂中加入质量百分比浓度2%的海藻酸钠,使第一菌乳剂与海藻酸钠的体积比为1:3,以获得第二菌乳剂;
S400、微胶囊的制备:将所述第二菌乳剂喷入质量百分比浓度3%的CaCl2溶液中,固化后获得第一微胶囊;
清洗所述第一微胶囊后获得第二微胶囊;
将所述第二微胶囊放入质量百分比浓度2%的壳聚糖溶液中成膜,获得第三微胶囊;
S500、干燥:利用干燥机干燥所述第三微胶囊,获得三联益生菌微胶囊。
上述三联益生菌微胶囊的制备方法的作用原理与有益效果如下所述:
1、充分满足了益生菌菌体的生长需要,加快了益生菌生长速度,使益生菌保持较高活性,有利于确保益生菌在进入肠道后能够快速繁殖,进而在微生物竞争中处于优势地位,形成优势菌群。
2、海藻酸钠与氯化钙发生离子交换形成海藻酸钙包被,形成第一次包被,有利于减少温度、酸度、压力等对益生菌的破坏,延长益生菌微胶囊的贮藏时间,而且因为海藻酸钙与壳聚糖等电点不同,而使壳聚糖在海藻酸钙表面形成第二次包被,从而又构成海藻酸钠-壳聚糖复合保护体系,进而对益生菌具有了双重保护屏障的独特作用,进一步地确保益生菌的活性更强。
3、在整个制备过程中,自始而终都可以有效防止温度、压力、酸度等对益生菌活性的破坏,进一步有效保护了益生菌的活性。
4、所制备微胶囊的耐胃酸较强,可以保护益生菌安全通过胃环境,且具有肠溶性和耐胆盐性,进而确保益生菌具有足够的数量到达肠道或定居肠道发挥有益作用。
5、所制备微胶囊包括嗜酸乳杆菌、粪肠球菌以及酿酒酵母等多种益生菌,功能更多样,应用范围更广泛,推广价值更大。
6、所述制备的微胶囊大小均匀,相互不粘连,机械强度大,且微胶囊可以储存1年以上,更易于储存和运输。
7、制备微胶囊的工艺步骤非常简单,制备周期更短,且所用原料和设备均为现有或常见,大幅度节约了生产成本,进而使本实用新型的制备方法更适于大规模、工业化生产。
优选的,在步骤S200中,培养条件为相对湿度60%~65%、温度37℃、时间24h,并且每隔3h在摇床上180r/min震荡15min。由此,使菌体与培养基充分接触,满足菌体的生长需要,加快益生菌生长速度。另外,酿酒酵母摇床培养可以得到菌丝聚集球,能更有效地发挥其作用。
优选的,在步骤S300中,利用混匀设备制备第一菌乳剂,制备条件为温度37℃、常压、转速60r/min、时间15min;
利用均质设备制备第二菌乳剂,制备条件为温度37℃、常压、转速120r/min、时间30min。
由此,使黄芪多糖与菌液充分混合制成均质液体,使海藻酸钠与第一菌乳剂充分混合,达到“水包油、油包水”的效果,为后期微胶囊制备时进一步提高包被率打好基础。
优选的,在步骤S400中,固化条件为温度37℃、常压、搅拌转速20r/min、时间60min,以及
成膜条件为温度37℃、常压、静置、时间90min。
由此,所制备的微胶囊在低转速下进行固化,既能使第二菌乳剂充分与CaCl2进行反应,又可防止过高转速使微胶囊成型过程中出现拉丝现象;固化的微胶囊在壳聚糖溶液中成膜,构成海藻酸钠-壳聚糖复合体系,从而使制得的微胶囊具备一定的耐酸能力,更好的保护短乳杆菌安全通过胃环境,另外,壳聚糖是一种带正电荷的聚合物,能与带负电荷的肠道上皮细胞互相结合,因此具有良好的肠道吸附性。
可选的,在步骤S400中,利用蒸馏水在温度37℃条件下清洗所述第一微胶囊。由此,使制备的微胶囊呈现初级产品性状。
可选的,在步骤S400中,利用喷洒设备喷洒所述第二菌乳剂,所述喷洒设备装配有多个喷嘴,且所述喷嘴的直径大小、喷射频率、喷射速度以及喷射角度均可调节。由此,使得喷洒的效率相同,制备的微胶囊大小均匀一致,不会粘连,且有利于进一步确保微胶囊壁材更加完整无损。另外,制备微胶囊的速度更快,大幅度节省原料,显著提供了生产效率,进而利于规模化、工业化生产。
可选的,在步骤S500中,将所述第三微胶囊在恒温箱中以37℃恒温定型,再用干燥机以温度37~45℃条件干燥24h。由此,用适宜的培养温度将微胶囊进行干燥,减少干燥过程中对益生菌的破坏。
上述三联益生菌微胶囊的制备方法可以取得至少如下所述的有益效果:
1、可以有针对性的对营养条件要求高、对氧较为敏感、对低pH值耐性差、产品在常温下销售和消费过程中活菌含量迅速下降以及容易失活等缺点的益生菌进行包被处理,且有效降低益生菌对外界环境及胃肠道不良因素的反应。
2、使海藻酸钠与氯化钙发生离子交换形成海藻酸钙包被,减少温度、酸度、压力等对益生菌的破坏,延长益生菌微胶囊的贮藏时间。
3、采用海藻酸钙与壳聚糖等电点不同使壳聚糖在海藻酸钙表面形成二次包被,构成海藻酸钠-壳聚糖复合体系,从而使制得的微胶囊具备更强的耐酸能力,更好地保护益生菌的活性。
4、微胶囊的包埋率均高于89%,益生菌被严密地包裹在微胶囊的壁材之内,且微胶囊的壁材分布均匀、厚度一致,且完整无破损。
5、微胶囊还具有肠溶性和耐胆盐性,有利于确保益生菌在进入肠道后能够快速繁殖,进而在微生物竞争中处于优势地位,形成优势菌群。
6、制备的微胶囊具有表面光滑、大小均匀一致、相互不粘连以及机械强度大等优点,且微胶囊的稳定性可达1年以上。
7、制备微胶囊的工艺步骤非常简单,制备周期更短,且所用原料和设备均为现有或常见,大幅度节约了生产成本,进而有利于大规模、工业化生产。
相关技术人员可以理解的是,前面关于三联益生菌微胶囊的制备方法所描述的特征和有益效果,当然地也适用于本实用新型的制备系统,不再赘述。
根据本实用新型的实施例,本实用新型的制备系统所制备的三联益生菌微胶囊及其应用如下所述:
该微胶囊的壁材配方为:菌液与海藻酸钠溶液的体积比为1:3、海藻酸钠溶液的质量百分比浓度为2%、氯化钙的质量百分比浓度为3%、壳聚糖的质量百分比浓度为2%;以及
将所述微胶囊应用于药品制备、疾病防治、保健品制备或食品生产。
其有益效果及其应用价值如下:在此配方条件下制备的微胶囊,粒径较小,粒径分布范围较窄,呈球性较好。另外,微胶囊可以耐胃酸,具有肠溶性,耐胆盐,理论上可以储存1年以上,可应用于药品制备、疾病防治、保健品制备或食品生产等,具有巨大的市场应用价值。
相关技术人员可以理解的是,前面关于该微胶囊及其应用所描述的特征和有益效果,当然地也适用于本实用新型的制备系统,不再赘述。
本实用新型的附加方面和优点将在下面的描述中部分给出,部分将从下面的描述中变得明显,或通过本实用新型的实践了解到。
附图说明
本实用新型的上述和/或附加的方面和优点从结合下面附图对实施例的描述中将变得明显和容易理解,其中:
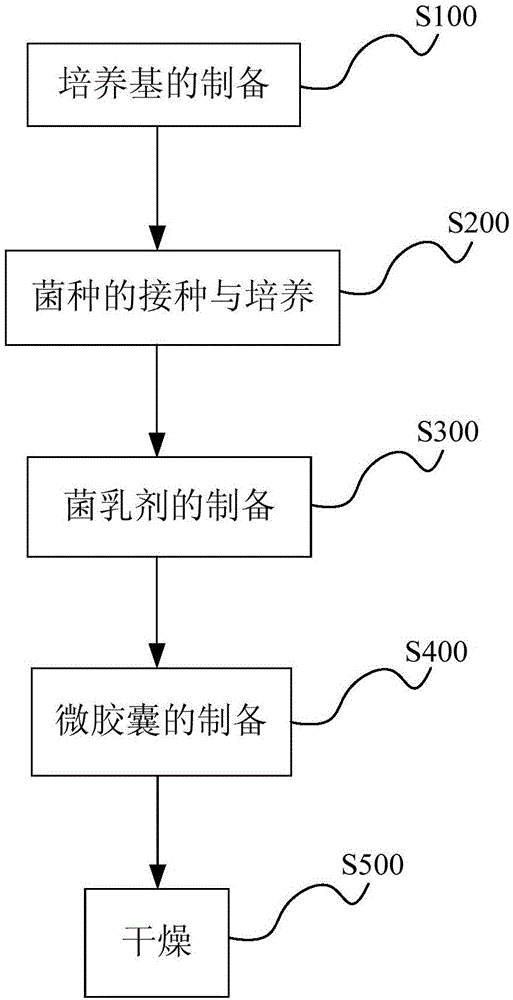
图1是根据本实用新型一个实施例中的三联益生菌微胶囊制备方法的工艺流程示意图;
图2是根据本实用新型一个实施例中的三联益生菌微胶囊制备系统的结构示意图;
图3是根据本实用新型又一个实施例中的三联益生菌微胶囊制备系统的结构示意图;
图4是根据本实用新型另外一个实施例中的三联益生菌微胶囊制备系统的结构示意图。
附图标记:
100-培养基制备系统;200-菌种接种与培养系统;300-菌乳剂制备系统;310-混匀设备;320-均质设备;400-微胶囊制备系统;410-喷洒设备;411-喷嘴;412-喷射泵;413-控制器;420-清洗设备;430-搅拌设备;500-干燥系统;510-恒温箱;520-干燥机。
具体实施方式
下面通过具体的实施例,并结合附图对本实用新型做进一步的详细描述。需要说明的是,在不冲突的情况下,本申请中的实施例及实施例中的特征可以相互组合。另外,实施例是示例性的,仅用于解释本实用新型,而不能理解为对本实用新型的限制。
在本实用新型的描述中,需要说明的是,除非另有明确的规定和限定,术语“安装”、“卸载”、“相连”、“连接”应做广义理解,例如,可以是固定连接,也可以是可拆卸连接,或一体地连接;可以是机械连接,也可以是电连接;可以是直接相连,也可以通过中间媒介间接相连,可以是两个元件内部的连通。对于本领域的普通技术人员而言,可以根据具体情况理解上述术语在本实用新型中的具体含义。
在本实用新型的描述中,需要理解的是,术语“厚度”、“上”、“下”等指示的方位或位置关系为基于附图所示的方位或位置关系,仅是为了便于描述本实用新型和简化描述,而不是指示或暗示所指的装置或元件必须具有特定的方位、以特定的方位构造和操作,因此不能理解为对本实用新型的限制。
术语“第一”、“第二”仅用于描述目的,而不能理解为指示或暗示相对重要性或者隐含指明所指示的技术特征的数量。由此,限定有“第一”、“第二”的特征可以明示或者隐含地包括一个或者更多个该特征。在本实用新型的描述中,“多个”的含义是两个或两个以上,除非另有明确具体的限定。
本实用新型公开了一种三联益生菌微胶囊的制备系统,该制备系统所制备的三联益生菌微胶囊包括:嗜酸乳杆菌、粪肠球菌以及酿酒酵母,根据本实用新型的实施例,如图2-4所示,该制备系统包括:
培养基制备系统100;
菌种接种与培养系统200;
菌乳剂制备系统300:所述菌乳剂制备系统包括:混匀设备310和均质设备320;
微胶囊制备系统400:所述微胶囊制备系统包括喷洒设备410、清洗设备420、搅拌设备430;以及
干燥系统500:所述干燥系统包括恒温箱510和干燥机520。
根据本实用新型的实施例,利用本实用新型的制备系统在制备微胶囊时,如图1所示,制备方法包括如下步骤:
S100、培养基的制备
在MRS肉汤培养基中加入黄芪多糖,以使黄芪多糖的含量为0.2mg/mL,且PH 5.7±0.2,以获得组合培养基。
S200、菌种的接种与培养
将活化后的嗜酸乳杆菌、粪肠球菌以及酿酒酵母接种到所述组合培养基中,然后置于培养箱中培养。
S300、菌乳剂的制备
洗下菌苔获得菌悬液,菌悬液中加入黄芪多糖,以使黄芪多糖的含量为2mg/mL,以获得第一菌乳剂,以及
在所述第一菌乳剂中加入质量百分比浓度2%的海藻酸钠,使第一菌乳剂与海藻酸钠的体积比为1:3,以获得第二菌乳剂。
S400、微胶囊的制备
将所述第二菌乳剂喷入质量百分比浓度3%的CaCl2溶液中,固化后获得第一微胶囊;
清洗所述第一微胶囊后获得第二微胶囊;
将所述第二微胶囊放入质量百分比浓度2%的壳聚糖溶液中成膜,获得第三微胶囊。
S500、干燥
利用干燥机干燥第三微胶囊,获得三联益生菌微胶囊。
根据本实用新型的实施例,本实用新型的技术方案在上述基础上,还可以做进一步的优化,具体的优化技术方案已在实用新型内容部分得以直接或间接阐述,或将在以下部分得以进一步阐述,故在此不予重复阐述。
下面结合附图1-4,通过具体的实施例,对本实用新型做进一步的说明,需要说明的是这些实施例仅仅是为了说明目的,而不能以任何方式解释成对本实用新型的限制。另外,在下列实施例中如果没有特别说明,则所采用的设备和材料均为市售可得的。
实施例1
1.1实验原料
嗜酸乳杆菌、粪肠球菌以及酿酒酵母均为公众可从市场获得的商品,例如烟台三禾畜牧养殖环境净化工程有限公司的产品等,下同。
1.2操作步骤
(1)制备培养基:在MRS肉汤培养基中加入黄芪多糖,以使黄芪多糖的含量为0.2mg/mL,且PH 5.7±0.2,以获得组合培养基;
(2)接种与培养:将活化后的嗜酸乳杆菌、粪肠球菌以及酿酒酵母菌液稀释100倍,然后以1%的接种量加入不同比例的含黄芪多糖的液体培养基中,置于培养箱中培养,培养条件为相对湿度60%~65%、温度37℃、时间24h,并且每隔3h在摇床上180r/min震荡15min。
(3)制备菌乳剂:洗下菌苔获得菌悬液,菌悬液中加入黄芪多糖,以使黄芪多糖的含量为2mg/mL,以获得第一菌乳剂;
在第一菌乳剂中加入质量百分比浓度2%的海藻酸钠,使第一菌乳剂与海藻酸钠的体积比为1:3,获得第二菌乳剂。
(4)制备微胶囊:将第二菌乳剂喷入质量百分比浓度3%的CaCl2溶液中,固化后获得第一微胶囊;
清洗第一微胶囊后获得第二微胶囊;
将第二微胶囊放入质量百分比浓度2%的壳聚糖溶液中成膜,获得第三微胶囊;
(5)干燥:将第三微胶囊在恒温箱510中以37℃恒温定型,再用干燥机520以温度37~45℃条件干燥24h,获得三联益生菌微胶囊,保存。
实施例2
操作步骤如下:
(1)制备培养基:在MRS肉汤培养基中加入黄芪多糖,以使黄芪多糖的含量为0.2mg/mL,且PH 5.7±0.2,以获得组合培养基;
(2)接种与培养:将活化后的嗜酸乳杆菌、粪肠球菌以及酿酒酵母菌液稀释100倍,然后以1%的接种量加入不同比例的含黄芪多糖的液体培养基中,置于培养箱中培养,培养条件为相对湿度60%~65%、温度37℃、时间24h,并且每隔3h在摇床上180r/min震荡15min。
(3)制备菌乳剂:洗下菌苔获得菌悬液,菌悬液中加入黄芪多糖,利用混匀设备310进行混匀,混匀条件为温度37℃、常压、转速60r/min、时间15min,以使黄芪多糖的含量为2mg/mL,获得第一菌乳剂;
在第一菌乳剂中加入质量百分比浓度2%的海藻酸钠,使第一菌乳剂与海藻酸钠的体积比为1:3,利用均质设备320制备进行均质,均质条件为温度37℃、常压、转速120r/min、时间30min,获得第二菌乳剂。
(4)制备微胶囊:利用喷洒设备410将第二菌乳剂喷入质量百分比浓度3%的CaCl2溶液中,搅拌设备430以温度37℃、常压、搅拌转速20r/min条件搅拌60min,固化后获得第一微胶囊;
在清洗设备420中利用蒸馏水在温度37℃条件下清洗第一微胶囊,获得第二微胶囊;
将第二微胶囊放入质量百分比浓度2%的壳聚糖溶液中成膜,成膜条件为温度37℃、常压、静置、时间90min,获得第三微胶囊。
(5)干燥:将第三微胶囊在恒温箱510中以37℃恒温定型,再用干燥机520以温度37~45℃条件干燥24h,获得三联益生菌微胶囊,保存。
微胶囊性能指标的检测
对上述实施例所制备的三联益生菌微胶囊进行性能指标的检测,具体检测方法和结果如下所述:
(1)外观检测:利用扫描电子显微镜测定微胶囊的外观,发现微胶囊的表面光滑,大小均匀一致,且微胶囊之间互不粘连。
(2)粒径与截面的检测:利用扫描电子显微镜测定微胶囊的粒径,发现微胶囊粒径较小,粒径分布范围较窄,呈球性较好;利用背散射电子衍射仪检测微胶囊截面,发现益生菌被严密地包裹在微胶囊的壁材之内,微胶囊的壁材分布均匀、厚度一致,且完整无破损。
(3)包埋率的检测:
配置解囊液:称取14.2g Na2HPO4和9.6g柠檬酸,加水溶解并定容至1000mL,调节pH值为7.25,121℃灭菌20min。
检测包埋率:称取lg微胶囊2份,分别加入到9mL PBS缓冲液和9mL解囊液中,在胶囊待胀溶和溶解完全时,分别采用试管10倍稀释法稀释,并将稀释后的液体倾注于平板上,置培养箱中培养24h后进行活菌计数,并计算包囊效率:
包囊效率=(B2-B1)/B2×100%
式中:B2为微胶囊的活菌数(微胶囊表面与其内部活菌数之和);B1为微胶囊表面的活菌数。
检测结果:发现微胶囊的包埋率均高于89%。
(4)耐酸性的检测:
配置人工胃酸:量取0.1mol/L稀盐酸16.4mL,加蒸馏水约800mL和胃蛋白酶10g,摇匀后加蒸馏水定容至1000mL,用1mol/L NaOH调节PH为2.5。
检测耐酸性:称取1g微胶囊溶于9mL人工胃液中,充分搅拌,分别在60和90min时取样,将微胶囊过滤,用生理盐水洗涤至中性,干燥,将干燥好的微胶囊制剂用上述解囊液处理后,采用10倍稀释法进行活菌计数。
检测结果:发现60min后微胶囊在人工胃液中不崩解释放,对益生菌菌体起到很好的保护,活菌数变化不大,在90min后活菌数仍达能到128cfu/g以上。
(5)肠溶性的检测:
配制肠溶液:称取KH2PO4 6.8g,加入500mL蒸馏水溶解,用4g/L NaOH调节pH为6.8,121℃灭菌20min。称取胰酶10g,加适量无菌水使之溶解。将上述2液混合后,无菌水定容至1000mL,即得人工肠液。
检测方法:称取1g微胶囊2份,置于盛有100mL人工肠液中,于37℃恒温水浴中搅拌,搅拌速度50r/min,分别于0、40、60min时取样,以人工肠液为空白对照组,在680nm波长下测定其透光率(OD680),根据OD680值变化来分析人工肠液中微胶囊的溶出情况。
检测结果:在处理的前40min,OD680值上升较多,处理40min后,OD680值基本稳定,处理60min后,其OD680值基本稳定,观察可知在60min时,人工肠液中已不含固体颗粒。由此可知,微胶囊在人工肠液中完全崩解的时间为60min。
(6)稳定性的检测:
检测方法:称取10g微胶囊,以铂纸密封,置于相对湿度60%~65%、37℃恒温培养箱中放置3个月,每月取1份(1g),采用10倍稀释法进行活菌计数。
检测结果:检测结果见下表1,由此可知,微胶囊化后的益生菌对外界不利因素的抵抗力较强,微胶囊的稳定性得到了提高,依据Van’t Hoff规律可推断,微胶囊的室温储存时间为1年。
表1微胶囊的稳定性试验结果
以上所述仅为本实用新型的优选实施例而已,并不用于限制本实用新型,本实用新型可以有各种更改和变化。凡在本实用新型的精神和原则之内,所作的任何修改、等同替换、改进等,均应包含在本实用新型的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!