包含稀有脂肪酸的代谢改善剂的制作方法
本发明涉及含有稀有脂肪酸的代谢改善剂。更具体地讲,本发明涉及代谢改善剂,其利用了稀有脂肪酸(如氧代脂肪酸、羟基脂肪酸等)的生理学功能,例如,改善脂质、糖和能量的代谢的效果。本发明也涉及含有所述药剂的食物、药物产品、饲料等。
背景技术:
近年来,由于暴饮暴食、缺乏锻炼等造成的肥胖,特别是伴随有内脏脂肪累积的与生活方式相关的疾病,已经成为社会问题。代谢综合征指代这样的状况,其中并发高血糖、高血压和脂质异常中的至少两项,并且由于内脏脂肪型肥胖而容易发展成动脉硬化。在年龄40-74的日本人中,估计每两名男性中有一位而每五名女性中有一位患有或可能患有代谢综合征。因此,已经提出了以预防或解决代谢综合征中的脂质累积进展为目标,通过饮食疗法调整热量摄入的重要性。
对于摄入、进食据报道具有脂质代谢改善效果、糖尿病改善效果等的功能性脂质,有着相当大的兴趣,所述功能性脂质包括:共轭脂肪酸(如共轭亚油酸等)(非专利文件1)、ω3多不饱和脂肪酸(如二十碳五烯酸、二十二碳六烯酸等)(专利文件1)、中链脂肪酸(专利文件2)等。
另外,近年来已经报道了番茄中含有的一部分氧代脂肪酸(如9-氧代-十八碳二烯酸、13-氧代-十八碳二烯酸等)具有改善与生活方式相关的疾病的活性,如改善脂质代谢等(专利文件3;非专利文件2、3)。因此,稀有脂肪酸(如氧代脂肪酸、羟基脂肪酸等)的生理学功能也备受关注。
关于稀有脂肪酸(如氧代脂肪酸、羟基化脂肪酸等)的生产,已报道过C10-位羟基化脂肪酸和C10-位氧代脂肪酸的生产方法,所述脂肪酸各自均含有18个碳原子,所述方法使用来源于植物乳杆菌(Lactobacillus plantarum)的水合脱水酶,并且所述酶是由本发明人发现的(专利文件4)。另外,也已经报道了与这些C10-位羟基化脂肪酸和C10-位氧代脂肪酸相关的代谢改善效果(专利文件5)和肠保护作用(专利文件6)。然而,尚未报道过合适的生产各自含有18个以外的碳原子数的羟基化脂肪酸和氧代脂肪酸或在C10-位以外的位置分别含有羟基、羰基的羟基化脂肪酸和氧代脂肪酸的方法。此外,这些稀有脂肪酸衍生物的生理学功能也是未知的。
[文件列表]
[专利文件]
专利文件1:国际专利申请号2006-521368的国家公布
专利文件2:重新公布的专利号2009/096570
专利文件3:JP-A-2011-184411
专利文件4:WO 2013/168310
专利文件5:WO 2014/069227
专利文件6:WO 2014/129384
[非专利文件]
非专利文件1:Nagao K, (2005), J. Biosci.Bioeng., 第100卷, 第2号, 第152-157页
非专利文件2:Kim Y-I,(2011), Mol.Nutr.Food Res., 第55卷, 第585-593页
非专利文件3:Kim Y-I,(2012), PLoS ONE, 第7卷, 2号, e31317。
[发明概述]
[本发明要解决的问题]
本发明的目的是提供含有稀有脂肪酸的新型代谢改善剂,其改善脂质和/或糖等的代谢。
[解决问题的方法]
考虑到上述问题,本发明人已经进行了深入研究并发现,羟基化脂肪酸,例如,13-羟基-顺-9-十八碳烯酸,或氧代脂肪酸,例如,13-氧代-顺-9-十八碳烯酸,具有过氧化物酶体增殖物激活受体(在下文中也称为“PPAR”)活化作用,这是在传统上未知的生理功能。
基于以上发现完成了本发明。
因此,本发明提供了下列内容:
[1] 包含下列脂肪酸的代谢改善剂:
(1) 含有18个碳原子并在13-位具有羟基或羰基的脂肪酸,
(2) 含有20个碳原子并在15-位具有羟基或羰基的脂肪酸,
(3) 含有20个碳原子并在12-位具有羟基或羰基的脂肪酸,
(4) 含有16个碳原子并在10-位具有羟基或羰基的脂肪酸;
[2] [1]的药剂,其包含下列脂肪酸:
(1) 含有18个碳原子并在13-位具有羟基或羰基的在6-位、9-位、15-位具有至少一个顺式双键的饱和脂肪酸或不饱和脂肪酸,
(2) 含有20个碳原子并在15-位具有羟基或羰基的在5-位、8-位、11-位、17-位具有至少一个顺式双键的不饱和脂肪酸,以及
(3) 含有20个碳原子并在12-位具有羟基或羰基的在5-位、8-位、14-位、17-位具有至少一个顺式双键的饱和脂肪酸或不饱和脂肪酸,或
(4) 含有16个碳原子并在10-位具有羟基或羰基的饱和脂肪酸;
[3] [2]的药剂,其包含下列脂肪酸:
(1) 含有18个碳原子并在13-位具有羟基或羰基的在6-位、9-位、15-位具有至少一个顺式双键的饱和脂肪酸或不饱和脂肪酸,或
(2) 含有20个碳原子并在15-位具有羟基或羰基的在5-位、8-位、11-位、17-位具有至少一个顺式双键的不饱和脂肪酸;
[4] [2]的药剂,其中
(1) 所述含有18个碳原子并在13-位具有羟基或羰基的在6-位、9-位、15-位具有至少一个顺式双键的饱和脂肪酸或不饱和脂肪酸是:13-羟基-顺-9-十八碳烯酸、13-羟基-顺-6,顺-9-十八碳二烯酸、13-羟基-顺-9,顺-15-十八碳二烯酸、13-羟基-顺-6,顺-9,顺-15-十八碳三烯酸、10,13-二羟基-十八烷酸、10,13-二羟基-顺-6-十八碳烯酸、10,13-二羟基-顺-15-十八碳烯酸、10,13-二羟基-顺-6,顺-15-十八碳二烯酸、10-氧代-13-羟基-十八烷酸、10-氧代-13-羟基-顺-6-十八碳烯酸、10-氧代-13-羟基-顺-15-十八碳烯酸、10-氧代-13-羟基-顺-6,顺-15-十八碳二烯酸、13-羟基-顺-5,顺-9-十八碳二烯酸、13-羟基-反-5,顺-9-十八碳二烯酸、13-氧代-顺-9-十八碳烯酸、13-氧代-顺-6,顺-9-十八碳二烯酸、13-氧代-顺-9,顺-15-十八碳二烯酸、13-氧代-顺-6,顺-9,顺-15-十八碳三烯酸、10,13-二氧代-十八烷酸、10,13-二氧代-顺-6-十八碳烯酸、10,13-二氧代-顺-15-十八碳烯酸、10,13-二氧代-顺-6,顺-15-十八碳二烯酸、13-氧代-顺-5,顺-9-十八碳二烯酸或13-氧代-反-5,顺-9-十八碳二烯酸,
(2) 所述含有20个碳原子并在15-位具有羟基或羰基的在5-位、8-位、11-位、17-位具有至少一个顺式双键的不饱和脂肪酸是:15-羟基-顺-11-二十碳烯酸、15-羟基-顺-11,顺-17-二十碳二烯酸、15-羟基-顺-8,顺-11-二十碳二烯酸、15-羟基-顺-5,顺-8,顺-11-二十碳三烯酸、15-羟基-顺-8,顺-11,顺-17-二十碳三烯酸、15-羟基-顺-5,顺-11-二十碳二烯酸、15-羟基-顺-5,顺-11,顺-17-二十碳三烯酸、15-氧代-顺-11-二十碳烯酸、15-氧代-顺-11,顺-17-二十碳二烯酸、15-氧代-顺-8,顺-11-二十碳二烯酸、15-氧代-顺-5,顺-8,顺-11-二十碳三烯酸、15-氧代-顺-8,顺-11,顺-17-二十碳三烯酸、15-氧代-顺-5,顺-11-二十碳二烯酸或15-氧代-顺-5,顺-11,顺-17-二十碳三烯酸,
(3) 所述含有20个碳原子并在12-位具有羟基或羰基的在5-位、8-位、14-位、17-位具有至少一个顺式双键的饱和脂肪酸或不饱和脂肪酸是:12-羟基-顺-14-二十碳烯酸、12-羟基-顺-14,顺-17-二十碳二烯酸、12-羟基-顺-8,顺-14-二十碳二烯酸、12-羟基-顺-5,顺-8-二十碳二烯酸、12-羟基-顺-8,顺-14,顺-17-二十碳三烯酸、12-羟基-顺-5,顺-8,顺-14-二十碳三烯酸、12-氧代-顺-14-二十碳烯酸、12-氧代-顺-14,顺-17-二十碳二烯酸、12-氧代-顺-8,顺-14-二十碳二烯酸、12-氧代-顺-5,顺-8-二十碳二烯酸、12-氧代-顺-8,顺-14,顺-17-二十碳三烯酸或12-氧代-顺-5,顺-8,顺-14-二十碳三烯酸,并且
(4) 所述含有16个碳原子并在10-位具有羟基或羰基的饱和脂肪酸是10-羟基-十六烷酸或10-氧代-十六烷酸;
[5] [3]的药剂,其中
(1) 所述含有18个碳原子并在13-位具有羟基或羰基的在6-位、9-位、15-位具有至少一个顺式双键的饱和脂肪酸或不饱和脂肪酸是:13-羟基-顺-9-十八碳烯酸、13-羟基-顺-6,顺-9-十八碳二烯酸、13-羟基-顺-9,顺-15-十八碳二烯酸、10,13-二羟基-十八烷酸、10,13-二羟基-顺-6-十八碳烯酸、10,13-二羟基-顺-15-十八碳烯酸、13-氧代-顺-9-十八碳烯酸、13-氧代-顺-6,顺-9-十八碳二烯酸或13-氧代-顺-9,顺-15-十八碳二烯酸,并且
(2) 所述含有20个碳原子并在15-位具有羟基或羰基的在5-位、8-位、11-位、17-位具有至少一个顺式双键的不饱和脂肪酸是15-羟基-顺-5,顺-8,顺-11-二十碳三烯酸;
[6] [1]-[5]中任一项的药剂,其用于预防或改善选自肥胖症、糖尿病、脂质代谢异常、高脂血症和脂肪肝的至少一种。
[7] [1]-[5]中任一项的药剂,其是食物或食物添加剂。
[8] [1]-[5]中任一项的药剂,其是药物产品。
[9] [1]-[5]中任一项的药剂,其是饲料或饲料添加剂。
[10] 包含下列脂肪酸的PPAR活性促进剂:
(1) 含有18个碳原子并在13-位具有羟基或羰基的脂肪酸,
(2) 含有20个碳原子并在15-位具有羟基或羰基的脂肪酸,
(3) 含有20个碳原子并在12-位具有羟基或羰基的脂肪酸,
(4) 含有16个碳原子并在10-位具有羟基或羰基的脂肪酸;
[11] [10]的促进剂,其包含下列脂肪酸:
(1) 含有18个碳原子并在13-位具有羟基或羰基的在6-位、9-位、15-位具有至少一个顺式双键的饱和脂肪酸或不饱和脂肪酸,
(2) 含有20个碳原子并在15-位具有羟基或羰基的在5-位、8-位、11-位、17-位具有至少一个顺式双键的不饱和脂肪酸,
(3) 含有20个碳原子并在12-位具有羟基或羰基的在5-位、8-位、14-位、17-位具有至少一个顺式双键的饱和脂肪酸或不饱和脂肪酸,或
(4) 含有16个碳原子并在10-位具有羟基或羰基的饱和脂肪酸;
[12] [11]的促进剂,其包含下列脂肪酸:
(1) 含有18个碳原子并在13-位具有羟基或羰基的在6-位、9-位、15-位具有至少一个顺式双键的饱和脂肪酸或不饱和脂肪酸,或
(2) 含有20个碳原子并在15-位具有羟基或羰基的在5-位、8-位、11-位、17-位具有至少一个顺式双键的不饱和脂肪酸;
[13] [11]的促进剂,其中
(1) 所述含有18个碳原子并在13-位具有羟基或羰基的在6-位、9-位、15-位具有至少一个顺式双键的饱和脂肪酸或不饱和脂肪酸是:13-羟基-顺-9-十八碳烯酸、13-羟基-顺-6,顺-9-十八碳二烯酸、13-羟基-顺-9,顺-15-十八碳二烯酸、13-羟基-顺-6,顺-9,顺-15-十八碳三烯酸、10,13-二羟基-十八烷酸、10,13-二羟基-顺-6-十八碳烯酸、10,13-二羟基-顺-15-十八碳烯酸、10,13-二羟基-顺-6,顺-15-十八碳二烯酸、10-氧代-13-羟基-十八烷酸、10-氧代-13-羟基-顺-6-十八碳烯酸、10-氧代-13-羟基-顺-15-十八碳烯酸、10-氧代-13-羟基-顺-6,顺-15-十八碳二烯酸、13-羟基-顺-5,顺-9-十八碳二烯酸、13-羟基-反-5,顺-9-十八碳二烯酸、13-氧代-顺-9-十八碳烯酸、13-氧代-顺-6,顺-9-十八碳二烯酸、13-氧代-顺-9,顺-15-十八碳二烯酸、13-氧代-顺-6,顺-9,顺-15-十八碳三烯酸、10,13-二氧代-十八烷酸、10,13-二氧代-顺-6-十八碳烯酸、10,13-二氧代-顺-15-十八碳烯酸、10,13-二氧代-顺-6,顺-15-十八碳二烯酸、13-氧代-顺-5,顺-9-十八碳二烯酸或13-氧代-反-5,顺-9-十八碳二烯酸,
(2) 所述含有20个碳原子并在15-位具有羟基或羰基的在5-位、8-位、11-位、17-位具有至少一个顺式双键的不饱和脂肪酸是:15-羟基-顺-11-二十碳烯酸、15-羟基-顺-11,顺-17-二十碳二烯酸、15-羟基-顺-8,顺-11-二十碳二烯酸、15-羟基-顺-5,顺-8,顺-11-二十碳三烯酸、15-羟基-顺-8,顺-11,顺-17-二十碳三烯酸、15-羟基-顺-5,顺-11-二十碳二烯酸、15-羟基-顺-5,顺-11,顺-17-二十碳三烯酸、15-氧代-顺-11-二十碳烯酸、15-氧代-顺-11,顺-17-二十碳二烯酸、15-氧代-顺-8,顺-11-二十碳二烯酸、15-氧代-顺-5,顺-8,顺-11-二十碳三烯酸、15-氧代-顺-8,顺-11,顺-17-二十碳三烯酸、15-氧代-顺-5,顺-11-二十碳二烯酸或15-氧代-顺-5,顺-11,顺-17-二十碳三烯酸,
(3) 所述含有20个碳原子并在12-位具有羟基或羰基的在5-位、8-位、14-位、17-位具有至少一个顺式双键的饱和脂肪酸或不饱和脂肪酸是:12-羟基-顺-14-二十碳烯酸、12-羟基-顺-14,顺-17-二十碳二烯酸、12-羟基-顺-8,顺-14-二十碳二烯酸、12-羟基-顺-5,顺-8-二十碳二烯酸、12-羟基-顺-8,顺-14,顺-17-二十碳三烯酸、12-羟基-顺-5,顺-8,顺-14-二十碳三烯酸、12-氧代-顺-14-二十碳烯酸、12-氧代-顺-14,顺-17-二十碳二烯酸、12-氧代-顺-8,顺-14-二十碳二烯酸、12-氧代-顺-5,顺-8-二十碳二烯酸、12-氧代-顺-8,顺-14,顺-17-二十碳三烯酸或12-氧代-顺-5,顺-8,顺-14-二十碳三烯酸,并且
(4) 所述含有16个碳原子并在10-位具有羟基或羰基的饱和脂肪酸是10-羟基-十六烷酸或10-氧代-十六烷酸;
[14] [12]的促进剂,其中
(1) 所述含有18个碳原子并在13-位具有羟基或羰基的在6-位、9-位、15-位具有至少一个顺式双键的饱和脂肪酸或不饱和脂肪酸是:13-羟基-顺-9-十八碳烯酸、13-羟基-顺-6,顺-9-十八碳二烯酸、13-羟基-顺-9,顺-15-十八碳二烯酸、10,13-二羟基-十八烷酸、10,13-二羟基-顺-6-十八碳烯酸、10,13-二羟基-顺-15-十八碳烯酸、13-氧代-顺-9-十八碳烯酸、13-氧代-顺-6,顺-9-十八碳二烯酸或13-氧代-顺-9,顺-15-十八碳二烯酸,并且
(2) 所述含有20个碳原子并在15-位具有羟基或羰基的在5-位、8-位、11-位、17-位具有至少一个顺式双键的不饱和脂肪酸是15-羟基-顺-5,顺-8,顺-11-二十碳三烯酸;
[15] [10]―[14]中任一项的促进剂,其中所述PPAR是PPARα或PPARγ;
[16] 预防或治疗代谢相关疾病的方法,包括向患者施用有效量的[1]-[5]中任一项的脂肪酸;
[17] [16]的方法,其中所述代谢相关疾病是选自肥胖症、糖尿病、脂质代谢异常、高脂血症和脂肪肝的至少一种;
[18] [1]-[5]中任一项的脂肪酸,用于预防或治疗代谢相关疾病;
[19] [18]的脂肪酸,其中所述代谢相关疾病是选自肥胖症、糖尿病、脂质代谢异常、高脂血症和脂肪肝的至少一种;
[20] [1]-[5]中任一项的脂肪酸在生产用于代谢相关疾病的预防或治疗剂中的用途;
[21] [20]的用途,其中所述代谢相关疾病是选自肥胖症、糖尿病、脂质代谢异常、高脂血症和脂肪肝的至少一种。
发明效果
在本发明中,据发现,羟基化脂肪酸或氧代脂肪酸(如13-羟基-顺-9-十八碳烯酸和13-氧代-顺-9-十八碳烯酸)(在下文中也称为羟基化脂肪酸等)具有PPAR活化作用,这是在传统上未知的生理学功能。
基于此种功能,本发明提供了含有稀有脂肪酸(如上述羟基化脂肪酸等)的代谢改善剂。由于所述药剂可以用于如药物产品、食物、饲料等各个领域,所以本发明在工业上极为有用。
[附图说明]
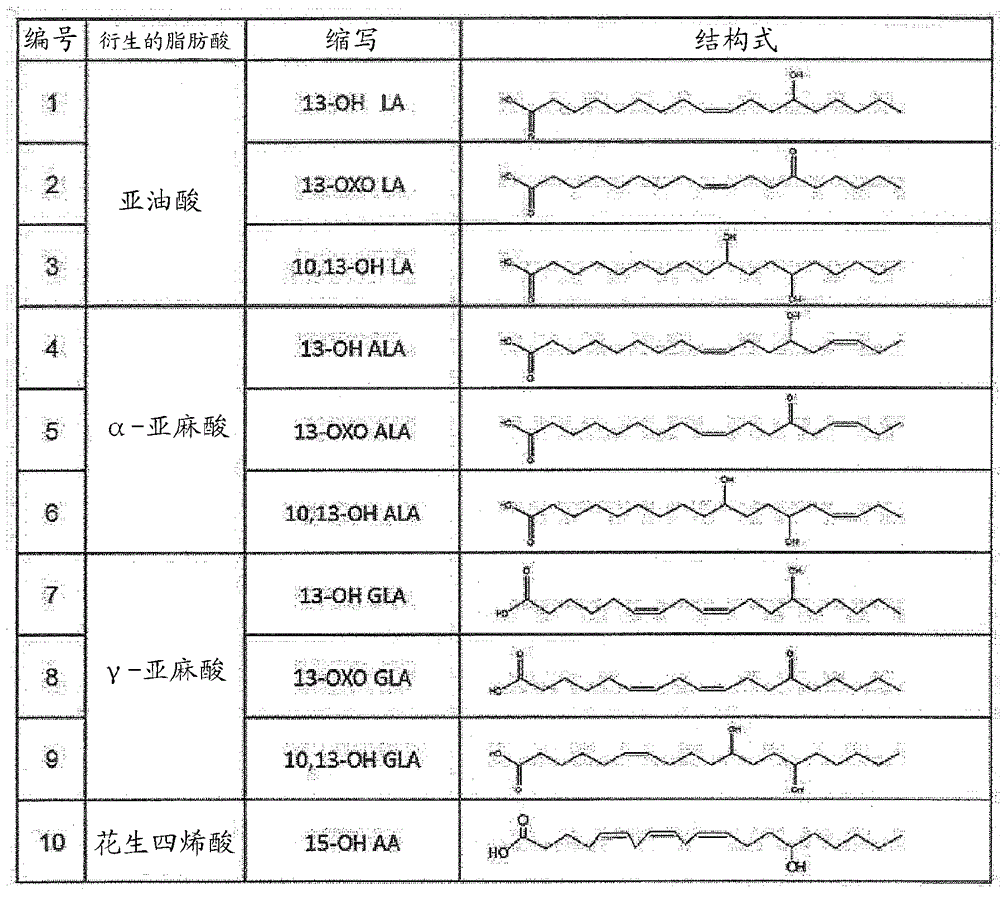
图1示出了针对其PPARα/γ激动剂活性所测量的羟基化脂肪酸和氧代脂肪酸的结构式。
图2示出了羟基化脂肪酸和氧代脂肪酸的PPARα激动剂活性的结果,其中EtOH显示阴性对照(加入乙醇),GW7647显示阳性对照(加入PPARα激动剂),而纵轴显示相对的萤光素酶活性。
图3示出了羟基化脂肪酸和氧代脂肪酸的PPARγ激动剂活性的结果,其中EtOH显示阴性对照(加入乙醇),Tro显示阳性对照(加入PPARγ激动剂),而纵轴显示相对的萤光素酶活性。
[实施方案说明]
本发明详细解释于下。
在本发明中,“代谢改善”意指脂质和/或糖和/或能量的代谢得到改善。具体地讲,例如,脂质代谢改善意指促进存在于身体组织、血液或淋巴组织中的脂质的分解、抑制脂质合成、防止和/或抑制身体组织(如脂肪组织等)中脂质的累积或减少累积在身体组织等中的脂质。“脂质”是甘油三酯和/或胆固醇,包括脂肪酸。
改善糖代谢意指抑制存在于血液中的糖和/或糖化血红蛋白(HbA1c)、空腹血糖水平的升高或促进进食后的糖代谢。此外,糖代谢改善也包括改善葡萄糖耐受性不良(不包括在正常类型或糖尿病型以及糖尿病前期中的病理)。“糖”指代单糖、二糖或多糖。
改善能量代谢意指将能量摄入水平与能量释放水平的平衡异常状态或能量摄入水平与能量释放水平的平衡的无法得到控制的状态带到正常状态或接近正常状态。
作为上述代谢改善的指标,可以测量PPAR活性。已知PPAR包括至少3种亚型:PPARα、PPARδ(同β)和PPARγ。PPARα主要在肝、心、肾、骨骼肌、棕色脂肪细胞等中表达,并且涉及对与脂肪酸β氧化相关的许多基因的控制。相对地,PPARδ在全身表达(脑、脂肪组织、皮肤等)。PPARγ有至少3种同工型,主要在白色脂肪细胞和巨噬细胞中表达,并且涉及脂肪细胞分化等。当是否存在来自这些PPAR中的至少一种PPAR的配体(激动剂、拮抗剂)活性得到确认并发现了激动剂活性时,则断定具有代谢改善效果的可能性高或存在代谢改善效果。作为一个实例,可以进行FEBS Letters 514 (2002) 第315-322页中所述的PPAR报告基因测定。然而,该方法不限于此。
作为另外一种选择,作为代谢改善的指标,本发明的稀有脂肪酸可施用于肥胖症或糖尿病动物模型,测量了体重、器官重量、血糖水平、中性脂肪值、耗氧量水平、直肠温度等,并可以确认其是否存在改变。肥胖症或糖尿病动物模型不受限制,只要其为显示这些特性的动物。例如,作为上述动物模型,可以列举出可商购的KKAy小鼠、NOD小鼠、NSY小鼠、TSOD小鼠、ZDF/Crl-Leprfa大鼠、SDT/Jcl大鼠等。体重、器官重量、血糖水平、中性脂肪值、耗氧量水平、直肠温度等可以由已知方法测量。使用这些作为指标,当观察到体重或器官重量、或血糖水平、中性脂肪值下降时,或当观察到耗氧量水平或直肠温度上升时,则断定具有代谢改善效果的可能性高或存在代谢改善效果。
作为另外一种选择,作为代谢改善的指标,可以确认加入本发明的稀有脂肪酸是否抑制了由LXR激动剂诱导的脂质合成促进作用。作为其方法,可以参考例如,Journal of Lipid Research 47 (2006) 2712-2717,但所述方法不限于此。上述文件中所述的方法包括:加入LXR激动剂,并且(1) 测量脂质合成相关因子(例如,SREBP-1c、成熟和不成熟的SREBP-1、SCD-1、FAS、ACC1和/或ACC2)的mRNA和/或蛋白质的表达水平;(2) 测量细胞内三酰甘油水平;或(3) 进行萤光素酶测定。LXR激动剂的实例包括但不限于T0901317、22(R)-羟基胆固醇、24(S)-羟基胆固醇等。当脂质合成相关因子的mRNA和/或蛋白质的表达水平下降时,则断定脂质合成受到抑制,并且具有代谢改善效果的可能性高或存在代谢改善效果。
在本发明中,含有18个碳原子并在13-位具有羟基或羰基的脂肪酸指含有18个碳原子并在13-位具有羟基的羟基化脂肪酸(在下文中有时简称“13-羟基脂肪酸”)或含有18个碳原子并在13-位具有羰基的氧代脂肪酸(在下文中有时简称“13-氧代脂肪酸”)。如本文所用,在“13-羟基脂肪酸”或“13-氧代脂肪酸”的一个实施方案中也涵盖了含有18个碳原子并在10-位和13-位具有羟基或羰基的脂肪酸(在下文中有时简称“10,13-二羟基脂肪酸”或“10,13-二氧代脂肪酸”)以及含有18个碳原子并在13-位具有羟基而在10-位具有羰基的脂肪酸(在下文中有时简称“10-氧代-13-羟基脂肪酸”)。另外,所述含有18个碳原子并在13-位具有羟基或羰基的脂肪酸可以是饱和脂肪酸或不饱和脂肪酸。当其为不饱和脂肪酸时,优选在6-位、9-位和15-位具有至少一个顺式双键的不饱和脂肪酸。
在本发明中,含有20个碳原子并在15-位具有羟基或羰基的脂肪酸指含有20个碳原子并在15-位具有羟基的羟基化脂肪酸(在下文中有时简称“15-羟基脂肪酸”)或含有20个碳原子并在15-位具有羰基的氧代脂肪酸(在下文中有时简称“15-氧代脂肪酸”)。另外,所述含有20个碳原子并在15-位具有羟基或羰基的脂肪酸可以是饱和脂肪酸或不饱和脂肪酸。当其为不饱和脂肪酸时,优选在5-位、8-位、11-位、17-位具有至少一个顺式双键的不饱和脂肪酸。
在本发明中,含有20个碳原子并在12-位具有羟基或羰基的脂肪酸指含有20个碳原子并在12-位具有羟基的羟基化脂肪酸(在下文中有时简称“12-羟基脂肪酸”)或含有20个碳原子并在12-位具有羰基的氧代脂肪酸(在下文中有时简称“12-氧代脂肪酸”)。另外,所述含有20个碳原子并在12-位具有羟基或羰基的脂肪酸可以是饱和脂肪酸或不饱和脂肪酸。当其为不饱和脂肪酸时,优选在5-位、8-位、14-位、17-位具有至少一个顺式双键的不饱和脂肪酸。
在本发明中,含有16个碳原子并在10-位具有羟基或羰基的脂肪酸指含有16个碳原子并在10-位具有羟基的羟基化脂肪酸(在下文中有时简称“10-羟基脂肪酸”)或含有16个碳原子并在10-位具有羰基的氧代脂肪酸(在下文中有时简称“10-氧代脂肪酸”)。另外,所述含有16个碳原子并在10-位具有羟基或羰基的脂肪酸可以是饱和脂肪酸或不饱和脂肪酸。
更具体地讲,虽然所述含有18个碳原子并在13-位具有羟基或羰基的在6-位、9-位、15-位具有至少一个顺式双键的饱和脂肪酸或不饱和脂肪酸不受特别限制,但可以提及:13-羟基-顺-9-十八碳烯酸、13-羟基-顺-6,顺-9-十八碳二烯酸、13-羟基-顺-9,顺-15-十八碳二烯酸、13-羟基-顺-6,顺-9,顺-15-十八碳三烯酸、10,13-二羟基-十八烷酸、10,13-二羟基-顺-6-十八碳烯酸、10,13-二羟基-顺-15-十八碳烯酸、10,13-二羟基-顺-6,顺-15-十八碳二烯酸、10-氧代-13-羟基-十八烷酸、10-氧代-13-羟基-顺-6-十八碳烯酸、10-氧代-13-羟基-顺-15-十八碳烯酸、10-氧代-13-羟基-顺-6,顺-15-十八碳二烯酸、13-羟基-顺-5,顺-9-十八碳二烯酸、13-羟基-反-5,顺-9-十八碳二烯酸、13-氧代-顺-9-十八碳烯酸、13-氧代-顺-6,顺-9-十八碳二烯酸、13-氧代-顺-9,顺-15-十八碳二烯酸、13-氧代-顺-6,顺-9,顺-15-十八碳三烯酸、10,13-二氧代-十八烷酸、10,13-二氧代-顺-6-十八碳烯酸、10,13-二氧代-顺-15-十八碳烯酸、10,13-二氧代-顺-6,顺-15-十八碳二烯酸、13-氧代-顺-5,顺-9-十八碳二烯酸或13-氧代-反-5,顺-9-十八碳二烯酸等;更优选地,可以提及:13-羟基-顺-9-十八碳烯酸、13-羟基-顺-6,顺-9-十八碳二烯酸、13-羟基-顺-9,顺-15-十八碳二烯酸、10,13-二羟基-十八烷酸、10,13-二羟基-顺-6-十八碳烯酸、10,13-二羟基-顺-15-十八碳烯酸、13-氧代-顺-9-十八碳烯酸、13-氧代-顺-6,顺-9-十八碳二烯酸或13-氧代-顺-9,顺-15-十八碳二烯酸。
虽然所述含有20个碳原子并在15-位具有羟基或羰基的在5-位、8-位、11-位、17-位具有至少一个顺式双键的不饱和脂肪酸不受特别限制,但可以提及:15-羟基-顺-11-二十碳烯酸、15-羟基-顺-11,顺-17-二十碳二烯酸、15-羟基-顺-8,顺-11-二十碳二烯酸、15-羟基-顺-5,顺-8,顺-11-二十碳三烯酸、15-羟基-顺-8,顺-11,顺-17-二十碳三烯酸、15-羟基-顺-5,顺-11-二十碳二烯酸、15-羟基-顺-5,顺-11,顺-17-二十碳三烯酸、15-氧代-顺-11-二十碳烯酸、15-氧代-顺-11,顺-17-二十碳二烯酸、15-氧代-顺-8,顺-11-二十碳二烯酸、15-氧代-顺-5,顺-8,顺-11-二十碳三烯酸、15-氧代-顺-8,顺-11,顺-17-二十碳三烯酸、15-氧代-顺-5,顺-11-二十碳二烯酸或15-氧代-顺-5,顺-11,顺-17-二十碳三烯酸等;更优选地,可以提及15-羟基-顺-5,顺-8,顺-11-二十碳三烯酸。
虽然所述含有20个碳原子并在12-位具有羟基或羰基的在5-位、8-位、14-位、17-位具有至少一个顺式双键的饱和脂肪酸或不饱和脂肪酸不受特别限制,但可以提及:12-羟基-顺-14-二十碳烯酸、12-羟基-顺-14,顺-17-二十碳二烯酸、12-羟基-顺-8,顺-14-二十碳二烯酸、12-羟基-顺-5,顺-8-二十碳二烯酸、12-羟基-顺-8,顺-14,顺-17-二十碳三烯酸、12-羟基-顺-5,顺-8,顺-14-二十碳三烯酸、12-氧代-顺-14-二十碳烯酸、12-氧代-顺-14,顺-17-二十碳二烯酸、12-氧代-顺-8,顺-14-二十碳二烯酸、12-氧代-顺-5,顺-8-二十碳二烯酸、12-氧代-顺-8,顺-14,顺-17-二十碳三烯酸或12-氧代-顺-5,顺-8,顺-14-二十碳三烯酸等。
虽然所述含有16个碳原子并在10-位具有羟基或羰基的饱和脂肪酸不受特别限制,但可以提及10-羟基-十六烷酸或10-氧代-十六烷酸等。
作为要用于本发明的稀有脂肪酸(如氧代脂肪酸、羟基化脂肪酸等),羟基化脂肪酸是由新型脂肪酸水合酶(FA-HY)从含有16、18、20个碳原子的不饱和脂肪酸生产的,而氧代脂肪酸可以通过由酶反应或化学反应进一步氧化所述羟基化脂肪酸的羟基来生产。具体地讲,其可以通过以下方法制备。
上述新型脂肪酸水合酶“FA-HY”是
(a) 由SEQ ID NO: 2所示的氨基酸序列组成的酶蛋白质;
(b) 蛋白质,其包含氨基酸序列并且具有酶活性,在所述氨基酸序列中SEQ ID NO: 2所示的所述氨基酸序列中的一个或多个氨基酸被缺失和/或取代和/或插入和/或添加,所述酶活性是由SEQ ID NO: 2所示的氨基酸序列组成的酶蛋白质所具有的酶活性;或
(c) 蛋白质,其由碱基序列编码并且具有酶活性,所述碱基序列在严格条件下杂交至核酸,所述核酸由与SEQ ID NO: 1所示的碱基序列互补的链序列组成,所述酶活性是由SEQ ID NO: 2所示的氨基酸序列组成的酶蛋白质所具有的酶活性。
上述(b)的更具体的实例包括含有以下的蛋白质:(i)氨基酸序列,其是SEQ ID NO: 2所示的氨基酸序列,其中1 - 20、优选1 - 10、更优选1 - 几个(5、4、3或2)氨基酸被缺失,(ii) 氨基酸序列,其是SEQ ID NO: 2所示的氨基酸序列,其中1 - 20、优选1 - 10、更优选1 – 几个数目(5、4、3或2)的氨基酸被添加,(iii)氨基酸序列,其是SEQ ID NO: 2所示的氨基酸序列,其中1 - 20、优选1 - 10、更优选1 – 几个(5、4、3或2)氨基酸被插入,(iv) 氨基酸序列,其是SEQ ID NO: 2所示的氨基酸序列,其中1 - 20、优选1 - 10、更优选1 – 几个(5、4、3或2)氨基酸被其它氨基酸取代,或(v) 通过将其组合而获得的氨基酸序列。当具有相似特性的氨基酸(例如,甘氨酸和丙氨酸、缬氨酸和亮氨酸和异亮氨酸、丝氨酸和苏氨酸、天冬氨酸和谷氨酸、天冬酰胺和谷氨酰胺、赖氨酸和精氨酸、半胱氨酸和甲硫氨酸、苯丙氨酸和酪氨酸等)彼此取代等时,可能有更大数目的取代等。
当如上所述氨基酸被缺失、取代或插入时,缺失、取代和插入的位置不受特别限制,只要上述酶活性得以保持。
在上述(c)中,“严格条件”是这样的条件:在该条件下,具有高同一性(例如,70、80、90、95或99%或以上的同一性)的核苷酸序列相互杂交,而具有低于所述的同一性的核苷酸序列不杂交;具体地讲,于对应于常规DNA杂交的洗涤条件中那些的盐浓度和温度(60℃, 1xSSC, 0.1% SDS, 优选地,0.1xSSC, 0.1% SDS, 更优选地, 68℃, 0.1xSSC, 0.1% SDS)等,洗涤一次、更优选2 – 3次的条件。
关于上述(b)或(c),由SEQ ID NO: 2所示的氨基酸序列组成的酶蛋白质所具有的酶活性不受特别限制,只要其具有下列中的至少一项、优选全部:(1)能够将用作底物的含有18个碳原子并在12-位具有顺式双键的不饱和脂肪酸(在下文中有时简称“顺-12不饱和脂肪酸”)转化成含有18个碳原子并在13-位具有羟基的羟基化脂肪酸(13-羟基脂肪酸)(反应 1)的酶活性;(2)能够将用作底物的含有16个碳原子并在9-位具有顺式双键的不饱和脂肪酸(在下文中有时简称“顺-9不饱和脂肪酸”)转化成含有16个碳原子并在10-位具有羟基的羟基化脂肪酸(10-羟基脂肪酸)(反应 2)的酶活性;(3)能够将用作底物的含有20个碳原子并在14-位具有顺式双键的不饱和脂肪酸(在下文中有时简称“顺-14不饱和脂肪酸”)转化成含有20个碳原子并在15-位具有羟基的羟基化脂肪酸(15-羟基脂肪酸)(反应 3)的酶活性;(4)能够将用作底物的含有20个碳原子并在11-位具有顺式双键的不饱和脂肪酸(在下文中有时简称“顺-11不饱和脂肪酸”)转化成含有20个碳原子并在12-位具有羟基的羟基化脂肪酸(12-羟基脂肪酸)(反应 4)的酶活性、能够将顺-4,顺-7,顺-10,顺-13,顺-16,顺-19-二十二碳六烯酸(DHA)转化成14-羟基-顺-4,顺-7,顺-10,顺-16,顺-19-二十二碳五烯酸(反应 A)的酶活性以及能够将顺-9-十四碳烯酸(肉豆蔻脑酸)转化成10-羟基-十四烷酸(反应 I)的酶活性。
上述“顺-12不饱和脂肪酸”、“顺-9不饱和脂肪酸”、“顺-14不饱和脂肪酸”和“顺-11不饱和脂肪酸”不受特别限制,只要其分别是含有18个碳原子并在12-位具有顺式双键的不饱和脂肪酸、含有16个碳原子并在9-位具有顺式双键的不饱和脂肪酸、含有20个碳原子并在14-位具有顺式双键的不饱和脂肪酸、含有20个碳原子并在11-位具有顺式双键的不饱和脂肪酸,并且可以提及例如,单价不饱和脂肪酸、二价不饱和脂肪酸、三价不饱和脂肪酸、四价不饱和脂肪酸、五价不饱和脂肪酸等。在本说明书中,“脂肪酸”不仅涵盖了游离酸,而且涵盖了酯的形式、与碱性化合物的盐等。“DHA”和“肉豆蔻脑酸”也不仅涵盖了游离酸,而且涵盖了酯的形式、与碱性化合物的盐等。
上述FA-HY可以通过本身已知的蛋白质分离和纯化技术分离自,例如,嗜酸乳杆菌(Lactobacillus acidophilus)的菌体、培养基。作为另外一种选择,FA-HY可作为含有FA-HY的嗜酸乳杆菌的菌体或其菌体碎片使用。含有FA-HY的嗜酸乳杆菌的菌体不受特别限制,只要其含有上述FA-HY,并且,例如,可以提及于2014年1月17日在NITE专利微生物保藏中心(NPMD)保藏的NITE BP-01788等。作为另外一种选择,FA-HY也可以通过如下步骤作为重组蛋白质生产:分离编码FA-HY的基因,将所述基因亚克隆到合适的载体中,将所述载体引入到合适的宿主(如大肠杆菌(Escherichia coli)等)中并培养所述宿主。FA-HY可以是经过纯化或粗纯化的。作为另外一种选择,可以在菌体(如大肠杆菌等)中表达水合酶,并且可使用所述菌体自身或可使用其培养基。此外,所述酶可以是游离形式或由各种载体固定化的。
作为含有编码上述FA-HY的核酸的载体,适用于将要引入所述载体的宿主细胞的载体可以根据目标(例如,蛋白质表达)而恰当选择并使用。就表达载体而言,其含有本发明的核酸,所述核酸可操作地连接至适当的启动子,并且优选地在本发明的核酸的下游含有转录终止信号,即,终止子区。此外,其也可以含有用以选择转化体的选择标记基因(耐药基因、补充营养缺陷型突变的基因等)。其也可含有编码标签序列的序列,所述标签序列用于分离和纯化所表达蛋白质等。另外,可将载体整合入靶宿主细胞的基因组中。可以通过本身已知的转化方法(如感受态细胞法、原生质体法、磷酸钙共沉淀法等)将本发明的载体引入到靶宿主细胞中。
在本说明书中,“宿主细胞”可以是任何细胞,只要其可以表达含有编码上述FA-HY的核酸的载体,并且可以提及细菌、酵母、真菌、高等真核细胞等。细菌的实例包括革兰氏阳性细菌(如芽孢杆菌、链霉菌属(Streptomyces)等)和革兰氏阴性细菌(如大肠杆菌等)。引入了含有编码FA-HY的核酸的载体的重组细胞可以通过本身已知的适用于所述宿主细胞的方法来培养。
“纯化”上述FA-HY可以通过本身已知的方法进行,例如,将通过离心等收集到的菌体通过超声处理或玻璃珠等破裂,将固体(如细胞碎片)通过离心等移除等以得到粗酶溶液,使所述粗酶溶液经受盐析法(使用硫酸铵、硫酸钠等)、层析(如离子交换层析、凝胶过滤层析、亲和层析等)、凝胶电泳等。
如上所述,上述FA-HY具有能够将用作底物的顺-12不饱和脂肪酸、顺-9不饱和脂肪酸、顺-14不饱和脂肪酸、顺-11不饱和脂肪酸、DHA、肉豆蔻脑酸分别转化成13-羟基脂肪酸、10-羟基脂肪酸、15-羟基脂肪酸、12-羟基脂肪酸、14-羟基-顺-4,顺-7,顺-10,顺-16,顺-19-二十二碳五烯酸、10-羟基-十四烷酸的酶活性。因此,提供了[1]通过使用上述FA-HY的水合反应从顺-12不饱和脂肪酸生产13-羟基脂肪酸的方法(生产方法 1),[2]通过使用上述FA-HY的水合反应从顺-9不饱和脂肪酸生产10-羟基脂肪酸的方法(生产方法 2),[3]通过使用上述FA-HY的水合反应从顺-14不饱和脂肪酸生产15-羟基脂肪酸的方法(生产方法 3),[4]通过使用上述FA-HY的水合反应从顺-11不饱和脂肪酸生产12-羟基脂肪酸的方法(生产方法 4),[A]通过使用上述FA-HY的水合反应从DHA生产14-羟基-顺-4,顺-7,顺-10,顺-16,顺-19-二十二碳五烯酸的方法(生产方法 A)和[I]通过使用本发明的FA-HY的水合反应从肉豆蔻脑酸生产10-羟基-十四烷酸的方法(生产方法 I)。
上述生产方法1中的“顺-12不饱和脂肪酸”的实例包括:顺-9,顺-12-十八碳二烯酸(亚油酸)、顺-6,顺-9,顺-12-十八碳三烯酸(γ-亚麻酸)、顺-9,顺-12,顺-15-十八碳三烯酸(α-亚麻酸)、顺-6,顺-9,顺-12,顺-15-十八碳四烯酸((6Z,9Z,12Z,15Z)-6,9,12,15-十八碳四烯酸)以及现在可以通过WO 2013/168310生产的10-羟基-顺-12-十八碳烯酸、10-羟基-顺-6,顺-12-十八碳二烯酸、10-羟基-顺-12,顺-15-十八碳二烯酸、10-羟基-顺-6,顺-12,顺-15-十八碳三烯酸、10-氧代-顺-12-十八碳烯酸、10-氧代-顺-6,顺-12-十八碳二烯酸、10-氧代-顺-12,顺-15-十八碳二烯酸、10-氧代-顺-6,顺-12,顺-15-十八碳三烯酸、顺-5,顺-9,顺-12-十八碳三烯酸(皮诺敛酸)、反-5,顺-9,顺-12-十八碳三烯酸(哥伦比亚酸)等。这些底物可以通过WO 2013/168310以外的方法获得。
由上述生产方法1所生产的“13-羟基脂肪酸”的实例包括:由顺-9,顺-12-十八碳二烯酸(亚油酸)诱导的13-羟基-顺-9-十八碳烯酸、由顺-6,顺-9,顺-12-十八碳三烯酸(γ-亚麻酸)诱导的13-羟基-顺-6,顺-9-十八碳二烯酸、由顺-9,顺-12,顺-15-十八碳三烯酸(α-亚麻酸)诱导的13-羟基-顺-9,顺-15-十八碳二烯酸、由顺-6,顺-9,顺-12,顺-15-十八碳四烯酸((6Z,9Z,12Z,15Z)-6,9,12,15-十八碳四烯酸)诱导的13-羟基-顺-6,顺-9,顺-15-十八碳三烯酸、由10-羟基-顺-12-十八碳烯酸诱导的10,13-二羟基-十八烷酸、由10-羟基-顺-6,顺-12-十八碳二烯酸诱导的10,13-二羟基-顺-6-十八碳烯酸、由10-羟基-顺-12,顺-15-十八碳二烯酸诱导的10,13-二羟基-顺-15-十八碳烯酸、由10-羟基-顺-6,顺-12,顺-15-十八碳三烯酸诱导的10,13-二羟基-顺-6,顺-15-十八碳二烯酸、由10-氧代-顺-12-十八碳烯酸诱导的10-氧代-13-羟基-十八烷酸、由10-氧代-顺-6,顺-12-十八碳二烯酸诱导的10-氧代-13-羟基-顺-6-十八碳烯酸、由10-氧代-顺-12,顺-15-十八碳二烯酸诱导的10-氧代-13-羟基-顺-15-十八碳烯酸、由10-氧代-顺-6,顺-12,顺-15-十八碳三烯酸诱导的10-氧代-13-羟基-顺-6,顺-15-十八碳二烯酸、由顺-5,顺-9,顺-12-十八碳三烯酸(皮诺敛酸)诱导的13-羟基-顺-5,顺-9-十八碳二烯酸、由反-5,顺-9,顺-12-十八碳三烯酸 (哥伦比亚酸)诱导的13-羟基-反-5,顺-9-十八碳二烯酸等。
上述生产方法2中的“顺-9不饱和脂肪酸”的实例包括:顺-9-十六碳烯酸(棕榈油酸)等。
由上述生产方法2所生产的“10-羟基脂肪酸”的实例包括:由顺-9-十六碳烯酸(棕榈油酸)诱导的10-羟基-十六烷酸等。
上述生产方法3中的“顺-14不饱和脂肪酸”的实例包括:顺-11,顺-14-二十碳二烯酸、顺-11,顺-14,顺-17-二十碳三烯酸、顺-8,顺-11,顺-14-二十碳三烯酸(二高-γ-亚麻酸)、顺-5,顺-8,顺-11,顺-14-二十碳四烯酸(花生四烯酸)、顺-8,顺-11,顺-14,顺-17-二十碳四烯酸、顺-5,顺-11,顺-14-二十碳三烯酸(5(Z),11(Z),14(Z)-二十碳三烯酸)、顺-5,顺-11,顺-14,顺-17-二十碳四烯酸((5Z,11Z,14Z,17Z)-5,11,14,17-二十碳四烯酸)等。
由本发明的生产方法3所生产的“15-羟基脂肪酸”的实例包括:由顺-11,顺-14-二十碳二烯酸诱导的15-羟基-顺-11-二十碳烯酸、由顺-11,顺-14,顺-17-二十碳三烯酸诱导的15-羟基-顺-11,顺-17-二十碳二烯酸、由顺-8,顺-11,顺-14-二十碳三烯酸(二高-γ-亚麻酸)诱导的15-羟基-顺-8,顺-11-二十碳二烯酸、由顺-5,顺-8,顺-11,顺-14-二十碳四烯酸(花生四烯酸)诱导的15-羟基-顺-5,顺-8,顺-11-二十碳三烯酸、由顺-8,顺-11,顺-14,顺-17-二十碳四烯酸诱导的15-羟基-顺-8,顺-11,顺-17-二十碳三烯酸、由顺-5,顺-11,顺-14-二十碳三烯酸(5(Z),11(Z),14(Z)-二十碳三烯酸)诱导的15-羟基-顺-5,顺-11-二十碳二烯酸、由顺-5,顺-11,顺-14,顺-17-二十碳四烯酸((5Z,11Z,14Z,17Z)-5,11,14,17-二十碳四烯酸)诱导的15-羟基-顺-5,顺-11,顺-17-二十碳三烯酸等。
本发明的生产方法4中的“顺-11不饱和脂肪酸”的实例包括:顺-11,顺-14-二十碳二烯酸、顺-11,顺-14,顺-17-二十碳三烯酸、顺-8,顺-11,顺-14-二十碳三烯酸(二高-γ-亚麻酸)、顺-5,顺-8,顺-11-二十碳三烯酸((5Z,8Z,11Z)-二十碳-5,8,11-三烯酸)、顺-8,顺-11,顺-14,顺-17-二十碳四烯酸、顺-5,顺-8,顺-11,顺-14-二十碳四烯酸(花生四烯酸)等。
由本发明的生产方法4所生产的“12-羟基脂肪酸”的实例包括:由顺-11,顺-14-二十碳二烯酸诱导的12-羟基-顺-14-二十碳烯酸、由顺-11,顺-14,顺-17-二十碳三烯酸诱导的12-羟基-顺-14,顺-17-二十碳二烯酸、由顺-8,顺-11,顺-14-二十碳三烯酸(二高-γ-亚麻酸)诱导的12-羟基-顺-8,顺-14-二十碳二烯酸、由顺-5,顺-8,顺-11-二十碳三烯酸((5Z,8Z,11Z)-二十碳-5,8,11-三烯酸)诱导的12-羟基-顺-5,顺-8-二十碳二烯酸、由顺-8,顺-11,顺-14,顺-17-二十碳四烯酸诱导的12-羟基-顺-8,顺-14,顺-17-二十碳三烯酸、由顺-5,顺-8,顺-11,顺-14-二十碳四烯酸(花生四烯酸)诱导的12-羟基-顺-5,顺-8,顺-14-二十碳三烯酸等。
水合反应可以在合适的缓冲液(例如,磷酸盐缓冲液、Tris缓冲液、硼酸盐缓冲液等)中通过以下进行:将作为底物的不饱和脂肪酸与上述FA-HY于合适的浓度混合并温育所述混合物。底物浓度为,例如,1 - 1000 g/L,优选10 - 500 g/L,更优选20 - 250 g/L。将要加入的上述FA-HY的量为,例如,0.001 - 10 mg/mL,优选0.1 - 5 mg/mL,更优选0.2 - 2 mg/mL。
“辅因子”可用于水合反应(反应 1 - 4、反应 A 或 反应 I)并且,例如,可使用FAD等。添加的浓度可以是任意的,只要所述水合反应有效地进行。优选0.001 – 20 mM,更优选0.01 – 10 mM。
此外,“激活剂”可用于所述水合反应并且,例如,可以提及选自NADH和NADPH的1种或2种化合物。其添加的浓度可以是任意的,只要所述水合反应有效地进行。优选0.1 – 20 mM,更优选1 – 10 mM。
期望的是,水合反应在上述FA-HY的优选温度下和优选pH范围内进行。例如,反应温度为5 - 50℃,优选20 - 45℃。反应混合物的pH为,例如,pH 4 - 10,优选pH 5 - 9。反应时间不受特别限制,并且其为,例如,10 分钟 - 72 小时,优选30 分钟 - 36 小时。
在本发明的一个优选的实施方案中,将上述FA-HY以重组细胞(例如,大肠杆菌、枯草芽孢杆菌(Bacillus subtilis)、酵母、昆虫细胞、动物细胞等)的形式提供给反应体系,所述重组细胞中引入了含有编码所述酶的核酸的表达载体。在这种情况下,水合反应也可以通过如下进行:在适合于所述细胞的培养、并加入了辅因子和底物以及在必要时激活剂的液体培养基中培养所述细胞。
此外,通过脱氢反应或使用铬酸的化学氧化,从在上述生产方法 1 - 4、生产方法 A、生产方法 I中获得的13-羟基脂肪酸生产了含有18个碳原子并在13-位具有羰基的氧代脂肪酸(在下文中有时简称“13-氧代脂肪酸”)(反应 5),从10-羟基脂肪酸生产了含有16个碳原子并在10-位具有羰基的氧代脂肪酸(在下文中有时简称“10-氧代脂肪酸”)(反应 6),从15-羟基脂肪酸生产了含有20个碳原子并在15-位具有羰基的氧代脂肪酸(在下文中有时简称“15-氧代脂肪酸”)(反应 7),从12-羟基脂肪酸生产了含有20个碳原子并在12-位具有羰基的氧代脂肪酸(在下文中有时简称“12-氧代脂肪酸”)(反应 8),从14-羟基-顺-4,顺-7,顺-10,顺-16,顺-19-二十二碳五烯酸生产了14-氧代-顺-4,顺-7,顺-10,顺-16,顺-19-二十二碳五烯酸(反应 B),以及从10-羟基-十四烷酸生产了10-氧代-十四烷酸(反应 II)。
因此,提供了:[5] 生产13-氧代脂肪酸的方法,包括使顺-12不饱和脂肪酸经受使用上述FA-HY的水合反应以诱导13-羟基脂肪酸,并使所述13-羟基脂肪酸经受脱氢反应或化学氧化(生产方法 5);[6] 生产10-氧代脂肪酸的方法,包括使顺-9不饱和脂肪酸经受使用上述FA-HY的水合反应以诱导10-羟基脂肪酸,并使所述10-羟基脂肪酸经受脱氢反应或化学氧化(生产方法 6);[7] 生产15-氧代脂肪酸的方法,包括使顺-14不饱和脂肪酸经受使用上述FA-HY的水合反应以诱导15-羟基脂肪酸,并使所述15-羟基脂肪酸经受脱氢反应或化学氧化(生产方法 7);[8] 生产12-氧代脂肪酸的方法,包括使顺-11不饱和脂肪酸经受使用上述FA-HY的水合反应以诱导12-羟基脂肪酸,并使所述12-羟基脂肪酸经受脱氢反应或化学氧化(生产方法 8);[B] 生产14-氧代-顺-4,顺-7,顺-10,顺-16,顺-19-二十二碳五烯酸的方法,包括使DHA经受使用本发明的FA-HY的水合反应以诱导14-羟基-顺-4,顺-7,顺-10,顺-16,顺-19-二十二碳五烯酸,并使所述14-羟基-顺-4,顺-7,顺-10,顺-16,顺-19-二十二碳五烯酸经受脱氢反应或化学氧化(生产方法 B);以及 [II] 生产10-氧代-十四烷酸的方法,包括使肉豆蔻脑酸经受使用本发明的FA-HY的水合反应以诱导10-羟基-十四烷酸,并使所述10-羟基-十四烷酸经受脱氢反应或化学氧化(生产方法 II)。
上述生产方法5-8中的“顺-12不饱和脂肪酸”、“顺-9不饱和脂肪酸”、“顺-14不饱和脂肪酸”、“顺-11不饱和脂肪酸”与上述生产方法1-4中的底物相同。
由上述生产方法5所生产的“13-氧代脂肪酸”的实例包括:由顺-9,顺-12-十八碳二烯酸(亚油酸)诱导的13-氧代-顺-9-十八碳烯酸、由顺-6,顺-9,顺-12-十八碳三烯酸(γ-亚麻酸)诱导的13-氧代-顺-6,顺-9-十八碳二烯酸、由顺-9,顺-12,顺-15-十八碳三烯酸(α-亚麻酸)诱导的13-氧代-顺-9,顺-15-十八碳二烯酸、由顺-6,顺-9,顺-12,顺-15-十八碳四烯酸((6Z,9Z,12Z,15Z)-6,9,12,15-十八碳四烯酸)诱导的13-氧代-顺-6,顺-9,顺-15-十八碳三烯酸、由10-羟基-顺-12-十八碳烯酸或10-氧代-顺-12-十八碳烯酸诱导的10,13-二氧代-十八烷酸、由10-羟基-顺-6,顺-12-十八碳二烯酸或10-氧代-顺-6,顺-12-十八碳二烯酸诱导的10,13-二氧代-顺-6-十八碳烯酸、由10-羟基-顺-12,顺-15-十八碳二烯酸或10-氧代-顺-12,顺-15-十八碳二烯酸诱导的10,13-二氧代-顺-15-十八碳烯酸、由10-羟基-顺-6,顺-12,顺-15-十八碳三烯酸或10-氧代-顺-6,顺-12,顺-15-十八碳三烯酸诱导的10,13-二氧代-顺-6,顺-15-十八碳二烯酸、由顺-5,顺-9,顺-12-十八碳三烯酸(皮诺敛酸)诱导的13-氧代-顺-5,顺-9-十八碳二烯酸、由反-5,顺-9,顺-12-十八碳三烯酸 (哥伦比亚酸)诱导的13-氧代-反-5,顺-9-十八碳二烯酸等。
由上述生产方法6所生产的“10-氧代脂肪酸”的实例包括:由顺-9-十六碳烯酸(棕榈油酸)诱导的10-氧代-十六烷酸等。
由上述生产方法7所生产的“15-氧代脂肪酸”的实例包括:由顺-11,顺-14-二十碳二烯酸诱导的15-氧代-顺-11-二十碳烯酸、由顺-11,顺-14,顺-17-二十碳三烯酸诱导的15-氧代-顺-11,顺-17-二十碳二烯酸、由顺-8,顺-11,顺-14-二十碳三烯酸(二高-γ-亚麻酸)诱导的15-氧代-顺-8,顺-11-二十碳二烯酸、由顺-5,顺-8,顺-11,顺-14-二十碳四烯酸(花生四烯酸)诱导的15-氧代-顺-5,顺-8,顺-11-二十碳三烯酸、由顺-8,顺-11,顺-14,顺-17-二十碳四烯酸诱导的15-氧代-顺-8,顺-11,顺-17-二十碳三烯酸、由顺-5,顺-11,顺-14-二十碳三烯酸(5(Z),11(Z),14(Z)-二十碳三烯酸)诱导的15-氧代-顺-5,顺-11-二十碳二烯酸、由顺-5,顺-11,顺-14,顺-17-二十碳四烯酸((5Z,11Z,14Z,17Z)-5,11,14,17-二十碳四烯酸)诱导的15-氧代-顺-5,顺-11,顺-17-二十碳三烯酸等。
由上述生产方法8所生产的“12-氧代脂肪酸”的实例包括:由顺-11,顺-14-二十碳二烯酸诱导的12-氧代-顺-14-二十碳烯酸、由顺-11,顺-14,顺-17-二十碳三烯酸诱导的12-氧代-顺-14,顺-17-二十碳二烯酸、由顺-8,顺-11,顺-14-二十碳三烯酸(二高-γ-亚麻酸)诱导的12-氧代-顺-8,顺-14-二十碳二烯酸、由顺-5,顺-8,顺-11-二十碳三烯酸((5Z,8Z,11Z)-二十碳-5,8,11-三烯酸)诱导的12-氧代-顺-5,顺-8-二十碳二烯酸、由顺-8,顺-11,顺-14,顺-17-二十碳四烯酸诱导的12-氧代-顺-8,顺-14,顺-17-二十碳三烯酸、由顺-5,顺-8,顺-11,顺-14-二十碳四烯酸(花生四烯酸)诱导的12-氧代-顺-5,顺-8,顺-14-二十碳三烯酸等。
上述生产方法5-8、生产方法B或生产方法II中所用的脱氢酶不受特别限制,只要其是这样的酶:能够将用作底物的13-羟基脂肪酸、10-羟基脂肪酸、15-羟基脂肪酸、12-羟基脂肪酸、14-羟基-顺-4,顺-7,顺-10,顺-16,顺-19-二十二碳五烯酸、10-羟基-十四烷酸分别转化成13-氧代脂肪酸、10-氧代脂肪酸、15-氧代脂肪酸、12-氧代脂肪酸、14-氧代-顺-4,顺-7,顺-10,顺-16,顺-19-二十二碳五烯酸、10-氧代-十四烷酸,并且,例如,优选来源于乳杆菌的羟基化脂肪酸– 脱氢酶(CLA-DH)。更优选的是来源于植物乳杆菌的CLA-DH,并且特别优选的是来源于植物乳杆菌FERM BP-10549菌株的CLA-DH。CLA-DH可以由JP-A-2007-259712中所述的方法、WO 2013/168310中所述的方法获得。脱氢酶可以是经过纯化或粗纯化的。作为另外一种选择,可以在菌体(如大肠杆菌等)中表达脱氢酶,并且可使用所述菌体自身或可使用其培养基。此外,所述酶可以是游离形式或由各种载体固定化的。
脱氢反应可以在合适的缓冲液(例如,磷酸盐缓冲液、Tris缓冲液、硼酸盐缓冲液等)中通过以下进行:将作为底物的13-羟基脂肪酸、10-羟基脂肪酸、15-羟基脂肪酸、12-羟基脂肪酸、14-羟基-顺-4,顺-7,顺-10,顺-16,顺-19-二十二碳五烯酸、10-羟基-十四烷酸与脱氢酶于合适的浓度混合并温育所述混合物。底物浓度为,例如,0.01 - 100 g/L,优选0.05 - 50 g/L,更优选0.1 - 5 g/L。将要加入的脱氢酶的量为,例如,0.001 - 10 mg/mL,优选0.005 - 1 mg/mL,更优选0.05 - 0.2 mg/mL。
“辅因子”可用于脱氢反应并且,例如,可使用NAD+、NADP+等。其添加的浓度可以是任意的,只要所述水合反应有效地进行。优选0.001 – 20 mM,更优选0.01 – 10 mM。
期望的是,脱氢反应在脱氢酶的优选温度和优选pH范围内进行。例如,反应温度为5 - 50℃,优选20 - 45℃。反应混合物的pH为,例如,pH 4 - 10,优选pH 5 - 9。反应时间不受特别限制,并且其为,例如,10 分钟 - 72 小时,优选30 分钟 - 36 小时。
在本发明的一个实施方案中,使脱氢酶以重组细胞(例如,大肠杆菌、枯草芽孢杆菌、酵母、昆虫细胞、动物细胞等)的形式经受反应体系,所述重组细胞中引入了含有编码所述脱氢酶的核酸的表达载体。在这种情况下,氧化反应也可以通过如下进行:在适合于所述细胞的培养、并加入了底物以及在必要时辅因子和激活剂的液体培养基中培养所述细胞。
另外,通过用使用铬酸的化学氧化来替代脱氢反应,可以以化学方式获得类似于通过酶反应所得到的氧代脂肪酸。
作为化学氧化,可以提及本身已知的方法,例如,铬酸氧化,优选琼斯氧化(Jones oxidation)等。作为铬酸,可以使用所述化合物的盐或络合物如无水铬酸 CrO3、铬酸 H2CrO4 和重铬酸 H2Cr2O7。具体来说,将硫酸(2.3 ml)和水(7.7 ml)加入无水铬酸(2.67 g)中,并将丙酮(90 ml)加入所述混合物中以得到铬酸溶液。将2 g 羟基化脂肪酸和40 ml 丙酮加入锥形瓶中,并在置于冰上的搅拌器中搅拌下将上述铬酸溶液逐滴滴入。当溶液由蓝色变为茶绿色时,停止逐滴加入所述铬酸溶液,并用异丙醇终止反应。将沉淀的沉积物通过滤纸过滤,置于分液漏斗中,加入二乙醚(150 ml)和Milli-Q水(300 ml),将混合物充分振荡,并用Milli-Q水洗涤二乙醚层几次。向洗涤后的二乙醚层中加入适量的(无水)硫酸钠,搅拌混合物并移除残余水。通过滤纸将所加入的无水硫酸钠滤掉,使用旋转蒸发器浓缩所得的二乙醚层,并提取反应产物(氧代脂肪酸)和未反应的底物。
使通过使用无水铬酸的氧化反应所获得的提取物(含有底物和所得产物(氧代脂肪酸)的混合物)经受中等压力层析,将从柱中流出的溶液回收于级分中。通过LC/MS和气相层析分析所回收的各个级分,收集仅含有氧代脂肪酸的级分并通过旋转蒸发器浓缩。将获得的最终所得产物的一部分甲酯化,通过气相层析评价氧代脂肪酸的纯度,而可以获得具有不低于98%的纯度的氧代脂肪酸。
本发明的含有稀有脂肪酸的代谢改善剂也可应用于改善与生活方式相关的疾病。“与生活方式相关的疾病”是生活习惯(如饮食习惯、锻炼习惯、休息、抽烟、饮酒等)与其发病和进展有关的一组疾病,并且包括病理如成人肥胖、儿童肥胖、营养失调、食欲缺乏、胃癌、大肠癌、痛风、高血压、动脉硬化、肾结石、心肌梗死、心绞痛、胃溃疡、肾病、骨质疏松症、牙周炎、酒精性肝炎、肝硬变、肝癌、肺癌、支气管炎、肺气肿、牙周病、大脑卒中、大脑梗死、动脉瘤、过劳死、失眠症等。
此外,本发明的代谢改善剂也可以用于预防或改善糖尿病(1型糖尿病、2型糖尿病、妊娠糖尿病等)、糖尿病并发症(动脉硬化疾病、糖尿病性视网膜病、糖尿病肾病、糖尿病性神经病变等)、脂质代谢异常、高脂血症、高胆固醇血症、高甘油三酯血症、胰岛素抵抗和脂肪肝。
作为另外一种选择,通过向人或人以外的动物(例如,狗、猫、小鼠、大鼠、仓鼠、豚鼠、兔、猪、牛、鸡、长尾小鹦鹉、鹩哥、山羊、马、绵羊、猴子等)施用,本发明的代谢改善剂可以用于预防或治疗选自肥胖症、糖尿病、脂质代谢异常、高脂血症、高胆固醇血症、高甘油三酯血症、胰岛素抵抗和脂肪肝的至少一种。
本发明的稀有脂肪酸也可以用作PPAR活性促进剂。PPAR包括至少3种亚型:PPARα、PPARδ(同β)和PPARγ。如下述实施例中所示,本发明的稀有脂肪酸对PPARα、PPARγ具有激动剂活性。因此,当确认了来自这些PPAR中的至少一种PPAR(优选PPARα或PPARγ)存在或不存在配体(激动剂、拮抗剂)活性并且显示了激动剂活性时,其可以用作PPAR活性的促进剂以改善代谢。
本发明的含有稀有脂肪酸的代谢改善剂(或PPAR活性促进剂)可以用作,例如,药物产品、食物、饲料、化妆品等,或通过向其加入所述药剂。
药物产品的剂型包括,分散剂、颗粒、丸剂、软胶囊、硬胶囊、片剂、可咀嚼片剂、快速崩解片剂、糖浆、液体、悬浮液、栓剂、软膏、乳膏、凝胶、粘合剂、吸入剂、注射剂等。其制剂是根据常规方法配制的。由于羟基化脂肪酸等难溶于水,所以将其溶解于非亲水性有机溶剂(如植物来源的油、动物来源的油等)中或将其与乳化剂、分散剂、表面活性剂等一起通过匀浆器(高压匀浆器)分散或乳化于水溶液中且使用。
可用于配制的添加剂的实例包括:动物和植物油,如大豆油、红花油、橄榄油、胚芽油、葵花油、牛脂肪、沙丁鱼油等;多元醇,如聚乙二醇、丙二醇、甘油、山梨糖醇等;表面活性剂,如脂肪酸的脱水山梨糖醇酯、脂肪酸的蔗糖酯、甘油脂肪酸酯、脂肪酸的聚甘油酯等;赋形剂,如纯净水、乳糖、淀粉、结晶纤维素、D-甘露糖醇、卵磷脂、阿拉伯树胶、山梨糖醇溶液、碳水化合物溶液等;增甜剂、着色剂、pH调节剂、食用香料等。在使用时,可将液体制剂溶解或悬浮于水或其它合适介质中。片剂和颗粒也可通过众所周知的方法包被。
对于以注射剂的形式施用,优选静脉内、腹膜内、肌内、皮下、经皮、关节内、滑膜内、鞘内、骨膜内、舌下、口服等,并且尤其优选静脉内施用或腹膜内施用。静脉内施用可以是滴注施用和快速灌注(bolus)施用中的任一种。
当本发明的营养改善剂用作食物或食物添加剂时,所述食物的形式不受特别限制,只要其允许经口摄入,如溶液、悬浮剂、粉末、固体形成的制品等。特定的实例包括:补充剂(粉末、颗粒、软胶囊、硬胶囊、片剂、可咀嚼片剂、快速崩解片剂、糖浆、液体等);饮料(碳酸饮料、乳酸饮料、运动饮料、果汁饮料、蔬菜饮料、豆奶饮料、咖啡饮料、茶饮料、粉末饮料、浓缩饮料、营养饮料、酒精饮料等);糖食(橡皮糖、果冻、口香糖、巧克力、饼干、糖果、焦糖、日本糖食、小吃等);即食食物(方便面、甑煮食物(retort food)、罐头、微波炉食物、即食汤、味噌汤、冻干食物等);油、脂肪和油脂食物(蛋黄酱、调味品、黄油、乳油、人造奶油等);小麦粉产品(面包、意大利面、面条、蛋糕粉、面包屑等);调味品(酱汁、番茄加工调味品、风味调味品、烹饪混合物、汤等);经过加工的肉类产品(肉火腿、香肠等)。
上述食物在必要时可以含有:各种营养物、各种维生素(维生素A、维生素B1、维生素B2、维生素B6、维生素C、维生素D、维生素E、维生素K等)、各种矿物质(镁、锌、铁、钠、钾、硒等)、膳食纤维、分散剂、稳定剂如乳化剂等、增甜剂、调味组分(柠檬酸、苹果酸等)、食用香料、蜂王胶、蜂胶、蘑菇属(Agaricus)等。
当本发明的营养改善剂用作饲料或饲料添加剂时,所述饲料为,例如,宠物食物、畜牧业或水产养殖业饲料添加剂等。
当本发明的营养改善剂用作化妆品或化妆品添加剂时,所述化妆品为,例如,乳膏、凝胶、乳液(skin milk)、精华液(serum)、化妆水(toner)、微乳精华、面膜、粉底、口红、眼影、洗发水、护发素、沐浴添加剂等,并且可以在其中混合香料等。
羟基化脂肪酸和氧代脂肪酸等中仅一种可以与本发明的药物产品、食物、饲料、化妆品等掺合,或者可以组合使用其中的两种或更多种。
本发明的药物产品的剂量或本发明的食物的摄入量可以根据患者或摄取所述药物产品或食物的那些人的年龄和体重、症状、施用时间、剂型、施用方法、药物组合等来恰当地确定。例如,当本发明的药物产品为口服时,作为活性成分的所述羟基化脂肪酸等的总量为成人每天0.02 – 100 mg/kg 体重,优选0.2 – 50 mg/kg 体重;或通过肠胃外施用0.002 mg – 50 mg/kg 体重,优选0.02 – 50 mg/kg 体重,其可以每日一次或几(2 – 5)份/天施用。当其作为食物摄入时,可以将其添加到食物中从而使得作为活性成分的所述羟基化脂肪酸等的总摄入量为成人每天1 – 6000 mg,优选10 – 3000 mg。本发明的饲料的摄入量和本发明的化妆品的使用量可以各自根据上述食物的摄入量和上述药物产品的剂量来恰当地确定。
以下参考实施例对本发明进行了更详细的说明。实施例仅仅是本发明的示范而不以任何方式限制本发明的范围。
实施例
根据上述方法制备了用于本发明的羟基化脂肪酸和氧代脂肪酸等,如:(1) 13-羟基-顺-9-十八碳烯酸(表示为“13-OH LA”);(2) 13-氧代-顺-9-十八碳烯酸(表示为“13-OXO LA”);(3) 10,13-二羟基-十八烷酸(表示为“10,13-OH LA”);(4) 13-羟基-顺-9,顺-15-十八碳二烯酸(表示为“13-OH ALA”);(5) 13-氧代-顺-9,顺-15-十八碳二烯酸(表示为“13-OXO ALA”);(6) 10,13-二羟基-顺-15-十八碳烯酸(表示为“10,13-OH ALA”);(7) 13-羟基-顺-6,顺-9-十八碳二烯酸(表示为“13-OH GLA”);(8) 13-氧代-顺-6,顺-9-十八碳二烯酸(表示为“13-OXO GLA”);(9) 10,13-二羟基-顺-6-十八碳烯酸(表示为“10,13-OH GLA”);(10) 15-羟基-顺-5,顺-8,顺-11-二十碳三烯酸(表示为“15-OH AA”)等。结构式(1)-(10)及由其衍生的脂肪酸示于图1中。GW7647(PPARα激动剂)和曲格列酮(PPARγ激动剂)购自Sigma-Aldrich,而其它试剂购自Wako Pure Chemical Industries, Ltd.或Nacalai Tesque等。
(实施例1)测量PPARα、γ配体活性
为了评价羟基化脂肪酸和氧代脂肪酸等的功能,首先测量了PPARα、γ活化作用。所述测量参考Nobuyuki Takahashi 等人, FEBS Letters 514 (2002) 第315-322页, “Dual action of isoprenols from herbal medicines on both PPARgamma and PPARalpha in 3T3-L1 adipocytes and HepG2 hepatocytes.”, 材料与方法部分 “Reporter plasmids and luciferase assays”进行。具体地讲,PPARα、γ配体活性是通过基于萤光素酶的表达,评价对PPAR配体结合区与GAL4 DNA结合区的融合蛋白的结合以及靶基因活化的报道分子测定来测量的。具体地,将包含编码PPARα、γ配体结合区与GAL4 DNA结合区的融合蛋白的DNA的质粒和其中萤光素酶连接至结合了GAL4的DNA序列的报道分子质粒引入CV-1细胞中,将下述配体加入所述细胞中,温育细胞并检测萤光素酶活性。
用乙醇调整样品的浓度(10 μM和30 μM)。将乙醇用作阴性对照,而将PPARα、γ配体GW7647(10 nM)和曲格列酮(5 μM)用作阳性对照。结果示于图2、图3中。
从图2、3中看出,在全部脂肪酸(1)-(10)中均发现了PPARα和γ激动剂活性。另外,(8) 13-OXO GLA表现出强烈的PPARα激动剂活性,而(5) 13-OXO ALA表现出强烈的PPARγ激动剂活性。
虽然已经着重从优选的实施方案描述了本发明,但对于本领域技术人员显而易见的是,所述优选的实施方案是可以修改的。
本文所引用的任何出版物(包括专利和专利申请)中所公开的内容,均在此整体引入作为参考,其程度如同其已在本文中公开。
[工业适用性]
本发明已经阐明,羟基化脂肪酸等具有在传统上未知的脂质和/或糖和/或能量代谢改善效果作为其生理学功能。含有所述羟基化脂肪酸和/或氧代脂肪酸等的脂质和/或糖和/或能量代谢改善剂适用于如药物产品、食物、饲料等各个领域,并且本发明在工业上极为有用。
本申请基于在日本提交的专利申请号2014-011871(申请日:2014年1月24日),其内容全文并入本文。
序列表
<110> Kyoto University
Nitto Pharmaceutical Industries, Ltd.
<120> 包含稀有脂肪酸的代谢改善剂
<130> 092263
<150> JP 2014-011871
<151> 2014-01-24
<160> 2
<170> PatentIn version 3.5
<210> 1
<211> 1773
<212> DNA
<213> 嗜酸乳杆菌(Lactobacillus acidophilus)
<220>
<221> CDS
<222> (1)..(1773)
<400> 1
atg cat tat agt agt ggt aat tat gaa gct ttt gta aac gca agt aaa 48
Met His Tyr Ser Ser Gly Asn Tyr Glu Ala Phe Val Asn Ala Ser Lys
1 5 10 15
cct aag gat gtc gat cag aag tcc gca tat ctt gtt ggt tca ggt ttg 96
Pro Lys Asp Val Asp Gln Lys Ser Ala Tyr Leu Val Gly Ser Gly Leu
20 25 30
gca tcg ctt gct agt gct gta ttt tta att cgt gat ggt cac atg aag 144
Ala Ser Leu Ala Ser Ala Val Phe Leu Ile Arg Asp Gly His Met Lys
35 40 45
ggt gat aga att cat atc ctt gaa gaa ttg agc ctt cca ggt ggt tca 192
Gly Asp Arg Ile His Ile Leu Glu Glu Leu Ser Leu Pro Gly Gly Ser
50 55 60
atg gat ggg atc tat aat aag caa aaa gaa agc tac atc att cgt ggt 240
Met Asp Gly Ile Tyr Asn Lys Gln Lys Glu Ser Tyr Ile Ile Arg Gly
65 70 75 80
ggt cgt gaa atg gaa gcc cat ttt gaa tgc ttg tgg gac ttg ttt aga 288
Gly Arg Glu Met Glu Ala His Phe Glu Cys Leu Trp Asp Leu Phe Arg
85 90 95
tcg att cca tca gct gaa aat aaa gat gaa tcg gtc ctg gat gaa ttt 336
Ser Ile Pro Ser Ala Glu Asn Lys Asp Glu Ser Val Leu Asp Glu Phe
100 105 110
tac cgt tta aat aga aaa gat cca agt ttc gca aag act cgt gtc att 384
Tyr Arg Leu Asn Arg Lys Asp Pro Ser Phe Ala Lys Thr Arg Val Ile
115 120 125
gtt aac cgc gga cat gaa ctt cca act gac ggt caa tta ctt ctt act 432
Val Asn Arg Gly His Glu Leu Pro Thr Asp Gly Gln Leu Leu Leu Thr
130 135 140
ccc aag gct gtt aaa gaa att att gat ctt tgc tta act cct gaa aaa 480
Pro Lys Ala Val Lys Glu Ile Ile Asp Leu Cys Leu Thr Pro Glu Lys
145 150 155 160
gat tta caa aat aaa aaa att aat gaa gtc ttt agt aaa gaa ttt ttt 528
Asp Leu Gln Asn Lys Lys Ile Asn Glu Val Phe Ser Lys Glu Phe Phe
165 170 175
gaa tca aac ttc tgg ctt tac tgg tca acg atg ttt gcc ttt gag cca 576
Glu Ser Asn Phe Trp Leu Tyr Trp Ser Thr Met Phe Ala Phe Glu Pro
180 185 190
tgg gca agt gcg atg gaa atg cgt cgt tac tta atg cgt ttt gtt caa 624
Trp Ala Ser Ala Met Glu Met Arg Arg Tyr Leu Met Arg Phe Val Gln
195 200 205
cac gtt tct aca ctt aag aat tta tca tca cta cgc ttt act aag tat 672
His Val Ser Thr Leu Lys Asn Leu Ser Ser Leu Arg Phe Thr Lys Tyr
210 215 220
aac caa tat gaa tca tta att tta cca atg gtt aaa tac ttg aaa gat 720
Asn Gln Tyr Glu Ser Leu Ile Leu Pro Met Val Lys Tyr Leu Lys Asp
225 230 235 240
cgc ggc gtg caa ttc cat tac aac acc gtt gtt gat aat atc ttt gtt 768
Arg Gly Val Gln Phe His Tyr Asn Thr Val Val Asp Asn Ile Phe Val
245 250 255
aac cgt tca aat ggt gaa aag att gct aag caa att ctt tta act gaa 816
Asn Arg Ser Asn Gly Glu Lys Ile Ala Lys Gln Ile Leu Leu Thr Glu
260 265 270
aac ggt gaa aaa aag agc atc gat tta aca gaa aat gac ctc gtc ttc 864
Asn Gly Glu Lys Lys Ser Ile Asp Leu Thr Glu Asn Asp Leu Val Phe
275 280 285
gtt act aac ggt tca att act gaa agt aca act tat ggt gat aac ttg 912
Val Thr Asn Gly Ser Ile Thr Glu Ser Thr Thr Tyr Gly Asp Asn Leu
290 295 300
cac cca gct tct gag gaa cat aaa tta ggt gct act tgg aaa tta tgg 960
His Pro Ala Ser Glu Glu His Lys Leu Gly Ala Thr Trp Lys Leu Trp
305 310 315 320
caa aac ttg gca gcg caa gat gat gac ttc ggt cac cca gat gtc ttc 1008
Gln Asn Leu Ala Ala Gln Asp Asp Asp Phe Gly His Pro Asp Val Phe
325 330 335
tgc aag gat att cca aag gct aac tgg gta atg tct gct aca att act 1056
Cys Lys Asp Ile Pro Lys Ala Asn Trp Val Met Ser Ala Thr Ile Thr
340 345 350
ttt aag aat aat gat att gtg cca ttc att gaa gca gtt aat aag aag 1104
Phe Lys Asn Asn Asp Ile Val Pro Phe Ile Glu Ala Val Asn Lys Lys
355 360 365
gat cca cac agc ggc tca att gta act agt ggg cct act acg att aag 1152
Asp Pro His Ser Gly Ser Ile Val Thr Ser Gly Pro Thr Thr Ile Lys
370 375 380
gat tct aac tgg cta ctt ggt tat tca atc agt cgt cag cct cac ttt 1200
Asp Ser Asn Trp Leu Leu Gly Tyr Ser Ile Ser Arg Gln Pro His Phe
385 390 395 400
gaa gca caa aag cct aac gaa ttg att gta tgg ctt tat ggt ttg ttc 1248
Glu Ala Gln Lys Pro Asn Glu Leu Ile Val Trp Leu Tyr Gly Leu Phe
405 410 415
tca gac acc aaa ggt aac tat gtt gaa aag act atg cct gac tgt aac 1296
Ser Asp Thr Lys Gly Asn Tyr Val Glu Lys Thr Met Pro Asp Cys Asn
420 425 430
ggt att gaa tta tgt gaa gaa tgg ctt tac cac atg ggt gtt cct gaa 1344
Gly Ile Glu Leu Cys Glu Glu Trp Leu Tyr His Met Gly Val Pro Glu
435 440 445
gaa aga atc cca gaa atg gct tca gct gct acg act att cca gca cac 1392
Glu Arg Ile Pro Glu Met Ala Ser Ala Ala Thr Thr Ile Pro Ala His
450 455 460
atg cca tat att act tca tac ttc atg cca aga gca tta ggc gac aga 1440
Met Pro Tyr Ile Thr Ser Tyr Phe Met Pro Arg Ala Leu Gly Asp Arg
465 470 475 480
ccc aag gtt gtg cca gac cac tca aag aac ttg gcc ttc att ggt aac 1488
Pro Lys Val Val Pro Asp His Ser Lys Asn Leu Ala Phe Ile Gly Asn
485 490 495
ttt gct gaa acg cca aga gac act gtc ttt acc act gaa tac tct gtc 1536
Phe Ala Glu Thr Pro Arg Asp Thr Val Phe Thr Thr Glu Tyr Ser Val
500 505 510
aga act gcg atg gaa gct gta tac acc ttg ctt aac att gat cgt ggt 1584
Arg Thr Ala Met Glu Ala Val Tyr Thr Leu Leu Asn Ile Asp Arg Gly
515 520 525
gtg cca gaa gta ttt gca tct gcc ttc gat gtc aga atg ctc atg aac 1632
Val Pro Glu Val Phe Ala Ser Ala Phe Asp Val Arg Met Leu Met Asn
530 535 540
gca atg tac tac ttg aat gat caa aag aag ctt gaa gat ctt gat ttg 1680
Ala Met Tyr Tyr Leu Asn Asp Gln Lys Lys Leu Glu Asp Leu Asp Leu
545 550 555 560
cct att gct gaa aag ttg gca att aag ggg atg ctc aag aaa gtt aag 1728
Pro Ile Ala Glu Lys Leu Ala Ile Lys Gly Met Leu Lys Lys Val Lys
565 570 575
ggc act tat ata gag gaa ttg ctt aag aag tat aag ttg gtt tag 1773
Gly Thr Tyr Ile Glu Glu Leu Leu Lys Lys Tyr Lys Leu Val
580 585 590
<210> 2
<211> 590
<212> PRT
<213> 嗜酸乳杆菌(Lactobacillus acidophilus)
<400> 2
Met His Tyr Ser Ser Gly Asn Tyr Glu Ala Phe Val Asn Ala Ser Lys
1 5 10 15
Pro Lys Asp Val Asp Gln Lys Ser Ala Tyr Leu Val Gly Ser Gly Leu
20 25 30
Ala Ser Leu Ala Ser Ala Val Phe Leu Ile Arg Asp Gly His Met Lys
35 40 45
Gly Asp Arg Ile His Ile Leu Glu Glu Leu Ser Leu Pro Gly Gly Ser
50 55 60
Met Asp Gly Ile Tyr Asn Lys Gln Lys Glu Ser Tyr Ile Ile Arg Gly
65 70 75 80
Gly Arg Glu Met Glu Ala His Phe Glu Cys Leu Trp Asp Leu Phe Arg
85 90 95
Ser Ile Pro Ser Ala Glu Asn Lys Asp Glu Ser Val Leu Asp Glu Phe
100 105 110
Tyr Arg Leu Asn Arg Lys Asp Pro Ser Phe Ala Lys Thr Arg Val Ile
115 120 125
Val Asn Arg Gly His Glu Leu Pro Thr Asp Gly Gln Leu Leu Leu Thr
130 135 140
Pro Lys Ala Val Lys Glu Ile Ile Asp Leu Cys Leu Thr Pro Glu Lys
145 150 155 160
Asp Leu Gln Asn Lys Lys Ile Asn Glu Val Phe Ser Lys Glu Phe Phe
165 170 175
Glu Ser Asn Phe Trp Leu Tyr Trp Ser Thr Met Phe Ala Phe Glu Pro
180 185 190
Trp Ala Ser Ala Met Glu Met Arg Arg Tyr Leu Met Arg Phe Val Gln
195 200 205
His Val Ser Thr Leu Lys Asn Leu Ser Ser Leu Arg Phe Thr Lys Tyr
210 215 220
Asn Gln Tyr Glu Ser Leu Ile Leu Pro Met Val Lys Tyr Leu Lys Asp
225 230 235 240
Arg Gly Val Gln Phe His Tyr Asn Thr Val Val Asp Asn Ile Phe Val
245 250 255
Asn Arg Ser Asn Gly Glu Lys Ile Ala Lys Gln Ile Leu Leu Thr Glu
260 265 270
Asn Gly Glu Lys Lys Ser Ile Asp Leu Thr Glu Asn Asp Leu Val Phe
275 280 285
Val Thr Asn Gly Ser Ile Thr Glu Ser Thr Thr Tyr Gly Asp Asn Leu
290 295 300
His Pro Ala Ser Glu Glu His Lys Leu Gly Ala Thr Trp Lys Leu Trp
305 310 315 320
Gln Asn Leu Ala Ala Gln Asp Asp Asp Phe Gly His Pro Asp Val Phe
325 330 335
Cys Lys Asp Ile Pro Lys Ala Asn Trp Val Met Ser Ala Thr Ile Thr
340 345 350
Phe Lys Asn Asn Asp Ile Val Pro Phe Ile Glu Ala Val Asn Lys Lys
355 360 365
Asp Pro His Ser Gly Ser Ile Val Thr Ser Gly Pro Thr Thr Ile Lys
370 375 380
Asp Ser Asn Trp Leu Leu Gly Tyr Ser Ile Ser Arg Gln Pro His Phe
385 390 395 400
Glu Ala Gln Lys Pro Asn Glu Leu Ile Val Trp Leu Tyr Gly Leu Phe
405 410 415
Ser Asp Thr Lys Gly Asn Tyr Val Glu Lys Thr Met Pro Asp Cys Asn
420 425 430
Gly Ile Glu Leu Cys Glu Glu Trp Leu Tyr His Met Gly Val Pro Glu
435 440 445
Glu Arg Ile Pro Glu Met Ala Ser Ala Ala Thr Thr Ile Pro Ala His
450 455 460
Met Pro Tyr Ile Thr Ser Tyr Phe Met Pro Arg Ala Leu Gly Asp Arg
465 470 475 480
Pro Lys Val Val Pro Asp His Ser Lys Asn Leu Ala Phe Ile Gly Asn
485 490 495
Phe Ala Glu Thr Pro Arg Asp Thr Val Phe Thr Thr Glu Tyr Ser Val
500 505 510
Arg Thr Ala Met Glu Ala Val Tyr Thr Leu Leu Asn Ile Asp Arg Gly
515 520 525
Val Pro Glu Val Phe Ala Ser Ala Phe Asp Val Arg Met Leu Met Asn
530 535 540
Ala Met Tyr Tyr Leu Asn Asp Gln Lys Lys Leu Glu Asp Leu Asp Leu
545 550 555 560
Pro Ile Ala Glu Lys Leu Ala Ile Lys Gly Met Leu Lys Lys Val Lys
565 570 575
Gly Thr Tyr Ile Glu Glu Leu Leu Lys Lys Tyr Lys Leu Val
580 585 590
- 还没有人留言评论。精彩留言会获得点赞!
- 一种基于动态pet影像的心肌脂肪酸代谢量化检测方法
- 作为抗脂解药用于治疗血脂异常等代谢相关疾病的5-取代的2h-吡唑-3-甲酸衍生物的制作方法
- 用作抗异常脂肪血症及相关疾病的fxr调节剂的2,3-取代的吲唑或4,5,6,7-四氢-吲唑类的制作方法
- 一种脂肪酸代谢显像剂β-甲基-15-对氟[的制作方法
- 作为RXR激动剂用于治疗异常脂肪血症、高胆固醇血症和糖尿病的1
- 微拟球藻NgAUREO1基因在调控脂肪酸代谢中的应用的制作方法
- 人参皂苷代谢物m1单脂肪酸酯类化合物的制备方法
- 一种用于治疗水液代谢异常的中药组合物及其制备方法
- 软骨代谢异常疾病改善用健康食品及药品组合物的制作方法
- 作为rxr激动剂用于治疗异常脂肪血症、高胆固醇血症和糖尿病的二氢-[1h]-喹啉-2-酮 ...的制作方法