用于治疗严重痤疮的阿达帕林和过氧化苯甲酰的组合的制作方法
背景
技术领域:
本申请涉及在单一制剂中联合给予0.3%重量的阿达帕林和2.5%重量的过氧化苯甲酰,用于治疗严重痤疮。
背景和/或相关技术和/或现有技术的描述:
6-[3-(1-金刚烷基)-4-甲氧基苯基]-2-萘甲酸(下文称为阿达帕林)是具有类视黄醇和抗炎特性的萘甲酸衍生物。这个分子是用于寻常痤疮和对类视黄醇敏感的皮肤病的局部治疗的开发的主题。
阿达帕林在商标名differin®下,以0.1%的重量浓度,以"含醇洗剂"溶液、水性凝胶和霜剂的形式上市。这些组合物可用于治疗痤疮。wo03/075908a1描述用于治疗痤疮的0.3%重量浓度的阿达帕林组合物。
此外,wo03/055472描述了包含阿达帕林和过氧化苯甲酰(bpo)以及ph非依赖性胶凝剂的稳定的药用组合物。协同治疗痤疮损伤的这样的组合物的使用描述于wo2008/006888a1中。0.1%重量阿达帕林和2.5%重量过氧化苯甲酰的水性凝胶以商标名epiduo®上市。
发明概述
在第一方面,本文提供一种在罹患严重痤疮的受试者中治疗性治疗痤疮损伤的方案,所述方案包括将合并在单一制剂中的、作为活性成分的0.3%重量的阿达帕林或其药学上可接受的盐和2.5%重量的过氧化苯甲酰,局部施用于所述受试者的皮肤,所述单一制剂将所述活性成分一起递送,以在一组这样的受试者中获得至少约30%的成功率,其中百分比重量是相对于单一制剂的重量。所述单一制剂优选每日施用一次或两次,持续8-12周的时期。
在第二方面,本文提供一种在罹患严重痤疮的受试者中治疗性治疗痤疮损伤的方案,所述方案包括将合并在单一制剂中的、作为活性成分的0.3%重量的阿达帕林或其药学上可接受的盐和2.5%重量的过氧化苯甲酰,局部施用于所述受试者的皮肤,所述单一制剂将所述活性成分一起递送以减少炎性损伤的数量,其中百分比重量是相对于单一制剂的重量。所述单一制剂优选每日施用一次或两次,持续4-12周的时期。
在第三方面,本文提供作为活性成分的0.3%重量的阿达帕林或其药学上可接受的盐和2.5%重量的过氧化苯甲酰在制备药物中的联合使用,所述药物是通过局部应用将所述活性成分一起递送以治疗性治疗严重痤疮的单一制剂,其中百分比重量是相对于单一制剂的重量。
换言之,本发明涉及作为活性成分的0.3%重量的阿达帕林或其药学上可接受的盐和2.5%重量的过氧化苯甲酰在制备药物中的用途,所述药物是局部应用的单一制剂,其含有用于治疗性治疗严重痤疮的两种活性成分,其中百分比重量是相对于所述单一制剂的重量。
在第四方面,本文提供包含作为活性成分的0.3%重量阿达帕林和2.5%重量过氧化苯甲酰的单一制剂,所述单一制剂将所述活性成分一起局部递送,其中百分比重量是相对于单一制剂的重量,和单一制剂用于治疗严重痤疮,特别是用于治疗严重痤疮的炎性损伤。
换言之,本发明涉及一种包含作为活性成分的0.3%重量的阿达帕林或其药学上可接受的盐和2.5%重量的过氧化苯甲酰的药用组合物,其中百分比重量是相对于组合物的总重量,其通过局部给药用于治疗炎性痤疮损伤。所述组合物优选用于治疗罹患严重痤疮的受试者。
现在已令人吃惊地证明,0.3%重量阿达帕林和2.5%重量过氧化苯甲酰(bpo)的治疗组合可在罹患严重痤疮的患者中产生一定程度的成功和减少炎性损伤方面的改进,该治疗组合优于基于阿达帕林0.1%和bpo2.5%的组合的治疗,而同时保持相同的皮肤耐受性。
因此示例性实施方案的特征是以规定剂量0.3%重量制备药用组合物的阿达帕林或其药学上可接受的盐的制剂,其与规定剂量2.5%重量的过氧化苯甲酰(bpo)在单一制剂中一起给药,用于治疗严重痤疮,特别是减少炎性痤疮损伤的数量,并在这样的治疗中达到高的成功率。
痤疮最初以角质化障碍为特征,其有时是肉眼看不见的。然后发展为可见的痤疮损伤,同时皮脂腺的大小和皮脂的产生增加。
示例性实施方案还涉及在罹患严重痤疮的受试者中的痤疮损伤。术语"痤疮损伤"意指由痤疮引起的非-炎性损伤(开放和封闭的黑头粉刺)和炎性损伤(丘疹、脓疱、结节和囊肿)。根据本发明,严重痤疮患者的炎性损伤用如本文描述的0.3%阿达帕林/2.5%过氧化苯甲酰单一制剂治疗。
更优选地,药用组合物通过每日或每日两次皮肤局部应用来给予。
术语"阿达帕林盐"意指与药学上可接受的碱,特别是无机碱例如氢氧化钠、氢氧化钾和氨或有机碱例如赖氨酸、精氨酸或n-甲葡糖胺所成的盐。术语"阿达帕林盐"也意指与脂肪胺例如二辛胺和十八烷胺所成的盐。
当阿达帕林的盐用于本发明的单一制剂(或药用组合物)时,确定其量以获得0.3%重量的阿达帕林的量,即是说,0.3%重量的酸(非成盐)形式的金刚烷基)-4-甲氧基苯基]-2-萘甲酸。
措辞"0.3%重量的阿达帕林或其盐与2.5%重量的过氧化苯甲酰的组合"意指包含指定的百分比的阿达帕林或其盐和过氧化苯甲酰二者的单一组合物/单一制剂,这些百分比是相对于单一制剂/组合物的总重量的百分比重量。
根据本发明,药用组合物是固定的组合并在药学上可接受的介质中包含:(i)至少一种选自阿达帕林及其药学上可接受的盐的化合物(相当于0.3%重量的阿达帕林的量)和(ii)2.5%重量的量的过氧化苯甲酰(bpo)。优选地,药用组合物意欲每日单次或每日两次局部应用。
术语"药学上可接受的介质"意指与人类的皮肤、粘膜和体被相容的介质。
术语"固定的组合"应被理解为意指其活性要素以特定的固定剂量合并在同一媒介中的组合(单一制剂),其将它们一起递送到应用点。优选地,呈固定的组合形式的药用组合物是凝胶;在这种情况下,两个活性要素在制备期间被分散和紧密地混合在同一的媒介中,其在严重痤疮的治疗中,在凝胶的应用期间,将它们一起递送。
治疗具有可变的持续时间,取决于患者和他的痤疮的严重性。治疗期因此可进行数周至数月。合适的治疗期或方案是至少4周,优选地从1至6个月且更优选地,约8周-3个月(12周)的持续时间是优选的,如果必要,在罹患严重痤疮的患者中,治疗的持续时间可能要延长。
附图简述
附属于本公开内容的图1-12举例说明在此后的实施例中描述的临床研究期间获得的结果,其涉及0.3%阿达帕林/2.5%过氧化苯甲酰凝胶、以商标名epiduo®上市的0.1%阿达帕林/2.5%过氧化苯甲酰凝胶,及相应的媒介凝胶的应用。
图1是研究部署的示意图。
图2是随时间的推移,比较0.3%阿达帕林/2.5%过氧化苯甲酰凝胶、0.1%阿达帕林/2.5%过氧化苯甲酰(epiduo®)凝胶和媒介凝胶在意向治疗(intent-to-treat)(itt)群体(患有中度和重度痤疮)的百分比成功率的图。
图3是随时间的推移,在itt群体(患有中度和重度痤疮)中,对于所述3种凝胶的每一个的炎性损伤计数平均变化的图。
图4是随时间的推移,在itt群体(患有中度和重度痤疮),对于所述3种凝胶的每一个的非-炎性损伤计数平均变化的图。
图5是在itt群体(患有中度和重度痤疮)中,对于基线iga=4,对于所述3种凝胶的每一个在第12周的成功率和炎性和非-炎性损伤计数变化的图。
图6是随时间的推移,所述3种凝胶在患有严重痤疮的受试者中的成功率(百分比)的图。
图7是随时间的推移,所述3种凝胶在患有严重痤疮的受试者中炎性损伤计数的平均变化的图。
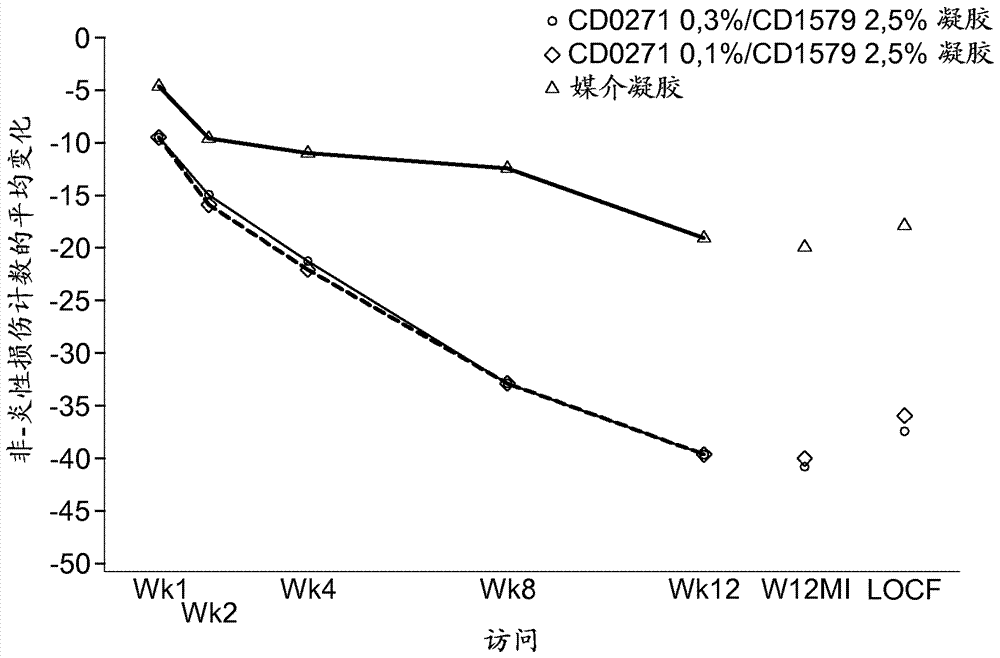
图8是随时间的推移,对于所述3种凝胶的每一个在患有严重痤疮的受试者中非-炎性损伤计数的平均变化的图。
图9是随时间的推移,对于所述3种凝胶的每一个的红斑平均发生率的图。
图10是随时间的推移,对于所述3种凝胶的每一个的起鳞平均发生率的图。
图11是随时间的推移,对于所述3种凝胶的每一个的干燥皮肤的平均发生率的图。
图12是随时间的推移,对于所述3种凝胶的每一个的刺痛和灼烧感的平均发生率的图。
发明详述
在上文概述中公开的本发明的第一和第二方面中,以下实施方案无论是独立的或是组合的,都是值得注意的:
(a)单一制剂每日施用一次;
(b)单一制剂是水性凝胶、凝胶-霜剂、霜剂或洗剂;
(c)单一制剂是水性凝胶;
(d)水性凝胶包含ph非依赖性胶凝剂;
(e)ph非依赖性胶凝剂是丙烯酰胺/丙烯酰二甲基牛磺酸钠共聚物和异十六烷和聚山梨醇酯80(例如以商标名simulgel600销售的产品)或聚丙烯酰胺和异链烷烃和月桂醇聚醚-7(例如以商标名sepigel305销售的产品);
(f)ph非依赖性胶凝剂是丙烯酰胺/丙烯酰二甲基牛磺酸钠共聚物(例如以商标名simulgel600销售的产品);
(g)水性凝胶还包含丙二醇、甘油和泊洛沙姆;
(h)所述单一制剂的安全性特征可比得上在相同条件下对于包含作为活性成分的0.1%重量阿达帕林和2.5%重量过氧化苯甲酰的比较性单一制剂所观察到的安全性特征。
在上文概述中公开的本发明的第三和第四方面中,以下实施方案无论是独立的或是组合的,都是值得注意的:
(a)在一组受试者中使用,给予所述单一制剂,每日一次或两次,持续8-12周的时期,特别是,以获得至少约30%的成功率;
(b)在受试者中使用,给予所述单一制剂,每日一次或两次,持续4-12周的时期,特别是减少炎性损伤的数量;
(c)其中单一制剂是水性凝胶、凝胶-霜剂、霜剂或洗剂的应用;
(d)其中单一制剂是水性凝胶的应用;
(e)其中水性凝胶包含ph非依赖性胶凝剂的应用;
(f)其中ph非依赖性胶凝剂是丙烯酰胺/丙烯酰二甲基牛磺酸钠共聚物和异十六烷和聚山梨醇酯80(例如以商标名simulgel600销售的产品)或聚丙烯酰胺和异链烷烃和月桂醇聚醚-7(例如以商标名sepigel305销售的产品)的应用;
(g)其中ph非依赖性胶凝剂是丙烯酰胺/丙烯酰二甲基牛磺酸钠共聚物(例如以商标名simulgel600销售的产品)的应用;
(h)其中水性凝胶还包含丙二醇、甘油和泊洛沙姆的应用;
(i)其中所述单一制剂的安全性特征可比得上在相同条件下,对于包含作为活性成分的0.1%重量阿达帕林和2.5%重量过氧化苯甲酰的比较性单一制剂所观察到的安全性特征的应用。
示例性药用组合物/单一制剂特别适合于局部治疗皮肤和粘膜,并可呈现为软膏剂、霜剂、乳剂(milks)、润发油、粉末剂、浸垫、溶液剂、凝胶、凝胶-霜剂、喷雾剂、洗剂或混悬剂的形式。它们也可呈现为微球或纳米球的悬浮液或脂质或聚合物囊泡,或聚合物贴剂和水凝胶的形式用于控制释放。用于局部应用的这些组合物可以呈无水的形式、水性形式或乳液的形式。
在优选的实施方案中,药用组合物呈现凝胶(特别是水性凝胶)、霜剂、凝胶-霜剂或洗剂的形式。
术语"水性凝胶"意指含有在含水相中的由胶体悬浮液(胶凝剂)形成的粘弹性物质的组合物。
在特定的实施方案中,水性凝胶含有"ph非依赖性胶凝剂",其意指能够赋予组合物粘性的胶凝剂,其足以使阿达帕林和过氧化苯甲酰保持在悬浮液中,即使在由过氧化苯甲酰释放苯甲酸引起的ph变化的影响下。
可以提及的ph非依赖性胶凝剂的非限制性实例包括聚丙烯酰胺家族的胶凝剂,例如由seppic公司在名称simulgel600下销售的丙烯酰胺/丙烯酰基二甲基牛磺酸钠共聚物和异十六烷和聚山梨醇酯80的混合物,聚丙烯酰胺和异链烷烃c13-12和月桂醇聚醚-7的混合物,例如由seppic公司在名称sepigel305下销售的产品,偶联于疏水链的丙烯酸类聚合物家族,例如在名称aculyn44下销售的peg-150/癸基/smdi共聚物(至少包含含有150或180mol的环氧乙烷的聚乙二醇、癸醇和亚甲基双(4-异氰酸环己酯)(smdi)作为组分的缩聚物,以在丙二醇(39%)和水(26%)的混合物中的35%重量存在),改性淀粉的家族,例如在名称structuresolanace下销售的改性的马铃薯淀粉,或其混合物。
优选的胶凝剂源自聚丙烯酰胺家族,例如simulgel600或sepigel305,或其混合物。
如上所述的胶凝剂可以范围从0.1%至15%和更优选范围从0.5%至5%重量(相对于组合物的总重量)的优先的浓度使用。
或者,如果适合,水性凝胶可含有可选的或另外的胶凝剂例如卡波姆(卡波姆940或卡波姆980等)。
示例性单一制剂药用组合物也可含有惰性添加剂或这些添加剂的组合,例如
-湿润剂;
-增香剂;
-防腐剂例如对羟基苯甲酸酯;
-稳定剂;
-湿度调节剂;
-ph调节剂;
-渗透压调节剂;
-乳化剂;
-uv-a和uv-b屏蔽剂;和
-抗氧化剂,例如α-生育酚、丁羟基茴香醚或丁羟甲苯、超氧化物岐化酶、泛醇或某些金属螯合剂。
当然,本领域技术人员将谨慎选择以这样一种方式加入这些组合物中的可选的化合物,所述方式通过考虑的加入对与本发明本质相关的有利性质没有,或基本上没有不利的影响。
包含2.5%重量的过氧化苯甲酰和0.3%重量的阿达帕林和胶凝剂,特别是ph非依赖性胶凝剂的凝胶,有利地至少包含水并且还可包含促渗透剂(pro-penetratingagents)和/或液体润湿表面活性剂。
可用于本发明的组合物可含有范围从0%至20%和更优选范围从2%至6%重量(相对于组合物的总重量)的优先浓度的一种或多种促渗透剂。它们一般在所用的百分比时不应溶解活性剂,不应引起任何有害于过氧化苯甲酰的放热反应,应帮助活性剂的令人满意的分散,且应具有消泡性能。在优选使用的促渗透剂中有化合物例如丙二醇、二丙二醇、丙二醇二壬酸酯、丙二醇单月桂酸酯(lauroglycol)和乙氧基二甘醇(ethoxydiglycol),但不受限于此列表。
优选的促渗透剂是丙二醇。
有利地,可用于本发明的组合物还可含有范围从0%至10%和更优选范围从0.1%至2%重量(相对于组合物的总重量)的优先浓度的一种或多种液体润湿表面活性剂。湿润力是液体扩散到整个表面的趋势。
它们优选地是具有从7至9的hlb(亲水亲油平衡)值的表面活性剂,或非离子表面活性剂例如聚氧乙烯化和/或聚氧丙烯化共聚物。它们应该是液体,以便容易地掺入组合物中,而不必加热它们。
在优选使用的湿润剂中有泊洛沙姆家族的化合物且更特别是泊洛沙姆124和/或泊洛沙姆182,但不受限于此列表。
组合物还可包含如前所述的通常用于化妆品或药物领域的任何添加剂,例如螯合剂、抗氧化剂、防晒剂、防腐剂、填料、电解质、保湿剂、着色剂、普通无机或有机酸或碱、香料、香精油、化妆品活性剂、湿润剂、维生素、必需脂肪酸、鞘脂、自晒黑化合物例如dha,和镇静剂(calmants)和用于皮肤的保护剂例如尿囊素。不用说,本领域技术人员将谨慎选择这种或这些任选的另外的化合物,和/或其用量,以使示例性组合物的有利特性不会,或基本上不会受到不利影响。
这些添加剂可以相对于组合物总重量的从0%至20%重量的比例存在于组合物中。
可以提及的螯合剂的实例包括乙二胺四乙酸(edta),并且还有其衍生物或盐、二羟乙基甘氨酸、柠檬酸和酒石酸,或其混合物。
可以提及的防腐剂的实例包括苯扎氯铵、苯氧乙醇、苯甲醇、重氮咪唑烷基脲(diazolidinylurea)和对羟苯甲酸酯,或其混合物。
可以提及的湿润剂的实例包括甘油和山梨醇。
丙二醇、甘油和泊洛沙姆作为水性凝胶的添加剂是特别合乎需要的,其中胶凝剂是simulgel600或sepigel305或其它ph非依赖性胶凝剂。
水性凝胶的示例性含水相可包含水、花露水(floralwater)如矢车菊水(cornflowerwater),或天然矿物或泉水,其选自例如eaudevittel,vichy盆地、eaud'uriage、eaudelarocheposay、eaudelabourboule、eaud'enghien-les-bains、eaudesaintgervais-les-bains、eaudeneris-les-bains、eaud'allevard-les-bains、eaudedigne、eaudemaizieres、eaudeneyrac-les-bains、eaudelons-le-saunier、leseauxbonnes、eauderochefort、eaudesaintchristau、eaudesfumades、eaudetercis-les-bains、eaud'avene或eaud'aixlesbains的水。
所述含水相可以相对于组合物的总重量的10%-90%重量之间和优选地20%-80%重量之间的含量存在。
本文优选的具体水性凝胶组合物包含(相对于水性凝胶总重量的百分比重量):
示例性单一制剂药用组合物尤其意欲用于治疗严重痤疮,特别是普通痤疮(寻常痤疮)、黑头粉刺、多形性痤疮、结节囊肿性痤疮、聚合性痤疮,和继发性痤疮例如太阳、药物相关或职业性痤疮。措辞“严重痤疮”指具有[iga]=4的痤疮,其中iga意指调查性整体评估(investigativeglobalassessment)。
为了进一步举例说明示例性实施方案及其优点,给出以下具体实施例,要理解所述实施例仅仅是打算为示例性的,而非限制性的。在以下实施例中,份数和百分率以相对于各个组合物的总重量的重量计,除非另外指明。
实施例:
在以下临床研究及其总结中,各种标识为"cd02710.3%/cd15792.5%凝胶"、"cd02710.3%/cd15792.5%局部凝胶"、"阿达帕林0.3%/过氧化苯甲酰2.5%局部凝胶"和"0.3%a/bpo"的组合物是包含以下组分的水性凝胶,表示为%重量/总重量:
在临床研究和总结中各种称为"epiduo凝胶"、"cd02710.1%/cd15792.5%凝胶"、"阿达帕林0.1%/过氧化苯甲酰2.5%局部凝胶"和"0.1%a/bpo"的组合物是包含以下组分的水性凝胶,表示为%重量/总重量:
在临床研究和总结中称为"媒介凝胶"或"媒介"的组合物具有与以上描述的两种试验凝胶相同的组成,但不含阿达帕林和过氧化苯甲酰。
下文公开的研究显示,阿达帕林0.3%/过氧化苯甲酰2.5%局部凝胶允许获得治疗中度和重度寻常痤疮的良好结果。这个研究比较了在患有中度和重度痤疮的受试者中(总群体[op]),和在op的亚群(仅仅是重度痤疮受试者)(重症群体[sp])中阿达帕林0.3%/过氧化苯甲酰2.5%(0.3%a/bpo)局部凝胶对比媒介的功效和安全性。该研究还在sp中比较了0.3%a/bpo与阿达帕林0.1%/过氧化苯甲酰2.5%(0.1%a/bpo)局部凝胶。
这个多中心、随机、双盲、平行组、媒介-和活性剂-对照研究包括了总共503位受试者。受试者被随机施用0.3%a/bpo(n=217)、0.1%a/bpo(n=217)或媒介(n=69),每日一次,持续12周。op包括患有中度(调查者总体评估[iga]=3)和重度(iga=4)痤疮的受试者,同时sp仅由患有严重疾病(iga=4)的受试者组成。共同主要功效终点(co-primaryefficacyendpoints)包括了成功率(对iga的至少2-级改善)和从基线至第12周的炎性(in)和非-炎性(nin)损伤计数的变化。
在op中,0.3%a/bpo在成功率(33.7%对比11.0%),和in(-27.0对比-14.4)和nin损伤计数(-40.1对比-18.4)的变化,以及in(-68.7%对比-39.2%)和nin损伤计数(分别为-68.3%对比-37.3%;所有p<0.001)的百分率变化方面优于媒介。类似地,在sp中,0.3%a/bpo在成功率(31.9%对比11.8%;p=0.029),和in(-35.1对比-15.4)和nin损伤计数(-45.6对比-17.2)的变化,以及in(-74.4%对比-33.0%)和nin损伤计数(分别为-72.0%对比-30.7%;全部均p<0.001)的百分率变化方面优于媒介。
此外,0.3%a/bpo在sp中以成功率的11.4%差异(95%置信区间[ci]:-0.5%,23.2%),和in和nin损伤计数变化-3.25[ci:-7.15,0.64]和-2.51[ci:-8.08,3.06],显示出趋向于优于0.1%a/bpo的积极趋势。
至于安全性,0.3%a/bpo是良好耐受的,具有与0.1%a/bpo类似的局部耐受性特征。治疗-相关的不良事件(aes)(分别为在12位受试者中的15个aes[5.5%]对比在1位受试者中的2个aes[0.5%])在严重性方面是轻度至中度。在0.3%a/bpo组中只有1位受试者(0.2%)由于ae(特应性皮炎耀斑)而中断治疗,并且没有严重的aes被报告。
阿达帕林0.3%/bpo2.5%局部凝胶在一般群体中显示出优于媒介的卓越功效,而在患有严重痤疮的受试者中表现出更大功效。0.3%a/bpo的安全性特征是可接受的并比得上对0.1%a/bpo观察到的安全性特征。
研究的执行概要:
这个研究是一项多中心、随机、双盲、平行组、媒介-和活性剂-对照的12周研究,其调查了在患有中度和重度寻常痤疮受试者中,每日一次应用的cd02710.3%/cd15792.5%局部凝胶,对比每日一次局部应用的epiduo凝胶(阿达帕林/bpo)和媒介凝胶的功效和安全性。这项研究已由fda作为特殊方案评价(specialprotocolassessment)的一部分进行了检查并得到认可。
来自31个临床基地的总共503位受试者被随机分配到研究中,其中217、217和69位受试者被分别随机分配到cd02710.3%/cd15792.5%局部凝胶、epiduo凝胶和媒介组中。所有503位受试者被包括在itt和安全性群体中,和459位受试者被包括在pp群体中。研究被分层,约50%的受试者被分级为iga=3-中度(251位受试者)和50%被分级为iga=4-重度(252位受试者)。
3个功效目标按分级次序预先指定。3个目标按照下面列出的次序进行试验,各自有条件地取决于前一目标的成功。
1.证实cd02710.3%/cd15792.5%凝胶对比凝胶媒介在中度(iga=3)和重度痤疮(iga=4)的总群体中治疗寻常痤疮至多12周的功效的优越性。
2.证实cd02710.3%/cd15792.5%凝胶对比凝胶媒介在患有严重痤疮(iga=4)的受试者亚群中的功效的优越性。
3.通过对比epiduo凝胶的数值差异的点评估和差异的95%ci,评价cd02710.3%/cd15792.5%对比epiduo凝胶在患有严重痤疮(iga=4)的受试者亚群中的优越性。
如果满足目标(1)和(2),则研究在功效结果方面被认为是积极的。
此外,在研究期间评估了耐受性和安全性。
结果总结:
主要目标的结果如下:
cd02710.3%/cd15792.5%凝胶超过媒介凝胶的优越性在总研究群体(iga3中度和iga4重度)中,对成功率(在iga中,分级“明确的”或“几乎明确的”具有至少2-级改善的受试者)(33.7%对比11.0%,p<0.001)和对炎性(-27.04对比-14.40,p<0.001)和非-炎性损伤计数(-40.18对比-18.47,p<0.001)的改变得到证实。
在严重层(iga=4)中,cd02710.3%/cd15792.5%凝胶超过媒介凝胶的统计学优越性对成功率(在iga中,分级“明确的”或“几乎明确的”具有至少2-级改善的受试者)(31.9%对比11.8%,p=0.029)和对炎性(-35.17对比-15.46,p<0.001)和非-炎性损伤计数(-45.61对比-17.25,p<0.001)的改变得到证实。
cd02710.3%/cd15792.5%凝胶与epiduo凝胶在严重层(iga=4)中的差异和95%置信区间(cis)对于成功率被估计为11.4%[-0.5%,23.2%],对于炎性损伤计数的改变为-3.25[-7.15,0.64];和对于非-炎性损伤计数的改变为-2.51[-8.08,3.06],所有的终点显示出趋向于优于epiduo凝胶的积极趋势。研究并未强力证实这一比较的统计学显著性。
次要功效目标:
在总群体中,cd02710.3%/cd15792.5%凝胶超过媒介凝胶的统计学优越性对炎性(-68.70%对比-39.23%,p-值<0.001)和非-炎性损伤计数(-68.34%对比-37.38%,p-值<0.001)的百分比变化得到证实。
安全性目标:
cd02710.3%/cd15792.5%在该研究中是良好耐受的。局部耐受性特征类似于epiduo凝胶的耐受性特征,显示在第1周的体征和症状峰,接着是伴随连续治疗的进行性消散。很少的治疗突发性不良事件(treatmentemergentadverseevents)(teaes)一般在性质上是皮肤病学的和在严重程度上为轻度至中度。在cd02710.3%/cd15792.5%凝胶组中,只有一位受试者(0.2%)由于ae(特应性皮炎耀斑)而中断治疗。在cd02710.3%/cd15792.5%组中未报告有严重的不良事件。
一般结论:
这项研究证实,在iga成功率(明确的/几乎明确的且至少2级的改变)和炎性和非-炎性损伤计数变化的共同主要终点(co-primaryendpoints)方面,cd02710.3%/cd15792.5%凝胶优于媒介。统计学显著性始终高(p<0.001)且临床结果引人注目。该研究是可靠的,在pp群体中和敏感性分析方面呈现一致的结果。
在患有严重痤疮(iga=4)的受试者亚组中,cd02710.3%/cd15792.5%凝胶在iga成功率(p=0.029)、炎性(p<0.001)和非-炎性损伤计数(p<0.001)的变化方面优于媒介。该结果得到可靠的敏感性分析的支持。
cd02710.3%/cd15792.5%凝胶与epiduo凝胶在iga成功率、炎性和非-炎性损伤计数的变化方面比较的数值优越性的趋势在患有严重痤疮(iga=4)的受试者中被观察到。
cd02710.3%/cd15792.5%凝胶是良好耐受性的,具有可接受的安全性特征。
研究设计:
这是一项多中心、随机、双盲、平行组、媒介-和活性剂对照的12周研究,其调查了每日一次应用的cd02710.3%/cd15792.5%局部凝胶,对比每日一次应用的epiduo凝胶和媒介凝胶在患有中度和重度寻常痤疮的受试者中的功效和安全性。
随机化通过调查基地和iga严重性分层,以致50%的受试者分别具有3和4的iga分数。包括患有严重痤疮的受试者意欲允许证实在该受试者亚组中的功效。
合格的受试者被随机按3:3:1比例接受cd02710.3%/cd15792.5%局部凝胶、epiduo凝胶或者媒介凝胶12周。
主要的入选标准包括:具有按照iga等级的3(中度)或4(重度)的评分并在面部(包括鼻子)存在20-100个炎性损伤、30-150个非-炎性损伤,和在面部的至多2个结节的中度至重度面部痤疮的临床诊断。表现为面部和躯干寻常痤疮的受试者参与该研究;然而,只评价了面部痤疮损伤。
研究结果总结:
研究特征:
来自31个临床基地的总共503位受试者被随机分配到cd02710.3%/cd15792.5%局部凝胶、epiduo凝胶或媒介凝胶:217、217和69位受试者分别在cd02710.3%/cd15792.5%局部凝胶、epiduo凝胶或媒介凝胶组中。
所有503位受试者被包括在itt和安全性群体中,和459位受试者被包括在pp群体中。研究部署示于图1。
总共53位受试者(10.5%)过早中断研究。两个中断都是由于不良事件(在cd02710.3%/cd15792.5%局部凝胶组中的特应性皮炎耀斑和在epiduo凝胶组中的痤疮加重)。
各治疗组关于人口和基线特征是可比较的。在总共503位受试者中,有263(52.3%)位是女性,389(77.3%)是白种人,和平均年龄是19.6岁(中位数17.0岁)。
功效:
主要功效分析:
共同的主要功效终点被定义为:
1.成功率,具有明确的或几乎明确的iga(因此在第12周意向治疗[itt]中,自基线的至少2-级改善)的受试者的百分比;
2.炎性损伤计数从基线至第12周(itt)的变化;
3.非-炎性损伤计数从基线至12周(itt)的变化;
进行统计学分析以比较并以逐步的方式解释:
通过形式的推理假设检验,在中度和重度痤疮的总群体中,cd02710.3%/cd15792.5%凝胶对比局部凝胶媒介。
通过形式的推理假设检验,在患有严重痤疮(调查者的总体评估(investigator’sglobalassessment)iga=4)的受试者的亚组中,cd02710.3%/cd15792.5%凝胶对比局部凝胶媒介。
在患有严重痤疮(iga=4)的受试者的亚组中,通过利用对比媒介凝胶的数值差异的点评估和差异的95%ci,cd02710.3%/cd15792.5%对比epiduo凝胶(阿达帕林/bpo)。
多重填补(multipleimputation,mi)程序被用作主要填补法以补足缺少的功效数据。
主要功效分析(第12周mi,itt)显示(表2),在共同-主要终点,cd02710.3%/cd15792.5%凝胶比媒介凝胶是统计学上更有效的:
1.成功率(mi,itt)(cd02710.3%/cd15792.5%凝胶对比媒介之间的差异是22.7%,伴有[12.8%,32.6%],p<0.001的95%ci),
2.炎性损伤计数从基线至第12周(mi,itt)的变化(在cd02710.3%/cd15792.5%凝胶对比媒介之间的最小平方均差是-12.64个损伤,伴有[-15.82,-9.46],p<0.001的95%ci),
3.非炎性损伤计数从基线至第12周(mi,itt)的变化(在cd02710.3%/cd15792.5%凝胶对比媒介之间的最小平方均差是-21.71个损伤,伴有[-26.66,-16.76],p<0.001的95%ci)。
对缺失的数据使用传统locf填补法,主要功效分析结果还在pp分析和敏感性分析中得到证实。结果在下表1和图2-4中示出。
表1-全人群初步分析的概述(mi,itt)
在严重层(iga=4)中,主要功效分析(第12周mi,itt)还显示(表2和图6-8),对于在第12周的成功率(31.9%对比11.8%;p=0.029)和炎性(-35.2对比-15.5;p<0.001)和非炎性损伤计数(-45.6对比-17.3;p<0.001)的变化,cd02710.3%/cd15792.5%凝胶比媒介凝胶在统计学上更有效。
对于具有基线iga=4(严重)的受试者的主要分析结果通过敏感性分析的一致性结果所证实。
cd02710.3%/cd15792.5%凝胶与epiduo凝胶在iga成功率(11.4%差异)、炎性损伤计数的变化(3.25差异)和非-炎性损伤计数的变化(2.51差异)中比较的数值优越性的趋势在患有严重痤疮(iga=4)的受试者中被观察到。
对于这样的比较未计划形式的假设检验,因为对于在两种有效治疗之间的这种比较而言,认为样本规模太小。然而,治疗差异评估及其95%置信区间显示出接近显著性的积极趋势。置信区间举例说明于图5中。
表2-严重层(基线iga=4)(mi,itt)中主要分析的总结
炎性和非-炎性损伤计数的百分比变化(次级分析)
与两个次要终点关联的多重控制通过使用hochberg程序实现。在合并的总群体(表3)和在严重群体(表4)二者中,这些次级功效终点的分析与媒介对比在统计学也是显著的(p<0.001)。
表3-在全人群中炎性损伤计数和非-炎性损伤计数的百分比变化的概述(mi,itt)
表4-在患有严重痤疮(基线iga=4)的受试者中炎性和非-炎性损伤计数的百分比变化的概述(mi,itt)
安全性:
治疗持续时间:
按照方案计划的治疗期持续时间是12周。在该研究中,实际平均治疗持续时间对于cd02710.3%/cd15792.5%凝胶是79.0天,对于epiduo凝胶是78.3天,和对于媒介凝胶是78.4天。
不良事件:
关于aes本章节概述了总aes,接着是相关的aes,导致中断的aes,严重aes和特殊意义的aes。
总不良事件:
在研究期间,在105位受试者中报告了总共167个aes:50位受试者(23.0%)在cd02710.3%/cd15792.5%凝胶组中,42位受试者(19.4%)在epiduo组中和13位受试者(18.8%)在媒介组中(表5)。
表5-总不良事件的总结(安全性群体)
在cd02710.3%/cd15792.5%凝胶组中,最常见的aes(表6a)(在任何组中≥2%)是鼻咽炎[14位受试者(6.5%)],皮肤刺激[9位受试者(4.1%)]。
在epiduo凝胶组中,最常见的aes(≥2%)(表6a)是鼻咽炎[11位受试者(5.1%)]、上呼吸道感染[5位受试者(2.3%)]。
在媒介凝胶组中,上呼吸道感染是在超过2%的受试者[4位受试者(5.8%)]中报告的唯一的ae(表6a)。
皮肤和皮下组织疾病种类中的不良事件(aes)在cd02710.3%/cd15792.5%凝胶组的受试者[20位受试者(9.2%)]中比epiduo凝胶组[8位受试者(3.7%)]和媒介凝胶组[2位受试者(2.9%)]更频繁地观察到。
表6a-最常见的不良事件(≥2%)的总结(全部安全性群体)
与3个治疗组中的总群体相比,在患有严重痤疮(基线iga=4)的受试者的亚组中,安全性特征是类似的。
在患有严重痤疮(基线iga=4)的受试者的亚组中,皮肤和皮下组织疾病种类中的最常见的不良事件(在任何组中≥2%)(表6b),在cd02710.3%/cd15792.5%凝胶组的受试者[6位受试者(5.7%)]与epiduo凝胶组[6位受试者(5.4%)]比较时观察到类似的频率,两组都比媒介凝胶组[1位受试者(2.9%)]更频繁地观察到。有趣的是,在严重层中,cd02710.3%/cd15792.5%凝胶组中很少的受试者报告有皮肤刺激。
表6b-最常见的不良事件(≥2%)的总结(安全性群体,iga=4)
相关的不良事件:
在研究期间,在13位受试者(2.6%)中报告了据认为与研究药物相关的总共17个aes:在cd02710.3%/cd15792.5%凝胶组中的12位受试者(5.5%)报告了15个相关的aes,和在epiduo组中的1位受试者(0.5%)报告了2个相关的aes,而在媒介组中未报告相关的aes(表7)。
在据认为与研究药物相关的17个aes中,10具有轻度严重性,7位具有中度严重性,并且未报告重度ae。绝大多数事件在性质上是皮肤病学的(见下文)。两个相关的非-皮肤病学事件都在cd02710.3%/cd15792.5%凝胶组中。一个是眼睑红斑的情况(编为眼疾病),而另一个是皮肤感觉异常的情况(编为神经系统疾病)。
在据认为与研究药物相关的17个aes中,有15个报告自患有中度痤疮(基线iga=3)的受试者亚组中的11位受试者,其中cd02710.3%/cd15792.5%凝胶组有10位受试者,和epiduo凝胶组有一位。只有2个从患有严重痤疮(基线iga=4)的受试者亚组中的2位受试者中报告。两位受试者均在cd02710.3%/cd15792.5%凝胶组中。
在cd02710.3%/cd15792.5%凝胶组中,最常见的相关的aes是皮肤刺激[6位受试者(2.8%)]和皮肤灼烧感[2位受试者(0.9%)]。这些全是轻度或中度的,且不导致研究中断。在cd02710.3%/cd15792.5%凝胶组中的一个相关的aes(特应性皮炎耀斑)导致受试者从研究中断。在该组中的大多数相关的aes的发生是在该研究的第一个月内,仅有一个发生在第二个月(面部刺激)和一个发生在第三个月(颈前刺激)。
表7-相关的不良事件的概述
严重的不良事件:
对于该研究未有死亡报告。
在cd02710.3%/cd15792.5%凝胶和在媒介组中未报告有saes。在研究期间,只有1位受试者(在epiduo组中)被报告具有一个非-相关性中度严重的不良事件(概括为焦虑症)。
导致中断的不良事件:
在研究期间有两个aes导致中断:一个相关的不良事件(特应性皮炎耀斑)报告于cd02710.3%/cd15792.5%凝胶组的1位受试者(0.5%),一个非-相关的不良事件(痤疮恶化)报告于epiduo组的1位受试者,而在媒介组中未有导致中断的aes。
严重不良事件:
在cd02710.3%/cd15792.5%凝胶和epiduo组中未报告有严重不良事件。总共一个非-相关的严重不良事件(显著地降低钾水平)报告于媒介组中的一位(1.4%)受试者。
特定意义的不良事件:
在该研究中,特定意义的不良事件(aesi)被定义为疑似致敏。总共一个aesi报告于cd02710.3%/cd15792.5%凝胶组的1位受试者(0.5%)中。aesi(具有疑似过敏的刺激性皮炎)被认为是相关的且在严重性方面属于轻度。它出现在第19天并持续12天。受试者被给予测试的贴剂,但被拒绝并中止研究。
局部耐受性:
局部耐受性参数(红斑、起鳞、干燥、刺痛/灼烧)根据4-分等级评价:在每次访问时,0=无,1=轻度,2=中度,3=重度。表8和表9提供对于总安全性群体和对于基线iga=4亚组的差于基线的最高评分的小结。
对于红斑、起鳞和干燥,与媒介凝胶组相比,在cd02710.3%/cd15792.5%凝胶组中的发生率高于epiduo凝胶组。对于刺痛/灼烧,在cd02710.3%/cd15792.5%凝胶组和在epiduo凝胶组中,发生率相当,且均比媒介凝胶组高。
局部耐受性体征和症状的平均评分在第1周增加至峰值,此后如在图9-12中所示随时间的推移而下降。cd02710.3%/cd15792.5%凝胶的峰值分数比epiduo凝胶略高。局部耐受性的体征和症状大多数是轻度或中度,极少数是重度。
表8–比基线更差的最高局部耐受性评分(安全性群体)
在患有严重痤疮(基线iga=4)的受试者的亚组中,局部耐受性特征是类似的。
表9–在患有严重痤疮(基线iga=4,安全性群体)的受试者中比基线更差的最高局部耐受性评分。
讨论:
iga成功率,一个二分参数,在严重群体中需要至少3分的变化至几乎明确的和明确的。在此cd02710.3%/cd15792.5%凝胶和epiduo之间的差异是最突出的,或许反映了在新产品中的较高浓度的阿达帕林的更有效的效果。特别地,对于cd02710.3%/cd15792.5%凝胶在该结果中对比媒介的治疗效果差异是20.1%并有统计学意义(p=0.029),而对于epiduo凝胶在该结果中对比媒介的治疗效果差异是8.8%并且没有统计学意义(名义上的p=0.443;事后分析(post-hocanalysis)不作为限定的统计学计划的一部分进行)。
有趣的是注意到,用cd02710.3%/cd15792.5%凝胶观察到的皮肤相关的不良事件在重症组中是较不频繁的,而正是这个组表明了有关治疗效果的较大增值。这种有利的效益风险状况很好地表明有利于在重症群体中使用该产品。
结论:
该研究证实,cd02710.3%/cd15792.5%凝胶在共同-主要终点iga成功率(明确的/几乎明确的和2级改变)和炎性和非-炎性损伤计数的变化方面优于媒介。统计学显著性始终高(p<0.001)且临床结果引人注目。研究是可靠的,在pp群体和敏感性分析中呈现一致的结果。
在患有严重痤疮(iga=4)的受试者亚组中,cd02710.3%/cd15792.5%凝胶在iga成功率(p=0.029),炎性(p<0.001)和非-炎性损伤计数(p<0.001)的变化方面优于媒介。该结果由可靠的敏感性分析支持。
在患有严重痤疮(iga=4)的受试者中,观察到cd02710.3%/cd15792.5%凝胶与epiduo凝胶比较在iga成功率、炎性和非-炎性损伤计数的变化方面的数值优越性的趋势。
cd02710.3%/cd15792.5%凝胶是良好耐受的,具有可接受的安全性特征。
虽然示例性实施方案已根据各种特定和优选的实施方案进行了描述,技术人员将意识到,各种修饰、取代、省约和改变可在不背离其精神的情况下进行。因此,意欲使本申请的范围仅受以下权利要求书的范围的限制。
- 还没有人留言评论。精彩留言会获得点赞!