利用ACTRII配体陷阱治疗心血管疾病的制作方法
1.相关申请的交叉引用
本申请要求2014年10月9日提交的美国临时专利申请no.62/062,021;2014年11月11日提交的美国临时专利申请no.62/078,321;2015年1月14日提交的美国临时专利申请no.62/103,515;2015年5月27日提交的美国临时专利申请no.62/167,052;和2015年6月2日提交的美国临时专利申请no.62/170,015的优先权;为了所有目的将它们每一篇的全部内容通过引用合并在文本中。
2.政府许可权
本发明是利用国家卫生研究所颁发的款项编号dk070790和dk089137的政府支持下作出的。政府在本发明中拥有一定权利。
3.序列表
本申请与文件名为12827_934_228_seqlisting.txt、大小208千字节、2015年10月6日创建的序列表一起提交。为了所有目的,序列表通过完全引用合并在本文中。
4.技术领域
本文提供的是治疗和/或预防对象的心血管疾病、血管钙化、与血管钙化相关和/或由血管钙化引起的心血管疾病、和/或与肾病相关和/或由肾病引起的心血管疾病的方法,包括向所述对象施用激活素ii型受体信号转导抑制剂(actrii信号转导抑制剂,例如,激活素配体陷阱(activinligandtrap))。更具体地,本文提供的是选择对象来治疗心血管疾病、血管钙化、动脉硬化水平升高、左心室肥大、与血管钙化相关和/或由血管钙化引起的心血管疾病、与动脉硬化水平升高相关和/或由动脉硬化水平升高引起的心血管疾病、与左心室肥大相关和/或由左心室肥大引起的心血管疾病、和/或与肾病相关和/或由肾病引起的心血管疾病的方法,通过利用一种或更多种生物标记物的水平和/或活性,特别是,snail同源物1(snai1)、phosphosmad2、phosphosmad3、尿蛋白、dickkopf同源物1(dkk1)、1型胶原蛋白alpha1(col1a1)、激活素(例如,游离激活素)、runt相关转录因子2(runx2)、碱性磷酸酶(alp)、骨特异性碱性磷酸酶(bsap)、osterix、c-末端1型胶原蛋白端肽(ctx)、klotho、alpha-平滑肌动蛋白(alpha-sma)、心肌素(myocardin,myocd)、axis抑制蛋白质2(axin2)和/或平滑肌蛋白22-alpha(sm22-alpha),作为用激活素ii型受体(actrii)信号转导抑制剂治疗的对象对治疗的响应、治疗效果或适当剂量的指示。本文提供的是降低对象的骨吸收的方法,包括向所述对象施用actrii信号转导抑制剂。更具体地,本文提供的是选择对象来降低骨吸收的方法,通过利用一种或更多种生物标记物的水平和/或活性,特别是snai1、phosphosmad2、phosphosmad3、尿蛋白、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、osterix、ctx、klotho、alpha-sma、myocd和/或sm22-alpha,作为用actrii信号转导抑制剂治疗的对象对治疗的响应、治疗效果或适当剂量的指示。
5.背景
涉及贫血的肾病的常见并发症是血管钙化,在很多情况下其导致心血管疾病。在肾脏对象中,除了肾脏疾病本身相关的死亡之外,动脉粥样硬化和所产生的心血管疾病可能导致显著的死亡。因而,对于发现和开发用于肾脏对象的心血管疾病的新药物以及治疗和/或预防方法存在着持续的需求。另外,由于肾脏对象经常患有贫血,有益的是用单一的治疗剂来治疗贫血和伴随的心血管疾病,这是当前使用的红细胞生成刺激试剂(esas)例如促红细胞生成素所不具有的能力。
两种相关的ii型受体actriia和actriib已经被鉴定为激活素的ii型受体(mathewsandvale,1991,cell65:973-982;attisanoetal.,1992,cell68:97-108)。除了激活素之外,actriia和actriib可以与几种其他的tgf-beta家族蛋白,包括bmp7、nodal、gdf8和gdf11生物化学地相互作用(yamashitaetal.,1995,j.cellbiol.130:217-226;leeandmcpherron,2001,proc.natl.acad.sci.98:9306-9311;yeoandwhitman,2001,mol.cell7:949-957;ohetal.,2002,genesdev.16:2749-54)。alk4是激活素的主要的i型受体,特别是对于激活素a,alk-7也可以充当激活素的受体,特别是对于激活素b。
激活素配体陷阱,由人源化的融合蛋白组成,所述融合蛋白由激活素iia型受体(actriia)的细胞外结构域和人igg1fc组成(在此称为actriia-hfc或“sotatercept”;seqidno:7),当前在ii期临床试验中被评估,用于治疗患有与终末期肾病(esrd)相关的贫血和骨失调的对象以及患有beta-地中海贫血的那些对象。在健康的绝经后女性中,actriia-hfc也显示了显著地提高血细胞比容(hct)和血红蛋白(hgb)以及骨矿物密度。
6.概述
本文提供的是治疗和/或预防对象的血管钙化的方法,包括向所述对象施用药学上有效剂量的激活素ii型受体(actrii)信号转导抑制剂(例如,激活素配体陷阱),其中所述对象具有:(a)与参考群体中的runx2水平相比提高的runx2水平;(b)与参考群体中的alp水平相比提高的alp水平;(c)与参考群体中的snai1水平相比提高的snai1水平;(d)与参考群体中的phosphosmad2水平相比提高的phosphosmad2水平;(e)与参考群体中的dkk1水平相比提高的dkk1水平;(f)与参考群体中的col1a1水平相比提高的col1a1水平;(g)与参考群体中的激活素水平相比提高的激活素(例如,游离激活素)水平;(h)与参考群体中的bsap水平相比提高的bsap水平;(i)与参考群体中的osterix水平相比提高的osterix水平;(j)与参考群体中的ctx水平相比提高的ctx水平;(k)与参考群体中的klotho水平相比降低的klotho水平;(l)与参考群体中的alpha-sma水平相比降低的alpha-sma水平;(m)与参考群体中的myocd水平相比降低的myocd水平;(n)与参考群体中的sm22-alpha水平相比降低的sm22-alpha水平;(o)与参考群体中的phosphosmad3水平相比提高的phosphosmad3水平;(p)与参考群体中的尿蛋白水平相比提高的尿蛋白水平;和/或(q)与参考群体中的actriia水平相比降低的激活素2a型受体(actriia)水平。参见,例如,8.6章节对参考群体的描述。
本文提供的是治疗和/或预防对象的心血管疾病的方法,包括向所述对象施用药学上有效剂量的激活素ii型受体(actrii)信号转导抑制剂(例如,激活素配体陷阱),其中所述对象具有:(a)与参考群体中的runx2水平相比提高的runx2水平;(b)与参考群体中的alp水平相比提高的alp水平;(c)与参考群体中的snai1水平相比提高的snai1水平;(d)与参考群体中的phosphosmad2水平相比提高的phosphosmad2水平;(e)与参考群体中的dkk1水平相比提高的dkk1水平;(f)与参考群体中的col1a1水平相比提高的col1a1水平;(g)与参考群体中的激活素水平相比提高的激活素(例如,游离激活素)水平;(h)与参考群体中的bsap水平相比提高的bsap水平;(i)与参考群体中的osterix水平相比提高的osterix水平;(j)与参考群体中的ctx水平相比提高的ctx水平;(k)与参考群体中的klotho水平相比降低的klotho水平;(l)与参考群体中的alpha-sma水平相比降低的alpha-sma水平;(m)与参考群体中的myocd水平相比降低的myocd水平;(n)与参考群体中的sm22-alpha水平相比降低的sm22-alpha水平;(o)与参考群体中的phosphosmad3水平相比提高的phosphosmad3水平;(p)与参考群体中的尿蛋白水平相比提高的尿蛋白水平;和/或(q)与参考群体中的actriia水平相比降低的actriia水平。
本文提供的是治疗和/或预防对象的心血管疾病的方法,包括向所述对象施用药学上有效剂量的激活素ii型受体(actrii)信号转导抑制剂(例如,激活素配体陷阱),其中所述对象具有:(a)与参考群体中的runx2水平相比提高的runx2水平;(b)与参考群体中的alp水平相比提高的alp水平;(c)与参考群体中的snai1水平相比提高的snai1水平;(d)与参考群体中的phosphosmad2水平相比提高的phosphosmad2水平;(e)与参考群体中的dkk1水平相比提高的dkk1水平;(f)与参考群体中的col1a1水平相比提高的col1a1水平;(g)与参考群体中的激活素水平相比提高的激活素(例如,游离激活素)水平;(h)与参考群体中的bsap水平相比提高的bsap水平;(i)与参考群体中的osterix水平相比提高的osterix水平;(j)与参考群体中的ctx水平相比提高的ctx水平;(k)与参考群体中的klotho水平相比降低的klotho水平;(l)与参考群体中的alpha-sma水平相比降低的alpha-sma水平;(m)与参考群体中的myocd水平相比降低的myocd水平;(n)与参考群体中的sm22-alpha水平相比降低的sm22-alpha水平;(o)与参考群体中的phosphosmad3水平相比提高的phosphosmad3水平;(p)与参考群体中的尿蛋白水平相比提高的尿蛋白水平;和/或(q)与参考群体中的actriia水平相比降低的actriia水平,以及其中所述心血管疾病与血管钙化相关和/或由血管钙化引起。
本文提供的是治疗和/或预防对象的心血管疾病的方法,包括向所述对象施用药学上有效剂量的激活素ii型受体(actrii)信号转导抑制剂(例如,激活素配体陷阱),其中所述对象具有:(a)与参考群体中的runx2水平相比提高的runx2水平;(b)与参考群体中的alp水平相比提高的alp水平;(c)与参考群体中的snai1水平相比提高的snai1水平;(d)与参考群体中的phosphosmad2水平相比提高的phosphosmad2水平;(e)与参考群体中的dkk1水平相比提高的dkk1水平;(f)与参考群体中的col1a1水平相比提高的col1a1水平;(g)与参考群体中的激活素水平相比提高的激活素(例如,游离激活素)水平;(h)与参考群体中的bsap水平相比提高的bsap水平;(i)与参考群体中的osterix水平相比提高的osterix水平;(j)与参考群体中的ctx水平相比提高的ctx水平;(k)与参考群体中的klotho水平相比降低的klotho水平;(l)与参考群体中的alpha-sma水平相比降低的alpha-sma水平;(m)与参考群体中的myocd水平相比降低的myocd水平;(n)与参考群体中的sm22-alpha水平相比降低的sm22-alpha水平;(o)与参考群体中的phosphosmad3水平相比提高的phosphosmad3水平;(p)与参考群体中的尿蛋白水平相比提高的尿蛋白水平;和/或(q)与参考群体中的actriia水平相比降低的actriia水平,以及其中所述心血管疾病与肾病相关和/或由肾病引起。
本文提供的是降低对象的骨吸收的方法,包括向所述对象施用药学上有效剂量的激活素ii型受体(actrii)信号转导抑制剂(例如,激活素配体陷阱),其中所述对象具有:(a)与参考群体中的runx2水平相比提高的runx2水平;(b)与参考群体中的alp水平相比提高的alp水平;(c)与参考群体中的snai1水平相比提高的snai1水平;(d)与参考群体中的phosphosmad2水平相比提高的phosphosmad2水平;(e)与参考群体中的dkk1水平相比提高的dkk1水平;(f)与参考群体中的col1a1水平相比提高的col1a1水平;(g)与参考群体中的激活素水平相比提高的激活素(例如,游离激活素)水平;(h)与参考群体中的bsap水平相比提高的bsap水平;(i)与参考群体中的osterix水平相比提高的osterix水平;(j)与参考群体中的ctx水平相比提高的ctx水平;(k)与参考群体中的klotho水平相比降低的klotho水平;(l)与参考群体中的alpha-sma水平相比降低的alpha-sma水平;(m)与参考群体中的myocd水平相比降低的myocd水平;(n)与参考群体中的sm22-alpha水平相比降低的sm22-alpha水平;(o)与参考群体中的phosphosmad3水平相比提高的phosphosmad3水平;(p)与参考群体中的尿蛋白水平相比提高的尿蛋白水平;和/或(q)与参考群体中的actriia水平相比降低的actriia水平。
本文提供的是治疗和/或预防对象的动脉硬化的方法,包括向所述对象施用药学上有效剂量的激活素ii型受体(actrii)信号转导抑制剂(例如,激活素配体陷阱),其中所述对象具有:(a)与参考群体中的runx2水平相比提高的runx2水平;(b)与参考群体中的alp水平相比提高的alp水平;(c)与参考群体中的snai1水平相比提高的snai1水平;(d)与参考群体中的phosphosmad2水平相比提高的phosphosmad2水平;(e)与参考群体中的dkk1水平相比提高的dkk1水平;(f)与参考群体中的col1a1水平相比提高的col1a1水平;(g)与参考群体中的激活素水平相比提高的激活素(例如,游离激活素)水平;(h)与参考群体中的bsap水平相比提高的bsap水平;(i)与参考群体中的osterix水平相比提高的osterix水平;(j)与参考群体中的ctx水平相比提高的ctx水平;(k)与参考群体中的klotho水平相比降低的klotho水平;(l)与参考群体中的alpha-sma水平相比降低的alpha-sma水平;(m)与参考群体中的myocd水平相比降低的myocd水平;(n)与参考群体中的sm22-alpha水平相比降低的sm22-alpha水平;(o)与参考群体中的phosphosmad3水平相比提高的phosphosmad3水平;(p)与参考群体中的尿蛋白水平相比提高的尿蛋白水平;和/或(q)与参考群体中的actriia水平相比降低的actriia水平。
本文提供的是治疗和/或预防对象的左心室肥大的方法,包括向所述对象施用药学上有效剂量的激活素ii型受体(actrii)信号转导抑制剂(例如,激活素配体陷阱),其中所述对象具有:(a)与参考群体中的runx2水平相比提高的runx2水平;(b)与参考群体中的alp水平相比提高的alp水平;(c)与参考群体中的snai1水平相比提高的snai1水平;(d)与参考群体中的phosphosmad2水平相比提高的phosphosmad2水平;(e)与参考群体中的dkk1水平相比提高的dkk1水平;(f)与参考群体中的col1a1水平相比提高的col1a1水平;(g)与参考群体中的激活素水平相比提高的激活素(例如,游离激活素)水平;(h)与参考群体中的bsap水平相比提高的bsap水平;(i)与参考群体中的osterix水平相比提高的osterix水平;(j)与参考群体中的ctx水平相比提高的ctx水平;(k)与参考群体中的klotho水平相比降低的klotho水平;(l)与参考群体中的alpha-sma水平相比降低的alpha-sma水平;(m)与参考群体中的myocd水平相比降低的myocd水平;(n)与参考群体中的sm22-alpha水平相比降低的sm22-alpha水平;(o)与参考群体中的phosphosmad3水平相比提高的phosphosmad3水平;(p)与参考群体中的尿蛋白水平相比提高的尿蛋白水平;和/或(q)与参考群体中的actriia水平相比降低的actriia水平。
在某些实施方式中,所述药学上有效剂量的所述actrii信号转导抑制剂是约15mg、约30mg、约45mg、约60mg、约75mg、约90mg或约1g或约0.1mg/kg、约0.13mg/kg、约0.2mg/kg、约0.26mg/kg、约0.3mg/kg、约0.4mg/kg、约0.5mg/kg、约0.6mg/kg、约0.7mg/kg、约0.8mg/kg、约0.9mg/kg、约1.0mg/kg、约1.1mg/kg、约1.2mg/kg、约1.3mg/kg、约1.4mg/kg或约1.5mg/kg。在某些实施方式中,所述药学上有效剂量的actrii信号转导抑制剂是约0.1mg/kg。在某些实施方式中,所述药学上有效剂量的actrii信号转导抑制剂是约0.3mg/kg。在某些实施方式中,所述药学上有效剂量的actrii信号转导抑制剂是约0.5mg/kg。在某些实施方式中,所述药学上有效剂量的actrii信号转导抑制剂是约0.7mg/kg。
在某些实施方式中,所述药学上有效的剂量通过注射来施用。在某些实施方式中,所述药学上有效的剂量(i)每28天一次;或(ii)每42天一次施用。在某些实施方式中,所述药学上有效的剂量每14天施用一次。在某些实施方式中,所述药学上有效的剂量每21天施用一次。在某些实施方式中,所述药学上有效的剂量连续地和/或无限地施用。
在某些实施方式中,snai1、phosphosmad2、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、phosphosmad3、尿蛋白和/或osterix的提高的水平分别比参考群体中snai1、phosphosmad2、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、phosphosmad3、尿蛋白和/或osterixs水平高约10%、20%、25%、30%、40%、50%、60%、70%、75%、80%、90%、100%、200%或500%。
在某些实施方式中,snai1、phosphosmad2、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、phosphosmad3、尿蛋白和/或osterix的提高的水平分别等于或约10%、20%、25%、30%、40%、50%、60%、70%、75%、80%、90%、100%、200%或500%高于参考群体的前10%、前5%、前4%、前3%、前2%或前1%中snai1、phosphosmad2、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、phosphosmad3、尿蛋白和/或osterixs的水平。
在某些实施方式中,klotho、alpha-sma、myocd、actriia、axin2和/或sm22-alpha的降低的水平分别比参考群体中klotho、alpha-sma、myocd、actriia、axin2和/或sm22-alpha的水平低约10%、20%、25%、30%、40%、50%、60%、70%、75%、80%、90%或100%。
在某些实施方式中,klotho、alpha-sma、myocd、actriia、axin2和/或sm22-alpha的降低的水平分别等于或约10%、20%、25%、30%、40%、50%、60%、70%、75%、80%、90%或100%低于参考群体的后10%、后5%、后4%、后3%、后2%或后1%中klotho、alpha-sma、myocd、actriia、axin2和/或sm22-alpha的水平。
本文提供的是治疗和/或预防对象的血管钙化的方法,其中所述方法包括:(a)向所述对象施用初始剂量的actrii信号转导抑制剂;(b)进行所述对象中snai1、phosphosmad2、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、osterix、klotho、alpha-sma、myocd、phosphosmad3、尿蛋白、actriia、axin2和/或sm22-alpha水平的第一次测量;(c)一段时间以后,进行所述对象中snai1、phosphosmad2、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、osterix、klotho、alpha-sma、myocd、phosphosmad3、尿蛋白、actriia、axin2和/或sm22-alpha水平的第二次测量;和(d)向所述对象施用调整的剂量的所述激活素ii型受体信号转导抑制剂。在某些实施方式中,所述调整的剂量是基于所述第一次测量和所述第二次测量之间检测到的变化。在某些实施方式中,所述剂量是如章节8.3.4中描述调整的。
本文提供的是治疗和/或预防对象的心血管疾病的方法,其中所述方法包括:(a)向所述对象施用初始剂量的actrii信号转导抑制剂;(b)进行所述对象中snai1、phosphosmad2、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、osterix、klotho、alpha-sma、myocd、phosphosmad3、尿蛋白、actriia、axin2和/或sm22-alpha水平的第一次测量;(c)一段时间以后,进行所述对象中snai1、phosphosmad2、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、osterix、klotho、alpha-sma、myocd、phosphosmad3、尿蛋白、actriia、axin2和/或sm22-alpha水平的第二次测量;和(d)向所述对象施用调整的剂量的所述激活素ii型受体信号转导抑制剂。在某些实施方式中,所述调整的剂量是基于所述第一次测量和所述第二次测量之间检测到的变化。在某些实施方式中,所述剂量是如章节8.3.4中描述调整的。
本文提供的是治疗和/或预防对象的心血管疾病的方法,其中所述方法包括:(a)向所述对象施用初始剂量的actrii信号转导抑制剂;(b)进行所述对象中snai1、phosphosmad2、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、osterix、klotho、alpha-sma、myocd、phosphosmad3、尿蛋白、actriia、axin2和/或sm22-alpha水平的第一次测量;(c)一段时间以后,进行所述对象中snai1、phosphosmad2、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、osterix、klotho、alpha-sma、myocd、phosphosmad3、尿蛋白、actriia、axin2和/或sm22-alpha水平的第二次测量;和(d)向所述对象施用调整的剂量的所述激活素ii型受体信号转导抑制剂;其中所述心血管疾病与血管钙化相关和/或由血管钙化引起。在某些实施方式中,所述调整的剂量是基于所述第一次测量和所述第二次测量之间检测到的变化。在某些实施方式中,所述剂量是如章节8.3.4中描述调整的。
本文提供的是治疗和/或预防对象的心血管疾病的方法,其中所述方法包括:(a)向所述对象施用初始剂量的actrii信号转导抑制剂;(b)进行所述对象中snai1、phosphosmad2、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、osterix、klotho、alpha-sma、myocd、phosphosmad3、尿蛋白、actriia、axin2和/或sm22-alpha水平的第一次测量;(c)一段时间以后,进行所述对象中snai1、phosphosmad2、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、osterix、klotho、alpha-sma、myocd、phosphosmad3、尿蛋白、actriia、axin2和/或sm22-alpha水平的第二次测量;和(d)向所述对象施用调整的剂量的所述激活素ii型受体信号转导抑制剂;其中所述心血管疾病与肾病相关和/或由肾病引起。在某些实施方式中,所述调整的剂量是基于所述第一次测量和所述第二次测量之间检测到的变化。在某些实施方式中,所述剂量是如章节8.3.4中描述调整的。
本文提供的是降低对象的骨吸收的方法,其中所述方法包括:(a)向所述对象施用初始剂量的actrii信号转导抑制剂;(b)进行所述对象中snai1、phosphosmad2、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、osterix、klotho、alpha-sma、myocd、phosphosmad3、尿蛋白、actriia、axin2和/或sm22-alpha水平的第一次测量;(c)一段时间以后,进行所述对象中snai1、phosphosmad2、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、osterix、klotho、alpha-sma、myocd、phosphosmad3、尿蛋白、actriia、axin2和/或sm22-alpha水平的第二次测量;和(d)向所述对象施用调整的剂量的所述激活素ii型受体信号转导抑制剂。在某些实施方式中,骨吸收是如章节8.6中评估的。在某些实施方式中,所述调整的剂量是基于所述第一次测量和所述第二次测量之间检测到的变化。在某些实施方式中,所述剂量是如章节8.3.4中描述调整的。
本文提供的是治疗和/或预防对象的动脉硬化的方法,其中所述方法包括:(a)向所述对象施用初始剂量的actrii信号转导抑制剂;(b)进行所述对象中snai1、phosphosmad2、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、osterix、klotho、alpha-sma、myocd、phosphosmad3、尿蛋白、actriia、axin2和/或sm22-alpha水平的第一次测量;(c)一段时间以后,进行所述对象中snai1、phosphosmad2、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、osterix、klotho、alpha-sma、myocd、phosphosmad3、尿蛋白、actriia、axin2和/或sm22-alpha水平的第二次测量;和(d)向所述对象施用调整的剂量的所述激活素ii型受体信号转导抑制剂。在某些实施方式中,动脉硬化的是如章节8.6中评估的。在某些实施方式中,所述调整的剂量是基于所述第一次测量和所述第二次测量之间检测到的变化。在某些实施方式中,所述剂量是如章节8.3.4中描述调整的。
本文提供的是治疗和/或预防对象的左心室肥大的方法,其中所述方法包括:(a)向所述对象施用初始剂量的actrii信号转导抑制剂;(b)进行所述对象中snai1、phosphosmad2、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、osterix、klotho、alpha-sma、myocd、phosphosmad3、尿蛋白、actriia、axin2和/或sm22-alpha水平的第一次测量;(c)一段时间以后,进行所述对象中snai1、phosphosmad2、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、osterix、klotho、alpha-sma、myocd、phosphosmad3、尿蛋白、actriia、axin2和/或sm22-alpha水平的第二次测量;和(d)向所述对象施用调整的剂量的所述激活素ii型受体信号转导抑制剂。在某些实施方式中,所述调整的剂量是基于所述第一次测量和所述第二次测量之间检测到的变化。在某些实施方式中,所述剂量是如章节8.3.4中描述调整的。
在某些实施方式中,所述初始剂量的所述actrii信号转导抑制剂是约15mg、约30mg、约45mg、约60mg、约75mg、约90mg或约1g或约0.1mg/kg、约0.13mg/kg、约0.2mg/kg、约0.26mg/kg、约0.3mg/kg、约0.4mg/kg、约0.5mg/kg、约0.6mg/kg、约0.7mg/kg、约0.8mg/kg、约0.9mg/kg、约1.0mg/kg、约1.1mg/kg、约1.2mg/kg、约1.3mg/kg、约1.4mg/kg或约1.5mg/kg。在某些实施方式中,所述初始剂量的所述actrii信号转导抑制剂是约0.1mg/kg。在某些实施方式中,所述初始剂量的所述actrii信号转导抑制剂是约0.3mg/kg。在某些实施方式中,所述初始剂量的所述actrii信号转导抑制剂是约0.5mg/kg。在某些实施方式中,所述初始剂量的所述actrii信号转导抑制剂是约0.7mg/kg。
在某些实施方式中,所述初始剂量是通过注射施用的。在某些实施方式中,所述初始剂量是(i)每28天施用一次;或(ii)每42天施用一次。在某些实施方式中,所述初始剂量是每14天施用一次。在某些实施方式中,所述初始剂量是每21天施用一次。
在某些实施方式中,actrii信号转导抑制剂的所述调整的剂量大于所述初始剂量,如果:(a)与参考群体中runx2的水平相比runx2的水平升高;(b)与参考群体中alp的水平相比alp的水平升高;(c)与参考群体中snai1的水平相比snai1的水平升高;(d)与参考群体中phosphosmad2的水平相比phosphosmad2的水平升高;(e)与参考群体中dkk1的水平相比dkk1的水平升高;(f)与参考群体中col1a1的水平相比col1a1的水平升高;(g)与参考群体中激活素的水平相比激活素的水平升高;(h)与参考群体中bsap的水平相比bsap的水平升高;(i)与参考群体中ctx的水平相比ctx的水平升高;(j)与参考群体中osterix的水平相比osterix的水平升高;(k)与参考群体中klotho的水平相比klotho的水平降低;(l)与参考群体中alpha-sma的水平相比alpha-sma的水平降低;(m)与参考群体中myocd的水平相比myocd的水平降低;(n)与参考群体中sm22-alpha的水平相比sm22-alpha的水平降低;(o)与参考群体中phosphosmad3的水平相比ppospposmad3的水平升高;(p)与参考群体中尿蛋白的水平相比尿蛋白的水平升高;(q)与参考群体中actriia的水平相比actriia的水平降低;和/或(r)与参考群体中axin2的水平相比axin2的水平降低。
在某些实施方式中,所述调整的剂量是约2.5mg、约5mg、约10mg、约15mg、约20mg或约35mg大于所述初始剂量,或约0.05mg/kg、约0.1mg/kg、约0.15mg/kg、约0.25mg/kg、约0.3mg/kg、约0.35mg/kg、约0.4mg/kg或约0.5mg/kg大于所述初始剂量。在某些实施方式中,所述调整的剂量比所述初始剂量更频繁地施用。在某些实施方式中,所述调整的剂量每5、10、15、20、25、28、30、35或40天施用。
在某些实施方式中,actrii信号转导抑制剂的所述调整的剂量小于所述初始剂量,如果:(a)与参考群体中runx2的水平相比runx2的水平降低;(b)与参考群体中alp的水平相比alp的水平降低;(c)与参考群体中bsap的水平相比bsap的水平降低;(d)与参考群体中snai1的水平相比snai1的水平降低;(e)与参考群体中phosphosmad2的水平相比phosphosmad2的水平降低;(f)与参考群体中dkk1的水平相比dkk1的水平降低;(g)与参考群体中col1a1的水平相比col1a1的水平降低;(h)与参考群体中激活素(例如,游离激活素)的水平相比激活素(例如,游离激活素)的水平降低;(i)与参考群体中ctx的水平相比ctx的水平降低;(j)与参考群体中osterix的水平相比osterix的水平降低;(k)与参考群体中klotho的水平相比klotho的水平升高;(l)与参考群体中alpha-sma的水平相比alpha-sma的水平升高;(m)与参考群体中myocd的水平相比myocd的水平升高;(n)与参考群体中sm22-alpha的水平相比sm22-alpha的水平升高;(o)与参考群体中phosphosmad3的水平相比ppospposmad3的水平降低;(p)与参考群体中尿蛋白的水平相比尿蛋白的水平降低;(q)与参考群体中actriia的水平相比actriia的水平升高;和/或(r)与参考群体中axin2的水平相比axin2的水平升高。
在某些实施方式中,所述调整的剂量是约2.5mg、约5mg、约10mg、约15mg、约20mg或约35mg小于所述初始剂量,或约0.05mg/kg、约0.1mg/kg、约0.15mg/kg、约0.25mg/kg、约0.3mg/kg、约0.35mg/kg、约0.4mg/kg或约0.5mg/kg小于所述初始剂量。在某些实施方式中,所述调整的剂量比所述初始剂量较少频繁地施用。在某些实施方式中,所述调整的剂量每30、35、40、42、50、60、70、80或90天施用。在某些实施方式中,所述调整的剂量连续地和/或无限地施用。
在某些实施方式中,所述第一次测量在治疗的开始之前进行。在某些实施方式中,所述第一次测量在治疗的开始之后立即进行,或在其最多1天、2天、3天、4天、5天、6天或1周、2周、3周、4周或2个月之内进行。在某些实施方式中,所述第二次测量在治疗开始后立即进行,或在其最多1天、2天、3天、4天、5天、6天或1周、2周、1个月、2个月、3个月、4个月、5个月、6个月、7个月、8个月、9个月、10个月、11个月或12个月之内进行。
在某些实施方式中,(a)snai1、phosphosmad2、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、phosphosmad3、尿蛋白和/或osterix的升高的水平分别高于参考群体中snai1、phosphosmad2、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、phosphosmad3、尿蛋白和/或osterix的水平约10%、20%、25%、30%、40%、50%、60%、70%、75%、80%、90%、100%、200%或500%;和/或(b)klotho、alpha-sma、myocd、actriia、axin2和/或sm22-alpha的降低的水平分别低于参考群体中klotho、alpha-sma、myocd、actriia、axin2和/或sm22-alpha的水平约10%、20%、25%、30%、40%、50%、60%、70%、75%、80%、90%或100%。
在某些实施方式中,(a)snai1、phosphosmad2、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、phosphosmad3、尿蛋白和/或osterix的升高的水平分别等于或约10%、20%、25%、30%、40%、50%、60%、70%、75%、80%、90%、100%、200%或500%高于参考群体中的前10%、前5%、前4%、前3%、前2%或前1%中snai1、phosphosmad2、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、phosphosmad3、尿蛋白和/或osterix的水平;(b)klotho、alpha-sma、myocd、actriia、axin2和/或sm22-alpha的降低的水平分别等于或约10%、20%、25%、30%、40%、50%、60%、70%、75%、80%、90%或100%低于参考群体中的后10%、后5%、后4%、后3%、后2%或后1%中klotho、alpha-sma、myocd、actriia、axin2和/或sm22-alpha的水平。
在某些实施方式中,(a)klotho、alpha-sma、myocd、actriia、axin2和/或sm22-alpha的升高的水平分别高于参考群体中klotho、alpha-sma、myocd、actriia、axin2和/或sm22-alpha的水平约10%、20%、25%、30%、40%、50%、60%、70%、75%、80%、90%、100%、200%或500%,和/或(b)snai1、phosphosmad2、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、phosphosmad3、尿蛋白和/或osterix的降低的水平分别低于参考群体snai1、phosphosmad2、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、phosphosmad3、尿蛋白和/或osterix的水平约10%、20%、25%、30%、40%、50%、60%、70%、75%、80%、90%或100%。
在某些实施方式中,(a)klotho、alpha-sma、myocd、actriia、axin2和/或sm22-alpha的升高的水平分别等于或约10%、20%、25%、30%、40%、50%、60%、70%、75%、80%、90%、100%、200%或500%高于参考群体的前10%、前5%、前4%、前3%、前2%或前1%中klotho、alpha-sma、myocd、actriia、axin2和/或sm22-alpha的水平;和/或(b)snai1、phosphosmad2、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、phosphosmad3、尿蛋白和/或osterix的降低的水平分别等于或约10%、20%、25%、30%、40%、50%、60%、70%、75%、80%、90%或100%低于参考群体的后10%、后5%、后4%、后3%、后2%或后1%中snai1、phosphosmad2、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、phosphosmad3、尿蛋白和/或osterix的水平。
在某些实施方式中,snai1、phosphosmad2、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、osterix、klotho、alpha-sma、myocd、phosphosmad3、尿蛋白、actriia、axin2和/或sm22-alpha的水平分别是snai1、phosphosmad2、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、osterix、klotho、alpha-sma、myocd、phosphosmad3、尿蛋白、actriia、axin2和/或sm22-alpha的蛋白质水平。在某些实施方式中,所述蛋白质水平通过酶联免疫吸附分析(elisa)来测定。在某些实施方式中,进行elisa,用(a)runx2-特异性抗体sc-390715(santacruz)来测定runx2水平;(b)用alp-特异性抗体sc-98652(santacruz)来测定alp水平;(c)snai1-特异性抗体sc-393172(santacruz)来测定snai1水平;(d)用phosphosmad2-特异性抗体sc-101801(santacruz)来测定phosphosmad2水平;(e)用dkk1-特异性抗体sc-374574(santacruz)来测定dkk1水平;(f)用col1a1-特异性抗体sc-8784(santacruz)来测定col1a1水平;(g)用激活素-特异性抗体a1594(sigmaaldrich)来测定激活素水平;(h)用bsap-特异性抗体sc-98652(santacruz)来测定bsap水平;(i)用ctx-特异性抗体abin1173415(antibodiesonline)来测定ctx水平;(j)用osterix-特异性抗体sc-22538(santacruz)来测定osterix水平;(k)用klotho-特异性抗体sc-22218(santacruz)来测定klotho水平;(l)用alpha-sma-特异性抗体sc-53142(santacruz)来测定alpha-sma水平;(m)用myocd-特异性抗体sc-21561(santacruz)来测定myocd水平;(n)用sm22-alpha-特异性抗体sc-271719(santacruz)来测定sm22-alpha水平;(o)用phosphosmad3-特异性抗体sc-11769(santacruz)来测定phosphosmad3水平;和/或(p)用actriia-特异性抗体ab135634(abcam)来测定actriia水平。
在某些实施方式中,snai1、dkk1、col1a1、激活素、runx2、alp、bsap、ctx、osterix、klotho、alpha-sma、myocd、phosphosmad3、phosphosmad3、尿蛋白、actriia、axin2和/或sm22-alpha的平分别是snai1、dkk1、col1a1、激活素、runx2,alp,bsap,ctx,osterix、klotho、alpha-sma、myocd、phosphosmad3、phosphosmad3、尿蛋白、actriia、axin2和/或sm22-alpha的mrna水平。在某些实施方式中,所述mrna水平通过定量逆转录聚合酶链式反应(qrt-pcr)来测定。在某些实施方式中,进行qrt-pcr,用(a)runx2-特异性引物(seqidno:48和49)来测定runx2水平;(b)用alp-特异性引物(seqidno:50和51)来测定alp水平;(c)用snai1-特异性引物(seqidno:78和79)来测定snai1水平;(d)用dkk1-特异性引物(seqidno:80和81)来测定dkk1水平;(e)用col1a1-特异性引物(seqidno:82和83)来测定col1a1水平;(f)用激活素-特异性引物(seqidno:84和85)来测定激活素水平;(g)用osterix-特异性引物(seqidno:52和53)来测定osterix水平;(h)用klotho-特异性引物(seqidno:54和55)来侧klotho水平;和/或(i)用sm22-alpha-特异性引物(seqidno:56和57)来测定sm22-alpha水平。
在某些实施方式中,snai1、phosphosmad2、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、osterix、klotho、sm22-alpha、myocd、phosphosmad3、尿蛋白、actriia、axin2、actriia、axin2和/或alpha-sma水平是组织中的。在某些实施方式中,所述组织是主动脉。在某些实施方式中,所述组织是肾脏。在某些实施方式中,所述组织是骨。在某些实施方式中,所述组织是血清。在优选的实施方式中,runx2、dkk1、alp、osterix、sm22-alpha、klotho、alpha-sma、myocd、actriia、axin2水平和/或活性是在主动脉中的。在优选的实施方式中,phosphosmad3、尿蛋白、phosphosmad2、actriia、axin2和col1a1水平和/或活性是在肾脏中的。在优选的实施方式中,所述激活素水平和/或活性是在血清中的。
在某些实施方式中,snai1、phosphosmad2、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、osterix、klotho、sm22-alpha、myocd、actriia、axin2和/或alpha-sma水平是主动脉中的。
在某些实施方案中,所述血管钙化是钙化性动脉粥样硬化、钙化的中层血管病变(也称为
在某些实施方式中,所述心血管疾病是与以下相关的疾病:血管钙化例如动脉粥样硬化、高脂血症、骨质疏松症、高血压、炎症、2型糖尿病、终末期肾病、所需截肢、弹性假黄瘤、先天性二尖瓣、风湿性心脏病、门静脉高压症或肝脏疾病。
在某些实施方式中,所述心血管疾病是继发于慢性肾病的。在某些实施方式中,所述慢性肾病是3、4或5期慢性肾病。在某些实施方式中,所述慢性肾病是慢性肾病矿物质和骨骼疾病。
在某些实施方式中,所述对象患有高周转性骨病,例如,高周转性肾性骨营养不良(rod)。
本文还提供的是一种治疗高周转性骨病,例如,高周转性rod的方法,包括向对象施用药学上有效量的actrii信号转导抑制剂。
在某些实施方式中,所述actrii信号转导抑制剂是包含选自以下构成的组的氨基酸序列的多肽:(a)90%相同于seqidno:2;(b)95%相同于seqidno:2;(c)98%相同于seqidno:2;(d)seqidno:2;(e)90%相同于seqidno:3;(f)95%相同于seqidno:3;(g)98%相同于seqidno:3;(h)seqidno:3;(i)90%相同于seqidno:6;(j)95%相同于seqidno:6;(k)98%相同于seqidno:6;(l)seqidno:6;(m)90%相同于seqidno:7;(n)95%相同于seqidno:7;(o)98%相同于seqidno:7;(p)seqidno:7;(q)90%相同于seqidno:12;(r)95%相同于seqidno:12;(s)98%相同于seqidno:12;(t)seqidno:12;(u)90%相同于seqidno:17;(v)95%相同于seqidno:17;(w)98%相同于seqidno:17;(x)seqidno:17;(y)90%相同于seqidno:20;(z)95%相同于seqidno:20;(aa)98%相同于seqidno:20;(bb)seqidno:20;(cc)90%相同于seqidno:21;(dd)95%相同于seqidno:21;(ee)98%相同于seqidno:21;以及(ff)seqidno:21。在某些实施方式中,所述actrii信号转导抑制剂是包含seqidno:7的氨基酸序列的多肽。在某些实施方式中,所述actrii信号转导抑制剂是由actriia的细胞外结构域和人igg1fc结构域组成的人源化的融合蛋白。
在某些实施方式中,所述actrii信号转导抑制剂是sotatercept(seqidno:7;参见,例如,章节9)。sotatercept是一种激活素配体陷阱,其在本文描述的方法中是有用的(参见章节8)。
在某些实施方式中,所述对象是人类。
7.附图简述
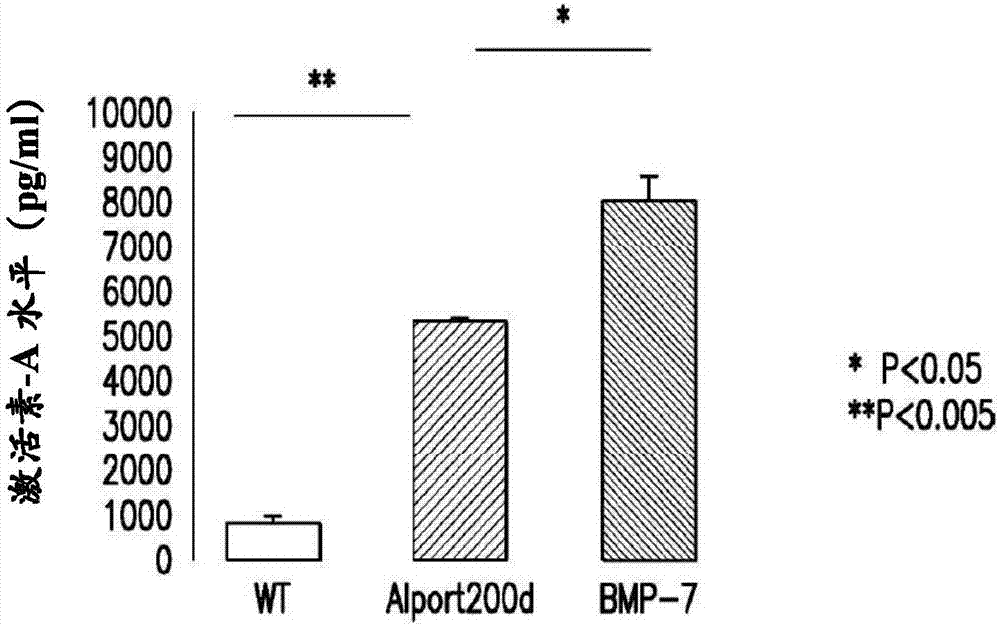
附图1a描绘了与野生型和假(sham)模型相比在肾病的间质性纤维化模型(ckd-3)中提高的激活素-a水平(pg/ml)。附图1b描绘了与野生型(wt)相比在肾病的aiports模型(aiport200d)中提高的激活素-a水平(pg/ml)以及在用bmp-7治疗时提高的激活素-a水平。
附图2描绘了与假的相比在ckd-3模型(ckd-3v)的肾脏和主动脉中提高的激活素a(抑制素beta)mrna水平。用mactriia-fc治疗降低了ckd-3模型中的激活素amrna(mactriia-fc)。
附图3a描绘了野生型小鼠主动脉中的actrii水平。附图3b描绘了在假治疗的小鼠主动脉中的actrii水平。附图3c描绘了与附图3a和/或附图3b相比在ckd-3模型的小鼠主动脉中提高的actrii水平。附图3d描绘了与附图3c相比在mactriia-fc治疗的ckd-3模型的小鼠主动脉中降低的actrii水平。
附图4a描绘了在有(ckd3+actrii-fc)和没有(ckd3+v)actrii信号转导抑制剂治疗时慢性肾病小鼠模型中runx2的mrna水平。附图4b描绘了在有(ckd3+actrii-fc)和没有(ckd3+v)actrii信号转导抑制剂治疗时慢性肾病小鼠模型中alp的mrna水平。附图4c描绘了在有(ckd3+actrii-fc)和没有(ckd3+v)actrii信号转导抑制剂治疗时慢性肾病小鼠模型中klotho的mrna水平。附图4d描绘了在有(ckd3+actrii-fc)和没有(ckd3+v)actrii信号转导抑制剂治疗时慢性肾病小鼠模型中心肌素(myocd)的mrna水平。附图4e描绘了在有(ckd3+actrii-fc)和没有(ckd3+v)actrii信号转导抑制剂治疗时慢性肾病小鼠模型中sm22-alpha(sm22α)的mrna水平。
附图4f描绘了与用单独的溶媒(ckd3+vehicle)治疗或伪治疗的ckd3相比,在用actrii信号转导抑制剂(ckd3+actrii-fc)治疗的ckd-3模型中肌动蛋白alpha-平滑肌、runx2、klotho、myocd和alpha-微管蛋白的蛋白质水平。
附图5a描绘了在用溶媒(veh.rx)治疗时ckd-3诱导的血管钙化。附图5b描绘了用actrii信号转导抑制剂(mactriia-fcrx)治疗时降低的ckd-3诱导的血管钙化。
附图6a描绘了与野生型(wt)、假的、用溶媒治疗的ckd-3模型(ckd-3veh)相比,钙水平的ckd-3诱导的提高(ckd-322wk)。用mactriia-fc治疗降低了ckd-3诱导的钙积累(mactriia-fc)。附图6b描绘了用actrii信号转导抑制剂(mactriia-fc)治疗的野生型小鼠(wt)、假治疗的小鼠(sham)、ckd-3小鼠模型(ckd-3)或小鼠模型ckd-3的骨量。附图6c描绘了用actrii信号转导抑制剂(mactriia-fc)治疗的野生型小鼠(wt)、假治疗的小鼠(sham)、ckd-3小鼠模型(ckd-3)或小鼠模型ckd-3的破骨细胞数目。附图6d描绘了用actrii信号转导抑制剂(mactriia-fc)治疗的野生型小鼠(wt)、假治疗的小鼠(sham)、ckd-3小鼠模型(ckd-3)或小鼠模型ckd-3的破骨细胞表面。
附图7a描绘了在gnz小鼠(stolleretal,genesis,2008)培育成内皮特异性tie2-cre(也称为“tek-cre”)小鼠中进行的细胞谱系跟踪的策略。附图7b描绘了假的小鼠中的内皮细胞谱系跟踪。附图7c描绘了ckd小鼠中的内皮细胞谱系跟踪。附图7d描绘了ckd小鼠中的内皮细胞谱系跟踪。
附图8描绘了对象分布。注意:“·”表示对象在基线和第225天有匹配的qct测量。“*”表示接受安慰剂的对象具有提高的血清促红细胞生成素水平,表明方案之外的促红细胞生成素施用。
附图9a描绘了在每个治疗类别中具有大于2%的股骨颈部皮层骨提高的对象百分比。附图9b描绘了在每个治疗组中有腰椎小梁骨质量的任何提高或降低的对象百分比。
附图10a描绘了每个治疗类别中总agatston得分改变的对象的百分比。附图10b描绘了每个治疗类别中平方根转化的总体积得分改变的对象的百分比。
附图11描绘了安慰剂(pbo)治疗的对象或用剂量0.3mg/kg(0.3)或0.5mg/kg(0.5)的actrii信号转导抑制剂治疗的对象的骨吸收生物标记物(ctx)变化的百分比。
附图12a表明用mactriia-fc(ckd-3r)以10mg/kg每周两次皮下地治疗的ckd-3小鼠对菊糖清除没有影响。附图12b表明用mactriia-fc(ckd-3r)以10mg/kg每周两次皮下地治疗的ckd-3小鼠对bun没有影响。附图12a和附图12b利用了带有ablativeckd的血管钙化模型,如章节9.4.1.1中描述的,来产生与称为ckd-3的人类ckd3期类似的降低的肾脏功能(溶媒治疗的为ckd-3v),通过菊糖清除和bun来估计,与wtc57b6小鼠(wt)相比具有gfr的70%降低。附图12c表明200天龄的col4α5缺陷小鼠(alport)具有与人类3-4期ckd相当的菊糖清除降低。*p<0.05。附图12d表明200天龄的col4α5缺陷小鼠(alport)具有与人类3-4期cdk相当的bun提高。*p<0.05。
附图13表明ckd提高循环中的激活素以及肾脏和主动脉的actriia表达。“wt”=野生型;“sham”=假治疗的小鼠;“ckd-3v”=用溶媒治疗的小鼠;“ckd-3r”=用mactriia-fc治疗的小鼠。附图13a描绘了在如章节9.4.1.1中描述的ldlr-/-高脂肪饲喂的ckd-3小鼠模型中通过ckd的循环激活素-a诱导。附图13b描绘了在如章节9.4.1.1中描述的alport’s综合征小鼠中ckd对循环激活素-a的诱导。附图13c表明小鼠肾脏和主动脉中的抑制素betaa表达(激活素-a由抑制素betaa基因的同二聚体形成)。附图13d表明肾脏匀浆中抑制素betaa的蛋白水平。1,2和3是指单个样品。附图13e描绘了主动脉actriia的免疫组织化学。在野生型(wt)和假操作的ldlr-/-高脂肪饲喂小鼠(sham)的主动脉中检测到actriia表达,其是在用溶媒(ckd-3v)或mactriia-fc(ckd-3mactriia-fc)治疗的ckd-3小鼠中刺激出的。比例尺是20μm。附图13f表明,与wt和sham小鼠相比,在ckd-3小鼠(用溶媒治疗的,ckd-3v;或用mactriia-fc治疗的,ckd-3r)中循环卵泡抑素水平没有改变。*p<0.05,***p<0.005。附图13g表明,与wt和sham小鼠相比,在ckd-3小鼠(用溶媒治疗的,ckd-3v;或用mactriia-fc治疗的,ckd-3r)中循环卵泡抑素样3(fstl3)水平没有改变。*p<0.05,***p<0.005。
附图14表明ckd刺激的内皮向间充质转变。附图14a描绘了小鼠繁育策略的图表。rosa26gnz敲入小鼠(gnz小鼠)具有带终止密码子的序列,其防止核定位的gfp-lacz报告物的表达(gnz)。当与在内皮细胞中表达cre重组酶(cre)的tek-cre小鼠繁育时,cre重组酶(cre)删除了侧翼有loxp的序列,内皮来源的所有细胞产生gnz报告物蛋白。附图14b到附图14d展现了使用dapi核染色,对于内皮细胞标志物cd31和gfp,tek-cre/gnz小鼠主动脉的双倍免疫染色。箭头指向双重染色的内皮细胞。在假操作的小鼠中(附图14b),仅内皮细胞显示了核和细胞质的gfp染色。在ckd3小鼠中,(附图14c和附图14d)除了内皮细胞之外,主动脉中层和外膜的细胞显现了gfp染色(箭头)。比例尺是20μm。附图14e描绘了与enmt相关的转录因子snai1(medici,d.,etal.,2008.molecularbiologyofthecell19:4875-4887.)的主动脉mrna水平,相比野生型(wt)小鼠,在75天龄的alport’s小鼠中提高。alpha微管蛋白充当加载对照。1和2是指单独的样品。
附图15描绘了在有ckd-3的ldlr-/-高脂肪饲喂小鼠中mactriia-fc对血管钙化的作用。附图15a描绘了来自溶媒-(ckd-3v)和mactriia-fc治疗的(ckd-3mactriia-fc)ckd-3小鼠的近端主动脉动脉粥样硬化斑块的茜素红染色的切片。附图15b描绘了小鼠的组中的主动脉钙水平:野生型(wt);假操作的ldlr-/-高脂肪饲喂(sham);在治疗的建立之时,在22周安乐死的ckd-3(ckd-3);从22到28周用溶媒治疗的ckd-3(ckd-3v);从22到28周用mactriia-fc、10mg/kg每周两次皮下治疗的ckd-3(ckd-3r)。方框代表中值(框中的线条),四分位数范围从25th到75th百分位。误差棒代表四分位数范围的1.5倍。各组用anovaholm-sidak方法进行比较,进行多重比较,p<0.05为显著差异水平。*p<0.02,每个组的n为8-12。
附图16表明降低的actriia信号转导对ckd刺激的心脏病的作用。附图16a表明ldlr-/-高脂肪饲喂小鼠中的ckd-3提高了心脏重量,与假治疗的小鼠相比,这在mactriia-fc治疗的组中是反转的。ckd-3-l是指用碳酸镧治疗的ckd-3小鼠。附图16b表明产生了主要在左心室的心脏肥大(中间),与sham小鼠(左侧)相比,这在mactriia-fc治疗的组(右侧)中被防止。三色染色,比例尺1mm。附图16c描绘了在更高放大率下的左室性肌细胞的三色染色,没有展现心脏纤维化的证据。比例尺20μm。
附图17展现了ldlr-/-高脂肪饲喂的ckd-3小鼠中ckd-3对血管硬化的作用,以及dkk1中和作用的缺乏。附图17a描绘了左颈总动脉的如早先的报道(wagenseil,j.e.,etal.,2009.circulationresearch104:1217-1224;wagenseil,j.e.,etal.,2005.ajp-heartandcirculatoryphysiology289:h1209-h1217.)进行的压力-直径关系。附图17b描绘了来自野生型(wt-28周)、假操作的(sham-28周)、ckd-3(28周)和用dkk1单克隆抗体治疗的ckd-3(dkk1mab-28周)小鼠的升主动脉。对于附图17,黑色代表wt或假操作的小鼠,而空心或灰色代表ckd-3小鼠。数值以平均值±标准偏差来呈现。对于颈动脉,n=5-6只小鼠,升主动脉为3-6只。
附图18展现了肾脏和主动脉中的actriia信号转导。附图18a描绘了来自假治疗的、ckd-3溶媒-(ckd-3v)和mactriia-fc治疗的(ckd-3r)小鼠的肾脏(左侧)和主动脉(右侧)的组织匀浆通过westerns测定的激活素信号转导。在肾脏组织匀浆中而不是在主动脉组织匀浆中激活素水平提高,alk4(acvr1b)和alk2(acvr1)1型受体存在于肾脏组织匀浆,而ckd-3不提高alk4磷酸化。alk4和alk1(acvrl1)存在于主动脉组织匀浆中。ckd-3提高了肾脏中而非主动脉中的smad2/3磷酸化,并提高了肾脏col1a1水平。mactriia-fcz治疗降低了肾脏phosphosmad2/3和col1a1水平。在主动脉中,ckd-3不仅对phosphosmad2/3水平没有影响,对phosphoerk1/2水平也没有影响。runx2水平通过ckd-3提高,而通过mactriia-fc归一化。附图18b描绘了ckd-3小鼠的肾脏中klothomrna表达的降低,以及通过mactriia-fc治疗对它的纠正。附图18c描绘了来自假治疗的、ckd-3溶媒和mactriia-fc治疗的小鼠(左侧)的肾脏和主动脉组织匀浆的westerns中通过dkk1蛋白表达来标记的wnt信号转导,以及ckd-3和mactriia-fc对血浆dkk1水平(右侧)的影响。
附图19描绘了患有3期ckd的患者(n=30)对比健康供体(n=10)的血浆激活素-a水平。通过使用商业的elisa试剂盒(r&dsystems,minneapolis,mn)一式两份测量样品来产生数据。分析的变异系数是2.7%。***p<0.002学生t检验。
附图20描绘了野生型小鼠(wt)、假治疗的小鼠(sham)、ckd-3小鼠(ckd-3v)或用mactriia-fc治疗的ckd-3小鼠(ckd-3r)中fgf-23的水平。
附图21a描绘了野生型小鼠(wt)、假操作的小鼠(sham)、用溶媒治疗的ckd-3小鼠(ckd-3v)或用mactriia-fc治疗的ckd-3小鼠(ckd-3r)中循环激活素a的水平。*表示p<0.005。附图21b描绘了假操作的小鼠(sham)、用溶媒治疗的ckd-3小鼠(ckd-3v)或用mactriia-fc治疗的ckd-3小鼠(ckd-3r)的成骨细胞数量/骨骼周长数/100mm。ckd-3vvs.ckd-3的p<0.05。附图21c描绘了假操作的小鼠(sham)、用溶媒治疗的ckd-3小鼠(ckd-3v)或用mactriia-fc治疗的ckd-3小鼠(ckd-3r)的成骨细胞表面/骨表面的百分比。ckd-3vvs.ckd-3的p<0.05。附图21d描绘了假操作的小鼠(sham)、用溶媒治疗的ckd-3小鼠(ckd-3v)或用mactriia-fc治疗的ckd-3小鼠(ckd-3r)的骨形成率/成骨细胞。ckd-3vvs.ckd-3的p<0.05。
附图22a描绘了在以标明的剂量用安慰剂或mactriia-fc治疗时,在研究的过程中的对象分布。y轴的上的每个数字代表单独的对象。附图22b描绘了在以标明的剂量用安慰剂或mactriia-fc治疗时,在对象的腹部主动脉的总agatston得分上有<15%的发展的对象比例。附图22c描绘了在以标明的剂量用安慰剂或mactriia-fc治疗时,在股骨颈部皮层bmd方面有>2%提高的对象的比例。
附图23a描绘了actriia的细胞外结构域与igg1的fc结构域的小鼠融合蛋白(mactriia-fc)的示意图。附图23b描绘了在ldlr-/-高脂肪饲喂小鼠中mactriia-fc对ckd-mbd的影响的实验设计。从12周(wks)龄开始,四个组中的小鼠饲喂高脂肪饮食。在12周进行假手术(so)或电灼皮层损伤(ec)。在14周,进行so或对侧肾切除(nx)。在生命的22周,研究10mg/kg皮下每周两次的溶媒治疗或mactriia-fc。wt野生型小鼠食物饮食为正常参考水平。sham,假操作的ldlr-/-高脂肪饲喂小鼠;ckd-3,在治疗开始时在22周研究以建立血管钙水平的ckd-3ldlr-/-高脂肪饲喂小鼠;ckd-3v,溶媒治疗的ckd-3ldlr-/-高脂肪饲喂小鼠;ckd-3r,mactriia-fc治疗的ldlr-/-高脂肪饲喂小鼠;wt、sham、ckd-3v和ckd-3r小鼠在28周龄处死。
附图24a描绘了通过westerns对主动脉组织匀浆中的actriia测定的、小鼠主动脉中actriia的表达。附图24b描绘了附图24a的免疫印迹定量。对于定量,n=4,**p<0.0l。附图24c描绘了sham小鼠的主动脉中actriia的免疫荧光检测。附图24d描绘了ckd-3小鼠的主动脉中actriia的免疫荧光检测。actriia在主动脉vsmc中表达,但在内皮细胞中没有检出。与sham相比,在ckd中vsmcactriia水平保持为可检测的。cd31(箭头)用作内皮细胞标志物。核用dapi染色。比例尺20μm。
附图25a显示了ckd-3引起成骨细胞蛋白质(runx2和碱性磷酸酶(alpl))的提高的mrna表达,以及降低水平的主动脉平滑肌细胞22α(tagln)这些全部被mactriia-fc的治疗反转。主动脉的心肌素(myocd)水平被ckd降低,但是不受mactriia-fc影响。附图25b描绘了主动脉组织匀浆中蛋白质的westerns。附图25c描绘了附图25b的westerns的免疫印迹定量。ckd引起主动脉的α-平滑肌细胞肌动蛋白的水平降低,以及成骨细胞的runx2的水平提高,其被mactriia-fc的治疗反转,但是心肌素水平没有改变。对于定量,n=4,**p<0.01。
附图26a描绘了在患有ckd-3的ldlr-/-高脂肪饲喂小鼠中ckd和actriia配体陷阱对主动脉钙化的影响,显示了用来自溶媒的茜素红对近端主动脉动脉粥样硬化斑块的染色切片。附图26b描绘了在患有ckd-3并用mactriia-fc治疗的ldlr-/-高脂肪饲喂小鼠中ckd和actriia配体陷阱对主动脉钙化的影响,如茜素红染色的近端主动脉动脉粥样硬化斑块所示。箭头表示内膜中的钙沉积(i);m-中层。比例尺100μm。附图26c描绘了小鼠的组中的主动脉钙水平:野生型(wt);假操作的ldlr-/-高脂肪饲喂(sham);在治疗的建立之时,在22周安乐死的ckd-3(ckd-3);从22到28周用溶媒治疗的ckd-3(ckd-3v);从22到28周用mactriia-fc、10mg/kg每周两次皮下治疗的ckd-3(ckd-3r)。方框代表中值(框中的线条),四分位数范围从25th到75th百分位。误差棒代表四分位数范围的1.5倍。l各组用anovaholm-sidak方法进行比较;进行多重比较;p<0.05作为显着差异水平。*p<0.02;每个组的n为8-12。
附图27a描绘了来自假治疗的、ckd-3溶媒和ckd-3mactriia-fc治疗的小鼠的主动脉组织匀浆的westerns的actriia信号转导分析。组织匀浆的免疫印迹来自每个组中动物的两条主动脉。在来自ckd-3小鼠的主动脉组织匀浆中actriia和激活素(抑制素β-a)水平降低。alk4(acvr1b)和alk1(acvrl1)1型受体存在于主动脉组织匀浆中。ckd-3降低了主动脉中的smad2/2磷酸化,其被mactriia-fc治疗提高。ckd-3降低了磷酸-erk1/2水平。runx2水平通过ckd-3提高,而通过mactriia-fc归一化。附图27b描绘了p-smad2/3免疫印迹定量,n=4,**p<0.01。
附图28a描绘了野生型小鼠的主动脉中beta-连环蛋白(catenin)表达的免疫荧光显微术。附图28b描绘了ckd小鼠的主动脉中beta-连环蛋白表达的免疫荧光显微术。血管平滑肌细胞中没有beta-连环蛋白的免疫荧光。来自ckd小鼠的主动脉的内皮中有beta-连环蛋白表达。箭头,内皮细胞中beta-连环蛋白和cd31的共同定位。比例尺20μm。附图28c描绘了主动脉的axin2mrna表达水平。附图28d描绘了来自sham、ckd-3v和ckd-3r治疗的小鼠的主动脉组织匀浆的westerns中,通过dkk1蛋白表达来标记的wnt信号转导的分析,以及免疫印迹定量,n=4。附图28e描绘了ckd-3v和mactriia-fc对血浆dkk1水平的影响。*p<0.05,**p<0.01。
附图29a描绘了mactriia-fc治疗对肾脏klothomrna水平的影响,表明ckd-3降低肾脏组织匀浆中的klotho基因表达水平,相比ckd-3v,mactriia-fc治疗显著地提高它们。*p<0.05,**p<0.01,***p<0.005。附图29b描绘了来自假治疗的、ckd-3溶媒和ckd-3mactriia-fc治疗的小鼠的肾脏组织匀浆的westerns的actriia信号转导分析。所有的免疫印迹是来自3或4个肾脏的组织匀浆的表示。actriia不受ckd-3或mactriia-fc的影响。激活素a(抑制素β-a)水平在ckd-3小鼠的肾脏组织匀浆中提高(定量在附图30a-b中显示),被mactriia-fc降低。alk4(acvr1b)和alk2(acvr1)1型受体存在于肾脏组织匀浆中,但是ckd-3v或ckd-3r不显著影响alk4的磷酸化。ckd-3提高了肾脏的smad2/3磷酸化,mactriia-fc治疗降低了肾脏的磷酸smad2/3。附图29c描绘了附图29b的免疫印迹定量),*p<0.01。
附图30a描绘了来自ckd-3vmactriia-fc治疗的小鼠的肾脏切片的三色染色。附图30b描绘了来自ckd-3vmactriia-fc治疗的小鼠的肾脏切片的三色染色。附图30c描绘了来自ckd-3vmactriia-fc治疗的小鼠的肾脏切片的三色染色。附图30d描绘了来自ckd-3mactriia-fc治疗的小鼠的肾脏切片的三色染色。间质性纤维化的区域通过箭头标出。ckd-3mactriia-fc治疗的小鼠的肾脏具有降低的间质性纤维化。比例尺50μm。整个肾脏冠状面的标记参见附图35,从其中采集了显微照片的切片。附图30e描绘了mactriia-fc对尿蛋白的影响。在ckd-3v小鼠中有显著的蛋白尿,这通过mactriia-fc治疗降低了,*p<0.05。
附图31a描绘了在动脉粥样硬化的ldlr-/-高脂肪饲喂的ckd-3小鼠中通过ckd对循环激活素-a的诱导。附图31b描绘了在如本文描述的alport’s综合征小鼠中ckd对循环激活素-a的诱导。附图31c描绘了小鼠肾脏中抑制素betaa(inhba)mrna表达(激活素-a是抑制素betaa的同二聚体形成的)。附图31d描绘了用于肾脏组织匀浆中的抑制素β-a的westerns。附图31e描绘了附图31d的免疫印迹定量,免疫印迹定量的n=6;*p<0.05、**p<0.01、***p<0.005。
附图32a显示了sham中的肾脏inhba免疫染色。附图32b显示了ckd-3溶媒小鼠中的肾脏inhba免疫染色。在sham小鼠中,偶尔的管周间质细胞表达激活素-a,但是在ckd-3小鼠中,更多的管周间质细胞在不同强度下对于激活素-a是阳性的。比例尺50μm。
附图33a和附图33b描绘了小鼠中类似于人3期肾病的慢性肾病。在小鼠模型中按照与人类ckd的分期类似的方式将ckd分期。如方法(章节9.10.1)中描述的带有消融性ckd的血管钙化模型用于产生与称为ckd-3的人类ckd3期类似的降低的肾脏功能(溶媒治疗的为ckd-3v),通过菊糖清除和bun来估计,与wtc57b6小鼠(wt)相比具有gfr的70%降低。10mg/kg每周两次皮下地用mactriia-fc治疗ckd-3小鼠(ckd-3r)对于菊糖清除或bun没有影响。
附图34描绘了来自tsuchida等(cellcomm.andsignaling,2009)的actriia信号转导的示意图。激活素、肌肉生长抑制素和gdf11结合ii型受体,actriia(主要对于激活素)和actriib(主要对于肌肉生长抑制素和gdf11)活化信号转导途径,包括通过smad2,3的典型途径。
附图35a和附图35b显示了ckd-3溶媒治疗的小鼠的肾脏(肾脏三色染色)。附图35c和附图35d显示了ckd-3mactriia-fc治疗的小鼠的肾脏(肾脏三色染色)。比例尺1mm。来自电灼损伤的皮层表面瘢痕由箭头标出。箭头指向了附图36中拍摄高功率显微照片的点。比例尺1mm。
附图36a描绘了与wt和sham小鼠相比,在ckd-3小鼠中循环卵泡抑素水平没有改变。附图36b描绘了与wt和sham小鼠相比,在ckd-3小鼠中循环卵泡抑素样3(fstl3)水平没有改变。
附图37描绘了ckd-3小鼠的组织中激活素受体相互作用蛋白arip1和arip2)的水平。arip1在ckd-3小鼠的残余肾脏中强烈表达,是arip2表达的两倍。arip1在ckd-3小鼠的主动脉中以低水平表达,而主动脉中的arip2表达是arip1的两倍。
8.详细说明
8.1概述
在一个方面,本文提供的是治疗和/或预防心血管疾病、血管钙化、与血管钙化相关和/或由血管钙化引起的心血管疾病、和/或与肾病相关和/或由肾病引起的心血管疾病、动脉硬化水平升高(例如,通过降低的血管顺应性所指示的)、和/或左心室肥大(lvh),包括与动脉硬化水平升高相关和/或由动脉硬化水平升高引起的心血管疾病和/或lvh的方法,其中所述方法包括向需要治疗和/或预防的对象施用actrii信号转导抑制剂(例如,激活素配体陷阱)。在某些实施方式中,所述对象是肾脏的对象。所述actrii信号转导抑制剂可以是actriia信号转导和/或actriib信号转导的抑制剂。
特别地,本文提供的是治疗和/或预防心血管疾病、血管钙化、与血管钙化相关和/或由血管钙化引起的心血管疾病、与肾病相关和/或由肾病引起的心血管疾病、动脉硬化水平升高和/或左心室肥大(lvh)的方法,使用snai1、phosphosmad2、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、osterix、klotho、alpha-sma、myocd、phosphosmad3、尿蛋白、actriia、axin2和/或sm22-alpha的水平和/或活性作为患者群体的指示、作为对象对用actrii信号转导抑制剂治疗和/或预防的响应性的指示、作为用actrii信号转导抑制剂治疗的效力的指示或作为用actrii信号转导抑制剂治疗的适当剂量的指示。snai1、phosphosmad2、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、osterix、klotho、alpha-sma、myocd、phosphosmad3、尿蛋白、actriia、axin2和/或sm22-alpha也可以用于鉴定用actrii信号转导抑制剂治疗和/或预防的疾病和/或状况。本文描述的方法中使用的actrii信号转导抑制剂可以是actriia信号转导和/或actriib信号转导的抑制剂,例如,本文描述的或本领域已知的任何抑制剂。在优选的实施方式中,actrii信号转导抑制剂是人源化的融合蛋白,其由actriia的细胞外结构域和人类igg1fc结构域组成(“actriia-fc,”例如,seqidno:7)。
本文提供的方法部分地基于以下发现,与野生型小鼠相比,在慢性肾病诱导的血管钙化的小鼠模型中,snai1、phosphosmad2、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、phosphosmad3、尿蛋白和osterix的水平提高,klotho、alpha-sma、myocd、actriia和sm22-alpha的水平降低。进一步的,不受理论的限制,mactriia-fc的配体捕获降低了慢性肾病小鼠模型(ldlr-/-小鼠,高脂肪饮食)中的血管钙化。如本文呈现的实施例中所显示的(参见章节9),用mactriia-fc治疗慢性肾病小鼠降低了血管钙化、降低了主动脉的钙水平、降低了phosphosmad3水平、降低了尿蛋白水平、降低了phosphosmad2水平、降低了dkk1水平、降低了runx2水平、降低了alp水平、降低了bsap水平、降低了ctx水平以及降低了osterix水平,并提高了klotho水平、提高了alpha-sma水平、提高了axin2水平和提高了sm22-alpha水平。此外,本文提供的方法部分地基于以下发现,在用mactriia-fc治疗时在慢性肾病小鼠中血管钙化的降低与dkk1、phosphosmad2、runx2、alp、bsap、ctx、phosphosmad3、尿蛋白和/或osterix水平的降低相关,以及与klotho、alpha-sma、axin2和/或sm22-alpha水平的提高相关(参见实施例,章节9)。合起来,本文呈现的数据表明,snai1、phosphosmad2、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、osterix、klotho、alpha-sma、myocd、phosphosmad3、尿蛋白、actriia、axin2和/或sm22-alpha水平可以鉴定哪些对象可能响应actriia-fc,和/或可以用于监测对actrii信号转导抑制剂的临床响应,和/或选择目标患者群体。本文呈现的数据还表明,actriia-fc(例如,mactriia-fc或actriia-hfc,例如seqidno:7)在治疗与慢性肾病相关的血管钙化中是有用的。另外,本文呈现的数据还表明,actriia-fc(例如,mactriia-fc或actriia-hfc例如seqidno:7)在治疗与snai1、phosphosmad2、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、phosphosmad3、尿蛋白和/或osterix的水平升高相关的疾病,或与klotho、alpha-sma、myocd、actriia和/或sm22-alpha的水平降低相关的疾病方面是有用的。最后,本文呈现的数据还表明,actriia-fc(例如,mactriia-fc或hactriia-hfc,例如seqidno:7)在降低主动脉粥样化中的钙沉积、降低主动脉钙水平、逆转ckd诱导的心脏重量增加、以及降低肾脏纤维化方面是有用的,因而,在治疗心血管疾病方面是有用的。
实施例(参见章节9)中说明的、本文描述的发现表明,检测snai1、phosphosmad2、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、osterix、klotho、alpha-sma、myocd、phosphosmad3、尿蛋白、actriia、axin2或sm22-alpha的水平和/或活性可以用作(i)对象的血管钙化程度的标志物(例如,血清标志物),(ii)测量对象对actrii信号转导抑制剂(例如actriia-fc)的响应的标志物,或(iii)评估治疗之后对象种actrii信号转导抑制剂(例如actriia-fc)的药效,其中所述对象是患有心血管疾病、血管钙化、与血管钙化相关和/或由血管钙化引起的心血管疾病、和/或与肾病相关和/或由肾病引起的心血管疾病的对象。因而,在某些实施方式中,snai1、phosphosmad2、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、osterix、klotho、alpha-sma、myocd、phosphosmad3、尿蛋白、axin2和/或sm22-alpha可以用于本文描述的方法,作为actriia-fc(例如,actriia-hfc,如seqidno:7)治疗的效力的指示物,和/或作为对actriia-fc(例如,actriia–hfc,如seqidno:7)治疗没有响应的指示物。此外,如本文描述的,snai1、phosphosmad2、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、osterix、klotho、alpha-sma、myocd、phosphosmad3、尿蛋白、actriia、axin2和/或sm22-alpha可以用作可靠的分子标志物来评估actriia-fc(例如,actriia-hfc,如seqidno:7)的时间-过程治疗效力。进一步,在具体的实施方式中,本文提供的是一种方法,其包括检测血液中snai1、phosphosmad2、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、osterix、klotho、alpha-sma、myocd、phosphosmad3、尿蛋白、actriia、axin2和/或sm22-alpha的水平和/或活性(例如,检测与受损的血管平滑肌细胞功能相关的疾病中的异常表达),以及以对snai1、phosphosmad2、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、osterix、klotho、alpha-sma、myocd、phosphosmad3、尿蛋白、actriia、axin2和/或sm22-alpha的活性和/或水平剂量依赖性的方式施用actrii信号转导抑制剂,例如,actriia-fc。
在某些实施方式中,所述actrii信号转导抑制剂是sotatercept(seqidno:7;参见,例如,章节9)。sotatercept是一种激活素配体陷阱,其在本文描述的方法中是有用的(参见章节8)。
8.2缩写
如本文使用的,“snai1”或“snai1”是指snail同源物1。参见,例如twiggandwilkie,1999,humgenet.105(4):320-326,genbanktm登记号nm_005985.3提供了示范性的人类snai1核酸序列。genbanktm登记号np_005976.2提供了示范性的人类snai1氨基酸序列。
如本文使用的,“phosphosmad3”是指针对decapentaplegic同源物3的磷酸化的母本(phosphorylatedmothersagainstdecapentaplegichomolog3)。参见,例如matsuzaki,2013,cytokinegrowthfactorrev,24(4):385-399。genbanktm登记号nm_005902.3提供了示范性的人类phosphosmad3核酸序列。genbanktm登记号np_005893.1提供了示范性的人类phosphosmad3氨基酸序列。
如本文使用的,“phosphosmad2”是指针对decapentaplegic同源物2的磷酸化的母本。参见,例如matsuzaki,2013,cytokinegrowthfactorrev,24(4):385-399。genbanktm登记号nm_001003652.3提供了示范性的人类phosphosmad2核酸序列。genbanktm登记号np_001003652.1提供了示范性的人类phosphosmad2氨基酸序列。
如本文使用的,“dkk1”是指dickkopf相关蛋白1。参见,例如fang,y.,etal.,2014.jamsocnephrol25:1760-1763。genbanktm登记号nm_012242.2提供了示范性的人类dkk1核酸序列。genbanktm登记号np_036374.1提供了示范性的人类dkk1氨基酸序列。
如本文使用的,“col1a1”是指1型胶原蛋白alpha1。参见,例如korkkoetal.,1998,am.j.hum.genet.,62:98-110。genbanktm登记号xm_005257059.2提供了示范性的人类col1a1核酸序列。genbanktm登记号xp_005257116.2提供了示范性的人类col1a1氨基酸序列。
如本文使用的,“runx2”是指runt相关的转录因子2。参见,例如komori,2010,advexpmedbiol,658:43-49。genbanktm登记号nm_001145920.2提供了示范性的人类runx2核酸序列。genbanktm登记号np_001139392.1提供了示范性的人类runx2氨基酸序列。
如本文使用的,“alp”或“alpl”是指碱性磷酸酶。如本文使用的,“bsap”是指骨骼特异性碱性磷酸酶。参见,例如martinsetal.,2013,bone,56(2):390-397。genbanktm登记号nm_000478.4提供了示范性的人类alp核酸序列。genbanktm登记号np_000469.3提供了示范性的人类alp氨基酸序列。
如本文使用的,“ctx”是指i型胶原蛋白的c-末端端肽。参见,例如rosenetal,2000,calciftissueint.66(2):100-103。
如本文使用的,“osterix”是指osterix,也称为sp7转录因子。参见,例如caoetal.,2005,cancerres.65(4):1124-1128。genbanktm登记号nm_001173467.2提供了示范性的人类osterix核酸序列。genbanktm登记号np_001166938.1提供了示范性的人类osterix氨基酸序列。
如本文使用的,“klotho”是指klotho。参见,例如matsumuraetal.1998,biochembiophysrescommun,242:626-630。genbanktm登记号nm_004795.3提供了示范性的人类klotho核酸序列。genbanktm登记号np_004786.2提供了示范性的人类klotho氨基酸序列。
如本文使用的,“alpha-sma”或“αsma”或“α-sma”是指alpha平滑肌肌动蛋白。参见,例如nowaketal.,1999,nat.genet.23:208-212。genbanktm登记号nm_001100.3提供了示范性的人类alpha-sma核酸序列。genbanktm登记号np_001091.1提供示范性的人类alpha-sma氨基酸序列。
如本文使用的,“myocd”是指心肌素。参见,例如imamuraetal.,2010,gene,464:1-10。genbanktm登记号nm_001146312.2提供了示范性的人类myocd核酸序列。genbanktm登记号np_001139784.1提供了示范性的人类myocd氨基酸序列。
如本文使用的,“sm22-alpha”或“sm22α”或“sm22-α”是指平滑肌蛋白22alpha,也称为“transgelin”、“tagln”或“tagln1”。参见,例如camoretti-mercado,1998,genomics,49:452-457。genbanktm登记号nm_001001522.1提供了示范性的人类sm22-alpha核酸序列。genbanktm登记号np_001001522.1提供了示范性的人类sm22-alpha氨基酸序列。
如本文使用的,“actrii”是指激活素ii型受体。如本文使用的,“actriia”是指激活素iia型受体。参见,例如mathewsandvale,1991,cell65:973-982。genbanktm登记号nm_001278579.1提供了示范性的人类actriia核酸序列。genbanktm登记号np_001265508.1提供了示范性的人类actriia氨基酸序列。如本文使用的,“actriib”是指激活素iib型受体。参见,例如attisanoetal.,1992,cell68:97-108。genbanktm登记号nm_001106.3提供了示范性的人类actriib核酸序列。genbanktm登记号np_001097.2提供了示范性的人类actriib氨基酸序列。
如本文使用的,“axin2”是指轴抑制剂2(axisinhibitor2)。genbanktm登记号nm_004655.3提供了示范性的人类axin2核酸序列。genbanktm登记号np_004646.3提供了示范性的人类氨基酸序列。
如本文使用的,“mactriia-fc”或“actriia-mfc”是指小鼠激活素iia型受体-igg1融合蛋白。参见,例如,美国专利no.8,173,601。如本文使用的,“mactriib-fc”或“actriib-mfc”是指小鼠激活素iib型受体-igg1融合蛋白。参见,例如,美国专利no.8,173,601。如本文使用的,““hactriia-fc”或“actriia-hfc”是指人类激活素iia型受体-igg1融合蛋白。参见,例如,美国专利no.8,173,601。如本文使用的,“hactriib-fc”或“actriib-hfc”是指人类激活素iib型受体-igg1融合蛋白。参见,例如,美国专利no.8,173,601。
如本文使用的,“lvh”是指左心室肥大。
8.3治疗和/或预防的方法
8.3.1心血管疾病和/或血管钙化
在某些实施方式中,本文提供的是治疗和/或预防对象的心血管疾病、血管钙化、与血管钙化相关和/或由血管钙化引起的心血管疾病、与动脉硬化水平升高相关和/或由动脉硬化水平升高引起的心血管疾病、动脉硬化水平升高、左心室肥大、与左心室肥大相关和/或由左心室肥大引起的心血管疾病、和/或与肾病相关和/或由肾病引起的心血管疾病,包括向所述对象施用药学上有效剂量的actrii信号转导抑制剂(例如,激活素配体陷阱)。在某些实施方式中,所述对象是肾脏的对象。在某些其他实施方式中,所述对象被诊断为患有慢性肾病-矿物质骨骼失调。在某些其他实施方式中,所述对象没有被诊断为患有慢性肾病-矿物质骨骼失调。
在某些实施方式中,所述对象具有与参考群体中runx2的水平和/或活性相比升高的runx2水平和/或活性,与参考群体中alp的水平和/或活性相比升高的alp水平和/或活性,与参考群体中snai1的水平和/或活性相比升高的snai1水平和/或活性,与参考群体中phosphosmad2的水平和/或活性相比升高的phosphosmad2水平和/或活性,与参考群体中中phosphosmad3的水平和/或活性相比升高的phosphosmad3水平和/或活性,与参考群体中中尿蛋白的水平和/或活性相比升高的尿蛋白水平和/或活性,与参考群体中中dkk1的水平和/或活性相比升高的dkk1水平和/或活性,与参考群体中中激活素(例如,游离激活素)的水平和/或活性相比升高的激活素(例如,游离激活素)水平和/或活性,与参考群体中col1a1的水平和/或活性相比升高的col1a1水平和/或活性,与参考群体中bsap的水平和/或活性相比升高的bsap水平和/或活性,与参考群体中ctx的水平和/或活性相比升高的ctx水平和/或活性,与参考群体中osterix的水平和/或活性相比升高的osterix水平和/或活性,与参考群体中klotho的水平和/或活性相比降低的klotho水平和/或活性,与参考群体中alpha-sma的水平和/或活性相比降低的alpha-sma水平和/或活性,与参考群体中myocd的水平和/或活性相比降低的myocd水平和/或活性,与参考群体中sm22-alpha的水平和/或活性相比降低的sm22-alpha水平和/或活性;和/或与参考群体中actriia的水平和/或活性相比降低的actriia水平和/或活性。
在某些实施方式中,所述对象具有与所述对象中在先的runx2水平和/或活性相比升高的runx2水平和/或活性,与所述对象中在先的alp水平和/或活性相比升高的alp水平和/或活性,与所述对象中在先的snai1水平和/或活性相比升高的snai1水平和/或活性,与所述对象中在先的phosphosmad2水平和/或活性相比升高的phosphosmad2水平和/或活性,与所述对象中在先的phosphosmad3水平和/或活性相比升高的phosphosmad3水平和/或活性,与所述对象中在先的尿蛋白水平和/或活性相比升高的尿蛋白水平和/或活性,与所述对象中在先的dkk1水平和/或活性相比升高的dkk1水平和/或活性,与所述对象中在先的激活素(例如,游离激活素)水平和/或活性相比升高的激活素(例如,游离激活素)水平和/或活性,与所述对象中在先的col1a1水平和/或活性相比升高的col1a1水平和/或活性,与所述对象中在先的bsap水平和/或活性相比升高的bsap水平和/或活性,与所述对象中在先的ctx水平和/或活性相比升高的ctx水平和/或活性,与所述对象中在先的osterix水平和/或活性相比升高的osterix水平和/或活性,与所述对象中在先的klotho水平和/或活性相比降低的klotho水平和/或活性,与所述对象中在先的alpha-sma水平和/或活性相比降低的alpha-sma水平和/或活性,与所述对象中在先的myocd水平和/或活性相比降低的myocd水平和/或活性,与所述对象中在先的actriia水平和/或活性相比降低的actriia水平和/或活性,和/或与所述对象中在先的sm22-alpha水平和/或活性相比降低的sm22-alpha水平和/或活性。在某些实施方式中,所述对象中在先的runx2水平和/或活性、所述对象中在先的alp水平和/或活性、所述对象中在先的snai1水平和/或活性、所述对象中在先的phosphosmad2水平和/或活性、所述对象中在先的phosphosmad3水平和/或活性、所述对象中在先的尿蛋白水平和/或活性、所述对象中在先的dkk1水平和/或活性、所述对象中在先的激活素(例如,游离激活素)水平和/或活性、所述对象中在先的col1a1水平和/或活性、所述对象中在先的bsap水平和/或活性、所述对象中在先的ctx水平和/或活性、所述对象中在先的osterix水平和/或活性、所述对象中在先的klotho水平和/或活性、所述对象中在先的alpha-sma水平和/或活性、所述对象中在先的myocd水平和/或活性、所述对象中在先的actriia水平和/或活性、所述对象中在先的sm22-alpha水平和/或活性是(i)心血管疾病;(ii)血管钙化;(iii)与血管钙化相关和/或由血管钙化引起的心血管疾病;(iv)与肾病相关和/或由肾病引起的心血管疾病;(v)动脉硬化水平升高;和/或左心室肥大(lvh)的症状发作或诊断之前1、2、3、4、5、6、8、10、12、18、24或48个月的相应水平。
在某些实施方式中,所述对象根据8.3.4中描述的方法治疗。在某些实施方式中,所述对象的血管钙化通过如章节8.6中描述的测定agatston评分来分析。
在某些实施方式中,用本文提供的方法治疗的对象具有如章节8.6中描述的snai1、phosphosmad2、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、osterix、klotho、alpha-sma、myocd、phosphosmad3、尿蛋白、actriia、axin2和/或sm22-alpha的水平和/或活性。因而,在某些具体的实施方式中,本文提供的方法包括(i)根据如章节8.6中描述的snai1、phosphosmad2、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、osterix、klotho、alpha-sma、myocd、phosphosmad3、尿蛋白、actriia和/或sm22-alpha的水平和/或活性选择对象;和(ii)施用药学上有效剂量的actrii信号转导抑制剂(例如,激活素配体陷阱)。在具体的实施方式中,所述对象患有心血管疾病。在具体的实施方式中,所述对象患有血管钙化。在具体的实施方式中,所述对象患有与血管钙化相关和/或由血管钙化引起的心血管疾病。在具体的实施方式中,所述对象患有与肾病相关和/或由肾病引起的心血管疾病。在具体的实施方式中,所述对象患有肾病。在某些其他实施方式中,所述对象被诊断为患有慢性肾病-矿物质骨骼失调。在某些其他实施方式中,所述对象没有被诊断为患有慢性肾病-矿物质骨骼失调。在某些实施方式中,所述对象的血管钙化通过如章节8.6中描述的测定agatston评分来分析。在具体的实施方式中,所述对象被诊断患有动脉硬化水平升高。在具体的实施方式中,所述对象被诊断患有lvh。在具体的实施方式中,所述对象患有与动脉硬化水平升高相关和/或由动脉硬化水平升高引起的心血管疾病。在具体的实施方式中,所述对象患有与lvh相关和/或由lvh引起的心血管疾病。
在某些实施方式中,snai1、phosphosmad2、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、osterix、klotho、alpha-sma、myocd、phosphosmad3、尿蛋白、actriia、axin2和/或sm22-alpha的水平和/或活性如章节8.6中描述的测定。在某些实施方式中,snai1、phosphosmad2、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、osterix、klotho、alpha-sma、myocd、phosphosmad3、尿蛋白、actriia、axin2和/或sm22-alpha的水平和/或活性分别是snai1、phosphosmad2、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、osterix、klotho、alpha-sma、myocd、phosphosmad3、尿蛋白、actriia、axin2和/或sm22-alpha的蛋白质水平和/或活性。在某些实施方式中,snai1、phosphosmad2、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、osterix、klotho、alpha-sma、myocd、phosphosmad3、尿蛋白、actriia、axin2和/或sm22-alpha的水平和/或活性分别是snai1、phosphosmad2、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、osterix、klotho、alpha-sma、myocd、phosphosmad3、尿蛋白、actriia、axin2和/或sm22-alpha的mrna水平和/或活性。在某些实施方式中,snai1、phosphosmad2、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、osterix、klotho、sm22-alpha、myocd和/或actriia、axin2、alpha-sma水平是在组织中的。在某些实施方式中,所述组织是主动脉。在某些实施方式中,所述组织是肾脏。在某些实施方式中,所述组织是骨骼。在某些实施方式中,所述组织是血清。在优选的实施方式中,runx2、dkk1、alp、osterix、sm22-alpha、klotho、alpha-sma、myocd、actriia、axin2水平和/或活性是在主动脉中的。在优选的实施方式中,phosphosmad2、phosphosmad3、尿蛋白、actriia、axin2和col1a1的水平和/或活性是在肾脏中的。在优选的实施方式中,所述激活素水平和/或活性是在血清中的。在某些实施方式中,相对于参考群体,激活素的水平在所述对象中升高。在某些实施方式中,所述对象中卵泡抑素的水平约等于参考群体中卵泡抑素的水平。
在某些实施方式中,所述参考群体是章节8.6中描述的群体。在某些实施方式中,所述对象是章节8.4中描述的对象。
在某些实施方式中,所述actrii信号转导抑制剂是actriia-fc,例如actriia-hfc(例如,seqidno:7)。在某些实施方式中,所述actrii信号转导抑制剂是如章节8.5中描述的actrii信号转导抑制剂。
在某些实施方式中,所述药学上有效的剂量是如章节8.7中描述的剂量。在某些实施方式中,所述药学上有效的剂量是初始剂量。在某些实施方式中,所述药学上有效的剂量以如章节8.7中描述的频率施用。在某些实施方式中,所述药学上有效的剂量如章节8.7中描述的施用。
在某些实施方式中,如章节8.8中描述的,本文提供的方法与第二药学活性试剂组合使用。
在某些实施方式中,在心血管疾病或慢性肾病的上下文中“治疗(treat)”、“治疗(treatment)”或“治疗(treating)”分别包括改善心血管疾病或慢性肾病的至少一种症状。
本领域技术人员将认识到,runx2、alp、snai1、phosphosmad2、dkk1、col1a1、激活素、bsap、ctx、osterix、klotho、alpha-sma、myocd、actriia、axin2、sm22-alpha、phosphosmad3和尿蛋白的水平和/或活性可以分别与相应参考群体中的水平和/或活性比较。因而,在某些实施方式中,runx2、alp、snai1、phosphosmad2、dkk1、col1a1、激活素、bsap、ctx、osterix、klotho、alpha-sma、myocd、sm22-alpha、phosphosmad3、actriia、axin2和尿蛋白的水平和/或活性与相应参考群体中它们的水平和/或活性比较。因而,在某些实施方式中,runx2、alp、snai1、phosphosmad2、dkk1、col1a1、激活素、bsap、ctx、osterix、klotho、alpha-sma、myocd、sm22-alpha、phosphosmad3、actriia、axin2和尿蛋白的两种的水平和/或活性与相应参考群体中它们的水平和/或活性比较。因而,在某些实施方式中,runx2、alp、snai1、phosphosmad2、dkk1、col1a1、激活素、bsap、ctx、osterix、klotho、alpha-sma、myocd、sm22-alpha、phosphosmad3、actriia、axin2和尿蛋白的三种的水平和/或活性与相应参考群体中它们的水平和/或活性比较。因而,在某些实施方式中,runx2、alp、snai1、phosphosmad2、dkk1、col1a1、激活素、bsap、ctx、osterix、klotho、alpha-sma、myocd、sm22-alpha、phosphosmad3、actriia、axin2和尿蛋白的三种的水平和/或活性与相应参考群体中它们的水平和/或活性比较。因而,在某些实施方式中,runx2、alp、snai1、phosphosmad2、dkk1、col1a1、激活素、bsap、ctx、osterix、klotho、alpha-sma、myocd、sm22-alpha、phosphosmad3、actriia、axin2和尿蛋白的四种的水平和/或活性与相应参考群体中它们的水平和/或活性比较。因而,在某些实施方式中,runx2、alp、snai1、phosphosmad2、dkk1、col1a1、激活素、bsap、ctx、osterix、klotho、alpha-sma、myocd、sm22-alpha、phosphosmad3、actriia、axin2和尿蛋白的五种的水平和/或活性与相应参考群体中它们的水平和/或活性比较。因而,在某些实施方式中,runx2、alp、snai1、phosphosmad2、dkk1、col1a1、激活素、bsap、ctx、osterix、klotho、alpha-sma、myocd、sm22-alpha、phosphosmad3、actriia、axin2和尿蛋白的六种的水平和/或活性与相应参考群体中它们的水平和/或活性比较。因而,在某些实施方式中,runx2、alp、snai1、phosphosmad2、dkk1、col1a1、激活素、bsap、ctx、osterix、klotho、alpha-sma、myocd、sm22-alpha、phosphosmad3、actriia、axin2和尿蛋白的七种的水平和/或活性与相应参考群体中它们的水平和/或活性比较。因而,在某些实施方式中,runx2、alp、snai1、phosphosmad2、dkk1、col1a1、激活素、bsap、ctx、osterix、klotho、alpha-sma、myocd、sm22-alpha、phosphosmad3、actriia、axin2和尿蛋白的八种的水平和/或活性与相应参考群体中它们的水平和/或活性比较。因而,在某些实施方式中,runx2、alp、snai1、phosphosmad2、dkk1、col1a1、激活素、bsap、ctx、osterix、klotho、alpha-sma、myocd、sm22-alpha、phosphosmad3、actriia、axin2和尿蛋白的九种的水平和/或活性与相应参考群体中它们的水平和/或活性比较。因而,在某些实施方式中,runx2、alp、snai1、phosphosmad2、dkk1、col1a1、激活素、bsap、ctx、osterix、klotho、alpha-sma、myocd、sm22-alpha、phosphosmad3、actriia、axin2和尿蛋白的十种的水平和/或活性与相应参考群体中它们的水平和/或活性比较。因而,在某些实施方式中,runx2、alp、snai1、phosphosmad2、dkk1、col1a1、激活素、bsap、ctx、osterix、klotho、alpha-sma、myocd、sm22-alpha、phosphosmad3、actriia、axin2和尿蛋白的十一种的水平和/或活性与相应参考群体中它们的水平和/或活性比较。因而,在某些实施方式中,runx2、alp、snai1、phosphosmad2、dkk1、col1a1、激活素、bsap、ctx、osterix、klotho、alpha-sma、myocd、sm22-alpha、phosphosmad3、actriia、axin2和尿蛋白的十二种的水平和/或活性与相应参考群体中它们的水平和/或活性比较。因而,在某些实施方式中,runx2、alp、snai1、phosphosmad2、dkk1、col1a1、激活素、bsap、ctx、osterix、klotho、alpha-sma、myocd、sm22-alpha、phosphosmad3、actriia、axin2和尿蛋白的十三种的水平和/或活性与相应参考群体中它们的水平和/或活性比较。因而,在某些实施方式中,runx2、alp、snai1、phosphosmad2、dkk1、col1a1、激活素、bsap、ctx、osterix、klotho、alpha-sma、myocd、sm22-alpha、phosphosmad3、actriia、axin2和尿蛋白的十四种的水平和/或活性与相应参考群体中它们的水平和/或活性比较。因而,在某些实施方式中,runx2、alp、snai1、phosphosmad2、dkk1、col1a1、激活素、bsap、ctx、osterix、klotho、alpha-sma、myocd、sm22-alpha、phosphosmad3、actriia、axin2和尿蛋白的十五种的水平和/或活性与相应参考群体中它们的水平和/或活性比较。因而,在某些实施方式中,runx2、alp、snai1、phosphosmad2、dkk1、col1a1、激活素、bsap、ctx、osterix、klotho、alpha-sma、myocd、sm22-alpha、phosphosmad3、actriia、axin2和尿蛋白的十六种的水平和/或活性与相应参考群体中它们的水平和/或活性比较。因而,在某些实施方式中,runx2、alp、snai1、phosphosmad2、dkk1、col1a1、激活素、bsap、ctx、osterix、klotho、alpha-sma、myocd、sm22-alpha、phosphosmad3、actriia、axin2和尿蛋白的十七种的水平和/或活性与相应参考群体中它们的水平和/或活性比较。因而,在某些实施方式中,runx2、alp、snai1、phosphosmad2、dkk1、col1a1、激活素、bsap、ctx、osterix、klotho、alpha-sma、myocd、sm22-alpha、phosphosmad3、actriia、axin2和尿蛋白的每一种的水平和/或活性与相应参考群体中它们的水平和/或活性比较。
8.3.2与snai1、phosphosmad2、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、osterix、klotho、alpha-sma、myocd、phosphosmad3、尿蛋白、actriia、axin2和/或sm22-alpha相关的疾病
在某些实施方式中,本文提供的是治疗和/或预防与snai1、phosphosmad2、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、osterix、klotho、alpha-sma、myocd、phosphosmad3、尿蛋白、actriia、axin2和/或sm22-alpha相关的一种或更多种疾病的方法,包括向对象施用药学上有效剂量的actrii信号转导抑制剂(例如,激活素配体陷阱)。
在某些实施方式中,所述对象是章节8.4中描述的对象。
在某些实施方式中,所述actrii信号转导抑制剂是actriia-fc,例如actriia-hfc(例如,seqidno:7)。在某些实施方式中,所述actrii信号转导抑制剂是如章节8.5中描述的actrii信号转导抑制剂。
在某些实施方式中,所述药学上有效的剂量是如章节8.7中描述的剂量。在某些实施方式中,所述药学上有效的剂量是初始剂量。在某些实施方式中,所述药学上有效的剂量以如章节8.7中描述的频率施用。在某些实施方式中,所述药学上有效的剂量如章节8.7中描述的施用。在某些实施方式中,所述药学上有效的剂量取决于本文描述的某些生物标记物的水平和/或活性来调整。
在某些实施方式中,如章节8.8中描述的,本文提供的方法与第二药学活性试剂组合使用。
8.3.3慢性肾病-矿物质/骨骼失调
在某些实施方式中,本文提供的是治疗对象的慢性肾病-矿物质骨骼失调的方法,包括向所述对象施用药学上有效剂量的actrii信号转导抑制剂(例如,激活素配体陷阱)。在某些实施方式中,提供的是降低对象中的骨吸收的方法,包括向所述对象施用药学上有效剂量的actrii信号转导抑制剂。在某些实施方式中,所述对象患有心血管疾病。在某些实施方式中,所述对象患有血管钙化。在某些实施方式中,所述对象患有与血管钙化相关和/或由血管钙化引起的心血管疾病。在某些实施方式中,所述对象患有与肾病相关和/或由肾病引起的心血管疾病。在某些实施方式中,所述对象是肾脏的对象。在某些其他实施方式中,所述对象被诊断为患有慢性肾病-矿物质骨骼失调。在某些其他实施方式中,所述对象没有被诊断为患有慢性肾病-矿物质骨骼失调。
在某些实施方式中,所述对象具有与参考群体中runx2的水平和/或活性相比升高的runx2水平和/或活性,与参考群体中alp的水平和/或活性相比升高的alp水平和/或活性,与参考群体中snai1的水平和/或活性相比升高的snai1水平和/或活性,与参考群体中phosphosmad2的水平和/或活性相比升高的phosphosmad2水平和/或活性,与参考群体中phosphosmad3的水平和/或活性相比升高的phosphosmad3水平和/或活性,与参考群体中尿蛋白的水平和/或活性相比升高的尿蛋白水平和/或活性,与参考群体中dkk1的水平和/或活性相比升高的dkk1水平和/或活性,与参考群体中col1a1的水平和/或活性相比升高的col1a1水平和/或活性,与参考群体中激活素(例如,游离激活素)的水平和/或活性相比升高的激活素(例如,游离激活素)水平和/或活性,与参考群体中bsap的水平和/或活性相比升高的bsap水平和/或活性,与参考群体中ctx的水平和/或活性相比升高的ctx水平和/或活性,与参考群体中osterix的水平和/或活性相比升高的osterix水平和/或活性,与参考群体中klotho的水平和/或活性相比降低的klotho水平和/或活性,与参考群体中alpha-sma的水平和/或活性相比降低的alpha-sma水平和/或活性,与参考群体中myocd的水平和/或活性相比降低的myocd水平和/或活性,与参考群体中actriia的水平和/或活性相比降低的actriia水平和/或活性,和/或与参考群体中sm22-alpha的水平和/或活性相比降低的sm22-alpha水平和/或活性。在某些实施方式中,snai1、phosphosmad2、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、osterix、klotho、sm22-alpha、myocd、phosphosmad3、尿蛋白、actriia、axin2、actriia、axin2和/或alpha-sma水平是组织中的。在某些实施方式中,所述组织是主动脉。在某些实施方式中,所述组织是肾脏。在某些实施方式中,所述组织是骨骼。在某些实施方式中,所述组织是血清。在优选的实施方式中,runx2、dkk1、alp、osterix、sm22-alpha、klotho、alpha-sma、myocd和/或actriia水平和/或活性是在主动脉中的。在优选的实施方式中,phosphosmad2、phosphosmad3、尿蛋白和col1a1和/或actriia水平和/或活性是在肾脏中的。在优选的实施方式中,所述激活素水平和/或活性是在血清中的。在某些实施方式中,snai1、phosphosmad2、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、osterix、klotho、sm22-alpha、myocd、actriia和/或alpha-sma水平是在主动脉中的。
在某些实施方式中,所述对象具有与对象中在先的runx2水平和/或活性相比升高的runx2水平和/或活性,与对象中在先的alp水平和/或活性相比升高的alp水平和/或活性,与对象中在先的snai1水平和/或活性相比升高的snai1水平和/或活性,与对象中在先的phosphosmad2水平和/或活性相比升高的phosphosmad2水平和/或活性,与对象中在先的phosphosmad3水平和/或活性相比升高的phosphosmad3水平和/或活性,与对象中在先的尿蛋白水平和/或活性相比升高的尿蛋白水平和/或活性,与对象中在先的dkk1水平和/或活性相比升高的dkk1水平和/或活性,与对象中在先的激活素(例如,游离激活素)水平和/或活性相比升高的激活素(例如,游离激活素)水平和/或活性,与所述对象中在先的col1a1水平和/或活性相比升高的col1a1水平和/或活性,与所述对象中在先的bsap水平和/或活性相比升高的bsap水平和/或活性,与所述对象中在先的ctx水平和/或活性相比升高的ctx水平和/或活性,与所述对象中在先的osterix水平和/或活性相比升高的osterix水平和/或活性,与所述对象中在先的klotho水平和/或活性相比降低的klotho水平和/或活性,与所述对象中在先的alpha-sma水平和/或活性相比降低的alpha-sma水平和/或活性,与所述对象中在先的myocd水平和/或活性相比降低的myocd水平和/或活性,与所述对象中在先的actriia水平和/或活性相比降低的actriia水平和/或活性,和/或与所述对象中在先的sm22-alpha水平和/或活性相比降低的sm22-alpha水平和/或活性。在某些实施方式中,所述对象中在先的runx2水平和/或活性、所述对象中在先的alp水平和/或活性、所述对象中在先的snai1水平和/或活性、所述对象中在先的phosphosmad2水平和/或活性、所述对象中在先的phosphosmad3水平和/或活性、所述对象中在先的尿蛋白水平和/或活性、所述对象中在先的dkk1水平和/或活性、所述对象中在先的激活素(例如,游离激活素)水平和/或活性、所述对象中在先的col1a1水平和/或活性、所述对象中在先的bsap水平和/或活性、所述对象中在先的ctx水平和/或活性、所述对象中在先的osterix水平和/或活性、所述对象中在先的klotho水平和/或活性、所述对象中在先的alpha-sma水平和/或活性、所述对象中在先的myocd水平和/或活性、所述对象中在先的actriia水平和/或活性、所述对象中在先的sm22-alpha水平和/或活性是ckd-mbd的症状发作或诊断之前1、2、3、4、5、6、8、10、12、18、24或48个月的相应水平。
在某些实施方式中,所述对象根据章节8.3.4中描述的方法治疗。在某些实施方式中,所述对象的血管钙化通过如章节8.6中描述的测定agatston评分来分析。
在某些实施方式中,用本文提供的方法治疗的对象具有如章节8.6中描述的snai1、phosphosmad2、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、osterix、klotho、alpha-sma、myocd、phosphosmad3、尿蛋白、actriia、axin2和/或sm22-alpha的水平和/或活性。因而,在某些具体的实施方式中,本文提供的方法包括(i)根据如章节8.6中描述的snai1、phosphosmad2、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、osterix、klotho、alpha-sma、myocd、phosphosmad3、尿蛋白、actriia和/或sm22-alpha的水平和/或活性选择对象;和(ii)施用药学上有效剂量的actrii信号转导抑制剂(例如,激活素配体陷阱)。在具体的实施方式中,所述对象患有心血管疾病。在具体的实施方式中,所述对象患有血管钙化。在具体的实施方式中,所述对象患有与血管钙化相关和/或由血管钙化引起的心血管疾病。在具体的实施方式中,所述对象患有与肾病相关和/或由肾病引起的心血管疾病。在具体的实施方式中,所述对象患有肾病。在某些其他实施方式中,所述对象被诊断为患有慢性肾病-矿物质骨骼失调。在某些其他实施方式中,所述对象没有被诊断为患有慢性肾病-矿物质骨骼失调。在具体的实施方式中,所述对象患有动脉硬化水平升高。在具体的实施方式中,所述对象患有与动脉硬化水平升高相关和/或由动脉硬化水平升高引起的心血管疾病。在具体的实施方式中,所述对象患有lvh。在具体的实施方式中,所述对象患有与lvh相关和/或由lvh引起的心血管疾病。
在某些实施方式中,snai1、phosphosmad2、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、osterix、klotho、alpha-sma、myocd、phosphosmad3、尿蛋白、actriia、axin2和/或sm22-alpha的水平和/或活性如章节8.6中描述的测定。在某些实施方式中,snai1、phosphosmad2、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、phosphosmad3、尿蛋白和/或osterix的升高的水平是如章节8.6中描述的。在某些实施方式中,klotho、alpha-sma、myocd、actriia和/或sm22-alpha的降低的水平是如章节8.6中描述的。在某些实施方式中,snai1、phosphosmad2、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、osterix、klotho、sm22-alpha、myocd、phosphosmad3、尿蛋白、actriia、axin2、actriia、axin2和/或alpha-sma水平是组织中的。在某些实施方式中,所述组织是主动脉。在某些实施方式中,所述组织是肾脏。在某些实施方式中,所述组织是骨骼。在某些实施方式中,所述组织是血清。在优选的实施方式中,runx2、dkk1、alp、osterix、sm22-alpha、klotho、alpha-sma、actriia、axin2和myocd水平和/或活性是在主动脉中的。在优选的实施方式中,phosphosmad2、phosphosmad3、尿蛋白、actriia和col1a1水平和/或活性是在肾脏中的。在优选的实施方式中,所述激活素水平和/或活性是在血清中的。在某些实施方式中,snai1、phosphosmad2、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、osterix、klotho、alpha-sma、myocd、phosphosmad3、尿蛋白、actriia和/或sm22-alpha的水平和/或活性分别是snai1、phosphosmad2、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、osterix、klotho、alpha-sma、myocd、phosphosmad3、尿蛋白、actriia和/或sm22-alpha的蛋白质水平和/或活性。在某些实施方式中,snai1、phosphosmad2、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、osterix、klotho、alpha-sma、myocd、phosphosmad3、尿蛋白、actriia和/或sm22-alpha的水平和/或活性分别是snai1、phosphosmad2、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、osterix、klotho、alpha-sma、myocd、phosphosmad3、尿蛋白、actriia和/或sm22-alpha的mrna水平和/或活性。在某些实施方式中,相对于参考群体,激活素的水平在所述对象中升高。在某些实施方式中,所述对象中卵泡抑素的水平约等于参考群体中卵泡抑素的水平。
在某些实施方式中,所述参考群体是章节8.6中描述的群体。在某些实施方式中,所述对象是章节8.4中描述的对象。
在某些实施方式中,所述actrii信号转导抑制剂是actriia-fc,例如actriia-hfc(例如,seqidno:7)。在某些实施方式中,所述actrii信号转导抑制剂是如章节8.5中描述的actrii信号转导抑制剂。
在某些实施方式中,所述药学上有效的剂量是如章节8.7中描述的剂量。在某些实施方式中,所述药学上有效的剂量是初始剂量。在某些实施方式中,所述药学上有效的剂量以如章节8.7中描述的频率施用。在某些实施方式中,所述药学上有效的剂量如章节8.7中描述的施用。
在某些实施方式中,如章节8.8中描述的,本文提供的方法与第二药学活性试剂组合使用。
在某些实施方式中,本文提供的是治疗对象的末期肾病的方法,包括向所述对象施用药学上有效剂量的actrii信号转导抑制剂(例如,激活素配体陷阱),其中所述对象在血液透析,以及其中所述对象早先施用了促红细胞生成素刺激剂。在某些实施方式中,本文提供的是治疗对象的末期肾病的方法,包括以每14天一次的间隔时间向所述对象皮下地施用0.13mg/kg的actrii信号转导抑制剂(例如,激活素配体陷阱),其中所述对象在血液透析,以及其中所述对象早先施用了促红细胞生成素刺激剂。在某些实施方式中,本文提供的是治疗对象的末期肾病的方法,包括以每14天一次的间隔时间向所述对象皮下地施用0.26mg/kg的actrii信号转导抑制剂(例如,激活素配体陷阱),其中所述对象在血液透析,以及其中所述对象早先施用了促红细胞生成素刺激剂。在某些实施方式中,本文提供的是治疗对象的末期肾病的方法,包括以每28天一次的间隔时间向所述对象皮下地施用0.3mg/kg的actrii信号转导抑制剂(例如,激活素配体陷阱),其中所述对象在血液透析,以及其中所述对象早先施用了促红细胞生成素刺激剂。在某些实施方式中,本文提供的是治疗对象的末期肾病的方法,包括以每28天一次的间隔时间向所述对象皮下地施用0.5mg/kg的actrii信号转导抑制剂(例如,激活素配体陷阱),其中所述对象在血液透析,以及其中所述对象早先施用了促红细胞生成素刺激剂。在某些实施方式中,本文提供的是治疗对象的末期肾病的方法,包括以每28天一次的间隔时间向所述对象皮下地施用0.7mg/kg的actrii信号转导抑制剂(例如,激活素配体陷阱),其中所述对象在血液透析,以及其中所述对象早先施用了促红细胞生成素刺激剂。在某些实施方式中,本文提供的是治疗对象的末期肾病的方法,包括以每14天一次的间隔时间向所述对象静脉内地施用0.1mg/kg的actrii信号转导抑制剂(例如,激活素配体陷阱),其中所述对象在血液透析,以及其中所述对象早先施用了促红细胞生成素刺激剂。在某些实施方式中,本文提供的是治疗对象的末期肾病的方法,包括以每14天一次的间隔时间向所述对象皮下地施用0.2mg/kg的actrii信号转导抑制剂(例如,激活素配体陷阱),其中所述对象在血液透析,以及其中所述对象早先施用了促红细胞生成素刺激剂。在某些实施方式中,所述actrii信号转导抑制剂是actriia-hfc(seqidno:7)。
8.3.4调整的给药
snai1、phosphosmad2、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、osterix、klotho、alpha-sma、myocd、phosphosmad3、尿蛋白、actriia、axin2和/或sm22-alpha的水平和/或活性可以进一步用于(i)评估对象的适当的给药,其中所述对象是用actrii信号转导抑制剂(例如,激活素配体陷阱)治疗的或将要治疗的候选者;(ii)评估在治疗期间是否调整actrii信号转导抑制剂的剂量;和/或(iii)评估actrii信号转导抑制剂的适当的维持剂量。如果snai1、phosphosmad2、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、osterix、klotho、alpha-sma、myocd、phosphosmad3、尿蛋白、actriia、axin2和/或sm22-alpha水平和/或活性大于或小于参考群体中的水平和/或活性,分别取决于snai1、phosphosmad2、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、osterix、klotho、alpha-sma、myocd、phosphosmad3、尿蛋白、actriia、axin2和/或sm22-alpha的水平和/或活性,用actrii信号转导抑制剂的给药可以启动、提高、降低、延迟或终止。在某些实施方式中,本文提供的是治疗和/或预防对象的心血管疾病、血管钙化、与血管钙化相关和/或由血管钙化引起的心血管疾病、与肾病相关和/或由肾病引起的心血管疾病、ckd-mbd、动脉硬化水平升高、lvh、与动脉硬化水平升高相关和/或由动脉硬化水平升高引起的心血管疾病和/或与lvh相关和/或由lvh引起的心血管疾病的方法,包括(i)向所述对象施用初始剂量的actrii信号转导抑制剂;(ii)进行所述对象中snai1、phosphosmad2、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、osterix、klotho、alpha-sma、myocd、phosphosmad3、尿蛋白、actriia、axin2和/或sm22-alpha的水平和/或活性的第一次测量;(iii)一段时间以后,进行所述对象中snai1、phosphosmad2、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、osterix、klotho、alpha-sma、myocd、phosphosmad3、尿蛋白、actriia、axin2和/或sm22-alpha的水平和/或活性的第二次测量;和(v)向所述对象施用调整剂量的actrii信号转导抑制剂。在某些实施方式中,所述actrii信号转导抑制剂是actriia-fc,例如actriia-hfc(例如,seqidno:7)。在某些实施方式中,所述actrii信号转导抑制剂是如章节8.5中描述的actrii信号转导抑制剂。在某些其他实施方式中,所述对象被诊断为患有慢性肾病-矿物质骨骼失调。在某些其他实施方式中,所述对象没有被诊断为患有慢性肾病-矿物质骨骼失调。在某些实施方式中,所述对象的血管钙化通过如章节8.6.6中描述的测定agatston评分来分析。在某些实施方式中,所述调整的剂量是基于所述第一次测量和所述第二次测量之间检测到的变化。
在某些实施方式中,snai1、phosphosmad2、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、osterix、klotho、alpha-sma、myocd、phosphosmad3、尿蛋白、actriia、axin2和/或sm22-alpha的水平和/或活性如章节8.6中描述的测定。在某些实施方式中,snai1、phosphosmad2、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、osterix、klotho、alpha-sma、myocd、phosphosmad3、尿蛋白、actriia、axin2和/或sm22-alpha的水平和/或活性分别是snai1、phosphosmad2、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、osterix、klotho、alpha-sma、myocd、phosphosmad3、尿蛋白和/或sm22-alpha的蛋白质水平和/或活性。在某些实施方式中,snai1、phosphosmad2、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、osterix、klotho、alpha-sma、myocd、phosphosmad3、尿蛋白、actriia、axin2和/或sm22-alpha的水平和/或活性分别是snai1、phosphosmad2、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、osterix、klotho、alpha-sma、myocd、phosphosmad3、尿蛋白、actriia、axin2和/或sm22-alpha的mrna水平和/或活性。在某些实施方式中,snai1、phosphosmad2、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、osterix、klotho、sm22-alpha、myocd、phosphosmad3、尿蛋白、actriia、axin2和/或alpha-sma水平是组织中的。在某些实施方式中,所述组织是主动脉。在某些实施方式中,所述组织是肾脏。在某些实施方式中,所述组织是骨骼。在某些实施方式中,所述组织是血清。在优选的实施方式中,runx2、dkk1、alp、osterix、sm22-alpha、klotho、alpha-sma、myocd、actriia或axin2和平和/或活性是在主动脉中的。在优选的实施方式中,phosphosmad2、phosphosmad3、尿蛋白、actriia、axin2和col1a1的水平和/或活性是在肾脏中的。在优选的实施方式中,所述激活素水平和/或活性是在血清中的。在某些实施方式中,相对于参考群体,激活素的水平在所述对象中升高。在某些实施方式中,相对于参考群体,卵泡抑素的水平在所述对象中是正常的。在某些实施方式中,所述对象的血管钙化通过如章节8.6中描述的测定agatston评分来分析。
在某些实施方式中,所述参考群体是章节8.6中描述的群体。在某些实施方式中,所述对象是章节8.4中描述的对象。
在某些实施方式中,所述初始剂量是如章节8.7中描述的剂量。在某些实施方式中,所述初始剂量以如章节8.7中描述的频率施用。在某些实施方式中,所述初始剂量如章节8.7中描述的施用。
在某些实施方式中,所述第一次测量和/或所述第二次测量如章节8.6中描述的进行。在某些实施方式中,所述第一次测量在治疗的开始之前进行。在某些实施方式中,所述第一次测量在治疗的开始之后,或在其最多1天、2天、3天、4天、5天、6天或1周、2周、3周、4周或两个月之内进行。在某些实施方式中,所述第二次测量在治疗开始后立即进行,或在其最多1天、2天、3天、4天、5天、6天或1周、2周、1个月、2个月、3个月、4个月、5个月、6个月、7个月、8个月、9个月、10个月、11个月或12个月之内进行。
在某些实施方式中,如果与参考群体中runx2的水平和/或活性相比runx2的水平和/或活性升高,与参考群体中alp的水平和/或活性相比alp的水平和/或活性升高,与参考群体中snai1的水平和/或活性相比snai1的水平和/或活性升高,与参考群体中phosphosmad2的水平和/或活性相比phosphosmad2的水平和/或活性升高,与参考群体中phosphosmad3的水平和/或活性相比phosphosmad3的水平和/或活性升高,与参考群体中尿蛋白的水平和/或活性相比尿蛋白的水平和/或活性升高,与参考群体中dkk1的水平和/或活性相比dkk1的水平和/或活性升高,与参考群体中col1a1的水平和/或活性相比col1a1的水平和/或活性升高,与参考群体中激活素(例如,游离激活素)的水平和/或活性相比激活素(例如,游离激活素)的水平和/或活性升高,与参考群体中bsap的水平和/或活性相比bsap的水平和/或活性升高,与参考群体中ctx的水平和/或活性相比ctx的水平和/或活性升高,与参考群体中osterix的水平和/或活性相比osterix的水平和/或活性升高,与参考群体中klotho的水平和/或活性相比klotho的水平和/或活性降低,与参考群体中alpha-sma的水平和/或活性相比alpha-sma的水平和/或活性降低,与参考群体中myocd的水平和/或活性相比myocd的水平和/或活性降低,与参考群体中actriia的水平和/或活性相比actriia的水平和/或活性降低,与参考群体中axin2的水平和/或活性相比axin2的水平和/或活性降低,和/或与参考群体中sm22-alpha的水平和/或活性相比sm22-alpha的水平和/或活性降低,所述actrii信号转导抑制剂的调整的剂量大于所述初始剂量。在某些实施方式中,snai1、phosphosmad2、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、phosphosmad3、尿蛋白和/或osterix的升高的水平是如章节8.6中描述的。在某些实施方式中,klotho、alpha-sma、alp、actriia、axin2和/或sm22-alpha的降低的水平是如章节8.6中描述的。在某些实施方式中,snai1、phosphosmad2、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、osterix、klotho、sm22-alpha、myocd、phosphosmad3、尿蛋白、actriia、axin2和/或alpha-sma水平是组织中的。在某些实施方式中,所述组织是主动脉。在某些实施方式中,所述组织是肾脏。在某些实施方式中,所述组织是骨骼。在某些实施方式中,所述组织是血清。在优选的实施方式中,runx2、dkk1、alp、osterix、sm22-alpha、klotho、alpha-sma、actriia、axin2和myocd水平和/或活性是在主动脉中的。在优选的实施方式中,phosphosmad2、phosphosmad3、尿蛋白、actriia、axin2和col1a1的水平和/或活性是在肾脏中的。在优选的实施方式中,所述激活素水平和/或活性是在血清中的。
在某些实施方式中,所述调整的剂量是如章节8.7中描述的剂量。在某些实施方式中,所述调整的剂量以如章节8.7中描述的频率施用。在某些实施方式中,所述调整的剂量如章节8.7中描述的施用。
在某些实施方式中,所述对象具有与对象中在先的runx2水平和/或活性相比升高的runx2水平和/或活性,与对象中在先的alp水平和/或活性相比升高的alp水平和/或活性,与对象中在先的snai1水平和/或活性相比升高的snai1水平和/或活性,与对象中在先的phosphosmad2水平和/或活性相比升高的phosphosmad2水平和/或活性,与对象中在先的phosphosmad3水平和/或活性相比升高的phosphosmad3水平和/或活性,与对象中在先的尿蛋白水平和/或活性相比升高的尿蛋白水平和/或活性,与对象中在先的dkk1水平和/或活性相比升高的dkk1水平和/或活性,与对象中在先的激活素(例如,游离激活素)水平和/或活性相比升高的激活素(例如,游离激活素)水平和/或活性,与所述对象中在先的col1a1水平和/或活性相比升高的col1a1水平和/或活性,与所述对象中在先的bsap水平和/或活性相比升高的bsap水平和/或活性,与所述对象中在先的ctx水平和/或活性相比升高的ctx水平和/或活性,与所述对象中在先的osterix水平和/或活性相比升高的osterix水平和/或活性,与所述对象中在先的klotho水平和/或活性相比降低的klotho水平和/或活性,与所述对象中在先的alpha-sma水平和/或活性相比降低的alpha-sma水平和/或活性,与所述对象中在先的myocd水平和/或活性相比降低的myocd水平和/或活性,与所述对象中在先的actriia水平和/或活性相比降低的actriia水平和/或活性,与所述对象中在先的axin2水平和/或活性相比降低的axin2水平和/或活性,和/或与所述对象中在先的sm22-alpha水平和/或活性相比降低的sm22-alpha水平和/或活性。在某些实施方式中,所述对象中在先的runx2水平和/或活性、所述对象中在先的alp水平和/或活性、所述对象中在先的snai1水平和/或活性、所述对象中在先的phosphosmad2水平和/或活性、所述对象中在先的phosphosmad3水平和/或活性、所述对象中在先的尿蛋白水平和/或活性、所述对象中在先的dkk1水平和/或活性、所述对象中在先的激活素(例如,游离激活素)水平和/或活性、所述对象中在先的col1a1水平和/或活性、所述对象中在先的bsap水平和/或活性、所述对象中在先的ctx水平和/或活性、所述对象中在先的osterix水平和/或活性、所述对象中在先的klotho水平和/或活性、所述对象中在先的alpha-sma水平和/或活性、所述对象中在先的myocd水平和/或活性、所述对象中在先的actriia水平和/或活性、所述对象中在先的actriia水平和/或活性、所述对象中在先的axin2水平和/或活性、所述对象中在先的axin2水平和/或活性、和/或所述对象中在先的sm22-alpha水平和/或活性是(i)心血管疾病;(ii)血管钙化;(iii)与血管钙化相关和/或由血管钙化引起的心血管疾病;(iv)与肾病相关和/或由肾病引起的心血管疾病;(v)ckd-mbd;(vi)动脉硬化水平升高;(vii)lvh;(viii)与动脉硬化水平升高相关和/或由动脉硬化水平升高引起的心血管疾病;和/或(ix)与lvh相关和/或由lvh引起的心血管疾病的症状发作或诊断之前1、2、3、4、5、6、8、10、12、18、24或48个月的相应水平。
在某些实施方式中,如果与参考群体中runx2的水平和/或活性相比runx2的水平和/或活性降低,与参考群体中alp的水平和/或活性相比alp的水平和/或活性降低,与参考群体中snai1的水平和/或活性相比snai1的水平和/或活性降低,与参考群体中phosphosmad2的水平和/或活性相比phosphosmad2的水平和/或活性降低,与参考群体中phosphosmad3的水平和/或活性相比phosphosmad3的水平和/或活性降低,与参考群体中尿蛋白的水平和/或活性相比尿蛋白的水平和/或活性降低,与参考群体中dkk1的水平和/或活性相比dkk1的水平和/或活性降低,与参考群体中col1a1的水平和/或活性相比col1a1的水平和/或活性降低,与参考群体中激活素(例如,游离激活素)的水平和/或活性相比激活素(例如,游离激活素)的水平和/或活性降低,与参考群体中bsap的水平和/或活性相比bsap的水平和/或活性降低,与参考群体中ctx的水平和/或活性相比ctx的水平和/或活性降低,与参考群体中osterix的水平和/或活性相比osterix的水平和/或活性降低,与参考群体中klotho的水平和/或活性相比klotho的水平和/或活性升高,与参考群体中alpha-sma的水平和/或活性相比alpha-sma的水平和/或活性升高,与参考群体中myocd的水平和/或活性相比myocd的水平和/或活性升高,与参考群体中actriia的水平和/或活性相比actriia的水平和/或活性升高,与参考群体中axin2的水平和/或活性相比axin2的水平和/或活性升高,和/或与参考群体中sm22-alpha的水平和/或活性相比sm22-alpha的水平和/或活性升高,所述actrii信号转导抑制剂(例如,激活素配体陷阱)的调整的剂量小于所述初始剂量。在某些实施方式中,klotho、alpha-sma、myocd、actriia、axin2和/或sm22-alpha的升高的水平是如章节8.6中描述的。在某些实施方式中,snai1、phosphosmad2、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、phosphosmad3、尿蛋白和/或osterix的降低的水平是如章节8.6中描述的。在某些实施方式中,snai1、phosphosmad2、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、osterix、klotho、sm22-alpha、myocd、phosphosmad3、尿蛋白、actriia、axin2和/或alpha-sma水平是组织中的。在某些实施方式中,所述组织是主动脉。在某些实施方式中,所述组织是肾脏。在某些实施方式中,所述组织是骨骼。在某些实施方式中,所述组织是血清。在优选的实施方式中,runx2、dkk1、alp、osterix、sm22-alpha、klotho、alpha-sma、actriia、axin2和myocd水平和/或活性是在主动脉中的。在优选的实施方式中,phosphosmad2、phosphosmad3、尿蛋白、actriia、axin2和col1a1的水平和/或活性是在肾脏中的。在优选的实施方式中,所述激活素水平和/或活性是在血清中的。在某些实施方式中,snai1、phosphosmad2、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、osterix、klotho、sm22-alpha、myocd、actriia、axin2和/或alpha-sma水平是主动脉中的。
在某些实施方式中,所述参考群体是章节8.6中描述的群体。在某些实施方式中,所述调整的剂量是如章节8.7中描述的剂量。在某些实施方式中,所述调整的剂量以如章节8.7中描述的频率施用。在某些实施方式中,所述调整的剂量如章节8.7中描述的施用。
在某些实施方式中,如章节8.8中描述的,本文提供的方法与第二药学活性试剂组合使用。
本领域技术人员将认识到,runx2、alp、snai1、phosphosmad2、dkk1、col1a1、激活素、bsap、ctx、osterix、klotho、alpha-sma、myocd、actriia、axin2、sm22-alpha、phosphosmad3和尿蛋白的水平和/或活性可以分别与相应参考群体中的水平和/或活性独立比较,例如,如上文在章节8.3.1中描述的。
8.4患者群体
根据本文描述的方法治疗的对象可以是任何哺乳动物,例如啮齿动物和灵长类,在优选的实施方式中,是人类。在某些实施方式中,本文描述的方法可以用于在任何哺乳动物例如啮齿动物和灵长类中,在优选的实施方式中,在人类对象中治疗心血管疾病、血管钙化、与血管钙化相关和/或由血管钙化引起的心血管疾病、与肾病相关和/或由肾病引起的心血管疾病、高周转rod、动脉硬化水平升高、与动脉硬化水平升高相关和/或由动脉硬化水平升高引起的心血管疾病、lvh和/或与lvh相关和/或由lvh引起的心血管疾病;或者监视和/或降低血管钙化、动脉的(例如,血管的)硬化、lvh、主动脉钙水平、内皮向间充质转变和/或骨形成,和/或提高骨骼矿物密度和/或血管平滑肌细胞功能。
在某些实施方式中,与参考群体中的激活素水平相比,根据本文描述的方法治疗的对象具有升高的激活素水平。在某些实施方式中,所述激活素水平是肾脏、血浆或主动脉的激活素水平。在某些实施方式中,所述激活素是激活素a。在某些实施方式中,与参考群体中的卵泡抑素水平相比,根据本文描述的方法治疗的对象具有大约相等的卵泡抑素水平。在某些实施方式中,与参考群体中的卵泡抑素水平相比,根据本文描述的方法治疗的对象不具有升高的卵泡抑素水平。在某些实施方式中,与参考群体中的卵泡抑素水平相比,根据本文描述的方法治疗的对象不具有降低的卵泡抑素水平。在某些实施方式中,与参考群体中的卵泡抑素样3水平相比,根据本文描述的方法治疗的对象具有大约相等的卵泡抑素样3水平。在某些实施方式中,与参考群体中的卵泡抑素样3水平相比,根据本文描述的方法治疗的对象不具有升高的卵泡抑素样3水平。在某些实施方式中,与参考群体中的卵泡抑素样3水平相比,根据本文描述的方法治疗的对象不具有降低的卵泡抑素样3水平。在某些实施方式中,与参考群体中的抑制素水平相比,根据本文描述的方法治疗的对象具有大约相等的抑制素水平。在某些实施方式中,与参考群体中的抑制素水平相比,根据本文描述的方法治疗的对象不具有升高的抑制素水平。在某些实施方式中,与参考群体中的抑制素水平相比,根据本文描述的方法治疗的对象不具有降低的抑制素水平。在某些实施方式中,对象中的游离激活素水平通过抑制素、卵泡抑素、卵泡抑素样3水平对激活素水平的化学当量来确定。因而,在某些实施方式中,根据本文描述的方法治疗的对象具有提高的游离激活素水平。
在某些实施方式中,与章节8.6中描述的参考群体相比,根据本文描述的方法治疗的对象不具有phosphoerk1/2的提高。在某些实施方式中,phosphoerk1/2是主动脉的phosphoerk1/2。
在某些实施方式中,与参考群体中的enmt相比,根据本文描述的方法治疗的对象具有提高的内皮向间充质转变(enmt)。在某些实施方式中,根据本文描述的方法治疗的对象具有与enmt相关的转录因子,例如snai1的提高的表达。在某些实施方式中,与参考群体中的成骨细胞转变相比,对象中提高的enmt引起对象中提高的成骨细胞转变。在某些实施方式中,与参考群体中的血管硬化相比,对象中提高的enmt引起对象中提高的血管硬化。在某些实施方式中,与参考群体中的血管钙化相比,对象中提高的enmt引起对象中提高的血管钙化。在某些实施方式中,与参考群体中的血管平滑肌功能相比,对象中提高的enmt引起对象中降低的血管平滑肌功能。在某些实施方式中,与参考群体中的lvh相比,对象中提高的enmt引起对象中提高的lvh。
在某些实施方式中,根据本文提供的方法治疗的对象患有肾脏纤维化。在某些实施方式中,根据本文提供的方法治疗的对象患有肾小球硬化症。
在某些实施方式中,分别与参考群体中snai1、phosphosmad2、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、phosphosmad3、尿蛋白、osterix、klotho、alpha-sma、myocd、actriia和/或sm22-alpha的水平相比,根据本文描述的方法治疗的对象具有升高的snai1、phosphosmad2、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、phosphosmad3、尿蛋白和/或osterix的水平和/或活性,和/或降低的klotho、alpha-sma、myocd、actriia和/或sm22-alpha水平和/或活性。在某些实施方式中,根据本文描述的方法治疗的对象具有(i)血管钙化;和(ii)分别与参考群体中snai1、phosphosmad2、phosphosmad3、尿蛋白、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、osterix、klotho、alpha-sma、myocd、actriia、axin2和/或sm22-alpha的水平相比,升高的snai1、phosphosmad2、phosphosmad3、尿蛋白、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx和/或osterix水平和/或活性,和/或降低的klotho、alpha-sma、myocd、actriia和/或sm22-alpha水平和/或活性。在某些实施方式中,根据本文描述的方法治疗的对象具有(i)心血管疾病;和(ii)分别与参考群体中snai1、phosphosmad2、phosphosmad3、尿蛋白、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、osterix、klotho、alpha-sma、myocd、actriia和/或sm22-alpha的水平相比,升高的snai1、phosphosmad2、phosphosmad3、尿蛋白、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx和/或osterix水平和/或活性,和/或降低的klotho、alpha-sma、myocd、actriia和/或sm22-alpha水平和/或活性。在某些实施方式中,根据本文描述的方法治疗的对象具有(i)与血管钙化相关和/或由血管钙化引起的心血管疾病;和(ii)分别与参考群体中snai1、phosphosmad2、phosphosmad3、尿蛋白、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、osterix、klotho、alpha-sma、myocd、actriia和/或sm22-alpha的水平相比,升高的snai1、phosphosmad2、phosphosmad3、尿蛋白、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx和/或osterix水平和/或活性,和/或降低的klotho、alpha-sma、myocd、actriia和/或sm22-alpha水平和/或活性。在某些实施方式中,根据本文描述的方法治疗的对象具有(i)与肾病相关和/或由肾病引起的心血管疾病;和(ii)分别与参考群体中snai1、phosphosmad2、phosphosmad3、尿蛋白、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、osterix、klotho、alpha-sma、myocd、actriia、axin2和/或sm22-alpha的水平相比,升高的snai1、phosphosmad2、phosphosmad3、尿蛋白、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx和/或osterix水平和/或活性,和/或降低的klotho、alpha-sma、myocd、actriia和/或sm22-alpha水平和/或活性。在某些实施方式中,根据本文描述的方法治疗的对象具有(i)ckd-mbd;和(ii)分别与参考群体中snai1、phosphosmad2、phosphosmad3、尿蛋白、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、osterix、klotho、alpha-sma、myocd、actriia和/或sm22-alpha的水平相比,升高的snai1、phosphosmad2、phosphosmad3、尿蛋白、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx和/或osterix水平和/或活性,和/或降低的klotho、alpha-sma、myocd、actriia和/或sm22-alpha水平和/或活性。在某些实施方式中,根据本文描述的方法治疗的对象具有(i)动脉硬化水平升高;和(ii)分别与参考群体中snai1、phosphosmad2、phosphosmad3、尿蛋白、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、osterix、klotho、alpha-sma、myocd、actriia和/或sm22-alpha的水平相比,升高的snai1、phosphosmad2、phosphosmad3、尿蛋白、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx和/或osterix水平和/或活性,和/或降低的klotho、alpha-sma、myocd、actriia和/或sm22-alpha水平和/或活性。在某些实施方式中,根据本文描述的方法治疗的对象具有(i)与动脉硬化水平升高相关和/或由动脉硬化水平升高引起的心血管疾病;和(ii)分别与参考群体中snai1、phosphosmad2、phosphosmad3、尿蛋白、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、osterix、klotho、alpha-sma、myocd、actriia和/或sm22-alpha的水平相比,升高的snai1、phosphosmad2、phosphosmad3、尿蛋白、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx和/或osterix水平和/或活性,和/或降低的klotho、alpha-sma、myocd、actriia和/或sm22-alpha水平和/或活性。在某些实施方式中,根据本文描述的方法治疗的对象具有(i)lvh;和(ii)分别与参考群体中snai1、phosphosmad2、phosphosmad3、尿蛋白、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、osterix、klotho、alpha-sma、myocd、actriia和/或sm22-alpha的水平相比,升高的snai1、phosphosmad2、phosphosmad3、尿蛋白、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx和/或osterix水平和/或活性,和/或降低的klotho、alpha-sma、myocd、actriia和/或sm22-alpha水平和/或活性。在某些实施方式中,根据本文描述的方法治疗的对象具有(i)与lvh相关和/或由lvh引起的心血管疾病;和(ii)与参考群体中snai1、phosphosmad2、phosphosmad3、尿蛋白、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、osterix、klotho、alpha-sma、myocd、actriia和/或sm22-alpha的水平相比,升高的snai1、phosphosmad2、phosphosmad3、尿蛋白、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx和/或osterix水平和/或活性,和/或降低的klotho、alpha-sma、myocd、actriia和/或sm22-alpha水平和/或活性。
在某些实施方式中,根据本文描述的方法治疗的对象分别与在(i)心血管疾病;(ii)血管钙化;(iii)与血管钙化相关和/或由血管钙化引起的心血管疾病;(iv)与肾病相关和/或由肾病引起的心血管疾病;(v)ckd-mbd;(vi)动脉硬化水平升高;(vii)lvh;(viii)与动脉硬化水平升高相关和/或由动脉硬化水平升高引起的心血管疾病;和/或(ix)与lvh相关和/或由lvh引起的心血管疾病的症状发作或诊断之前1、2、3、4、5、6、8、10、12、18、24或48个月之时,所述对象中snai1、phosphosmad2、phosphosmad3、尿蛋白、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、osterix、klotho、alpha-sma、myocd、actriia和/或sm22-alpha的在先水平相比,具有升高的snai1、phosphosmad2、phosphosmad3、尿蛋白、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx和/或osterix水平和/或活性,和/或降低的klotho、alpha-sma、myocd、actriia和/或sm22-alpha水平和/或活性。
在某些其他实施方式中,所述对象被诊断为患有慢性肾病-矿物质骨骼失调。在某些其他实施方式中,所述对象没有被诊断为患有慢性肾病-矿物质骨骼失调。在某些实施方式中,所述参考群体是章节8.6中描述的群体。在某些实施方式中,snai1、phosphosmad2、phosphosmad3、尿蛋白、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx和/或osterix的升高的水平是如章节8.6中描述的。在某些实施方式中,klotho、alpha-sma、myocd、actriia和/或sm22-alpha的降低的水平是如章节8.6中描述的。
在某些实施方式中,根据本文提供的方法治疗的对象患有与升高的snai1水平相关的疾病。在某些实施方式中,根据本文提供的方法治疗的对象患有与升高的phosphosmad2水平相关的疾病。在某些实施方式中,根据本文提供的方法治疗的对象患有与升高的phosphosmad3水平相关的疾病。在某些实施方式中,根据本文提供的方法治疗的对象患有与升高的尿蛋白水平相关的疾病。在某些实施方式中,根据本文提供的方法治疗的对象患有与升高的dkk1水平相关的疾病。在某些实施方式中,根据本文提供的方法治疗的对象患有与升高的col1a1水平相关的疾病。在某些实施方式中,根据本文提供的方法治疗的对象患有与升高的runx2水平相关的疾病。在某些实施方式中,根据本文提供的方法治疗的对象患有与升高的alp水平相关的疾病。在某些实施方式中,根据本文提供的方法治疗的对象患有与升高的bsap水平相关的疾病。在某些实施方式中,根据本文提供的方法治疗的对象患有与升高的ctx水平相关的疾病。在某些实施方式中,根据本文提供的方法治疗的对象患有与升高的osterix水平相关的疾病。在某些实施方式中,根据本文提供的方法治疗的对象患有与升高的actriia水平相关的疾病。在某些实施方式中,根据本文提供的方法治疗的对象患有与降低的klotho水平相关的疾病。在某些实施方式中,根据本文提供的方法治疗的对象患有与降低的alpha-sma水平相关的疾病。在某些实施方式中,根据本文提供的方法治疗的对象患有与降低的myocd水平相关的疾病。在某些实施方式中,根据本文提供的方法治疗的对象患有与降低的sm22-alpha水平相关的疾病。在某些实施方式中,根据本文提供的方法治疗的对象患有与降低的actriia水平相关的疾病。
在某些实施方式中,根据本文提供的方法治疗的对象患有心血管疾病。在某些实施方式中,根据本文提供的方法治疗的对象患有血管钙化。在某些实施方式中,根据本文提供的方法治疗的对象患有与血管钙化相关和/或由血管钙化引起的心血管疾病。在某些实施方式中,所述血管钙化是如章节8.6中描述的确定的。在某些实施方式中,所述血管钙化是通过agatston评分确定的。在某些实施方案中,所述血管钙化是钙化性动脉粥样硬化、钙化的中层血管病变(也称为
在某些实施方式中,根据本文描述的方法治疗的对象与如章节8.6中描述的参考群体相比具有不希望的高水平的主动脉钙、血管钙化、动脉硬化水平升高和/或成骨细胞数量。在某些实施方式中,根据本文描述的方法治疗的对象与如章节8.6中描述的参考群体相比具有发生不希望的高水平的主动脉钙、血管钙化、动脉硬化水平升高和/或成骨细胞数量的风险,例如,患有慢性肾病的对象。在某些实施方式中,根据本文提供的方法治疗的对象与如章节8.6中描述的参考群体相比具有主动脉粥样斑中的钙沉积。在某些实施方式中,根据本文提供的方法治疗的对象与如章节8.6中描述的参考群体相比具有主动脉硬化形式的动脉硬化水平升高。在某些实施方式中,根据本文提供的方法治疗的对象与如章节8.6中描述的参考群体相比具有提高高血压的动脉硬化水平升高水平。
在某些实施方式中,根据本文提供的方法治疗的对象患有与肾病相关和/或由肾病引起的心血管疾病。在某些实施方式中,所述肾病是慢性肾病。在某些实施方式中,根据本文提供的方法治疗的对象患有慢性肾病。在某些实施方式中,所述对象患有继发于慢性肾病的心血管疾病。在某些实施方式中,所述慢性肾病达到3期、4期、5期或5d期。在具体的实施方式中,所述肾病是终末期肾病。在某些实施方式中,所述对象具有成年人的小于60ml/分钟/1.73m2或儿童对象的小于89ml/分钟/1.73m2的肾小球过滤率。参见moeetal.,2006,kidneyinternational69:1945-1953。在某些实施方式中,所述对象是成年人,其中所述对象具有小于50ml/分钟/1.73m2、40ml/分钟/1.73m2、30ml/分钟/1.73m2、20ml/分钟/1.73m2或小于10ml/分钟/1.73m2的肾小球过滤率。在某些实施方式中,所述对象是儿童对象,其中所述儿童对象具有小于80ml/分钟/1.73m2、70ml/分钟/1.73m2、60ml/分钟/1.73m2、50ml/分钟/1.73m2、40ml/分钟/1.73m2、30ml/分钟/1.73m2、20ml/分钟/1.73m2或小于10ml/分钟/1.73m2的肾小球过滤率。不受理论的限制,在成年人对象中小于60ml/分钟/1.73m2以及在儿童对象中小于89ml/分钟/1.73m2的肾小球过滤率引起钙水平、磷水平、pth水平和维生素d新陈代谢方面可检测的异常;这些标志物的异常水平引起骨骼疾病。在某些实施方式中,所述对象具有参考群体降低的菊糖清除率,例如,如章节8.6中描述的参考群体。在某些实施方式中,所述对象具有参考群体降低的血尿氮水平,例如,如章节8.6中描述的参考群体。在某些实施方式中,所述对象是高磷酸盐血的。在某些实施方式中,所述对象患有肾脏纤维化。
在某些实施方式中,所述对象患有alport’s综合征。在某些实施方式中,所述对象在与alport’s综合征相关的col4a5基因中有一个或更多个体细胞突变。
在某些实施方式中,根据本文提供的方法治疗的对象具有与慢性肾病相关的骨骼病理,即,ckd-矿物质/骨骼失调(ckd-mbd)。参见moeetal.,2006,kidneyinternational69:1945-1953。在某些实施方式中,与参考群体,例如,如章节8.6中描述的参考群体相比,所述对象具有降低的小梁骨体积。在某些实施方式中,与参考群体,例如,如章节8.6中描述的参考群体的小梁厚度相比,所述对象具有降低的小梁厚度。在某些实施方式中,与参考群体,例如,如章节8.6中描述的参考群体的侵蚀面骨表面比相比,所述对象具有提高的侵蚀面骨骼表面比。在某些实施方式中,与参考群体,例如,如章节8.6中描述的参考群体的破骨细胞水平相比,所述对象具有提高的破骨细胞水平。在某些实施方式中,与参考群体,例如,如章节8.6中描述的参考群体的成骨细胞表面骨骼表面比相比,所述对象具有提高的成骨细胞表面骨骼表面比。在某些实施方式中,与参考群体,例如,如章节8.6中描述的参考群体的成骨细胞水平相比,所述对象具有提高的成骨细胞水平。在某些实施方式中,与参考群体中,例如,如章节8.6中描述的参考群体的骨形成率相比,所述对象具有降低的骨形成率。在某些实施方式中,所述ckd-mbd由肾性骨营养不良和血管钙化组成。在某些实施方式中,所述ckd-mbd由肾性骨营养不良组成。在某些实施方式中,所述ckd-mbd是低周转ckd-mbd。在某些实施方式中,所述ckd-mbd由动脉硬化水平升高和/或lvh组成。低周转ckd-mbd可以通过以下的表1中列出的组织学特征来诊断。参见nationalkidneyfoundation,kidneydiseaseoutcomesqualityinitiativeguidelinesatthewebsiteofthenationalkidneyfoundation。在某些实施方式中,所述对象具有高周转rod。
表1.低周转ckd-mbd的组织学特征
在某些实施方式中,所述对象正经历血液透析。
在某些实施方式中,根据本文描述的方法治疗的对象患有终末期肾病。在某些实施方式中,根据本文描述的方法治疗的对象经历透析。
在某些实施方式中,根据本文描述的方法治疗的对象具有与参考群体中的骨吸收相比提高的骨吸收。在某些实施方式中,所述提高的骨吸收通过ctx的水平确定。在某些实施方式中,所述ctx是害怕如章节8.6中描述的确定。在某些实施方式中,所述骨吸收如章节8.6中描述的评估。
在某些实施方式中,根据本文描述的方法治疗的对象可以是任何年龄。在某些实施方式中,根据本文描述的方法治疗的对象是小于18岁。在具体的实施方式中,根据本文描述的方法治疗的对象是小于13岁。在另一个具体的实施方式中,根据本文描述的方法治疗的对象是小于12岁、小于11岁、小于10岁、小于9岁、小于8岁、小于7岁、小于6岁或小于5岁。在另一个具体的实施方式中,根据本文描述的方法治疗的对象是1-3岁、3-5岁、5-7岁、7-9岁、9-11岁、11-13岁、13-15岁、15-20岁、20-25岁、25-30岁或大于30岁。在另一个具体的实施方式中,根据本文描述的方法治疗的对象是30-35岁、35-40岁、40-45岁、45-50岁、50-55岁、55-60岁或大于60岁。在另一个具体的实施方式中,根据本文描述的方法治疗的对象是60-65岁、65-70岁、70-75岁、75-80岁或大于80岁。
在某些实施方式中,根据本文提高的方法治疗的对象患有终末期肾病。在某些实施方式中,根据本文提供的方法治疗的对象在血液透析。在某些实施方式中,根据本文提供的方法治疗的对象早先施用了促红细胞生成素刺激剂。在某些实施方式中,根据本文提供的方法治疗的对象患有终末期肾病,在血液透析,并且早先施用了促红细胞生成素刺激剂。
本领域技术人员将认识到,runx2、alp、snai1、phosphosmad2、dkk1、col1a1、激活素、bsap、ctx、osterix、klotho、alpha-sma、myocd、actriia、axin2、sm22-alpha、phosphosmad3和尿蛋白的水平和/或活性可以分别与相应参考群体中的水平和/或活性独立比较,例如,如上文在章节8.3.1中描述的。
8.5actrii信号转导抑制剂
本节中描述的和本领域已知的actrii信号转导抑制剂可以用于本文提供的方法。在某些实施方式中,本节描述的actrii信号转导抑制剂可以用于本文提供的方法中(参见,章节8.3)。
本文涵盖的actrii信号转导抑制剂包括actriia信号转导抑制剂和actriib信号转导抑制剂(见下文)。在某些实施方式中,actrii信号转导抑制剂是特异于actriia信号转导的。在其他实施方式中,actrii信号转导抑制剂是特异于actriib信号转导的。在某些实施方式中,actrii信号转导抑制剂优先地抑制actriia信号转导。在其他实施方式中,actrii信号转导抑制剂优先地抑制actriib信号转导。在某些实施方式中,actrii信号转导抑制剂抑制actriia信号转导和actriib信号转导两者。
在某些实施方式中,actrii信号转导抑制剂可以是包含actrii的激活素结合结构域的多肽。不受理论的限制,这种包含激活素结合结构域的多头隔离了激活素,从而阻止激活素信号转导。这些包含激活素结合结构域的多肽可以包含actrii的细胞外结构域的全部或一部分(即,actriia的全部或部分细胞外结构域,或actriib的全部或部分细胞外结构域)。在具体的实施方式中,actrii的细胞外结构域是可溶的。
在某些实施方式中,包含激活素结合结构域的多肽连接到抗体的fc部分(即,产生包含actrii受体的包含激活素结合结构域的多肽与抗体的fc部分的轭合物)。不受理论的限制,抗体部分为所述轭合物赋予了提高的稳定性。在某些实施方式中,激活素结合结构域通过接头,例如肽接头连接到抗体的fc部分。
本文描述的组合物和方法中使用的actrii信号转导抑制剂包含直接地或间接地、细胞外地或细胞内地抑制actriia信号转导和/或actriib信号转导的分子。在某些实施方式中,本文描述的组合物和方法中使用的actriia信号转导和/或actriib信号转导的抑制剂通过与其本身的受体相互作用来抑制actriia信号转导和/或actriib信号转导。在其他实施方式中,本文描述的组合物和方法中使用的actriia信号转导和/或actriib信号转导的抑制剂通过与actriia和/或actriib配体,例如激活素的相互作用抑制actriia信号转导和/或actriib信号转导。
8.5.1actriia信号转导的抑制剂
如本文使用的,术语“actriia”是指来自任何物种的激活素iia型受体(actriia)蛋白的家族,以及通过诱变或其他修饰衍生自这些actriia蛋白的变体。本文提及actriia被理解为是提及当前鉴定的形式的任一种。actriia家族的成员一般是跨膜的蛋白质,由具有富半胱氨酸区的配体结合细胞外结构域、跨膜结构域、以及具有预测的丝氨酸/苏氨酸激酶活性的细胞质结构域组成。
本文描述的组合物和方法中使用的actriia信号转导抑制剂非限制性地包括,结合激活素的可溶的actriia多肽;结合激活素(特别是激活素a或b亚基,还成为βa或βb)并破坏actriia结合的抗体;结合actriia并破坏激活素结合的抗体;对于激活素或actriia结合而选择的非抗体蛋白质(参见,例如wo/2002/088171,wo/2006/055689,wo/2002/032925,wo/2005/037989,us2003/0133939,和us2005/0238646,它们的每一个通过完全引用合并在本文中,作为这类蛋白质和设计与选择这类蛋白质的实例);为激活素或actriia结合而选择的随机肽,它们可以轭合到fc结构域。
在某些实施方式中,具有激活素或actriia结合活性的两种或更多种不同的蛋白质(或其他部分),特别是分别阻断i型(例如,可溶的i型激活素受体)和ii型(例如,可溶的ii型激活素受体)结合位点的激活素结合物可以连接在一起,产生抑制actriia信号转导的双功能或多功能结合分子,因而可以用于本文描述的组合物和方法。在某些实施方式中,抑制actriia信号转导的激活素-actriia信号转导轴拮抗剂包括核酸适体、小分子和其他试剂,用于本文描述的组合物和方法中。
8.5.1.1包含actriia多肽的actriia信号转导抑制剂
术语“actriia多肽”包括这些多肽,其包含actriia家族成员的任何天然发生的多肽以及保持了有用活性的其任何变体(包括突变体、片段、融合物和肽模拟物形式)。例如,actriia多肽包括一些多肽,其衍生自任何已知的actriia的序列、具有至少约80%相同于actriia多肽的序列的序列,任选地至少85%、90%、95%、97%、98%、99%或更高的同一性。例如,actriia多肽可以结合并抑制actriia蛋白质和/或激活素的功能。可以针对其促进骨骼生长和骨矿化的能力选择actriib多肽。actriia多肽的实例包括人actriia前体多肽(seqidno:1)和可溶的人actriia多肽(例如,seqidno:2、3、7和12)。对于氨基酸序列在seqidno:1中描述的actriia前体多肽,人actriia前体多肽的信号肽位于氨基酸位置1到20;细胞外结构域位于氨基酸位置21到135,人actriia前体多肽(seqidno:1)的n-连接的糖基化位点位于seqidno:1的氨基酸位置43和56。编码seqidno:1的人actriib前体多肽的核酸序列被公开为seqidno:4(genbank条目nm_001616的核苷酸164-1705)。编码seqidno:2的可溶的人actriia多肽的核酸序列被公开为seqidno:5。序列的描述参见表21。
在具体的实施方式中,本文描述的组合物和方法中使用的actriia多肽是可溶的actriia多肽。actriia蛋白的细胞外结构域可以结合激活素,一般是可溶的,因而可以称为可溶的激活素结合actriia多肽。因而,如本文使用的,术语“可溶的actriia多肽”一般是指包含actriia蛋白的细胞外结构域的多肽,包括actriia蛋白的任何天然发生的细胞外结构域以及其任何变体(包括突变体、片段、肽模拟物形式)。可溶的actriia多肽可以结合激活素;然而,野生型actriia蛋白在结合激活素与gdf8/11方面不展现显著的选择性。天然的或改变的actriia蛋白可以添加对激活素的特异性,通过将它们与第二激活素选择结合试剂偶联。可溶的激活素结合actriia多肽的实例包括seqidno:2、3、7、12和13中例举的可溶多肽。可溶的激活素结合actriia多肽的其他实例除了actriia蛋白的细胞外结构域之外包括信号序列,例如,蜜蜂蜂毒前导序列(seqidno:8)、组织纤溶酶原激活物(tpa)前导区(seqidno:9)或天然actriia前导区(seqidno:10)。seqidno:13中例举的actriia-hfc多肽使用tpa前导区。
在某些实施方式中,本文描述的组合物和方法中使用的actriia信号转导的抑制剂包含轭合物/融合蛋白,其包含与抗体的fc部分连接的actriia的激活素结合结构域。在某些实施方式中,激活素结合结构域通过接头,例如肽接头连接到抗体的fc部分。任选地,所述fc结构域在残基例如asp-265、赖氨酸322和asn-434处具有一个或更多个突变。在某些情况下,具有一个或更多个这些突变(例如,asp-265突变)的突变fc结构域相对于野生型fc结构域具有降低的结合fcγ受体的能力。在其它情况下,具有一个或更多个这些突变(例如,asn-434突变)的突变fc结构域相对于野生型fc结构域具有提高的结合mhci类相关fc受体(fcrn)的能力。包含与fc结构域融合的actriia的可溶细胞外结构域的示范性的融合蛋白在seqidno:6、7、12和13中列出。
在具体的实施方式中,本文描述的组合物和方法中使用的actriia信号转导抑制剂包含与抗体的fc部分连接的actriia的细胞外结构域,或其部分,其中所述actriia信号转导抑制剂包含至少75%相同于选自seqidno:6、7、12和13的氨基酸序列的氨基酸序列。在另一个具体的实施方式中,本文描述的组合物和方法中使用的actriia信号转导抑制剂包含与抗体的fc部分连接的actriia的细胞外结构域,或其部分,其中所述actriia信号转导抑制剂包含至少80%、85%、90%、95%、96%、97%、98%或99%相同于选自seqidno:6、7、12和13的氨基酸序列的氨基酸序列。
在某些实施方式中,本文描述的组合物和方法中使用的actriia信号转导的抑制剂包含actriia的细胞外结构域的截短的形式。所述截短可以是在actriia多肽的羧基末端和/或氨基末端。在某些实施方式中,相对于成熟的actriib多肽细胞外结构域,所述截短可以是1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24或25个氨基酸长度。在某些实施方式中,所述截短可以是1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24或25个成熟actriia多肽细胞外结构域的n-末端氨基酸。在某些实施方式中,所述截短可以是1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24或25个成熟actriia多肽细胞外结构域的c-末端氨基酸。例如,actriia的截短形式包括具有氨基酸20-119;20-128;20-129;20-130;20-131;20-132;20-133;20-134;20-131;21-131;22-131;23-131;24-131;和25-131的多肽,其中所述氨基酸位置参考seqidno:1中的氨基酸位置。
在某些实施方式中,本文描述的组合物和方法中使用的actriia信号转导的抑制剂包含具有一个或更多个氨基酸取代的actriia的细胞外结构域。在某些实施方式中,本文描述的组合物和方法中使用的actriia信号转导的抑制剂包含还带有氨基酸取代的actriia细胞外结构域的截短的形式。
在具体的实施方式中,用于本文描述的组合物和方法的actriia信号转导抑制剂是人actriia受体的细胞外结构域与igg1的fc部分之间的融合蛋白。在另一个具体的实施方式中,用于本文描述的组合物和方法的actriia信号转导抑制剂是人actriia受体的截短的细胞外结构域与igg1的fc部分之间的融合蛋白。在另一个具体的实施方式中,用于本文描述的组合物和方法的actriia信号转导抑制剂是人actriia受体的截短的细胞外结构域与igg1的fc部分之间的融合蛋白,其中所述人actriia受体的截短的细胞外结构域具有一个或更多个氨基酸取代。
例如,通过筛选重组地产自编码actriia多肽的核酸的相应片段的多肽,可以获得actriia多肽的功能活性片段。此外,片段可以使用本领域已知的技术例如,常规的merrifield固相f-moc或t-boc化学作用来化学地合成。所述片段可以被产生(重组地或通过化学合成)和测试,来鉴定可以用作actriia蛋白的或激活素介导的信号转导的拮抗剂(抑制剂)的那些肽片段。
此外,例如,通过筛选重组地产自编码actriia多肽的相应诱变核酸的修饰多肽的文库,可以获得actriia多肽的功能活性的变体。所述变体可以被产生和测试,来鉴定可以用作actriia蛋白的或激活素介导的信号转导的拮抗剂(抑制剂)的那些。在某些实施方式中,actriia多肽的功能变体包含至少75%相同于选自seqidno:2或3的氨基酸序列的氨基酸序列。在某些情况下,所述功能变体具有至少80%、85%、90%、95%、97%、98%、99%或100%相同于选自seqidno:2或3的氨基酸序列的氨基酸序列。
例如,通过为了诸如增强效力或稳定性(例如,体外货架寿命或对体内蛋白水解降解的抗性)的目的修饰actriia多肽的结构,可以产生功能变体。当被选择以保持激活素结合时,这种修饰的actriia多肽可以被认为是天然发生的actriia多肽的功能等效物。例如,通过氨基酸取代、删除或添加,也可以产生修饰的actriia多肽。例如,合理的是预计,亮氨酸用异亮氨酸或缬氨酸、天冬氨酸用谷氨酸、苏氨酸用丝氨酸的独立替换,或氨基酸用结构相关氨基酸的相似性替换(例如,保守突变)将不会对产生的分子的生物学活性有重大的影响。保守性替换是在其侧链相关的氨基酸家族内发生的替换。通过评估变体actriia多肽在细胞中以类似于野生型actriia多肽的方式产生反应的能力,actriia多肽的氨基酸序列改变是否产生功能性同源物可以容易地测定。
在某些实施方式中,在本文提供的描述的组合物和方法中使用的actriia信号转导抑制剂可以包含actriia多肽,所述actriia多肽具有可以改变所述多肽的糖基化的一个或更多个特定突变。这样的突变可以引入或除去一个或更多个糖基化位点,例如,o-连接的或n-连接的糖基化位点。天冬酰胺连接的糖基化识别位点一般包含三肽序列,天冬酰胺-x-苏氨酸(或天冬酰胺-x-丝氨酸)(其中“x”是任意氨基酸),其被适当的细胞糖基化酶特异性地识别。也可以通过向野生型actriia多肽的序列中添加或取代一个或多个丝氨酸或苏氨酸残基(用于o-连接的糖基化位点)来进行改变。在糖基化识别位点的第一或第三个氨基酸位置的一个或两个上的各种氨基酸取代或删除(和/或在第二位置上的氨基酸删除)引起所述修饰的三肽序列处的非糖基化。提高actriia多肽上碳水化合物部分的数量的另一种方式是通过糖苷对actriia多肽的化学或酶学偶联。取决于使用的偶联方式,糖可以附着于(a)精氨酸和组氨酸;(b)游离羧基基团;(c)游离巯基基团,例如半胱氨酸的;(d)游离羧基基团,例如,丝氨酸、苏氨酸或羟脯氨酸的;(e)芳香族残基,例如苯丙氨酸、酪氨酸或色氨酸的;或(f)谷氨酰胺的酰胺基团。这些方法在1987年9月11日公开的wo87/05330中,以及在aplinandwriston(1981)crccrit.rev.biochem.,pp.259-306中描述了,通过引用合并在本文中。除去actriia多肽上存在的一个或更多个碳水化合物部分可以化学地或酶学地实现。化学的脱糖基化可能涉及例如将actriia多肽暴露于化合物三氟甲磺酸或相当的化合物。这种处理引起除了连接的糖(n-乙酰葡萄糖胺或n-乙酰半乳糖胺)之外大部分或所有的糖的裂解,而保留氨基酸序列完整。化学的脱糖基化由hakimuddinetal.(1987)arch.biochem.biophys.259:52和edgeetal.(1981)anal.biochem.118:131进一步描述了。actriia多肽上碳水化合物部分的酶裂解可以通过使用多种内切和外切糖苷酶来实现,如thotakuraetal.(1987)meth.enzymol.138:350所描述的。actriia多肽的序列可以被调整,视情况,取决于使用的表达系统的类型,因为哺乳动物、酵母、昆虫和植物细胞可能都引入不同的糖基化模式,其可能受到肽的氨基酸序列的影响。一般地,用于人类的actriia蛋白可以在提供适当的糖基化的哺乳动物细胞系中表达,例如,hek293或cho细胞系,而其他表达系统,例如其他哺乳动物表达细胞系、具有工程化的糖基化酶的酵母细胞系以及昆虫细胞预计也是有用的。
本文进一步提供的是产生突变体的方法,特别是actriia多肽的组合突变体的集合,以及截短突变体;组合突变体的库对于鉴定功能性变体序列是特别有用的。筛选这种组合文库的目的可以是产生,例如,可以用作激动剂或拮抗剂的actriia多肽变体,或作为选择,其一起具有新的活性。下文提供了多种筛选分析,这样的分析可以用于评估变体。例如,可以筛选actriia多肽变体结合actriia配体,防止actriia配体与actriia多肽结合,或干扰由actriia配体引起的信号转导的能力。
可以产生组合衍生的变体,其相对于天然发生的actriia多肽具有选择的或一般提高的效价。同样,诱变可导致细胞内半衰期与相应的野生型actriia多肽显著不同的变体。例如,改变的蛋白可以变得对引起天然actriia多肽的破坏或灭活的蛋白水解降解或其他细胞代谢过程更稳定或更不稳定。这样的变体和编码它们的基因可以被利用通过调节actriia多肽的半衰期来改变actriia多肽水平。例如,短的半衰期可以产生更短暂的生物学效果,可以容许对象体内重组actriia多肽水平的紧密的控制。在fc融合蛋白中,突变可以在接头(如果有的话)和/或fc部分进行,来改变蛋白质的半衰期。
通过编码多肽文库的简并基因文库的方式可以产生组合文库,所述多肽文库各自包括可能的actriia多肽序列的至少一部分。例如,合成的寡核苷酸的混合物可以酶学连接到基因序列中,从而可能的actriia多肽核苷酸序列的简并集合可以作为单独的多肽表达,或作为选择,作为更大的融合蛋白的集合(例如,用于噬菌体展示)。
有许多方法可以从简并寡核苷酸序列中产生可能的同源物的文库。可以在自动dna合成仪中进行简并基因序列的化学合成,合成的基因然后可以连接到适合的载体中用于表达。简并寡核苷酸的合成是本领域公知的(参见,例如narang,sa(1983)tetrahedron39:3;itakuraetal.,(1981)recombinantdna,proc.3rdclevelandsympos.macromolecules,ed.agwalton,amsterdam:elsevierpp273-289;itakuraetal.,(1984)annu.rev.biochem.53:323;itakuraetal.,(1984)science198:1056;ikeetal.,(1983)nucleicacidres.11:477)。这样的技术已经用于其他蛋白质的定向进化(参见,例如scottetal.,(1990)science249:386-390;robertsetal.,(1992)pnasusa89:2429-2433;devlinetal.,(1990)science249:404-406;cwirlaetal.,(1990)pnasusa87:6378-6382;以及美国专利nos.5,223,409,5,198,346和5,096,815)。
做为选择,可以利用其他形式的诱变来产生组合文库。例如,actriia多肽变体可以通过筛选来从文库中产生和分离,利用,例如,丙氨酸扫描诱变等(rufetal.,(1994)biochemistry33:1565-1572;wangetal.,(1994)j.biol.chem.269:3095-3099;balintetal.,(1993)gene137:109-118;grodbergetal.,(1993)eur.j.biochem.218:597-601;nagashimaetal.,(1993)j.biol.chem.268:2888-2892;lowmanetal.,(1991)biochemistry30:10832-10838;和cunninghametal.,(1989)science244:1081-1085),通过接头扫描诱变(gustinetal.,(1993)virology193:653-660;brownetal.,(1992)mol.cellbiol.12:2644-2652;mcknightetal.,(1982)science232:316);通过饱和诱变(meyersetal.,(1986)science232:613);通过pcr诱变(leungetal.,(1989)methodcellmolbiol1:11-19);或通过随机诱变,包括化学诱变等(milleretal.,(1992)ashortcourseinbacterialgenetics,cshlpress,coldspringharbor,n.y.;和greeneretal.,(1994)strategiesinmolbiol7:32-34)。接头扫描诱变,特别是在组合场景中,是鉴定actriia多肽的截短形式(生物活性)的吸引人的方法。
大量的技术是本领域已知的,用于筛选由点突变或截短产生的组合库的基因产物,就此而言,用于筛选cdna库中具有某些性质的基因产物。这些技术一般将适合于通过actriia多肽的组合诱变产生的基因库的快速筛选。用于筛选大的基因文库的最广泛使用的技术一般包括将基因文库克隆到可复制的表达载体中,用产生的载体库转化合适的细胞,并在一定条件下表达组合的基因,在所述条件中期望的活性的检测便于相对容易地分离编码被检出产物的基因的载体。优选的分析包括激活素结合分析和激活素介导的细胞信号转导分析。
在某些实施方式中,本文描述的方法和组合物的抑制剂中使用的actriia多肽可以进一步包含翻译后修饰,除了天然存在于所述actriia多肽中的之外。这种的修饰可以包括但不限于,乙酰化、羧基化、糖基化、磷酸化、脂质化和酰化。结果,修饰的actriia多肽可以含有非氨基酸元件,例如,聚乙二醇、脂质、聚糖或单体和磷酸盐。这种非氨基酸元件对actriia多肽的功能的影响可以通过熟练技术人员已知的任何方法来测试。当通过裂解actriia多肽的新生形式来在细胞中产生actriia多肽时,翻译后的加工对于蛋白质的正确折叠和/或功能可能也是重要的。不同的细胞(例如cho、hela、mdck、293、w138、nih-3t3或hek293)具有这种翻译后活性的特定细胞机制和特征性的机制,可以选择来确保actriia多肽的正确修饰和加工。
在某些方面,本文描述的方法和组合物的抑制剂中使用的actriia多肽的功能变体或修饰形式包括具有至少一部分actriia多肽和一个或更多个融合结构域的融合蛋白。这样的融合结构域的公知的实例包括但不限于,多组氨酸、glu-glu、谷胱甘肽s转移酶(gst)、硫氧还蛋白、蛋白a、蛋白g、免疫球蛋白重链恒定区(fc)、麦芽糖结合蛋白(mbp)或人血清白蛋白。可以选择融合结构域以赋予期望的性质。例如,某些融合结构域对于通过亲和层析分离融合蛋白是特别有用的。对于亲和纯化来说,使用亲和层析的相关基质,例如,谷胱甘肽-、淀粉酶-和镍-或钴-轭合的树脂。许多这样的基质是以“试剂盒”形式可获得的,例如,对于(his6)融合配体有用的pharmaciagst纯化系统,以及qiaexpress.tm.系统(qiagen)。作为另一个实例,可以选择融合结构域以促进actriia多肽的检测。这样的检测结构域的实例包括各种荧光蛋白(例如,gfp),以及“表位标签”,其通常是有特异性抗体的短肽序列。特异性单克隆抗体容易获得的公知的表位标签包括flag、流感病毒血凝素(ha)和c-myc标签。在某些情况下,融合结构域具有蛋白酶裂解位点,例如,因子xa或凝血酶的,其容许相关蛋白酶部分地消化所述融合蛋白,从而由此释放重组蛋白质。释放的蛋白质然后可以通过随后的层析分离与融合结构域分离。在某些优选的实施方式中,actriia多肽与使所述actriia多肽在体内稳定化的结构域融合(“稳定物”结构域)。“稳定”是指提高血清半衰期的任何事,不论是由于降低的破坏、降低的肾脏清除、还是其他的药物动力学效应。已知与免疫球蛋白的fc部分融合为大范围的蛋白质赋予期望的药物动力学性质。同样地,与人血清白蛋白融合可以赋予期望的性质。可以选择的其他类型的融合结构域包括多聚化(例如,二聚化、四聚化)结构域和功能结构域(赋予其他生物学功能的,例如,进一步刺激骨骼生长或肌肉生长,如所希望的)。
要理解的是融合蛋白的不同元件可以以与期望的功能一致的任何方式布置。例如,actriia多肽可以置于异源结构域的c-末端,或做为选择,异源结构域可以置于actriia多肽的c-末端。actriia多肽结构域和异源结构域不必在融合蛋白中相邻,其他的结构域或氨基酸序列可以被包括在任一结构域的c-末端或n-末端,或两个结构域之间。
在某些实施方式中,本文描述的方法和组合物的抑制剂中使用的actriia多肽可以含有能够稳定化所述actriia多肽的一个或更多个修饰。例如,这样的修饰可以增强actriia多肽的体外半衰期,增强actriia多肽的循环半衰期,或降低actriia多肽的蛋白水解酶降解。这样的稳定化修饰可以包括,但不限于,融合蛋白(包括,例如,包含actriia多肽和稳定化结构域的融合蛋白)、糖基化位点的修饰(包括,例如,向actriia多肽添加糖基化位点),以及碳水化合物部分的修饰(包括,例如,从actriia多肽除去碳水化合物部分)。对于融合蛋白来说,actriia多肽融合到稳定物结构域,例如igg分子(例如,fc结构域)。如本文使用的,术语“稳定物结构域”不仅是指融合蛋白情况下的融合结构域(例如,fc),还包括非蛋白性的修饰,例如,碳水化合物部分,或非蛋白性的聚合物,例如,聚乙二醇。
在某些实施方式中,分离自或基本上没有其他蛋白质的actriia多肽的分离的和/或纯化的形式可以用于本文描述的方法和组合物。actriia多肽一般可以通过从重组核酸表达来产生。
在某些方面,本文描述的组合物和方法中使用的actriia多肽使用分离的和/或重组的核酸产生,所述核酸编码任一种actriia多肽(例如,可溶的actriia多肽),包括本文公开的片段、功能变体和融合蛋白。例如,是4编码天然发生的人actriia前体多肽,而seqidno:5编码actriia的加工的细胞外结构域。这样的核酸可以是单链的或是双链的。所述核酸可以是dna或rna分子。这些核酸可以用于,例如,制造actriia多肽的方法,或作为直接的治疗试剂(例如,在基因治疗方法中)。
在某些方面,编码actriia多肽的核酸可以包括作为seqidno:4或5的变体的核酸。变体核苷酸序列包括差异在于一个或更多个核苷酸取代、添加或删除的序列,例如,等位变体。
在某些实施方式中,编码actriia多肽的分离的或重组的核酸序列可以是至少80%、85%、90%、95%、97%、98%、99%或100%相同于seqidno:4或5。本领域普通技术人员将理解,与seqidno:4或5互补的核酸序列以及seqidno:4或5的变体可以用于生产适用于本文描述的方法和组合物的actriia多肽。在进一步的实施方式中,这样的核酸序列可以是分离的,重组的和/或融合到异源核苷酸序列的,或是来自dna文库。
在其他实施方式中,用于生产适用于本文描述的方法和组合物的actriia多肽的核酸可以包括在高度严格条件下与seqidno:4或5指定的核苷酸序列、seqidno:4或5的互补序列或其片段杂交的核苷酸序列。本领域普通技术人员将理解,促进dna杂交的合适的严格条件可以是变化的。例如,人们可以在6.0倍氯化钠/柠檬酸钠(ssc)、大约45℃下杂交,最后2.0倍ssc在50℃下洗涤。例如,洗涤步骤中的盐浓度可以选自50℃下的约2.0倍ssc的低严格度,到50℃下约0.2倍ssc的高严格度。此外,洗涤步骤中的温度可以从室温约22℃下的低严格条件,提高到大约65℃的高严格条件。温度和盐度可以都变化,或者温度或盐浓度保持不变而另一个变量发生改变。在一个实施方式中,在6倍ssc室温下的低严格条件下杂交、随后在室温下2倍ssc洗涤的核酸可以用于本文描述的方法和组合物。
由于遗传密码的简并性而不同于seqidno:4或5中所列核酸的分离的核酸也可以用于生产适用于本文描述的方法和组合物的actriia多肽。例如,许多氨基酸由超过一种三联体指定。指定相同氨基酸的密码子,或同义密码子(例如,cau和cac对于组氨酸是同义的)可以产生“沉默”突变,其不影响蛋白质的氨基酸序列。然而,预计的是,引起目标蛋白质的氨基酸序列改变的dna序列多态性将存在于哺乳动物细胞。本领域技术人员将理解,编码特定蛋白质的核酸的一个或更多个核苷酸(达到核苷酸的约3-5%)中的这些变异由于天然的等位变异可以存在于给定物种的个体中。
在某些实施方式中,重组核酸可以可操作连接到表达构建体中的一个或更多个调节核苷酸序列。调节核苷酸序列一般将适合于用来表达的宿主细胞。许多类型的适当的表达载体和适合的调节序列是本领域已知的,用于多种宿主细胞。一般地,所述一个或更多个调节核苷酸序列可以包括,但不限于,启动子序列、前导区或信号序列、核糖体结合位点、转录起始和终止序列、翻译起始和终止序列,以及增强子或激活物序列。本领域已知的组成型或可诱导启动子是本文期待的。启动子可以是天然发生的启动子,或组合了超过一种启动子的元件的杂合启动子。表达构建体可以存在于细胞中或游离体例如质粒上,或者表达构建体可以插入染色体中。在优选的实施方式中,表达载体含有选择性标记基因以容许选择转化的宿主细胞。选择性标记基因是本领域公知的,将随使用的宿主细胞而变化。
在某些方面,适用于本文描述的方法和组合物的actriia多肽的生产中使用的核酸可以在表达载体中提供,所述表达载体包含编码actriia多肽的核苷酸序列并与至少一个调节序列可操作连接。调节序列是公知的,被选择来指导actriia多肽的表达。因而,术语调节序列包括启动子、增强子和其他表达控制元件。示范性的调节序列在goeddel;geneexpressiontechnology:methodsinenzymology,academicpress,sandiego,calif.(1990)中描述。例如,控制与之可操作地连接的dna序列的表达的各种表达控制序列的任一种,可以用于这些载体来表达编码actriia多肽的dna序列。这类有用的表达控制序列包括,例如,sv40的早期和晚期启动子、tet启动子、腺病毒或巨细胞病毒即时早期启动子、rsv启动子、lac系统、trp系统、tac或trc系统、其表达由t7rna聚合酶指导的t7启动,噬菌体λ的主要操纵子和启动子区域,ft衣壳蛋白的控制区域、3-磷酸甘油酸激酶或其他糖酵解酶的启动子、酸性磷酸酶例如pho5的启动子、酵母.alpha.接合因子的启动子、杆状病毒系统的多面体启动子,以及已知控制原核和真核细胞以及它们的病毒的基因表达的其他序列,以及它们的各种组合。要理解的是,表达载体的设计可以取决于这些因素,如要转化的宿主细胞的选择,和/或希望表达的蛋白质的类型。此外,还应当考虑载体的拷贝数、控制拷贝数的能力以及载体编码的任何其他蛋白质的表达,例如抗生素标志物。
适用于本文描述的方法和组合物的actriia多肽的生产中使用的重组核酸可以通过将克隆的基因或其部分连接到适合于在原核细胞、真核细胞(酵母、禽类、昆虫或哺乳动物)或两者中表达的载体中来产生。用于重组actriia多肽的生产的表达载体包括质粒和其他载体。例如,适合的载体包括质粒类型:pbr322衍生的质粒、pembl衍生的质粒、pex衍生的质粒、pbtac衍生的质粒和puc-衍生的质粒,用于在原核细胞例如e.coli中表达。
某些哺乳动物表达载体含有原核序列来促进载体在细菌中的增殖,以及含有一种或更多种在真核细胞中表达的真核转录单位。pcdnai/amp、pcdnai/neo、prc/cmv、psv2gpt、psv2neo、psv2-dhfr、ptk2、prsvneo、pmsg、psvt7、pko-neo和phyg衍生的载体是适合于转染真核细胞的哺乳动物表达载体的实例。这些载体的一些被来自细菌质粒例如pbr322表达序列修饰,来促进在原核和真核细胞两者中的复制和药物抗性选择。做为选择,病毒的衍生物,例如,牛乳头状瘤病毒(bpv-1)或epstein-barr病毒(phebo、prep-衍生的和p205)可以用于蛋白质在真核细胞中的短暂表达。其他病毒(包括逆转录病毒)表达系统的实例可以在下文基因治疗递送系统的说明中找到。制备质粒和转化宿主生物体所采用的各种方法是本领域公知的。对于原核和真核细胞都适合的其他表达系统,以及一般的重组过程,参见molecularcloningalaboratorymanual,3rded.,ed.bysambrook,fritschandmaniatis(coldspringharborlaboratorypress,2001)。在某些情况下,可能希望的是通过使用杆状病毒表达系统来表达重组多肽。这样的杆状病毒表达系统的实例包括pvl衍生的载体(例如,pvl1392、pvl1393和pvl941)、pacuw衍生的载体(例如pacuw1)和pbluebac-衍生的载体(例如含有.beta.-gal的pbluebaciii)。
载体可以被设计用于在cho细胞中生产目标actriia多肽,例如,pcmv-script载体(stratagene,lajolla,calif.)、pcdna4载体(invitrogen,carlsbad,calif.)和pci-neo载体(promega,madison,wis.)。明显的是,目标基因构建体可以用于引起目标actriia多肽在培养物中增殖的细胞中表达,例如,来产生蛋白质,包括融合蛋白或变体蛋白,用于纯化。
用包括一种或更多种目标actriia多肽的编码序列(例如,seqidno:4或5)的重组基因转染的宿主细胞可以用于生产适用于本文描述的方法和组合物的actriia多肽。所述宿主细胞可以是任何原核或真核细胞。例如,本文提供的actriia多肽可以在细菌细胞例如e.coli、昆虫细胞(例如,使用杆状病毒表达系统)、酵母或哺乳动物细胞中表达。其他适合的宿主细胞是本领域技术人员公知的。
因而,本文提供的是生产actriia多肽的方法。例如,用编码actriia多肽的表达载体转染的宿主细胞可以在适当的条件下培养来容许发生actriia多肽的表达。从细胞与含有actriia多肽的培养基的混合物中,可以分泌和分离actriia多肽。做为选择,actriia多肽可以细胞质地或在膜部分中保持,收获细胞、裂解并分离蛋白。细胞培养物包括宿主细胞、培养基和其他副产物。用于细胞培养的适合的培养基是本领域公知的。利用本领域已知的用于纯化蛋白质的技术,可以从细胞培养介质、宿主细胞或两者分离目标actriia多肽,包括离子交换层析、凝胶过滤层析、超滤、电泳、使用特异于actriia多肽的特定表位的抗体的免疫亲和纯化、以及使用结合与actriia多肽融合的结构域的试剂的亲和纯化(例如,蛋白a柱可以用于纯化actriia-fc融合物)。在优选的实施方式中,actriia多肽是含有便于其纯化的结构域的融合蛋白。在一个实施方式中,纯化通过一系列柱层析步骤来实现,包括,例如,三种或更多种以下的,按任何顺序:蛋白a层析、q琼脂糖层析、苯基琼脂糖层析、空间排阻层析和阳离子交换层析。纯化可以用病毒过滤和缓冲液交换来完成。如本文表明的,actriia-hfc蛋白可以纯化到通过空间排阻层折测定的>98%的纯度,和通过sds-page测定的>95%的纯度。这一水平的纯度足以在小鼠中对骨骼实现期望的效果,以及在小鼠、大鼠和非人灵长类中实现可接受的安全分布。
在另一个实施方式中,编码位于重组actriia多肽的期望部分的n-末端的纯化前导序列例如聚-(his)/肠激酶裂解位点序列的融合基因可以容许表达的融合蛋白通过利用ni2+金属树脂的亲和层析来纯化。纯化前导序列然后通过用肠激酶处理来除去,以提供纯化的actriia多肽(例如,参见hochulietal.,(1987)j.chromatography411:177;和janknechtetal.,pnasusa88:8972)。
用于制造融合基因的技术是公知的。基本上,根据常规技术进行编码不同多肽序列的各种dna片段的连接,采用钝末端的或交错末端的末端用于连接,限制酶消化来提供适当的末端,视情况填充粘末端,碱性磷酸酶处理来避免不希望的连接,以及酶连接。在另一个实施方式中,融合基因可以通过常规技术,包括自动的dna合成仪来合成。做为选择,可以使用锚引物来进行基因片段的pcr扩增,所述锚引物产生两个连续基因片段之间的互补的突出,其随后可以退火来产生嵌合基因序列(参见,例如currentprotocolsinmolecularbiology,eds.ausubeletal.,johnwiley&sons:1992)。
actriia-fc融合蛋白可以从paid4载体(sv40ori/增强子,cmv启动子)在稳定地转染的cho-dukxbl1细胞中表达,使用seqidno:9的组织血纤蛋白溶酶原前导序列。fc部分是人igg1fc序列,如seqidno:7所示。在某些实施方式中,在表达时,平均起来,所含的蛋白质具有每分子的actriia-fc融合蛋白约1.5到2.5摩尔的唾液酸。
在某些实施方式中,actriia-fc融合物的长血清半衰期可以是在人类对象中25-32天。另外,相比在人293细胞中表达的actriia-hfc融合蛋白所报告的,cho细胞表达的材料可以具有更高的对激活素b配体的亲和力(delreetal.,jbiolchem.2004dec17;279(51):53126-35)。另外,不受理论的限制,使用比其他前导序列提供更高生产的tpa前导序列,不同于用天然前导区表达的actriia-fc,可以提供高纯度的n-末端序列。使用天然前导序列可能产生两种主要种类的actriia-fc,各自具有不同的n-末端序列。
8.5.2actriib信号转导的抑制剂
如本文使用的,术语“actriib”是指来自任何物种的激活素iib型受体(actriib)蛋白的家族,以及通过诱变或其他修饰衍生自这些actriib蛋白的变体。本文提及actriib被理解为是提及所述受体的当前鉴定的形式的任一种。actriib家族的成员一般是跨膜的蛋白质,由具有富半胱氨酸区的配体结合细胞外结构域、跨膜结构域、以及具有预测的丝氨酸/苏氨酸激酶活性的细胞质结构域组成。
本文描述的组合物和方法中使用的actriib信号转导抑制剂包括,非限制性地,激活素结合可溶actriib多肽;结合激活素(特别是激活素a或b亚基,也称为βa或βb)并破坏actriib结合的抗体;结合actriib并破坏激活素结合的抗体;为激活素或actriib结合选择的非抗体蛋白质;以及为激活素或actriib结合选择的随机肽,其可以轭合到fc结构域。
在某些实施方式中,具有激活素或actriib结合活性的两种或更多种不同的蛋白质(或其他部分),特别是分别阻断i型(例如,可溶的i型激活素受体)和ii型(例如,可溶的ii型激活素受体)结合位点的激活素结合物可以连接在一起,产生抑制actriib信号转导的双功能或多功能结合分子,因而可以用于本文描述的组合物和方法。在某些实施方式中,抑制actriib的激活素-actriib信号转导轴拮抗剂包括核酸适体、小分子和其他试剂,用于本文描述的组合物和方法中。
8.5.2.1包含actriib多肽的actriib信号转导抑制剂
如本文使用的,术语“actriib多肽”是指这些多肽,其包含actriib家族成员的任何天然发生的多肽以及保持了有用活性的其任何变体(包括突变体、片段、融合物和肽模拟物形式)例如,actriib多肽包括一些多肽,其衍生自任何已知的actriib受体的序列、具有至少约80%相同于actriib多肽的序列的序列,任选地至少85%、90%、95%、96%、97%、98%、99%或更高的同一性。例如,actriib多肽可以结合并抑制actriib蛋白质和/或激活素的功能。actriib多肽的实例包括人actriib前体多肽(seqidno:16或seqidno:28)。对于氨基酸序列描述为seqidno:16或seqidno:28的actriib前体多肽(即,人actriib前体多肽),actriib前体多肽的信号肽位于氨基酸1到18;细胞外结构域位于氨基酸19到134,潜在的n-连接的糖基化位点位于氨基酸位置42和65。编码seqidno:16的人actriib前体多肽的核酸序列以seqidno:19公开(seqidno:19提供了在相应于氨基酸位置64的密码子处的丙氨酸,但是可以由本领域技术人员使用本领域已知的方法容易地修饰,来提供相应于氨基酸位置64的密码子处的精氨酸作为替代)。序列的描述参见表21。
本文描述的所有actriib相关的多肽的氨基酸编号是基于seqidno:16和seqidno:28(其仅在位置64表达的氨基酸不同)的氨基酸编号,除非另外指定。例如,如果一actriib多肽被描述为在氨基酸位置79具有取代/突变,这将被理解为该位置79是指seqidno:16或seqidno:28中的第79个氨基酸,从其中衍生出所述actriib多肽。同样地,如果一种actriib多肽被描述为在氨基酸位置64具有丙氨酸或精氨酸,这将被理解为位置64是指seqidno:16或seqidno:28中的第64个氨基酸,从其中衍生出所述actriib多肽。
在某些实施方式中,本文描述的组合物和方法中使用的actriib信号转导的抑制剂包含多肽,所述多肽包含actriib的激活素结合结构域。在某些实施方式中,actriib的激活素结合结构域包含actriib的细胞外结构域,或其部分。在具体的实施方式中,actriib的细胞外结构域或其部分是可溶的。actriib多肽的说明性的修饰形式在美国专利申请公开no.20090005308和20100068215中公开了,其公开内容通过完全引用合并在本文中。
在具体的实施方式中,本文描述的组合物和方法中使用的actriib多肽是可溶的actriib多肽。术语“可溶的actriib多肽”一般是指包含actriib蛋白的细胞外结构域的多肽,包括actriib蛋白的任何天然发生的细胞外结构域以及其任何变体(包括突变体、片段和肽模拟物形式)。可溶的actriib多肽可以结合激活素;然而,在结合激活素与gdf8/11方面野生型actriib蛋白不展现显著的选择性。在某些实施方式中,具有不同结合性质的改变形式的actriib可以用于本文提供的方法中。这样的改变的形式公开于,例如,国际专利申请公开no.wo2006/012627和wo2010/019261,其公开内容通过完全引用合并在本文中。通过将它们与第二激活素选择性结合试剂偶联,天然的或改变的actriib蛋白可以被给与添加的对激活素的特异性。示范性的可溶的actriib多肽包括人actriib多肽的细胞外结构域(例如,seqidno:17、18、23、26、27、29、30、31、32、33、36、37、42和43)。
具有hildenetal.(blood,1994,83(8):2163-70)公开的actriib细胞外序列的fc融合蛋白,其在相应于actriib前体氨基酸序列即seqidno:16的氨基酸64的位置具有丙氨酸(本文称为“a64”),已经被证明具有对激活素和gdf-11的相对低的亲和力。相比之下,在actriib前体氨基酸序列的位置64处具有精氨酸(本文称为“r64”)的fc融合蛋白具有处于低纳摩尔到高皮摩尔范围内的对激活素和gdf-11的亲和力(参见,例如,美国专利申请公开或20100068215,其公开内容完全合并在本文中)。在位置64具有精氨酸的actriib前体氨基酸序列在seqidno:28中示出。因而,在某些实施方式中,根据本文描述的组合物和方法使用的actriib多肽可以包含(在相应于actriib前体氨基酸序列的氨基酸64的位置上的丙氨酸,即seqidno:16;或(ii)在actriib前体序列的位置64的精氨酸,即seqidno:28)。在其他实施方式中,根据本文描述的组合物和方法使用的actriib多肽可以包含在相应于actriib前体氨基酸序列,即seqidno:16或seqidno:28的氨基酸64的位置上的不是丙氨酸或精氨酸的氨基酸。
已经显示的是,删除处于actriib的细胞外结构域的c-末端的脯氨酸结降低了受体对激活素的亲和力(参见,例如,attisanoetal.,cell,1992,68(1):97-108)。相对于包括脯氨酸结区域和完整的近膜结构域、含有seqidno:28的氨基酸20-134的actriib-fc融合蛋白“actriib(20-134)-fc”,含有seqidno:28的氨基酸20-119(即,seqidno:32)的actriib-fc融合蛋白“actriib(20-119)-fc”具有降低的对gdf-11和激活素的结合。然而,相对于actriib的未截短的细胞外结构域,含有seqidno:28的氨基酸20-129的actriib-fc融合蛋白“actriib(20-129)-fc”保持了相似的但稍微降低的活性,尽管其脯氨酸结区域被破坏。因而,包含在seqidno:28的氨基酸134、133、132、131、130和129处停止的细胞外结构域的actriib多肽都被预期是有活性的,但是在氨基酸134或133停止的构建体可能具有最大活性。类似地,在残基129-134的任一个上的突变预期不会大幅度改变配体结合亲和力,如seqidno:28的p129和p130的突变实质上不降低配体结合的事实所指示的。因此,根据本文描述的方法和组合物使用的actriib多肽可以早至seqidno:28(或seqidno:16)的氨基酸109(即,最后的半胱氨酸)结束,然而,终止于seqidno:28(或seqidno:16)的氨基酸位置109到119或这之间的形式预计不具有降低的配体结合能力。
seqidno:16和seqidno:28的氨基酸29代表actriib前体序列中的最初的半胱氨酸。预计的是,在seqidno:16或seqidno:28的n-末端的氨基酸29开始或在这些氨基酸位置之前开始的actriib将保持配体结合活性。在seqidno:16或seqidno:28的位置24处丙氨酸到天冬酰胺的突变引入n-连接的糖基化位点而基本上不影响配体结合。这确认了在相应于seqidno:16或seqidno:28的氨基酸20-29的信号裂解肽和半胱氨酸交联区之间的突变是良好耐受的。特别地,在seqidno:16或seqidno:28的氨基酸位置20、21、22、23和24开始的actriib多肽将保持活性,在seqidno:16或seqidno:28的氨基酸位置25、26、27、28和29开始的actriib多肽也预期保持活性。在seqidno:16或seqidno:28的氨基酸位置22、23、24或25开始的actriib多肽将具有最大活性。
合起来,根据本文描述的方法和组合物使用的actriib前体蛋白(即,seqidno:16或seqidno:28)的活性部分(即,actriib多肽)一般将包含seqidno:16或seqidno:28的氨基酸29-109,这样的actriib多肽可以,例如,开始于与seqidno:16或seqidno:28的氨基酸19-29的任一个相应的残基,结束于与seqidno:16或seqidno:28的氨基酸109-134的任一个相应的位置。本文涵盖的actriib多肽的具体实例包括开始于seqidno:16或seqidno:28的19-29、20-29或21-29的氨基酸位置、结束于seqidno:16或seqidno:28的119-134、119-133或129-134、129-133的氨基酸位置的那些。本文涵盖的actriib多肽的其他具体实例包括开始于seqidno:16或seqidno:28的20-24(或21-24,或22-25)的氨基酸位置、结束于seqidno:16或seqidno:28的109-134(或109-133)、119-134(或119-133)或129-134(或129-133)的氨基酸位置的那些。落入这些范围的变体actriib多肽也是期待的,特别是与seqidno:16或seqidno:28的相应部分具有至少80%、85%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%的序列同一性或序列同源性的那些。
在某些实施方式中,本文描述的组合物和方法中使用的actriib信号转导的抑制剂包含actriib的细胞外结构域的截短的形式。所述截短可以是在actriib多肽的羧基末端和/或氨基末端。在某些实施方式中,相对于成熟的actriib多肽细胞外结构域,所述截短可以是1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24或25个氨基酸长度。在某些实施方式中,所述截短可以是1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24或25个成熟actriib多肽细胞外结构域的n-末端氨基酸。在某些实施方式中,所述截短可以是1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24或25个成熟actriib多肽细胞外结构域的c-末端氨基酸。例如,actriib的截短形式包括具有氨基酸20-119;20-128;20-129;20-130;20-131;20-132;20-133;20-134;20-131;21-131;22-131;23-131;24-131;和25-131的多肽,其中所述氨基酸位置参考seqidno:16或seqidno:28中的氨基酸位置。
actriib的其他示范性的截短形式包括(i)开始于seqidno:16或seqidno:28的氨基酸21-29的任一个的氨基酸(任选地开始于seqidno:16或seqidno:28的21-25)以及结束于seqidno:16或seqidno:28的氨基酸109-134的任一个的多肽;(ii)开始于seqidno:16或seqidno:28的氨基酸20-29的任一个(任选地开始于seqidno:16或seqidno:28的20-25)以及结束于seqidno:16或seqidno:28的氨基酸109-133的任一个的多肽;(iii)开始于seqidno:16或seqidno:28的氨基酸20-24的任一个(任选地开始于seqidno:16或seqidno:28的20-25)以及结束于seqidno:16或seqidno:28的氨基酸109-133的任一个的多肽;(iv)开始于seqidno:16或seqidno:28的氨基酸21-24的任一个以及结束于seqidno:16或seqidno:28的氨基酸109-134的任一个的多肽;(v)开始于seqidno:16或seqidno:28的氨基酸20-24的任一个以及结束于seqidno:16或seqidno:28的氨基酸118-133的任一个的多肽;(vi)开始于seqidno:16或seqidno:28的氨基酸21-24的任一个以及结束于seqidno:16或seqidno:28的氨基酸118-134的任一个的多肽;(vii)开始于seqidno:16或seqidno:28的氨基酸20-24的任一个以及结束于seqidno:16或seqidno:28的氨基酸128-133的任一个的多肽;(viii)开始于seqidno:16或seqidno:28的氨基酸20-24的任一个以及结束于seqidno:16或seqidno:28的氨基酸128-133的任一个的多肽;(ix)开始于seqidno:16或seqidno:28的氨基酸21-29的任一个以及结束于seqidno:16或seqidno:28的氨基酸118-134的任一个的多肽;(x)开始于seqidno:16或seqidno:28的氨基酸20-29的任一个以及结束于seqidno:16或seqidno:28的氨基酸118-133的任一个的多肽;(xi)开始于seqidno:16或seqidno:28的氨基酸21-29的任一个以及结束于seqidno:16或seqidno:28的氨基酸128-134的任一个的多肽;和(xii)开始于seqidno:16或seqidno:28的氨基酸20-29的任一个以及结束于seqidno:16或seqidno:28的氨基酸128-133的任一个的多肽。在具体的实施方式中,actriib多肽包含,基本上由以下组成,或由以下组成,开始于seqidno:16或seqidno:28的氨基酸位置25、并结束于seqidno:16或seqidno:28的氨基酸位置131的氨基酸序列。在另一个具体的实施方式中,actriib由以下组成或基本上由以下组成,seqidno:17、18、23、26、27、29、30、31、32、33、36、37、42或43的氨基酸序列。
本文描述的组合物和方法中使用的actriib多肽的任一个可以作为同二聚体生产。本文描述的组合物和方法中使用的actriib多肽的任一个可以被配制为具有异源部分的融合蛋白,其包含来自igg重链的恒定区,例如fc结构域。本文描述的组合物和方法中使用的actriib多肽的任一个可以包含处在相应于seqidno:16或seqidno:28的位置79的位置上的酸性氨基酸,任选地与相对于seqidno:16或seqidno:28的一个或更多个其他的氨基酸取代、删除或插入组合。
在具体的实施方式中,本文描述的组合物和方法中使用的actriib信号转导的抑制剂包含具有一个或更多个氨基酸取代/突变的actriib的细胞外结构域。这样的氨基酸取代/突变可以是,例如,seqidno:16或seqidno:28的氨基酸位置79处的亮氨酸交换为酸性氨基酸,例如,天冬氨酸或谷氨酸。例如,seqidno:16或seqidno:28的位置l79可以在actriib细胞外结构域多肽中改变,来赋予改变的激活素-肌肉生长抑制素(gdf-11)结合性质。相比激活素结合,l79a和l79p突变更大程度地降低gdf-11结合。l79e和l79d突变保持了gdf-11结合,而展现了大大地降低的激活素结合。
在某些实施方式中,本文描述的组合物和方法中使用的actriib信号转导的抑制剂包含截短形式的actriib细胞外结构域,其还带有氨基酸取代,例如,seqidno:16或seqidno:28的氨基酸位置79处的亮氨酸改变为酸性氨基酸,例如,天冬氨酸或谷氨酸。在具体的实施方式中,本文描述的组合物和方法中使用的还带有氨基酸取代的actriib多肽的细胞外结构域的截短形式是seqidno:23。截短的和/或带有一个或更多个氨基酸取代的actriib的形式可以如以上讨论的连接到抗体的fc结构域。
例如,通过筛选重组地产自编码actriib多肽的核酸的相应片段的多肽,可以获得actriib多肽的功能活性片段。此外,片段可以使用本领域已知的技术例如,常规的merrifield固相f-moc或t-boc化学作用来化学地合成。本领域技术人员将认识到的是,其他技术,包括例如用于肽合成的各种树脂和液相系统可以用于合成本文描述的肽基片段。所述片段可以被产生(重组地或通过化学合成)和测试,来鉴定可以用作actriib蛋白或激活素介导的信号转导的拮抗剂(抑制剂)的那些肽片段。
此外,例如,通过筛选重组地产自编码actriib多肽的相应诱变核酸的修饰多肽的文库,可以获得actriib多肽的功能活性的变体。所述变体可以被产生和测试,来鉴定可以用作actriib蛋白的或激活素介导的信号转导的拮抗剂(抑制剂)的那些。在某些实施方式中,actriib多肽的功能变体包括至少75%相同于选自seqidno:17、18、23、26、27、29、30、31、32、33、36、37、42和43的氨基酸序列的氨基酸序列。在某些实施方式中,所述功能变体具有至少80%、85%、90%、95%、96%、97%、98%或99%相同于选自seqidno:17、18、23、26、27、29、30、31、32、33、36、37、42和43的氨基酸序列的氨基酸序列。
例如,通过为了诸如增强效力或稳定性(例如,体外货架寿命或对体内蛋白水解降解的抗性)的目的修饰actriib多肽的结构,可以产生功能变体。当被选择以保持激活素结合时,这种修饰的actriib多肽可以被认为是天然发生的actriib多肽的功能等效物。例如,通过氨基酸取代、删除或添加,也可以产生修饰的actriib多肽。例如,合理的是预计,亮氨酸用异亮氨酸或缬氨酸、天冬氨酸用谷氨酸、苏氨酸用丝氨酸的独立替换,或氨基酸用结构相关氨基酸的相似性替换(例如,保守突变)将不会对产生的分子的生物学活性有重大的影响。保守性替换是在其侧链相关的氨基酸家族内发生的替换。通过评估变体actriib多肽在细胞中以类似于野生型actriib多肽的方式产生反应的能力,actriib多肽的氨基酸序列改变是否产生功能性同源物可以容易地测定。
actriib多肽突变体,特别是actriib多肽的组合突变体的集合,以及截短突变体;组合突变体的库,对于鉴定可用于本文描述的方法和组合物的功能变体序列是特别有用的。筛选这种组合文库的目的可以是产生,例如,可以用作激动剂或拮抗剂的actriib多肽变体,或作为选择,其一起具有新的活性。
已经证明的是,由seqidno:16或seqidno:28的残基y31、n33、n35、l38到t41、e47、e50、q53到k55、l57、h58、y60、s62、k74、w78到n83、y85、r87、a92和e94到f101定义了actriib的配体结合口袋。在这些位置上,预计的是保守性突变将是耐受的,而k74a突变是良好耐受的,r40a、k55a、f82a和位置l70的突变也是。在非洲蟾蜍(xenopus)中r40是k,表明这个位置的碱性氨基酸是耐受的。在牛actriib中q53是r,在非洲蟾蜍actriib中是k,因而包括r、k、q、n和h的氨基酸在这个位置将是耐受的。因而,用于本文描述的方法和组合物的actriib多肽的通式是,包含seqidno:16或seqidno:28的氨基酸29-109,但任选地开始于seqidno:16或seqidno:28的20-24或22-25的氨基酸位置,以及结束于seqidno:16或seqidno:28的129-134的氨基酸位置,在配体结合口袋中包含不超过1、2、5或15个保守氨基酸改变,以及在配体结合口袋中seqidno:16或seqidno:28的氨基酸位置40、53、55、74、79和/或82的零个、一个或更多个非保守改变。这样的actriib多肽可以保持与seqidno:16或seqidno:28的氨基酸29-109的序列大于80%、90%、95%或99%的序列同一性或序列同源性。结合口袋之外的位点,在此变异性是特别好地耐受的,包括actriib的细胞外结构域的氨基和羧基末端,以及位置42-46和65-73。seqidno:16或seqidno:28的位置65处天冬酰胺到丙氨酸的改变(n65a)实际上改善了a64背景下的配体结合,因而预计在r64背景下对配体结合没有不利影响。这种改变可能除去了a64背景下在n65处的糖基化,因而表明这个区域的显著改变可能是耐受的。虽然r64a改变是不良耐受的,r64k是良好耐受的,因而另一种碱性残基,例如,h可以在位置64处耐受。
作为在配体结合结构域中有突变的actriib多肽的具体实例,actriib的配体结合结构域的带正电氨基酸残基asp(d80)可以突变为不同的氨基酸残基,从而变体actriib多肽优先地结合gdf8而不是激活素。在具体的实施方式中,d80残基被改变为选自以下构成的组的氨基酸残基:不带电的氨基酸残基、负电氨基酸残基和疏水性氨基酸残基。作为进一步的具体实例,疏水性残基l79可以改变为酸性氨基酸天冬氨酸或谷氨酸,来大大降低激活素结合而保持gdf11结合。本领域技术人员将认识到,大多数所描述的突变体、变体或修饰体可以在核酸水平制备,或在某些情况下,通过翻译修饰或化学合成制备。这样的技术是本领域公知的。
在具体的实施方式中,本文描述的组合物和方法中使用的actriib信号转导的抑制剂包含轭合物/融合蛋白,其包含与抗体的fc部分连接的actriib受体的细胞外结构域(例如,激活素结合结构域)。这样的轭合物/融合蛋白可以包含本文公开的任何actriib多肽(例如,seqidno:17、18、23、26、27、29、30、31、32、33、36、37、42或43的任一个)、任何本领域已知的actriib多肽或使用本领域已知的和/或本文提供的方法产生的任何actriib多肽。
在某些实施方式中,细胞外结构域通过接头,例如肽接头连接到抗体的fc部分。示范性的接头包括短多肽序列,例如2-10、2-5、2-4、2-3个氨基酸残基(例如,甘氨酸残基),例如,gly-gly-gly接头。在具体的实施方式中,所述接头包含氨基酸序列gly-gly-gly(ggg)。在另一个具体的实施方式中,所述接头包含氨基酸序列thr-gly-gly-gly(tggg)。任选地,所述fc结构域在残基例如asp-265、赖氨酸322和asn-434处具有一个或更多个突变。在某些情况下,具有一个或更多个这些突变(例如,asp-265突变)的突变fc结构域具有相对于野生型fc结构域降低的结合fcγ受体的能力。在其它情况下,具有一个或更多个这些突变(例如,asn-434突变)的突变fc结构域相对于野生型fc结构域具有提高的结合mhci类相关fc受体(fcrn)的能力。包含与fc结构域融合的actriib的可溶细胞外结构域的示范性的融合蛋白在seqidno:20、21、24、25、34、35、38、39、40、41、44、46和47中列出。
在具体的实施方式中,本文描述的组合物和方法中使用的actriib信号转导抑制剂包含与抗体的fc部分连接的actriib的细胞外结构域,或其部分,其中所述actriib信号转导抑制剂包含至少75%相同于选自seqidno:20、21、24、25、34、35、38、39、40、41、44、46和47的氨基酸序列的氨基酸序列。在另一个具体的实施方式中,本文描述的组合物和方法中使用的actriib信号转导抑制剂包含与抗体的fc部分连接的actriib的细胞外结构域,或其部分,其中所述actriib信号转导抑制剂包含至少80%、85%、90%、95%、96%、97%、98%或99%相同于选自seqidno:20、21、24、25、34、35、38、39、40、41、44、46和47的氨基酸序列的氨基酸序列。
在具体的实施方式中,用于本文描述的组合物和方法的actriib信号转导抑制剂是人actriib受体的细胞外结构域与igg1的fc部分之间的融合蛋白。在另一个具体的实施方式中,用于本文描述的组合物和方法的actriib信号转导抑制剂是人actriib受体的截短的细胞外结构域与igg1的fc部分之间的融合蛋白。在另一个具体的实施方式中,用于本文描述的组合物和方法的actriib信号转导抑制剂是人actriib受体的截短的细胞外结构域与igg1的fc部分之间的融合蛋白,其中所述人actriib受体的截短的细胞外结构域具有相应于seqidno:16或seqidno:28的氨基酸79的氨基酸位置处的氨基酸取代。在一个实施方式中,在相应于seqidno:16或seqidno:28的氨基酸79的氨基酸位置处的氨基酸取代是亮氨酸到天冬氨酸的取代(即,l79d突变)。
在具体的实施方式中,用于本文描述的组合物和方法的actriib信号转导抑制剂是seqidno:24或25,其代表人actriib受体的细胞外结构域与igg1的fc部分之间的融合蛋白,其中所述actriib细胞外结构域包含带有l79d突变的seqidno:28的氨基酸25-131。编码seqidno:24的actriib-fc融合蛋白的核酸序列在seqidno:45中示出。
在另一个具体的实施方式中,用于本文描述的组合物和方法的actriib信号转导抑制剂是seqidno:34或35,其代表人actriib受体的细胞外结构域与igg1的fc部分之间的融合蛋白,其中所述actriib细胞外结构域包含带有l79d突变的seqidno:16的氨基酸25-131。
天冬酰胺连接的糖基化识别位点一般包含三肽序列,天冬酰胺-x-苏氨酸(或天冬酰胺-x-丝氨酸)(其中“x”是任意氨基酸),其被适当的细胞糖基化酶特异性地识别。也可以通过向野生型actriib多肽的序列中添加或取代一个或多个丝氨酸或苏氨酸残基(用于o-连接的糖基化位点)来进行改变。在糖基化识别位点的第一或第三个氨基酸位置的一个或两个上的各种氨基酸取代或删除(和/或在第二位置上的氨基酸删除)引起所述修饰的三肽序列处的非糖基化。提高actriib多肽上碳水化合物部分的数量的另一种方式是通过糖苷对actriib多肽的化学或酶学偶联。取决于使用的偶联方式,糖可以附着于(a)精氨酸和组氨酸;(b)游离羧基基团;(c)游离巯基基团,例如半胱氨酸的;(d)游离羧基基团,例如,丝氨酸、苏氨酸或羟脯氨酸的;(e)芳香族残基,例如苯丙氨酸、酪氨酸或色氨酸的;或(f)谷氨酰胺的酰胺基团。这些方法在1987年9月11日公开的wo87/05330中,以及在aplinandwriston(1981)crccrit.rev.biochem.,pp.259-306中描述了,通过引用合并在本文中。除去actriib多肽上存在的一个或更多个碳水化合物部分可以化学地或酶学地实现。化学的脱糖基化可能涉及例如将actriib多肽暴露于化合物三氟甲磺酸或相当的化合物。这种处理引起除了连接的糖(n-乙酰葡萄糖胺或n-乙酰半乳糖胺)之外大部分或所有的糖的裂解,而保留氨基酸序列完整。化学的脱糖基化由hakimuddinetal.(1987)arch.biochem.biophys.259:52和edgeetal.(1981)anal.biochem.118:131进一步描述了。actriib多肽上碳水化合物部分的酶裂解可以通过使用多种内切和外切糖苷酶来实现,如thotakuraetal.(1987)meth.enzymol.138:350所描述的。actriib多肽的序列可以被调整,视情况,取决于使用的表达系统的类型,因为哺乳动物、酵母、昆虫和植物细胞可能都引入不同的糖基化模式,其可能受到肽的氨基酸序列的影响。一般地,用于人类的actriib蛋白将在提供适当的糖基化的哺乳动物细胞系中表达,例如,hek293或cho细胞系,而其他表达系统,例如其他哺乳动物表达细胞系、具有工程化的糖基化酶的酵母细胞系以及昆虫细胞预计也是有用的。
在具体的实施方式中,相对于actriib(r64)-fc形式,包含了提高actriib-fc融合蛋白的血清半衰期的进一步的n-连接的糖基化位点(n-x-s/t)的突变的actriib多肽可以用于本文描述的方法和组合物中。在具体的实施方式中,在seqidno:16或seqidno:28的位置24处引入天冬酰胺(a24n)产生了赋予更长半衰期的nxt序列。其他nx(t/s)序列可以在42-44(nqs)和65-67(nss)中找到,而后者可能不不能用位置64的r有效地糖基化(即,在r64多肽中)。n-x-s/t序列一般可以引入到actriib的配体结合口袋之外的位置,其在上文中详述了。对于引入非内源的n-x-s/t序列特别适合的位点包括seqidno:16或seqidno:28的氨基酸20-29、20-24、22-25、109-134、120-134或129-134。n-x-s/t序列还可以导入到actriib序列与fc或其他融合部件之间的接头中。因而,产生n-连接的糖基化位点的可取的改变是:a24n、r64n、s67n(可能与n65a改变组合)、e106n、r112n、g120n、e123n、p129n、a132n、r112s和r112t(所有氨基酸位置相应于它们在seqidno:16或seqidno:28中的位置)。预计诶糖基化的任何s可以改变为t,而不产生免疫原性位点,因为由糖基化提供了保护。同样地,预计被糖基化的任何t可以改变为s。因而,改变s67t和s44t被涵盖在此。同样地,在a24n变体中,可以使用s26t改变。因而,actriib多肽可以包括一个或更多个额外的、非内源的n-连接的糖基化共有序列。
多种筛选分析可以用于评估actriib多肽变体。例如,可以筛选actriib多肽变体结合actriib配体,防止actriib配体与actriib多肽结合,或干扰由actriib配体引起的信号转导的能力。actriib多肽或其变体活性也可以在基于细胞的或体内的分析中测试。
可以产生组合衍生的变体,其相对于天然发生的actriib多肽具有选择的或一般提高的效价。同样,诱变可导致细胞内半衰期与相应的野生型actriib多肽显著不同的变体。例如,改变的蛋白可以变得对引起天然actriib多肽的破坏或灭活的蛋白水解降解或其他细胞代谢过程更稳定或更不稳定。这样的变体和编码它们的基因可以被利用通过调节actriib多肽的半衰期来改变actriib多肽水平。例如,短的半衰期可以产生更短暂的生物学效果,可以容许对象体内重组actriib多肽水平的紧密的控制。在fc融合蛋白中,突变可以在接头(如果有的话)和/或fc部分进行,来改变蛋白质的半衰期。
通过编码多肽文库的简并基因文库的方式可以产生组合文库,所述多肽文库各自包括可能的actriib多肽序列的至少一部分。例如,合成的寡核苷酸的混合物可以酶学连接到基因序列中,从而可能的actriib多肽核苷酸序列的简并集合可以作为单独的多肽表达,或作为选择,作为更大的融合蛋白的集合(例如,用于噬菌体展示)。
有许多方法可以从简并寡核苷酸序列中产生可能的同源物的文库。可以在自动dna合成仪中进行简并基因序列的化学合成,合成的基因然后可以连接到适合的载体中用于表达。简并寡核苷酸的合成是本领域公知的(参见,例如,narang,sa(1983)tetrahedron39:3;itakuraetal.,(1981)recombinantdna,proc.3rdclevelandsympos.macromolecules,ed.agwalton,amsterdam:elsevierpp273-289;itakuraetal.,(1984)annu.rev.biochem.53:323;itakuraetal.,(1984)science198:1056;ikeetal.,(1983)nucleicacidres.11:477)。这样的技术已经应用于其他蛋白质的定向进化(参见,例如,scottetal.,(1990)science249:386-390;robertsetal.,(1992)pnasusa89:2429-2433;devlinetal.,(1990)science249:404-406;cwirlaetal.,(1990)pnasusa87:6378-6382;以及美国专利nos.5,223,409、5,198,346和5,096,815)。
做为选择,可以利用其他形式的诱变来产生组合文库。例如,actriib多肽变体可以通过筛选来从文库中产生和分离,利用,例如,丙氨酸扫描诱变等(rufetal.,(1994)biochemistry33:1565-1572;wangetal.,(1994)j.biol.chem.269:3095-3099;balintetal.,(1993)gene137:109-118;grodbergetal.,(1993)eur.j.biochem.218:597-601;nagashimaetal.,(1993)j.biol.chem.268:2888-2892;lowmanetal.,(1991)biochemistry30:10832-10838;和cunninghametal.,(1989)science244:1081-1085),通过接头扫描诱变(gustinetal.,(1993)virology193:653-660;brownetal.,(1992)mol.cellbiol.12:2644-2652;mcknightetal.,(1982)science232:316);通过饱和诱变(meyersetal.,(1986)science232:613);通过pcr诱变(leungetal.,(1989)methodcellmolbiol1:11-19);或通过随机诱变,包括化学诱变等(milleretal.,(1992)ashortcourseinbacterialgenetics,cshlpress,coldspringharbor,n.y.;和greeneretal.,(1994)strategiesinmolbiol7:32-34)。接头扫描诱变,特别是在组合场景中,是鉴定actriib多肽的截短形式(生物活性)的吸引人的方法。
大量的技术是本领域已知的,用于筛选由点突变或截短产生的组合库的基因产物,就此而言,用于筛选cdna库中具有某些性质的基因产物。这些技术一般将适合于通过actriib多肽的组合诱变产生的基因库的快速筛选。用于筛选大的基因文库的最广泛使用的技术一般包括将基因文库克隆到可复制的表达载体中,用产生的载体库转化合适的细胞,并在一定条件下表达组合的基因,在所述条件中期望的活性的检测便于相对容易地分离编码被检出产物的基因的载体。优选的分析包括激活素结合分析和激活素介导的细胞信号转导分析。
在某些实施方式中,本文描述的方法和组合物的抑制剂中使用的actriib多肽可以进一步包含翻译后修饰,除了天然存在于所述actriib多肽中的之外。这种的修饰可以包括但不限于,乙酰化、羧基化、糖基化、磷酸化、脂质化和酰化。结果,修饰的actriib多肽可以含有非氨基酸元件,例如,聚乙二醇、脂质、聚糖或单体和磷酸盐。这种非氨基酸元件对actriib多肽的功能的影响可以通过熟练技术人员已知的任何方法来测试。当通过裂解actriib多肽的新生形式来在细胞中产生actriib多肽时,翻译后的加工对于蛋白质的正确折叠和/或功能可能也是重要的。不同的细胞(例如cho、hela、mdck、293、w138、nih-3t3或hek293)具有这种翻译后活性的特定细胞机制和特征性的机制,可以选择来确保actriib多肽的正确修饰和加工。
在某些方面,actriib多肽的功能变体或修饰形式包括具有至少一部分actriib多肽和一个或更多个融合结构域的融合蛋白。这样的融合结构域的公知的实例包括但不限于,多组氨酸、glu-glu、谷胱甘肽s转移酶(gst)、硫氧还蛋白、蛋白a、蛋白g、免疫球蛋白重链恒定区(fc)、麦芽糖结合蛋白(mbp)或人血清白蛋白。可以选择融合结构域以赋予期望的性质。例如,某些融合结构域对于通过亲和层析分离融合蛋白是特别有用的。对于亲和纯化来说,使用亲和层析的相关基质,例如,谷胱甘肽-、淀粉酶-和镍-或钴-轭合的树脂。许多这样的基质是以“试剂盒”形式可获得的,例如,对于(his6)融合配体有用的pharmaciagst纯化系统,以及qiaexpresstm系统(qiagen)。作为另一个实例,可以选择融合结构域以促进actriib多肽的检测。这样的检测结构域的实例包括各种荧光蛋白(例如,gfp),以及“表位标签”,其通常是有特异性抗体的短肽序列。特异性单克隆抗体容易获得的公知的表位标签包括flag、流感病毒血凝素(ha)和c-myc标签。在某些情况下,融合结构域具有蛋白酶裂解位点,例如,因子xa或凝血酶的,其容许相关蛋白酶部分地消化所述融合蛋白,从而由此释放重组蛋白。释放的蛋白质然后可以通过随后的层析分离从融合结构域中分离。在某些优选的实施方式中,actriib多肽与使所述actriib多肽在体内稳定化的结构域融合(“稳定物”结构域)。“稳定”是指提高血清半衰期的任何事,不论是由于降低的破坏、降低的肾脏清除、还是其他的药物动力学效应。已知与免疫球蛋白的fc部分融合为大范围的蛋白质赋予期望的药物动力学性质。同样地,与人血清白蛋白融合可以赋予期望的性质。可以选择的其他类型的融合结构域包括多聚化(例如,二聚化、四聚化)结构域和功能结构域(赋予其他生物学功能的,例如,进一步刺激骨骼生长或肌肉生长,如所希望的)。
要理解的是融合蛋白的不同元件可以以与期望的功能一致的任何方式布置。例如,actriib多肽可以置于异源结构域的c-末端,或做为选择,异源结构域可以置于actriib多肽的c-末端。actriib多肽结构域和异源结构域不必在融合蛋白中相邻,其他的结构域或氨基酸序列可以被包括在任一结构域的c-末端或n-末端,或两个结构域之间。
在某些实施方式中,本文描述的方法和组合物的抑制剂中使用的actriib多肽可以含有能够稳定化所述actriib多肽的一个或更多个修饰。例如,这样的修饰可以增强actriib多肽的体外半衰期,增强actriib多肽的循环半衰期,或降低actriib多肽的蛋白水解酶降解。这样的稳定化修饰可以包括,但不限于,融合蛋白(包括,例如,包含actriib多肽和稳定化结构域的融合蛋白)、糖基化位点的修饰(包括,例如,向actriib多肽添加糖基化位点),以及碳水化合物部分的修饰(包括,例如,从actriib多肽除去碳水化合物部分)。对于融合蛋白来说,actriib多肽融合到稳定结构域,例如igg分子(例如,fc结构域)。如本文使用的,术语“稳定物结构域”不仅是指融合蛋白情况下的融合结构域(例如,fc),还包括非蛋白性的修饰,例如,碳水化合物部分,或非蛋白性的聚合物,例如,聚乙二醇。
在某些实施方式中,本文描述的方法和组合物使用分离的或纯化的actriib多肽,即,分离自或基本上没有其他蛋白质的actriib多肽可以用于本文描述的方法和组合物。一般将通过从重组核酸表达来产生actriib多肽。
在某些方面,本文描述的方法和组合物中使用的actriib多肽由分离的和/或重组的核酸编码,包括本文公开的片段、功能变体和融合蛋白。例如,seqidno:19编码天然发生的人actriib前体多肽。目标核酸可以是单链的或是双链的。这样的核酸可以是dna或rna分子。这些核酸可以用于,例如,制造actriib多肽的方法,或作为直接的治疗试剂(例如,在基因治疗方法中)。
在某些方面,可以用生产适用于本文描述的方法和组合物的actriib多肽的核酸进一步被理解为包括作为seqidno:19的变体的核酸,以及编码可溶actriib多肽的那些核酸序列的变体(例如,编码seqidno:17、18、23、26、27、29、30、31、32、33、36、37、42和43的核酸)。变体核苷酸序列包括差异在于一个或更多个核苷酸取代、添加或删除的序列,例如,等位变体。
在某些实施方式中,可以用于生产适用于本文描述的方法和组合物的actriib多肽的分离的或重组的核酸序列是至少80%、85%、90%、95%、97%、98%、99%或100%相同于seqidno:19或编码可溶actriib多肽的那些核酸序列(例如,编码seqidno:17、18、23、26、27、29、30、31、32、33、36、37、42和43的核酸)。本领域普通技术人员将理解,与seqidno:19或编码可溶actriib多肽的那些核酸序列(例如,编码seqidno:17、18、23、26、27、29、30、31、32、33、36、37、42和43的核酸)互补的核酸序列,以及seqidno:19或编码可溶actriib多肽的那些核酸序列(例如,编码seqidno:17、18、23、26、27、29、30、31、32、33、36、37、42和43的核酸)的变体可以用于本文描述的方法和组合物。在进一步的实施方式中,所述核酸序列可以是分离的,重组和/或融合到异源核苷酸序列的,或是在dna文库中。
在其他实施方式中,可以用于生产适用于本文描述的方法和组合物的actriib多肽的核酸包括在高度严格条件与seqidno:19中指定的核苷酸序列或编码可溶actriib多肽的那些核酸序列(例如,编码seqidno:17、18、23、26、27、29、30、31、32、33、36、37、42和43的核酸)、seqidno:19的互补序列或编码可溶actriib多肽的那些核酸序列(例如,编码seqidno:17、18、23、26、27、29、30、31、32、33、36、37、42和43的核酸)或其片段杂交的核苷酸序列。本领域普通技术人员将理解,促进dna杂交的合适的严格条件可以是变化的。例如,人们可以在6.0倍氯化钠/柠檬酸钠(ssc)、大约45℃下杂交,最后2.0倍ssc在50℃下洗涤。例如,洗涤步骤中的盐浓度可以选自50℃下的约2.0倍ssc的低严格度,到50℃下约0.2倍ssc的高严格度。此外,洗涤步骤中的温度可以从室温约22℃下的低严格条件,提高到大约65℃的高严格条件。温度和盐度可以都变化,或者温度或盐浓度保持不变而另一个变量发生改变。在一个实施方式中,在6倍ssc室温下的低严格条件下杂交、随后在室温下2倍ssc洗涤的核酸可以用于本文描述的方法和组合物。
由于遗传密码方面的简并性而不同于seqidno:19中所列的核酸或编码可溶actriib多肽的那些核酸序列(例如,编码seqidno:17、18、23、26、27、29、30、31、32、33、36、37、42和43的核酸)的分离的核酸也可以用于生产适用于本文描述的方法和组合物的actriib多肽。例如,许多氨基酸由超过一种三联体指定。指定相同氨基酸的密码子,或同义密码子(例如,cau和cac对于组氨酸是同义的)可以产生“沉默”突变,其不影响蛋白质的氨基酸序列。然而,预计的是,引起目标蛋白质的氨基酸序列改变的dna序列多态性将存在于哺乳动物细胞。本领域技术人员将理解,编码特定蛋白质的核酸的一个或更多个核苷酸(达到核苷酸的约3-5%)中的这些变异由于天然的等位变异可以存在于给定物种的个体中。任何和所有的这类核苷酸变异和产生的氨基酸多态性可以用于本文描述的方法和组合物。
在某些实施方式中,可以用于生产适用于本文描述的方法和组合物的actriib多肽的重组核酸可以可操作连接到表达构建体中的一个或更多个调节核苷酸序列。调节核苷酸序列一般将适合于用来表达的宿主细胞。许多类型的适当的表达载体和适合的调节序列是本领域已知的,用于多种宿主细胞。一般地,所述一个或更多个调节核苷酸序列可以包括,但不限于,启动子序列、前导区或信号序列、核糖体结合位点、转录起始和终止序列、翻译起始和终止序列,以及增强子或激活物序列。本领域已知的组成型或可诱导启动子可以用于本文描述的方法和组合物。启动子可以是天然发生的启动子,或组合了超过一种启动子的元件的杂合启动子。表达构建体可以存在于细胞中或游离体例如质粒上,或者表达构建体可以插入染色体中。在优选的实施方式中,表达载体含有选择性标记基因以容许选择转化的宿主细胞。选择性标记基因是本领域公知的,将随使用的宿主细胞而变化。
在某些方面,可用于生产适用于本文描述的方法和组合物的actriib多肽的核酸可以在表达载体中提供,所述表达载体包含编码actriib多肽的核苷酸序列并与至少一个调节序列可操作连接。调节序列是公知的,被选择来指导actriib多肽的表达。因而,术语调节序列包括启动子、增强子和其他表达控制元件。示范性的调节序列在goeddel;geneexpressiontechnology:methodsinenzymology,academicpress,sandiego,calif.(1990)中描述。例如,控制与之可操作地连接的dna序列的表达的各种表达控制序列的任一种,可以用于这些载体来表达编码actriib多肽的dna序列。这类有用的表达控制序列包括,例如,sv40的早期和晚期启动子、tet启动子、腺病毒或巨细胞病毒即时早期启动子、rsv启动子、lac系统、trp系统、tac或trc系统、其表达由t7rna聚合酶指导的t7启动,噬菌体λ的主要操纵子和启动子区域,ft衣壳蛋白的控制区域、3-磷酸甘油酸激酶或其他糖酵解酶的启动子、酸性磷酸酶例如pho5的启动子、酵母.alpha.接合因子的启动子、杆状病毒系统的多面体启动子,以及已知控制原核和真核细胞以及它们的病毒的基因表达的其他序列,以及它们的各种组合。要理解的是,表达载体的设计可以取决于这些因素,如要转化的宿主细胞的选择,和/或希望表达的蛋白质的类型。此外,还应当考虑载体的拷贝数、控制拷贝数的能力以及载体编码的任何其他蛋白质的表达,例如抗生素标志物。
重组核酸可以通过将克隆的基因或其部分连接到适合于在原核细胞、真核细胞(酵母、禽类、昆虫或哺乳动物)或两者中表达的载体中来产生。用于重组actriib多肽的生产的表达载体包括质粒和其他载体。例如,适合的载体包括质粒类型:pbr322衍生的质粒、pembl衍生的质粒、pex衍生的质粒、pbtac衍生的质粒和puc-衍生的质粒,用于在原核细胞例如e.coli中表达。
某些哺乳动物表达载体含有原核序列来促进载体在细菌中的增殖,以及含有一种或更多种在真核细胞中表达的真核转录单位。pcdnai/amp、pcdnai/neo、prc/cmv、psv2gpt、psv2neo、psv2-dhfr、ptk2、prsvneo、pmsg、psvt7、pko-neo和phyg衍生的载体是适合于转染真核细胞的哺乳动物表达载体的实例。这些载体的一些被来自细菌质粒例如pbr322表达序列修饰,来促进在原核和真核细胞两者中的复制和药物抗性。做为选择,病毒的衍生物,例如,牛乳头状瘤病毒(bpv-1)或epstein-barr病毒(phebo、prep-衍生的和p205)可以用于蛋白质在真核细胞中的短暂表达。其他病毒(包括逆转录病毒)表达系统的实例可以在下文基因治疗递送系统的说明中找到。制备质粒和转化宿主生物体所采用的各种方法是本领域公知的。对于原核和真核细胞都适合的其他表达系统,以及一般的重组过程,参见molecularcloningalaboratorymanual,3rded.,ed.bysambrook,fritschandmaniatis(coldspringharborlaboratorypress,2001)。在某些情况下,可能希望的是通过使用杆状病毒表达系统来表达重组多肽。这样的杆状病毒表达系统的实例包括pvl衍生的载体(例如,pvl1392、pvl1393和pvl941)、pacuw衍生的载体(例如pacuw1)和pbluebac-衍生的载体(例如含有.beta.-gal的pbluebaciii)。
在一个实施方式中,载体可以被设计用于在cho细胞中生产本文描述的方法和组合物中使用的actriib多肽,例如pcmv-script载体(stratagene,lajolla,calif.)、pcdna4载体(invitrogen,carlsbad,calif.)和pci-neo载体(promega,madison,wis.)。明显的是,目标基因构建体可以用于引起目标actriib多肽在培养物中增殖的细胞中表达,例如,来产生蛋白质,包括融合蛋白或变体蛋白,用于纯化。
用包括一种或更多种目标actriib多肽的编码序列(例如,seqidno:19或编码可溶actriib多肽的那些核酸序列(例如,编码seqidno:17、18、23、26、27、29、30、31、32、33、36、37、42和43的核酸)))的重组基因转染的宿主细胞可以用于生产适用于本文描述的方法和组合物的actriib多肽。所述宿主细胞可以是任何原核或真核细胞。例如,本文提供的actriib多肽可以在细菌细胞例如e.coli、昆虫细胞(例如,使用杆状病毒表达系统)、酵母或哺乳动物细胞中表达。其他适合的宿主细胞是本领域技术人员公知的。
因而,本文提供的是生产用于本文描述的方法和组合物的actriib多肽的方法。例如,用编码actriib多肽的表达载体转染的宿主细胞可以在适当的条件下培养来容许发生actriib多肽的表达。从细胞与含有actriib多肽的培养基的混合物中,可以分泌和分离actriib多肽。做为选择,actriib多肽可以细胞质地或在膜部分中保持,收获细胞、裂解并分离蛋白。细胞培养物包括宿主细胞、培养基和其他副产物。用于细胞培养的适合的培养基是本领域公知的。利用本领域已知的用于纯化蛋白质的技术,可以从细胞培养介质、宿主细胞或两者分离目标actriib多肽,包括离子交换层析、凝胶过滤层析、超滤、电泳、使用特异于actriib多肽的特定表位的抗体的免疫亲和纯化、以及使用结合与actriib多肽融合的结构域的试剂的亲和纯化(例如,蛋白a柱可以用于纯化actriib-fc融合物)。在优选的实施方式中,actriib多肽是含有便于其纯化的结构域的融合蛋白。在优选的实施方式中,纯化通过一系列柱层析步骤来实现,包括,例如,三种或更多种以下的,按任何顺序:蛋白a层析、q琼脂糖层析、苯基琼脂糖层析、空间排阻层析和阳离子交换层析。纯化可以用病毒过滤和缓冲液交换来完成。如本文表明的,actriib-hfc蛋白可以纯化到通过空间排阻层折测定的>98%的纯度,和通过sds-page测定的>95%的纯度。这一水平的纯度足以在小鼠中对骨骼实现期望的效果,以及在小鼠、大鼠和非人灵长类中实现可接受的安全分布。
在另一个实施方式中,编码位于重组actriia多肽的期望部分的n-末端的纯化前导序列例如聚-(his)/肠激酶裂解位点序列的融合基因可以容许表达的融合蛋白通过利用ni2+金属树脂的亲和层析来纯化。纯化前导序列然后通过用肠激酶处理来除去,以提供纯化的actriib多肽(例如,参见hochulietal.,(1987)j.chromatography411:177;和janknechtetal.,pnasusa88:8972)。
制造融合物基因的技术是公知的。基本上,根据常规技术进行编码不同多肽序列的各种dna片段的连接,采用钝末端的或交错末端的末端用于连接,限制酶消化来提供适当的末端,视情况填充粘末端,碱性磷酸酶处理来避免不希望的连接,以及酶连接。在另一个实施方式中,融合基因可以通过常规技术,包括自动的dna合成仪来合成。做为选择,可以使用锚引物来进行基因片段的pcr扩增,所述锚引物产生两个连续基因片段之间的互补的突出,其随后可以退火来产生嵌合基因序列(参见,例如currentprotocolsinmolecularbiology,eds.ausubeletal.,johnwiley&sons:1992)。
actriib-fc融合蛋白可以从paid4载体(sv40ori/增强子,cmv启动子)在稳定地转染的cho-dukxbl1细胞中表达,使用seqidno:8的组织血纤蛋白溶酶原前导序列。fc部分可以包含人igg1fc序列,如seqidno:7所示。在某些实施方式中,在表达时,平均起来,所含的蛋白质具有每分子的actriib-fc融合蛋白约1.5到2.5摩尔的唾液酸。
在某些实施方式中,actriib-fc融合物的长血清半衰期可以是在人类对象中25-32天。另外,相比在人293细胞中表达的actriib-hfc融合蛋白所报告的,cho细胞表达的材料可以具有更高的对激活素b配体的亲和力(delreetal.,jbiolchem.2004dec17;279(51):53126-35)。另外,不受理论的限制,使用比其他前导序列提供更高生产的tpa前导序列,不同于用天然前导区表达的actriib-fc,可以提供高纯度的n-末端序列。使用天然前导序列可能产生两种主要种类的actriib-fc,各自具有不同的n-末端序列。
8.5.3其他actrii受体信号转导抑制剂
在某些实施方式中,本文描述的组合物和方法中使用的actrii信号转导抑制剂是核酸化合物。
抑制actrii受体的核酸化合物的类别的实例包括反义核酸、sirna或rnai构建体以及催化性核酸构建体。核酸化合物可以是单链的或双链的。双链的化合物还可以包括突出的或非互补的区域,其中链的一条或另一条是单链的。单链的化合物可以包括自我互补的区域,意味着所述化合物可以形成所谓的“发夹”或“茎-环”结构,带有双螺旋结构的区域。
在某些实施方式中,抑制actrii受体的核酸化合物可以包含与一区域互补的核苷酸序列,所述区域由全长actrii受体核酸序列或激活素核酸序列(例如,激活素a或激活素b亚基,也称为βa或βb的核酸序列)的不超过1000个、不超过500个、不超过250个、不超过100个或不超过50、35、30、25、22、20或18个核苷酸组成。在具体的实施方式中,互补的区域将是至少8个核苷酸,任选地至少10个或至少15个核苷酸,任选地在15到25个核苷酸之间。互补的区域可以落入内含子、目标转录产物的编码序列或非编码序列,例如编码序列部分。一般地,抑制actrii受体的核酸化合物将具有约8个到约500个核苷酸或碱基对的长度,任选地所述长度是约14个到约50个核苷酸。抑制actrii受体的核酸化合物可以是dna(特别是作为反义使用的)、rna或rna:dna杂交物。任一条链可以包括dna和rna的混合物,以及不容易被分类为dna或rna的修饰形式。同样地,双链的核酸化合物可以是dna:dna、dna:rna或rna:rna,任一条链还可以包括dna和rna的混合物,以及不容易被分类为dna或rna的修饰形式。
抑制actrii受体的核酸化合物可以包括各种修饰的任一种,包括对主干(天然核酸中的糖-磷酸部分,包括核苷酸间连键)或碱基部分(天然核酸的嘌呤或嘧啶部分)的一个或多个修饰。在某些实施方式中,反义核酸化合物将具有约15个到约30个核苷酸的长度,通常将含有一个或更多个修饰来改善某些特性,例如,血清中的稳定性、细胞中的稳定性、化合物可能被递送的部位中的稳定性,例如,就口服递送来说是胃部,以及对于吸入的化合物来说是肺部。对于rnai构建体来说,与目标转录产物互补的链一般将是rna或其修饰体。其他的链可以是rna、dna或任何其他的变异体。在某些实施方式中,双链的或单链的“发夹”rnai构建体的双螺旋部分可以具有18到40个核苷酸的长度,任选地约21到23个核苷酸长度,只要它起到dicer底物的作用。催化性或酶性核酸可以是核酶或dna每,也可以含有修饰的形式。在某些实施方式中,在生理条件下以及在无义或正义对照很少作用或没有作用的浓度下,抑制actrii受体的核酸化合物可以抑制它的目标的表达达到约50%、60%、70%、75%、80%、85%、90%、95%、99%或更多,测试核酸化合物的作用的浓度包括1、5、10微摩尔,或更高。
在其他实施方式中,本文描述的组合物和方法中使用的actrii信号转导抑制剂是抗体。这样的抗体包括结合激活素(特别是激活素a或b亚基,也称为βa或βb)并破坏actrii受体结合的抗体;以及结合actrii受体多肽(例如,可溶的actriia或可溶的actriib多肽)并破坏激活素结合的抗体。
通过使用衍生自actrii受体多肽或激活素多肽的免疫原,抗蛋白质/抗肽的抗血清或单克隆抗体可以通过标准方案产生(参见,例如,antibodies:alaboratorymanualed.byharlowandlane(coldspringharborpress:1988))。哺乳动物,例如,小鼠、仓鼠或家兔可以用actrii受体多肽的免疫原性形式、能够引发抗体反应的抗原性片段或融合蛋白来免疫。对蛋白质或肽赋予免疫原性的技术包括结合到载体,或本领域公知的其他技术。actrii受体或激活素多肽的免疫原性部分可以在存在佐剂的情况下施用。免疫的进展可以通过检测血浆或血清中的抗体滴度来监视。标准的elisa或其他免疫分析可以使用免疫原作为抗原来评估抗体的水平。
在用actrii受体多肽的抗原性制品免疫动物之后,可以获得抗血清,如果希望,可以从血清分离多克隆抗体。为了产生单克隆抗体,抗体生产细胞(淋巴细胞)可以从免疫的动物中收获,通过标准的体细胞融合过程与永生化细胞如骨髓瘤细胞融合来产生杂交瘤细胞。这样的技术是本领域公知的,包括,例如,杂交瘤技术(由kohlerandmilstein,(1975)nature,256:495-497最早开发)、人b细胞杂交瘤技术(kozbaretal.,(1983)immunologytoday,4:72)以及ebv杂交瘤技术来生产人单克隆抗体(coleetal.,(1985)monoclonalantibodiesandcancertherapy,alanr.liss,inc.pp.77-96)。可以免疫化学地筛选杂交瘤细胞中与actrii受体多肽特异性反应的抗体生产,从包含这样的杂交瘤细胞的培养物中分离单克隆抗体。
如本文使用的术语“抗体”意图包括也特异性地与目标多肽反应的抗体的片段。抗体可以使用常规技术片段化,按上文对完整抗体描述的相同的方式为了实用性筛选片段。例如,f(ab)2片段可以通过用胃蛋白酶处理抗体产生。产生的f(ab)2片段可以进行处理来还原二硫键,产生fab片段。抗体进一步意图包括双特异性的、单链的、嵌合的、人源化的和完全的人分子,其具有由抗体的至少一个cdr区赋予的对actrii受体或激活素多肽的亲和力。抗体可以进一步包含附着于其上并能被检测的标签(例如,所述标签可以是放射性同位素、荧光化合物、酶或酶辅助因子)。
在某些实施方式中,抗体是重组抗体,该术语涵盖部分通过分子生物学技术产生的任何抗体,包括cdr移植的或嵌合的抗体、从文库选择的抗体结构域中组装的人抗体或其他抗体、单链抗体和单结构域抗体(例如,人vh蛋白或骆驼化的vhh蛋白)。在某些实施方式中,抗体可以是单克隆抗体,以及在某些实施方式中。例如,产生特异性结合actrii受体多肽或激活素多肽的单克隆抗体的方法可以包括,向小鼠施用一定数量的包含有效刺激可检测免疫应答的抗原多肽的免疫原性组合物,从小鼠获得抗体生产细胞(例如,来自脾脏的细胞),将所述抗体生产细胞与骨髓瘤细胞融合来获得抗体生产杂交瘤,以及测试所述抗体生产杂交瘤来鉴定产生特异性结合所述抗原的单克隆抗体的杂交瘤。一旦获得杂交瘤,杂交瘤可以在细胞培养物中增殖,任选地在杂交瘤衍生的细胞产生特异性结合抗原的单克隆抗体的培养条件下培养。单克隆抗体可以从细胞培养物中纯化。
提及抗体时使用的形容词“特异性反应”意图是指,如本领域一般理解的,在目标抗原(例如,actrii受体多肽)和非目标的其他抗原之间所述抗体是足够有选择性的,使得所述抗体至少在检测特定类型的生物样品中目标抗原的存在方面是有用的。在采用抗体的某些方法例如治疗应用中,更高程度的结合特异性是希望的。单克隆抗体一般具有更高的倾向(相比多克隆抗体)来有效地区分期望的抗原和交叉反应的多肽。影响抗体:抗原相互作用的特异性的一个特征是抗体对抗原的亲和力。虽然可以在大范围的不同亲和力下实现期望的特异性,一般地优选的抗体将具有约10-6、10-7、10-8、10-9或更低的亲和力(解离常数)。考虑到激活素与actrii受体之间非常紧密的结合,预计的是中和性抗激活素或抗actrii受体抗体一般应具有10-10或更低的解离常数。
此外,用于筛选抗体来鉴定期望的抗体的技术可能影响所获得的抗体的性质。例如,如果抗体用于结合溶液中的抗原,可能希望的是测试溶液结合。多种不同的技术可以用于测试抗体与抗原之间的相互作用来鉴定特别希望的抗体。这样的技术包括elisa、表面胞质团共振结合分析(例如,biacore.tm.结合分析,biacoreab,uppsala,sweden)、夹心分析(例如,igeninternationalinc.的顺磁性的珠子系统,gaithersburg,md.)、western印迹、免疫沉淀分析和免疫组织化学。
在某些实施方式中,用于本文描述的组合物和方法的actrii信号转导抑制剂包括可选择形式的激活素,特别是在i型受体结合结构域中具有改变、可以结合ii型受体并且不能形成活性的三元复合物的那些。在某些实施方式中,抑制激活素a、b、c或e或特别是actrii受体表达的核酸,例如,反义分子、sirna或核酶,可以用于本文描述的组合物和方法中。在某些实施方式中,用于本文描述的组合物和方法的actrii信号转导抑制剂展现了相比抑制tnf-beta家族的其他成员、抑制gdf11介导的信号转导的选择性,特别是对于gdf8和激活素。
在其他实施方式中,本文描述的组合物和方法中使用的actrii信号转导抑制剂是具有actrii受体拮抗剂活性的非抗体蛋白,包括抑制素(即,抑制素alpha亚基)、卵泡抑素(例如,卵泡抑素-288和卵泡抑素-315)、cerberus、卵泡抑素相关蛋白(“fsrp”)、内皮糖蛋白(endoglin)、激活素c、alpha(2)-巨球蛋白和m108a(位置108处甲硫氨酸到丙氨酸的改变)突变的激活素a。
在具体的实施方式中,用于本文描述的组合物和方法的actrii信号转导抑制剂是拮抗激活素生物活性和/或结合激活素的卵泡抑素多肽。术语“卵泡抑素多肽”包括这些多肽,其包含卵泡抑素的任何天然发生的多肽以及保持了有用活性的其任何变体(包括突变体、片段、融合物和肽模拟物形式),进一步包括卵泡抑素的任何功能单体或多聚体。保持了激活素结合性质的卵泡抑素多肽变体可以根据涉及卵泡抑素和激活素相互作用的早先的研究来鉴定。例如,wo2008/030367公开了显示对激活素结合重要的特定的卵泡抑素结构域(“fsds”),通过全部引用将其合并在本文中。卵泡抑素多肽包括一些多肽,其衍生自任何已知的卵泡抑素的序列、具有至少约80%相同于卵泡抑素多肽的序列的序列,任选地至少85%、90%、95%、96%、97%、98%、99%或更高的同一性。卵泡抑素多肽的实例包括成熟的卵泡抑素多肽或较短的同种型或人卵泡抑素前体多肽的其他变体,例如,在wo2005/025601中描述的,通过全部引用将其合并在本文中。
在具体的实施方式中,用于本文描述的组合物和方法的actrii信号转导抑制剂是拮抗激活素生物活性和/或结合激活素的卵泡抑素-样相关基因(flrg)。术语“flrg多肽”包括这些多肽,其包含flrg的任何天然发生的多肽以及保持了有用活性的其任何变体(包括突变体、片段、融合物和肽模拟物形式)保持了激活素结合性质的flrg多肽变体可以使用分析flrg和激活素相互作用的常规方法来鉴定。参见,例如,美国专利no.6,537,966,通过全部引用将其包括在本文中。flrg多肽包括一些多肽,其衍生自任何已知的flrg的序列、具有至少约80%相同于flrg多肽的序列的序列,任选地至少85%、90%、95%、96%、97%、98%、99%或更高的同一性。
在某些实施方式中,卵泡抑素多肽和flrg多肽的功能变体或修饰形式包括具有卵泡抑素多肽或flrg多肽的至少一部分以及一个或更多个融合结构域的融合蛋白,所述融合结构域例如,促进多肽的分离检测或稳定化或多聚化的结构域。上文参考actriia和actriib多肽详细地讨论了适合的融合结构域。在一个实施方式中,actrii信号转导抑制剂是包含与fc结构域融合的卵泡抑素多肽的激活素结合部分的融合蛋白。在另一个实施方式中,actrii信号转导抑制剂是包含与fc结构域融合的flrg多肽的激活素结合部分的融合蛋白。
8.6分析
各种actrii多肽变体或可溶的actrii多肽变体,可以测试它们抑制actrii的能力。此外,化合物可以测试它们抑制actrii的能力。一旦确认了actrii信号转导抑制剂活性,这些化合物可以用于本文提供的方法。actrii可以是actriia或actriib。以下对actriia描述的分析也可以类似地对actriib进行。
8.6.1评估snai1、phosphosmad2、phosphosmad3、尿蛋白、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、osterix、klotho、alpha-sma、myocd、actriia、axin2和/或sm22-alpha水平和/或活性
snai1、phosphosmad2、phosphosmad3、尿蛋白、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、osterix、klotho、alpha-sma、myocd、actriia、axin2和/或sm22-alpha的水平和/或活性可以通过本领域已知的或本文描述的任何方法来测定。例如,组织样品中snai1、尿蛋白、dkk1、col1a1、激活素、runx2、alp、bsap、ctx、osterix、klotho、alpha-sma、myocd、actriia、axin2和/或sm22-alpha的水平可以利用例如northern印迹、pcr分析、实时pcr分析或本领域已知的或本文描述的任何其他技术,通过评估(例如,定量)样品中snai1、尿蛋白、dkk1、col1a1、激活素、runx2、osterix、alp、bsap、ctx、klotho、alpha-sma、myocd、actriia、axin2和/或sm22-alpha的转录的rna来测定。本领域技术人员将认识到,runx2、alp、snai1、phosphosmad2、dkk1、col1a1、激活素、bsap、ctx、osterix、klotho、alpha-sma、myocd、actriia、axin2、sm22-alpha、phosphosmad3和尿蛋白的一种或更多种的水平和/或活性可以与相应参考群体中的水平和/或活性分别地和独立地比较,例如,如上文在章节8.3.1中描述的。在一个实施方式中,组织样品中snai1、尿蛋白、dkk1、col1a1、激活素、runx2、alp、bsap、ctx、osterix、klotho、alpha-sma、myocd、actriia、axin2和/或sm22-alpha的水平可以分别通过评估(例如,定量)样品中snai1、尿蛋白、dkk1、col1a1、激活素、runx2、alp、bsap、ctx、osterix、klotho、alpha-sma、myocd、actriia、axin2和/或sm22-alpha的mrna来测定。在具体的实施方式中,snai1、尿蛋白、dkk1、col1a1、激活素、runx2、alp、bsap、ctx、osterix、klotho、alpha-sma、myocd、actriia、axin2和/或sm22-alpha的mrna水平通过定量逆转录酶聚合酶链式反应(qrt-pcr)来测定。在具体的实施方式中,runx2mrna的核酸序列包含seqidno:58的核酸序列。在具体的实施方式中,alpmrna的核酸序列包含seqidno:59的核酸序列。在具体的实施方式中,snai1mrna的核酸序列包含seqidno:74的核酸序列。在具体的实施方式中,dkk1mrna的核酸序列包含seqidno:75的核酸序列。在具体的实施方式中,col1a1mrna的核酸序列包含seqidno:76的核酸序列。在具体的实施方式中,激活素mrna的核酸序列包含seqidno:77的核酸序列。在具体的实施方式中,osterix的核酸序列包含seqidno:60的核酸序列。在具体的实施方式中,klotho的核酸序列包含seqidno:61的核酸序列。在具体的实施方式中,alpha-smamrna的核酸序列包含seqidno:70的核酸序列。在具体的实施方式中,myocdmrna的核酸序列包含seqidno:71的核酸序列。在具体的实施方式中,sm22-alphamrna的核酸序列包含seqidno:62的核酸序列。在具体的实施方式中,使用runx2特异性引物(seqidno:48和49)进行qrt-pcr来测定runx2水平。在具体的实施方式中,使用alp特异性引物(seqidno:50和51)进行qrt-pcr来测定alp水平。在具体的实施方式中,使用snai1特异性引物(seqidno:78和79)进行qrt-pcr来测定snai1水平。在具体的实施方式中,使用dkk1特异性引物(seqidno:80和81)进行qrt-pcr来测定dkk1水平。在具体的实施方式中,使用col1a1特异性引物(seqidno:82和83)进行qrt-pcr来测定col1a1水平。在具体的实施方式中,使用激活素特异性引物(seqidno:84和85)进行qrt-pcr来测定激活素水平。在具体的实施方式中,使用osterix特异性引物(seqidno:52和53)进行qrt-pcr来测定osterix水平。在具体的实施方式中,使用klotho特异性引物(seqidno:54和55)进行qrt-pcr来测定klotho水平。在具体的实施方式中,使用sm22-alpha特异性引物(seqidno:56和57)进行qrt-pcr来测定sm22-alpha水平。
组织样品中snai1、phosphosmad2、phosphosmad3、尿蛋白、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、osterix、klotho、alpha-sma、myocd、actriia、axin2和/或sm22-alpha的水平也可以利用例如免疫组织化学分析、western印迹、elisa、免疫沉淀、流式细胞计分析或本领域已知的或本文描述的任何其他技术通过分别评估(例如,定量)样品中snai1、phosphosmad2、phosphosmad3、尿蛋白、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、osterix、klotho、alpha-sma、myocd、actriia、axin2和/或sm22-alpha的蛋白表达水平来测定。在具体的实施方式中,runx2蛋白的氨基酸序列包含seqidno:63的氨基酸序列。在具体的实施方式中,alp蛋白的氨基酸序列包含seqidno:64的氨基酸序列。在具体的实施方式中,snai1蛋白的氨基酸序列包含seqidno:86的氨基酸序列。在具体的实施方式中,dkk1蛋白的氨基酸序列包含seqidno:87的氨基酸序列。在具体的实施方式中,col1a1蛋白的氨基酸序列包含seqidno:88的氨基酸序列。在具体的实施方式中,激活素(例如,游离激活素)蛋白的氨基酸序列包含seqidno:89的氨基酸序列。在具体的实施方式中,bsap蛋白的氨基酸序列包含seqidno:72的氨基酸序列。在具体的实施方式中,osterix蛋白的氨基酸序列包含seqidno:65的氨基酸序列。在具体的实施方式中,klotho蛋白的氨基酸序列包含seqidno:66的氨基酸序列。在具体的实施方式中,alpha-sma蛋白的氨基酸序列包含seqidno:68的氨基酸序列。在具体的实施方式中,myocd的氨基酸序列包含seqidno:69的氨基酸序列。在具体的实施方式中,sm22-alpha蛋白的氨基酸序列包含seqidno:67的氨基酸序列。在具体的实施方式中,actriia蛋白的氨基酸序列包含seqidno:1的氨基酸序列。在具体的实施方式中,actriia蛋白的氨基酸序列包含seqidno:2的氨基酸序列。在具体的实施方式中,actriia蛋白的氨基酸序列包含seqidno:3的氨基酸序列。在具体的实施方式中,actriia蛋白的氨基酸序列包含seqidno:4的氨基酸序列。在具体的实施方式中,actriia蛋白的氨基酸序列包含seqidno:5的氨基酸序列。在具体的实施方式中,axin2蛋白的氨基酸序列包含seqidno:87的氨基酸序列。在特定的实施方式中,snai1、phosphosmad2、phosphosmad3、尿蛋白、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、osterix、klotho、alpha-sma、myocd、actriia、axin2和/或sm22-alpha的水平和/或活性通过western印迹来测定。在特定的实施方式中,snai1、phosphosmad2、phosphosmad3、尿蛋白、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、osterix、klotho、alpha-sma、myocd、actriia、axin2和/或sm22-alpha的活性通过snai1、phosphosmad2、phosphosmad3、尿蛋白、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、osterix、klotho、alpha-sma、myocd、actriia、axin2或sm22-alpha所调节的蛋白质的western印迹分析来测定。在特定的实施方式中,snai1、phosphosmad2、phosphosmad3、尿蛋白、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、osterix、klotho、alpha-sma、myocd、actriia、axin2和/或sm22-alpha的水平通过能够分别定量对象的组织样品中(例如,人血清中)存在的snai1、phosphosmad2、phosphosmad3、尿蛋白、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、osterix、klotho、alpha-sma、myocd、actriia、axin2和/或sm22-alpha的数量的方法,和/或能够分别检测在用actrii信号转导抑制剂治疗之后snai1、phosphosmad2、phosphosmad3、尿蛋白、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、osterix、klotho、alpha-sma、myocd、actriia、axin2和/或sm22-alpha水平的矫正的方法来测定。在一个实施方式中,组织样品中snai1、phosphosmad2、phosphosmad3、尿蛋白、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、osterix、klotho、alpha-sma、myocd、actriia、axin2和/或sm22-alpha的水平通过利用elisa分别评估(例如,定量)样品中snai1、phosphosmad2、phosphosmad3、尿蛋白、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、osterix、klotho、alpha-sma、myocd、actriia、axin2和/或sm22-alpha的蛋白质表达来测定。例如,snai1、phosphosmad2、phosphosmad3、尿蛋白、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、osterix、klotho、alpha-sma、myocd、actriia、axin2和/或sm22-alpha可以利用elisa方法在人血清中鉴定和定量。用于测定组织样品中snai1、phosphosmad2、phosphosmad3、尿蛋白、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、osterix、klotho、alpha-sma、myocd、actriia、axin2和/或sm22-alpha的水平的elisa方法可以包括用组织样品(例如,人血清)包被elisa平板,并分别检测所述组织样品(例如,人血清)中分别结合snai1、phosphosmad2、phosphosmad3、尿蛋白、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、osterix、klotho、alpha-sma、myocd、actriia、axin2和/或sm22-alpha特异性抗体的snai1、phosphosmad2、phosphosmad3、尿蛋白、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、osterix、klotho、alpha-sma、myocd、actriia、axin2和/或sm22-alpha。在某些实施方式中,如本文描述的用于测定snai1、phosphosmad2、phosphosmad3、尿蛋白、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、osterix、klotho、alpha-sma、myocd、actriia、axin2和/或sm22-alpha的水平和/或活性的方法(例如,elisa)能够检测100pg/ml起的snai1、phosphosmad2、phosphosmad3、尿蛋白、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、osterix、klotho、alpha-sma、myocd、actriia、axin2和/或sm22-alpha。在具体的实施方式中,用runx2特异性抗体sc-390715(santacruz)进行elisa来测定runx2水平。在具体的实施方式中,用alp特异性抗体sc-98652(santacruz)进行elisa来测定alp水平。在具体的实施方式中,用snai1特异性抗体sc-393172(santacruz)进行elisa来测定snai1水平。在具体的实施方式中,用phosphosmad2特异性抗体sc-101801(santacruz)进行elisa来测定phosphosmad2水平。在具体的实施方式中,用phosphosmad3特异性抗体sc-130218(santacruz)进行elisa来测定phosphosmad2水平。在具体的实施方式中,用dkk1特异性抗体sc-374574(santacruz)进行elisa来测定dkk1水平。在具体的实施方式中,用col1a1特异性抗体sc-8784(santacruz)进行elisa来测定col1a1水平。在具体的实施方式中,用激活素特异性抗体a1594(sigmaaldrich)进行elisa来测定激活素(例如,游离激活素)水平。在具体的实施方式中,用bsap特异性抗体sc-98652(santacruz)进行elisa来测定ctx水平。在具体的实施方式中,用ctx特异性抗体abin1173415(antibodiesonline)进行elisa来测定ctx水平。在具体的实施方式中,用osterix特异性抗体sc-22538(santacruz)进行elisa来测定osterix水平。在具体的实施方式中,用klotho特异性抗体sc-22218(santacruz)进行elisa来测定klotho水平。在具体的实施方式中,用alpha-sma特异性抗体sc-53142(santacruz)进行elisa来测定alpha-sma水平。在具体的实施方式中,用myocd特异性抗体sc-21561(santacruz)进行elisa来测定myocd水平。在具体的实施方式中,用sm22-alpha特异性抗体sc-271719(santacruz)进行elisa来测定sm22-alpha水平。在具体的实施方式中,用actriia特异性抗体ab135634(abcam)进行elisa来测定actriia水平。
本文描述的elisa分子中描述的runx2、alp、snai1、phosphosmad2、dkk1、col1a1、激活素、bsap、ctx、osterix、klotho、alpha-sma、myocd、actriia、axin2、sm22-alpha、phosphosmad3和尿蛋白的一种或更多种的水平可以与相应的参考群体中的水平和/或活性独立地和分别地比较,如上文在章节8.3.1中描述的。
在测量样品中(例如,组织样品中,例如,主动脉、血液、血清、血浆、肝脏、脾脏和/或骨髓的样品)snai1、phosphosmad2、phosphosmad3、尿蛋白、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、osterix、klotho、alpha-sma、myocd、actriia、axin2和/或sm22-alpha的水平的分析中使用的抗体是本领域已知的,或可以利用本领域技术人员已知的途径容易地开发。可以用于测量样品中runx2水平的分析中的单克隆抗体的实例包括来自lifespanbiosciencesinc.,seattle,wa、目录编号ls-b4293、ls-b4294、ls-b4296的抗体;可从santacruzbiotechnology,inc.,santacruz,ca获得的、目录编号sc-390715的抗体;以及可从sigma-aldrichco.llc获得的、产品号码:wh0000860m1的抗体。可以用于测量样品中alp水平的分析中的单克隆抗体的实例包括来自lifespanbiosciencesinc.,seattle,wa、目录编号ls-b2877、ls-b1844、ls-c169212的抗体;可从santacruzbiotechnology,inc.,santacruz,ca获得的、目录编号sc-98652的抗体;以及可从sigma-aldrichco.llc获得的、产品号码:sab1405449的抗体。可以用于测量样品中snai1水平的分析中的单克隆抗体的实例包括来自lifespanbiosciencesinc.,seattle,wa、目录编号ls-c161335、ls-c198229和ls-c169298的抗体;可从santacruzbiotechnology,inc.,santacruz,ca获得的、目录编号sc-393172的抗体;以及可从sigma-aldrichco.llc获得的、产品号码:sab1404386的抗体。可用于测量样品中phosphosmad2水平的分析中的抗体的实例包括来自santacruzbiotechnology,inc.,santacruz,ca、目录编号sc-101801的抗体;以及可从sigma-aldrichco.llc获得的、产品号码:sab4200251和sab4300252的抗体。可用于测量样品中phosphosmad3水平的分析中的抗体的实例包括来自santacruzbiotechnology,inc.,santacruz,ca、目录编号sc-130218的抗体;以及可从sigma-aldrichco.llc获得的、产品号码:sab4300253和sab4504210的抗体。可以用于测量样品中dkk1水平的分析中的单克隆抗体的实例包括来自lifespanbiosciencesinc.,seattle,wa、目录编号ls-c108793、ls-c105116和ls-c105117的抗体;可从santacruzbiotechnology,inc.,santacruz,ca获得的、目录编号sc-374574的抗体;以及可从sigma-aldrichco.llc获得的、产品号码:wh0022943m1的抗体。可用于测量样品中col1a1水平的分析中的单克隆抗体的实例包括来自lifespanbiosciencesinc.,seattle,wa、目录编号ls-b5932的抗体;可从santacruzbiotechnology,inc.,santacruz,ca获得的、目录编号sc-8784的抗体;以及可从sigma-aldrichco.llc获得的、产品号码:c2456的抗体。可用于测量样品中激活素(例如,游离激活素)水平的分析中的单克隆抗体的实例包括来自lifespanbiosciencesinc.,seattle,wa、目录编号ls-c308491抗体;以及可从sigma-aldrichco.llc获得的、产品号码:a1719的抗体。可以用于测量样品中bsap水平的分析中的单克隆抗体的实例包括来自lifespanbiosciencesinc.,seattle,wa、目录编号ls-b2877、ls-b1844和ls-c169212的抗体;可从santacruzbiotechnology,inc.,santacruz,ca获得的、目录编号sc-98652的抗体;以及可从sigma-aldrichco.llc获得的、产品号码:sab1405449的抗体。可用于测量样品中ctx水平的分析中的单克隆抗体的实例包括abin1173415(antibodiesonline)。可以用于测量样品中osterix水平的分析中的单克隆抗体的实例包括来自lifespanbiosciencesinc.,seattle,wa、目录编号ls-c139215、ls-c132610、ls-b6531的抗体;可从santacruzbiotechnology,inc.,santacruz,ca获得的、目录编号sc-133871的抗体;以及可从sigma-aldrichco.llc获得的、产品号码:wh0121340m1的抗体。可以用于测量样品中klotho水平的分析中的单克隆抗体的实例包括来自lifespanbiosciencesinc.,seattle,wa、目录编号ls-c165587、ls-c145689、ls-c8376的抗体;可从santacruzbiotechnology,inc.,santacruz,ca获得的、目录编号sc-22218的抗体;以及可从sigma-aldrichco.llc获得的、产品号码:sab1306662的抗体。可用于测量样品中alpha-sma水平的分析中的抗体的实例包括来自lifespanbiosciencesinc.,seattle,wa、目录编号ls-b6000、ls-b5966、ls-b2161的抗体;可从santacruzbiotechnology,inc.,santacruz,ca获得的、目录编号sc-21561的抗体;以及可从sigma-aldrichco.llc获得的、产品号码:a5228的抗体。可用于测量样品中myocd水平的分析中的抗体的实例包括来自lifespanbiosciencesinc.,seattle,wa、目录编号ls-c37407、ls-c153495、ls-c137255的抗体;可从santacruzbiotechnology,inc.,santacruz,ca获得的、目录编号sc-53142的抗体;以及可从sigma-aldrichco.llc获得的、产品号码:m8948的抗体。可以用于测量样品中sm22-alpha水平的分析中的单克隆抗体的实例包括来自lifespanbiosciencesinc.,seattle,wa、目录编号ls-b2563、ls-c139114、ls-c210979的抗体;可从santacruzbiotechnology,inc.,santacruz,ca获得的、目录编号sc-271719的抗体;以及可从sigma-aldrichco.llc获得的、产品号码:sab2501014的抗体。可用于测量样品中actriia水平的分析中的单克隆抗体的实例包括来自abcam、产品码ab135634的抗体。
snai1、phosphosmad2、phosphosmad3、尿蛋白、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、osterix、klotho、alpha-sma、myocd、actriia、axin2和/或sm22-alpha的活性可以通过本领域已知的任何分析来测量,非限制性地包括报告基因分析(例如,分别含有snai1、phosphosmad2、phosphosmad3、尿蛋白、dkk1、col1a1、激活素、runx2、alp、bsap、ctx、osterix、klotho、alpha-sma、myocd、actriia、axin2或sm22-alpha响应报告基因构建体),或任何其他生物活性分析。
snai1、phosphosmad2、phosphosmad3、尿蛋白、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、osterix、klotho、alpha-sma、myocd、actriia、axin2和/或sm22-alpha的水平和/或活性可以在获自根据本文描述的方法治疗的对象的任何组织样品中分析。在某些实施方式中,snai1、phosphosmad2、phosphosmad3、尿蛋白、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、osterix、klotho、alpha-sma、myocd、actriia、axin2和/或sm22-alpha水平和/或活性在获自根据本文描述的方法治疗的对象的主动脉、血清、肝脏、脾脏或骨髓的样品中评估。在一个实施方式中,snai1、phosphosmad2、phosphosmad3、尿蛋白、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、osterix、klotho、alpha-sma、myocd、actriia、axin2和/或sm22-alpha水平和/或活性在获自根据本文描述的方法治疗的对象的血清的样品中评估。在另一个实施方式中,snai1、phosphosmad2、phosphosmad3、尿蛋白、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、osterix、klotho、alpha-sma、myocd、actriia、axin2和/或sm22-alpha水平和/或活性在获自根据本文描述的方法治疗的对象的主动脉、脾脏的样品中评估。在一个实施方式中,snai1、phosphosmad2、phosphosmad3、尿蛋白、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、osterix、klotho、alpha-sma、myocd、actriia、axin2和/或sm22-alpha水平和/或活性在获自根据本文描述的方法治疗的对象的骨髓的样品中评估。
本领域技术人员将认识到,利用本领域已知的和本文描述的分析测定的runx2、alp、snai1、phosphosmad2、dkk1、col1a1、激活素、bsap、osterix、klotho、alpha-sma、myocd、actriia、axin2、sm22-alpha、phosphosmad3和尿蛋白的一种或更多种的活性可以分别与相应参考群体中的水平和/或活性来比较,例如,如上文在章节8.3.1中描述的。
在某些实施方式中,对象的组织样品中snai1、phosphosmad2、phosphosmad3、尿蛋白、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、osterix、klotho、alpha-sma、myocd、actriia、axin2和/或sm22-alpha的水平和/或活性分别与如章节8.6中描述的参考群体的组织样品中(例如,来自相同组织的样品中)snai1、phosphosmad2、phosphosmad3、尿蛋白、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、osterix、klotho、alpha-sma、myocd、actriia、axin2和/或sm22-alpha的水平和/或活性比较。在某些实施方式中,对象的组织样品中snai1、phosphosmad2、phosphosmad3、尿蛋白、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、osterix、klotho、alpha-sma、myocd、actriia、axin2和/或sm22-alpha的水平和/或活性分别与较早时间点(例如,疾病发作之前、治疗开始之前或在治疗期间)时对象的组织样品中(例如,来自相同组织的样品中)snai1、phosphosmad2、phosphosmad3、尿蛋白、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、osterix、klotho、alpha-sma、myocd、actriia、axin2和/或sm22-alpha的水平和/或活性比较。在某些实施方式中,对象的组织样品(例如,主动脉、血清、脾脏、肝脏或血液骨髓)中snai1、phosphosmad2、phosphosmad3、尿蛋白、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、osterix、klotho、alpha-sma、myocd、actriia、axin2和/或sm22-alpha的水平和/或活性分别与对象的其他组织样品中snai1、phosphosmad2、phosphosmad3、尿蛋白、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、osterix、klotho、alpha-sma、myocd、actriia、axin2和/或sm22-alpha的水平和/或活性比较。在某些实施方式中,对象的组织样品中snai1、phosphosmad2、phosphosmad3、尿蛋白、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、osterix、klotho、alpha-sma、myocd、actriia、axin2和/或sm22-alpha的水平和/或活性与对象的组织样品中其他基因产物(例如,b-肌动蛋白、激活素a、激活素b)的水平和/或活性比较。
在某些实施方式中,对象的组织样品中snai1、phosphosmad2、phosphosmad3、尿蛋白、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、osterix、klotho、alpha-sma、myocd、actriia、axin2和/或sm22-alpha的水平和/或活性分别与参考群体的组织样品中snai1、phosphosmad2、phosphosmad3、尿蛋白、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、osterix、klotho、alpha-sma、myocd、actriia、axin2和/或sm22-alpha的水平和/或活性比较。在某些实施方式中,分别与参考群体中snai1、phosphosmad2、phosphosmad3、尿蛋白、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、osterix、klotho、alpha-sma、myocd、actriia、axin2和/或sm22-alpha的水平和/或活性相比、snai1、phosphosmad2、phosphosmad3、尿蛋白、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、osterix、klotho、alpha-sma、myocd、actriia、axin2和/或sm22-alpha的升高的水平和/或活性的检出,继之以施用激活素受体信号转导抑制剂(例如本文描述的一种或更多种激活素受体信号转导抑制剂)。在某些实施方式中,施用激活素受体信号转导抑制剂(例如本文描述的一种或更多种激活素受体信号转导抑制剂)继之以监视snai1、phosphosmad2、phosphosmad3、尿蛋白、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、ctx、osterix、klotho、alpha-sma、myocd、actriia、axin2和/或sm22-alpha的水平和/或活性,任选地,将所述snai1、phosphosmad2、phosphosmad3、尿蛋白、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、osterix、klotho、alpha-sma、myocd、actriia、axin2和/或sm22-alpha的水平和/或活性分别与参考群体中snai1、phosphosmad2、phosphosmad3、尿蛋白、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、osterix、klotho、alpha-sma、myocd、actriia、axin2和/或sm22-alpha的水平和/或活性比较。在某些实施方式中,施用第一剂量的actrii信号转导抑制剂(例如,actriia-hfc如seqidno:7),继之以测定snai1、phosphosmad2、phosphosmad3、尿蛋白、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、osterix、klotho、alpha-sma、myocd、actriia、axin2和/或sm22-alpha的水平和/或活性,如果snai1、phosphosmad2、phosphosmad3、尿蛋白、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx和/或osterix的水平和/或活性分别相比参考群体中snai1、phosphosmad2、phosphosmad3、尿蛋白、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx和/或osterix的水平和/或活性升高,和/或如果klotho、alpha-sma、myocd、actriia、axin2和/或sm22-alpha的水平和/或活性分别相比参考群体中klotho、alpha-sma、myocd、actriia、axin2和/或sm22-alpha的水平和/或活性降低,施用比所述第一剂量更高(例如,1.25、1.5、1.75、2、2.5、3、4、5、6、7、8、9或10倍高)的第二剂量的actrii信号转导抑制剂,如果snai1、phosphosmad2、phosphosmad3、尿蛋白、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx和/或osterix的水平和/或活性分别相比参考群体中snai1、phosphosmad2、phosphosmad3、尿蛋白、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx和/或osterix的水平和/或活性降低,和/或如果klotho、alpha-sma、myocd、actriia、axin2和/或sm22-alpha的水平和/或活性分别相比参考群体中klotho、alpha-sma、myocd、actriia、axin2和/或sm22-alpha的水平和/或活性升高,施用比所述第一剂量更低(例如,1.25、1.5、1.75、2、2.5、3、4、5、6、7、8、9或10倍低)的第二剂量的actrii信号转导抑制剂。在某些实施方式中,所述参考群体是章节8.6中描述的群体。
在某些实施方式中,治疗的对象的组织样品中snai1、phosphosmad2、phosphosmad3、尿蛋白、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、osterix、klotho、alpha-sma、myocd、actriia、axin2和/或sm22-alpha的水平和/或活性分别与来自一个或更多个健康对象的相同组织的样品中的snai1、phosphosmad2、phosphosmad3、尿蛋白、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、osterix、klotho、alpha-sma、myocd、actriia、axin2和/或sm22-alpha的水平和/或活性比较。在某些实施方式中,评估snai1、phosphosmad2、phosphosmad3、尿蛋白、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、osterix、klotho、alpha-sma、myocd、actriia、axin2和/或sm22-alpha的水平和/或活性的组织是主动脉、血清、骨髓、肝脏或脾脏。在一个实施方式中,评估snai1、phosphosmad2、phosphosmad3、尿蛋白、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、osterix、klotho、alpha-sma、myocd、actriia、axin2和/或sm22-alpha的水平和/或活性的组织是血清。
在某些实施方式中,snai1、phosphosmad2、phosphosmad3、尿蛋白、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx和/或osterix的升高的水平和/或活性分别高于参考群体中snai1、phosphosmad2、phosphosmad3、尿蛋白、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx和/或osterix的水平和/或活性约10%、20%、25%、30%、40%、50%、60%、70%、75%、80%、90%、100%、200%或500%;和/或klotho、alpha-sma、myocd、actriia、axin2和/或sm22-alpha的降低的水平分别低于参考群体中klotho、alpha-sma、myocd、actriia、axin2和/或sm22-alpha的水平和/或活性约10%、20%、25%、30%、40%、50%、60%、70%、75%、80%、90%或100%。在某些实施方式中,snai1、phosphosmad2、phosphosmad3、尿蛋白、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx和/或osterix的升高的水平和/或活性分别等于或约10%、20%、25%、30%、40%、50%、60%、70%、75%、80%、90%、100%、200%或500%高于参考群体的前10%、前5%、前4%、前3%、前2%或前1%中snai1、phosphosmad2、phosphosmad3、尿蛋白、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx和/或osterix的水平和/或活性;和/或klotho、alpha-sma、myocd、actriia、axin2和/或sm22-alpha的降低的水平分别等于或约10%、20%、25%、30%、40%、50%、60%、70%、75%、80%、90%或100%低于参考群体的后10%、后5%、后4%、后3%、后2%或后1%中klotho、alpha-sma、myocd、actriia、axin2和/或sm22-alpha的水平和/或活性。在某些实施方式中,所述参考群体是如章节8.6中描述的。
在某些实施方式中,klotho、alpha-sma、myocd、actriia、axin2和/或sm22-alpha的升高的水平和/或活性分别是约10%、20%、25%、30%、40%、50%、60%、70%、75%、80%、90%、100%、200%或500%大于参考群体中klotho、alpha-sma、myocd、actriia、axin2和/或sm22-alpha的水平和/或活性;和/或snai1、phosphosmad2、phosphosmad3、尿蛋白、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx和/或osterix的降低的水平和/或活性分别是约10%、20%、25%、30%、40%、50%、60%、70%、75%、80%、90%或100%低于参考群体中snai1、phosphosmad2、phosphosmad3、尿蛋白、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx和/或osterix的水平和/或活性。在某些实施方式中,klotho、alpha-sma、myocd、actriia、axin2和/或sm22-alpha的升高的水平和/或活性分别等于或约10%、20%、25%、30%、40%、50%、60%、70%、75%、80%、90%、100%、200%或500%高于参考群体的前10%、前5%、前4%、前3%、前2%或前1%中klotho、alpha-sma、myocd、actriia、axin2和/或sm22-alpha的水平和/或活性;和/或snai1、phosphosmad2、phosphosmad3、尿蛋白、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx和/或osterix的降低的水平和/或活性分别等于或约10%、20%、25%、30%、40%、50%、60%、70%、75%、80%、90%或100%低于参考群体的后10%、后5%、后4%、后3%、后2%或后1%中snai1、phosphosmad2、phosphosmad3、尿蛋白、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx和/或osterix的水平和/或活性。在某些实施方式中,所述参考群体是如章节8.6中描述的。
在某些实施方式中,激活素的水平是游离激活素的水平,例如,不与如卵泡抑素、卵泡抑素样3或抑制素缔合的激活素。游离激活素的水平可以通过例如(i)定量样品中,例如血浆中激活素的浓度;(ii)定量样品中与激活素缔合的蛋白质,例如卵泡抑素、卵泡抑素样3和抑制素的浓度;和(iii)计算激活素浓度与激活素缔合蛋白的浓度的化学计量比来确定。
本文描述的分析还可以用于测定其他的蛋白质和/或转录产物的水平和/或活性,例如,fgf23、卵泡抑素、卵泡抑素样3、抑制素、涉及内皮向间充质转变的蛋白质和/或转录产物。
在某些实施方式中,snai1、phosphosmad2、phosphosmad3、尿蛋白、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、osterix、klotho、alpha-sma、myocd、actriia、axin2和/或sm22-alpha的水平和/或活性是组织(例如,组织样品)中的。在某些实施方式中,所述组织是主动脉。在某些实施方式中,所述组织是肾脏。在某些实施方式中,所述组织是骨骼。在某些实施方式中,所述组织是血清。在优选的实施方式中,runx2、dkk1、alp、osterix、sm22-alpha、klotho、alpha-sma、actriia、axin2和myocd水平和/或活性是在主动脉中的。在优选的实施方式中,phosphosmad2、phosphosmad3、尿蛋白、actriia、axin2和col1a1的水平和/或活性是在肾脏中的。在优选的实施方式中,所述激活素水平和/或活性是在血清中的。在某些实施方式中,所述升高的激活素水平是在管周肌成纤维细胞中的。在某些实施方式中,所述升高的激活素水平不是在肾脏上皮中的。在某些实施方式中,所述升高的激活素水平是在管周肌成纤维细胞中的,并且所述升高的激活素水平不是在肾脏上皮中的。
本领域技术人员将认识到,runx2、alp、snai1、phosphosmad2、dkk1、col1a1、激活素、bsap、ctx、osterix、klotho、alpha-sma、myocd、actriia、axin2、sm22-alpha、phosphosmad3和尿蛋白的一种或更多种的水平和/或活性可以与相应参考群体中的水平和/或活性分别地和独立地比较,例如,如上文在章节8.3.1中描述的。
8.6.2参考群体
在某些实施方式中,利用获自本文描述的参考群体的数据(例如,生物标记物水平或临床症状)来确定从根据本文提供的方法治疗的或要治疗的对象获得的类似数据是病理学上高的(例如,提高的)还是低的(例如,降低的)。
在某些实施方式中,参考群体的大小可以是1、5、10、25、50、75、100、200、250、300、400、500或1000个个体。在某些实施方式中,所述参考群体由随机的志愿者组成。在某些实施方式中,所述参考群体由健康人组成。在某些实施方式中,所述参考群体由与章节8.4中描述的患者群体相同年龄、体重和/或性别的人组成。在某些实施方式中,所述参考群体由没有心血管疾病的人组成。在某些实施方式中,所述参考群体由没有血管钙化的人组成。在某些实施方式中,所述参考群体由没有心血管疾病的人组成。在某些实施方式中,所述参考群体由没有与血管钙化相关和/或由血管钙化引起的心血管疾病的人组成。在某些实施方式中,所述参考群体由没有肾病的人组成。在某些实施方式中,所述参考群体由没有慢性肾病的人组成。在某些实施方式中,所述参考群体由没有动脉硬化水平病理性升高的人组成。在某些实施方式中,所述参考群体由没有与动脉硬化水平升高相关和/或由动脉硬化水平升高引起的心血管疾病的人组成。在某些实施方式中,所述参考群体由没有lvh的人组成。在某些实施方式中,所述参考群体由没有与lvh相关和/或由lvh引起的心血管疾病的人组成。
在某些实施方式中,所述参考群体是指在心血管疾病的一种或更多种症状发作之前根据本文提供的方法治疗的对象。在某些实施方式中,所述参考群体是指在血管钙化的一种或更多种症状发作之前根据本文提供的方法治疗的对象。在某些实施方式中,所述参考群体是指在慢性肾病的一种或更多种症状发作之前根据本文提供的方法治疗的对象。在某些实施方式中,所述参考群体是指在动脉硬化水平升高的一种或更多种症状发作之前根据本文提供的方法治疗的对象。在某些实施方式中,所述参考群体是指在lvh的一种或更多种症状发作之前根据本文提供的方法治疗的对象。在某些实施方式中,所述参考群体是指在诊断对象的心血管疾病之前根据本文提供的方法治疗的对象。在某些实施方式中,所述参考群体是指在诊断对象的血管钙化之前根据本文提供的方法治疗的对象。在某些实施方式中,所述参考群体是指在诊断对象的慢性肾病之前根据本文提供的方法治疗的对象。在某些实施方式中,所述参考群体是指在诊断对象的1期慢性肾病之前根据本文提供的方法治疗的对象。在某些实施方式中,所述参考群体是指在诊断对象的2期慢性肾病之前根据本文提供的方法治疗的对象。在某些实施方式中,所述参考群体是指在诊断对象的3期慢性肾病之前根据本文提供的方法治疗的对象。在某些实施方式中,所述参考群体是指在诊断对象的4期慢性肾病之前根据本文提供的方法治疗的对象。在某些实施方式中,所述参考群体是指在诊断对象的5期慢性肾病之前根据本文提供的方法治疗的对象。在某些实施方式中,所述参考群体是指在诊断对象的动脉硬化水平升高之前根据本文提供的方法治疗的对象。在某些实施方式中,所述参考群体是指在诊断对象的lvh之前根据本文提供的方法治疗的对象。在某些实施方式中,所述参考群体由在根据本文提供的方法治疗之前或被诊断患有本文描述的疾病之前显示了动脉硬化提高的人组成。在某些实施方式中,所述参考群体由在根据本文提供的方法治疗之前或被诊断患有本文描述的疾病之前显示了概述(参见章节6)中记载的标志物之一的上升倾向的人组成。在某些实施方式中,所述参考群体由在根据本文提供的方法治疗之前或被诊断患有本文描述的疾病之前显示了提高水平的runx2、alp、snai1、phosphosmad2、dkk1、col1a1、激活素、bsap、ctx、osterix、phosphosmad3和/或尿蛋白的人组成。在某些实施方式中,所述参考群体由在根据本文提供的方法治疗之前或被诊断患有本文描述的疾病之前显示了概述(参见章节6)中记载的标志物之一的下降倾向的人组成。在某些实施方式中,所述参考群体由在根据本文提供的方法治疗之前或被诊断患有本文描述的疾病之前显示了降低水平的alpha-sma、myocd、sm22-alpha或actriia的人组成。
8.6.3内皮-间充质转变
在某些实施方式中,根据本文提供的方法治疗的对象中的enmt可以通过谱系跟踪分析来监视,以确定细胞群体的结局。在某些实施方式中,根据本文提供的方法治疗的对象中的enmt可以通过定量与enmt相关的一种或更多种蛋白质或转录产物的水平和/或活性来监视,例如,snai1。
8.6.4骨周转
骨周转的各种循环标志物可以用于诊断骨失调,例如,低骨周转。骨周转的循环标志物是骨形成的标志物,例如,骨特异性碱性磷酸酶(bap)、osteocalcin、前胶原i型c-末端原肽(picp)和胰岛素样生长因子-1(igf-1),一些是骨吸收的标志物,例如,吡啶啉、脱氧吡啶啉、酒石酸抗性酸性磷酸酶(trap)、5b型trap、吡啶啉、脱氧吡啶啉和前胶原i型c-末端端肽(ictp),血清或尿胶原蛋白交联(n-端肽或c-端肽)和25羟基维生素d。也可以使用测量整个甲状旁腺激素(pth)分子的分析。熟练的技术人员了解容许评估骨矿物密度(bmd)、骨体积、小梁骨体积和小梁厚度的成象方法。参见,例如tilmanb.druekeandsharonm.moe,disturbancesofboneandmineralmetabolisminchronickidneydisease:aninternationalinitiativetoimprovediagnosisandtreatment,nephroldialtransplant(2004)19:534–536;okunos,inabam.,biochemicalmarkersofboneturnover.newaspect.dialysisandbonemetabolicmarker,clincalcium.2009aug;19(8):1084-91;herberthj,monier-faugeremc,mawadhw,branscumaj,herberthz,wangg,cantort,malluchehh,thefivemostcommonlyusedintactparathyroidhormoneassaysareusefulforscreeningbutnotfordiagnosingboneturnoverabnormalitiesinckd-5subjects,clinnephrol.2009jul;72(1):5-14;lehmanng,ottu,kaemmererd,schuetzej,wolfg.,bonehistomorphometryandbiochemicalmarkersofboneturnoverinsubjectswithchronickidneydiseasestages3–5,clinnephrol.2008oct;70(4):296-305;drüeketb.,isparathyroidhormonemeasurementusefulforthediagnosisofrenalbonedisease?,kidneyint.2008mar;73(6):674-6;yamadas,inabam,kurajohm,shidarak,imanishiy,ishimurae,nishizaway.,utilityofserumtartrate-resistantacidphosphatase(tracp5b)asaboneresorptionmarkerinsubjectswithchronickidneydisease:independencefromrenaldysfunction.,clinendocrinol(oxf).2008aug;69(2):189-96.epub2008jan23。还参见,pauld.miller,diagnosisandtreatmentofosteoporosisinchronicrenaldisease,2009。
监视患有轻微的肾脏功能障碍的ckd对象中骨吸收的另一个标志物是i型胶原蛋白n-端肽(s-ntx)的血清浓度。参见,例如hamanot,fujiin,nagasaway,isakay,moriyamat,okadan,imaie,horiom,itot.,serumntxisapracticalmarkerforassessingantiresorptivetherapyforglucocorticoidtreatedsubjectswithchronickidneydisease.,bone.2006nov;39(5):1067-72.epub2006jun16。
定量的计算机断层扫描(qct)也可以用于测定骨周转。
可以评估标志物,例如runx2和alp,来监视对象中的成骨细胞转变。可以评估标志物,例如sm22-alpha,来监视血管平滑肌功能和分化的血管平滑肌细胞的水平。
8.6.5钙水平
可以通过本领域技术人员已知的方法,例如,钙离子选择电极来分析钙水平。在某些实施方式中,总钙水平是在血清、血液、主动脉或尿液中测量的。
8.6.6血管钙化
用于成像冠状动脉钙化程度(cac)的非对比计算机断层扫描(ct)和用于非侵入性冠状动脉造影(cta)的对比ct是通常用于诊断阻塞性冠心病的发展。也可以使用用于诊断性和预后性心脏评估的放射性核素强度测试、冠状动脉钙扫描和非侵入性冠状动脉血管造影。参见:bermands,shawlj,hachamovitchr,friedmanjd,polkdm,hayessw,thomsonle,germanog,wongnd,kangx,rozanskia.,comparativeuseofradionuclidestresstesting,coronaryarterycalciumscanning,andnoninvasivecoronaryangiographyfordiagnosticandprognosticcardiacassessment,seminnuclmed.2007jan;37(1):2-16。
来自无症状对象的冠状动脉钙筛查结果可以用作比较。例如,当血管钙化与肾病相关时,在肾病发作之前获得的钙筛查结果可以用作比较。
用于检测和定量冠状动脉钙化(cac)的可能的方法包括,但不限于,x-射线计算机断层扫描和心肌灌流单光子发射计算机断层照相(spect)。moserkw,o’keefejhjr,batemantm,mcghieia.,coronarycalciumscreeninginasymptomaticsubjectsasaguidetoriskfactormodificationandstressmyocardialperfusionimaging,jnuclcardiol.2003nov-dec;10(6):590-8。多检测器计算机断层扫描(mdct)也可以用于检测血管钙化(参见,例如,burrilletal.,2007,postgrad.med.j.83(985):698-704)。
血管钙化的另一种诊断方法是联合正电子发射断层扫描(pet)/计算机断层扫描(ct)在胸主动脉壁中的氟18氟脱氧葡萄糖(fdg)摄取。参见:tatsumim,cohadec,nakamotoy,wahlrl.,fluorodeoxyglucoseuptakeintheaorticwallatpet/ct:possiblefindingforactiveatherosclerosis,radiology.2003dec;229(3):831-7.epub2003oct30。
在再另一个实施方式中,超快速ct可以用于检测动脉粥样硬化性冠心病的存在。参见,例如breenjf,sheedypf2nd,schwartzrs,stansonaw,kaufmannrb,mollpp,rumbergerja,coronaryarterycalcificationdetectedwithultrafastctasanindicationofcoronaryarterydisease,radiology.1992nov;185(2):435-9。
电子束计算机断层扫描也可以用于诊断冠状动脉病。参见:schmermunda,baumgartd,sacks,
血管钙化的另一个测试涉及致丛性和血栓栓塞性肺动脉高压中的斑块组成。慢性血栓栓塞性肺动脉高血压与带有富含血型糖蛋白的松软核心的动脉粥样硬化斑块相关,致丛性肺动脉高血压与纤维状斑块相关。血栓栓塞材料在松软核心的形成中起到关键作用,其中红血球膜衍生的血型糖蛋白是主要成分。因而,研究了慢性血栓栓塞性和致丛性肺动脉高血压(原发性和继发性(eisenmenger综合征))。参见:arbustinie,morbinip,d’arminiam,repettoa,minzionig,piovellaf,viganóm,tavazzil,plaquecompositioninplexogenicandthromboembolicpulmonaryhypertension:thecriticalroleofthromboticmaterialinpultaceouscoreformation,heart.2002aug;88(2):177-82。
agatston评分,一种基于沉积的钙斑块的密度测定的钙评分系统,可以用于定量血管钙化。在这一系统中,血管钙化的水平可以通过多检测器计算机断层扫描(mdct)来测量,可以评估agatston评分中进展速率的减弱。(参见,例如sharmaetal.,2010,vasc.healthriskmanag.6:603-611)。
进一步的,血管钙化可以使用adragaoetal.,2004,nephrol.dial.transplant19:1480-1488中描述的方法评估。
用于定量对象中的血管钙化的另一种分析是病变特异性钙评分,其包括由冠状动脉钙化ct检查产生的钙测量方法。这种方法由例如akramandvoros,2008,int.j.cardiovac.imaging14:743-749描述。
8.6.7心脏大小和心脏肥大
心脏大小和心脏肥大可以通过熟练的技术人员已知的任何方法来测定,例如,磁共振成象、心电图描记术、超声波心动描记术和非对比增强的心脏计算机断层扫描。
8.6.8动脉硬化
动脉硬化的水平可以通过熟练的技术人员已知的任何方法来测量,例如,超声多普勒测试,包括磁共振动脉造影的磁共振成像,包括ct血管造影的计算机断层扫描(ct)和本领域已知的其他血管造影形式。
8.6.9肾脏疾病
肾小球滤过率、菊糖清除率、高磷酸血症和bun水平可以通过本领域技术人员已知的任何方法来测定,以确定肾脏疾病。肾脏纤维化和/或肾小球硬化症可以通过熟练的技术人员已知的任何方法诊断和/或监视,例如,肾脏组织的活检以及组织瘢痕形成检查。肾脏纤维化和/或肾小球硬化症还可以通过例如测量肾小球过滤率和/或进行肾脏超声来诊断和/或监视。参见国家的肾脏基金会的网站。
8.6.10动物模型
动脉粥样硬化性低密度脂蛋白受体缺陷(ldlr-/-)的雄性(c57bl/6j背景)可以购自jackson实验室,在12周龄开始用高脂肪饮食(42%的卡路里来自脂肪)(teklad#_)饲喂。小鼠在22周龄时是肥胖的、胰岛素抗性的,在28周龄时是糖尿病的,并且是高胆固醇血症的。
早先描述了用来产生慢性肾病的两步过程(davies,m.r.,etal.,2003.jamsocnephrol14:1559-1567;davies,m.r.,etal.,2005.jamsocnephrol16:917-928.)。电灼可以在出生后12周通过2厘米的侧腹切口施用于右肾,随后在14周龄左侧进行全肾切除术。改变烧灼的强度,以产生中度的(ckd-3)肾脏损伤,其通过20周龄时的菊糖清除率来确认。对照组的小鼠,野生型c57bl/6j小鼠饲喂常规的饮食,其是用于使对照值标准化的正常肾功能和饮食的组。第二组是饲喂高脂肪饮食和假操作的ldlr-/-小鼠,其具有正常的肾脏功能,充当对照组来测定肾脏疾病的作用。第三个组是具有相当于人ckd3期的降低的gfr、饲喂高脂肪饮食(ckd-3)的ldlr-/-小鼠,在22周安乐死,是基线血管钙化组(ckd-3)。第四个组是在22周开始每周两次接受溶媒的皮下注射的患有ckd-3的ldlr-/-小鼠,直到第28周安乐死(ckd-3v)。第五个组是在22周开始每周两次接受10mg/kg的mactriia-fc(celgene,summit,nj)的皮下注射的患有ckd-3的ldlr-/-小鼠,直到第28周安乐死(ckd-3mactriia-fc)。使用的剂量是早先在pk/pd研究中对于刺激骨形成有效的剂量(lotinun,s.,etal.,2010.bone46:1082-1088.)。
使用的第二个ckd的模型是x-连锁的alport’s综合征的鼠同源物,其在iv型胶原蛋白的α5链的基因上是缺陷的,col4a5(rheault,m.n.,etal.,2004.journaloftheamericansocietyofnephrology15:1466-1474.)。这是自发性肾脏疾病的模型。繁育对可以购自jackson实验室,并繁育用于实验。半合子雄性在出生后200天自发地发生与人3-4期ckd可比较的肾脏疾病。
第三个ckd模型是在用于细胞谱系追踪的转基因小鼠gnz小鼠中的肾脏消融,类似于ldlr-/-方案。gnz报告物雌性小鼠()和tek-cre转基因雄性小鼠()可以购自jackson实验室,并繁育产生gnz/tek-cre+小鼠用于实验。gnz/tek-cre-同窝出生作为阴性对照。可以通过使用厂家推荐用于gnz和tek-cre小鼠品系的特异性引物进行小鼠基因分型。
8.6.11转录反应分析
在某些实施方式中,转录反应分析可以用于测试actrii信号转导抑制剂或snai1、phosphosmad2、phosphosmad3、尿蛋白、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx、osterix、klotho、actriia、axin2和/或sm22-alpha的活性。在actrii、snai1、phosphosmad2、phosphosmad3、尿蛋白、dkk1、col1a1、激活素(例如,游离激活素)、runx2、osterix、alp、bsap、ctx、klotho、actriia、axin2和/或sm22-alpha信号转导时,某些基因的转录被上调或下调。可以测量使用的细胞培养系统和转录反应(例如,通过rt-pcr)。试剂对转录反应的影响是其有效性或活性的度量。在某些实施方式中,已知对actrii、snai1、phosphosmad2、phosphosmad3、尿蛋白、dkk1、col1a1、激活素(例如,游离激活素)、runx2、osterix、alp、bsap、ctx、klotho、actriia、axin2和/或sm22-alpha信号转导响应的启动子区域可以被克隆到报告基因的上游。这样,可以简化分析,从而仅需要分析报告基因的活性。
8.6.12筛选分析
各种actrii多肽变体或可溶的actrii多肽变体,可以测试它们抑制actrii的能力。此外,化合物可以测试它们抑制actrii的能力。一旦确认了actrii信号转导抑制剂活性,这些化合物可以用于本文提供的方法。actrii可以是actriia或actriib。以下对actriia描述的分析也可以类似地对actriib进行。
例如,可以评估actriia多肽变体对涉及骨生产或骨破坏的基因的表达的影响。根据需要,这可以在存在一种或更多种重组的actriia配体蛋白(例如,激活素)的情况下进行,细胞可以被转染,以产生actriia多肽和/或其变体,任选地,产生actriia配体。同样地,actriia多肽可以施用给小鼠或其他动物,可以评估一种或更多种骨性质,例如密度或体积。还可以评估骨折的治愈率。双能x射线吸收测定法(dexa)是一种用于评估动物骨密度的成熟的非侵入性定量技术。在人类中,中枢dexa系统可以用于评估脊柱和骨盆的骨密度。这些是总体骨密度的最佳预测值。外周dexa系统可以用于评估外周骨中的骨密度,包括,例如,手、腕部、踝和脚的骨骼。传统的x射线成像系统,包括cat扫描,可以用于评估骨生长和骨折愈合。此外,骨密度可以使用定量计算机断层扫描(qct)来测量。还可以评估骨的机械强度。
在某些方面,本文提供的是actriia多肽(例如,可溶的actriia多肽)和激活素多肽鉴定作为激活素-actriia信号转导途径的激动剂或拮抗剂的化合物(试剂)的用途。可以测试通过这种筛选鉴定的化合物,来评估它们在体外调节骨生长或矿化的能力。任选地,这些化合物可以进一步在动物模型中测试,来评估它们在体内调节组织生长的能力。
有许多方法来筛选通过靶向激活素和actriia多肽调节组织生长的治疗试剂。在某些实施方式中,可以进行化合物的高通量筛选,来鉴定干扰激活素或actriia介导的骨影响的试剂。在某些实施方式中,进行分析来筛选或鉴定特异性抑制或降低actriia多肽与激活素的结合的化合物。做为选择,所述分析可以用于鉴定增强actriia多肽与激活素的结合的化合物。在进一步的实施方式中,可以通过与激活素或actriia多肽相互作用的能力来鉴定化合物。
多种分析形式将是足够的,根据当前的公开,本文没有明确描述的那些仍然可被本领域普通技术人员理解。如本文描述的,本文使用的测试化合物(试剂)可以通过任何组合化学方法来创造。做为选择,目标化合物可以是体内或体外合成的天然发生的生物分子。例如,要测试其作为组织生长调节物的能力的化合物(试剂)可以通过例如细菌、酵母、植物或其他生物体(例如,天然产物)产生,化学地产生(例如,小分子,包括肽模拟物),或重组地产生。本文期待的测试化合物包括非肽基有机分子、肽、多肽、肽模拟物、糖类、激素和核酸分子。在具体的实施方式中,测试试剂是具有小于约2000道尔顿分子量的小的有机分子。
测试化合物可以作为单个的、离散的实体提供,或在更大复杂性的文库中提供,例如,通过组合化学作用制备。这些文库可以包含,例如,醇类、卤烃类、胺类、酰胺类、酯类、醛类、醚类和其他类别的有机化合物。测试化合物向测试系统的呈现可以是分离的形式,或作为化合物的混合物,特别是在初步的筛选步骤中。任选地,化合物可以用其他化合物衍生化,并具有便于化合物分离的衍生基团。衍生基团的非限制性实例包括生物素、荧光素、地加氧原素、绿色荧光蛋白、同位素、多组氨酸、磁珠、谷胱甘肽s转移酶(gst)、光活化性交联剂或其任何组合。
在测试化合物和天然提取物的库的许多药物筛选程序中,高通量分析是期望的,以最大化在给定时间内调查的化合物的数量。在无细胞系统中进行、例如可以用纯化的或半纯化的蛋白质衍生化的分析,通常优选的作为“初级”筛选,因为它们可以被产生以允许快速开发和相对容易地检测由测试化合物介导的分子目标中的改变。此外,测试化合物的细胞毒性和/或生物利用率的影响一般可以在体外系统中忽视,该分析反而主要集中于药物对分子目标的影响,在actriia多肽和激活素之间结合亲和性的改变方面这可能是明显的。
仅为了说明,在示范性的筛选分析中,感兴趣的化合物与分离的和纯化的actriia多肽接触,所述actriia多肽通常能够结合激活素。然后向化合物和actriia多肽的混合物中添加含有actriia配体的组合物。actriia/激活素复合物的检测和定量提供了一种手段来测定化合物抑制(或强化)actriia多肽与激活素之间复合物形成的能力。化合物的效力可以通过从使用各种浓度的测试化合物获得的数据产生剂量反应曲线来评定。此外,还可以进行对照分析来提供用于对比的基线。例如,在对照分析中,分离的和纯化的激活素被添加到含有actriia多肽的组合物中,在不存在测试化合物的情况下测定actriia/激活素复合物的形成。要理解的是,一般地,混合反应物的顺序可以变化,可以同时地混合。此外,代替纯化的蛋白质,细胞提取物和溶胞产物可以用于实现适合的无细胞分析系统。
actriia多肽与激活素之间的复合物形成可以通过多种技术来检测。例如,使用例如可检测地标记的蛋白质,例如放射性标记的(例如,32p、35s、14c或3h)、荧光标记的(例如,fitc)或酶标记的actriia多肽或激活素,通过免疫分析,或通过层析检测,可以测定复合物形成的调节。
在某些实施方式中,在直接地或间接地测量actriia多肽与它的结合蛋白之间的相互作用程度时,本文期待的是使用荧光偏振分析和荧光共振能量传递(fret)分析。进一步的,其他检测方式,例如,基于光波导(pct公开wo96/26432和美国专利no.5,677,196)、表面胞质团共振(spr)、表面电荷传感器和表面力传感器的那些,与本文描述的许多实施方式是相容的。
此外,相互作用陷阱分析,也称为“双杂交分析”可以用于鉴定破坏或强化actriia多肽与它的结合蛋白之间的相互作用的试剂。参见,例如,美国专利no.5,283,317;zervosetal.(1993)cell72:223-232;maduraetal.(1993)jbiolchem268:12046-12054;barteletal.(1993)biotechniques14:920-924;和iwabuchietal.(1993)oncogene8:1693-1696)。在具体的实施方式中,本文期待的是使用反转的双杂交系统来鉴定解除actriia多肽与它的结合蛋白之间的相互作用的化合物(例如,小分子或肽)。参见,例如vidalandlegrain,(1999)nucleicacidsres27:919-29;vidalandlegrain,(1999)trendsbiotechnol17:374-81;和美国专利nos.5,525,490;5,955,280;和5,965,368。
在某些实施方式中,通过它们与actriia或激活素多肽相互作用的能力来鉴定出目标化合物。化合物与actriia或激活素多肽之间的相互作用可以是共价的或是非共价的。例如,这样的相互作用可以使用体外的生物化学方法在蛋白质水平上鉴定,包括光交联、放射性标记的配体结合和亲和层析(jakobywbetal.,1974,methodsinenzymology46:1)。在某些情况下,化合物可以在基于机制的分析中筛选,例如,检测与激活素或actriia多肽结合的化合物的分析。这可以包括固相或液相的结合事件。做为选择,编码激活素或actriia多肽的基因可以与报告物系统(例如,β-半乳糖苷酶、荧光素酶或绿色荧光蛋白)一起转染到细胞中,并优选地通过高通量筛选针对文库来筛选,或用文库的独立成员来筛选。可以使用其他基于机制的结合分析,例如,检测自由能变化的分析。结合分析可以用固定在反应孔、珠子或芯片上或通过固定化抗体捕获的或通过毛细管电泳分辨的靶标来进行。结合的化合物通常可以使用比色或荧光或表面胞质团共振来检测。
在某些方面,本文提供的是调节(刺激或抑制)骨形成和提高骨质量的方法和试剂。因而,所鉴定的任何化合物可以在完整细胞或组织中体外或体内地测试,来确认它们调节骨生长或矿化的能力。为此目标可以利用本领域已知的各种方法。特别地,化合物可以测试它们提高骨周转的能力。
例如,actriia或激活素多肽或测试化合物对骨或软骨生长的影响,可以通过在基于细胞的分析中测量msx2的诱导或骨祖细胞向成骨细胞的分化来测定(参见,例如daluiskietal.,natgenet.2001,27(1):84-8;hinoetal.,frontbiosci.2004,9:1520-9)。基于细胞的分析的其他实例包括分析目标actriia或激活素多肽以及测试化合物在间充质祖代和成骨细胞中的成骨活性。举例来说,可以构建表达激活素或actriia多肽的重组腺病毒,来感染多能的间充质祖代c3h10t1/2细胞、前成骨细胞性c2cl2细胞以及成骨细胞性te-85细胞。然后通过测量碱性磷酸酶的诱导、骨钙素和基质矿化来确定成骨活性(参见,例如chengetal.,jbonejointsurgam.2003,85-a(8):1544-52).
本文还提供的是测量骨或软骨生长的体内分析。例如,公开了namkung-matthaietal.,bone,28:80-86(2001)大鼠骨质疏松模型,在其中研究了骨折后早期的骨修复。kuboetal.,steroidbiochemistry&molecularbiology,68:197-202(1999)也公开了大鼠骨质疏松模型,在其中研究了骨折后早期的骨修复。描述了小鼠骨质疏松症模型,其中小鼠是切除卵巢的,这引起小鼠丢失实质的骨矿物含量以及骨矿物密度,其小梁骨损失大约50%的骨矿物密度。通过施用因子例如甲状旁腺激素,切除卵巢的小鼠中的骨密度可以提高。在某些方面,可以使用本领域已知的骨折愈合分析。这些分析包括骨折技术、组织学分析和生物力学分析,其在例如美国专利no.6,521,750中描述了,对于它引起以及测量骨折的程度和修复过程的实验方案公开内容,通过将其完全引用合并在本文中。
8.7激活素ii型受体信号转导抑制剂的剂量
在某些实施方式中,actrii信号转导抑制剂是章节8.5.1中阐述的actriia信号转导的抑制剂。在其他实施方式中,actrii抑制剂是章节8.5.2中阐述的actriib信号转导的抑制剂。在某些实施方式中,actrii信号转导抑制剂是actriia信号转导抑制剂与actriib信号转导抑制剂的组合。
在某些实施方式中,actrii信号转导抑制剂以足以实现0.2微克/kg或更高的血清浓度的间隔和数量给药,1微克/kg或2微克/kg或更高的血清水平对于实现对骨密度和强度的显著影响是希望的。可以设计给药方案来达到0.2到15微克/kg之间的血清浓度,任选的1到5微克/kg之间。在人类中,0.2微克/kg的血清水平可以用0.1mg/kg或更高的单次剂量来实现,1微克/kg的血清水平可以用0.3mg/kg或更高的单次剂量来实现。观察到的分子血清半衰期在约20到30天之间,实质上更长于大多数fc融合蛋白,因而可以实现持续有效的血清水平,例如,通过用0.2-0.4mg/kg每周或每两周给药,或者更高的剂量可以与给药之间更长的间隔一起运用。例如,可以在每月或每两个月的基础上使用1-3mg/kg的剂量,对骨的作用可能足够耐久,从而仅需要每3、4、5、6、9、12或更多个月给药一次。actrii信号转导抑制剂的血清水平可以通过熟练的技术人员已知的任何手段来测量。例如,利用例如elisa,针对actrii信号转导抑制剂的抗体可以用于测定actrii信号转导抑制剂的血清水平。
在某些实施方式中,actrii信号转导抑制剂的剂量静脉内地是0.01到3.0mg/kg,或皮下地是0.03到0.1mg/kg。在某些实施方式中,actrii信号转导抑制剂的剂量是约0.01mg/kg、约0.1mg/kg、约0.13mg/kg、约0.2mg/kg、约0.26mg/kg、约0.3mg/kg、约0.4mg/kg、约0.5mg/kg、约0.6mg/kg、约0.7mg/kg、约0.8mg/kg、约0.9mg/kg、约1.0mg/kg、约1.5mg/kg、约2.0mg/kg、约2.5mg/kg、约3.0mg/kg、约3.5mg/kg、约4.0mg/kg、约4.5mg/kg或约5.0mg/kg。在某些实施方式中,actrii信号转导抑制剂的剂量是约10.0mg/kg、约15.0mg/kg、约20.0mg/kg、约25.0mg/kg或约30.0mg/kg。在某些实施方式中,actrii信号转导抑制剂的剂量是在0.01mg/kg到0.1mg/kg之间、0.1mg/kg到0.3mg/kg之间、0.3mg/kg到0.5mg/kg之间、0.3mg/kg到0.8mg/kg之间、0.5mg/kg到1.0mg/kg之间、1.0mg/kg到2.0mg/kg之间、1.0mg/kg到3.0mg/kg之间、2.0mg/kg到3.0mg/kg之间、2.0mg/kg到4.0mg/kg之间、3.0mg/kg到5.0mg/kg之间、5.0mg/kg到10.0mg/kg之间、10.0mg/kg到15.0mg/kg之间、10.0mg/kg到20.0mg/kg之间、15.0mg/kg到20.0mg/kg之间或20.0mg/kg到30.0mg/kg之间。在某些实施方式中,所述剂量是约15mg、约30mg、约45mg、约60mg、约75mg、约90mg或约1g。在某些实施方式中,所述剂量是约0.1mg/kg。在某些实施方式中,所述剂量是约0.3mg/kg。在某些实施方式中,所述剂量是约0.5mg/kg。在某些实施方式中,所述剂量是约0.7mg/kg。
在某些实施方式中,所述剂量是药学上有效的剂量。在某些实施方式中,所述药学上有的效剂量是约15mg、约30mg、约45mg、约60mg、约75mg、约90mg或约1g或约0.1mg/kg、约0.13mg/kg、约0.2mg/kg、约0.26mg/kg、约0.3mg/kg、约0.4mg/kg、约0.5mg/kg、约0.6mg/kg、约0.7mg/kg、约0.8mg/kg、约0.9mg/kg、约1.0mg/kg、约1.1mg/kg、约1.2mg/kg、约1.3mg/kg、约1.4mg/kg或约1.5mg/kg。在某些实施方式中,所述药学上有效的剂量是约0.1mg/kg。在某些实施方式中,所述药学上有效的剂量是约0.3mg/kg。在某些实施方式中,所述药学上有效的剂量是约0.5mg/kg。在某些实施方式中,所述药学上有效的剂量是约0.7mg/kg。
在某些实施方式中,所述剂量是初始剂量。在某些实施方式中,所述初始剂量是约15mg、约30mg、约45mg、约60mg、约75mg、约90mg或约1g或约0.1mg/kg、约0.13mg/kg、约0.2mg/kg、约0.26mg/kg、约0.3mg/kg、约0.4mg/kg、约0.5mg/kg、约0.6mg/kg、约0.7mg/kg、约0.8mg/kg、约0.9mg/kg、约1.0mg/kg、约1.1mg/kg、约1.2mg/kg、约1.3mg/kg、约1.4mg/kg或约1.5mg/kg。在某些实施方式中,所述药学上有效的剂量是约0.1mg/kg。在某些实施方式中,所述初始剂量是约0.3mg/kg。在某些实施方式中,所述初始剂量是约0.5mg/kg。在某些实施方式中,所述初始剂量是约0.7mg/kg。在某些实施方式中,所述初始剂量是(i)每28天施用一次;或(ii)每42天施用一次。在某些实施方式中,所述初始剂量是每14天施用一次。在某些实施方式中,所述初始剂量是每21天施用一次。
在某些实施方式中,所述初始剂量每1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24、25、26、27或28天施用一次。在某些实施方式中,所述初始剂量每1、2、3、4、5或6周施用一次。在某些实施方式中,所述初始剂量每2周施用一次。在某些实施方式中,所述初始剂量是约0.1mg/kg、约0.13mg/kg、约0.2mg/kg、约0.26mg/kg、约0.3mg/kg、约0.4mg/kg、约0.5mg/kg、约0.6mg/kg、约0.7mg/kg、约0.8mg/kg、约0.9mg/kg、约1.0mg/kg、约1.1mg/kg、约1.2mg/kg、约1.3mg/kg、约1.4mg/kg或约1.5mg/kg,并且每1、2、3、4、5或6周施用一次。在某些实施方式中,所述初始剂量在约0.3到约0.8mg/kg之间并且每2周施用一次。在某些实施方式中,所述初始剂量是约0.1mg/kg、约0.13mg/kg、约0.3mg/kg、约0.4mg/kg、约0.5mg/kg、约0.6mg/kg、约0.7mg/kg、约0.8mg/kg、约0.9mg/kg、约1.0mg/kg、约1.1mg/kg、约1.2mg/kg、约1.3mg/kg、约1.4mg/kg或约1.5mg/kg,并且每1、2、3、4、5或6周施用一次。。在某些实施方式中,所述初始剂量是约0.3mg/kg、约0.4mg/kg、约0.5mg/kg、约0.6mg/kg、约0.7mg/kg、约0.8mg/kg、约0.9mg/kg、约1.0mg/kg、约1.1mg/kg、约1.2mg/kg、约1.3mg/kg、约1.4mg/kg或约1.5mg/kg,并且每2周施用一次。。在某些实施方式中,所述初始剂量是约0.3mg/kg,并且每2周施用一次。在某些实施方式中,所述初始剂量是约0.5mg/kg,并且每2周施用一次。在某些实施方式中,所述初始剂量是约0.7mg/kg,并且每2周施用一次。在某些实施方式中,所述初始剂量是约0.8mg/kg,并且每2周施用一次。
在某些实施方式中,所述剂量是调整的剂量。在某些实施方式中,所述调整的剂量大于所述初始剂量。在某些实施方式中,所述调整剂量是约2.5mg、约5mg、约10mg、约15mg、约20mg或约35mg大于所述初始剂量,或约0.05mg/kg、约0.1mg/kg、约0.15mg/kg、约0.25mg/kg、约0.3mg/kg、约0.35mg/kg、约0.4mg/kg或约0.5mg/kg大于所述初始剂量。在某些实施方式中,所述调整的剂量比所述初始剂量更频繁地施用。在某些实施方式中,所述调整的剂量每5、10、15、20、25、28、30、35或40天施用。
在某些实施方式中,所述调整的剂量小于所述初始剂量。在某些实施方式中,所述调整的剂量是约2.5mg、约5mg、约10mg、约15mg、约20mg或约35mg小于所述初始剂量,或约0.05mg/kg、约0.1mg/kg、约0.15mg/kg、约0.25mg/kg、约0.3mg/kg、约0.35mg/kg、约0.4mg/kg或约0.5mg/kg小于所述初始剂量。在某些实施方式中,所述调整的剂量比所述初始剂量较少频繁地施用。在某些实施方式中,所述调整的剂量每30、35、40、42、50、60、70、80或90天施用。
在某些实施方式中,所述剂量通过注射施用。在某些实施方式中,所述剂量每28天施用一次,或每42天施用一次。在某些实施方式中,连续地和/或无限地施用所述剂量。
在某些实施方式中,与参考群体(例如,如章节8.6中描述的参考群体)中激活素的水平和/或活性相比,根据本文提供的方法向对象施用的actrii信号转导抑制剂的剂量足以降低所述对象中激活素的水平和/或活性至少5%、10%、15%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、95%或至少100%,或最多5%、10%、15%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、95%或最多100%。在某些实施方式中,所述激活素是游离激活素,例如,不与卵泡抑素、卵泡抑素样3或抑制素缔合的激活素。在某些实施方式中,所述激活素是激活素a。在某些实施方式中,激活素水平和/或活性通过如章节8.6中描述的分析来测定。
在某些实施方式中,与参考群体(例如,如章节8.6中描述的参考群体)中的smad依赖性信号转导相比,根据本文提供的方法向对象施用的actrii信号转导抑制剂的剂量足以降低所述对象中的smad依赖性信号转导至少5%、10%、15%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、95%或至少100%,或最多5%、10%、15%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、95%或最多100%。在某些实施方式中,smad依赖性信号转导通过如章节8.6中描述的分析来测定。
在某些实施方式中,与参考群体(例如,如章节8.6中描述的参考群体)中runx2的水平和/或活性相比,根据本文提供的方法向对象施用的actrii信号转导抑制剂的剂量足以降低所述对象中runx2的水平和/或活性至少5%、10%、15%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、95%或至少100%,或最多5%、10%、15%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、95%或最多100%。在某些实施方式中,runx2水平和/或活性通过如章节8.6中描述的分析来测定。
在某些实施方式中,与参考群体(例如,如章节8.6中描述的参考群体)中alp的水平和/或活性相比,根据本文提供的方法向对象施用的actrii信号转导抑制剂的剂量足以降低所述对象中alp的水平和/或活性达至少5%、10%、15%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、95%或至少100%,或最多5%、10%、15%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、95%或最多100%。在某些实施方式中,alp水平和/或活性通过如章节8.6中描述的分析来测定。
在某些实施方式中,与参考群体(例如,如章节8.6中描述的参考群体)中snai1的水平和/或活性相比,根据本文提供的方法向对象施用的actrii信号转导抑制剂的剂量足以降低所述对象中snai1的水平和/或活性达至少5%、10%、15%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、95%或至少100%,或最多5%、10%、15%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、95%或最多100%。在某些实施方式中,snai1水平和/或活性通过如章节8.6中描述的分析来测定。
在某些实施方式中,与参考群体(例如,如章节8.6中描述的参考群体)中phosphosmad2的水平和/或活性相比,根据本文提供的方法向对象施用的actrii信号转导抑制剂的剂量足以降低所述对象中phosphosmad2的水平和/或活性达至少5%、10%、15%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、95%或至少100%,或最多5%、10%、15%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、95%或最多100%。在某些实施方式中,phosphosmad2水平和/或活性通过如章节8.6中描述的分析来测定。
在某些实施方式中,与参考群体(例如,如章节8.6中描述的参考群体)中phosphosmad3的水平和/或活性相比,根据本文提供的方法向对象施用的actrii信号转导抑制剂的剂量足以降低所述对象中phosphosmad3的水平和/或活性达至少5%、10%、15%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、95%或至少100%,或最多5%、10%、15%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、95%或最多100%。在某些实施方式中,phosphosmad3水平和/或活性通过如章节8.6中描述的分析来测定。
在某些实施方式中,与参考群体(例如,如章节8.6中描述的参考群体)中尿蛋白的水平和/或活性相比,根据本文提供的方法向对象施用的actrii信号转导抑制剂的剂量足以降低所述对象中尿蛋白的水平和/或活性达至少5%、10%、15%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、95%或至少100%,或最多5%、10%、15%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、95%或最多100%。在某些实施方式中,尿蛋白水平和/或活性通过如章节8.6中描述的分析来测定。
在某些实施方式中,与参考群体(例如,如章节8.6中描述的参考群体)中dkk1的水平和/或活性相比,根据本文提供的方法向对象施用的actrii信号转导抑制剂的剂量足以降低所述对象中dkk1的水平和/或活性达至少5%、10%、15%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、95%或至少100%,或最多5%、10%、15%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、95%或最多100%。在某些实施方式中,dkk1水平和/或活性通过如章节8.6中描述的分析来测定。
在某些实施方式中,与参考群体(例如,如章节8.6中描述的参考群体)中col1a1的水平和/或活性相比,根据本文提供的方法向对象施用的actrii信号转导抑制剂的剂量足以降低所述对象中col1a1的水平和/或活性达至少5%、10%、15%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、95%或至少100%,或最多5%、10%、15%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、95%或最多100%。在某些实施方式中,col1a1水平和/或活性通过如章节8.6中描述的分析来测定。
在某些实施方式中,与参考群体(例如,如章节8.6中描述的参考群体)中bsap的水平和/或活性相比,根据本文提供的方法向对象施用的actrii信号转导抑制剂的剂量足以降低所述对象中bsap的水平和/或活性达至少5%、10%、15%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、95%或至少100%,或最多5%、10%、15%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、95%或最多100%。在某些实施方式中,bsap水平和/或活性通过如章节8.6中描述的分析来测定。
在某些实施方式中,与参考群体(例如,如章节8.6中描述的参考群体)中ctx的水平和/或活性相比,根据本文提供的方法向对象施用的actrii信号转导抑制剂的剂量足以降低所述对象中ctx的水平和/或活性达至少5%、10%、15%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、95%或至少100%,或最多5%、10%、15%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、95%或最多100%。在某些实施方式中,ctx水平和/或活性通过如章节8.6中描述的分析来测定。
在某些实施方式中,与参考群体(例如,如章节8.6中描述的参考群体)中osterix的水平和/或活性相比,根据本文提供的方法向对象施用的actrii信号转导抑制剂的剂量足以降低所述对象中osterix的水平和/或活性达至少5%、10%、15%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、95%或至少100%,或最多5%、10%、15%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、95%或最多100%。在某些实施方式中,osterix水平和/或活性通过如章节8.6中描述的分析来测定。
在某些实施方式中,与参考群体(例如,如章节8.6中描述的参考群体)中actriia的水平和/或活性相比,根据本文提供的方法向对象施用的actrii信号转导抑制剂的剂量足以降低所述对象中actriia的水平和/或活性达至少5%、10%、15%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、95%或至少100%,或最多5%、10%、15%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、95%或最多100%。在某些实施方式中,actriia水平和/或活性通过如章节8.6中描述的分析来测定。
在某些实施方式中,与参考群体(例如,如章节8.6中描述的参考群体)中klotho的水平和/或活性相比,根据本文提供的方法向对象施用的actrii信号转导抑制剂的剂量足以提高所述对象中klotho的水平和/或活性达至少5%、10%、15%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、100%、125%、150%、175%、200%、250%、300%、350%、400%、450%或至少500%,或最多5%、10%、15%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、100%、125%、150%、175%、200%、250%、300%、350%、400%、450%或最多500%。在某些实施方式中,klotho水平和/或活性通过如章节8.6中描述的分析来测定。
在某些实施方式中,与参考群体(例如,如章节8.6中描述的参考群体)中alpha-sma的水平和/或活性相比,根据本文提供的方法向对象施用的actrii信号转导抑制剂的剂量足以提高所述对象中alpha-sma的水平和/或活性达至少5%、10%、15%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、100%、125%、150%、175%、200%、250%、300%、350%、400%、450%或至少500%,或最多5%、10%、15%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、100%、125%、150%、175%、200%、250%、300%、350%、400%、450%或最多500%。在某些实施方式中,alpha-sma水平和/或活性通过如章节8.6中描述的分析来测定。
在某些实施方式中,与参考群体(例如,如章节8.6中描述的参考群体)中myocd的水平和/或活性相比,根据本文提供的方法向对象施用的actrii信号转导抑制剂的剂量足以提高所述对象中myocd的水平和/或活性达至少5%、10%、15%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、100%、125%、150%、175%、200%、250%、300%、350%、400%、450%或至少500%,或最多5%、10%、15%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、100%、125%、150%、175%、200%、250%、300%、350%、400%、450%或最多500%。在某些实施方式中,myocd水平和/或活性通过如章节8.6中描述的分析来测定。
在某些实施方式中,与参考群体(例如,如章节8.6中描述的参考群体)中axin2的水平和/或活性相比,根据本文提供的方法向对象施用的actrii信号转导抑制剂的剂量足以提高所述对象中axin2的水平和/或活性达至少5%、10%、15%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、100%、125%、150%、175%、200%、250%、300%、350%、400%、450%或至少500%,或最多5%、10%、15%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、100%、125%、150%、175%、200%、250%、300%、350%、400%、450%或最多500%。在某些实施方式中,axin2水平和/或活性通过如章节8.6中描述的分析来测定。
在某些实施方式中,与参考群体(例如,如章节8.6中描述的参考群体)中血管平滑肌蛋白质水平相比,根据本文提供的方法向对象施用的actrii信号转导抑制剂的剂量足以提高所述对象中血管平滑肌蛋白质水平,例如,sm22-alpha。在某些实施方式中,血管平滑肌蛋白质水平和/或活性通过如章节8.6中描述的分析来测定。在某些实施方式中,与参考群体(例如,如章节8.6中描述的参考群体)中sm22-alpha的水平和/或活性相比,根据本文提供的方法向对象施用的actrii信号转导抑制剂的剂量足以提高所述对象中sm22-alpha的水平和/或活性达至少5%、10%、15%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、100%、125%、150%、175%、200%、250%、300%、350%、400%、450%或至少500%,或最多5%、10%、15%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、100%、125%、150%、175%、200%、250%、300%、350%、400%、450%或最多500%。在某些实施方式中,sm22-alpha水平和/或活性通过如章节8.6中描述的分析来测定。
在某些实施方式中,与参考群体(例如,如章节8.6中描述的参考群体)中的骨体积相比,根据本文提供的方法向对象施用的actrii信号转导抑制剂的剂量足以提高所述对象中的骨体积达至少5%、10%、15%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、95%或至少100%,或最多5%、10%、15%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、95%或最多100%。在某些实施方式中,骨体积通过如章节8.6中描述的分析来测定。
在某些实施方式中,与参考群体(例如,如章节8.6中描述的参考群体)中破骨细胞凹陷表面相比,根据本文提供的方法向对象施用的actrii信号转导抑制剂的剂量足以降低所述对象中破骨细胞凹陷表面达至少5%、10%、15%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、95%或至少100%,或最多5%、10%、15%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、95%或最多100%。在某些实施方式中,破骨细胞凹陷表面通过如章节8.6中描述的分析来测定。
在某些实施方式中,与参考群体(例如,如章节8.6中描述的参考群体)中的骨形成率相比,根据本文提供的方法向对象施用的actrii信号转导抑制剂的剂量足以维持所述对象的骨形成率,或最低限度地提高或降低所述对象的骨形成率,例如,最多1%、2.5%、5%、10%或15%。在某些实施方式中,骨形成率通过如章节8.6中描述的分析来测定。
在某些实施方式中,与参考群体(例如,如章节8.6中描述的参考群体)中的成骨细胞表面相比,根据本文提供的方法向对象施用的actrii信号转导抑制剂的剂量足以维持所述对象的成骨细胞表面,或最低限度地提高或降低所述对象的成骨细胞表面,例如,最多1%、2.5%、5%、10%或15。在某些实施方式中,成骨细胞表面通过如章节8.6中描述的分析来测定。
在某些实施方式中,与参考群体(例如,如章节8.6中描述的参考群体)中主动脉的成骨细胞转变相比,根据本文提供的方法向对象施用的actrii信号转导抑制剂的剂量足以降低所述对象中主动脉的成骨细胞转变达至少5%、10%、15%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、95%或至少100%,或最多5%、10%、15%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、95%或最多100%。在某些实施方式中,主动脉的成骨细胞转变通过如章节8.6中描述的分析来测定。
在某些实施方式中,与参考群体(例如,如章节8.6中描述的参考群体)中的成骨细胞数量相比,根据本文提供的方法向对象施用的actrii信号转导抑制剂的剂量足以降低所述对象的成骨细胞数量达至少5%、10%、15%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、95%或至少100%,或最多5%、10%、15%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、95%或最多100%。在某些实施方式中,成骨细胞数量通过如章节8.6中描述的分析来测定。
在某些实施方式中,与参考群体(例如,如章节8.6中描述的参考群体)中的成骨细胞表面与骨表面比相比,根据本文提供的方法向对象施用的actrii信号转导抑制剂的剂量足以降低所述对象的成骨细胞表面与骨表面比达至少5%、10%、15%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、95%或至少100%,或最多5%、10%、15%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、95%或最多100%。在某些实施方式中,成骨细胞表面与骨表面比通过如章节8.6中描述的分析来测定。
在某些实施方式中,与参考群体(例如,如章节8.6中描述的参考群体)中的破骨细胞数量相比,根据本文提供的方法向对象施用的actrii信号转导抑制剂的剂量足以降低所述对象的破骨细胞数量达至少5%、10%、15%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、95%或至少100%,或最多5%、10%、15%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、95%或最多100%。在某些实施方式中,破骨细胞数量通过如章节8.6中描述的分析来测定。
在某些实施方式中,与参考群体(例如,如章节8.6中描述的参考群体)中的破骨细胞表面与骨表面比相比,根据本文提供的方法向对象施用的actrii信号转导抑制剂的剂量足以降低所述对象的破骨细胞表面与骨表面比达至少5%、10%、15%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、95%或至少100%,或最多5%、10%、15%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、95%或最多100%。在某些实施方式中,破骨细胞表面与骨表面比通过如章节8.6中描述的分析来测定。
在某些实施方式中,与参考群体(例如,如章节8.6中描述的参考群体)中的小梁骨体积相比,根据本文提供的方法向对象施用的actrii信号转导抑制剂的剂量足以提高所述对象的小梁骨体积达至少5%、10%、15%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、100%、125%、150%、175%、200%、250%、300%、350%、400%、450%或至少500%,或最多5%、10%、15%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、100%、125%、150%、175%、200%、250%、300%、350%、400%、450%或最多500%。在某些实施方式中,小梁骨体积通过如章节8.6中描述的分析来测定。
在某些实施方式中,与参考群体(例如,如章节8.6中描述的参考群体)中的小梁厚度相比,根据本文提供的方法向对象施用的actrii信号转导抑制剂的剂量足以提高所述对象的小梁厚度达至少5%、10%、15%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、100%、125%、150%、175%、200%、250%、300%、350%、400%、450%或至少500%,或最多5%、10%、15%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、100%、125%、150%、175%、200%、250%、300%、350%、400%、450%或最多500%。在某些实施方式中,小梁厚度通过如章节8.6中描述的分析来测定。
在某些实施方式中,与参考群体(例如,如章节8.6中描述的参考群体)中的血管平滑肌功能相比,根据本文提供的方法向对象施用的actrii信号转导抑制剂的剂量足以提高所述对象的血管平滑肌功能达至少5%、10%、15%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、100%、125%、150%、175%、200%、250%、300%、350%、400%、450%或至少500%,或最多5%、10%、15%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、100%、125%、150%、175%、200%、250%、300%、350%、400%、450%或最多500%。在某些实施方式中,血管平滑肌功能通过如章节8.6中描述的分析来测定。
在某些实施方式中,与参考群体(例如,如章节8.6中描述的参考群体)中的血管钙化相比,根据本文提供的方法向对象施用的actrii信号转导抑制剂的剂量足以降低所述对象的血管钙化达至少5%、10%、15%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、95%或至少100%,或最多5%、10%、15%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、95%或最多100%。在某些实施方式中,血管钙化通过如章节8.6中描述的分析来测定。在某些实施方式中,与参考群体(例如,如章节8.6中描述的参考群体)中的血管钙水平相比,根据本文提供的方法向对象施用的actrii信号转导抑制剂的剂量足以降低所述对象的血管钙水平达至少5%、10%、15%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、95%或至少100%,或最多5%、10%、15%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、95%或最多100%。在某些实施方式中,血管钙水平通过如章节8.6中描述的分析来测定。
在某些实施方式中,与参考群体(例如,如章节8.6中描述的参考群体)中的主动脉钙水平相比,根据本文提供的方法向对象施用的actrii信号转导抑制剂的剂量足以降低所述对象的主动脉钙水平达至少5%、10%、15%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、95%或至少100%,或最多5%、10%、15%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、95%或最多100%。在某些实施方式中,主动脉钙水平通过如章节8.6中描述的分析来测定。在某些实施方式中,与参考群体(例如,如章节8.6中描述的参考群体)的主动脉粥样斑中的钙沉积相比,根据本文提供的方法向对象施用的actrii信号转导抑制剂的剂量足以降低所述对象的主动脉粥样斑中的钙沉积达至少5%、10%、15%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、95%或至少100%,或最多5%、10%、15%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、95%或最多100%。在某些实施方式中,主动脉粥样斑中的钙沉积通过如章节8.6中描述的分析来测定。
在某些实施方式中,与参考群体(例如,如章节8.6中描述的参考群体)中的enmt相比,根据本文提供的方法向对象施用的actrii信号转导抑制剂的剂量足以降低所述对象中ckd诱导的内皮向间充质转变(enmt)达至少5%、10%、15%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、95%或至少100%,或最多5%、10%、15%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、95%或最多100%。在某些实施方式中,enmt通过如章节8.6中描述的分析来测定。
在某些实施方式中,与参考群体(例如如章节8.6中描述的参考群体)中的心脏大小(例如,心脏重量)相比,根据本文提供的方法向对象施用的actrii信号转导抑制剂的剂量足以降低所述对象的心脏大小(例如,心脏重量)达至少1%、2%、3%、4%、5%、6%、7%、8%、9%或至少10%,或最多1%、2%、3%、4%、5%、6%、7%、8%、9%或至少10%。在某些实施方式中,心脏大小通过如章节8.6中描述的分析来测定。
在某些实施方式中,与参考群体(例如,如章节8.6中描述的参考群体)中的分化的血管平滑肌细胞水平相比,根据本文提供的方法向对象施用的actrii信号转导抑制剂的剂量足以提高所述对象的分化的血管平滑肌细胞水平达至少5%、10%、15%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、95%、100%、125%、150%、175%、200%、250%、300%、350%、400%、450%或至少500%,或最多5%、10%、15%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、95%、100%、125%、150%、175%、200%、250%、300%、350%、400%、450%或最多500%。在某些实施方式中,血分化的血管平滑肌细胞水平通过如章节8.6中描述的分析来测定。
在某些实施方式中,与参考群体(例如,如章节8.6中描述的参考群体)中的动脉硬化相比,根据本文提供的方法向对象施用的actrii信号转导抑制剂的剂量足以降低所述对象的动脉硬化水平升高达至少5%、10%、15%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、95%或至少100%,或最多5%、10%、15%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、95%或最多100%。在某些实施方式中,动脉硬化通过如章节8.6中描述的分析来测定。在某些实施方式中,与参考群体(例如,如章节8.6中描述的参考群体)中的动脉硬化相比,根据本文提供的方法施用的actrii信号转导抑制剂的剂量足以降低所述对象的动脉硬化水平升高达至少5%、10%、15%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、95%或至少100%,或最多5%、10%、15%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、95%或最多100%。在某些实施方式中,动脉硬化通过如章节8.6中描述的分析来测定。
在某些实施方式中,与参考群体(例如,如章节8.6中描述的参考群体)中的矿物质合并率相比,根据本文提供的方法向对象施用的actrii信号转导抑制剂的剂量足以维持所述对象的矿物质合并率,或最低限度地提高或降低所述对象的最小合并率,例如,最多1%、2.5%、5%、10%或15%。在某些实施方式中,矿物质合并率通过如章节8.6中描述的分析来测定。
在某些实施方式中,与参考群体(例如,如章节8.6中描述的参考群体)中的高磷酸血症相比,根据本文提供的方法向对象施用的actrii信号转导抑制剂的剂量足以维持所述对象的高磷酸血症,或最低限度地提高或降低所述对象的高磷酸血症,例如,最多1%、2.5%、5%、10%或15%。在某些实施方式中,高磷酸血症通过如章节8.6中描述的分析来测定。
在某些实施方式中,与参考群体(例如,如章节8.6中描述的参考群体)中的fgf23水平相比,根据本文提供的方法向对象施用的actrii信号转导抑制剂的剂量足以维持所述对象的fgf23水平,或最低限度地提高或降低所述对象的fgf23水平,例如,最多1%、2.5%、5%、10%或15%。在某些实施方式中,fgf水平和/或活性通过如章节8.6中描述的分析来测定。
在某些实施方式中,与参考群体(例如,如章节8.6中描述的参考群体)中的肾脏纤维化相比,根据本文提供的方法向对象施用的actrii信号转导抑制剂的剂量足以降低所述对象的肾脏纤维化达至少5%、10%、15%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、95%或至少100%,或最多5%、10%、15%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、95%或最多100%。在某些实施方式中,肾脏纤维化通过如章节8.6中描述的分析来测定。在某些实施方式中,与参考群体(例如,如章节8.6中描述的参考群体)中的肾小球硬化症相比,根据本文提供的方法向对象施用的actrii信号转导抑制剂的剂量足以降低所述对象的肾小球硬化症达至少5%、10%、15%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、95%或至少100%,或最多5%、10%、15%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、95%或最多100%。在某些实施方式中,肾小球硬化症通过如章节8.6中描述的分析来测定。
在某些实施方式中,根据本文提供的方法向对象施用的actrii信号转导抑制剂的剂量足以归一化本文提供的一种或更多种生物标记物(例如,runx2、alp、snai1、phosphosmad2、dkk1、col1a1、激活素、bsap、ctx、osterix、klotho、alpha-sma、myocd、sm22-alpha、phosphosmad3、尿蛋白和/或actriia)的水平。例如,在某些实施方式中,根据本文提供的方法向对象施用的actrii信号转导抑制剂的剂量足以提高或降低本文提供的一种或更多种生物标记物(例如,runx2、alp、snai1、phosphosmad2、dkk1、col1a1、激活素、bsap、ctx、osterix、klotho、alpha-sma、myocd、sm22-alpha、phosphosmad3、尿蛋白和/或actriia)的水平到参考群体(例如,如章节8.6中描述的参考群体)中相应生物标记物的水平。
在某些实施方式中,根据本文提供的方法向对象施用的actrii信号转导抑制剂的剂量足以治疗和/或预防所述对象的心脏肥大。在某些实施方式中,心脏肥大通过如章节8.6中描述的分析来测定。在某些实施方式中,根据本文提供的方法向对象施用的actrii信号转导抑制剂的剂量足以治疗和/或预防所述对象的lvh。
当与本文提供的剂量(例如,actrii信号转导抑制剂的剂量或第二活性试剂的剂量)一起使用时,词语“约”是指参考数量的1%、5%或10%以内的任何数量。
在某些实施方式中,本文描述的actrii信号转导抑制剂根据本文提供的方法皮下地或静脉内地施用给对象。
在某些实施方式中,0.13mg/kg的actriia-hfc(seqidno:7)以每14天一次的间隔皮下地施用给根据所提供的方法治疗的对象。在某些实施方式中,0.26mg/kg的actriia-hfc(seqidno:7)以每14天一次的间隔皮下地施用给根据所提供的方法治疗的对象。在某些实施方式中,0.1mg/kg的actriia-hfc(seqidno:7)以每14天一次的间隔静脉内地施用给根据所提供的方法治疗的对象。在某些实施方式中,0.2mg/kg的actriia-hfc(seqidno:7)以每14天一次的间隔静脉内地施用给根据所提供的方法治疗的对象。在某些实施方式中,0.3mg/kg的actriia-hfc(seqidno:7)以每28天一次的间隔皮下地施用给根据所提供的方法治疗的对象。在某些实施方式中,0.5mg/kg的actriia-hfc(seqidno:7)以每28天一次的间隔皮下地施用给根据所提供的方法治疗的对象。在某些实施方式中,0.7mg/kg的actriia-hfc(seqidno:7)以每28天一次的间隔皮下地施用给根据所提供的方法治疗的对象。
8.8组合治疗
在某些实施方式中,本文提供的方法与第二药学活性试剂组合地进行。这样的组合治疗可以通过治疗的单独成分的同时、连续或独立给药的方式来实现。此外,当作为这种组合治疗的成分施用时,actrii信号转导抑制剂与第二药学活性试剂可以是协同的,从而与通常作为单一治疗给予的每种成分的剂量相比,两种成分的任一种或两种的日剂量可以被降低。做为选择,当作为这种组合治疗的成分施用时,本文提供的actrii信号转导抑制剂与第二药学活性试剂可以是加成的,从而与通常作为单一治疗给予的每种成分的剂量相比,每种成分的日剂量是相似的或相同的。
在某些实施方式中,本文提供的actrii信号转导抑制剂与第二药学活性试剂在同一天施用。在某些实施方式中,actrii信号转导抑制剂在第二药学活性试剂之前一天、两天、三天或更多天施用。在某些实施方式中,actrii信号转导抑制剂在第二药学活性试剂之后一天、两天、三天或更多天施用。在某些实施方式中,actrii信号转导抑制剂在第二药学活性试剂一周、两周、三周或更多周之内施用。
在某些实施方式中所述第二药学活性试剂是snai1、phosphosmad2、phosphosmad3、尿蛋白、dkk1、col1a1、激活素(例如,游离激活素)、runx2、alp、bsap、ctx和/或osterix的拮抗剂,例如抗体或其片段、小分子信号转导抑制剂、反义核酸、小干扰核酸、显性阴性蛋白或其片段。在某些实施方式中,所述第二药学活性试剂是klotho、alpha-sma、myocd、axin2和/或sm22-alpha的激动剂,例如,抗体或其片段或小分子
在某些实施方式中,所述第二药学活性试剂是用于治疗心血管疾病、血管钙化、与血管钙化相关和/或由血管钙化引起的心血管疾病和/或与肾病相关和/或由肾病引起的心血管疾病的活性试剂,例如,醛固酮信号转导抑制剂、血管紧张素ii受体阻断剂、beta-阻断剂、钙离子通道阻断剂、降胆固醇药物、地高辛、利尿剂、变力性治疗、钾或镁、血管扩张剂和/或华法林。
在某些实施方式中,所述第二药学活性试剂是用于治疗慢性肾病的活性试剂,例如,血管紧张素ii受体阻断剂、beta-阻断剂、钙离子通道阻断剂、直接肾素信号传导抑制剂、利尿剂、血管舒张剂、促红细胞生成素治疗、铁替代治疗和/或维生素d.
在某些实施方式中,与治疗或改善心血管疾病、血管钙化、与血管钙化相关和/或由血管钙化引起的心血管疾病和/或与肾病相关和/或由肾病引起的心血管疾病、和/或慢性肾病的方法组合地进行本文提供的方法。
8.9药物组合物
在某些实施方式中,激活素-actrii拮抗剂(例如,actrii多肽)与药学上可接受的载体一起配制用于本文描述的方法。例如,actrii多肽可以单独施用或作为药物制剂的成分(治疗组合物)施用。目标化合物可以被配制以用于人类或兽医学的任何方便方式施用。actrii可以是actriia或actriib。
在某些实施方式中,本文提供的治疗方法包括系统地或作为植入物或设备局部地施用所述组合物(包含actrii信号转导抑制剂)。当施用时,用于本文提供的用途的治疗组合物是无热原的、生理学可接受的形式。还可以任选地被包括在如上所述的组合物中的actrii拮抗剂之外的治疗有用试剂,可以与目标化合物(例如,actrii多肽,例如,actriia和/或actriib多肽(参见,章节8.5))同时地或次序地施用。
一般地,actrii拮抗剂将胃肠外施用。适合于胃肠外施用的药物组合物可以包含一种或更多种actrii多肽,与一种或更多种药学上可接受的无菌的等渗水性或非水性溶液、分散体、悬浮液或乳剂或无菌粉末组合,所述无菌粉末在即将使用之前可重构为无菌可注射溶液或分散体,其可以含有抗氧化剂、缓冲剂、抑菌剂、使得制剂与预期的接受者的血液等渗的溶质,或悬浮剂或增稠剂。在用于本文描述的方法中的药物组合物中采用的适合的水性和非水性载体的实例包括,水、乙醇、多元醇(例如,甘油、丙二醇、聚乙二醇,等等)、以及其适合的混合物,植物油,例如橄榄油,和可注射的有机酯,例如油酸乙酯。例如,通过使用包被材料例如卵磷脂、在分散体的情况下通过维持所需的粒子大小、以及通过使用表面活性剂,可以维持适当的流动性。
进一步的,所述组合物可以以用于递送到目标组织位点(例如,骨)的形式被胶囊化或注射。在某些实施方式中,本文描述的方法中使用的组合物可以包括基质,其能将一种或更多种治疗化合物(例如,actriia多肽)递送到目标组织位点(例如,骨),提供一种结构用于显现组织以及最佳地能够被再吸收入身体。例如,所述基质可以提供actriia多肽的缓慢释放。这样的基质可以由当前用于其他植入医学应用的材料形成。
基质材料的选择基于生物相容性、生物降解能力、机械性质、美容的外观和接触面性质。目标组合物的特殊的应用将限定适当的制剂。组合物的可能的基质可以是生物可降解的和化学上定义的硫酸钙、磷酸三钙、羟基磷灰石、聚乳酸和聚酐。其他可能的材料是生物可降解的和生物学上明确定义的,例如骨或真皮胶原蛋白。进一步的基质包含纯的蛋白质或细胞外基质成分。其他可能的基质是非生物可降解的和化学上定义的,例如,烧结的羟磷灰石、生物玻璃、铝酸盐或其他陶瓷。基质可以包含任何上述材料类型的组合,例如聚乳酸和羟磷灰石,或胶原蛋白和磷酸三钙。生物陶瓷可以在组成上改变,例如在钙-铝酸盐-磷酸盐中,并被加工来改变孔径大小、颗粒大小、颗粒形状和生物降解能力。
在某些实施方式中,用于本文描述的方法的组合物(包含actrii信号转导抑制剂)可以口服施用,例如以胶囊、扁胶囊、丸剂、片剂、锭剂(使用调味的基底,通常是蔗糖和阿拉伯胶或黄芪胶)、粉末、颗粒或作为水性或非水性液体中的溶液或悬浮液,或作为水包油或油包水液体乳剂或作为酏剂或糖浆或作为软锭剂(使用惰性基底,例如明胶和甘油,或蔗糖和阿拉伯胶)和/或作为漱口剂等的形式,各自含有预定数量的试剂作为活性成分。试剂也可以作为弹丸、舔剂或糊剂来施用。
在用于口服施用的固体剂型中(胶囊、片剂、药丸、糖衣丸、粉未、颗粒,等),本文描述的一种或更多种治疗化合物可以与一种或多种药学上可接受的载体,例如柠檬酸钠或磷酸二钙和/或任何以下的混合:(1)填料或膨胀剂,例如淀粉、乳糖、蔗糖、葡萄糖、甘露醇和/或硅酸;(3)粘合剂,例如羧甲基纤维素、藻酸盐、明胶、聚乙烯基吡咯烷酮、蔗糖和/或阿拉伯树胶;(3)湿润剂,例如甘油;(4)崩解剂,例如,琼脂、碳酸钙、马铃薯或木薯淀粉、海藻酸、某些硅酸盐和碳酸钠;(5)溶液阻滞剂,例如,石蜡;(6)吸收加速剂,例如,季铵化合物;(7)润湿剂,例如,十六醇和单硬脂酸甘油酯;(8)吸附剂,例如,高岭土和班脱土;(9)润滑剂,例如,滑石粉、硬脂酸钙、硬脂酸镁、固体聚乙二醇、十二烷基硫酸钠和其混合物;和(在胶囊、片剂和丸剂的情况中,药物组合物还可以包含缓冲剂。类似类型的固体组合物也可以用作软和硬填充胶囊中的填料,使用这样的赋形剂如乳糖或奶糖,以及高分子量聚乙二醇等等。
用于口服施用的液体剂型包括药学上可接受的乳剂、微乳剂、溶液、悬浮液、糖浆和酏剂。除了活性成分之外,液体剂型可以含有本领域常用的惰性稀释剂,例如,水或其他溶剂、增溶剂以及乳化剂,例如乙醇、异丙醇、碳酸乙酯、乙酸乙酯、苯甲醇、苯甲酸苄酯、丙二醇、1,3-丁二醇、油(特别是,棉籽、花生、玉米、胚芽、橄榄、蓖麻以及芝麻油)、甘油、四氢呋喃醇类、聚乙二醇以及山梨聚醇的脂肪酸酯,和其混合物。除了惰性稀释剂之外,口腔组合物还可以包括佐剂例如润湿剂、乳化和悬浮剂、甜味剂、调味剂、着色剂、芳香剂和防腐剂。
除了活性化合物之外,悬浮液可以含有悬浮剂,例如,乙氧基异十八烷醇、聚氧乙烯山梨醇和山梨聚糖酯,微晶纤维素、偏氢氧化铝、斑脱土、琼脂和黄芪胶,以及其混合物。
本文描述的组合物还可以含有佐剂,例如,防腐剂、润湿剂、乳化剂和分散剂。可以通过包含各种抗菌和抗真菌剂,例如,对羟苯甲酸、氯代丁醇、苯酚、山梨酸,等,来实现对微生物作用的保护。还可能希望的是在组合物中包括等渗试剂,例如糖类、氯化钠等。此外,通过包含延迟吸收的试剂,例如,单硬脂酸铝和明胶,可以得到可注射药物形式的延长吸收。
要理解的是,给药方案将由主治医师考虑修饰本文描述的化合物(例如,actrii多肽,例如,actriia和/或actriib多肽)的作用的各种因素来决定。所述各种因素包括但不限于,希望形成的骨重量的数量,骨密度损失程度,骨损伤部位,骨损伤状况,对象的年龄、性别和饮食,可能导致骨损失的任何疾病的严重度,施用的时间和其他临床因素。任选地,所述剂量可以随重构中使用的基质的类型以及组合物中化合物的类型而变化。其他已知的生长因子向最终组合物中的添加也可能影响剂量。进展可以通过周期性评估骨生长和/或修复来监视,例如,x-射线(包括dexa)、组织形态学测定和四环素标记。
在某些实施方式中,本文提供的是用于actrii多肽的体内生产的基因治疗。通过将actrii多核苷酸序列导入具有上文列出的失调的细胞或组织,这样的疗法将实现其治疗效果。递送actrii多核苷酸序列可以利用重组表达载体,例如嵌合病毒或胶态分散体系统来实现。优选的,用于actrii多核苷酸序列的治疗递送的是使用靶向的脂质体。actrii多肽可以是actriia和/或actriib多肽(参见,章节8.5))。
在此教导的可以用于基因治疗的各种病毒载体包括腺病毒、疱疹病毒、牛痘,或优选地,rna病毒,例如逆转录病毒。优选地,逆转录病毒载体是鼠或禽类逆转录病毒的衍生物。其中可以插入单个外源基因的逆转录病毒载体的实例包括,但不限于,moloney鼠白血病毒(momulv)、harvey鼠肉瘤病毒(hamusv)、鼠类乳腺肿瘤病毒(mumtv)和劳氏肉瘤病毒(rsv)。许多其他逆转录病毒载体可以掺入多个基因。所有这些载体可以传递或掺入可选择标记物的基因,从而可以鉴定和产生转导的细胞。通过附着例如糖类、糖脂或蛋白质,逆转录病毒载体可以变为目标特异性的。优选的靶向是通过使用抗体实现的。技术人员将认识到,特异性多核苷酸序列可以插入逆转录病毒基因组中或附着于病毒包膜,以容许含有actrii多核苷酸的逆转录病毒载体的目标特异性递送。在优选的实施方式中,所述载体被靶向骨或软骨。
做为选择,通过常规的磷酸钙转染,组织培养细胞可以直接用编码逆转录病毒结构基因gag、pol和env的质粒转染。这些细胞然后用含有感兴趣基因的载体质粒转染。产生的细胞将逆转录病毒载体释放到培养基中。
actrii多核苷酸的另一种靶向递送系统是胶态分散体系统。胶态分散体系统包括大分子复合物、纳囊、微球体、珠子和基于脂质的系统,包括水包油乳剂、胶粒团、混合的胶粒团和脂质体。用于本文描述的方法的优选的胶态系统是脂质体。脂质体是人工的膜囊,其作为体外和体内的递送运载体是有用的。rna、dna和完整的病毒粒可以密封在水性的内部,并以生物学活性形式递送给细胞(参见,例如,fraley,etal.,trendsbiochem.sci.,6:77,1981)。利用脂质体载体的高效的基因转移方法是本领域已知的,参见,例如,mannino,etal.,biotechniques,6:682,1988。脂质体的组成通常是磷脂类的组合,通常与类固醇,特别是胆固醇组合。也可以使用其他磷脂或其他脂质。脂质体的物理性质取决于ph值、离子强度和二价阳离子的存在。
在脂质体生产中有用的脂质包括磷脂酰基化合物,例如,磷脂酰甘油、磷脂酰胆碱、磷脂酰丝氨酸、磷脂酰乙醇胺、鞘脂类、脑苷脂类和神经节苷脂类。说明性的磷脂包括卵磷脂酰胆碱、二棕榈酰磷脂酰胆碱和二硬脂酰磷脂酰胆碱。基于例如器官特异性、细胞特异性和细胞器特异性,脂质体的靶向也是可能的,是本领域已知的。
在某些实施方式中,actrii信号转导抑制剂在药物组合物中是基本上纯的。具体地,所述药物组合物中的最多20%、10%、5%、2.5%、1%、0.1%或最多0.05%的化合物是除了actrii信号转导抑制剂和药学上可接受的载体之外的化合物。
8.10试剂盒
本文提供的是包含一个或更多个容器的试剂盒,所述容器填充了一种或更多种试剂,来测定获自本文描述的对象的样品中本文描述的一种或更多种生物标记物(例如runx2、alp、snai1、phosphosmad2、dkk1、col1a1、激活素、bsap、ctx、osterix、klotho、alpha-sma、myocd、sm22-alpha、phosphosmad3、actriia、axin2和尿蛋白)的水平。在某些实施方式中,所述试剂盒包含一种或更多种试剂,来测定获自本文描述的对象的样品中本文描述的一种生物标记物(例如runx2、alp、snai1、phosphosmad2、dkk1、col1a1、激活素、bsap、ctx、osterix、klotho、alpha-sma、myocd、sm22-alpha、phosphosmad3、actriia、axin2和尿蛋白)的水平。在某些实施方式中,所述试剂盒包含一种或更多种试剂,来测定获自本文描述的对象的样品中runx2的水平。在某些实施方式中,所述试剂盒包含一种或更多种试剂,来测定获自本文描述的对象的样品中alp的水平。在某些实施方式中,所述试剂盒包含一种或更多种试剂,来测定获自本文描述的对象的样品中snai1的水平。在某些实施方式中,所述试剂盒包含一种或更多种试剂,来测定获自本文描述的对象的样品中phosphosmad2的水平。在某些实施方式中,所述试剂盒包含一种或更多种试剂,来测定获自本文描述的对象的样品中dkk1的水平。在某些实施方式中,所述试剂盒包含一种或更多种试剂,来测定获自本文描述的对象的样品中col1a1的水平。在某些实施方式中,所述试剂盒包含一种或更多种试剂,来测定获自本文描述的对象的样品中激活素的水平。在某些实施方式中,所述试剂盒包含一种或更多种试剂,来测定获自本文描述的对象的样品中bsap的水平。在某些实施方式中,所述试剂盒包含一种或更多种试剂,来测定获自本文描述的对象的样品中ctx的水平。在某些实施方式中,所述试剂盒包含一种或更多种试剂,来测定获自本文描述的对象的样品中osterix的水平。在某些实施方式中,所述试剂盒包含一种或更多种试剂,来测定获自本文描述的对象的样品中klotho的水平。在某些实施方式中,所述试剂盒包含一种或更多种试剂,来测定获自本文描述的对象的样品中alpha-sma的水平。在某些实施方式中,所述试剂盒包含一种或更多种试剂,来测定获自本文描述的对象的样品中myocd的水平。在某些实施方式中,所述试剂盒包含一种或更多种试剂,来测定获自本文描述的对象的样品中sm22-alpha的水平。在某些实施方式中,所述试剂盒包含一种或更多种试剂,来测定获自本文描述的对象的样品中phosphosmad3的水平。在某些实施方式中,所述试剂盒包含一种或更多种试剂,来测定获自本文描述的对象的样品中尿蛋白的水平。在某些实施方式中,所述试剂盒包含一种或更多种试剂,来测定获自本文描述的对象的样品中actriia的水平。在某些实施方式中,所述试剂盒包含一种或更多种试剂,来测定获自本文描述的对象的样品中axin2的水平。
在某些实施方式中,所述试剂盒包含一种或更多种试剂,来测定获自本文描述的对象的样品中本文描述的两种生物标记物(例如选自以下构成的组的两种生物标记物:runx2、alp、snai1、phosphosmad2、dkk1、col1a1、激活素、bsap、ctx、osterix、klotho、alpha-sma、myocd、sm22-alpha、phosphosmad3、actriia、axin2和尿蛋白)的水平。在某些实施方式中,所述试剂盒包含一种或更多种试剂,来测定获自本文描述的对象的样品中本文描述的三种生物标记物(例如选自以下构成的组的三种生物标记物:runx2、alp、snai1、phosphosmad2、dkk1、col1a1、激活素、bsap、ctx、osterix、klotho、alpha-sma、myocd、sm22-alpha、phosphosmad3、actriia、axin2和尿蛋白)的水平。在某些实施方式中,所述试剂盒包含一种或更多种试剂,来测定获自本文描述的对象的样品中本文描述的四种生物标记物(例如选自以下构成的组的四种生物标记物:runx2、alp、snai1、phosphosmad2、dkk1、col1a1、激活素、bsap、ctx、osterix、klotho、alpha-sma、myocd、sm22-alpha、phosphosmad四、actriia、axin2和尿蛋白)的水平。在某些实施方式中,所述试剂盒包含一种或更多种试剂,来测定获自本文描述的对象的样品中本文描述的五种生物标记物(例如选自以下构成的组的五种生物标记物:runx2、alp、snai1、phosphosmad2、dkk1、col1a1、激活素、bsap、ctx、osterix、klotho、alpha-sma、myocd、sm22-alpha、phosphosmad五个、actriia、axin2和尿蛋白)的水平。在某些实施方式中,所述试剂盒包含一种或更多种试剂,来测定获自本文描述的对象的样品中本文描述的六种生物标记物(例如选自以下构成的组的六种生物标记物:runx2、alp、snai1、phosphosmad2、dkk1、col1a1、激活素、bsap、ctx、osterix、klotho、alpha-sma、myocd、sm22-alpha、phosphosmad六、actriia、axin2和尿蛋白)的水平。在某些实施方式中,所述试剂盒包含一种或更多种试剂,来测定获自本文描述的对象的样品中本文描述的七种生物标记物(例如选自以下构成的组的七种生物标记物:runx2、alp、snai1、phosphosmad2、dkk1、col1a1、激活素、bsap、ctx、osterix、klotho、alpha-sma、myocd、sm22-alpha、phosphosmad七、actriia、axin2和尿蛋白)的水平。在某些实施方式中,所述试剂盒包含一种或更多种试剂,来测定获自本文描述的对象的样品中本文描述的八种生物标记物(例如选自以下构成的组的八种生物标记物:runx2、alp、snai1、phosphosmad2、dkk1、col1a1、激活素、bsap、ctx、osterix、klotho、alpha-sma、myocd、sm22-alpha、phosphosmad八、actriia、axin2和尿蛋白)的水平。在某些实施方式中,所述试剂盒包含一种或更多种试剂,来测定获自本文描述的对象的样品中本文描述的九种生物标记物(例如选自以下构成的组的九种生物标记物:runx2、alp、snai1、phosphosmad2、dkk1、col1a1、激活素、bsap、ctx、osterix、klotho、alpha-sma、myocd、sm22-alpha、phosphosmad九、actriia、axin2和尿蛋白)的水平。在某些实施方式中,所述试剂盒包含一种或更多种试剂,来测定获自本文描述的对象的样品中本文描述的十种生物标记物(例如选自以下构成的组的十种生物标记物:runx2、alp、snai1、phosphosmad2、dkk1、col1a1、激活素、bsap、ctx、osterix、klotho、alpha-sma、myocd、sm22-alpha、phosphosmad十、actriia、axin2和尿蛋白)的水平。在某些实施方式中,所述试剂盒包含一种或更多种试剂,来测定获自本文描述的对象的样品中本文描述的十一种生物标记物(例如选自以下构成的组的十一种生物标记物:runx2、alp、snai1、phosphosmad2、dkk1、col1a1、激活素、bsap、ctx、osterix、klotho、alpha-sma、myocd、sm22-alpha、phosphosmad十、actriia、axin2和尿蛋白)的水平。在某些实施方式中,所述试剂盒包含一种或更多种试剂,来测定获自本文描述的对象的样品中本文描述的十二种生物标记物(例如选自以下构成的组的十二种生物标记物:runx2、alp、snai1、phosphosmad2、dkk1、col1a1、激活素、bsap、ctx、osterix、klotho、alpha-sma、myocd、sm22-alpha、phosphosmad十、actriia、axin2和尿蛋白)的水平。在某些实施方式中,所述试剂盒包含一种或更多种试剂,来测定获自本文描述的对象的样品中本文描述的十三种生物标记物(例如选自以下构成的组的十三种生物标记物:runx2、alp、snai1、phosphosmad2、dkk1、col1a1、激活素、bsap、ctx、osterix、klotho、alpha-sma、myocd、sm22-alpha、phosphosmad十、actriia、axin2和尿蛋白)的水平。在某些实施方式中,所述试剂盒包含一种或更多种试剂,来测定获自本文描述的对象的样品中本文描述的十四种生物标记物(例如选自以下构成的组的十四种生物标记物:runx2、alp、snai1、phosphosmad2、dkk1、col1a1、激活素、bsap、ctx、osterix、klotho、alpha-sma、myocd、sm22-alpha、phosphosmad十、actriia、axin2和尿蛋白)的水平。在某些实施方式中,所述试剂盒包含一种或更多种试剂,来测定获自本文描述的对象的样品中本文描述的十五种生物标记物(例如选自以下构成的组的十五种生物标记物:runx2、alp、snai1、phosphosmad2、dkk1、col1a1、激活素、bsap、ctx、osterix、klotho、alpha-sma、myocd、sm22-alpha、phosphosmad十、actriia、axin2和尿蛋白)的水平。在某些实施方式中,所述试剂盒包含一种或更多种试剂,来测定获自本文描述的对象的样品中本文描述的十六种生物标记物(例如选自以下构成的组的十六种生物标记物:runx2、alp、snai1、phosphosmad2、dkk1、col1a1、激活素、bsap、ctx、osterix、klotho、alpha-sma、myocd、sm22-alpha、phosphosmad十、actriia、axin2和尿蛋白)的水平。在某些实施方式中,所述试剂盒包含一种或更多种试剂,来测定获自本文描述的对象的样品中本文描述的十七种生物标记物(例如选自以下构成的组的十七种生物标记物:runx2、alp、snai1、phosphosmad2、dkk1、col1a1、激活素、bsap、ctx、osterix、klotho、alpha-sma、myocd、sm22-alpha、phosphosmad十、actriia、axin2和尿蛋白)的水平。在某些实施方式中,所述试剂盒包含一种或更多种试剂,来测定获自本文描述的对象的样品中本文描述的十八种生物标记物(例如选自以下构成的组的十八种生物标记物:runx2、alp、snai1、phosphosmad2、dkk1、col1a1、激活素、bsap、ctx、osterix、klotho、alpha-sma、myocd、sm22-alpha、phosphosmad十、actriia、axin2和尿蛋白)的水平。在某些实施方式中,所述测定生物标记物的水平的一种或更多种试剂是如章节8.6.1中描述的。在某些实施方式中,所述试剂盒进一步包含actriia-hfc(seqidno:7)。在某些实施方式中,所述试剂盒进一步包含第二容器,其包含actriia-hfc(seqidno:7)。
9.实施例
在此呈现的实施例表明,在某些形式的慢性肾病中runx2、alp、bsap、ctx和osterixmrna水平升高,klotho、alpha-sma、myocd、actriia、axin2和sm22-alphamrna水平可降低。这些实施例进一步表明,用激活素配体陷阱治疗降低了runx2、alp、ctx、actriia和/或osterixmrna水平,提高了klotho、alpha-sma、myocd、axin2和/或sm22-alphamrna水平,这与血管钙化的降低相关。因而,本文提供的实施例表明runx2、alp、ctx、osterix、klotho、alpha-sma、myocd、actriia、axin2和/或sm22-alpha可以用作生物标记物,用于治疗心血管疾病、血管钙化、与血管钙化相关和/或由血管钙化引起的心血管疾病、与肾病相关和/或由肾病引起的心血管疾病、动脉硬化水平升高、与动脉硬化水平升高相关和/或由动脉硬化水平升高引起的心血管疾病、lvh和/或与lvh相关和/或由lvh引起的心血管疾病。
9.1实施例1.用激活素受体2a型的配体陷阱治疗ckd-mbd
ckd-mbd可以包括血管钙化,一种骨营养不良,以及在它发端时对骨骼的骨细胞fgf23分泌的刺激,以及高磷酸血症,其在进程的晚期发生进一步刺激血管钙化。这个实施例表明,抑制actriia信号转导,一种由ckd诱导的、通过激活素iia型受体(actriia)的tgfβ超家族信号转导的成员,抑制了血管钙化并预防心脏肥大。
9.1.1方法
带有高磷酸血症和gfr60%降低的ckd(ckd-3)在2型糖尿病ldlr-/-小鼠、血管钙化高脂肪饲喂模型中在14周龄诱导。一些ckd小鼠用激活素2a型受体(mactriia)配体陷阱mactriia-fc治疗,在22周龄开始每周ip注射,在28周时研究。测量了主动脉的ca2+水平、成骨细胞的和血管平滑肌蛋白质的表达、骨骼组织形态和microct成像、血清化学以及fgf23和pth水平。激活素、卵泡抑素和抑制素水平通过elisa、rt-pcr和western印迹测量。
9.1.2结果
循环激活素水平在两种不同的肾脏疾病模型中提高:间质性纤维化和x-连锁aiports(附图1a和附图1b)。此外,激活素amrna水平在ckd模型的主动脉和肾脏中提高(附图2)。激活素水平在血管系统和循环中提高,而没有卵泡抑素的改变(附图2a、附图2b和附图2c)。通过用激活素2a型受体(mactriia)配体陷阱(mactriia-fc;参见,例如美国专利8,173,601,其公开内容通过完全引用合并在本文中)治疗,ckd刺激的血管钙化降低到低于22周的水平(附图3a、附图3b、附图3c、附图3d、附图5a和附图5b),预防了心脏肥大。ckd诱导了主动脉的runx2、osterix和alp信息和蛋白质的表达,这些被激活素2a型受体(mactriia)配体陷阱mactriia-fc反转(对于runx2和alpmrna,分别是附图4a和附图4b;对于runx2蛋白,附图4f)。ckd降低了klotho和sm22-alpha信息和蛋白质,用激活素2a型受体(mactriia)配体陷阱mactriia-fc治疗归一化了klotho和sm22-alpha表达(对klotho和sm22-alphamrna分别是附图4c和附图4e;附图4f为蛋白质)。此外,ckd降低了myocd信息(附图4d)。此外,ckd降低了alpha-平滑肌肌动蛋白(肌动蛋白alpha-平滑肌)蛋白质(附图4f)。进一步的,ckd刺激了钙水平的提高,其被mactriia-fc治疗降低(附图6a)。激活素2a型受体(mactriia)配体陷阱mactriia-fc治疗提高了骨体积,破骨细胞凹陷表面降低,但是骨形成率和成骨细胞表面不受影响(附图6b、附图6c和附图6d)。激活素2a型受体(mactriia)配体陷阱mactriia-fc治疗没有改变高磷酸血症和fgf23水平。
用激活素2a型受体(mactriia)配体陷阱mactriia-fc治疗抑制了骨吸收并提高了骨体积。用激活素2a型受体(mactriia)配体陷阱mactriia-fc治疗抑制了smad依赖性信号转导,阻断了主动脉的成骨细胞的转变,提高了血管平滑肌蛋白质水平,并降低了ckd刺激的血管钙化和心脏肥大。
9.2实施例2.慢性肾病(ckd)刺激主动脉的内皮向间充质转变(enmt),其引起血管钙化并被激活素配体陷阱抑制
在慢性肾病中血管钙化的基础分子机制是不完全了解的。然而,激活素水平在ckd刺激的血管钙化中提高。为了评估激活素在ckd刺激的血管钙化中的作用,结合许多tgf-beta超家族配体的重组融合蛋白被用于动脉粥样硬化和2型糖尿病的模型中的慢性肾病的小鼠模型中。actriia-fc融合蛋白由同免疫球蛋白1(igg1)fc结构域连接的激活素受体iia(actriia)的细胞外结构域组成,该蛋白质作为tgf-beta超家族成员如激活素a、激活素b、生长分化因子-11(gdf11)和骨骼形态发生蛋白-10(bmp-10)的配体陷阱起作用。
早先已经显示了,通过在肾脏修复期间产生全身性wnt抑制,肾脏疾病引起血管钙化。这个实施例表明,ckd刺激的wnt抑制的血管作用是刺激血管的激活素,以及诱导smad依赖性enmt,激活素受体配体陷阱抑制了enmt和血管钙化。
9.2.1方法
具有升高的wnt抑制剂的ckd在谱系跟踪和血管钙化的小鼠模型中诱导。激活素、卵泡抑素和抑制素水平通过elisa、rt-pcr和western印迹测量。在繁育成内皮特异性tie2-cre小鼠的gnz小鼠(stolleretal,genesis,2008)中进行细胞谱系跟踪。带有gnz敲入的小鼠在cre介导的重组之后表达核gfp和lacz。
9.2.2结果
在肾脏疾病和ckd刺激的血管钙化的小鼠模型中,激活素水平在血管系统和循环中提高,而没有卵泡抑素水平的改变。在gnz的外膜和中层的细胞中ckd诱导gfp和lacz的表达;tie2-creckd小鼠与gnz相比较;tie2-cre小鼠具有正常的肾脏功能,其中gfp和lacz限于主动脉的内皮。tie2是内皮的谱系特异性受体,这表明ckd诱导主动脉的enmt(附图7a、附图7b、附图7c和附图7d)。ckd刺激的主动脉enmt产生了降低的血管平滑肌功能,成骨细胞转变和钙化。用激活素2a型受体(mactriia)配体陷阱(mactriia-fc;参见,例如,美国专利no.8,173,601,其公开内容通过引用全部合并在本文中)治疗抑制了smad依赖性信号转导,阻断了主动脉的成骨细胞转变,提高了血管平滑肌功能,并降低了ckd刺激的血管钙化。因而,ckd诱导血管激活素和enmt,用激活素2a型受体(mactriia)配体陷阱治疗降低了激活素信号转导抑制的血管去分化,成骨细胞转变和血管钙化。
9.3实施例3.以逐步提高的剂量治疗的血液透析对象中骨质量和血管钙化的初步信号搜寻定量计算机断层扫描结果
高周转的肾性骨营养不良(rod)的标志是提高的皮层孔隙度、更高的小梁骨质量和提高的骨折风险,一种在矫正血液透析(hd)对象的贫血中研究的激活素ariia-igg1融合蛋白配体陷阱actriia-fc阻断了激活素a信号转导,可以降低破骨细胞发生并促进骨中的成骨细胞成熟。利用定量的计算机断层照相(qct),在hd对象中的当前的分析评估了actriia-fc对骨矿物密度(bmd)和血管钙化的影响。
9.3.1方法
用actriia信号转导抑制剂治疗的、促红细胞生成素刺激剂(esa)响应性的血液透析对象被洗出esa作用直到血红蛋白(hb)<10g/dl,然后随机化为用以下剂量的actriia信号转导抑制剂治疗:0.3mg/kg(n=9)、0.5mg/kg(n=8)、0.7mg/kg(n=6)或安慰剂(pbo;n=7)每28天皮下地,直到8个剂量周期。评估对象的hb、骨矿物密度(bmd)和骨周转的生物标记物的影响。治疗失败(hb<9g/dl)用esa和/或红血细胞输血来挽救。在基线和225天的治疗期之后获得髋部和腰脊椎的定量计算机断层扫描(qct)。在基线和剂量周期3、5和7之后测量生物标记物bsap和ctx。
在基线和225天的治疗期之后获得髋部、腰脊椎和腹主动脉的qct。对象仰卧在mindways校准模型上(model3;mindwayssoftware,inc.,austin,tx)。使用标准软组织核重建2.5mm和512×512矩阵的切片厚度。mindways分析软件(版本5.0.3)用于评估体积的bmd(vbmd)。小梁的vbmd(mg/cm3)对l1-4内的2节脊椎测定(一般l1-2)。分析左侧股骨近端股骨头皮层,骨小梁和整个髋部的整合骨区室、股骨颈和髀枢的vbmd。
使用软件来评估腹主动脉的血管钙化,所述软件半自动地分段邻近于l1顶部到l4底部的区域内钙化的面积和体积。在每个对象的就诊之间保持了切片的数量和位置。如agatstonetal.,jamcollcardiol.1990;15:827-832andhokansonetal.,ajramjroentgenol.2004;182:1327-1332中描述的测定agatston和平方根转化的体积得分。更低的总agatston和平方根转化的总体积得分(mm3)表明更低水平的血管钙化(vc)。
通过parexel成像(parexelinternationalcorp.waltham,ma)中央地进行所有的图像质量控制和盲分析。
在基线和剂量周期1、3、5和7之后测量生物标记物,包括骨特异性碱性磷酸酶(bsap)、前胶原蛋白1型n-末端原肽(p1np)和c-末端1型胶原蛋白端肽(ctx)。
9.3.2结果
总共31名对象随机化,接受超过1个剂量的研究药物。
表2.随机化的对象和qct分析子集合
对象分布如附图8中描述,包括在基线和225天有成对的qct测量的对象。
大多数对象在治疗失败需要挽救(一般由于hb<9g/dl)之后停止研究治疗;没有对象因为有害事件(ae)停止治疗。
具有成对的qct测量的16名对象中,9人在治疗期内需要挽救疗法,9人在前3个剂量周期内需要挽救。
在具有成对的qct测量的对象中,基线的人口统计学和临床特征一般在处理组之间是相似的(表3);然而,在安慰剂组中有实质上更长的透析时间,这也是最年轻的组。在基线生物标记物和agatston得分方面各组之间也存在差异(表4)。
表3.具有成对的qct测量的对象的基线人口统计学和临床特征
表4.具有成对的qct测量的对象的平均基线生物标记物、面积bmd和agatston得分
pth=甲状旁腺激素。
*更低的agatston得分表明更低水平的血管钙化。
表5提供了髋部整体、股骨颈皮层、髋部皮层和腰椎骨面积bmd测量中距基线改变百分比。
表5.髋部整体、股骨颈皮层、髋部皮层和腰椎骨面积bmd中的基线和距基线改变百分比
皮层骨的2%提高可能降低骨折风险。在具有股骨颈部皮层骨的大于或等于2%提高的部分对象中,actriia信号转导抑制剂治疗与剂量依赖性提高相关(表5和附图9a)。
在高周转rod中,相比一般群体,小梁骨质量提高(即,不良质量的骨),通过腰脊椎bmd来测量,在eskd中在椎骨骨折率上没有降低。用actriia治疗预防了腰脊椎中小梁骨质量的提高(表5和附图9b)。
腹主动脉总计agatston得分的距基线改变在表6中提供。在总计agatston得分和平方根转化的总体积得分方面改变的类别显示在附图9和表7中。
表6.腹主动脉总计agatston得分和平方根转化的总体积得分方面的基线和距基线改变。
*更低的总计agatston和平方根转化的总体积得分表明更低水平的血管钙化。
十一位对象具有在10到10,000之间分布的基线agatston得分。五名对象可以被认为是基线处的逸出值(低逸出值:0.0、1.1和1.4agatston得分;高逸出值:21,033和44,356agatston得分)。因此,分析没有逸出值的agatston得分(表7和附图10)。
表7.排除5个逸出值在总计agatston得分方面的基线和改变
*更低的总计agatston和平方根转化的总体积得分表明更低水平的血管钙化。
通过对actriia信号转导抑制剂的暴露持续时间分析对象。通过暴露状态分析对象:接受达到3个剂量的actriia-fc对象,不考虑剂量水平(n=6),接受>3个剂量的actriia-fc接受者,不考虑剂量水平(n=7)。安慰剂基团(n=3)不变。除了性别和agatston得分之外,在接受≤3个剂量的actriia-fc的对象与接受>3个剂量的对象之间,关键的基线特征一般是相似的,在所有actriia-fc对象中对vc的暴露影响保持完整,排除了逸出值时也是一样(表10)。
表8.对象的基线人口统计学和临床特征,根据actriia-fc暴露
表9.根据actriia-fc暴露,在总计agatston得分和平方根转化的总体积得分方面的基线和距基线改变*
*更低的总计agatston得分和平方根转化的总体积得分表明更低水平的血管钙化。
表10.根据actriia-fc暴露,在总计agatston得分方面的基线和距基线改变,排除5个逸出值*
*更低的总计agatston得分和平方根转化的总体积得分表明更低水平的血管钙化。
评估了骨周转生物标记物。安慰剂组具有最高的基线处的pth、bsap、p1np和ctx水平(表4)。在磷、pth、fgf-23或硬骨素水平方面没有观察到一致的距基线改变,只是在安慰剂组中pth在所有时间点都低于基线(-15.2到-100.7ng/l)。对于骨生物标记物,在形成标志物bsap和bsapp1np方面没有见到百分比改变中的清楚变化,在再吸收标志物ctx中的百分比改变在附图11中示出。
接受0.5mg/kgactriia信号转导抑制剂的更多对象在再吸收标志物ctx方面存在有意义、持续的降低。
9.3.3结论
对于30名随机化的对象,13人具有成对的qct评估(对于pbo、0.3mg/kg和0.5mg/kg分别为n=3、6和4)。对于pbo、0.3mg/kg和0.5mg/kg距基线的相对bmd改变分别是股骨的颈部皮层的-0.9%、-1.4%和+1.9%,以及腰脊椎的+12.6%、+8.0%和1.9%。0.5mg/kg的生物标记物改变提示了有益的抗再吸收作用。
这些数据表明,actriia-fc0.5mg/kg的出现的剂量效应,其看起来逆转了高周转rod对皮层骨和松质骨的影响。pbo结果与预料相同。
9.4实施例4.肾脏疾病产生的循环肾脏修复因子引起心血管疾病
肾脏疾病与极其高的死亡率相关,这与它们产生心血管疾病相关(sarnak,m.j.etal.,2003.circulation108:2154-2169.)。一项进行中的regards计划的辅助研究表明,在具有持续性冠状动脉事件(心脏缺血或非致命性心肌梗塞)的患者中,在4年的中值跟踪中,第二心血管事件的发生率在患有肾脏疾病的患者中是35%,相比之下高风险组(吸烟者、糖尿病、高胆固醇血症)是19%,在高风险组中各种原因的死亡发生率是慢性肾病(ckd)组的一半(baber,u.,etal.,2013.amheartj166:373-380.)。与肾脏疾病相关的提高的心血管风险的原因在于2006年命名的一种综合征——慢性肾病-骨矿物失调(ckd-mbd)(moe,s.,etal.,2006.kidneyint69:1945-1953.)。在ckd-mbd中,已经发现三种新的心血管风险因素(block,g.a.,etal.,1998.amjkidneydis31:607-617;blacher,j.,etal.,2001.hypertension38:938-942;gutierrez,o.m.,etal.,2008.newengljmed359:584-592.),它们的风险因素状态在一般群体中得到确认(dhingra,r.,etal.,2007.archinternmed167:879-885;matsushita,k.,etal.,2014.journaloftheamericansocietyofnephrology;dalal,m.,etal.,2011.europeanjournalofendocrinology165:797-803.)。这些是高磷酸血症、血管钙化和升高的成纤维细胞生长因子23(fgf23)水平。ckd-mbd开始于ckd的早期阶段(2期)(fang,y.,etal.,2014.kidneyint85:142-150;pereira,r.c.,etal.,2009.bone45:1161-1168;fang,y.,etal.,2009.jamsocnephrol20:36a;hu,m.c.,etal.,2011.jamsocnephrol22:124-136.)由血管去分化/钙化、骨营养不良、klotho损失和提高的fgf23分泌组成(fang,y.,etal.,2014.kidneyint85:142-150.),但是在早期肾衰竭开始时进展为ckd-mbd的原因(hu,m.c.,etal.,2011.jamsocnephrol22:124-136;fang,y.,etal.,2014.jamsocnephrol25:1760-1763;deoliveira,r.b.,etal.,2013.nephrologydialysistransplantation28:2510-2517;sabbagh,y.2012.j.boneminer.r
已经证明肾脏疾病的再激活发展程序涉及疾病刺激的肾脏修复期间的肾发生(surendran,k.,etal.,2002.amjphysiolrenalphysiol282:f431-f441;surendran,k.,etal.,2005.jamsocnephrol16:2373-2384;maeshima,a.,etal.,2001.cytokine&growthfactorreviews12:289-298;terada,y.,etal.,2003.journaloftheamericansocietyofnephrology14:1223-1233;kawakami,t.,etal.,2013.jpathol229:221-231.)。在肾脏修复中重新激活的肾产生的因子之中,wnt(portmanteauofwinglessandintegrated)家族对于管状上皮重构是关键的(terada,y.,etal.,2003.journaloftheamericansocietyofnephrology14:1223-1233;kawakami,t.,etal.,2013.jpathol229:221-231;rinkevich,y.,etal.,2014.cellreports7:1270-1283.).在wnt功能的控制中,典型的信号转导转录性地诱导wnt抑制性蛋白家族的表达,它们是分泌的蛋白,用来限制wnt对自泌性或旁泌性因子的刺激的距离(niida,a.,etal.,2004.oncogene23:8520-8526;niehrs,c.2006.oncogene25:7469-7481;reya,t.,etal.,2003.nature423:409-414;chamorro,m.n.,etal.,2004.theembojournal24:73-84;gonzalez-sancho,j.m.,2004.oncogene24:1098-1103.)。wnt抑制剂是循环的因子,wnt抑制剂家族包括dickkopfs(dkk)、分泌的卷曲相关蛋白(sfrps)、硬骨素、sostdoc1、crescent、wnt抑制剂因子1(wif1)和icat(niehrs,c.2006.oncogene25:7469-7481).variousformsofkidneydiseaseincreaserenalexpressionofwntinhibitorsandincreasetheirlevelsinthecirculation(fang,y.,etal.,2014.jamsocnephrol25:1760-1763;surendran,k.,etal.,2005.jamsocnephrol16:2373-2384.)。
在ckd的循环中升高的关键wnt抑制剂的中和作用,dkk1,抑制ckd诱导的血管去分化、血管钙化和肾性骨营养不良(fang,y.,etal.,2014.jamsocnephrol25:1760-1763.)。这种效应是令人惊讶的,因为血管平滑肌中的wnt信号转导涉及刺激成骨细胞转变和血管钙化(al-aly,z.,etal.,2007.arteriosclerosis,thrombosis,andvascularbiology27:2589-2596;shao,j.s.,etal.,2005.journalofclinicalinvestigation115:1210-1220.)。然而,新近的研究表明,dkk1介导的主动脉wnt7b的抑制刺激了smad介导的主动脉内皮-间充质转变(enmt)和血管钙化(cheng,s.-l.,etal.,2013.arteriosclerosis,thrombosis,andvascularbiology33:1679-1689.)。enmt是涉及心脏瓣膜、心脏隔膜和主动脉根的发育的发育生理学的过程(eisenberg,l.m.,andmarkwald,r.r.1995.circulationresearch77:1-6;camenisch,t.d.,etal.,2002.developmentalbiology248:170-181.),它可能(zeisberg,e.m.,etal.,2007.natmed13:952-961.)或可能不(moore-morris,t.,etal.,2014.thejournalofclinicalinvestigation124:2921-2934.)在各种成年人疾病状态中促进心脏纤维化。这一因素研究了是否有来自tgfβ超家族的其他因子涉及肾脏疾病期间的尝试肾脏修复,并在ckd期间在循环中提高。
9.4.1方法
9.4.1.1动物模型的产生
动脉粥样硬化性低密度脂蛋白受体缺陷(ldlr-/-)的雄性(c57bl/6j背景)购自jackson实验室,在12周龄开始用高脂肪饮食(42%的卡路里来自脂肪)(teklad#_)饲喂。小鼠在22周龄时是肥胖的、胰岛素抗性的,在28周龄时是糖尿病的,并且是高胆固醇血症的。
早先描述了用来产生慢性肾病的两步过程(davies,m.r.,etal.,2003.jamsocnephrol14:1559-1567;davies,m.r.,etal.,2005.jamsocnephrol16:917-928.)。电灼可以在出生后12周通过2厘米的侧腹切口施用于右肾,随后在14周龄左侧进行全肾切除术。改变烧灼的强度,以产生中度的(ckd-3)肾脏损伤,其通过20周龄时的菊糖清除率来确认(附图12a)。对照动物接受假操作,其中暴露并移动适当的肾脏,但不以任何其他方式处理。五组小鼠用于这项研究(附图15b)。第一组是饲喂常规饮食的野生型c57bl/6j小鼠(wt)。这是用于标准对照值的正常肾脏功能和饮食的组。第二组是饲喂高脂肪饮食和假操作的ldlr-/-小鼠(sham)。这一组具有正常的肾脏的功能,它充当对照组来确定肾脏疾病的影响。第三组是具有相当于人ckd3期的降低的gfr、饲喂高脂肪饮食的ldlr-/-小鼠(ckd-3),在22周安乐死,是基线血管钙化组(ckd-3)。第四组是在22周开始每周两次接受溶媒的皮下注射的患有ckd-3的ldlr-/-小鼠,直到第28周安乐死(ckd-3v)。第五组是在22周开始每周两次接受10mg/kg的mactriia-fc(celgene,summit,nj)的皮下注射的患有ckd-3的ldlr-/-小鼠,直到第28周安乐死(ckd-3mactriia-fc)。
使用的第二种ckd的模型是x-连锁的alport's综合征的鼠同族体,其在iv型胶原蛋白的α5链的基因col4a5上是缺陷的(rheault,m.n.,etal.,2004.journaloftheamericansocietyofnephrology15:1466-1474.)。这是自发性肾脏疾病的模型,在整个结果中使用它来确认肾脏消融诱导的ckd的影响。繁育对可以购自jackson实验室,并繁育用于实验。半合子雄性在出生后200天自发地发生与人3-4期ckd可比较的肾脏疾病。
使用的第三种ckd模型是在用于细胞谱系追踪的转基因小鼠gnz小鼠中的肾脏消融,类似于ldlr-/-方案(附图14)。gnz报告物雌性小鼠(stoller,j.z.,etal.,2008.genesis(newyork,n.y.2000)46:200-204.)和tek-cre转基因雄性小鼠(koni,p.a.,etal.,2001.thejournalofexperimentalmedicine193:741-754.)购自jackson实验室,并繁育产生gnz/tek-cre+小鼠用于实验。gnz/tek-cre-同窝出生作为阴性对照。通过使用厂家推荐用于gnz和tek-cre小鼠品系的特异性引物进行小鼠基因分型。在所情况中,在麻醉下进行安乐死。腹膜腔内麻醉(甲苯噻嗪13mg/kg和氯胺酮87mg/kg)用于所有的过程。隐静脉的静脉血液样品在第二次手术后一周采集,来评估基线的术后肾脏功能。在处死时,通过心内穿刺采集血液,心脏和主动脉整体解剖。
9.4.1.2菊糖清除
如果安乐死在28周,在20周或26周根据厂家指导(biopalinc.,worcester,ma)进行菊糖清除。
9.4.1.3化学的钙化定量
在处死时解剖主动脉和心脏,在解剖显微镜下通过钝器解剖除去所有外部的组织。组织在60℃干燥20-24小时,称重,并用钵锤和研钵碾压成粉末。在4℃下在1nhcl中洗脱钙持续24小时。根据厂家的指导使用甲酚酞络合酮方法(sigma,stlouis)分析洗脱物的钙含量,结果相对干燥组织重量来校正。
9.4.1.4血液测试
通过标准的自动分析仪实验室方法,在抽血当天分析血液的血脲氮(bun)、钙和磷酸盐。血浆激活素(fitzgeraldindustries,acton,ma)、卵泡抑素(mybiosourceinc.,sandiego,ca)和卵泡抑素样3(mybiosourceinc.)水平在elisa分析中测定。血清dkk1用elisa分析r&dsystems,minn.,mn(r&dsystems,minn.,mn)。对于elisa分析,在安乐死时通过隐静脉或心脏穿刺抽取血液。所有血液样品在采集时置于冰上。血小板缺乏的edta血浆样品通过在4℃6000rpm5分钟和14000rpm2分钟的2步离心来制备。样品在-20℃或以下冷冻保存待用。
9.4.1.5组织学和免疫组织化学
主动脉、肾脏和心脏组织固定在10%中性缓冲的福尔马林中过夜,然后转移到4℃的70%乙醇中,包埋在石蜡中,制备5微米切片。切片在二甲苯中脱石蜡,在分级的乙醇系列中脱水,然后再水化。根据标准方案,masontrichome染色用于检测肾脏和心脏纤维化,茜素红染色用于检测钙化(gregory,c.a.,etal.,2004.analyticalbiochemistry329:77-84.)。对于免疫组织化学染色,内源的过氧化物酶用甲醇中3%h2o2阻断15分钟。非特异性结合用抗生物素蛋白和生物素封闭试剂(vectorlaboratories,burlingame,ca,usa)阻断30分钟,然后用3%正常驴血清阻断20分钟。在用pbs洗涤是指,切片与初级抗体在4℃孵育过夜,然后与生物素化的次级抗体(vectorlaboratories)在室温下孵育1小时,然后使用dab试剂盒(sk-4100,vectorlaboratories)进行链霉抗生物素蛋白结合的过氧化物酶染色。对于双重免疫荧光染色,切片在20%山羊血清中阻断,用第一初级和次级抗体以及第二初级和次级抗体连续染色,根据厂家指导,使用山羊抗兔alexa488和alexa568次级抗体1:400(lifetechnologies,a11008anda11011)或tsa试剂盒(lifetechnologies,t20932)用于信号放大。来自同一物种的初级抗体用于双重染色时,在第二次染色之前切片在柠檬酸盐缓冲液中在微波中加热5分钟(tothandmezey,2007)。初级抗体用于这项研究中用于免疫染色:兔多克隆抗actriia抗体1:250(abcam,ab135634)、兔多克隆抗抑制素betaa抗体1:100(santacruz,sc-50288)、兔多克隆抗cd31抗体1:50(abcam,ab28364)和兔多克隆抗gfp抗体1:1000(abcam,ab6556)。
9.4.1.6rt-pcr
使用rneasymini试剂盒(qiagen,valencia,ca)从主动脉和细胞培养物中提取rna。1μg的总rna用dnase处理,根据厂家的指导使用来自bio-rad(hercules,ca)的iscriptcdna合成试剂盒进行逆转录。使用vectornti(invitrogen,grandisland,ny)或primerexpress软件设计引物。perkin-elmerdna热循环仪用于进行反应。在如上述进行逆转录之后,使用steponeplus实时pcr仪(ab)、来自sigma(st.louis)的sybrgreen和来自invitrogen的pcr试剂盒进行实时。每个反应在95℃45秒、和60℃30秒和72℃60秒一式三份进行40个循环。随后是熔化循环,由60℃到95℃逐步提高的温度组成。在每个基因的解离曲线中观察到单一优势峰,支持了pcr产物的特异性。ct数(阈值)在pcr的指数期内设置,用于计算目标基因的表达水平。b2m用作内标准物,用于归一化所述值。由ct对比logcdna稀释度(相应于log拷贝数)组成的标准曲线通过扩增与未知数量的扩增子相应的cdna的连续稀释物来产生。通过在rt-pcr之前煮沸5分钟来确保基因组dna不被扩增,通过灭活逆转录酶来进行阴性对照。
9.4.1.7免疫印迹(western分析)
使用含有蛋白酶抑制剂混合物(santacruz)的ripa裂解缓冲液(thermoscientific),从小鼠的肾脏和主动脉制备全细胞溶胞产物蛋白.溶胞产物(20μg)装载到8-12%sds-page凝胶中,用针对抑制素β-a(santacruz)、α-微管蛋白(santacruz)、snai1(cellsignaling)、alpha-sma(sigma)、runx2(cellsignaling)、myocd(santacruz)、acvrl1(origene)、acvr1(cellsignaling)、erk1/2(cellsignaling)、磷酸-erk1/2(cellsignaling)、acvr1b(origene)、col1a1(santacruz)、smad2/3(cellsignaling)或磷酸-smad2/3(cellsignaling)的抗体进行免疫印迹。在免疫沉淀(ip)分析中,使用相同的全细胞溶胞产物蛋白。为了降低非特异性结合,使用预洗涤的蛋白a琼脂糖珠子(cellsignaling)预先清洗样品。预清洗的样品与磷酸丝氨酸抗体(abcam)孵育过夜。然后在蛋白a琼脂糖珠子上捕获ip-抗体复合物,通过免疫印迹分析检测蛋白质。
9.4.1.8人类研究
根据来自赫尔辛基声明的指南在给与知情同意之后将对象加入。如果大于18岁并患有3期ckd(估计的gfr30-59ml/分钟/1.73m2)使用肾病研究方程中的饮食修改(levey,a.s.,etal.,1999.anninternmed130:461-470.),对象是合格的。排除指标包括妊娠、骨疾病、心肌梗塞、充血性心力衰竭、心脏舒张功能障碍或严重的高血压。研究组的成员确定他们的临床患者满足包含指标并对研究感兴趣。在参与之前回顾医疗记录来确定最终的合格。在基线就诊时和治疗12个月后从每个对象获得血液样品。在获得血液样品的当天存在患者内的变异。从每份样品产生血浆等分量,直接用于生物化学测试或在-80℃冷冻。使用商业上可获得的elisa试剂盒根据厂家的说明(r&dsystems,minneapolis,mn)双份地测量激活素的血浆水平。
9.4.1.9统计
使用anova进行统计分析。所有数据表示为平均值±sd,触发在附图图例中另外指定。在使用fisherlsd法之后评估各组之间的差异,p<0.05认为是显著的。使用sigmastat统计软件(pointrichmond,ca)进行分析。所有组的数据有7-15的“n”。对于实时pcr分析,每个实验组中使用最少3个样品。不成对的t-测验用于比较mactriia-fc治疗的ckd-3小鼠和溶媒治疗的ckd-3v小鼠或假(sham-operated)操作的小鼠。在附图6中,方框代表中值和百分位范围(25th到75th百分位数),误差线代表低于25th和高于75th百分位数的百分位范围的1.5倍。使用用于多重比较的anovaholm–sidak方法比较平均值,p<0.05作为显著差异的临界水平。
9.4.2结果
9.4.2.1ckd模型中的肾功能
在三个实验模型中诱导类似于人3期ckd(ckd-3)的ckd。第一个模型是ckd刺激的动脉粥样硬化性血管钙化的模型:ldlr-/-高脂肪饲喂的小鼠(fang,y.,etal.,2014.kidneyint85:142-150;fang,y.,etal.,2014.jamsocnephrol25:1760-1763;davies,m.r.,etal.,2003.jamsocnephrol14:1559-1567;davies,m.r.,etal.,2005.jamsocnephrol16:917-928;lund,r.j.,etal.,2004.jamsocnephrol15:359-369;mathew,s.,etal.,2008.jamsocnephrol19:1092-1105.pmcid:pmc2396927;mathew,s.,etal.,2007.jamsocnephrol18:122-130;mathew,s.,etal.,2008.jamsocnephrol19:1509-1519.pmcid:pmc2488263.)。通过菊糖清除和通过bun水平测量的肾脏功能在ldlr-/-高脂肪饲喂小鼠中降低到人3期ckd的水平,如章节9.4.1.1中描述的,这些小鼠此后称为ckd-3(附图12a和附图12b)。此外,ckd-3小鼠是高磷酸盐血的(表11),这与人3b-4ckd一致。第二个ckd模型是自发性ckd,其在iv型胶原蛋白的α5链(col4α5)缺陷(alport’s综合征)的小鼠和人中发生(rheault,m.n.,etal.,2004.journaloftheamericansocietyofnephrology15:1466-1474.)。200天龄的col4α5缺陷小鼠具有相当于人3-4期ckd的菊糖清除降低和bun升高(附图12c和附图12d)。第三个模型,gnz小鼠中的ckd-3在章节9.4.1.1和下文中描述。
表11.各组动物的血清生化参数
9.4.2.2激活素水平和主动脉激活素iia型受体(actriia)
研究了ckd中的肾脏修复刺激tgfβ超家族成员的循环水平的能力。在ckd的模型中循环激活素水平提高(附图13a和附图13b)。分析肾脏和主动脉组织的激活素a(抑制素betaa的同二聚体(inhba))的mrna。在肾脏和主动脉中inhbamrna被ckd诱导(附图13c),在肾脏中蛋白质水平提高(附图13d)。分析来自患有ckd-3的小鼠的主动脉中tgfβ超家族ii型受体的诱导,所述受体是由ii型和i型(alk)受体组成的超家族受体杂多聚体的配体结合部件。ldlr-/-高脂肪饲喂的小鼠中产生的ckd-3诱导了主动脉血管平滑肌中的激活素ii型受体a(actriia)的上调(附图13e)。与调节的抑制因子卵泡抑素和卵泡抑素样3(fstl3)相关的激活素(welt,c.,etal.,2002.experimentalbiologyandmedicine227:724-752.),其循环水平(附图13f和附图13g)和组织水平不受ckd-3影响。在循环中卵泡抑素、fstl3和抑制素(总和620pg/ml加400pg/ml的未测出的抑制素)(sharpe,r.m.,etal.,1999.journalofandrology20:94-101.))对激活素a水平(>5000pg/ml)的化学当量表明,ckd产生了显著的游离激活素水平,是ckd中使得激活素a成为循环因子的病理事件。
9.4.2.3ckd中的主动脉内皮-间充质转变
ckd的第三个实验模型用于这些研究中。gnz小鼠被用于细胞谱系追踪(stoller,j.z.,etal.,2008.genesis(newyork,n.y.:2000)46:200-204.),一旦上游loxp侧翼的stop序列被移除,gnz小鼠表达核定位的绿色荧光蛋白和β半乳糖苷酶(gfp/lacz)(附图14a)。为了除去gnz小鼠中的loxp位点,它们与在酪氨酸激酶tek(tie2)启动子/增强子的指导下表达cre重组酶的tek-cre繁育。由于tie2是内皮谱系特异性血管生成素受体,gnz/tek-cre+小鼠在内皮谱系细胞中表达核的和细胞质的gfp(附图14a)(moore-morris,t.,etal.,2014.thejournalofclinicalinvestigation124:2921-2934.)。在gnz/tek-cre+小鼠中,与核dapi染色共同定位的主动脉gfp限于用cd31生物标记物标记的内皮细胞(附图14b,见箭头)。当在gnz/tek-cre+小鼠中产生ckd-3时,除了内皮细胞之外,主动脉中层和外膜中的细胞显现gfp染色,显示了这些细胞通过内皮-间充质转变(enmt)来源于内皮谱系(附图14c、14d,见箭头)。为了进一步分析ckd是否刺激enmt,在自发性ckd的模型、alports’s综合征小鼠中检查了涉及enmt的转录因子snai1的表达。在ckd的过程中snai1在早期是被上调的(75doa)(附图14e),与峰值激活素水平的时机一致(见下文)。
9.4.2.4ckd中抑制actriia信号转导的血管作用
使用配体陷阱(附图23a),其包含与igg1的fc结构域融合的actriia的细胞外结构域(在此称为mactriia-fc)。附图23b描绘了在血管钙化模型中使用mactriia-fc的实验设计,使用一治疗方案,其容许在研究mactriia-fc之前八周发生ckd-3刺激的血管钙化。使用这一方案,用actriia配体陷阱治疗ckd-3小鼠降低了ldlr-/-高脂肪饲喂ckd-3小鼠中ckd-3刺激的主动脉runx2表达和主动脉碱性磷酸酶(alp)表达(附图25a)。runx2和alp表达都代表了actriia信号转导的可能的下游效应,主动脉中成骨细胞转变的生物标记物被mactriia-fc治疗逆转。主动脉平滑肌22α(sm22-alpha),一种分化的血管平滑肌细胞的生物标记物,被ckd-3降低,被mactriia-fc刺激。ckd-3引起降低的主动脉心肌素(myocd)表达,是血管平滑肌细胞特异性的转录因子,但是心肌素不受mactriia-fc治疗的影响。相比肾脏,已与血管钙化相关联的(lim,k.,etal.,2012.circulation125:2243-2255.)主动脉klotho表达是极低的(数据未显示)。就附图25a中ckd-3和mactriia-fc治疗对mrna的主动脉蛋白质水平的影响而言,ckd提高主动脉runx2水平,mactriia-fc归一化主动脉runx2水平(附图25b)。ckd降低alpha平滑肌肌动蛋白(αsma)的主动脉水平,这是分化的血管平滑肌细胞的另一种生物标记物,mactriia-fc治疗提高αsma的主动脉水平(附图25b)。心肌素水平不被ckd或mactriia-fc治疗改变。
9.4.2.5降低的actriia信号转导对血管钙化的影响
血管钙化的ckd刺激在动脉粥样硬化和2型糖尿病的模型中研究(al-aly,z.,etal.,2007.arteriosclerosis,thrombosis,andvascularbiology27:2589-2596;towler,d.a.,etal.,1998.journalofbiologicalchemistry273:30427-30434.),患有消融性ckd的ldlr-/-高脂肪饲喂小鼠,如上文所描述的。在ckd-3溶媒治疗的小鼠(ckd-3v)中ckd-3引起主动脉粥样斑中钙沉积的积累(附图15a),其在用mactriia-fc治疗的ckd-3小鼠(ckd-3r)中不存在,主动脉组织钙含量降低到野生型小鼠中观察到的水平,显著低于开始mactriia-fc治疗之时表现的水平,ckd-3(附图15b)。
9.4.2.6降低的actriia信号转导对ckd刺激的心脏疾病的影响
在血管钙化模型中研究心脏疾病的ckd刺激。ckd-3v小鼠具有提高的心脏重量,其被mactriia-fc治疗逆转(附图16a),但是不被碳酸镧治疗(ckd-3l(fang,y.,etal.,2014.jamsocnephrol25:1760-1763.))逆转,ckd-3v诱导轻微的心脏肥大(附图16b)。然而,虽然没有心脏纤维化的证据(附图16c),存在肌细胞过度生长的证据,其被mactriia-fc治疗逆转。
由于ckd中血管钙化和心脏肥大相关性的一种机制是大动脉硬化,使用早先报道的方法(wagenseil,j.e.,etal.,2009.circulationresearch104:1217-1224;wagenseil,j.e.,etal.,2005.ajp-heartandcirculatoryphysiology289:h1209-h1217.)测量了血管硬化和血压。ldlr-/-高脂肪饲喂动脉粥样硬化的小鼠中的ckd-3不产生颈动脉或主动脉的血管硬化(附图19a和19b)或血压升高(表12)。此外,在不存在提高的硬化的情况下,在用针对dkk1的中和抗体(fang,y.,etal.,2014.jamsocnephrol25:1760-1763.)治疗的ckd-3小鼠中的dkk1中和对于主动脉硬化没有作用。
表12.28周龄小鼠的生理学心血管参数
sbp=收缩压,dbp=舒张压。值表示为平均值±平均标准误。每组n=4-6只小鼠。
9.4.2.7主动脉和肾脏中的actriia信号转导与肾脏纤维化
通过tgfβ超家族的典型的信号转导涉及结合ii型受体的配体活化它们的丝氨酸/苏氨酸激酶活性并刺激i型受体、alk激酶的缔合与磷酸化(参见附图20中的示意图)。存在七种alk激酶被tgfβ超家族利用,alk4(actrib)是最常与激活素/actriia信号转导相关的i型受体(abey,etal.,2004.growthfactors(chur,switzerland)22:105-110.)。在来自ckd-3小鼠模型的肾脏组织匀浆中,alk4磷酸化没有提高,与早先的研究一致(antsiferova,m.,andwerner,s.2012.journalofcellscience125:3929-3937.)(附图18a)。相比之下,phosphosmad2被ckd-3提高,被mactriia-fc降低(附图18a),表明另一种alk受体在ckd中肾脏激活素信号转导中的作用。在由间质性肾炎的患病的ckd-3肾脏中,col1a1被上调,mactriia-fc降低了col1a1水平(附图18a),与由mactriia-fc诱导的phosphosmad2降低一致。此外,在ckd-3v小鼠中诱导的肾脏klotho表达方面存在较大的降低,其被mactriia-fc矫正(附图18b)。结果,分析了在ckd-3v中表达激活素的肾脏区室,鉴定出在管周肌成纤维细胞中的重表达,而不在上皮中表达。
在主动脉平滑肌中,检测出alk4和alk1(附图18a),而没有alk5或alk2。alk4和alk1的水平不受ckd-3的影响。然而,ckd-3不提高主动脉phosphosmad2/3水平,mactriia-fc也不降低它们(附图18a)。然而,非经典actriia信号转导的分析(附图20)表明,map激酶(phosphoerk1/2)既不被ckd活化也不受mactriia-fc抑制,p38和jnk的血管平滑肌水平是非常低的。主动脉actin2水平也是非常低的,其不是ckd-3刺激的。axin2是典型的wnt信号转导的标准生物标志物。然而,由于dkk1是典型的wnt信号转导的转录靶点,分析了肾脏和主动脉中的dkk1水平作为wnt活性的生物标志物,表明在ckd-3小鼠中mactriia-fc治疗降低了肾脏dkk1水平(附图18c),产生血浆dkk1水平的显著降低(附图18c)。此外,主动脉dkk1水平被ckd-3提高,被mactriia-fc抑制(附图18c)。这表明肾脏和血管平滑肌的wnt信号转导以及dkk1的全身性释放受到激活素抑制的抑制。因而,ckd中升高的循环激活素通过提高的血管actriia发信号,活化wnt信号转导并刺激动脉粥样硬化性钙化。
9.4.2.8临床前研究向人类病理生理学和临床的转变
如附图19中所示,与健康对照相比,血清激活素水平在患有3期ckd的患者群组中提高。
9.4.3结论
这个实施例表明,激活素是涉及肾脏修复的第二种因子,其在ckd期间在循环中提高。不受理论的限制,结果表明,激活素表达在患病肾脏中提高,被释放到循环中,并刺激主动脉血管平滑肌去分化和成骨细胞转变,这受到内皮向间充质转变的促进,这些作用导致ckd刺激的动脉粥样硬化性钙化和心脏肥大。ckd上调了肌成纤维细胞中的肾脏激活素表达,通过提高肾脏纤维化刺激肾脏疾病的发展。抑制actriia信号转导抑制了主动脉中的成骨细胞转变和动脉粥样硬化性钙化。抑制actriia信号转导抑制了心脏肥大和肾脏纤维化。actriia配体陷阱mactriia-fc对早期ckd-mbd综合征的作用类似于ckd刺激的血管钙化中针对dkk1的单克隆抗体的作用(fang,y.,etal.,2014.jamsocnephrol25:1760-1763.)。这些数据表明,在患病肾脏中抑制actriia信号转导降低了wnt活化和循环wnt抑制剂。此外,在血管平滑肌中,激活素刺激了wnt活性,其受到mactriia-fc的抑制。因而,两种肾脏发育因子wnts和激活素激活素的重激活在ckd中产生了循环wnt抑制剂和激活素,引起血管和心脏疾病。这是肾脏疾病直接导致心血管疾病的证明,肾病过程的考虑不能与肾脏修复和后续的心血管疾病刺激相分离。
进一步的,这个实施例表明,肾脏的激活素表达在三种慢性肾病模型中提高,产生了提高的循环激活素,其超过了循环中激活素抑制剂的水平。循环激活素刺激了通过actriia受体的信号转导,产生主动脉血管平滑肌去分化、成骨细胞转变和动脉粥样硬化斑块的钙化。这些效应是由于循环激活素,得到了主动脉中不存在提高的激活素蛋白质水平、而ckd诱导提高的主动脉激活素mrna的支持(附图13b)。不受理论的限制,这些数据表明,血管的激活素信号转导通过肾脏的内分泌性激活素产生而被ckd刺激。
由于enmt是smad介导的过程(cooley,b.c.,etal.,2014.sciencetranslationalmedicine6:227ra234.),被tgfβ超家族的成员,包括tgfβ、骨骼形态发生蛋白(bmp)、激活素/抑制素以及生长与分化因子(gdf)活化(piek,e.,etal.,1999.thefasebjournal13:2105-2124.),分析了患有ckd-3的血管钙化模型的主动脉中tgfβ超家族的ii型受体水平的改变,其是受体的配体结合部件。激活素iia型受体(actriia)在主动脉血管平滑肌中被上调。施用与igg1的fc结构域的融合蛋白中的actriia细胞外结构域(mactriia-fc)表明,抑制actriia信号转导产生了在ckd刺激动脉粥样硬化模型中主动脉平滑肌细胞中成骨细胞转变的抑制,血管平滑肌细胞基因表达的刺激,以及主动脉钙化的逆转。此外,ckd刺激了谱系跟踪小鼠模型中的enmt。然而,激活素功能的主要位点看起来在血管平滑肌中,在此actriia表达提高。
心脏肥大,特别是左室性的,在ckd中是高度普遍的(moran,a.,etal.,2008.americanjournalofkidneydiseases52:839-848;park,m.,etal.,2012.journaloftheamericansocietyofnephrology23:1725-1734.)。此外,动脉粥样硬化性血管钙化模型的特征在于心脏肥大(附图16)。然而,模型中心脏肥大的产生在机制上不同于ckd刺激的血管硬化(townsend,r.r.2015.currentopinioninnephrologyandhypertension24:47-5310.1097/mnh.0000000000000086;merx,m.w.,etal.,2005.journaloftheamericansocietyofnephrology16:3357-3364.)、高血压和心脏再成型中的常见范式,高血压和心脏再成型,因为动脉粥样硬化的ckd-3小鼠(ldlr-/-高脂肪饲喂的糖尿病小鼠)不展现血管硬化也不展现高血压。由于mactriia-fc在不存在fgf23水平改变的情况下矫正了心脏肥大(附图19),ckd-3小鼠中的心脏肥大不太可能是由于fgf23(faul,c.,etal.,2011.jclininvest121:4393-4408.)。
总之,不受理论的限制,这个实施例表明,涉及肾脏修复的第二种因子在ckd期间在循环中提高,并引起心血管疾病。不受理论的限制,该实施例表明,激活素表达在患病肾脏中提高,被释放到循环中,并刺激主动脉血管平滑肌去分化和成骨细胞转变,这受到内皮向间充质转变的促进,这些作用导致ckd刺激的动脉粥样硬化性钙化和心脏肥大。ckd上调了肌成纤维细胞中的肾脏激活素表达,通过提高肾脏纤维化刺激肾脏疾病的发展。抑制actriia信号转导抑制了主动脉中的成骨细胞转变和动脉粥样硬化性钙化。抑制actriia信号转导抑制了心脏肥大和肾脏纤维化。actriia配体陷阱mactriia-fc对早期ckd-mbd综合征的影响显示,抑制患病肾脏中的actriia信号转导降低了wnt活化和循环wnt抑制剂。因而,不受理论的限制,两种肾脏发育因子wnts和激活素的重激活在ckd中产生了循环wnt抑制剂和激活素;因而,肾脏疾病引起心血管疾病。
9.5实施例5:肾脏损伤/修复通过全身性wnt抑制和激活素刺激血管疾病
9.5.1背景
这个实施例中呈现的结果涉及实施例4中呈现的结果(章节9.4)。
通过在肾脏修复期间产生全身性wnt抑制和激活素分泌,肾脏疾病导致动脉粥样硬化性血管钙化。慢性肾病(ckd)的血管效应是wnt抑制与激活素诱导的激活素受体功能调节的相互作用。
9.5.2方法
具有升高的wnt抑制剂特别是dkk1的ckd和激活素在谱系跟踪和血管钙化的小鼠模型中诱导,容许在alport’s小鼠中自发地发展。激活素、dkk1、激活素2a型受体(actriia)、phosphosmad2/3和胶原蛋白水平通过elisa、rt-pcr和western印迹来测量。血管平滑肌功能通过压力诱导的动脉扩张术来测量。在繁育成内皮特异性tie2-cre小鼠的rosa-tdt小鼠中进行细胞谱系跟踪。携带rosa--tdt的小鼠在携带cre重组酶的细胞中表达蕃茄红。mactriia-fc是指激活素a配体陷阱(参见,例如,美国专利no.8,173,601和carrancioetal.,2014,britishjournalofhaematology,165:870-882)。
9.5.3结果
ckd提高循环dkk1和激活素水平。在患病肾脏中,激活素在肌成纤维细胞中表达,通过phosphosmad3的actriia信号转导被提高。在患病肾脏中,actriia配体陷阱mactriia-fc抑制了肾脏的psmad3、col1a1表达、尿蛋白水平和dkk1水平,并提高了klotho水平。在血管系统中,actriia水平和信号转导受到ckd的损害,伴随降低的血管平滑肌分化和功能。在ckd小鼠血管系统中,mactriia-fc提高了血管平滑肌细胞分化,并抑制成骨细胞转变和血管钙化。在循环中,mactriia-fc降低dkk1水平。对比具有正常肾脏功能的tek-cre/rosa-tdt小鼠,在tek-cre/rosa-tdtckd小鼠的受损的股骨动脉的外膜的细胞中ckd诱导蕃茄红表达,其中番茄红限于股动脉内皮,表明在血管损伤期间ckd诱导tie2阳性细胞。
9.5.4结论
ckd降低血管平滑肌功能并刺激成骨细胞转变和血管钙化。使用mactriia-fc降低ckd中升高的激活素的作用,抑制了smad依赖性肾脏纤维化,阻断了主动脉成骨细胞转变,提高了血管平滑肌分化,并降低了血管钙化。
9.6实施例6:在ckd-mbd的肾性骨营养不良的病理中激活素信号转导的作用
9.6.1.1引言
慢性肾病-矿物质/骨失调(ckd-mbd)包括血管钙化和骨营养不良。ckd提高循环激活素(tgfβ超家族的配体)和激活素信号转导(附图21a)。用激活素iia型受体(actriia)配体陷阱(mactriia-fc)抑制actriia信号转导抑制了血管钙化并防止心脏肥大。这个实施例表明激活素信号转导在肾性骨营养不良的病理中的作用。
9.6.1.2方法
假操作的ldlr-/-高脂肪饲喂小鼠(sham;n=12)显现糖尿病和高胆固醇血症。具有高磷酸血症、升高的fgf-23和肾小球过滤率60%降低的ckd(ckd-3)通过在ldlr-/-高脂肪饲喂小鼠中在14周龄的5/6肾切除术来诱导,是动脉粥样硬化性血管钙化的模型。ckd-3小鼠用mactriia-fc10mg/kg(mactriia-fc;n=15)或溶媒(veh;n=13)治疗,在22周龄开始每周腹膜内注射,在28周通过骨组织形态学和微计算机断层扫描来研究。ckd-3的结果与野生型(wt;n=5)小鼠和sham比较。
9.6.2结果
相对于wt(松质骨体积/组织体积(bv/tv):12.90%),sham小鼠展现了与衰弱性骨疾病相关的降低的bv/tv(10.92%)ckd-3的诱导在veh小鼠中导致高周转骨疾病,和更低的bv/tv(11.22%);这被六周的mactriia-fc治疗逆转(13.28%)。ckd-3的诱导引起小梁厚度降低,这被6周的mactriia-fc治疗逆转。ckd-3veh治疗的小鼠展现了更高的侵蚀表明/骨表面和更高的破骨细胞数量/100mm骨长度(分别为1.83%和62.32/100mm),相比sham(1.05%和33.40/100mm),这被mactriia-fcmactriia-fc缓解(1.23%和38.37/100mm)。当与wt或sham(分别为附图21b和21c)相比时,ckd-3veh治疗的小鼠还导致更高的成骨细胞表面/骨表面和更高的成骨细胞数量/100mm骨长度(分别为1.58%和110.63/100mm;p<0.05)。与veh相比,mactriia-fc显著地降低成骨细胞表面/骨表面和成骨细胞数量/100mm骨长度(0.68%和43.18/100mm;p<0.05)。尽管相对于veh在成骨细胞数量方面明显降低,用mactriia-fc治疗的矿物质合并率被维持(分别为0.42和0.40μm3/天),伴有显著更高的骨形成率/成骨细胞(分别为0.17vs.0.48μm3/100个细胞/年;p<0.05vs.veh),这类似于wt(0.42μm3/100个细胞/年)(附图21d)。
表13.组织形态学结果(平均+sem)
sem=平均标准误
mactriia-fc不影响高磷酸血症和fgf-23水平。
9.6.3结论
提高的循环激活素促进了与ckd-3相关的高周转骨营养不良。用actriia配体陷阱mactriia-fc抑制激活素信号转导,通过抑制骨吸收和归一化矿物质合并率以及骨形成率/成骨细胞、对抗ckd的负面效果,提高了ckd-3中的骨体积。
9.7实施例7:在用逐步升高的hactriia-fc剂量水平治疗的血液透析对象中对骨质量和腹部主动脉血管钙化的定量计算机断层扫描结果
9.7.1引言
高周转肾性骨营养不良的标志是降低的皮层骨质量和提高的小梁骨质量,引起骨折风险提高。根据体外数据,激活素ii型受体-igg1融合蛋白hactriia-fc阻断了激活素a信号转导,可以降低破骨细胞发生,促进骨中的成骨细胞成熟。使用定量计算机断层扫描(qct)在血液透析(hd)的对象中当前的分析评估了hactriia-fc对骨矿物密度(bmd)和腹部主动脉血管钙化的影响。
9.7.2方法
在用于矫正贫血的hd的对象中对hactriia-fc的研究中,促红细胞生成素刺激剂(esa)响应性的对象被洗出他们的esa效应直到血红蛋白(hb)<10g/dl,任何随机化到每28天皮下施用直到8个剂量周期的hactriia-fc0.3mg/kg(n=9)、0.5mg/kg(n=8)、0.7mg/kg(n=9;7例完成,2例进行中)或安慰剂(pbo;n=9)中。利用14天剂量周期的剂量组是当前参与的。评估对象的对hb、安全性参数、bmd、血管钙化和骨周转的生物标记物的影响。治疗失败(hb<9g/dl)用esa/输血来挽救。在基线和225天的治疗期之后获得髋部、腰脊椎和腹主动脉的qct扫描。
9.7.3结果
在该项研究中被随机化的35名对象中,20名具有成对的qct评估(pbo:n=3;0.3mg/kg:n=6;0.5mg/kg:n=5和0.7mg/kg:n=6)。一些具有成对的qct的对象由于治疗失败而对hactriia-fc的暴露有限。表14展现了pbo和每个hactriia-fc剂量组的bmd和血管钙化结果。与pbo相比,hactriia-fc看起来缓解了高周转肾性骨营养不良对皮层和小梁bmd的影响,并减慢了血管钙化的发展。
表14
cfb=距基线改变。
9.7.4结论
这些数据表明,hactriia-fc以剂量依赖性的方式逆转了高周转肾性骨营养不良对皮层和小梁骨的影响,减慢了血管钙化的发展。
9.8实施例8.用逐步升高的actriia-hfc(seqidno:7;“sotatercept”)剂量水平治疗的血液透析对象中骨质量和腹部主动脉血管钙化的定量计算机断层扫描结果
9.8.1引言
参见实施例6(章节9.7)的引言(章节9.7.1)和方法(章节9.7.2)。这个实施例呈现了在研究的较晚时间获得的、实施例6(章节9.7)中进行的研究的其他数据。
9.8.2结果
总共35名对象进行随机化,接受至少一剂的安慰剂或actriia-hfc(seqidno:7;“sotatercept”),如表15中标明的。
表15.随机化的对象和qct分析子集合
对象分布在附图22a中描绘,包括在基线和225天有成对的qct测量的对象。停止研究治疗的大多数对象具有需要挽救的治疗识别,一般是因为血红蛋白浓度低于9g/dl。停止研究治疗的大多数对象接受了安慰剂或0.3mg/kg的sotatercept。没有对象因为有害事件停止治疗。进一步的,在具有成对的qct测量的21名对象中,12名由于在治疗期内的血红蛋白治疗失败而需要挽救治疗,需要挽救的人中的9人处于前3个剂量周期内。
在具有成对的qct测量的对象中,基线的人口统计学和临床特征在治疗组之间是一般相似的(表16)。然而,在安慰剂组中存在着实质上更久的在透析时间,这也是最年轻的组。在基线生物标记物和agatston得分方面各组之间也存在差异(表17)。
表16.具有成对的qct测量的对象的基线人口统计学和临床特征
*对象可以接受多种类型的结合剂
表17.具有成对的qct测量的对象的平均基线生物标记物、体积bmd和agatston得分
注意:n反映了具有成对的qct评定的随机化对象的数量;对每个参数可用的对象的实际数量可能变化。pth=甲状旁腺激素。
a骨=特异性碱性磷酸酶(bsap)参考范围:男性,6-30;女性(绝经前),3-19;女性(绝经后),6-26。
b1型前胶原n-原肽(p1np)参考范围:男性,30-110;女性20-108
cc-末端端肽(ctx)参考范围:男性,0-854,女性(绝经前),26-573;女性(绝经后),104-1,008
d更低的agatston得分表明更低水平的血管钙化。
严重有害事件一般被认为是与sotatercept不相关的,不引起停止,由继续治疗来解决。在sotatercept治疗组中没有报告死亡。有害事件在严重度上大多数是轻微的或中度的,与研究药物不相关,在治疗组之间是相对相似的,一般与对象的医学史一致。在前28天的剂量周期中和在225天治疗期期间,在任何治疗组的对象中,家庭血压测量值没有显示距基线的一致性或剂量依赖性的改变。
腹主动脉总计agatston得分的距基线改变在表18中提供。在腹主动脉总计agatston得分方面有<15%进展的对象的比例在附图22b中显示。
表18.在腹主动脉总计agatston得分和平方根转化的总体积得分方面的基线和距基线改变*
注意:n反映了具有成对的qct评定的随机化对象的数量;对每个参数可用的对象的实际数量可能变化。
*更低的总计agatston和平方根转化的总体积得分表明低水平的血管钙化。
进一步的,表19提供了股骨颈部皮层和平均腰脊椎小梁体积bmd测量的距基线改变百分比。分析了在股骨颈部皮层bmd中具有>2%增进的对象的比例,确定了用sotatercept治疗与股骨颈部皮层骨的≥2%提高的对象的比例提高相关(参见表19和附图22c)。还参见mallucheetal.,2014,clin.j.am.soc.nephrol.,9:1254-1262。此外,在高周转rod中,相比一般群体,通过腰椎小梁bmd测量的,小梁骨质量提高(即,不良质量的骨),在eskd中在椎骨骨折率上没有降低(参见,leonardmb,2009,semin.nephrol.,29:133-143,和duanetal.,1999,j.clin.endocrinol.metab.84:718-722)。在这个场景中,提高的小梁骨质量是品质不良的(参见mallucheetal,2012,j.am.soc.nephrol.23:525-532。用sotatercept治疗减慢了腰椎中小梁骨质量的提高(表19)。
表19.股骨颈部皮层和平均腰椎(l1、l2)小梁bmd的基线和距基线改变百分比
注意:n反映了具有成对的qct评定的随机化对象的数量;对每个参数可用的对象的实际数量可能变化。
9.8.3结论
根据基线生物标志物数据,这个实施例中的对象倾向于具有高周转rod。安慰剂组具有降低的皮层骨质量,提高的小梁骨质量和提高的血管钙化,其以与eskd中其他大研究相似的比例发生(raggietal.,2011,nephrol.dial.transplant.26:1327-1339),如对高周转rod所预计的。
在基线和225天(其是在达到八个28天剂量周期之后)测量的qct数据表明,用sotatercept治疗高周转rod引起了对多种ckd-mbd参数的影响,包括血管钙化的减慢的发展,提高的股骨颈部皮层骨质量,和腰脊椎骨质量的减慢的提高。血管钙化的降低和骨质量的提高与用于血管钙化的ldlr-/-高脂肪饲喂的、5/6肾切除术的小鼠模型中的组织学发现是一致的(fangetal.,2014,abstract,asnkidneyweek2014,november11-16,2014,philadelphia,pa)。
9.9实施例9:actriia-hfc(seqidno:7,“sotatercept”)影响终末期肾病的多种表现
9.9.1背景
这个实施例呈现了来自临床研究的数据。实施例7和8(章节9.7和章节9.8)也呈现了来自这项研究的数据。
这项进行中的、随机、单盲、安慰剂对照的研究评估了一种用于矫正血液透析对象的贫血的actriia-igg1融合蛋白配体陷阱actriia-hfc(seqidno:7;“sotatercept”)的药物动力学、安全性和血红蛋白作用,并使用定量计算机断层扫描探索它对血管钙化和骨矿物密度的影响。这个实施例提供了0.3、0.5和0.7mg/kg剂量组的中间的结果。
9.9.2方法
促红细胞生成素刺激剂(esa)响应性对象洗出esa效应直到血红蛋白<10g/dl,并随机化到每28天皮下施用安慰剂或sotatercept中持续≤8个剂量周期。治疗失败(血红蛋白<9g/dl)用esa或输血挽救;对象内的剂量递增不被允许。在基线和225天的治疗期之后获得髋部、腰脊椎和腹主动脉的定量计算机断层扫描扫描。报告的是药物动力学、安全性、家庭血压、血红蛋白、血管钙化和骨矿物密度作用的中间结果。
9.9.3结果
在用安慰剂(n=9)或sotatercept0.3mg/kg(n=9)、0.5mg/kg(n=8)和0.7mg/kg(n=9)治疗的对象中,有害事件大多数是轻微/中度的,与研究药物不相关,在各组之间在类型/严重度方面相对相似,一般与对象的医学史一致。在安慰剂组中发生两起死亡。在家庭血压方面没有剂量依赖性改变。在225天治疗期中,在用安慰剂或sotatercept0.3、0.5或0.7mg/kg治疗的对象中分别有33%、33%、63%和78%的血红蛋白>10g/dl。在分别用安慰剂或sotatercept0.3、0.5或0.7mg/kg治疗的4、6、5和6名对象中获得的成对的定量计算机断层照相显示在33%、80%、80%和100%对象中有<15%的血管钙化发展,在0%、20%、40%和75%的对象中有股骨颈部皮层骨矿物密度>2%提高。
9.9.4结论
sotatercept是耐受的,在血液透析中有可接受的安全性分布,在家庭血压方面没有提高。在血红蛋白、血管钙化和骨矿物密度方面存在着对sotatercept的剂量依赖性反应。
9.10实施例10:ckd中失调的actriia信号转导促进动脉粥样硬化性钙化和肾脏纤维化
这个实施例涉及本文的其他实施例中描述和进行的实验,包括实施例4。
9.10.1方法
9.10.1.1动物模型的产生
动脉粥样硬化性低密度脂蛋白受体缺陷(ldlr-/-)的雄性(c57bl/6j背景)购自jackson实验室,在12周龄开始饲喂高脂肪饮食(42%的卡路里来自脂肪)。小鼠在22周龄时是肥胖的、胰岛素抗性的,在28周龄时是糖尿病的,并且是高胆固醇血症的。
早先描述了用来产生慢性肾病的两步过程(daviesmr,etal.jamsocnephrol2003;14:1559-1567;daviesmr,etal.jamsocnephrol2005;16:917-928)。电灼可以在出生后12周通过2厘米的侧腹切口施用于右肾,随后在14周龄左侧进行全肾切除术。改变烧灼的强度,以产生中度的(ckd-3)肾脏损伤,其通过20周龄时的菊糖清除来确认(附图33a、b)。对照动物接受假操作,其中暴露并移动适当的肾脏,但不以任何其他方式处理。五组小鼠用于这项研究(附图23b)。第一组是饲喂常规饮食的野生型c57bl/6j小鼠(wt)。这是用于标准对照值的正常肾脏功能和饮食的组。第二组是饲喂高脂肪饮食和假操作的ldlr-/-小鼠(sham)。这一组充当对照组来确定肾脏疾病的影响。第三组是具有相当于人ckd3期的降低的gfr、饲喂高脂肪饮食的ldlr-/-小鼠(ckd-3),在22周安乐死,是附图25a、b中使用的基线血管钙化组(ckd-3)。第四组是在22周开始每周两次接受溶媒(磷酸盐缓冲盐水)的皮下注射的患有ckd-3的ldlr-/-小鼠,直到第28周安乐死(ckd-3v)。第五组是在22周开始每周两次接受10mg/kg的mactriia-fc(celgene,summit,nj)的皮下注射的患有ckd-3的ldlr-/-小鼠,直到第28周安乐死(ckd-3r)。使用的剂量是早先在pk/pd研究中显示对于刺激骨形成有效的剂量。
使用的第二个ckd模型是x-连锁的alport’s综合征的鼠同族体,其在iv型胶原蛋白的α5链col4a5的基因中是缺陷的。(rheaultmn,etal.j.theam.soc.neph.2004;15:1466-1474)。这是自发性肾脏疾病的模型,在整个结果中使用它来确认肾脏消融诱导的ckd的影响。繁育对可以购自jackson实验室,并繁育用于实验。半合子雄性在出生后150天自发地发展与人ckd3-4期可比较的肾脏疾病,在生命第75天发展血尿症。
在所情况中,在麻醉下进行安乐死。腹膜腔内麻醉(甲苯噻嗪13mg/kg和氯胺酮87mg/kg)用于所有的过程。隐静脉的静脉血液样品在第二次手术后一周采集,来评估基线的术后肾脏功能。在处死时,通过心内穿刺采集血液,心脏和主动脉整体解剖。
9.10.1.2菊糖清除
如果安乐死在28周,在20周或26周根据厂家指导(biopalinc.,worcester,ma)进行菊糖清除。
9.10.1.3化学的钙化定量
在处死时解剖主动脉,在解剖显微镜下通过钝器解剖除去所有外部的组织。组织在60℃干燥20-24小时,称重,并用钵锤和研钵碾压成粉末。钙在4℃在1nhcl中洗脱24小时。根据厂家的指导使用甲酚酞络合酮方法(sigma,stlouis,mo)分析洗脱物的钙含量,结果相对干燥组织重量来校正。
9.10.1.4血液测试
通过由动物机构进行的标准自动分析仪实验室方法,在抽血当天分析血液的血脲氮(bun)、钙和磷酸盐。血浆激活素(fitzgeraldindustries,acton,ma)、卵泡抑素(mybiosourceinc.,sandiego,ca)和卵泡抑素样3(mybiosourceinc.)水平在elisa分析中测定。血清dkk1用elisa分析(r&dsystems,minn.,mn)。对于elisa分析,在安乐死时通过隐静脉或心脏穿刺抽取血液。所有血液样品在采集时置于冰上。血小板缺乏的edta血浆样品通过在4℃6000rpm5分钟和14000rpm2分钟的2步离心来制备。样品在-20℃或以下冷冻保存待用。
9.10.1.5组织学和免疫组织化学
主动脉和肾脏组织固定在10%中性缓冲的福尔马林中过夜,然后转移到4℃的70%乙醇中,包埋在石蜡中,制备5微米切片。切片在二甲苯中脱石蜡,在分级的乙醇系列中脱水,然后再水化。根据标准方案,masontrichome染色用于检测肾脏和心脏纤维化,茜素红染色用于检测钙化。(gregoryca,etal.analyticalbiochem.2004;329:77-84)。对于免疫染色,切片在20%正常的山羊血清中阻断20分钟,与初级抗体在4℃孵育过夜。切片在pbs中洗涤,在20%正常的山羊血清中阻断20分钟,之后与山羊抗兔alexa488次级抗体1:400(lifetechnologies,a11008)在室温下孵育30分钟,或根据厂家指导(lifetechnologies,t20932)使用tsa试剂盒用于信号放大。对于双重免疫荧光染色,切片在20%山羊血清中阻断,用第一初级和次级抗体以及第二初级和次级抗体连续染色,根据厂家指导,使用山羊抗兔alexa488和alexa568次级抗体1:400(lifetechnologies,a11008和a11011)或tsa试剂盒(lifetechnologies,t20932和t20934)用于信号放大。来自同一物种的初级抗体用于双重染色时,在第二次染色之前切片在柠檬酸盐缓冲液中在微波中加热5分钟。(tóthze,j.histochem.&cytochem.2007;55:545-554)。初级抗体用于这项研究中用于免疫染色:兔多克隆抗actriia抗体1:250(abcam,ab135634)、兔多克隆抗抑制素betaa抗体1:100(santacruz,sc-50288)、兔多克隆抗cd31抗体1:50(abcam,ab28364)和兔多克隆抗β连环蛋白抗体1:500(abcam,ab32572)。
9.10.1.6rt-pcr
使用rneasymini试剂盒(qiagen,valencia,ca)从主动脉和肾脏中提取rna。根据厂家的指导在verititermal循环仪(appliedbiosystems)上,1μg的总rna进行dnase处理,使用来自bio-rad(hercules,ca)的iscriptcdna合成试剂盒进行逆转录。使用vectornti(invitrogen,grandisland,ny)或primerexpress(lifetechnologies,grandisland,ny)软件设计引物。在逆转录之后,使用steponeplus实时pcr仪(appliedbiosystems)、来sigma(st.louis)的sybrgreen和来自invitrogen的pcr试剂盒进行实时。每个反应在95℃45秒、和60℃30秒和72℃60秒一式三份进行40个循环。随后是熔化循环,由60℃到95℃逐步提高的温度组成。在每个基因的解离曲线中观察到单一优势峰,支持了pcr产物的特异性。ct数(阈值)在pcr的指数期内设置,用于计算目标基因的表达水平。b2m用作内标准物,归一化所述值。由ct对比logcdna稀释度(相应于log拷贝数)组成的标准曲线通过扩增与未知数量的扩增子相应的cdna的连续稀释物来产生。通过在rt-pcr之前煮沸5分钟来确保基因组dna不被扩增,通过灭活逆转录酶来进行阴性对照。
9.10.1.7免疫印迹(western分析)
使用含有蛋白酶抑制剂混合物(santacruz)的ripa裂解缓冲液(thermoscientific),从小鼠的肾脏和主动脉制备全细胞溶胞产物蛋白.溶胞产物(20μg)装载到8-12%sds-page凝胶中,用针对抑制素β-a(santacruz)、α-微管蛋白(santacruz)、actin-α平滑肌(sigma)、runx2(cellsignaling)、myocd(santacruz)、acvrl1(origene)、acvr1(cellsignaling)、erk1/2(cellsignaling)、磷酸-erk1/2(cellsignaling)、acvr1b(origene)、col1a1(santacruz)、smad2/3(cellsignaling)或磷酸-smad2/3(cellsignaling)的抗体进行免疫印迹。免疫沉淀(ip)分析使用相同的全细胞溶胞产物蛋白。为了降低非特异性结合,使用预洗涤的蛋白a琼脂糖珠子(cellsignaling)预先清洗样品。预清洁的样品与磷酸丝氨酸抗体(abcam)孵育过夜。然后在蛋白a琼脂糖珠子上捕获ip-抗体复合物,通过免疫印迹分析检测蛋白质。
使用anova进行统计分析。所有数据表示为平均值±sd,除非附图图例中另外指定。在使用fisherlsd法之后评估各组之间的差异,p<0.05认为是显著的。所有组的数据有7-15的“n”。对于实时pcr分析,每个实验组中使用最少3个样品。对于附图26c中的血管钙化数据,方框代表中值和百分位范围(25th到75th百分位数),误差线代表低于25th和高于75th百分位数的百分位范围的1.5倍。使用用于多重比较的anovaholm-sidak方法比较中值,p<0.05作为显著差异的临界水平。
9.10.2结果
9.10.2.1实验设计,以及ckd模型中的肾脏
高脂肪饲喂的ldlr-/-小鼠是动脉粥样硬化性血管钙化的模型,需要饮食和基因型两者来产生动脉粥样硬化性血管钙化。(daviesmr,etal.jamsocnephrol2003;14:1559-1567;towlerda,etal.j.biologicalchem.1998;273:30427-30434)。通过肾脏皮层损伤和对侧肾切除,在ldlr-/-高脂肪饲喂小鼠中肾脏功能类似于人3期ckd(ckd-3)降低(附图33a、b)。ckd-3小鼠是高磷酸盐血的(表20),这与人3b-4期ckd中的高磷酸血症发作一致。(isakovat,etal.kidneyint2011;79:1370-1378)。
表20:测试的动物中的血清生化参数
*:<0.05,与组2比较的组3和4。
9.10.2.2ckd中的iia型激活素受体(actriia)水平
分析来自患有ckd-3的高脂肪饲喂ldlr-/-小鼠的主动脉中的tgfβ超家族ii型受体,它们是由ii型和i型(alk)受体组成的超家族受体杂多聚物的一个配体结合部件。激活素ii型受体a(actriia)在主动脉血管平滑肌细胞(vsmc)中表达(附图24a、b)。ldlr-/-高脂肪饲喂小鼠中产生的ckd-3诱导主动脉中的actriia被下调(附图24a)。不受任何特定理论的限制,这与其他组织中报告的高循环配体水平产生的actriia内在化和降解一致。(simonend,etal.endocrinology1998;139:1147-1155;liuzh,etal.j.endocrinology2006;189:409-421).通过免疫化学和免疫荧光检测没有检出内皮细胞actriia(附图24b)。
9.10.2.3ckd中actriia配体陷阱的血管作用
在用溶媒或actriia配体陷阱(mactriia-fc)治疗的ckd-3小鼠的主动脉组织匀浆中分析ckd诱导的actriia水平抑制的影响(附图25a、b)。通过ldlr-/-高脂肪饲喂小鼠的主动脉中runx2和碱性磷酸酶(alpl)的mrna表达来评估ckd-3刺激的成骨细胞转变。ckd-3刺激了它们的表达,mactriia-fc治疗逆转了ckd的影响(附图25a)。runx2和alpl表达都代表了主动脉中成骨细胞转变的生物标记物,其被mactriia-fc治疗逆转。主动脉的平滑肌22α或转胶蛋白(tagln)的mrna,分化血管平滑肌细胞的生物标志物(lil,miano,etal.circulationres.1996;78:188-195),被ckd-3降低,并被mactriia-fc刺激。ckd-3还引起降低的主动脉心肌素(myocd)mrna表达,其是血管平滑肌细胞特异性的转录因子,但是心肌素不受mactriia-fc治疗的影响。就ckd-3和mactriia-fc治疗对附图25a中研究的相应mrna的主动脉蛋白质水平的影响而言,ckd提高主动脉runx2和alpl水平,mactriia-fc归一化它们(附图25b,alpl的数据未显示)。ckd降低tagln和alpha平滑肌肌动蛋白(αsma)的主动脉水平,其是分化的血管平滑肌细胞的另一种生物标志物,mactriia-fc治疗提高它们它们(附图25b,tagln的数据未显示)。心肌素水平不被ckd或mactriia-fc治疗改变。
ldlr-/-高脂肪饲喂小鼠是动脉粥样硬化、动脉粥样硬化性钙化和2型糖尿病的模型。(al-alyz,etal.arteriosclerosis,thrombosis,andvascularbiol.2007;27:2589-2596;towlerda,etal.j.biologicalchem.1998;273:30427-30434)。鉴定出的,特别是,ckd-3引起ckd-3溶媒治疗的小鼠(ckd-3v)的主动脉粥样斑中钙沉积的积累(附图26a),并提高总组织钙水平(附图26b)。在用mactriia-fc治疗的ckd-3小鼠(ckd-3mactriia-fc)中不存在可见的钙沉积。此外,,mactriia-fc将主动脉组织钙含量降低到如同野生型和sham小鼠中观察到的水平,以及比ckd-3组中mactriia-fc治疗开始时表现的水平显著低的水平(附图26b)。
9.10.2.4主动脉中的actriia信号转导
tgfβ超家族的典型的信号转导涉及结合ii型受体的配体活化它们的丝氨酸/苏氨酸激酶活性并刺激i型受体alk激酶的缔合与磷酸化(参见附图34中的示意图)。存在七种被tgfβ超家族利用的alk激酶,alk4(actrib)是与actriia信号转导最常相关的i型受体。(abeymt,etal.growthfactors(chur,switzerland)2004;22:105-110)。如附图24中证明的,在从ckd-3小鼠分离的主动脉组织匀浆中actriia没有降低,并且与alk4和alk1的降低的组织水平不相关(附图27a)。与actriia信号转导相关的其他1型受体,alk5和alk2是不可检测的。通过测量受体杂多聚化效应(例如,调节性smads的磷酸化)来评估actriia活性。ckd-3降低主动脉phosphosmad2/3水平(活化的smad2/3),mactriia-fc相比ckd-3v提高它们(附图27a、b)。还分析了非经典的actriia信号转导(附图34):(1)map激酶(磷酸-erk1/2)被ckd降低,没有进一步受到mactriia-fc的影响(附图27a),(2)p38和jnk的血管平滑肌水平是非常低的。并且,mactriia-fcp-akt水平保持不受影响,表明主动脉akt/pi3激酶不受actriia信号转导的影响。主动脉actriia信号转导(phosphosmad3)被ckd降低,被与actriia配体陷阱在动脉粥样硬化性主动脉中抑制成骨细胞转变相关的actriia配体陷阱刺激(附图25a、b、c)。
检查了另一种非典型的actriia信号转导途径,wnt途径(附图34)。wnt信号转导显现了在主动脉内皮和vsmc之间的差异性调节。主要的典型wnt诱导的转录因子主动脉β-连环蛋白被免疫荧光定位至内皮细胞,在vsmc中是不可检测的(附图28a、b)。分析了vsmc中的dkk1水平作为wnt活性的生物标志物。在ckd-3小鼠中,ckd提高vsmcdkk1水平,mactriia-fc治疗降低dkk1水平(附图28d)。主动脉dkk1水平被mactriia-fc降低表明血管平滑肌wnt信号转导受到actriia配体陷阱的抑制。此外,如下文显示的actriia配体陷阱降低肾脏wnt活性的效应引起了循环dkk1水平的较大的降低(附图28e)。全身性dkk1的降低最有可能影响内皮。这引起内皮中提高的wnt信号转导,其中beta-连环蛋白被表达,如主动脉axin2水平的提高或显示的(附图28c)。axin2是beta-连环蛋白刺激的即时早期基因,常用于评估wnt信号转导。(maoj,wangj,liub,etal.mol.cell2001;7:801-809)。
9.10.2.5actriia配体陷阱对αklotho和肾脏actriia信号转导的影响
检查了肾脏αklotho水平以及ckd-3和mactriia-fc治疗的影响。如附图29a所示,mactriia-fc治疗诱导了肾脏αklotho水平的显著提高。检查了肾脏actriia水平和actriia信号转导。肾脏actriia水平不受ckd-3的影响(附图29b)。主要的actriia配体,激活素a,在ckd-3小鼠中被强烈地诱导,被mactriia-fc治疗抑制(附图31a-d)。缺少可以的磷酸-alk抗体影响了i型受体活化的检测,作为替代需要磷酸丝氨酸抗体来免疫沉淀。用抗alk抗体进行沉淀的免疫印迹。在ckd-3模型的患病肾脏中或通过mactriia-fcmactriia-fc治疗,alk4磷酸化没有显著改变(附图29b)。然而,肾脏的phosphosmad2/3被ckd-3提高,被mactriia-fc降低,表明在ckd通过actriia的介导中肾脏smad2/3活化的部件涉及不同于alk4的alk(附图29c)。
检测了actriia配体陷阱对肾脏纤维化的影响。附图30a-d显示了相比ckd-3v治疗的小鼠(附图30a和附图30b),在来自ckd-3mactriia-fc治疗的小鼠三色染色的肾脏皮层切片中(附图30c和附图30d)降低的肾脏纤维化。附图35a-d显示了低放大率的冠状的肾脏切片,箭头指出了在附图30a-d中采集高功率切片的位置,箭头头部描绘了来自电灼肾脏损伤的瘢痕反应。mactriia-fc降低了瘢痕反应,与激活素在伤口愈合中的作用一致。此外,mactriia-fc降低了ckd-3刺激的蛋白尿(附图30e),与mactriia-fc治疗诱导肾脏phosphosmad2/3和纤维化的降低一致。
9.10.2.6ckd中可能的actriia配体
存在多种可能的actriia配体,包括激活素a和b,生长和分化因子11(gdf11),骨骼形态发生蛋白9和10(bmp9和10),以及其他bmp,例如bmp7,它们具有对受体的更低的亲和力。但是主要的actriia配体是激活素。使用两种ckd模型,鉴定出全身性循环激活素a水平在ldlr-/-消融性ckd模型中有10倍升高,在col4a5alport’s综合征小鼠模型中有5倍提高(附图31a、b)。在这些模型中,激活素b、gdf11和bmp9水平不受ckd影响。生理学上,认为在循环中存在少量游离的激活素。不受任何特定理论的限制,这可能是有感于化学计量地相等于激活素水平的抑制剂水平。激活素与循环抑制因子卵泡抑素和卵泡抑素样3(fstl3)相关(weltc,etal.experimentalbiol.andmed.2002;227:724-752)以及与循环水平和组织水平不受ckd-3的影响或降低的抑制素相关(附图36a、b)在循环中卵泡抑素、fstl3和抑制素(例如,620pg/ml的总和,加上400pg/ml未测出的抑制素(sharperm,etal.j.andrology1999;20:94-101)与激活素a水平(>5000pg/ml)的化学当量表明,ckd产生显著的游离激活素水平,是一种使得激活素a成为ckd中的活性循环因子的病理事件。这一数据表明,肾脏疾病产生一种或更多种循环actriia配体,它们可能下调血管的actriia。
分析来自ldlr-/-动脉粥样硬化性钙化模型的肾脏组织的激活素a(抑制素betaa的同二聚体(inhba))来鉴定提高的循环激活素的来源。在肾脏中inhbamrna被ckd提高(附图31c),激活素(抑制素β-a)蛋白质水平提高(附图31d)。肾脏的激活素表达定位于ckd-3小鼠的管周肌成纤维细胞中(附图32a、b)。
9.10.3结论
这个实施例表明,mactriia-fc提高通过磷酸化的smad2/3的水平评估的主动脉actriia信号转导。此外mactriia-rc治疗逆转了ckd诱导的血管平滑肌去分化、成骨细胞转变和新内膜斑块钙化。在患病肾脏中,mactriia-fc抑制了,而不是刺激了actriia信号转导,并降低肾脏纤维化和蛋白尿。mactriia-fc治疗降低肾脏和循环dkk1水平,表明wnt活化在actriia下游。这个实施例表明,ckd中失调的actriia信号转导促进了ckd-mbd和肾脏纤维化,将actriia信号转导鉴定为ckd的治疗靶点,并表明激活素配体陷阱(例如,mactriia-fc)可以用于ckd的治疗。
10.序列的说明
表21:序列信息
11.等同
虽然参考具体实施方式详细描述了本发明,要理解的是功能上等价的变体处于本发明的范围之内。实际上,根据以上的说明和附图,除了在此显示和描述的之外,本发明的各种修饰对于本领域技术人员而言是显而易见的。这种修改也将落在附随的权利要求的范围之中。本领域的技术人员将认识到或能够利用不超出常规的实验来确定本文描述的本发明的具体实施方式的许多等同形式。这样的等同形式预期由以下权利要求涵盖。
在本说明书中提及的所有出版物、专利和专利申请通过引用合并到本说明书中,达到如同每个单独的出版物、专利或专利申请被具体和分别地指明通过引用完全合并在此的相同程度。
序列表
<110>细胞基因公司
华盛顿大学
<120>利用actrii配体陷阱治疗心血管疾病
<130>12827-934-228
<150>62/062,021
<151>2014-10-09
<150>62/078,321
<151>2014-11-11
<150>62/103,515
<151>2015-01-14
<150>62/167,052
<151>2015-05-27
<150>62/170,015
<151>2015-06-02
<160>87
<170>patentinversion3.5
<210>1
<211>513
<212>prt
<213>智人
<220>
<223>人actriia前体多肽
<400>1
metglyalaalaalalysleualaphealavalpheleuilesercys
151015
serserglyalaileleuglyargsergluthrglnglucysleuphe
202530
pheasnalaasntrpglulysaspargthrasnglnthrglyvalglu
354045
procystyrglyasplysasplysargarghiscysphealathrtrp
505560
lysasnileserglyserilegluilevallysglnglycystrpleu
65707580
aspaspileasncystyraspargthraspcysvalglulyslysasp
859095
serprogluvaltyrphecyscyscysgluglyasnmetcysasnglu
100105110
lysphesertyrpheproglumetgluvalthrglnprothrserasn
115120125
provalthrprolysproprotyrtyrasnileleuleutyrserleu
130135140
valproleumetleuilealaglyilevalilecysalaphetrpval
145150155160
tyrarghishislysmetalatyrproprovalleuvalprothrgln
165170175
aspproglyproproproproserproleuleuglyleulysproleu
180185190
glnleuleugluvallysalaargglyargpheglycysvaltrplys
195200205
alaglnleuleuasnglutyrvalalavallysilepheproilegln
210215220
asplysglnsertrpglnasnglutyrgluvaltyrserleuprogly
225230235240
metlyshisgluasnileleuglnpheileglyalaglulysarggly
245250255
thrservalaspvalaspleutrpleuilethralaphehisglulys
260265270
glyserleuserasppheleulysalaasnvalvalsertrpasnglu
275280285
leucyshisilealagluthrmetalaargglyleualatyrleuhis
290295300
gluaspileproglyleulysaspglyhislysproalaileserhis
305310315320
argaspilelysserlysasnvalleuleulysasnasnleuthrala
325330335
cysilealaasppheglyleualaleulyspheglualaglylysser
340345350
alaglyaspthrhisglyglnvalglythrargargtyrmetalapro
355360365
gluvalleugluglyalaileasnpheglnargaspalapheleuarg
370375380
ileaspmettyralametglyleuvalleutrpgluleualaserarg
385390395400
cysthralaalaaspglyprovalaspglutyrmetleupropheglu
405410415
glugluileglyglnhisproserleugluaspmetglngluvalval
420425430
valhislyslyslysargprovalleuargasptyrtrpglnlyshis
435440445
alaglymetalametleucysgluthrilegluglucystrpasphis
450455460
aspalaglualaargleuseralaglycysvalglygluargilethr
465470475480
glnmetglnargleuthrasnileilethrthrgluaspilevalthr
485490495
valvalthrmetvalthrasnvalasppheproprolysgluserser
500505510
leu
<210>2
<211>115
<212>prt
<213>智人
<220>
<223>人actriia可溶的(细胞外的),加工的多肽序列
<400>2
ileleuglyargsergluthrglnglucysleuphepheasnalaasn
151015
trpglulysaspargthrasnglnthrglyvalgluprocystyrgly
202530
asplysasplysargarghiscysphealathrtrplysasnileser
354045
glyserilegluilevallysglnglycystrpleuaspaspileasn
505560
cystyraspargthraspcysvalglulyslysaspserprogluval
65707580
tyrphecyscyscysgluglyasnmetcysasnglulysphesertyr
859095
pheproglumetgluvalthrglnprothrserasnprovalthrpro
100105110
lyspropro
115
<210>3
<211>100
<212>prt
<213>人工序列
<220>
<223>人actriia可溶的(细胞外的),c-末端15个氨基酸删除的加工的多肽
序列
<400>3
ileleuglyargsergluthrglnglucysleuphepheasnalaasn
151015
trpglulysaspargthrasnglnthrglyvalgluprocystyrgly
202530
asplysasplysargarghiscysphealathrtrplysasnileser
354045
glyserilegluilevallysglnglycystrpleuaspaspileasn
505560
cystyraspargthraspcysvalglulyslysaspserprogluval
65707580
tyrphecyscyscysgluglyasnmetcysasnglulysphesertyr
859095
pheproglumet
100
<210>4
<211>1542
<212>dna
<213>智人
<220>
<223>编码人actriia前体蛋白的核酸序列
<400>4
atgggagctgctgcaaagttggcgtttgccgtctttcttatctcctgttcttcaggtgct60
atacttggtagatcagaaactcaggagtgtcttttctttaatgctaattgggaaaaagac120
agaaccaatcaaactggtgttgaaccgtgttatggtgacaaagataaacggcggcattgt180
tttgctacctggaagaatatttctggttccattgaaatagtgaaacaaggttgttggctg240
gatgatatcaactgctatgacaggactgattgtgtagaaaaaaaagacagccctgaagta300
tatttttgttgctgtgagggcaatatgtgtaatgaaaagttttcttattttccagagatg360
gaagtcacacagcccacttcaaatccagttacacctaagccaccctattacaacatcctg420
ctctattccttggtgccacttatgttaattgcggggattgtcatttgtgcattttgggtg480
tacaggcatcacaagatggcctaccctcctgtacttgttccaactcaagacccaggacca540
cccccaccttctccattactagggttgaaaccactgcagttattagaagtgaaagcaagg600
ggaagatttggttgtgtctggaaagcccagttgcttaacgaatatgtggctgtcaaaata660
tttccaatacaggacaaacagtcatggcaaaatgaatacgaagtctacagtttgcctgga720
atgaagcatgagaacatattacagttcattggtgcagaaaaacgaggcaccagtgttgat780
gtggatctttggctgatcacagcatttcatgaaaagggttcactatcagactttcttaag840
gctaatgtggtctcttggaatgaactgtgtcatattgcagaaaccatggctagaggattg900
gcatatttacatgaggatatacctggcctaaaagatggccacaaacctgccatatctcac960
agggacatcaaaagtaaaaatgtgctgttgaaaaacaacctgacagcttgcattgctgac1020
tttgggttggccttaaaatttgaggctggcaagtctgcaggcgatacccatggacaggtt1080
ggtacccggaggtacatggctccagaggtattagagggtgctataaacttcgaaagggat1140
gcatttttgaggatagatatgtatgccatgggattagtcctatgggaactggcttctcgc1200
tgtactgctgcagatggacctgtagatgaatacatgttgccatttgaggaggaaattggc1260
cagcatccatctcttgaagacatgcaggaagttgttgtgcataaaaaaaagaggcctgtt1320
ttaagagattattggcagaaacatgctggaatggcaatgctctgtgaaaccattgaagaa1380
tgttgggatcacgacgcagaagccaggttatcagctggatgtgtaggtgaaagaattacc1440
cagatgcagagactaacaaatattattaccacagaggacattgtaacagtggtcacaatg1500
gtgacaaatgttgactttcctcccaaagaatctagtctatga1542
<210>5
<211>345
<212>dna
<213>智人
<220>
<223>编码人actriia可溶的(细胞外的)多肽的核酸序列
<400>5
atacttggtagatcagaaactcaggagtgtcttttctttaatgctaattgggaaaaagac60
agaaccaatcaaactggtgttgaaccgtgttatggtgacaaagataaacggcggcattgt120
tttgctacctggaagaatatttctggttccattgaaatagtgaaacaaggttgttggctg180
gatgatatcaactgctatgacaggactgattgtgtagaaaaaaaagacagccctgaagta240
tatttttgttgctgtgagggcaatatgtgtaatgaaaagttttcttattttccagagatg300
gaagtcacacagcccacttcaaatccagttacacctaagccaccc345
<210>6
<211>228
<212>prt
<213>人工序列
<220>
<223>包含与fc结构域融合的actriia的可溶细胞外结构域的融合蛋白
<220>
<221>misc_feature
<222>(44)..(44)
<223>xaa=asp或ala
<220>
<221>misc_feature
<222>(102)..(102)
<223>xaa=lys或ala
<220>
<221>misc_feature
<222>(215)..(215)
<223>xaa=asn或ala
<400>6
thrhisthrcysproprocysproalaprogluleuleuglyglypro
151015
servalpheleupheproprolysprolysaspthrleumetileser
202530
argthrprogluvalthrcysvalvalvalaspxaavalserhisglu
354045
aspprogluvallyspheasntrptyrvalaspglyvalgluvalhis
505560
asnalalysthrlysproargglugluglntyrasnserthrtyrarg
65707580
valvalservalleuthrvalleuhisglnasptrpleuasnglylys
859095
glutyrlyscyslysxaavalserasnlysalaleuprovalproile
100105110
glulysthrileserlysalalysglyglnproarggluproglnval
115120125
tyrthrleuproproserarggluglumetthrlysasnglnvalser
130135140
leuthrcysleuvallysglyphetyrproseraspilealavalglu
145150155160
trpgluserasnglyglnprogluasnasntyrlysthrthrpropro
165170175
valleuaspseraspglyprophepheleutyrserlysleuthrval
180185190
asplysserargtrpglnglnglyasnvalphesercysservalmet
195200205
hisglualaleuhisasnxaahistyrthrglnlysserleuserleu
210215220
serproglylys
225
<210>7
<211>344
<212>prt
<213>人工序列
<220>
<223>与人fc结构域融合的人actriia的细胞外结构域
<400>7
ileleuglyargsergluthrglnglucysleuphepheasnalaasn
151015
trpglulysaspargthrasnglnthrglyvalgluprocystyrgly
202530
asplysasplysargarghiscysphealathrtrplysasnileser
354045
glyserilegluilevallysglnglycystrpleuaspaspileasn
505560
cystyraspargthraspcysvalglulyslysaspserprogluval
65707580
tyrphecyscyscysgluglyasnmetcysasnglulysphesertyr
859095
pheproglumetgluvalthrglnprothrserasnprovalthrpro
100105110
lysproprothrglyglyglythrhisthrcysproprocysproala
115120125
progluleuleuglyglyproservalpheleupheproprolyspro
130135140
lysaspthrleumetileserargthrprogluvalthrcysvalval
145150155160
valaspvalserhisgluaspprogluvallyspheasntrptyrval
165170175
aspglyvalgluvalhisasnalalysthrlysproarggluglugln
180185190
tyrasnserthrtyrargvalvalservalleuthrvalleuhisgln
195200205
asptrpleuasnglylysglutyrlyscyslysvalserasnlysala
210215220
leuprovalproileglulysthrileserlysalalysglyglnpro
225230235240
arggluproglnvaltyrthrleuproproserarggluglumetthr
245250255
lysasnglnvalserleuthrcysleuvallysglyphetyrproser
260265270
aspilealavalglutrpgluserasnglyglnprogluasnasntyr
275280285
lysthrthrproprovalleuaspseraspglyserphepheleutyr
290295300
serlysleuthrvalasplysserargtrpglnglnglyasnvalphe
305310315320
sercysservalmethisglualaleuhisasnhistyrthrglnlys
325330335
serleuserleuserproglylys
340
<210>8
<211>21
<212>prt
<213>人工序列
<220>
<223>蜜蜂蜂毒(hbml)的前导序列
<400>8
metlyspheleuvalasnvalalaleuvalphemetvalvaltyrile
151015
sertyriletyrala
20
<210>9
<211>22
<212>prt
<213>人工序列
<220>
<223>组织纤溶酶原激活物(tpa)的前导序列
<400>9
metaspalametlysargglyleucyscysvalleuleuleucysgly
151015
alavalphevalserpro
20
<210>10
<211>20
<212>prt
<213>未知
<220>
<223>天然actriia前导区
<400>10
metglyalaalaalalysleualaphealavalpheleuilesercys
151015
serserglyala
20
<210>11
<211>9
<212>prt
<213>人工序列
<220>
<223>actriia-hfc和mactriia-fcn-末端序列
<400>11
ileleuglyargsergluthrglnglu
15
<210>12
<211>329
<212>prt
<213>人工序列
<220>
<223>具有actriia的细胞外结构域的c-末端15个氨基酸删除的actriia-fc蛋白
<400>12
ileleuglyargsergluthrglnglucysleuphepheasnalaasn
151015
trpglulysaspargthrasnglnthrglyvalgluprocystyrgly
202530
asplysasplysargarghiscysphealathrtrplysasnileser
354045
glyserilegluilevallysglnglycystrpleuaspaspileasn
505560
cystyraspargthraspcysvalglulyslysaspserprogluval
65707580
tyrphecyscyscysgluglyasnmetcysasnglulysphesertyr
859095
pheproglumetthrglyglyglythrhisthrcysproprocyspro
100105110
alaprogluleuleuglyglyproservalpheleupheproprolys
115120125
prolysaspthrleumetileserargthrprogluvalthrcysval
130135140
valvalaspvalserhisgluaspprogluvallyspheasntrptyr
145150155160
valaspglyvalgluvalhisasnalalysthrlysproarggluglu
165170175
glntyrasnserthrtyrargvalvalservalleuthrvalleuhis
180185190
glnasptrpleuasnglylysglutyrlyscyslysvalserasnlys
195200205
alaleuprovalproileglulysthrileserlysalalysglygln
210215220
proarggluproglnvaltyrthrleuproproserarggluglumet
225230235240
thrlysasnglnvalserleuthrcysleuvallysglyphetyrpro
245250255
seraspilealavalglutrpgluserasnglyglnprogluasnasn
260265270
tyrlysthrthrproprovalleuaspseraspglyserphepheleu
275280285
tyrserlysleuthrvalasplysserargtrpglnglnglyasnval
290295300
phesercysservalmethisglualaleuhisasnhistyrthrgln
305310315320
lysserleuserleuserproglylys
325
<210>13
<211>369
<212>prt
<213>人工序列
<220>
<223>带有tpa前导序列的未加工的actriia-hfc
<400>13
metaspalametlysargglyleucyscysvalleuleuleucysgly
151015
alavalphevalserproglyalaalaileleuglyargsergluthr
202530
glnglucysleuphepheasnalaasntrpglulysaspargthrasn
354045
glnthrglyvalgluprocystyrglyasplysasplysargarghis
505560
cysphealathrtrplysasnileserglyserilegluilevallys
65707580
glnglycystrpleuaspaspileasncystyraspargthraspcys
859095
valglulyslysaspserprogluvaltyrphecyscyscysglugly
100105110
asnmetcysasnglulysphesertyrpheproglumetgluvalthr
115120125
glnprothrserasnprovalthrprolysproprothrglyglygly
130135140
thrhisthrcysproprocysproalaprogluleuleuglyglypro
145150155160
servalpheleupheproprolysprolysaspthrleumetileser
165170175
argthrprogluvalthrcysvalvalvalaspvalserhisgluasp
180185190
progluvallyspheasntrptyrvalaspglyvalgluvalhisasn
195200205
alalysthrlysproargglugluglntyrasnserthrtyrargval
210215220
valservalleuthrvalleuhisglnasptrpleuasnglylysglu
225230235240
tyrlyscyslysvalserasnlysalaleuprovalproileglulys
245250255
thrileserlysalalysglyglnproarggluproglnvaltyrthr
260265270
leuproproserarggluglumetthrlysasnglnvalserleuthr
275280285
cysleuvallysglyphetyrproseraspilealavalglutrpglu
290295300
serasnglyglnprogluasnasntyrlysthrthrproprovalleu
305310315320
aspseraspglyserphepheleutyrserlysleuthrvalasplys
325330335
serargtrpglnglnglyasnvalphesercysservalmethisglu
340345350
alaleuhisasnhistyrthrglnlysserleuserleuserprogly
355360365
lys
<210>14
<211>1113
<212>dna
<213>人工序列
<220>
<223>编码带有tpa前导序列的未加工的actriia-hfc的核酸序列
<400>14
atggatgcaatgaagagagggctctgctgtgtgctgctgctgtgtggagcagtcttcgtt60
tcgcccggcgccgctatacttggtagatcagaaactcaggagtgtctttttttaatgcta120
attgggaaaaagacagaaccaatcaaactggtgttgaaccgtgttatggtgacaaagata180
aacggcggcattgttttgctacctggaagaatatttctggttccattgaatagtgaaaca240
aggttgttggctggatgatatcaactgctatgacaggactgattgtgtagaaaaaaaaga300
cagccctgaagtatatttctgttgctgtgagggcaatatgtgtaatgaaaagttttctta360
ttttccggagatggaagtcacacagcccacttcaaatccagttacacctaagccacccac420
cggtggtggaactcacacatgcccaccgtgcccagcacctgaactcctggggggaccgtc480
agtcttcctcttccccccaaaacccaaggacaccctcatgatctcccggacccctgaggt540
cacatgcgtggtggtggacgtgagccacgaagaccctgaggtcaagttcaactggtacgt600
ggacggcgtggaggtgcataatgccaagacaaagccgcgggaggagcagtacaacagcac660
gtaccgtgtggtcagcgtcctcaccgtcctgcaccaggactggctgaatggcaaggagta720
caagtgcaaggtctccaacaaagccctcccagtccccatcgagaaaaccatctccaaagc780
caaagggcagccccgagaaccacaggtgtacaccctgcccccatcccgggaggagatgac840
caagaaccaggtcagcctgacctgcctggtcaaaggcttctatcccagcgacatcgccgt900
ggagtgggagagcaatgggcagccggagaacaactacaagaccacgcctcccgtgctgga960
ctccgacggctccttcttcctctatagcaagctcaccgtggacaagagcaggtggcagca1020
ggggaacgtcttctcatgctccgtgatgcatgaggctctgcacaaccactacacgcagaa1080
gagcctctccctgtctccggtaaatgagaattc1113
<210>15
<211>106
<212>prt
<213>人工序列
<220>
<223>人actriib可溶的(细胞外的),ec结构域的n-末端6个氨基酸删除、ec结构域的c-末端4个氨基酸删除(seqidno:28的氨基酸25-130)、具有l79d突变的加工的多肽序列
<400>15
gluthrargglucysiletyrtyrasnalaasntrpgluleugluarg
151015
thrasnglnserglyleugluargcysgluglygluglnasplysarg
202530
leuhiscystyralasertrpargasnserserglythrilegluleu
354045
vallyslysglycystrpaspaspasppheasncystyrasparggln
505560
glucysvalalathrglugluasnproglnvaltyrphecyscyscys
65707580
gluglyasnphecysasngluargphethrhisleuproglualagly
859095
glyprogluvalthrtyrglupropropro
100105
<210>16
<211>512
<212>prt
<213>智人
<220>
<223>人actriib前体蛋白序列(a64)
<400>16
metthralaprotrpvalalaleualaleuleutrpglyserleutrp
151015
proglyserglyargglyglualagluthrargglucysiletyrtyr
202530
asnalaasntrpgluleugluargthrasnglnserglyleugluarg
354045
cysgluglygluglnasplysargleuhiscystyralasertrpala
505560
asnserserglythrilegluleuvallyslysglycystrpleuasp
65707580
asppheasncystyraspargglnglucysvalalathrglugluasn
859095
proglnvaltyrphecyscyscysgluglyasnphecysasngluarg
100105110
phethrhisleuproglualaglyglyprogluvalthrtyrglupro
115120125
proprothralaprothrleuleuthrvalleualatyrserleuleu
130135140
proileglyglyleuserleuilevalleuleualaphetrpmettyr
145150155160
arghisarglysproprotyrglyhisvalaspilehisgluasppro
165170175
glyproproproproserproleuvalglyleulysproleuglnleu
180185190
leugluilelysalaargglyargpheglycysvaltrplysalagln
195200205
leumetasnaspphevalalavallysilepheproleuglnasplys
210215220
glnsertrpglnsergluarggluilepheserthrproglymetlys
225230235240
hisgluasnleuleuglnpheilealaalaglulysargglyserasn
245250255
leugluvalgluleutrpleuilethralaphehisasplysglyser
260265270
leuthrasptyrleulysglyasnileilethrtrpasngluleucys
275280285
hisvalalagluthrmetserargglyleusertyrleuhisgluasp
290295300
valprotrpcysargglygluglyhislysproserilealahisarg
305310315320
aspphelysserlysasnvalleuleulysseraspleuthralaval
325330335
leualaasppheglyleualavalargphegluproglylyspropro
340345350
glyaspthrhisglyglnvalglythrargargtyrmetalaproglu
355360365
valleugluglyalaileasnpheglnargaspalapheleuargile
370375380
aspmettyralametglyleuvalleutrpgluleuvalserargcys
385390395400
lysalaalaaspglyprovalaspglutyrmetleuprophegluglu
405410415
gluileglyglnhisproserleuglugluleuglngluvalvalval
420425430
hislyslysmetargprothrilelysasphistrpleulyshispro
435440445
glyleualaglnleucysvalthrilegluglucystrpasphisasp
450455460
alaglualaargleuseralaglycysvalglugluargvalserleu
465470475480
ileargargservalasnglythrthrseraspcysleuvalserleu
485490495
valthrservalthrasnvalaspleuproprolysgluserserile
500505510
<210>17
<211>116
<212>prt
<213>人工序列
<220>
<223>人actriib可溶的(细胞外的),加工的多肽序列(seqidno:16的氨基酸19-134)
<400>17
serglyargglyglualagluthrargglucysiletyrtyrasnala
151015
asntrpgluleugluargthrasnglnserglyleugluargcysglu
202530
glygluglnasplysargleuhiscystyralasertrpalaasnser
354045
serglythrilegluleuvallyslysglycystrpleuaspaspphe
505560
asncystyraspargglnglucysvalalathrglugluasnprogln
65707580
valtyrphecyscyscysgluglyasnphecysasngluargphethr
859095
hisleuproglualaglyglyprogluvalthrtyrglupropropro
100105110
thralaprothr
115
<210>18
<211>101
<212>prt
<213>人工序列
<220>
<223>人actriib可溶的(细胞外的),c-末端15个氨基酸删除的加工的多肽序列(seqidno:16的氨基酸19-119)
<400>18
serglyargglyglualagluthrargglucysiletyrtyrasnala
151015
asntrpgluleugluargthrasnglnserglyleugluargcysglu
202530
glygluglnasplysargleuhiscystyralasertrpalaasnser
354045
serglythrilegluleuvallyslysglycystrpleuaspaspphe
505560
asncystyraspargglnglucysvalalathrglugluasnprogln
65707580
valtyrphecyscyscysgluglyasnphecysasngluargphethr
859095
hisleuprogluala
100
<210>19
<211>1539
<212>dna
<213>智人
<220>
<223>编码人actriib(a64)前体蛋白的核酸序列
<400>19
atgacggcgccctgggtggccctcgccctcctctggggatcgctgtggcccggctctggg60
cgtggggaggctgagacacgggagtgcatctactacaacgccaactgggagctggagcgc120
accaaccagagcggcctggagcgctgcgaaggcgagcaggacaagcggctgcactgctac180
gcctcctgggccaacagctctggcaccatcgagctcgtgaagaagggctgctggctagat240
gacttcaactgctacgataggcaggagtgtgtggccactgaggagaacccccaggtgtac300
ttctgctgctgtgaaggcaacttctgcaacgagcgcttcactcatttgccagaggctggg360
ggcccggaagtcacgtacgagccacccccgacagcccccaccctgctcacggtgctggcc420
tactcactgctgcccatcgggggcctttccctcatcgtcctgctggccttttggatgtac480
cggcatcgcaagcccccctacggtcatgtggacatccatgaggaccctgggcctccacca540
ccatcccctctggtgggcctgaagccactgcagctgctggagatcaaggctcgggggcgc600
tttggctgtgtctggaaggcccagctcatgaatgactttgtagctgtcaagatcttccca660
ctccaggacaagcagtcgtggcagagtgaacgggagatcttcagcacacctggcatgaag720
cacgagaacctgctacagttcattgctgccgagaagcgaggctccaacctcgaagtagag780
ctgtggctcatcacggccttccatgacaagggctccctcacggattacctcaaggggaac840
atcatcacatggaacgaactgtgtcatgtagcagagacgatgtcacgaggcctctcatac900
ctgcatgaggatgtgccctggtgccgtggcgagggccacaagccgtctattgcccacagg960
gactttaaaagtaagaatgtattgctgaagagcgacctcacagccgtgctggctgacttt1020
ggcttggctgttcgatttgagccagggaaacctccaggggacacccacggacaggtaggc1080
acgagacggtacatggctcctgaggtgctcgagggagccatcaacttccagagagatgcc1140
ttcctgcgcattgacatgtatgccatggggttggtgctgtgggagcttgtgtctcgctgc1200
aaggctgcagacggacccgtggatgagtacatgctgccctttgaggaagagattggccag1260
cacccttcgttggaggagctgcaggaggtggtggtgcacaagaagatgaggcccaccatt1320
aaagatcactggttgaaacacccgggcctggcccagctttgtgtgaccatcgaggagtgc1380
tgggaccatgatgcagaggctcgcttgtccgcgggctgtgtggaggagcgggtgtccctg1440
attcggaggtcggtcaacggcactacctcggactgtctcgtttccctggtgacctctgtc1500
accaatgtggacctgccccctaaagagtcaagcatctaa1539
<210>20
<211>344
<212>prt
<213>人工序列
<220>
<223>包含与fc结构域融合的actriib的可溶的细胞外结构域(a64;seqidno:17)的融合蛋白
<400>20
serglyargglyglualagluthrargglucysiletyrtyrasnala
151015
asntrpgluleugluargthrasnglnserglyleugluargcysglu
202530
glygluglnasplysargleuhiscystyralasertrpalaasnser
354045
serglythrilegluleuvallyslysglycystrpleuaspaspphe
505560
asncystyraspargglnglucysvalalathrglugluasnprogln
65707580
valtyrphecyscyscysgluglyasnphecysasngluargphethr
859095
hisleuproglualaglyglyprogluvalthrtyrglupropropro
100105110
thralaprothrglyglyglythrhisthrcysproprocysproala
115120125
progluleuleuglyglyproservalpheleupheproprolyspro
130135140
lysaspthrleumetileserargthrprogluvalthrcysvalval
145150155160
valaspvalserhisgluaspprogluvallyspheasntrptyrval
165170175
aspglyvalgluvalhisasnalalysthrlysproarggluglugln
180185190
tyrasnserthrtyrargvalvalservalleuthrvalleuhisgln
195200205
asptrpleuasnglylysglutyrlyscyslysvalserasnlysala
210215220
leuprovalproileglulysthrileserlysalalysglyglnpro
225230235240
arggluproglnvaltyrthrleuproproserarggluglumetthr
245250255
lysasnglnvalserleuthrcysleuvallysglyphetyrproser
260265270
aspilealavalglutrpgluserasnglyglnprogluasnasntyr
275280285
lysthrthrproprovalleuaspseraspglyserphepheleutyr
290295300
serlysleuthrvalasplysserargtrpglnglnglyasnvalphe
305310315320
sercysservalmethisglualaleuhisasnhistyrthrglnlys
325330335
serleuserleuserproglylys
340
<210>21
<211>329
<212>prt
<213>人工序列
<220>
<223>包含与fc结构域融合的、带有c-末端15个氨基酸删除的(seqidno:18)actriib的可溶的细胞外结构域(a64)的融合蛋白
<400>21
serglyargglyglualagluthrargglucysiletyrtyrasnala
151015
asntrpgluleugluargthrasnglnserglyleugluargcysglu
202530
glygluglnasplysargleuhiscystyralasertrpalaasnser
354045
serglythrilegluleuvallyslysglycystrpleuaspaspphe
505560
asncystyraspargglnglucysvalalathrglugluasnprogln
65707580
valtyrphecyscyscysgluglyasnphecysasngluargphethr
859095
hisleuproglualaglyglyglythrhisthrcysproprocyspro
100105110
alaprogluleuleuglyglyproservalpheleupheproprolys
115120125
prolysaspthrleumetileserargthrprogluvalthrcysval
130135140
valvalaspvalserhisgluaspprogluvallyspheasntrptyr
145150155160
valaspglyvalgluvalhisasnalalysthrlysproarggluglu
165170175
glntyrasnserthrtyrargvalvalservalleuthrvalleuhis
180185190
glnasptrpleuasnglylysglutyrlyscyslysvalserasnlys
195200205
alaleuprovalproileglulysthrileserlysalalysglygln
210215220
proarggluproglnvaltyrthrleuproproserarggluglumet
225230235240
thrlysasnglnvalserleuthrcysleuvallysglyphetyrpro
245250255
seraspilealavalglutrpgluserasnglyglnprogluasnasn
260265270
tyrlysthrthrproprovalleuaspseraspglyserphepheleu
275280285
tyrserlysleuthrvalasplysserargtrpglnglnglyasnval
290295300
phesercysservalmethisglualaleuhisasnhistyrthrgln
305310315320
lysserleuserleuserproglylys
325
<210>22
<211>105
<212>prt
<213>人工序列
<220>
<223>人actriib可溶的(细胞外的),ec结构域的n-末端6个氨基酸删除、ec结构域的c-末端5个氨基酸删除(seqidno:28的氨基酸25-129)且具有l79d突变的加工的多肽序列
<400>22
gluthrargglucysiletyrtyrasnalaasntrpgluleugluarg
151015
thrasnglnserglyleugluargcysgluglygluglnasplysarg
202530
leuhiscystyralasertrpargasnserserglythrilegluleu
354045
vallyslysglycystrpaspaspasppheasncystyrasparggln
505560
glucysvalalathrglugluasnproglnvaltyrphecyscyscys
65707580
gluglyasnphecysasngluargphethrhisleuproglualagly
859095
glyprogluvalthrtyrglupropro
100105
<210>23
<211>107
<212>prt
<213>人工序列
<220>
<223>人actriib可溶的(细胞外的),ec结构域的n-末端6个氨基酸删除、ec结构域的c-末端3个氨基酸删除(seqidno:28的氨基酸25-131)、具有l79d突变的加工的多肽序列
<400>23
gluthrargglucysiletyrtyrasnalaasntrpgluleugluarg
151015
thrasnglnserglyleugluargcysgluglygluglnasplysarg
202530
leuhiscystyralasertrpargasnserserglythrilegluleu
354045
vallyslysglycystrpaspaspasppheasncystyrasparggln
505560
glucysvalalathrglugluasnproglnvaltyrphecyscyscys
65707580
gluglyasnphecysasngluargphethrhisleuproglualagly
859095
glyprogluvalthrtyrgluproproprothr
100105
<210>24
<211>360
<212>prt
<213>人工序列
<220>
<223>ec结构域的n-末端6个氨基酸删除、ec结构域的c-末端3个氨基酸删除(seqidno:28的氨基酸25-131)、具有l79d突变并具有tpa前导序列的未加工的actriib-fc融合蛋白
<400>24
metaspalametlysargglyleucyscysvalleuleuleucysgly
151015
alavalphevalserproglyalaalagluthrargglucysiletyr
202530
tyrasnalaasntrpgluleugluargthrasnglnserglyleuglu
354045
argcysgluglygluglnasplysargleuhiscystyralasertrp
505560
argasnserserglythrilegluleuvallyslysglycystrpasp
65707580
aspasppheasncystyraspargglnglucysvalalathrgluglu
859095
asnproglnvaltyrphecyscyscysgluglyasnphecysasnglu
100105110
argphethrhisleuproglualaglyglyprogluvalthrtyrglu
115120125
proproprothrglyglyglythrhisthrcysproprocysproala
130135140
progluleuleuglyglyproservalpheleupheproprolyspro
145150155160
lysaspthrleumetileserargthrprogluvalthrcysvalval
165170175
valaspvalserhisgluaspprogluvallyspheasntrptyrval
180185190
aspglyvalgluvalhisasnalalysthrlysproarggluglugln
195200205
tyrasnserthrtyrargvalvalservalleuthrvalleuhisgln
210215220
asptrpleuasnglylysglutyrlyscyslysvalserasnlysala
225230235240
leuproalaproileglulysthrileserlysalalysglyglnpro
245250255
arggluproglnvaltyrthrleuproproserarggluglumetthr
260265270
lysasnglnvalserleuthrcysleuvallysglyphetyrproser
275280285
aspilealavalglutrpgluserasnglyglnprogluasnasntyr
290295300
lysthrthrproprovalleuaspseraspglyserphepheleutyr
305310315320
serlysleuthrvalasplysserargtrpglnglnglyasnvalphe
325330335
sercysservalmethisglualaleuhisasnhistyrthrglnlys
340345350
serleuserleuserproglylys
355360
<210>25
<211>335
<212>prt
<213>人工序列
<220>
<223>ec结构域的n-末端6个氨基酸删除、ec结构域的c-末端3个氨基酸删除(seqidno:28的氨基酸25-131)、具有l79d突变的加工的actriib-fc融合蛋白
<400>25
gluthrargglucysiletyrtyrasnalaasntrpgluleugluarg
151015
thrasnglnserglyleugluargcysgluglygluglnasplysarg
202530
leuhiscystyralasertrpargasnserserglythrilegluleu
354045
vallyslysglycystrpaspaspasppheasncystyrasparggln
505560
glucysvalalathrglugluasnproglnvaltyrphecyscyscys
65707580
gluglyasnphecysasngluargphethrhisleuproglualagly
859095
glyprogluvalthrtyrgluproproprothrglyglyglythrhis
100105110
thrcysproprocysproalaprogluleuleuglyglyproserval
115120125
pheleupheproprolysprolysaspthrleumetileserargthr
130135140
progluvalthrcysvalvalvalaspvalserhisgluaspproglu
145150155160
vallyspheasntrptyrvalaspglyvalgluvalhisasnalalys
165170175
thrlysproargglugluglntyrasnserthrtyrargvalvalser
180185190
valleuthrvalleuhisglnasptrpleuasnglylysglutyrlys
195200205
cyslysvalserasnlysalaleuproalaproileglulysthrile
210215220
serlysalalysglyglnproarggluproglnvaltyrthrleupro
225230235240
proserarggluglumetthrlysasnglnvalserleuthrcysleu
245250255
vallysglyphetyrproseraspilealavalglutrpgluserasn
260265270
glyglnprogluasnasntyrlysthrthrproprovalleuaspser
275280285
aspglyserphepheleutyrserlysleuthrvalasplysserarg
290295300
trpglnglnglyasnvalphesercysservalmethisglualaleu
305310315320
hisasnhistyrthrglnlysserleuserleuserproglylys
325330335
<210>26
<211>115
<212>prt
<213>人工序列
<220>
<223>人actriib可溶的(细胞外的),加工的多肽序列(seqidno:16的氨基酸20-134)
<400>26
glyargglyglualagluthrargglucysiletyrtyrasnalaasn
151015
trpgluleugluargthrasnglnserglyleugluargcysglugly
202530
gluglnasplysargleuhiscystyralasertrpalaasnserser
354045
glythrilegluleuvallyslysglycystrpleuaspasppheasn
505560
cystyraspargglnglucysvalalathrglugluasnproglnval
65707580
tyrphecyscyscysgluglyasnphecysasngluargphethrhis
859095
leuproglualaglyglyprogluvalthrtyrgluproproprothr
100105110
alaprothr
115
<210>27
<211>100
<212>prt
<213>人工序列
<220>
<223>人actriib可溶的(细胞外的),c-末端15个氨基酸删除的加工的多肽序列(seqidno:16的氨基酸20-119)
<400>27
glyargglyglualagluthrargglucysiletyrtyrasnalaasn
151015
trpgluleugluargthrasnglnserglyleugluargcysglugly
202530
gluglnasplysargleuhiscystyralasertrpalaasnserser
354045
glythrilegluleuvallyslysglycystrpleuaspasppheasn
505560
cystyraspargglnglucysvalalathrglugluasnproglnval
65707580
tyrphecyscyscysgluglyasnphecysasngluargphethrhis
859095
leuprogluala
100
<210>28
<211>512
<212>prt
<213>智人
<220>
<223>人actriib前体蛋白序列(r64)
<400>28
metthralaprotrpvalalaleualaleuleutrpglyserleutrp
151015
proglyserglyargglyglualagluthrargglucysiletyrtyr
202530
asnalaasntrpgluleugluargthrasnglnserglyleugluarg
354045
cysgluglygluglnasplysargleuhiscystyralasertrparg
505560
asnserserglythrilegluleuvallyslysglycystrpleuasp
65707580
asppheasncystyraspargglnglucysvalalathrglugluasn
859095
proglnvaltyrphecyscyscysgluglyasnphecysasngluarg
100105110
phethrhisleuproglualaglyglyprogluvalthrtyrglupro
115120125
proprothralaprothrleuleuthrvalleualatyrserleuleu
130135140
proileglyglyleuserleuilevalleuleualaphetrpmettyr
145150155160
arghisarglysproprotyrglyhisvalaspilehisgluasppro
165170175
glyproproproproserproleuvalglyleulysproleuglnleu
180185190
leugluilelysalaargglyargpheglycysvaltrplysalagln
195200205
leumetasnaspphevalalavallysilepheproleuglnasplys
210215220
glnsertrpglnsergluarggluilepheserthrproglymetlys
225230235240
hisgluasnleuleuglnpheilealaalaglulysargglyserasn
245250255
leugluvalgluleutrpleuilethralaphehisasplysglyser
260265270
leuthrasptyrleulysglyasnileilethrtrpasngluleucys
275280285
hisvalalagluthrmetserargglyleusertyrleuhisgluasp
290295300
valprotrpcysargglygluglyhislysproserilealahisarg
305310315320
aspphelysserlysasnvalleuleulysseraspleuthralaval
325330335
leualaasppheglyleualavalargphegluproglylyspropro
340345350
glyaspthrhisglyglnvalglythrargargtyrmetalaproglu
355360365
valleugluglyalaileasnpheglnargaspalapheleuargile
370375380
aspmettyralametglyleuvalleutrpgluleuvalserargcys
385390395400
lysalaalaaspglyprovalaspglutyrmetleuprophegluglu
405410415
gluileglyglnhisproserleuglugluleuglngluvalvalval
420425430
hislyslysmetargprothrilelysasphistrpleulyshispro
435440445
glyleualaglnleucysvalthrilegluglucystrpasphisasp
450455460
alaglualaargleuseralaglycysvalglugluargvalserleu
465470475480
ileargargservalasnglythrthrseraspcysleuvalserleu
485490495
valthrservalthrasnvalaspleuproprolysgluserserile
500505510
<210>29
<211>116
<212>prt
<213>人工序列
<220>
<223>人actriib可溶的(细胞外的),加工的多肽序列(seqidno:28的氨基酸19-134)
<400>29
serglyargglyglualagluthrargglucysiletyrtyrasnala
151015
asntrpgluleugluargthrasnglnserglyleugluargcysglu
202530
glygluglnasplysargleuhiscystyralasertrpargasnser
354045
serglythrilegluleuvallyslysglycystrpleuaspaspphe
505560
asncystyraspargglnglucysvalalathrglugluasnprogln
65707580
valtyrphecyscyscysgluglyasnphecysasngluargphethr
859095
hisleuproglualaglyglyprogluvalthrtyrglupropropro
100105110
thralaprothr
115
<210>30
<211>101
<212>prt
<213>人工序列
<220>
<223>人actriib可溶的(细胞外的),c-末端15个氨基酸删除的加工的多肽序列(seqidno:28的氨基酸19-119)
<400>30
serglyargglyglualagluthrargglucysiletyrtyrasnala
151015
asntrpgluleugluargthrasnglnserglyleugluargcysglu
202530
glygluglnasplysargleuhiscystyralasertrpargasnser
354045
serglythrilegluleuvallyslysglycystrpleuaspaspphe
505560
asncystyraspargglnglucysvalalathrglugluasnprogln
65707580
valtyrphecyscyscysgluglyasnphecysasngluargphethr
859095
hisleuprogluala
100
<210>31
<211>115
<212>prt
<213>人工序列
<220>
<223>人actriib可溶的(细胞外的),加工的多肽序列(seqidno:28的氨基酸20-134)
<400>31
glyargglyglualagluthrargglucysiletyrtyrasnalaasn
151015
trpgluleugluargthrasnglnserglyleugluargcysglugly
202530
gluglnasplysargleuhiscystyralasertrpargasnserser
354045
glythrilegluleuvallyslysglycystrpleuaspasppheasn
505560
cystyraspargglnglucysvalalathrglugluasnproglnval
65707580
tyrphecyscyscysgluglyasnphecysasngluargphethrhis
859095
leuproglualaglyglyprogluvalthrtyrgluproproprothr
100105110
alaprothr
115
<210>32
<211>100
<212>prt
<213>人工序列
<220>
<223>人actriib可溶的(细胞外的),c-末端15个氨基酸删除的加工的多肽序列(seqidno:28的氨基酸20-119)
<400>32
glyargglyglualagluthrargglucysiletyrtyrasnalaasn
151015
trpgluleugluargthrasnglnserglyleugluargcysglugly
202530
gluglnasplysargleuhiscystyralasertrpargasnserser
354045
glythrilegluleuvallyslysglycystrpleuaspasppheasn
505560
cystyraspargglnglucysvalalathrglugluasnproglnval
65707580
tyrphecyscyscysgluglyasnphecysasngluargphethrhis
859095
leuprogluala
100
<210>33
<211>107
<212>prt
<213>人工序列
<220>
<223>人actriib可溶的(细胞外的),ec结构域的n-末端6个氨基酸删除、ec结构域的c-末端3个氨基酸删除(seqidno:16的氨基酸25-131)、具有l79d突变的加工的多肽序列
<400>33
gluthrargglucysiletyrtyrasnalaasntrpgluleugluarg
151015
thrasnglnserglyleugluargcysgluglygluglnasplysarg
202530
leuhiscystyralasertrpalaasnserserglythrilegluleu
354045
vallyslysglycystrpaspaspasppheasncystyrasparggln
505560
glucysvalalathrglugluasnproglnvaltyrphecyscyscys
65707580
gluglyasnphecysasngluargphethrhisleuproglualagly
859095
glyprogluvalthrtyrgluproproprothr
100105
<210>34
<211>360
<212>prt
<213>人工序列
<220>
<223>ec结构域的n-末端6个氨基酸删除、ec结构域的c-末端3个氨基酸删除(seqidno:16的氨基酸25-131)、具有l79d突变并具有tpa前导序列的未加工的actriib-fc融合蛋白
<400>34
metaspalametlysargglyleucyscysvalleuleuleucysgly
151015
alavalphevalserproglyalaalagluthrargglucysiletyr
202530
tyrasnalaasntrpgluleugluargthrasnglnserglyleuglu
354045
argcysgluglygluglnasplysargleuhiscystyralasertrp
505560
alaasnserserglythrilegluleuvallyslysglycystrpasp
65707580
aspasppheasncystyraspargglnglucysvalalathrgluglu
859095
asnproglnvaltyrphecyscyscysgluglyasnphecysasnglu
100105110
argphethrhisleuproglualaglyglyprogluvalthrtyrglu
115120125
proproprothrglyglyglythrhisthrcysproprocysproala
130135140
progluleuleuglyglyproservalpheleupheproprolyspro
145150155160
lysaspthrleumetileserargthrprogluvalthrcysvalval
165170175
valaspvalserhisgluaspprogluvallyspheasntrptyrval
180185190
aspglyvalgluvalhisasnalalysthrlysproarggluglugln
195200205
tyrasnserthrtyrargvalvalservalleuthrvalleuhisgln
210215220
asptrpleuasnglylysglutyrlyscyslysvalserasnlysala
225230235240
leuproalaproileglulysthrileserlysalalysglyglnpro
245250255
arggluproglnvaltyrthrleuproproserarggluglumetthr
260265270
lysasnglnvalserleuthrcysleuvallysglyphetyrproser
275280285
aspilealavalglutrpgluserasnglyglnprogluasnasntyr
290295300
lysthrthrproprovalleuaspseraspglyserphepheleutyr
305310315320
serlysleuthrvalasplysserargtrpglnglnglyasnvalphe
325330335
sercysservalmethisglualaleuhisasnhistyrthrglnlys
340345350
serleuserleuserproglylys
355360
<210>35
<211>335
<212>prt
<213>人工序列
<220>
<223>ec结构域的n-末端6个氨基酸删除、ec结构域的c-末端3个氨基酸删除(seqidno:16的氨基酸25-131)、具有l79d突变的加工的actriib-fc融合蛋白
<400>35
gluthrargglucysiletyrtyrasnalaasntrpgluleugluarg
151015
thrasnglnserglyleugluargcysgluglygluglnasplysarg
202530
leuhiscystyralasertrpalaasnserserglythrilegluleu
354045
vallyslysglycystrpaspaspasppheasncystyrasparggln
505560
glucysvalalathrglugluasnproglnvaltyrphecyscyscys
65707580
gluglyasnphecysasngluargphethrhisleuproglualagly
859095
glyprogluvalthrtyrgluproproprothrglyglyglythrhis
100105110
thrcysproprocysproalaprogluleuleuglyglyproserval
115120125
pheleupheproprolysprolysaspthrleumetileserargthr
130135140
progluvalthrcysvalvalvalaspvalserhisgluaspproglu
145150155160
vallyspheasntrptyrvalaspglyvalgluvalhisasnalalys
165170175
thrlysproargglugluglntyrasnserthrtyrargvalvalser
180185190
valleuthrvalleuhisglnasptrpleuasnglylysglutyrlys
195200205
cyslysvalserasnlysalaleuproalaproileglulysthrile
210215220
serlysalalysglyglnproarggluproglnvaltyrthrleupro
225230235240
proserarggluglumetthrlysasnglnvalserleuthrcysleu
245250255
vallysglyphetyrproseraspilealavalglutrpgluserasn
260265270
glyglnprogluasnasntyrlysthrthrproprovalleuaspser
275280285
aspglyserphepheleutyrserlysleuthrvalasplysserarg
290295300
trpglnglnglyasnvalphesercysservalmethisglualaleu
305310315320
hisasnhistyrthrglnlysserleuserleuserproglylys
325330335
<210>36
<211>115
<212>prt
<213>人工序列
<220>
<223>人actriib可溶的(细胞外的),具有l79d突变的加工的多肽序列(seqidno:28的氨基酸20-134)
<400>36
glyargglyglualagluthrargglucysiletyrtyrasnalaasn
151015
trpgluleugluargthrasnglnserglyleugluargcysglugly
202530
gluglnasplysargleuhiscystyralasertrpargasnserser
354045
glythrilegluleuvallyslysglycystrpaspaspasppheasn
505560
cystyraspargglnglucysvalalathrglugluasnproglnval
65707580
tyrphecyscyscysgluglyasnphecysasngluargphethrhis
859095
leuproglualaglyglyprogluvalthrtyrgluproproprothr
100105110
alaprothr
115
<210>37
<211>115
<212>prt
<213>人工序列
<220>
<223>人actriib可溶的(细胞外的),具有l79d突变的加工的多肽序列(seqidno:16的氨基酸20-134)
<400>37
glyargglyglualagluthrargglucysiletyrtyrasnalaasn
151015
trpgluleugluargthrasnglnserglyleugluargcysglugly
202530
gluglnasplysargleuhiscystyralasertrpalaasnserser
354045
glythrilegluleuvallyslysglycystrpaspaspasppheasn
505560
cystyraspargglnglucysvalalathrglugluasnproglnval
65707580
tyrphecyscyscysgluglyasnphecysasngluargphethrhis
859095
leuproglualaglyglyprogluvalthrtyrgluproproprothr
100105110
alaprothr
115
<210>38
<211>343
<212>prt
<213>人工序列
<220>
<223>人actriib可溶的(细胞外的),具有通过ggg接头与fc结构域融合的l79d突变的加工的多肽序列(seqidno:28的氨基酸20-134)
<400>38
glyargglyglualagluthrargglucysiletyrtyrasnalaasn
151015
trpgluleugluargthrasnglnserglyleugluargcysglugly
202530
gluglnasplysargleuhiscystyralasertrpargasnserser
354045
glythrilegluleuvallyslysglycystrpaspaspasppheasn
505560
cystyraspargglnglucysvalalathrglugluasnproglnval
65707580
tyrphecyscyscysgluglyasnphecysasngluargphethrhis
859095
leuproglualaglyglyprogluvalthrtyrgluproproprothr
100105110
alaprothrglyglyglythrhisthrcysproprocysproalapro
115120125
gluleuleuglyglyproservalpheleupheproprolysprolys
130135140
aspthrleumetileserargthrprogluvalthrcysvalvalval
145150155160
aspvalserhisgluaspprogluvallyspheasntrptyrvalasp
165170175
glyvalgluvalhisasnalalysthrlysproargglugluglntyr
180185190
asnserthrtyrargvalvalservalleuthrvalleuhisglnasp
195200205
trpleuasnglylysglutyrlyscyslysvalserasnlysalaleu
210215220
proalaproileglulysthrileserlysalalysglyglnproarg
225230235240
gluproglnvaltyrthrleuproproserarggluglumetthrlys
245250255
asnglnvalserleuthrcysleuvallysglyphetyrproserasp
260265270
ilealavalglutrpgluserasnglyglnprogluasnasntyrlys
275280285
thrthrproprovalleuaspseraspglyserphepheleutyrser
290295300
lysleuthrvalasplysserargtrpglnglnglyasnvalpheser
305310315320
cysservalmethisglualaleuhisasnhistyrthrglnlysser
325330335
leuserleuserproglylys
340
<210>39
<211>343
<212>prt
<213>人工序列
<220>
<223>人actriib可溶的(细胞外的),具有与fc结构域融合的l79d突变的加工的多肽序列(seqidno:16的氨基酸20-134)
<400>39
glyargglyglualagluthrargglucysiletyrtyrasnalaasn
151015
trpgluleugluargthrasnglnserglyleugluargcysglugly
202530
gluglnasplysargleuhiscystyralasertrpalaasnserser
354045
glythrilegluleuvallyslysglycystrpaspaspasppheasn
505560
cystyraspargglnglucysvalalathrglugluasnproglnval
65707580
tyrphecyscyscysgluglyasnphecysasngluargphethrhis
859095
leuproglualaglyglyprogluvalthrtyrgluproproprothr
100105110
alaprothrglyglyglythrhisthrcysproprocysproalapro
115120125
gluleuleuglyglyproservalpheleupheproprolysprolys
130135140
aspthrleumetileserargthrprogluvalthrcysvalvalval
145150155160
aspvalserhisgluaspprogluvallyspheasntrptyrvalasp
165170175
glyvalgluvalhisasnalalysthrlysproargglugluglntyr
180185190
asnserthrtyrargvalvalservalleuthrvalleuhisglnasp
195200205
trpleuasnglylysglutyrlyscyslysvalserasnlysalaleu
210215220
proalaproileglulysthrileserlysalalysglyglnproarg
225230235240
gluproglnvaltyrthrleuproproserarggluglumetthrlys
245250255
asnglnvalserleuthrcysleuvallysglyphetyrproserasp
260265270
ilealavalglutrpgluserasnglyglnprogluasnasntyrlys
275280285
thrthrproprovalleuaspseraspglyserphepheleutyrser
290295300
lysleuthrvalasplysserargtrpglnglnglyasnvalpheser
305310315320
cysservalmethisglualaleuhisasnhistyrthrglnlysser
325330335
leuserleuserproglylys
340
<210>40
<211>368
<212>prt
<213>人工序列
<220>
<223>人actriib可溶的(细胞外的),具有与fc结构域融合的l79d突变和tpa前导序列的加工的多肽序列(seqidno:28的氨基酸20-134)
<400>40
metaspalametlysargglyleucyscysvalleuleuleucysgly
151015
alavalphevalserproglyalaserglyargglyglualagluthr
202530
argglucysiletyrtyrasnalaasntrpgluleugluargthrasn
354045
glnserglyleugluargcysgluglygluglnasplysargleuhis
505560
cystyralasertrpargasnserserglythrilegluleuvallys
65707580
lysglycystrpaspaspasppheasncystyraspargglnglucys
859095
valalathrglugluasnproglnvaltyrphecyscyscysglugly
100105110
asnphecysasngluargphethrhisleuproglualaglyglypro
115120125
gluvalthrtyrgluproproprothralaprothrglyglyglythr
130135140
histhrcysproprocysproalaprogluleuleuglyglyproser
145150155160
valpheleupheproprolysprolysaspthrleumetileserarg
165170175
thrprogluvalthrcysvalvalvalaspvalserhisgluasppro
180185190
gluvallyspheasntrptyrvalaspglyvalgluvalhisasnala
195200205
lysthrlysproargglugluglntyrasnserthrtyrargvalval
210215220
servalleuthrvalleuhisglnasptrpleuasnglylysglutyr
225230235240
lyscyslysvalserasnlysalaleuproalaproileglulysthr
245250255
ileserlysalalysglyglnproarggluproglnvaltyrthrleu
260265270
proproserarggluglumetthrlysasnglnvalserleuthrcys
275280285
leuvallysglyphetyrproseraspilealavalglutrpgluser
290295300
asnglyglnprogluasnasntyrlysthrthrproprovalleuasp
305310315320
seraspglyserphepheleutyrserlysleuthrvalasplysser
325330335
argtrpglnglnglyasnvalphesercysservalmethisgluala
340345350
leuhisasnhistyrthrglnlysserleuserleuserproglylys
355360365
<210>41
<211>368
<212>prt
<213>人工序列
<220>
<223>人actriib可溶的(细胞外的),具有与fc结构域融合的l79d突变和tpa前导序列的加工的多肽序列(seqidno:16的氨基酸20-134)
<400>41
metaspalametlysargglyleucyscysvalleuleuleucysgly
151015
alavalphevalserproglyalaserglyargglyglualagluthr
202530
argglucysiletyrtyrasnalaasntrpgluleugluargthrasn
354045
glnserglyleugluargcysgluglygluglnasplysargleuhis
505560
cystyralasertrpalaasnserserglythrilegluleuvallys
65707580
lysglycystrpaspaspasppheasncystyraspargglnglucys
859095
valalathrglugluasnproglnvaltyrphecyscyscysglugly
100105110
asnphecysasngluargphethrhisleuproglualaglyglypro
115120125
gluvalthrtyrgluproproprothralaprothrglyglyglythr
130135140
histhrcysproprocysproalaprogluleuleuglyglyproser
145150155160
valpheleupheproprolysprolysaspthrleumetileserarg
165170175
thrprogluvalthrcysvalvalvalaspvalserhisgluasppro
180185190
gluvallyspheasntrptyrvalaspglyvalgluvalhisasnala
195200205
lysthrlysproargglugluglntyrasnserthrtyrargvalval
210215220
servalleuthrvalleuhisglnasptrpleuasnglylysglutyr
225230235240
lyscyslysvalserasnlysalaleuproalaproileglulysthr
245250255
ileserlysalalysglyglnproarggluproglnvaltyrthrleu
260265270
proproserarggluglumetthrlysasnglnvalserleuthrcys
275280285
leuvallysglyphetyrproseraspilealavalglutrpgluser
290295300
asnglyglnprogluasnasntyrlysthrthrproprovalleuasp
305310315320
seraspglyserphepheleutyrserlysleuthrvalasplysser
325330335
argtrpglnglnglyasnvalphesercysservalmethisgluala
340345350
leuhisasnhistyrthrglnlysserleuserleuserproglylys
355360365
<210>42
<211>141
<212>prt
<213>人工序列
<220>
<223>人actriib可溶的(细胞外的),具有变体c-末端序列的加工的多肽序列(wo2007/053775中公开的)
<400>42
glyargglyglualagluthrargglucysiletyrtyrasnalaasn
151015
trpgluleugluargthrasnglnserglyleugluargcysglugly
202530
gluglnasplysargleuhiscystyralasertrpargasnserser
354045
glythrilegluleuvallyslysglycystrpleuaspasppheasn
505560
cystyraspargglnglucysvalalathrglugluasnproglnval
65707580
tyrphecyscyscysgluglyasnphecysasngluargphethrhis
859095
leuproglualaglyglyprogluglyprotrpalaserthrthrile
100105110
proserglyglyproglualathralaalaalaglyaspglnglyser
115120125
glyalaleutrpleucysleugluglyproalahisglu
130135140
<210>43
<211>141
<212>prt
<213>人工序列
<220>
<223>人actriib可溶的(细胞外的),具有带l79d突变的变体c-末端序列的加工的多肽序列(wo2007/053775中公开的)
<400>43
glyargglyglualagluthrargglucysiletyrtyrasnalaasn
151015
trpgluleugluargthrasnglnserglyleugluargcysglugly
202530
gluglnasplysargleuhiscystyralasertrpargasnserser
354045
glythrilegluleuvallyslysglycystrpaspaspasppheasn
505560
cystyraspargglnglucysvalalathrglugluasnproglnval
65707580
tyrphecyscyscysgluglyasnphecysasngluargphethrhis
859095
leuproglualaglyglyprogluglyprotrpalaserthrthrile
100105110
proserglyglyproglualathralaalaalaglyaspglnglyser
115120125
glyalaleutrpleucysleugluglyproalahisglu
130135140
<210>44
<211>370
<212>prt
<213>人工序列
<220>
<223>人actriib可溶的(细胞外的),具有用tggg接头融合到fc结构域的l79d突变的变体c-末端序列的加工的多肽序列(wo2007/053775中公开的)
<400>44
glyargglyglualagluthrargglucysiletyrtyrasnalaasn
151015
trpgluleugluargthrasnglnserglyleugluargcysglugly
202530
gluglnasplysargleuhiscystyralasertrpargasnserser
354045
glythrilegluleuvallyslysglycystrpaspaspasppheasn
505560
cystyraspargglnglucysvalalathrglugluasnproglnval
65707580
tyrphecyscyscysgluglyasnphecysasngluargphethrhis
859095
leuproglualaglyglyprogluglyprotrpalaserthrthrile
100105110
proserglyglyproglualathralaalaalaglyaspglnglyser
115120125
glyalaleutrpleucysleugluglyproalahisgluthrglygly
130135140
glythrhisthrcysproprocysproalaprogluleuleuglygly
145150155160
proservalpheleupheproprolysprolysaspthrleumetile
165170175
serargthrprogluvalthrcysvalvalvalaspvalserhisglu
180185190
aspprogluvallyspheasntrptyrvalaspglyvalgluvalhis
195200205
asnalalysthrlysproargglugluglntyrasnserthrtyrarg
210215220
valvalservalleuthrvalleuhisglnasptrpleuasnglylys
225230235240
glutyrlyscyslysvalserasnlysalaleuproalaproileglu
245250255
lysthrileserlysalalysglyglnproarggluproglnvaltyr
260265270
thrleuproproserarggluglumetthrlysasnglnvalserleu
275280285
thrcysleuvallysglyphetyrproseraspilealavalglutrp
290295300
gluserasnglyglnprogluasnasntyrlysthrthrproproval
305310315320
leuaspseraspglyserphepheleutyrserlysleuthrvalasp
325330335
lysserargtrpglnglnglyasnvalphesercysservalmethis
340345350
glualaleuhisasnhistyrthrglnlysserleuserleuserpro
355360365
glylys
370
<210>45
<211>1083
<212>dna
<213>人工序列
<220>
<223>编码seqidno:24的核酸序列
<400>45
atggatgcaatgaagagagggctctgctgtgtgctgctgctgtgtggagcagtcttcgtt60
tcgcccggcgccgccgaaacccgcgaatgtatttattacaatgctaattgggaactcgaa120
cggacgaaccaatccgggctcgaacggtgtgagggggaacaggataaacgcctccattgc180
tatgcgtcgtggaggaactcctccgggacgattgaactggtcaagaaagggtgctgggac240
gacgatttcaattgttatgaccgccaggaatgtgtcgcgaccgaagagaatccgcaggtc300
tatttctgttgttgcgaggggaatttctgtaatgaacggtttacccacctccccgaagcc360
ggcgggcccgaggtgacctatgaacccccgcccaccggtggtggaactcacacatgccca420
ccgtgcccagcacctgaactcctggggggaccgtcagtcttcctcttccccccaaaaccc480
aaggacaccctcatgatctcccggacccctgaggtcacatgcgtggtggtggacgtgagc540
cacgaagaccctgaggtcaagttcaactggtacgtggacggcgtggaggtgcataatgcc600
aagacaaagccgcgggaggagcagtacaacagcacgtaccgtgtggtcagcgtcctcacc660
gtcctgcaccaggactggctgaatggcaaggagtacaagtgcaaggtctccaacaaagcc720
ctcccagcccccatcgagaaaaccatctccaaagccaaagggcagccccgagaaccacag780
gtgtacaccctgcccccatcccgggaggagatgaccaagaaccaggtcagcctgacctgc840
ctggtcaaaggcttctatcccagcgacatcgccgtggagtgggagagcaatgggcagccg900
gagaacaactacaagaccacgcctcccgtgctggactccgacggctccttcttcctctat960
agcaagctcaccgtggacaagagcaggtggcagcaggggaacgtcttctcatgctccgtg1020
atgcatgaggctctgcacaaccactacacgcagaagagcctctccctgtccccgggtaaa1080
tga1083
<210>46
<211>344
<212>prt
<213>人工序列
<220>
<223>包含与fc结构域融合的actriib的可溶的细胞外结构域(r64;seqidno:29)的融合蛋白
<400>46
serglyargglyglualagluthrargglucysiletyrtyrasnala
151015
asntrpgluleugluargthrasnglnserglyleugluargcysglu
202530
glygluglnasplysargleuhiscystyralasertrpargasnser
354045
serglythrilegluleuvallyslysglycystrpleuaspaspphe
505560
asncystyraspargglnglucysvalalathrglugluasnprogln
65707580
valtyrphecyscyscysgluglyasnphecysasngluargphethr
859095
hisleuproglualaglyglyprogluvalthrtyrglupropropro
100105110
thralaprothrglyglyglythrhisthrcysproprocysproala
115120125
progluleuleuglyglyproservalpheleupheproprolyspro
130135140
lysaspthrleumetileserargthrprogluvalthrcysvalval
145150155160
valaspvalserhisgluaspprogluvallyspheasntrptyrval
165170175
aspglyvalgluvalhisasnalalysthrlysproarggluglugln
180185190
tyrasnserthrtyrargvalvalservalleuthrvalleuhisgln
195200205
asptrpleuasnglylysglutyrlyscyslysvalserasnlysala
210215220
leuprovalproileglulysthrileserlysalalysglyglnpro
225230235240
arggluproglnvaltyrthrleuproproserarggluglumetthr
245250255
lysasnglnvalserleuthrcysleuvallysglyphetyrproser
260265270
aspilealavalglutrpgluserasnglyglnprogluasnasntyr
275280285
lysthrthrproprovalleuaspseraspglyserphepheleutyr
290295300
serlysleuthrvalasplysserargtrpglnglnglyasnvalphe
305310315320
sercysservalmethisglualaleuhisasnhistyrthrglnlys
325330335
serleuserleuserproglylys
340
<210>47
<211>329
<212>prt
<213>人工序列
<220>
<223>包含与fc结构域融合的、带有c-末端15个氨基酸删除的(seqidno:30)actriib的可溶的细胞外结构域(r64)的融合蛋白
<400>47
serglyargglyglualagluthrargglucysiletyrtyrasnala
151015
asntrpgluleugluargthrasnglnserglyleugluargcysglu
202530
glygluglnasplysargleuhiscystyralasertrpargasnser
354045
serglythrilegluleuvallyslysglycystrpleuaspaspphe
505560
asncystyraspargglnglucysvalalathrglugluasnprogln
65707580
valtyrphecyscyscysgluglyasnphecysasngluargphethr
859095
hisleuproglualaglyglyglythrhisthrcysproprocyspro
100105110
alaprogluleuleuglyglyproservalpheleupheproprolys
115120125
prolysaspthrleumetileserargthrprogluvalthrcysval
130135140
valvalaspvalserhisgluaspprogluvallyspheasntrptyr
145150155160
valaspglyvalgluvalhisasnalalysthrlysproarggluglu
165170175
glntyrasnserthrtyrargvalvalservalleuthrvalleuhis
180185190
glnasptrpleuasnglylysglutyrlyscyslysvalserasnlys
195200205
alaleuprovalproileglulysthrileserlysalalysglygln
210215220
proarggluproglnvaltyrthrleuproproserarggluglumet
225230235240
thrlysasnglnvalserleuthrcysleuvallysglyphetyrpro
245250255
seraspilealavalglutrpgluserasnglyglnprogluasnasn
260265270
tyrlysthrthrproprovalleuaspseraspglyserphepheleu
275280285
tyrserlysleuthrvalasplysserargtrpglnglnglyasnval
290295300
phesercysservalmethisglualaleuhisasnhistyrthrgln
305310315320
lysserleuserleuserproglylys
325
<210>48
<211>20
<212>dna
<213>人工序列
<220>
<223>runx2qrt-pcr引物1
<400>48
ccgcacgacaaccgcaccat20
<210>49
<211>20
<212>dna
<213>人工序列
<220>
<223>runx2qrt-pcr引物2
<400>49
cgctccggcccacaaatctc20
<210>50
<211>20
<212>dna
<213>人工序列
<220>
<223>alpqrt-pcr引物1
<400>50
acgtggctaagaatgtcatc20
<210>51
<211>19
<212>dna
<213>人工序列
<220>
<223>alpqrt-pcr引物2
<400>51
ctggtaggcgatgtcctta19
<210>52
<211>25
<212>dna
<213>人工序列
<220>
<223>osterixqrt-pcr引物1
<400>52
tagtggtttggggtttgtttaccgc25
<210>53
<211>26
<212>dna
<213>人工序列
<220>
<223>osterixqrt-pcr引物2
<400>53
aaccaaataactcttattccctaagt26
<210>54
<211>21
<212>dna
<213>人工序列
<220>
<223>klothoqrt-pcr引物1
<400>54
gctctcaaagcccacatactg21
<210>55
<211>20
<212>dna
<213>人工序列
<220>
<223>klothoqrt-pcr引物1
<400>55
gcagcataacgatagaggcc20
<210>56
<211>22
<212>dna
<213>人工序列
<220>
<223>sm22-alphaqrt-pcr引物1
<400>56
gttccagactgttgacctcttt22
<210>57
<211>20
<212>dna
<213>人工序列
<220>
<223>sm22-alphaqrt-pcr引物2
<400>57
ctgcgctttcttcataaacc20
<210>58
<211>5553
<212>dna
<213>智人
<220>
<223>人runx2mrna
<400>58
gtgtgaatgcttcattcgcctcacaaacaaccacagaaccacaagtgcggtgcaaacttt60
ctccaggaggacagcaagaagtctctggtttttaaatggttaatctccgcaggtcactac120
cagccaccgagaccaacagagtcatttaaggctgcaagcagtatttacaacagagggtac180
aagttctatctgaaaaaaaaaggagggactatggcatcaaacagcctcttcagcacagtg240
acaccatgtcagcaaaacttcttttgggatccgagcaccagccggcgcttcagccccccc300
tccagcagcctgcagcccggcaaaatgagcgacgtgagcccggtggtggctgcgcaacag360
cagcagcaacagcagcagcagcaacagcagcagcagcagcagcaacagcagcagcagcag420
caggaggcggcggcggcggctgcggcggcggcggcggctgcggcggcggcagctgcagtg480
ccccggttgcggccgccccacgacaaccgcaccatggtggagatcatcgccgaccacccg540
gccgaactcgtccgcaccgacagccccaacttcctgtgctcggtgctgccctcgcactgg600
cgctgcaacaagaccctgcccgtggccttcaaggtggtagccctcggagaggtaccagat660
gggactgtggttactgtcatggcgggtaacgatgaaaattattctgctgagctccggaat720
gcctctgctgttatgaaaaaccaagtagcaaggttcaacgatctgagatttgtgggccgg780
agtggacgaggcaagagtttcaccttgaccataaccgtcttcacaaatcctccccaagta840
gctacctatcacagagcaattaaagttacagtagatggacctcgggaacccagaaggcac900
agacagaagcttgatgactctaaacctagtttgttctctgaccgcctcagtgatttaggg960
cgcattcctcatcccagtatgagagtaggtgtcccgcctcagaacccacggccctccctg1020
aactctgcaccaagtccttttaatccacaaggacagagtcagattacagaccccaggcag1080
gcacagtcttccccgccgtggtcctatgaccagtcttacccctcctacctgagccagatg1140
acgtccccgtccatccactctaccaccccgctgtcttccacacggggcactgggcttcct1200
gccatcaccgatgtgcctaggcgcatttcagatgatgacactgccacctctgacttctgc1260
ctctggccttccactctcagtaagaagagccaggcaggtgcttcagaactgggccctttt1320
tcagaccccaggcagttcccaagcatttcatccctcactgagagccgcttctccaaccca1380
cgaatgcactatccagccacctttacttacaccccgccagtcacctcaggcatgtccctc1440
ggtatgtccgccaccactcactaccacacctacctgccaccaccctaccccggctcttcc1500
caaagccagagtggacccttccagaccagcagcactccatatctctactatggcacttcg1560
tcaggatcctatcagtttcccatggtgccggggggagaccggtctccttccagaatgctt1620
ccgccatgcaccaccacctcgaatggcagcacgctattaaatccaaatttgcctaaccag1680
aatgatggtgttgacgctgatggaagccacagcagttccccaactgttttgaattctagt1740
ggcagaatggatgaatctgtttggcgaccatattgaaattcctcagcagtggcccagtgg1800
tatctgggggccacatcccacacgtatcaatatatacatatatagagagagtgcatatat1860
atgtatatcgattagctatctacaaagtgcctattttttagaagatttttcattcactca1920
ctcagtcatgatcttgcagccataagagggtagatattgagaagcagaaggctcaagaga1980
gacaattgcaatcgagcttcagattgtttactatttaagatgtacttttacaaaggaaca2040
aagaagggaaaaggtatttttgtttttgttgtttggtctgttatcatcaataacctgttc2100
atatgccaattcagagaggtggactccaggttcaggagggagaagagcaaagccgcttcc2160
tctctgtgctttgaaacttcacaccctcacggtggcagctgtgtatggaccagtgccctc2220
cgcagacagctcacaaaaccagttgaggtgcactaaagggacatgaggtagaatggatgc2280
ttccatcacagtaccatcattcagaataactcttccaatttctgctttcagacatgctgc2340
aggtcctcatctgaactgttgggttcgtttttttttttttttttcctgctccaagaaagt2400
gacttcaaaaataactgatcaggatagattattttattttactttttaacactccttctc2460
cccttttcccactgaaccaaaaagaaatcccatccctaaaacctgccttctccttttatg2520
caaaactgaaaatggcaatacattattatagccataatggtatagatagtgattgcgttt2580
ggctatgtgttgttttctttttttttaaattatgaatatgtgtaaaatctgaggtaactt2640
gctaacgtgaatggtcatataactttaaagatatatttataattatttaatgacatttgg2700
acccttgaaacatttcttagtgtattgatatgttgacttcggtctctaaaagtgctcttt2760
attaaataacaaatttcttcagtggtctagagccatatctgaaatattgctaagcaattt2820
cagttcatccaggcacaatgtgattttaaaaaatacttccatctccaaatattttagata2880
tagattgtttttgtgatgtatgaaggaaatgttatgtttagttctttcagatctttgaat2940
gcctctaacacagctttgccttctaaagcggtaattagggatttaaaaaacaacctttag3000
ccctttatcagcatgaaatgctggagtgatgtggttttctaatttctttggggtaattat3060
gactcttgtcatattaaaaagacaagcacaagtaaatcattgaactacagaaaaatgttc3120
tgtggtttcatagttaagcaaaactctaaatcgccaggcttcatagcaaagacatagtca3180
gctaaaagccgcacatgtggatagagggttcaattatgagacacctagtacaggagagca3240
aaattgcaccagagattcttaaccaaccagccttaccaaacaacacaacaggggaacccc3300
aatctgccttacccaaggccccactggcagctttccacagaatttgcatttagaggagca3360
gaatgacatcactgtcctttgggagtaggtcctctgaaaaggcagcaggttccagcaggt3420
agctgagctgagaggacatatggcccacggggacctacagacagcctttgacatttgtat3480
ttcttacaatggagggccaaggagggcaaggggctgtggagtttggtgtctactagtgtg3540
tatgaatttgagctagagtccttctgtggcatgcactttgaccactcctggcagtcacat3600
ggcagatttccaagtgcaaatccttaatccaaacaaggatcatctaatgacaccaccagg3660
ccaatccctgctctcctccccgaaaagtcagggtcccttcattggaatcctccacccacc3720
caagcagaatttagcagagatttgccttcaaaccctaacggcccccttgttctctggtcc3780
ttctcaaacccacctttgtaggccacccagcattgcaggacagcgtgtggggcagctgga3840
cctgtgcttcctgcctgggagtctcccttggaattcatcctgactccttctaataaaaat3900
ggatgggaaagcaaaacactttgccttctaaaggccgtataccaagtatgcttagataaa3960
taagccacttttctattacttaagtaagaaggaagtagtaattgatactatttattgttt4020
gtgtgtggtagcttgaagcacaccactgtccatttatttgtaagtgtaaaatatgtgtgt4080
ttgtttcagcagcacttaaaaaagccagtgtctggttacacatttcaattttaattaatt4140
gacataaaaatgctaccgccagtgccagctgcatcctatttaattaaaaaggtactatat4200
ttgtacattattttttaatgttaaaagggcttttttaagtttacagtacacataccgagt4260
gactttagggatgcttttgtgttgaaatgttactatagtggctgcaggcagcaacccaga4320
aacactttagaagctttttttccttgggaaaaattcaagcacttcttccctccaccctca4380
ctccaaccaccccaatgggggtaattcacatttcttagaacaaattctgcccttttttgg4440
tctagggattaaaattttgtttttctttctttctttttttttttttttcactgaaccctt4500
aatttgcactgggtcatgtgtttgatttgtgatttcaagaccaaagcaaagtcttactac4560
tactgtggaaccatgtactagttcctgggaattaaaatagcgtggttctctttgtagcac4620
aaacattgctggaatttgcagtcttttcaatgcagccacatttttatccatttcagttgt4680
ctcacaaattttaacccatatcagagttccagaacaggtaccacagctttggttttagat4740
tagtggaataacattcagcccagaactgagaaactcaacagattaactatcgtttgctct4800
ttagacggtctcactgcctctcacttgccagagccctttcaaaatgagcagagaagtcca4860
caccattagggaccatctgtgataaattcagaagggaggagatgtgtgtacagctttaag4920
gattccctcaattccgaggaaagggactggcccagaatccaggttaatacatggaaacac4980
gaagcattagcaaaagtaataattatacctatggtatttgaaagaacaataataaaagac5040
acttcttccaaaccttgaatttgttgtttttagaaaacgaatgcatttaaaaatattttc5100
tatgtgagaattttttagatgtgtgtttacttcatgtttacaaataactgtttgcttttt5160
aatgcagtactttgaaatatatcagccaaaaccataacttacaataatttcttaggtatt5220
ctgaataaaattccatttcttttggatatgctttaccattcttaggtttctgtggaacaa5280
aaatatttgtagcattttgtgtaaatacaagctttcatttttattttttccaattgctat5340
tgcccaagaattgctttccatgcacatattgtaaaaattccgctttgtgccacaggtcat5400
gattgtggatgagtttactcttaacttcaaagggactatttgtattgtatgttgcaactg5460
taaattgaattatttggcatttttctcatgattgtaatattaatttgaagtttgaattta5520
attttcaataaaatggcttttttggttttgtta5553
<210>59
<211>3173
<212>dna
<213>智人
<220>
<223>人alpmrna
<400>59
cggcgggcggcagcagcctaggcagcagcagtagcagaagcagcagccgccgagcagcag60
caaggactctggagtcagagtaggactgtaggaccggagcctgagtggaacaggagtgga120
gctggcctgggagagagcggatccctcccagcaccctcaggccacccgttgcctgcactc180
tccctgccagacctccagagaggagagactcgggacagccagccccaggttcccccagct240
ctctccatctgcctggctccttgggacccgttccccagcctcaggatggcgtcctccctg300
cttgaggaggaagttcactatggctccagtcccctggccatgctgacggcagcgtgcagc360
aaatttggtggctctagccctctgcgggactcaacaactctgggcaaagcaggcacaaag420
aagccgtactctgtgggcagtgacctttcagcctccaaaaccatgggggatgcttatcca480
gccccctttacaagcactaatgggctcctttcacctgcaggcagtcctccagcacccacc540
tcaggctatgctaatgattaccctcccttttcccactcattccctgggcccacaggcacc600
caggaccctgggctactagtgcccaaggggcacagctcttctgactgtctgcccagtgtc660
tacacctctctggacatgacacacccctatggctcctggtacaaggcaggcatccatgca720
ggcatttcaccaggcccaggcaacactcctactccatggtgggatatgcaccctggaggc780
aactggctaggtggtgggcagggccagggtgatgggctgcaagggacactgcccacaggt840
ccagctcagcctccactgaacccccagctgcccacctacccatctgactttgctcccctt900
aatccagccccctacccagctccccacctcttgcaaccagggccccagcatgtcttgccc960
caagatgtctataaacccaaggcagtgggaaatagtgggcagctagaagggagtggtgga1020
gccaaacccccacggggtgcaagcactgggggtagtggtggatatgggggcagtggggca1080
gggcgctcctcctgcgactgccctaattgccaggagctagagcggctgggagcagcagcg1140
gctgggctgcggaagaagcccatccacagctgccacatccctggctgcggcaaggtgtat1200
ggcaaggcttcgcacctgaaggcccacttgcgctggcacacaggcgagaggcccttcgtc1260
tgcaactggctcttctgcggcaagaggttcactcgttcggatgagctggagcgtcatgtg1320
cgcactcacacccgggagaagaagttcacctgcctgctctgctccaagcgctttacccga1380
agcgaccacctgagcaaacaccagcgcacccatggagaaccaggcccgggtccccctccc1440
agtggccccaaggagctgggggagggccgcagcacgggggaagaggaggccagtcagacg1500
ccccgaccttctgcctcgccagcaaccccagagaaagcccctggaggcagccctgagcag1560
agcaacttgctggagatctgagccgggtggaaggtctcccaccccagggctgccctgaca1620
gtctctcttggctctctagaccactgcttgccaatcactctctttaccccatgcatgcca1680
tccttcggggctctctccctctgtctccctcctggccattctgggcttgggtatctcctt1740
gcatgcctcctcagctcaccttctctcttcaccatgagactggctttccacaaactctca1800
tctcaggccctccccttgtgcctgatacctgcactccggcttcctagactctggccctgc1860
cacaccaacacactttctatttgggctcccaacactatttctccatctcactccttgaca1920
tgtacccctttctgcttctcaagcttatttcctgctgtccctcagcctccaggcttcagt1980
cttcccaacttcttacaccattgctttccattctccagaactcttttttcctttttacaa2040
acacaatgataatgataatttattgccccctggtggcctcttcatcaggggtattggggt2100
tagtgacctggccagagggtgccaagaggggggcagaccagtggggatctgatcccaaag2160
atggggtgaccccagggtcagggaggctgcccccaggcctgtatatttaacccctatgta2220
ccaggagtaatgaatagtaataattctatttatgtaagttatgatgacgggtcaggtaga2280
gtgagctggggagggaagtggatccatttctgctaaggaaattctagtcaaatgcatctc2340
tgtatagacaaaatgttagtggagaagatcttgttaatagaatgtctatcatcagaatct2400
cagttgatagggtttctcttgtaatgaagtctctacaaattgggttagctacatctctgc2460
taaacagttgatggggtatctcttgattagggggatccctaatatccccagccccagcca2520
gaagctgtgaaacctcaagtcctatggaggggagaaggactggaatgtaccccatctccc2580
ttgactgcagagcaggttcctccactgccccaccccttagacaccatgaccccatcaggt2640
taatcccctgttgccatggttatggagagcttgcagctgccatcttagatgtgctctttg2700
gggaagcccatctaacaggaggacattggtttgggggtgcacctcctgaagaatgggtgg2760
ggaaggctttctctaggatcagattcaaataagtatgtattgagtgcctactctgtgcaa2820
ggcactatgctagatctggtgcctagaagccctgagaaagaacttaaagagctaggagga2880
cagaggcccccaagctgatctggtggtgcatccacgcacccccaccctgggactttggat2940
gctcccatctccacctccagtgacttttaaagccgcttcgtgcctttcctgtaacgttgg3000
atcctccttttctgtcccctgctgtctcaaggccccaagttaaagggttaaagccgctgg3060
agcttggggagagaacattgtggaatggaagggatcatgccctttgtggagtcttttttt3120
tttaatttaataaataaaagttggatttgaaaaaaaaaaaaaaaaaaaaaaaa3173
<210>60
<211>3173
<212>dna
<213>智人
<220>
<223>人osterixmrna
<400>60
cggcgggcggcagcagcctaggcagcagcagtagcagaagcagcagccgccgagcagcag60
caaggactctggagtcagagtaggactgtaggaccggagcctgagtggaacaggagtgga120
gctggcctgggagagagcggatccctcccagcaccctcaggccacccgttgcctgcactc180
tccctgccagacctccagagaggagagactcgggacagccagccccaggttcccccagct240
ctctccatctgcctggctccttgggacccgttccccagcctcaggatggcgtcctccctg300
cttgaggaggaagttcactatggctccagtcccctggccatgctgacggcagcgtgcagc360
aaatttggtggctctagccctctgcgggactcaacaactctgggcaaagcaggcacaaag420
aagccgtactctgtgggcagtgacctttcagcctccaaaaccatgggggatgcttatcca480
gccccctttacaagcactaatgggctcctttcacctgcaggcagtcctccagcacccacc540
tcaggctatgctaatgattaccctcccttttcccactcattccctgggcccacaggcacc600
caggaccctgggctactagtgcccaaggggcacagctcttctgactgtctgcccagtgtc660
tacacctctctggacatgacacacccctatggctcctggtacaaggcaggcatccatgca720
ggcatttcaccaggcccaggcaacactcctactccatggtgggatatgcaccctggaggc780
aactggctaggtggtgggcagggccagggtgatgggctgcaagggacactgcccacaggt840
ccagctcagcctccactgaacccccagctgcccacctacccatctgactttgctcccctt900
aatccagccccctacccagctccccacctcttgcaaccagggccccagcatgtcttgccc960
caagatgtctataaacccaaggcagtgggaaatagtgggcagctagaagggagtggtgga1020
gccaaacccccacggggtgcaagcactgggggtagtggtggatatgggggcagtggggca1080
gggcgctcctcctgcgactgccctaattgccaggagctagagcggctgggagcagcagcg1140
gctgggctgcggaagaagcccatccacagctgccacatccctggctgcggcaaggtgtat1200
ggcaaggcttcgcacctgaaggcccacttgcgctggcacacaggcgagaggcccttcgtc1260
tgcaactggctcttctgcggcaagaggttcactcgttcggatgagctggagcgtcatgtg1320
cgcactcacacccgggagaagaagttcacctgcctgctctgctccaagcgctttacccga1380
agcgaccacctgagcaaacaccagcgcacccatggagaaccaggcccgggtccccctccc1440
agtggccccaaggagctgggggagggccgcagcacgggggaagaggaggccagtcagacg1500
ccccgaccttctgcctcgccagcaaccccagagaaagcccctggaggcagccctgagcag1560
agcaacttgctggagatctgagccgggtggaaggtctcccaccccagggctgccctgaca1620
gtctctcttggctctctagaccactgcttgccaatcactctctttaccccatgcatgcca1680
tccttcggggctctctccctctgtctccctcctggccattctgggcttgggtatctcctt1740
gcatgcctcctcagctcaccttctctcttcaccatgagactggctttccacaaactctca1800
tctcaggccctccccttgtgcctgatacctgcactccggcttcctagactctggccctgc1860
cacaccaacacactttctatttgggctcccaacactatttctccatctcactccttgaca1920
tgtacccctttctgcttctcaagcttatttcctgctgtccctcagcctccaggcttcagt1980
cttcccaacttcttacaccattgctttccattctccagaactcttttttcctttttacaa2040
acacaatgataatgataatttattgccccctggtggcctcttcatcaggggtattggggt2100
tagtgacctggccagagggtgccaagaggggggcagaccagtggggatctgatcccaaag2160
atggggtgaccccagggtcagggaggctgcccccaggcctgtatatttaacccctatgta2220
ccaggagtaatgaatagtaataattctatttatgtaagttatgatgacgggtcaggtaga2280
gtgagctggggagggaagtggatccatttctgctaaggaaattctagtcaaatgcatctc2340
tgtatagacaaaatgttagtggagaagatcttgttaatagaatgtctatcatcagaatct2400
cagttgatagggtttctcttgtaatgaagtctctacaaattgggttagctacatctctgc2460
taaacagttgatggggtatctcttgattagggggatccctaatatccccagccccagcca2520
gaagctgtgaaacctcaagtcctatggaggggagaaggactggaatgtaccccatctccc2580
ttgactgcagagcaggttcctccactgccccaccccttagacaccatgaccccatcaggt2640
taatcccctgttgccatggttatggagagcttgcagctgccatcttagatgtgctctttg2700
gggaagcccatctaacaggaggacattggtttgggggtgcacctcctgaagaatgggtgg2760
ggaaggctttctctaggatcagattcaaataagtatgtattgagtgcctactctgtgcaa2820
ggcactatgctagatctggtgcctagaagccctgagaaagaacttaaagagctaggagga2880
cagaggcccccaagctgatctggtggtgcatccacgcacccccaccctgggactttggat2940
gctcccatctccacctccagtgacttttaaagccgcttcgtgcctttcctgtaacgttgg3000
atcctccttttctgtcccctgctgtctcaaggccccaagttaaagggttaaagccgctgg3060
agcttggggagagaacattgtggaatggaagggatcatgccctttgtggagtcttttttt3120
tttaatttaataaataaaagttggatttgaaaaaaaaaaaaaaaaaaaaaaaa3173
<210>61
<211>5003
<212>dna
<213>智人
<220>
<223>人klothomrna
<400>61
cgcgcagcatgcccgccagcgccccgccgcgccgcccgcggccgccgccgccgtcgctgt60
cgctgctgctggtgctgctgggcctgggcggccgccgcctgcgtgcggagccgggcgacg120
gcgcgcagacctgggcccgtgtctcgcggcctcctgcccccgaggccgcgggcctcttcc180
agggcaccttccccgacggcttcctctgggccgtgggcagcgccgcctaccagaccgagg240
gcggctggcagcagcacggcaagggtgcgtccatctgggacacgttcacccaccaccccc300
tggcacccccgggagactcccggaacgccagtctgccgttgggcgccccgtcgccgctgc360
agcccgccaccggggacgtagccagcgacagctacaacaacgtcttccgcgacacggagg420
cgctgcgcgagctcggggtcactcactaccgcttctccatctcgtgggcgcgagtgctcc480
ccaatggcagcgcgggcgtccccaaccgcgaggggctgcgctactaccggcgcctgctgg540
agcggctgcgggagctgggcgtgcagcccgtggtcaccctgtaccactgggacctgcccc600
agcgcctgcaggacgcctacggcggctgggccaaccgcgccctggccgaccacttcaggg660
attacgcggagctctgcttccgccacttcggcggtcaggtcaagtactggatcaccatcg720
acaacccctacgtggtggcctggcacggctacgccaccgggcgcctggcccccggcatcc780
ggggcagcccgcggctcgggtacctggtggcgcacaacctcctcctggctcatgccaaag840
tctggcatctctacaatacttctttccgtcccactcagggaggtcaggtgtccattgccc900
taagctctcactggatcaatcctcgaagaatgaccgaccacagcatcaaagaatgtcaaa960
aatctctggactttgtactaggttggtttgccaaacccgtatttattgatggtgactatc1020
ccgagagcatgaagaataacctttcatctattctgcctgattttactgaatctgagaaaa1080
agttcatcaaaggaactgctgacttttttgctctttgctttggacccaccttgagttttc1140
aacttttggaccctcacatgaagttccgccaattggaatctcccaacctgaggcaactgc1200
tttcctggattgaccttgaatttaaccatcctcaaatatttattgtggaaaatggctggt1260
ttgtctcagggaccaccaagagagatgatgccaaatatatgtattacctcaaaaagttca1320
tcatggaaaccttaaaagccatcaagctggatggggtggatgtcatcgggtataccgcat1380
ggtccctcatggatggtttcgagtggcacagaggttacagcatcaggcgtggactcttct1440
atgttgactttctaagccaggacaagatgttgttgccaaagtcttcagccttgttctacc1500
aaaagctgatagagaaaaatggcttccctcctttacctgaaaatcagcccctagaaggga1560
catttccctgtgactttgcttggggagttgttgacaactacattcaagtagataccactc1620
tgtctcagtttaccgacctgaatgtttacctgtgggatgtccaccacagtaaaaggctta1680
ttaaagtggatggggttgtgaccaagaagaggaaatcctactgtgttgactttgctgcca1740
tccagccccagatcgctttactccaggaaatgcacgttacacattttcgcttctccctgg1800
actgggccctgattctccctctgggtaaccagtcccaggtgaaccacaccatcctgcagt1860
actatcgctgcatggccagcgagcttgtccgtgtcaacatcaccccagtggtggccctgt1920
ggcagcctatggccccgaaccaaggactgccgcgcctcctggccaggcagggcgcctggg1980
agaacccctacactgccctggcctttgcagagtatgcccgactgtgctttcaagagctcg2040
gccatcacgtcaagctttggataacgatgaatgagccgtatacaaggaatatgacataca2100
gtgctggccacaaccttctgaaggcccatgccctggcttggcatgtgtacaatgaaaagt2160
ttaggcatgctcagaatgggaaaatatccatagccttgcaggctgattggatagaacctg2220
cctgccctttctcccaaaaggacaaagaggtggccgagagagttttggaatttgacattg2280
gctggctggctgagcccattttcggctctggagattatccatgggtgatgagggactggc2340
tgaaccaaagaaacaattttcttcttccttatttcactgaagatgaaaaaaagctaatcc2400
agggtacctttgactttttggctttaagccattataccaccatccttgtagactcagaaa2460
aagaagatccaataaaatacaatgattacctagaagtgcaagaaatgaccgacatcacgt2520
ggctcaactcccccagtcaggtggcggtagtgccctgggggttgcgcaaagtgctgaact2580
ggctgaagttcaagtacggagacctccccatgtacataatatccaacggaatcgatgacg2640
ggctgcatgctgaggacgaccagctgagggtgtattatatgcagaattacataaacgaag2700
ctctcaaagcccacatactggatggtatcaatctttgcggatactttgcttattcgttta2760
acgaccgcacagctccgaggtttggcctctatcgttatgctgcagatcagtttgagccca2820
aggcatccatgaaacattacaggaaaattattgacagcaatggtttcccgggcccagaaa2880
ctctggaaagattttgtccagaagaattcaccgtgtgtactgagtgcagtttttttcaca2940
cccgaaagtctttactggctttcatagcttttctattttttgcttctattatttctctct3000
cccttatattttactactcgaagaaaggcagaagaagttacaaatagttctgaacatttt3060
tctattcattcattttgaaataattatgcagacacatcagctgttaaccatttgcacctc3120
taagtgttgtgaaactgtaaatttcatacatttgacttctagaaaacatttttgtggctt3180
atgacagaggttttgaaatgggcataggtgatcgtaaaatattgaataatgcgaatagtg3240
cctgaatttgttctctttttgggtgattaaaaaactgacaggcactataatttctgtaac3300
acactaacaaaagcatgaaaaataggaaccacaccaatgcaacatttgtgcagaaatttg3360
aatgacaagattaggaatattttcttctgcacccacttctaaatttaatgtttttctgga3420
agtagtaattgcaagagttcgaatagaaagttatgtaccaagtaaccatttctcagctgc3480
cataataatgcctagtggcttcccctctgtcaaatctagtttcctatggaaaagaagatg3540
gcagatacaggagagacgacagagggtcctaggctggaatgttcctttcgaaagcaatgc3600
ttctatcaaatactagtattaatttatgtatctggttaatgacatacttggagagcaaat3660
tatggaaatgtgtattttatatgatttttgaggtcctgtctaaaccctgtgtccctgagg3720
gatctgtctcactggcatcttgttgagggccttgcacataggaaacttttgataagtatc3780
tgcggaaaaacaaacatgaatcctgtgatattgggctcttcaggaagcataaagcaattg3840
tgaaatacagtataccgcagtggctctaggtggaggaaaggaggaaaaagtgcttattat3900
gtgcaacattatgattaatctgattatacaccatttttgagcagatcttggaatgaatga3960
catgacctttccctagagaataaggatgaaataatcactcattctatgaacagtgacact4020
actttctattctttagctgtactgtaatttctttgagttgatagttttacaaattcttaa4080
taggttcaaaagcaatctggtctgaataacactggatttgtttctgtgatctctgaggtc4140
tattttatgtttttgctgctacttctgtggaagtagctttgaactagttttactttgaac4200
tttcacgctgaaacatgctagtgatatctagaaagggctaattaggtctcatcctttaat4260
gccccttaaataagtcttgctgattttcagacagggaagtctctctattacactggagct4320
gttttatagataagtcaatattgtatcaggcaagataaaccaatgtcataacaggcattg4380
ccaacctcactgacacagggtcatagtgtataataatatactgtactatataatatatca4440
tctttagaggtatgattttttcatgaaagataagcttttggtaatattcattttaaagtg4500
gacttattaaaattggatgctagagaatcaagtttattttatgtatatatttttctgatt4560
ataagagtaatatatgttcattgtaaaaatttttaaaacacagaaactatatgcaaagaa4620
aaaataaaaattatctataatctcagaacccagaaatagccactattaacatttcctacg4680
tattttattttacatagatcatattgtatatagttagtatctttattaatttttattatg4740
aaactttcctttgtcattattagtcttcaaaagcatgatttttaatagttgttgagtatt4800
ccaccacaggaatgtatcacaacttaaccgttcccgtttgttagactagtttcttattaa4860
tgttgatgaatgttgtttaaaaataattttgttgctacatttactttaatttccttgact4920
gtaaagagaagtaattttgctccttgataaagtattatattaataataaatctgcctgca4980
actttttgccttctttcataatc5003
<210>62
<211>1574
<212>dna
<213>智人
<220>
<223>人sm22-alphamrna
<400>62
tcaccacggcggcagccctttaaacccctcacccagccagcgccccatcctgtctgtccg60
aacccagacacaagtcttcactccttcctgcgagccctgaggaagccttgtgagtgcatt120
ggctggggcttggagggaagttgggctggagctggacaggagcagtgggtgcatttcagg180
caggctctcctgaggtcccaggcgccagctccagctccctggctagggaaacccaccctc240
tcagtcagcatgggggcccaagctccaggcagggtgggctggatcactagcgtcctggat300
ctctctcagactgggcagccccgggctcattgaaatgccccggatgacttggctagtgca360
gaggaattgatggaaaccaccggggtgagagggaggctccccatctcagccagccacatc420
cacaaggtgtgtgtaagggtgcaggcgccggccggttaggccaaggctctactgtctgtt480
gcccctccaggagaacttccaaggagctttccccagacatggccaacaagggtccttcct540
atggcatgagccgcgaagtgcagtccaaaatcgagaagaagtatgacgaggagctggagg600
agcggctggtggagtggatcatagtgcagtgtggccctgatgtgggccgcccagaccgtg660
ggcgcttgggcttccaggtctggctgaagaatggcgtgattctgagcaagctggtgaaca720
gcctgtaccctgatggctccaagccggtgaaggtgcccgagaacccaccctccatggtct780
tcaagcagatggagcaggtggctcagttcctgaaggcggctgaggactatggggtcatca840
agactgacatgttccagactgttgacctctttgaaggcaaagacatggcagcagtgcaga900
ggaccctgatggctttgggcagcttggcagtgaccaagaatgatgggcactaccgtggag960
atcccaactggtttatgaagaaagcgcaggagcataagagggaattcacagagagccagc1020
tgcaggagggaaagcatgtcattggccttcagatgggcagcaacagaggggcctcccagg1080
ccggcatgacaggctacggacgacctcggcagatcatcagttagagcggagagggctagc1140
cctgagcccggccctcccccagctccttggctgcagccatcccgcttagcctgcctcacc1200
cacacccgtgtggtaccttcagccctggccaagctttgaggctctgtcactgagcaatgg1260
taactgcacctgggcagctcctccctgtgcccccagcctcagcccaacttcttacccgaa1320
agcatcactgccttggcccctccctcccggctgcccccatcacctctactgtctcctccc1380
tgggctaagcaggggagaagcgggctgggggtagcctggatgtgggccaagtccactgtc1440
ctccttggcggcaaaagcccattgaagaagaaccagcccagcctgccccctatcttgtcc1500
tggaatatttttggggttggaactcaaaaaaaaaaaaaaaaaatcaatcttttctcaaaa1560
aaaaaaaaaaaaaa1574
<210>63
<211>521
<212>prt
<213>智人
<220>
<223>人runx2蛋白
<400>63
metalaserasnserleupheserthrvalthrprocysglnglnasn
151015
phephetrpaspproserthrserargargpheserproproserser
202530
serleuglnproglylysmetseraspvalserprovalvalalaala
354045
glnglnglnglnglnglnglnglnglnglnglnglnglnglnglngln
505560
glnglnglnglnglnglnglnglualaalaalaalaalaalaalaala
65707580
alaalaalaalaalaalaalaalaalavalproargleuargpropro
859095
hisaspasnargthrmetvalgluileilealaasphisproalaglu
100105110
leuvalargthraspserproasnpheleucysservalleuproser
115120125
histrpargcysasnlysthrleuprovalalaphelysvalvalala
130135140
leuglygluvalproaspglythrvalvalthrvalmetalaglyasn
145150155160
aspgluasntyrseralagluleuargasnalaseralavalmetlys
165170175
asnglnvalalaargpheasnaspleuargphevalglyargsergly
180185190
argglylysserphethrleuthrilethrvalphethrasnpropro
195200205
glnvalalathrtyrhisargalailelysvalthrvalaspglypro
210215220
arggluproargarghisargglnlysleuaspaspserlysproser
225230235240
leupheseraspargleuseraspleuglyargileprohisproser
245250255
metargvalglyvalproproglnasnproargproserleuasnser
260265270
alaproserpropheasnproglnglyglnserglnilethrasppro
275280285
argglnalaglnserserproprotrpsertyraspglnsertyrpro
290295300
sertyrleuserglnmetthrserproserilehisserthrthrpro
305310315320
leuserserthrargglythrglyleuproalailethraspvalpro
325330335
argargileseraspaspaspthralathrseraspphecysleutrp
340345350
proserthrleuserlyslysserglnalaglyalasergluleugly
355360365
propheseraspproargglnpheproserileserserleuthrglu
370375380
serargpheserasnproargmethistyrproalathrphethrtyr
385390395400
thrproprovalthrserglymetserleuglymetseralathrthr
405410415
histyrhisthrtyrleuproproprotyrproglyserserglnser
420425430
glnserglypropheglnthrserserthrprotyrleutyrtyrgly
435440445
thrserserglysertyrglnpheprometvalproglyglyasparg
450455460
serproserargmetleuproprocysthrthrthrserasnglyser
465470475480
thrleuleuasnproasnleuproasnglnasnaspglyvalaspala
485490495
aspglyserhisserserserprothrvalleuasnserserglyarg
500505510
metaspgluservaltrpargprotyr
515520
<210>64
<211>524
<212>prt
<213>智人
<220>
<223>人alp蛋白
<400>64
metileserpropheleuvalleualaileglythrcysleuthrasn
151015
serleuvalproglulysglulysaspprolystyrtrpargaspgln
202530
alaglngluthrleulystyralaleugluleuglnlysleuasnthr
354045
asnvalalalysasnvalilemetpheleuglyaspglymetglyval
505560
serthrvalthralaalaargileleulysglyglnleuhishisasn
65707580
proglyglugluthrargleuglumetasplyspheprophevalala
859095
leuserlysthrtyrasnthrasnalaglnvalproaspseralagly
100105110
thralathralatyrleucysglyvallysalaasngluglythrval
115120125
glyvalseralaalathrgluargserargcysasnthrthrglngly
130135140
asngluvalthrserileleuargtrpalalysaspalaglylysser
145150155160
valglyilevalthrthrthrargvalasnhisalathrproserala
165170175
alatyralahisseralaaspargasptrptyrseraspasnglumet
180185190
proproglualaleuserglnglycyslysaspilealatyrglnleu
195200205
methisasnileargaspileaspvalilemetglyglyglyarglys
210215220
tyrmettyrprolysasnlysthraspvalglutyrgluseraspglu
225230235240
lysalaargglythrargleuaspglyleuaspleuvalaspthrtrp
245250255
lysserphelysproargtyrlyshisserhispheiletrpasnarg
260265270
thrgluleuleuthrleuaspprohisasnvalasptyrleuleugly
275280285
leuphegluproglyaspmetglntyrgluleuasnargasnasnval
290295300
thraspproserleuserglumetvalvalvalalaileglnileleu
305310315320
arglysasnprolysglyphepheleuleuvalgluglyglyargile
325330335
asphisglyhishisgluglylysalalysglnalaleuhisgluala
340345350
valglumetaspargalaileglyglnalaglyserleuthrserser
355360365
gluaspthrleuthrvalvalthralaasphisserhisvalphethr
370375380
pheglyglytyrthrproargglyasnserilepheglyleualapro
385390395400
metleuseraspthrasplyslysprophethralaileleutyrgly
405410415
asnglyproglytyrlysvalvalglyglygluarggluasnvalser
420425430
metvalasptyralahisasnasntyrglnalaglnseralavalpro
435440445
leuarghisgluthrhisglyglygluaspvalalavalpheserlys
450455460
glyprometalahisleuleuhisglyvalhisgluglnasntyrval
465470475480
prohisvalmetalatyralaalacysileglyalaasnleuglyhis
485490495
cysalaproalaserseralaglyserleualaalaglyproleuleu
500505510
leualaleualaleutyrproleuservalleuphe
515520
<210>65
<211>431
<212>prt
<213>智人
<220>
<223>人osterix蛋白
<400>65
metalaserserleuleugluglugluvalhistyrglyserserpro
151015
leualametleuthralaalacysserlyspheglyglyserserpro
202530
leuargaspserthrthrleuglylysalaglythrlyslysprotyr
354045
servalglyseraspleuseralaserlysthrmetglyaspalatyr
505560
proalaprophethrserthrasnglyleuleuserproalaglyser
65707580
proproalaprothrserglytyralaasnasptyrpropropheser
859095
hisserpheproglyprothrglythrglnaspproglyleuleuval
100105110
prolysglyhisserserseraspcysleuproservaltyrthrser
115120125
leuaspmetthrhisprotyrglysertrptyrlysalaglyilehis
130135140
alaglyileserproglyproglyasnthrprothrprotrptrpasp
145150155160
methisproglyglyasntrpleuglyglyglyglnglyglnglyasp
165170175
glyleuglnglythrleuprothrglyproalaglnproproleuasn
180185190
proglnleuprothrtyrproseraspphealaproleuasnproala
195200205
protyrproalaprohisleuleuglnproglyproglnhisvalleu
210215220
proglnaspvaltyrlysprolysalavalglyasnserglyglnleu
225230235240
gluglyserglyglyalalysproproargglyalaserthrglygly
245250255
serglyglytyrglyglyserglyalaglyargsersercysaspcys
260265270
proasncysglngluleugluargleuglyalaalaalaalaglyleu
275280285
arglyslysproilehissercyshisileproglycysglylysval
290295300
tyrglylysalaserhisleulysalahisleuargtrphisthrgly
305310315320
gluargprophevalcysasntrpleuphecysglylysargphethr
325330335
argseraspgluleugluarghisvalargthrhisthrargglulys
340345350
lysphethrcysleuleucysserlysargphethrargserasphis
355360365
leuserlyshisglnargthrhisglygluproglyproglypropro
370375380
proserglyprolysgluleuglygluglyargserthrglygluglu
385390395400
glualaserglnthrproargproseralaserproalathrproglu
405410415
lysalaproglyglyserprogluglnserasnleuleugluile
420425430
<210>66
<211>1012
<212>prt
<213>智人
<220>
<223>人klotho蛋白
<400>66
metproalaseralaproproargargproargproproproproser
151015
leuserleuleuleuvalleuleuglyleuglyglyargargleuarg
202530
alagluproglyaspglyalaglnthrtrpalaargpheserargpro
354045
proalaproglualaalaglyleupheglnglythrpheproaspgly
505560
pheleutrpalavalglyseralaalatyrglnthrgluglyglytrp
65707580
glnglnhisglylysglyalaseriletrpaspthrphethrhishis
859095
proleualaproproglyaspserargasnalaserleuproleugly
100105110
alaproserproleuglnproalathrglyaspvalalaseraspser
115120125
tyrasnasnvalpheargaspthrglualaleuarggluleuglyval
130135140
thrhistyrargpheserilesertrpalaargvalleuproasngly
145150155160
seralaglyvalproasnarggluglyleuargtyrtyrargargleu
165170175
leugluargleuarggluleuglyvalglnprovalvalthrleutyr
180185190
histrpaspleuproglnargleuglnaspalatyrglyglytrpala
195200205
asnargalaleualaasphispheargasptyralagluleucysphe
210215220
arghispheglyglyglnvallystyrtrpilethrileaspasnpro
225230235240
tyrvalvalalatrphisglytyralathrglyargleualaprogly
245250255
ileargglyserproargleuglytyrleuvalalahisasnleuleu
260265270
leualahisalalysvaltrphisleutyrasnthrserpheargpro
275280285
thrglnglyglyglnvalserilealaleuserserhistrpileasn
290295300
proargargmetthrasphisserilelysglucysglnlysserleu
305310315320
aspphevalleuglytrpphealalysprovalpheileaspglyasp
325330335
tyrproglusermetlysasnasnleuserserileleuproaspphe
340345350
thrgluserglulyslyspheilelysglythralaaspphepheala
355360365
leucyspheglyprothrleuserpheglnleuleuaspprohismet
370375380
lyspheargglnleugluserproasnleuargglnleuleusertrp
385390395400
ileaspleuglupheasnhisproglnilepheilevalgluasngly
405410415
trpphevalserglythrthrlysargaspaspalalystyrmettyr
420425430
tyrleulyslyspheilemetgluthrleulysalailelysleuasp
435440445
glyvalaspvalileglytyrthralatrpserleumetaspglyphe
450455460
glutrphisargglytyrserileargargglyleuphetyrvalasp
465470475480
pheleuserglnasplysmetleuleuprolysserseralaleuphe
485490495
tyrglnlysleuileglulysasnglypheproproleuprogluasn
500505510
glnproleugluglythrpheprocysaspphealatrpglyvalval
515520525
aspasntyrileglnvalaspthrthrleuserglnphethraspleu
530535540
asnvaltyrleutrpaspvalhishisserlysargleuilelysval
545550555560
aspglyvalvalthrlyslysarglyssertyrcysvalasppheala
565570575
alaileglnproglnilealaleuleuglnglumethisvalthrhis
580585590
pheargpheserleuasptrpalaleuileleuproleuglyasngln
595600605
serglnvalasnhisthrileleuglntyrtyrargcysmetalaser
610615620
gluleuvalargvalasnilethrprovalvalalaleutrpglnpro
625630635640
metalaproasnglnglyleuproargleuleualaargglnglyala
645650655
trpgluasnprotyrthralaleualaphealaglutyralaargleu
660665670
cyspheglngluleuglyhishisvallysleutrpilethrmetasn
675680685
gluprotyrthrargasnmetthrtyrseralaglyhisasnleuleu
690695700
lysalahisalaleualatrphisvaltyrasnglulysphearghis
705710715720
alaglnasnglylysileserilealaleuglnalaasptrpileglu
725730735
proalacyspropheserglnlysasplysgluvalalagluargval
740745750
leuglupheaspileglytrpleualagluproilepheglysergly
755760765
asptyrprotrpvalmetargasptrpleuasnglnargasnasnphe
770775780
leuleuprotyrphethrgluaspglulyslysleuileglnglythr
785790795800
pheasppheleualaleuserhistyrthrthrileleuvalaspser
805810815
glulysgluaspproilelystyrasnasptyrleugluvalglnglu
820825830
metthraspilethrtrpleuasnserproserglnvalalavalval
835840845
protrpglyleuarglysvalleuasntrpleulysphelystyrgly
850855860
aspleupromettyrileileserasnglyileaspaspglyleuhis
865870875880
alagluaspaspglnleuargvaltyrtyrmetglnasntyrileasn
885890895
glualaleulysalahisileleuaspglyileasnleucysglytyr
900905910
phealatyrserpheasnaspargthralaproargpheglyleutyr
915920925
argtyralaalaaspglnphegluprolysalasermetlyshistyr
930935940
arglysileileaspserasnglypheproglyprogluthrleuglu
945950955960
argphecysproglugluphethrvalcysthrglucysserphephe
965970975
histhrarglysserleuleualapheilealapheleuphepheala
980985990
serileileserleuserleuilephetyrtyrserlyslysglyarg
99510001005
argsertyrlys
1010
<210>67
<211>201
<212>prt
<213>智人
<220>
<223>人sm22-alpha蛋白
<400>67
metalaasnlysglyprosertyrglymetserarggluvalglnser
151015
lysileglulyslystyraspglugluleuglugluargleuvalglu
202530
trpileilevalglncysglyproaspvalglyargproasparggly
354045
argleuglypheglnvaltrpleulysasnglyvalileleuserlys
505560
leuvalasnserleutyrproaspglyserlysprovallysvalpro
65707580
gluasnproprosermetvalphelysglnmetgluglnvalalagln
859095
pheleulysalaalagluasptyrglyvalilelysthraspmetphe
100105110
glnthrvalaspleuphegluglylysaspmetalaalavalglnarg
115120125
thrleumetalaleuglyserleualavalthrlysasnaspglyhis
130135140
tyrargglyaspproasntrpphemetlyslysalaglngluhislys
145150155160
arggluphethrgluserglnleuglngluglylyshisvalilegly
165170175
leuglnmetglyserasnargglyalaserglnalaglymetthrgly
180185190
tyrglyargproargglnileileser
195200
<210>68
<211>377
<212>prt
<213>智人
<220>
<223>人alpha-sma蛋白
<400>68
metcysgluglugluaspserthralaleuvalcysaspasnglyser
151015
glyleucyslysalaglyphealaglyaspaspalaproargalaval
202530
pheproserilevalglyargproarghisglnglyvalmetvalgly
354045
metglyglnlysaspsertyrvalglyaspglualaglnserlysarg
505560
glyileleuthrleulystyrproilegluhisglyileilethrasn
65707580
trpaspaspmetglulysiletrphishisserphetyrasngluleu
859095
argvalalaproglugluhisprothrleuleuthrglualaproleu
100105110
asnprolysalaasnargglulysmetthrglnilemetphegluthr
115120125
pheasnvalproalamettyrvalalaileglnalavalleuserleu
130135140
tyralaserglyargthrthrglyilevalleuaspserglyaspgly
145150155160
valthrhisasnvalproiletyrgluglytyralaleuprohisala
165170175
ilemetargleuaspleualaglyargaspleuthrasptyrleumet
180185190
lysileleuthrgluargglytyrserphevalthrthralagluarg
195200205
gluilevalargaspilelysglulysleucystyrvalalaleuasp
210215220
phegluasnglumetalathralaalaserserserserleuglulys
225230235240
sertyrgluleuproaspglyglnvalilethrileglyasngluarg
245250255
pheargcysprogluthrleupheglnproserpheileglymetglu
260265270
seralaglyilehisgluthrthrtyrasnserilemetlyscysasp
275280285
ileaspilearglysaspleutyralaasnasnvalleuserglygly
290295300
thrthrmettyrproglyilealaaspargmetglnlysgluilethr
305310315320
alaleualaproserthrmetlysilelysileilealaproproglu
325330335
arglystyrservaltrpileglyglyserileleualaserleuser
340345350
thrpheglnglnmettrpileserlysglnglutyraspglualagly
355360365
proserilevalhisarglyscysphe
370375
<210>69
<211>986
<212>prt
<213>智人
<220>
<223>人myocd蛋白
<400>69
metthrleuleuglysergluhisserleuleuileargserlysphe
151015
argservalleuglnleuargleuglnglnargargthrglnglugln
202530
leualaasnglnglyileileproproleulysargproalagluphe
354045
hisgluglnarglyshisleuaspserasplysalalysasnserleu
505560
lysarglysalaargasnargcysasnseralaaspleuvalasnmet
65707580
hisileleuglnalaserthralagluargserileprothralagln
859095
metlysleulysargalaargleualaaspaspleuasnglulysile
100105110
alaleuargproglyproleugluleuvalglulysasnileleupro
115120125
valaspseralavallysglualailelysglyasnglnvalserphe
130135140
serlysserthraspalaphealapheglugluaspserserserasp
145150155160
glyleuserproaspglnthrargsergluaspproglnasnserala
165170175
glyserproproaspalalysalaseraspthrproserthrglyser
180185190
leuglythrasnglnaspleualaserglysergluasnaspargasn
195200205
aspseralaserglnproserhisglnseraspalaglylysglngly
210215220
leuglyproproserthrproilealavalhisalaalavallysser
225230235240
lysserleuglyaspserlysasnarghislyslysprolysasppro
245250255
lysprolysvallyslysleulystyrhisglntyrileproproasp
260265270
glnlysalaglulysserproproprometaspseralatyralaarg
275280285
leuleuglnglnglnglnleupheleuglnleuglnileleusergln
290295300
glnglnglnglnglnglnhisargphesertyrleuglymethisgln
305310315320
alaglnleulysgluproasngluglnmetvalargasnproasnser
325330335
serserthrproleuserasnthrproleuserprovallysasnser
340345350
pheserglyglnthrglyvalserserphelysproglyproleupro
355360365
proasnleuaspaspleulysvalsergluleuargglnglnleuarg
370375380
ileargglyleuprovalserglythrlysthralaleumetasparg
385390395400
leuargpropheglnaspcysserglyasnprovalproasnphegly
405410415
aspilethrthrvalthrpheprovalthrproasnthrleuproasn
420425430
tyrglnserserserserthrseralaleuserasnglyphetyrhis
435440445
pheglyserthrserserserproproileserproalaserserasp
450455460
leuservalalaglyserleuproaspthrpheasnaspalaserpro
465470475480
serpheglyleuhisproserprovalhisvalcysthrglugluser
485490495
leumetserserleuasnglyglyservalprosergluleuaspgly
500505510
leuaspserglulysasplysmetleuvalglulysglnlysvalile
515520525
asngluleuthrtrplysleuglnglngluglnargglnvalgluglu
530535540
leuargmetglnleuglnlysglnlysargasnasncysserglulys
545550555560
lysproleupropheleualaalaserilelysglngluglualaval
565570575
sersercysprophealaserglnvalprovallysargglnserser
580585590
serserglucyshisproproalacysglualaalaglnleuglnpro
595600605
leuglyasnalahiscysvalgluserseraspglnthrasnvalleu
610615620
serserthrpheleuserproglncysserproglnhisserproleu
625630635640
glyalavallysserproglnhisileserleuproproserproasn
645650655
asnprohispheleuproserserserglyalaglnglygluglyhis
660665670
argvalserserproileserserglnvalcysthralaglnasnser
675680685
glyalahisaspglyhisproproserpheserprohisserserser
690695700
leuhispropropheserglyalaglnalaaspserserhisglyala
705710715720
glyglyasnprocysprolysserprocysvalglnglnlysmetala
725730735
glyleuhisserserasplysvalglyprolyspheserileproser
740745750
prothrpheserlysserserseralailesergluvalthrglnpro
755760765
prosertyrgluaspalavallysglnglnmetthrargserglngln
770775780
metaspgluleuleuaspvalleuilegluserglyglumetproala
785790795800
aspalaarggluasphissercysleuglnlysvalprolysilepro
805810815
argserserargserprothralavalleuthrlysproseralaser
820825830
phegluglnalaserserglyserglnilepropheaspprotyrala
835840845
thraspseraspgluhisleugluvalleuleuasnserglnserpro
850855860
leuglylysmetseraspvalthrleuleulysileglysergluglu
865870875880
prohispheaspglyilemetaspglypheserglylysalaalaglu
885890895
aspleupheasnalahisgluileleuproglyproleuserpromet
900905910
glnthrglnpheserproserservalaspserasnglyleuglnleu
915920925
serphethrgluserprotrpgluthrmetglutrpleuaspleuthr
930935940
proproasnserthrproglypheseralaleuthrthrserserpro
945950955960
serilepheasnileasppheleuaspvalthraspleuasnleuasn
965970975
sersermetaspleuhisleuglnglntrp
980985
<210>70
<211>1798
<212>dna
<213>智人
<220>
<223>人alpha-smamrna
<400>70
ctctccccgcccccgcggggcggcgcgcactcacccacccgcgccggagcggacctttgg60
cttggcttgtcagggcttgtccaggagttccgctcctctctccaaccggggtccccctcc120
agcgaccctaaagcttcccagacttccgcttcaattcctgtccgcaccccacgcccacct180
caacgtggagcgcagtggtctccgaggagcgccggagctgccccgcctgcccagcggggt240
cagcacttcgcatcaaggcccaagaaaagcaagtcctccagcgttctgagcacccgggcc300
tgagggaaggtcctaacagcccccgggagccagtctccaacgcctcccgcagcagcccgc360
cgctcccaggtgcccgcgtgcgccgctgccgccgcaatcccgcacgcgtcccgcgcccgc420
cccactttgcctatccccgggactaagacgggaatcctgtgaagcagctccagctatgtg480
tgaagaagaggacagcactgccttggtgtgtgacaatggctctgggctctgtaaggccgg540
ctttgctggggacgatgctcccagggctgttttcccatccattgtgggacgtcccagaca600
tcagggggtgatggtgggaatgggacaaaaagacagctacgtgggtgacgaagcacagag660
caaaagaggaatcctgaccctgaagtacccgatagaacatggcatcatcaccaactggga720
cgacatggaaaagatctggcaccactctttctacaatgagcttcgtgttgcccctgaaga780
gcatcccaccctgctcacggaggcacccctgaaccccaaggccaaccgggagaaaatgac840
tcaaattatgtttgagactttcaatgtcccagccatgtatgtggctatccaggcggtgct900
gtctctctatgcctctggacgcacaactggcatcgtgctggactctggagatggtgtcac960
ccacaatgtccccatctatgagggctatgccttgccccatgccatcatgcgtctggatct1020
ggctggccgagatctcactgactacctcatgaagatcctgactgagcgtggctattcctt1080
cgttactactgctgagcgtgagattgtccgggacatcaaggagaaactgtgttatgtagc1140
tctggactttgaaaatgagatggccactgccgcatcctcatcctcccttgagaagagtta1200
cgagttgcctgatgggcaagtgatcaccatcggaaatgaacgtttccgctgcccagagac1260
cctgttccagccatccttcatcgggatggagtctgctggcatccatgaaaccacctacaa1320
cagcatcatgaagtgtgatattgacatcaggaaggacctctatgctaacaatgtcctatc1380
agggggcaccactatgtaccctggcattgccgaccgaatgcagaaggagatcacggccct1440
agcacccagcaccatgaagatcaagatcattgcccctccggagcgcaaatactctgtctg1500
gatcggtggctccatcctggcctctctgtccaccttccagcagatgtggatcagcaaaca1560
ggaatacgatgaagccgggccttccattgtccaccgcaaatgcttctaaaacactttcct1620
gctcctctctgtctctagcacacaactgtgaatgtcctgtggaattatgccttcagttct1680
tttccaaatcattcctagccaaagctctgactcgttacctatgtgttttttaataaatct1740
gaaataggctactggtaaaaaaaaaaaaaaaaaaaaaaaaaaaaaaaaaaaaaaaaaa1798
<210>71
<211>8580
<212>dna
<213>智人
<220>
<223>人myocdmrna
<400>71
aatcgccggcagcctatgacatcagacaggaacgcctgggatgccgcgctgctcctggcc60
aacctccgaggaggaggagggtcccgccggctaagagttaattagccccgcacggcgagg120
ggggaggcgccagttttctggggacactggctgccactgtactcctacccaggggagctc180
acggagagttggatgaattctgggttgttagctgcggtcagctgggctcccgggagcctg240
ttgctggtggagaacagggggcgcctggccaagggaccagcggcttgctgagactcaaca300
tgacactcctggggtctgagcattccttgctgattaggagcaagttcagatcagttttac360
agttaagacttcaacaaagaaggacccaggaacaactggctaaccaaggcataataccac420
cactgaaacgtccagctgaattccatgagcaaagaaaacatttggatagtgacaaggcta480
aaaattccctgaagcgcaaagccagaaacaggtgcaacagtgccgacttggttaatatgc540
acatactccaagcttccactgcagagaggtccattccaactgctcagatgaagctgaaaa600
gagcccgactcgccgatgatctcaatgaaaaaattgctctacgaccagggccactggagc660
tggtggaaaaaaacattcttcctgtggattctgctgtgaaagaggccataaaaggtaacc720
aggtgagtttctccaaatccacggatgcttttgcctttgaagaggacagcagcagcgatg780
ggctttctccggatcagactcgaagtgaagacccccaaaactcagcgggatccccgccag840
acgctaaagcctcagataccccttcgacaggttctctggggacaaaccaggatcttgctt900
ctggctcagaaaatgacagaaatgactcagcctcacagcccagccaccagtcagatgcgg960
ggaagcaggggcttggcccccccagcacccccatagccgtgcatgctgctgtaaagtcca1020
aatccttgggtgacagtaagaaccgccacaaaaagcccaaggaccccaagccaaaggtga1080
agaagcttaaatatcaccagtacattcccccagaccagaaggcagagaagtcccctccac1140
ctatggactcagcctacgctcggctgctccagcaacagcagctgttcctgcagctccaaa1200
tcctcagccagcagcagcagcagcagcaacaccgattcagctacctagggatgcaccaag1260
ctcagcttaaggaaccaaatgaacagatggtcagaaatccaaactcttcttcaacgccac1320
tgagcaatacccccttgtctcctgtcaaaaacagtttttctggacaaactggtgtctctt1380
ctttcaaaccaggcccactcccacctaacctggatgatctgaaggtctctgaattaagac1440
aacagcttcgaattcggggcttgcctgtgtcaggcaccaaaacggctctcatggaccggc1500
ttcgacccttccaggactgctctggcaacccagtgccgaactttggggatataacgactg1560
tcacttttcctgtcacacccaacacgctgcccaattaccagtcttcctcttctaccagtg1620
ccctgtccaacggcttctaccactttggcagcaccagctccagccccccgatctccccag1680
cctcctctgacctgtcagtcgctgggtccctgccggacaccttcaatgatgcctccccct1740
ccttcggcctgcacccgtccccagtccacgtgtgcacggaggaaagtctcatgagcagcc1800
tgaatgggggctctgttccttctgagctggatgggctggactccgagaaggacaagatgc1860
tggtggagaagcagaaggtgatcaatgaactcacctggaaactccagcaagagcagaggc1920
aggtggaggagctgaggatgcagcttcagaagcagaaaaggaataactgttcagagaaga1980
agccgctgcctttcctggctgcctccatcaagcaggaagaggctgtctccagctgtcctt2040
ttgcatcccaagtacctgtgaaaagacaaagcagcagctcagagtgtcacccaccggctt2100
gtgaagctgctcaactccagcctcttggaaatgctcattgtgtggagtcctcagatcaaa2160
ccaatgtactttcttccacatttctcagcccccagtgttcccctcagcattcaccgctgg2220
gggctgtgaaaagcccacagcacatcagtttgcccccatcacccaacaaccctcactttc2280
tgccctcatcctccggggcccagggagaagggcacagggtctcctcgcccatcagcagcc2340
aggtgtgcactgcacagaactcaggagcacacgatggccatcctccaagcttctctcccc2400
attcttccagcctccacccgcccttctctggagcccaagcagacagcagtcatggtgccg2460
ggggaaacccttgtcccaaaagcccatgtgtacagcaaaagatggctggtttacactctt2520
ctgataaggtggggccaaagttttcaattccatccccaactttttctaagtcaagttcag2580
caatttcagaggtaacacagcctccatcctatgaagatgccgtaaagcagcaaatgaccc2640
ggagtcagcagatggatgaactcctggacgtgcttattgaaagcggagaaatgccagcag2700
acgctagagaggatcactcatgtcttcaaaaagtcccaaagatacccagatcttcccgaa2760
gtccaactgctgtcctcaccaagccctcggcttcctttgaacaagcctcttcaggcagcc2820
agatcccctttgatccctatgccaccgacagtgatgagcatcttgaagtcttattaaatt2880
cccagagccccctaggaaagatgagtgatgtcacccttctaaaaattgggagcgaagagc2940
ctcactttgatgggataatggatggattctctgggaaggctgcagaagacctcttcaatg3000
cacatgagatcttgccaggccccctctctccaatgcagacacagttttcaccctcttctg3060
tggacagcaatgggctgcagttaagcttcactgaatctccctgggaaaccatggagtggc3120
tggacctcactccgccaaattccacaccaggctttagcgccctcaccaccagcagcccca3180
gcatcttcaacatcgatttcctggatgtcactgatctcaatttgaattcttccatggacc3240
ttcacttgcagcagtggtagaatgcccaatgcaccagtgctatggaagaccaatggagtt3300
ccatgggggaaagcacacagccatacatactttactgtccaaaaacagaagaagaagaag3360
agaattaaaaagaagcaatgatttctgtgccaatgaacaagaacaaaagtcatttttaga3420
aatacatatactgtaatatttaccaacagtcagtaactgttaatgatttcaacaatgcat3480
taaaagaatgtgctttctcagattaaggatgccaaaaaagatatttcactgccttttcaa3540
agaccagtatattttctagcccataatttttctcaggcattgttggggcataagctcaca3600
ctgtaagcttttctcatgaattcactagacataacgtggaaggaaaacgtagtcttttgg3660
gagtacagggaagccagcccctcaaagcttatggaagacatacctgcaatggaagctgtt3720
gcccaatgtctccattactatctttcaaaagagaagccagacccagcttcagatcaaaag3780
ttcttgagacagaggaacaaaaccaatcgatttccagggaagctaatcaactctcttttc3840
cctctaccacaaaactgccctgctggagtggttctgaacctgtacccaggactcgatgtg3900
gtcactaataacaattaacctgaactgagtccacagaactccactcggaactttcttctt3960
ttttaactagtggcccaatcattcccaccatctctgtgctgataagtacgtgtcctagat4020
gagaaccctgaagaatgcagaccttcttcccccgaaggagatgccacaagctctccaaca4080
cagccccctttagttccaaagactagagatgaccacattggtagaagtatatctcgaggc4140
acaggaagggagccccaccagggataattcagacaggactagagaataacatcatttcac4200
ataccctgggataaacaccctgggttcctatagaaggactattacttatgggagtccaac4260
ttctccttttgttttgttattatcagtttatctttctcccactccacttttccttcaagg4320
taccaatcctttcctgttcctcgtttggccatctttctttttctgcctccacattgggag4380
gggaggacttctcagttctaacaagctgccatactcctaagaaagccatttttgaaaaat4440
ttaacaatccaggttcttctggagaactcattctccacacgcacagtttgctgcaaaagg4500
aagttgcaagaatttcttgaggaagaaactggtgacttggtccatcagtcacgaagttct4560
ttctattctcgtttagttttcaagaaattattggtttgtgttgctctggggaaattggaa4620
atcattacattgtaaagacaaatatggatgatatttacaagagagaatttcagatctggg4680
tttttgaaagaaaacagaattgcgcattgaaaacgatggaaggaaaaagacaatggtcta4740
atgtgcattcctcattacctctcgtggctttggctgggagttggaaaaagctaaaatttc4800
agaacagtctctgtaaggctctctgtggctccagttcaccattttatattgttgcatgct4860
gtagaaaggagctattgctgttgttttgtttttttatttaaatcactaaggcactgtttt4920
tatcttttgtaaaaaaaaaaaaaaagttgttcactgtgcacttatagaaaaaataatcaa4980
aaatgttgggattttagaagctctctttttgataaaccaaagatttagaagtcattccat5040
tgttaacttgtaaaaatgtgtgaacacagagagtttttggtgattgctactctgaaagct5100
gccagatcttattctgggggtgggatgtggaggaatacacatacacacacaaacatacat5160
gtatgtataatagatatatacatatgtgtatattatatctgtgtgtgcatgtatctccaa5220
aagcggcgttacagagttctacaccaaaagcctttaacccttaatctgctgtgaatgata5280
cctggcctttctcactatgaatttctgattaaccaaccagactacacgttgcctctctgt5340
gtatgactaacggctccaacccgatgactcacagctacttgcttatcgtgaacaagctca5400
tcttggcaatgaatatggatgtgaaaagacagaacagcttcaccattagtagctggaaat5460
ggtatcacagtctcttatagaggaatatgaaaggaacaagaaaatcattttacattcctt5520
ttatctgtattgtgctttaaaagatccacatggtaaattttttattttgcttttatgtca5580
gtcatcagaaccaaaaaaatccagaagaaaaaattgccagtgtttcctttgaagatgaag5640
ctactggggaagaaaaccttattaatacactccacacatttgttcattcctcagctgttg5700
gtgttttcttggggtcttgacaaagcttgctggtcagtgcacttttcaggtgtcacgttt5760
tgctgtttgtatgttttttcttccccttacttcctttggaaaacaaactcacacagtgcc5820
cctactctgagacctgggactgagtgttaattattttttccttgggtatttctatctgag5880
agactagacctagttaggaggcctctgtacttctccagattgtacctttttatggggatc5940
tttgaggctatgacccaggactgatagatatgccttacggaagacaaaagataaaatggt6000
tcctatatcctaatgcaaaccaacacagttaaaagagcagatctctggataactgctctc6060
aacctgcttctacagtctccacaaaccgcattcaccctctctcttcatagctcagacatg6120
aaatttgagggagaaaactggagataattgggagaaaattgatgaagttggctgcttcca6180
gtagatcagataatccatgaatttgtctcccattgagaattttattttaaattcttttaa6240
actcttcgttgtgtcttttgtgatgacaaatcaggcatgactaaaagatgtacagagact6300
tacgaagatggtcacattcaagttccctaatgctcttagaacctgaagatgaccatgtgt6360
agttttcttaagacctctgaacccccatggtgatgaagacttgaagacatttgcagctat6420
ctgctgcagtctggtagattcatacttatctaaagaagtcaaaaaatttattcgtgcaag6480
tgcttgcaggaagccagtgcttattagtagtgaccctgcttctatcaacgttattgagac6540
aacacatattctattctaagggagaaagagggaggaagagagggagggagggaggaagaa6600
gagggagggagcgaggaaggaagataggagatgggtaggggggtaaagagaaaaggaggg6660
agaagggaaggaaggaaagaagagaggaaagaaaggagggaaggaaaaaagggccaaact6720
ttctgatctatgaacttctcagttcagctgtcacattatgagaagtaaatcagaattttt6780
ttaaggagaagtcattcttagcactacaataattgtaccagtaattgaggaaaccaagac6840
aatcttcacctgaataatagagggtctgagaactgtcagccttttgccattcaaaaacat6900
ttatgtccaacctgaaaaaaaagcatcaataaaacctatcccaagcattcaaaatagtcc6960
tttccaaatgttatttattttaaagtcaatcagctcttttagaaacagattctggtctgg7020
ctgaaaactcccacaacaaatttactcatccagtggctaatatttaatgcccaccatggg7080
cagagcacacaaatcttcagataaacaatactgaattgattcagcacagattgttcagat7140
ttgaatgaccagggagttgtatttgcacatgcaagaacactaagaatctcccagtcctca7200
aactagaaacctttcagctacgatgaaaaaaaaaaaggggtcttcatttttccaagaggg7260
ggtggaggtggggatcactttttagctaaaagctatctctcacttcaaaattcttgtctt7320
tttctttgtggacaaacaccagtagtctatcacttggagatcttttaatatctcccatca7380
tttaaaacatccacgagagtttgaagatttgtgttgattgccagatacagaagccccttg7440
aaaataaggaaagggtggaggaagcatttttgtgtcctatccctacttatcgtagcagct7500
ctatagacaaaagggacacttactggtgagcctctggcccttaaaagaaaatcatctaag7560
aatatgaaggcaatttgatttccccccacagccctcagctgccttcctcacagaaggaag7620
ttcccaaaattgctggtacacagtttgcaatcaaatatcagatatgagaaaacctgtagt7680
gaagagtctgggttcttggttttctcataaatccaatataaatttgtaggttggttcagg7740
gtcaaaattgccagtgctttattagacagatgatactgatagacacacagagcccaggtc7800
ctggaacaagacaatcctgtagtgccaagatctggtcagttgcgttaaggagctgggttt7860
gattctagagtccaggtttatagagaaaccctggctagattgagcctacccatggggaga7920
cgatttcaagacaggatgagatctgggaagaattttgttgtcatctgccagggaaattat7980
cacaggactcattgaatgcaataacatgtgagtaagttcccttttgattctgggaatcag8040
cgattttccctgtggattaagacaaaccaacgccagaaggtctcctgtgcttattttaac8100
catctgctcccatcgtgaaccctggagcatgcatttcctagaagtggtttcatagctcct8160
gtgtgttcatggaaaaggggagtataatgatggggatgctggaagcttttttaatgtttt8220
ccaaaggaaaggaacccacactgctccccagagttcctttccaatggccctgcagtaaga8280
acggaggacaatgtattgctgggtgcttaaaatcctccctcagtgaagcacaaagagaca8340
ctttgtaaagaaaaaaagagcaagcataggttctctgtgggaccttgtggagtggtgttt8400
tcacgttggtctctttggctcaattgagcataatcagaaagaaatgtgggttattgggaa8460
gagacaaaaagcagtggctaaaataccaaagttggcatgtgttcttttttaaaaaaaaaa8520
aaaaatgcatatatttttaaataaaatgtttattttaaaaagaaaaaaaaaaaaaaaaaa8580
<210>72
<211>524
<212>prt
<213>智人
<220>
<223>人bsap蛋白
<400>72
metileserpropheleuvalleualaileglythrcysleuthrasn
151015
serleuvalproglulysglulysaspprolystyrtrpargaspgln
202530
alaglngluthrleulystyralaleugluleuglnlysleuasnthr
354045
asnvalalalysasnvalilemetpheleuglyaspglymetglyval
505560
serthrvalthralaalaargileleulysglyglnleuhishisasn
65707580
proglyglugluthrargleuglumetasplyspheprophevalala
859095
leuserlysthrtyrasnthrasnalaglnvalproaspseralagly
100105110
thralathralatyrleucysglyvallysalaasngluglythrval
115120125
glyvalseralaalathrgluargserargcysasnthrthrglngly
130135140
asngluvalthrserileleuargtrpalalysaspalaglylysser
145150155160
valglyilevalthrthrthrargvalasnhisalathrproserala
165170175
alatyralahisseralaaspargasptrptyrseraspasnglumet
180185190
proproglualaleuserglnglycyslysaspilealatyrglnleu
195200205
methisasnileargaspileaspvalilemetglyglyglyarglys
210215220
tyrmettyrprolysasnlysthraspvalglutyrgluseraspglu
225230235240
lysalaargglythrargleuaspglyleuaspleuvalaspthrtrp
245250255
lysserphelysproargtyrlyshisserhispheiletrpasnarg
260265270
thrgluleuleuthrleuaspprohisasnvalasptyrleuleugly
275280285
leuphegluproglyaspmetglntyrgluleuasnargasnasnval
290295300
thraspproserleuserglumetvalvalvalalaileglnileleu
305310315320
arglysasnprolysglyphepheleuleuvalgluglyglyargile
325330335
asphisglyhishisgluglylysalalysglnalaleuhisgluala
340345350
valglumetaspargalaileglyglnalaglyserleuthrserser
355360365
gluaspthrleuthrvalvalthralaasphisserhisvalphethr
370375380
pheglyglytyrthrproargglyasnserilepheglyleualapro
385390395400
metleuseraspthrasplyslysprophethralaileleutyrgly
405410415
asnglyproglytyrlysvalvalglyglygluarggluasnvalser
420425430
metvalasptyralahisasnasntyrglnalaglnseralavalpro
435440445
leuarghisgluthrhisglyglygluaspvalalavalpheserlys
450455460
glyprometalahisleuleuhisglyvalhisgluglnasntyrval
465470475480
prohisvalmetalatyralaalacysileglyalaasnleuglyhis
485490495
cysalaproalaserseralaglyserleualaalaglyproleuleu
500505510
leualaleualaleutyrproleuservalleuphe
515520
<210>73
<211>2606
<212>dna
<213>智人
<220>
<223>人bsapmrna
<400>73
ccgggcctcactcgggccccgcggccgcctttataaggcggcgggggtggtggcccgggc60
cgcgttgcgctcccgccactccgcgcccgctatcctggctccgtgctcccacgcgcttgt120
gcctggacggaccctcgccagtgctctgcgcaggattggaacatcagttaacatctgacc180
actgccagcccaccccctcccacccacgtcgattgcatctctgggctccagggataaagc240
aggtcttggggtgcaccatgatttcaccattcttagtactggccattggcacctgcctta300
ctaactccttagtgccagagaaagagaaagaccccaagtactggcgagaccaagcgcaag360
agacactgaaatatgccctggagcttcagaagctcaacaccaacgtggctaagaatgtca420
tcatgttcctgggagatgggatgggtgtctccacagtgacggctgcccgcatcctcaagg480
gtcagctccaccacaaccctggggaggagaccaggctggagatggacaagttccccttcg540
tggccctctccaagacgtacaacaccaatgcccaggtccctgacagcgccggcaccgcca600
ccgcctacctgtgtggggtgaaggccaatgagggcaccgtgggggtaagcgcagccactg660
agcgttcccggtgcaacaccacccaggggaacgaggtcacctccatcctgcgctgggcca720
aggacgctgggaaatctgtgggcattgtgaccaccacgagagtgaaccatgccaccccca780
gcgccgcctacgcccactcggctgaccgggactggtactcagacaacgagatgccccctg840
aggccttgagccagggctgtaaggacatcgcctaccagctcatgcataacatcagggaca900
ttgacgtgatcatggggggtggccggaaatacatgtaccccaagaataaaactgatgtgg960
agtatgagagtgacgagaaagccaggggcacgaggctggacggcctggacctcgttgaca1020
cctggaagagcttcaaaccgagatacaagcactcccacttcatctggaaccgcacggaac1080
tcctgacccttgacccccacaatgtggactacctattgggtctcttcgagccaggggaca1140
tgcagtacgagctgaacaggaacaacgtgacggacccgtcactctccgagatggtggtgg1200
tggccatccagatcctgcggaagaaccccaaaggcttcttcttgctggtggaaggaggca1260
gaattgaccacgggcaccatgaaggaaaagccaagcaggccctgcatgaggcggtggaga1320
tggaccgggccatcgggcaggcaggcagcttgacctcctcggaagacactctgaccgtgg1380
tcactgcggaccattcccacgtcttcacatttggtggatacaccccccgtggcaactcta1440
tctttggtctggcccccatgctgagtgacacagacaagaagcccttcactgccatcctgt1500
atggcaatgggcctggctacaaggtggtgggcggtgaacgagagaatgtctccatggtgg1560
actatgctcacaacaactaccaggcgcagtctgctgtgcccctgcgccacgagacccacg1620
gcggggaggacgtggccgtcttctccaagggccccatggcgcacctgctgcacggcgtcc1680
acgagcagaactacgtcccccacgtgatggcgtatgcagcctgcatcggggccaacctcg1740
gccactgtgctcctgccagctcggcaggcagccttgctgcaggccccctgctgctcgcgc1800
tggccctctaccccctgagcgtcctgttctgagggcccagggcccgggcacccacaagcc1860
cgtgacagatgccaacttcccacacggcagcccccccctcaaggggcagggaggtggggg1920
cctcctcagcctctgcaactgcaagaaaggggacccaagaaaccaaagtctgccgcccac1980
ctcgctcccctctggaatcttccccaagggccaaacccacttctggcctccagcctttgc2040
tccctccccgctgccctttggccaacagggtagatttctcttgggcaggcagagagtaca2100
gactgcagacattctcaaagcctcttatttttctagcgaacgtatttctccagacccaga2160
ggccctgaagcctccgtggaacattctggatctgaccctcccagtctcatctcctgaccc2220
tcccactcccatctccttacctctggaaccccccaggccctacaatgctcatgtccctgt2280
ccccaggcccagccctccttcaggggagttgaggtctttctcctcaggacaaggccttgc2340
tcactcactcactccaagaccaccagggtcccaggaagccggtgcctgggtggccatcct2400
acccagcgtggcccaggccgggaagagccacctggcagggctcacactcctgggctctga2460
acacacacgccagctcctctctgaagcgactctcctgtttggaacggcaaaaaaaaattt2520
ttttttctctttttggtggtggttaaaagggaacacaaaacatttaaataaaactttcca2580
aatatttccgaggacaaaaaaaaaaa2606
<210>74
<211>1722
<212>dna
<213>人工序列
<220>
<223>snai1mrna
<400>74
attcattgcgccgcggcacggcctagcgagtggttcttctgcgctactgctgcgcgaatc60
ggcgaccccagtgcctcgaccactatgccgcgctctttcctcgtcaggaagccctccgac120
cccaatcggaagcctaactacagcgagctgcaggactctaatccagagtttaccttccag180
cagccctacgaccaggcccacctgctggcagccatcccacctccggagatcctcaacccc240
accgcctcgctgccaatgctcatctgggactctgtcctggcgccccaagcccagccaatt300
gcctgggcctcccttcggctccaggagagtcccagggtggcagagctgacctccctgtca360
gatgaggacagtgggaaaggctcccagccccccagcccaccctcaccggctccttcgtcc420
ttctcctctacttcagtctcttccttggaggccgaggcctatgctgccttcccaggcttg480
ggccaagtgcccaagcagctggcccagctctctgaggccaaggatctccaggctcgaaag540
gccttcaactgcaaatactgcaacaaggaatacctcagcctgggtgccctcaagatgcac600
atccgaagccacacgctgccctgcgtctgcggaacctgcgggaaggccttctctaggccc660
tggctgctacaaggccatgtccggacccacactggcgagaagcccttctcctgtccccac720
tgcagccgtgccttcgctgaccgctccaacctgcgggcccacctccagacccactcagat780
gtcaagaagtaccagtgccaggcgtgtgctcggaccttctcccgaatgtccctgctccac840
aagcaccaagagtccggctgctcaggatgtccccgctgaccctcgaggctccctcttcct900
ctccatacctgcccctgcctgacagccttccccagctccagcaggaaggaccccacatcc960
ttctcactgccatggaattccctcctgagtgccccacttctggccacatcagccccacag1020
gactttgatgaagaccattttctggttctgtgtcctctgcctgggctctggaagaggcct1080
tcccatggccatttctgtggagggagggcagctggcccccagccctgggggattcctgag1140
ctggcctgtctgcgtgggtttttgtatccagagctgtttggatacagctgctttgagcta1200
caggacaaaggctgacagactcactgggaagctcccaccccactcaggggaccccactcc1260
cctcacacacacccccccacaaggaaccctcaggccaccctccacgaggtgtgactaact1320
atgcaataatccacccccaggtgcagccccagggcctgcggaggcggtggcagactagag1380
tctgagatgccccgagcccaggcagctatttcagcctcctgtttggtggggtggcacctg1440
tttcccgggcaatttaacaatgtctgaaaagggactgtgagtaatggctgtcacttgtcg1500
ggggcccaagtggggtgctctggtctgaccgatgtgtctcccagaactattctgggggcc1560
cgacaggtgggcctgggaggaagatgtttacatttttaaaggtacactggtatttatatt1620
tcaaacattttgtatcaaggaaacgttttgtatagttatatgtacagtttattgatattc1680
aataaagcagttaatttatatattaaaaaaaaaaaaaaaaaa1722
<210>75
<211>1815
<212>dna
<213>人工序列
<220>
<223>dkk1mrna
<400>75
gcagagctctgtgctccctgcagtcaggactctgggaccgcagggggctcccggaccctg60
actctgcagccgaaccggcacggtttcgtggggacccaggcttgcaaagtgacggtcatt120
ttctctttctttctccctcttgagtccttctgagatgatggctctgggcgcagcgggagc180
tacccgggtctttgtcgcgatggtagcggcggctctcggcggccaccctctgctgggagt240
gagcgccaccttgaactcggttctcaattccaacgctatcaagaacctgcccccaccgct300
gggcggcgctgcggggcacccaggctctgcagtcagcgccgcgccgggaatcctgtaccc360
gggcgggaataagtaccagaccattgacaactaccagccgtacccgtgcgcagaggacga420
ggagtgcggcactgatgagtactgcgctagtcccacccgcggaggggacgcaggcgtgca480
aatctgtctcgcctgcaggaagcgccgaaaacgctgcatgcgtcacgctatgtgctgccc540
cgggaattactgcaaaaatggaatatgtgtgtcttctgatcaaaatcatttccgaggaga600
aattgaggaaaccatcactgaaagctttggtaatgatcatagcaccttggatgggtattc660
cagaagaaccaccttgtcttcaaaaatgtatcacaccaaaggacaagaaggttctgtttg720
tctccggtcatcagactgtgcctcaggattgtgttgtgctagacacttctggtccaagat780
ctgtaaacctgtcctgaaagaaggtcaagtgtgtaccaagcataggagaaaaggctctca840
tggactagaaatattccagcgttgttactgtggagaaggtctgtcttgccggatacagaa900
agatcaccatcaagccagtaattcttctaggcttcacacttgtcagagacactaaaccag960
ctatccaaatgcagtgaactccttttatataatagatgctatgaaaaccttttatgacct1020
tcatcaactcaatcctaaggatatacaagttctgtggtttcagttaagcattccaataac1080
accttccaaaaacctggagtgtaagagctttgtttctttatggaactcccctgtgattgc1140
agtaaattactgtattgtaaattctcagtgtggcacttacctgtaaatgcaatgaaactt1200
ttaattatttttctaaaggtgctgcactgcctatttttcctcttgttatgtaaatttttg1260
tacacattgattgttatcttgactgacaaatattctatattgaactgaagtaaatcattt1320
cagcttatagttcttaaaagcataaccctttaccccatttaattctagagtctagaacgc1380
aaggatctcttggaatgacaaatgataggtacctaaaatgtaacatgaaaatactagctt1440
attttctgaaatgtactatcttaatgcttaaattatatttccctttaggctgtgatagtt1500
tttgaaataaaatttaacatttaatatcatgaaatgttataagtagacatacattttggg1560
attgtgatcttagaggtttgtgtgtgtgtacgtatgtgtgtgttctacaagaacggaagt1620
gtgatatgtttaaagatgatcagagaaaagacagtgtctaaatataagacaatattgatc1680
agctctagaataactttaaagaaagacgtgttctgcattgataaactcaaatgatcatgg1740
cagaatgagagtgaatcttacattactactttcaaaaatagtttccaataaattaataat1800
acctaaaaaaaaaaa1815
<210>76
<211>5927
<212>dna
<213>人工序列
<220>
<223>col1a1mrna
<400>76
tcgtcggagcagacgggagtttctcctcggggtcggagcaggaggcacgcggagtgtgag60
gccacgcatgagcggacgctaaccccctccccagccacaaagagtctacatgtctagggt120
ctagacatgttcagctttgtggacctccggctcctgctcctcttagcggccaccgccctc180
ctgacgcacggccaagaggaaggccaagtcgagggccaagacgaagacatcccaccaatc240
acctgcgtacagaacggcctcaggtaccatgaccgagacgtgtggaaacccgagccctgc300
cggatctgcgtctgcgacaacggcaaggtgttgtgcgatgacgtgatctgtgacgagacc360
aagaactgccccggcgccgaagtccccgagggcgagtgctgtcccgtctgccccgacggc420
tcagagtcacccaccgaccaagaaaccaccggcgtcgagggacccaagggagacactggc480
ccccgaggcccaaggggacccgcaggcccccctggccgagatggcatccctggacagcct540
ggacttcccggaccccccggaccccccggacctcccggaccccctggcctcggaggaaac600
tttgctccccagctgtcttatggctatgatgagaaatcaaccggaggaatttccgtgcct660
ggccccatgggtccctctggtcctcgtggtctccctggcccccctggtgcacctggtccc720
caaggcttccaaggtccccctggtgagcctggcgagcctggagcttcaggtcccatgggt780
ccccgaggtcccccaggtccccctggaaagaatggagatgatggggaagctggaaaacct840
ggtcgtcctggtgagcgtgggcctcctgggcctcagggtgctcgaggattgcccggaaca900
gctggcctccctggaatgaagggacacagaggtttcagtggtttggatggtgccaaggga960
gatgctggtcctgctggtcctaagggtgagcctggcagccctggtgaaaatggagctcct1020
ggtcagatgggcccccgtggcctgcctggtgagagaggtcgccctggagcccctggccct1080
gctggtgctcgtggaaatgatggtgctactggtgctgccgggccccctggtcccaccggc1140
cccgctggtcctcctggcttccctggtgctgttggtgctaagggtgaagctggtccccaa1200
gggccccgaggctctgaaggtccccagggtgtgcgtggtgagcctggcccccctggccct1260
gctggtgctgctggccctgctggaaaccctggtgctgatggacagcctggtgctaaaggt1320
gccaatggtgctcctggtattgctggtgctcctggcttccctggtgcccgaggcccctct1380
ggaccccagggccccggcggccctcctggtcccaagggtaacagcggtgaacctggtgct1440
cctggcagcaaaggagacactggtgctaagggagagcctggccctgttggtgttcaagga1500
ccccctggccctgctggagaggaaggaaagcgaggagctcgaggtgaacccggacccact1560
ggcctgcccggaccccctggcgagcgtggtggacctggtagccgtggtttccctggcgca1620
gatggtgttgctggtcccaagggtcccgctggtgaacgtggttctcctggccctgctggc1680
cccaaaggatctcctggtgaagctggtcgtcccggtgaagctggtctgcctggtgccaag1740
ggtctgactggaagccctggcagccctggtcctgatggcaaaactggcccccctggtccc1800
gccggtcaagatggtcgccccggacccccaggcccacctggtgcccgtggtcaggctggt1860
gtgatgggattccctggacctaaaggtgctgctggagagcccggcaaggctggagagcga1920
ggtgttcccggaccccctggcgctgtcggtcctgctggcaaagatggagaggctggagct1980
cagggaccccctggccctgctggtcccgctggcgagagaggtgaacaaggccctgctggc2040
tcccccggattccagggtctccctggtcctgctggtcctccaggtgaagcaggcaaacct2100
ggtgaacagggtgttcctggagaccttggcgcccctggcccctctggagcaagaggcgag2160
agaggtttccctggcgagcgtggtgtgcaaggtccccctggtcctgctggtccccgaggg2220
gccaacggtgctcccggcaacgatggtgctaagggtgatgctggtgcccctggagctccc2280
ggtagccagggcgcccctggccttcagggaatgcctggtgaacgtggtgcagctggtctt2340
ccagggcctaagggtgacagaggtgatgctggtcccaaaggtgctgatggctctcctggc2400
aaagatggcgtccgtggtctgactggccccattggtcctcctggccctgctggtgcccct2460
ggtgacaagggtgaaagtggtcccagcggccctgctggtcccactggagctcgtggtgcc2520
cccggagaccgtggtgagcctggtccccccggccctgctggctttgctggcccccctggt2580
gctgacggccaacctggtgctaaaggcgaacctggtgatgctggtgctaaaggcgatgct2640
ggtccccctggccctgccggacccgctggaccccctggccccattggtaatgttggtgct2700
cctggagccaaaggtgctcgcggcagcgctggtccccctggtgctactggtttccctggt2760
gctgctggccgagtcggtcctcctggcccctctggaaatgctggaccccctggccctcct2820
ggtcctgctggcaaagaaggcggcaaaggtccccgtggtgagactggccctgctggacgt2880
cctggtgaagttggtccccctggtccccctggccctgctggcgagaaaggatcccctggt2940
gctgatggtcctgctggtgctcctggtactcccgggcctcaaggtattgctggacagcgt3000
ggtgtggtcggcctgcctggtcagagaggagagagaggcttccctggtcttcctggcccc3060
tctggtgaacctggcaaacaaggtccctctggagcaagtggtgaacgtggtccccctggt3120
cccatgggcccccctggattggctggaccccctggtgaatctggacgtgagggggctcct3180
ggtgccgaaggttcccctggacgagacggttctcctggcgccaagggtgaccgtggtgag3240
accggccccgctggaccccctggtgctcctggtgctcctggtgcccctggccccgttggc3300
cctgctggcaagagtggtgatcgtggtgagactggtcctgctggtcccgccggtcctgtc3360
ggccctgttggcgcccgtggccccgccggaccccaaggcccccgtggtgacaagggtgag3420
acaggcgaacagggcgacagaggcataaagggtcaccgtggcttctctggcctccagggt3480
ccccctggccctcctggctctcctggtgaacaaggtccctctggagcctctggtcctgct3540
ggtccccgaggtccccctggctctgctggtgctcctggcaaagatggactcaacggtctc3600
cctggccccattgggccccctggtcctcgcggtcgcactggtgatgctggtcctgttggt3660
ccccccggccctcctggacctcctggtccccctggtcctcccagcgctggtttcgacttc3720
agcttcctgccccagccacctcaagagaaggctcacgatggtggccgctactaccgggct3780
gatgatgccaatgtggttcgtgaccgtgacctcgaggtggacaccaccctcaagagcctg3840
agccagcagatcgagaacatccggagcccagagggcagccgcaagaaccccgcccgcacc3900
tgccgtgacctcaagatgtgccactctgactggaagagtggagagtactggattgacccc3960
aaccaaggctgcaacctggatgccatcaaagtcttctgcaacatggagactggtgagacc4020
tgcgtgtaccccactcagcccagtgtggcccagaagaactggtacatcagcaagaacccc4080
aaggacaagaggcatgtctggttcggcgagagcatgaccgatggattccagttcgagtat4140
ggcggccagggctccgaccctgccgatgtggccatccagctgaccttcctgcgcctgatg4200
tccaccgaggcctcccagaacatcacctaccactgcaagaacagcgtggcctacatggac4260
cagcagactggcaacctcaagaaggccctgctcctccagggctccaacgagatcgagatc4320
cgcgccgagggcaacagccgcttcacctacagcgtcactgtcgatggctgcacgagtcac4380
accggagcctggggcaagacagtgattgaatacaaaaccaccaagacctcccgcctgccc4440
atcatcgatgtggcccccttggacgttggtgccccagaccaggaattcggcttcgacgtt4500
ggccctgtctgcttcctgtaaactccctccatcccaacctggctccctcccacccaacca4560
actttccccccaacccggaaacagacaagcaacccaaactgaaccccctcaaaagccaaa4620
aaatgggagacaatttcacatggactttggaaaatatttttttcctttgcattcatctct4680
caaacttagtttttatctttgaccaaccgaacatgaccaaaaaccaaaagtgcattcaac4740
cttaccaaaaaaaaaaaaaaaaaaagaataaataaataactttttaaaaaaggaagcttg4800
gtccacttgcttgaagacccatgcgggggtaagtccctttctgcccgttgggcttatgaa4860
accccaatgctgccctttctgctcctttctccacaccccccttggggcctcccctccact4920
ccttcccaaatctgtctccccagaagacacaggaaacaatgtattgtctgcccagcaatc4980
aaaggcaatgctcaaacacccaagtggcccccaccctcagcccgctcctgcccgcccagc5040
acccccaggccctgggggacctggggttctcagactgccaaagaagccttgccatctggc5100
gctcccatggctcttgcaacatctccccttcgtttttgagggggtcatgccgggggagcc5160
accagcccctcactgggttcggaggagagtcaggaagggccacgacaaagcagaaacatc5220
ggatttggggaacgcgtgtcaatcccttgtgccgcagggctgggcgggagagactgttct5280
gttccttgtgtaactgtgttgctgaaagactacctcgttcttgtcttgatgtgtcaccgg5340
ggcaactgcctgggggcggggatgggggcagggtggaagcggctccccattttataccaa5400
aggtgctacatctatgtgatgggtggggtggggagggaatcactggtgctatagaaattg5460
agatgcccccccaggccagcaaatgttcctttttgttcaaagtctatttttattccttga5520
tatttttctttttttttttttttttttgtggatggggacttgtgaatttttctaaaggtg5580
ctatttaacatgggaggagagcgtgtgcggctccagcccagcccgctgctcactttccac5640
cctctctccacctgcctctggcttctcaggcctctgctctccgacctctctcctctgaaa5700
ccctcctccacagctgcagcccatcctcccggctccctcctagtctgtcctgcgtcctct5760
gtccccgggtttcagagacaacttcccaaagcacaaagcagtttttccccctaggggtgg5820
gaggaagcaaaagactctgtacctattttgtatgtgtataataatttgagatgtttttaa5880
ttattttgattgctggaataaagcatgtggaaatgacccaaacataa5927
<210>77
<211>1203
<212>dna
<213>人工序列
<220>
<223>activinamrna
<400>77
atgcccttgctttggctgagaggatttctgttggcaagttgctggattatagtgaggagt60
tcccccaccccaggatccgaggggcacagcgcggcccccgactgtccgtcctgtgcgctg120
gccgccctcccaaaggatgtacccaactctcagccagagatggtggaggccgtcaagaag180
cacattttaaacatgctgcacttgaagaagagacccgatgtcacccagccggtacccaag240
gcggcgcttctgaacgcgatcagaaagcttcatgtgggcaaagtcggggagaacgggtat300
gtggagatagaggatgacattggaaggagggcagaaatgaatgaacttatggagcagacc360
tcggagatcatcacgtttgccgagtcaggttggtgctggcattggcagggggtggggagg420
ggtggggggtgggagggtaaaatatatttctttgacagtcccaggaggaacttcttttcc480
cttcagctggaaactgcctgggaaggttattagttattaggtgatggtagcggactagcc540
gacggagggcaggcaggggagggggagaggactttacagaaaaggaattctcggtcgagc600
tctgcctggagatgactggcttacacttactaaacccagcgggtcacacagagaggaagc660
tcggggccaatgttgagctggaaggcagactgtgaggggctgccttgccctgcctgtgaa720
acagatctgagcagccggaggaaagccgcggcattttcgggtgctaggggagcagaggag780
gcttccggaccccatccaagtttttattgagggtagaggggtgaatgtaccaggattgga840
gtggaatggcacagatgaagtcactctcttaaaacaaaccttcccctttaaaagtccaat900
ctggggccacattggagaagcagggcatatttatgagtgacagtcatttttacctttaga960
aaatgtctataagtgcacaggcaccacattcaagacagggaagagctactttgggggaca1020
gttgtcattgaaccagcagttacttttgggacactgacttttgctctctgaaagaaaaaa1080
aaataaataaaacaaccagttttgttctttctaaagttactaagagctctctgccaagga1140
acgaaccttgacaaagtactctcagatactacgctgaagtcactcaatcttaagaggaag1200
aag1203
<210>78
<211>21
<212>dna
<213>人工序列
<220>
<223>snai1引物1
<400>78
tcggaagcctaactacagcga21
<210>79
<211>20
<212>dna
<213>人工序列
<220>
<223>snai1引物2
<400>79
agatgagcattggcagcgag20
<210>80
<211>23
<212>dna
<213>人工序列
<220>
<223>dkk1引物1
<400>80
ccttgaactcggttctcaattcc23
<210>81
<211>23
<212>dna
<213>人工序列
<220>
<223>dkk1引物2
<400>81
caatggtctggtacttattcccg23
<210>82
<211>21
<212>dna
<213>人工序列
<220>
<223>col1a1引物1
<400>82
gagggccaagacgaagacatc21
<210>83
<211>21
<212>dna
<213>人工序列
<220>
<223>col1a1引物2
<400>83
cagatcacgtcatcgcacaac21
<210>84
<211>20
<212>dna
<213>人工序列
<220>
<223>activin引物1
<400>84
tcatcacgtttgccgagtca20
<210>85
<211>20
<212>dna
<213>人工序列
<220>
<223>activin引物2
<400>85
gctagtccgctaccatcacc20
<210>86
<211>4241
<212>dna
<213>智人
<220>
<223>人axin2mrna
<400>86
actggctccgcgagcctggcccgggggagtcggctggagccggctgcgctttgataaggt60
cctggcaactcagtaacagcccgagagccgggaaataaaaataacccctcagagcgatgg120
atttcggggccgcccggcggccgaggcgcccgccgaaggccctgctgtaaaagagaggag180
gttcagatgagcccctgctgacttgagagagacagagagaccacgccgattgctgagagg240
aactggaagaagaaaaattcccagactcagtgggaagagctccctcaccatgagtagcgc300
tatgttggtgacttgcctcccggaccccagcagcagcttccgtgaggatgccccgcggcc360
cccagtgccaggggaagaaggggagaccccaccgtgtcagccaggggtgggcaagggcca420
ggtcaccaaacccatgcctgtctcttccaacaccaggcggaacgaagatgggttggggga480
gccggaggggcgggcatctccggattcccctctgacccggtggaccaagtccttacactc540
cttattgggcgatcaagacggtgcttacctgttccgaactttcctggagagggagaaatg600
cgtggataccttagacttctggtttgcctgcaatggattcaggcagatgaacctgaagga660
taccaaaactttacgagtagccaaagcgatctacaaaaggtacattgagaacaacagcat720
tgtctccaagcagctgaagcctgccaccaagacctacataagagatggcatcaagaagca780
gcagattgattccatcatgtttgaccaggcgcagaccgagatccagtcggtgatggagga840
aaatgcctaccagatgtttttgacttctgatatatacctcgaatatgtgaggagtggggg900
agaaaacacagcttacatgagtaatgggggactcgggagcctaaaggtcgtgtgtggcta960
tctccccaccttgaatgaagaagaggagtggacttgtgccgacttcaagtgcaaactttc1020
gccaaccgtggttggcttgtccagcaaaactctgagggccacggcgagtgtgaggtccac1080
ggaaactgttgacagtggatacaggtccttcaagaggagcgatcctgttaatccttatca1140
cataggttctggctatgtctttgcaccagccaccagcgccaacgacagtgagatatccag1200
tgatgcgctgacggatgattccatgtccatgacggacagcagtgtagatggaattcctcc1260
ttatcgtgtgggcagtaagaaacagctccagagagaaatgcatcgcagtgtgaaggccaa1320
tggccaagtgtctctacctcatttcccgagaacccaccgcctgcccaaggagatgacccc1380
cgtggaacccgccacctttgcagctgagctgatctcgaggctggaaaagctgaagctgga1440
gttggagagccgccacagcctggaggagcgcctgcagcagatccgagaggatgaagagag1500
agagggctccgagctcacactcaattcgcgggagggggcgcccacgcagcaccccctctc1560
cctactgccctccggcagctacgaggaagacccgcagacgatactggacgatcacctgtc1620
cagggtcctcaagacccctggctgccagtctccaggcgtaggccgctatagcccccgctc1680
ccgctccccggaccaccaccaccaccaccattcgcagtaccactccctgctcccgcccgg1740
tggcaagctgcctcccgcggccgcctcgccgggcgcctgccccctcctcgggggcaaagg1800
ctttgtgaccaagcagacgacgaagcatgtccaccaccactacatccaccaccatgccgt1860
ccccaagaccaaggaggagatcgaggcggaggccacgcagcgggtgcactgcttctgccc1920
tgggggcagcgagtattactgctactcgaaatgcaaaagccactccaaggctccggaaac1980
catgcccagcgagcagtttggcggcagcagaggcagtaccttgcccaaacgcaatgggaa2040
aggcacggagccgggcctggccctgcccgccagggaaggaggggcccccggcggagctgg2100
ggccctgcagcttccccgggaggaaggagacaggtcgcaggatgtctggcagtggatgct2160
ggagagtgagcggcagagcaagcccaagccccatagtgcccaaagcacaaaaaaggccta2220
ccccttggagtctgcccgctcgtctccaggcgaacgagccagccggcaccatctgtgggg2280
gggcaacagcgggcacccccgcaccaccccccgtgcccacctgttcacccaggaccctgc2340
gatgcctcccctgaccccacccaacacgctggctcagctggaggaggcctgtcgcaggct2400
agctgaggtgtcgaagcccccaaagcagcggtgctgtgtggccagtcagcagagggacag2460
gaatcattcggccactgttcagacgggagccacacccttctccaatccaagcctggctcc2520
agaagatcacaaagagccaaagaaactggcaggtgtccacgcgctccaggccagtgagtt2580
ggttgtcacttactttttctgtggggaagaaattccataccggaggatgctgaaggctca2640
gagcttgaccctgggccactttaaagagcagctcagcaaaaagggaaattataggtatta2700
cttcaaaaaagcaagcgatgagtttgcctgtggagcggtgtttgaggagatctgggagga2760
tgagacggtgctcccgatgtatgaaggccggattctgggcaaagtggagcggatcgattg2820
agccctggggtctggctttggtgaactgttggagcccgaagctcttgtgaactgtcttgg2880
ctgtgagcaactgcgacaaaacattttgaaggaaaattaaaccaatgaagaagacaaagt2940
ctaaggaagaatcggccagtgggccttcgggagggcggggggaggttgattttcatgatt3000
catgagctgggtactgactgagataagaaaagcctgaactatttattaaaaacatgacca3060
ctcttggctattgaagatgctgcctgtatttgagagactgccatacataatatatgactt3120
cctagggatctgaaatccataaactaagagaaactgtgtatagcttacctgaacaggaat3180
ccttactgatatttatagaacagttgatttcccccatccccagtttatggatatgctgct3240
ttaaacttggaagggggagacaggaagttttaattgttctgactaaacttaggagttgag3300
ctaggagtgcgttcatggtttcttcactaacagaggaattatgctttgcactacgtccct3360
ccaagtgaagacagactgttttagacagactttttaaaatggtgccctaccattgacaca3420
tgcagaaattggtgcgttttgtttttttttttcctatgctgctctgttttgtcttaaagg3480
tcttgagggttgaccatgttgcgtcatcatcaacattttgggggttgtgttggatgggat3540
gatctgttgcagagggagaggcagggaaccctgctccttcgggccccaggttgatcctgt3600
gactgaggctccccctcatgtagcctccccaggcccagggccctgaggcctgctagaatc3660
actgccgctgtgctttcgtggaaatgacagttccttgttttttttgtttctgtttttgtt3720
ttacattagtcattggaccacagccattcaggaactaccccctgccccacaaagaaatga3780
acagttgtagggagacccagcagcacctttcctccacacaccttcattttgatgttcggg3840
tttttgtgttaagttaatctgtacattctgtttgccattgttacttgtactatacatctg3900
tatatagtgtacggcaaaagagtattaatccactatctctagtgcttgactttaaatcag3960
tacagtacctgtacctgcacggtcacccgctccgtgtgtcgccctatattgagggctcaa4020
gctttcccttgttttttgaaaggggtttatgtataaatatattttatgcctttttattac4080
aagtcttgtactcaatgacttttgtcatgacattttgttctacttatactgtaaattatg4140
cattataaagagttcatttaaggaaaattacttggtacaataattattgtaattaagaga4200
tgtagcctttattaaaattttatatttttcaaaaaaaaaaa4241
<210>87
<211>843
<212>prt
<213>智人
<220>
<223>人axin2氨基酸序列
<400>87
metserseralametleuvalthrcysleuproaspproserserser
151015
phearggluaspalaproargproprovalproglyglugluglyglu
202530
thrproprocysglnproglyvalglylysglyglnvalthrlyspro
354045
metprovalserserasnthrargargasngluaspglyleuglyglu
505560
progluglyargalaserproaspserproleuthrargtrpthrlys
65707580
serleuhisserleuleuglyaspglnaspglyalatyrleuphearg
859095
thrpheleugluargglulyscysvalaspthrleuaspphetrpphe
100105110
alacysasnglypheargglnmetasnleulysaspthrlysthrleu
115120125
argvalalalysalailetyrlysargtyrilegluasnasnserile
130135140
valserlysglnleulysproalathrlysthrtyrileargaspgly
145150155160
ilelyslysglnglnileaspserilemetpheaspglnalaglnthr
165170175
gluileglnservalmetglugluasnalatyrglnmetpheleuthr
180185190
seraspiletyrleuglutyrvalargserglyglygluasnthrala
195200205
tyrmetserasnglyglyleuglyserleulysvalvalcysglytyr
210215220
leuprothrleuasngluglugluglutrpthrcysalaaspphelys
225230235240
cyslysleuserprothrvalvalglyleuserserlysthrleuarg
245250255
alathralaservalargserthrgluthrvalaspserglytyrarg
260265270
serphelysargseraspprovalasnprotyrhisileglysergly
275280285
tyrvalphealaproalathrseralaasnaspsergluileserser
290295300
aspalaleuthraspaspsermetsermetthraspserservalasp
305310315320
glyileproprotyrargvalglyserlyslysglnleuglnargglu
325330335
methisargservallysalaasnglyglnvalserleuprohisphe
340345350
proargthrhisargleuprolysglumetthrprovalgluproala
355360365
thrphealaalagluleuileserargleuglulysleulysleuglu
370375380
leugluserarghisserleuglugluargleuglnglnileargglu
385390395400
aspglugluarggluglysergluleuthrleuasnserargglugly
405410415
alaprothrglnhisproleuserleuleuproserglysertyrglu
420425430
gluaspproglnthrileleuaspasphisleuserargvalleulys
435440445
thrproglycysglnserproglyvalglyargtyrserproargser
450455460
argserproasphishishishishishisserglntyrhisserleu
465470475480
leuproproglyglylysleuproproalaalaalaserproglyala
485490495
cysproleuleuglyglylysglyphevalthrlysglnthrthrlys
500505510
hisvalhishishistyrilehishishisalavalprolysthrlys
515520525
glugluileglualaglualathrglnargvalhiscysphecyspro
530535540
glyglyserglutyrtyrcystyrserlyscyslysserhisserlys
545550555560
alaprogluthrmetprosergluglnpheglyglyserargglyser
565570575
thrleuprolysargasnglylysglythrgluproglyleualaleu
580585590
proalaarggluglyglyalaproglyglyalaglyalaleuglnleu
595600605
proargglugluglyaspargserglnaspvaltrpglntrpmetleu
610615620
glusergluargglnserlysprolysprohisseralaglnserthr
625630635640
lyslysalatyrproleugluseralaargserserproglygluarg
645650655
alaserarghishisleutrpglyglyasnserglyhisproargthr
660665670
thrproargalahisleuphethrglnaspproalametproproleu
675680685
thrproproasnthrleualaglnleugluglualacysargargleu
690695700
alagluvalserlysproprolysglnargcyscysvalalasergln
705710715720
glnargaspargasnhisseralathrvalglnthrglyalathrpro
725730735
pheserasnproserleualaprogluasphislysgluprolyslys
740745750
leualaglyvalhisalaleuglnalasergluleuvalvalthrtyr
755760765
phephecysglyglugluileprotyrargargmetleulysalagln
770775780
serleuthrleuglyhisphelysgluglnleuserlyslysglyasn
785790795800
tyrargtyrtyrphelyslysalaseraspgluphealacysglyala
805810815
valpheglugluiletrpgluaspgluthrvalleupromettyrglu
820825830
glyargileleuglylysvalgluargileasp
835840
- 还没有人留言评论。精彩留言会获得点赞!