一种具有降血糖、降血脂、增强免疫力功效的富硒口服液及其制备方法与流程
本发明属于保健食品技术领域,具体涉及一种具有降血糖、降血脂、增强免疫力的口服液。
背景技术:
随着人们生活质量提高以及生活方式的改变,糖尿病的发病率呈逐年上升趋势。临床以Ⅱ型糖尿病患者居多,占糖尿病患者总数的90%。其主要特征是胰岛素抵抗,肝脏、骨骼肌、脂肪等组织对葡萄糖的摄取减少,造成血液中葡萄糖水平升高形成高血糖。高血脂、高血糖两者密切相关,高血脂会加重糖尿病,糖尿病合并高血脂易导致脑中风、肢体坏死、眼部病变、肾脏病变。半数以上的糖尿病患者兼得高血脂,控制血糖的同时积极降低血脂具有积极意义。
目前,治疗糖尿病的药物多为化学合成类药物,如磺胺类、双胍类、葡萄糖酶抑制剂、胰岛素增敏剂等。但化学类降糖药长期服用对肝肾损伤较大,副作用较强,且易产生耐药性,不利于长期服用。
技术实现要素:
本发明的目的在于提供一种具有降血糖、降血脂、增强免疫力功效的富硒口服液,具有良好的降血糖、降血脂、增强免疫力功效。
为了实现上述发明目的,本发明提供以下技术方案:
本发明提供了一种具有降血糖、降血脂、增强免疫力功效的富硒口服液,包括功能原料和硒蛋白,所述的功能原料包括青钱柳、湖北海棠、玉竹、皱皮木瓜。
优选的,包括以下组分的原料:青钱柳10~60%,湖北海棠10~60%,玉竹5~30%,皱皮木瓜5~30%和硒蛋白0.1~5%。
优选的,其原料配方按重量百分比为:青钱柳20~50%,湖北海棠20~50%,玉竹10~25%,皱皮木瓜10~25%和硒蛋白0.5~3%。
优选的,所述的硒蛋白中硒含量500~4000mg/kg。
本发明还提供了所述富硒口服液的制备方法,包括以下步骤:
1)将青钱柳、湖北海棠、玉竹和皱皮木瓜分别或混合后粉碎,得到4种原料粉末或混合原料粉末;
2)将所述步骤1)得到的4种原料粉末分别与水混合,加热回流,得到4种滤液或所述步骤1)得到的混合原料粉末与水混合加热回流,得到混合滤液;
3)将所述步骤2)得到的4种滤液合并后或所述步骤2)得到的混合滤液与絮凝剂混合进行絮凝,加热,固液分离,得到的液体部分为澄清液;
4)将所述步骤3)得到的澄清液浓缩,添加硒蛋白,调味,灭菌,灌装得到口服液。
优选的,所述步骤1)中粉碎后原料的粒径为10~200目。
优选的,所述步骤2)中加热的温度为30~100℃;加热时间为0.1~5h;加热回流重复的次数为1~10次。
优选的,所述步骤3)中絮凝剂与所述步骤1)中原料粉末的质量比为(0.1~1):100。
优选的,所述步骤3)中加热的温度为40~80℃,加热的时间为5~60min。
优选的,所述步骤4)中浓缩包括减压浓缩,超滤膜浓缩,冷冻浓缩中的一种或几种;浓缩倍数为1~10。
本发明提供的一种具有降血糖、降血脂、增强免疫力功效的富硒口服液,包括以下原料组分:青钱柳、湖北海棠、玉竹、皱皮木瓜和硒蛋白。组合物通过降低糖苷水解酶活性,减少机体葡糖糖摄入量,加快葡萄糖的吸收利用,促进恢复病变胰岛功能恢复,改善葡萄糖耐受量,协同降低血糖水平。植物组合物通过降低甘油三酯、总胆固醇水平,达到降血脂作用。同时,通过补硒增加机体细胞免疫能力,进而增强机体免疫力。
本发明提供的原料中青钱柳、湖北海棠属于食品新资源,玉竹、皱皮木瓜属于药食两用食材,均安全无毒,非常适合血糖偏高糖者、血脂偏高者长期服用。
本发明口服液澄清稳定,无明显沉淀。
附图说明
图1为本发明实施例21对各组小鼠血糖曲线下面积的影响;
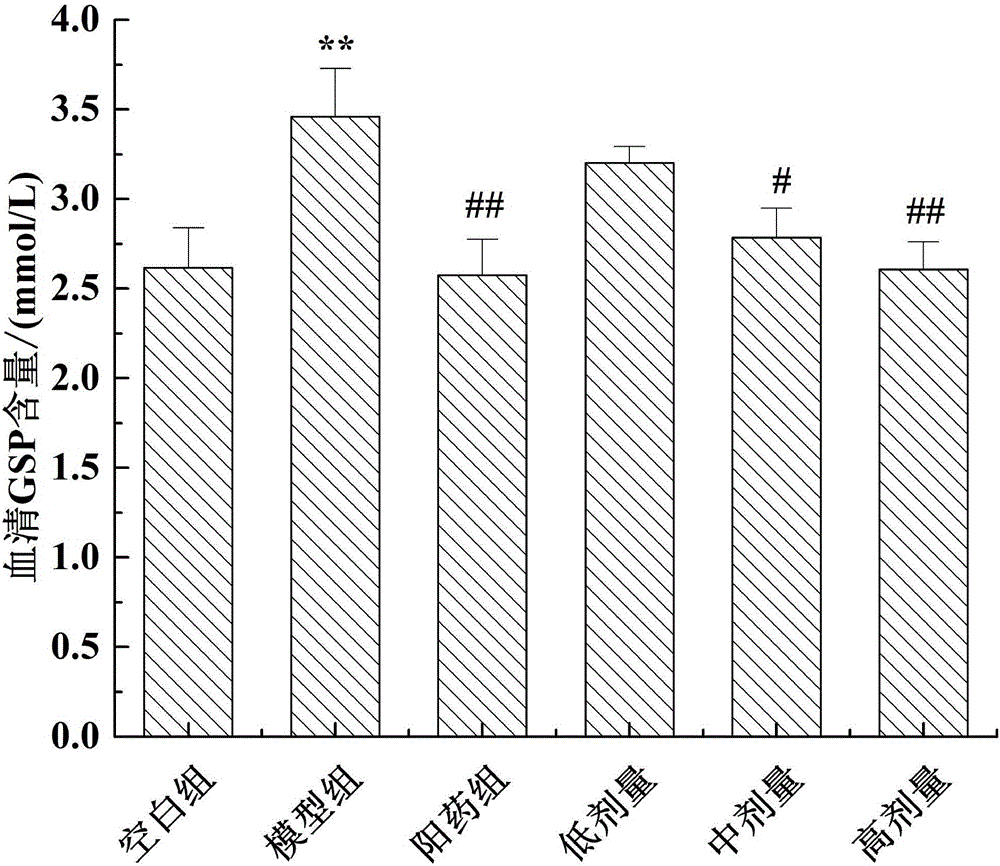
图2为本发明实施例21对各组小鼠糖化血清蛋白含量;
图3为本发明实施例21对各组小鼠肝糖原含量的影响;
图4为本发明实施例42对各组小鼠血清中总胆固醇(TC)含量的影响;
图5为本发明实施例42对各组小鼠血清中甘油三酯(TG)含量的影响;
图6为本发明实施例42对各组小鼠血清中高密度脂蛋白胆固醇(HDL-C)的影响;
图7为本发明实施例42对各组小鼠血清中低密度脂蛋白胆固醇(LDL-C)含量的影响。
图8为本发明实施例43对各组小鼠脾脏免疫细胞MTT转化实验刺激指数(SI)的影响。
具体实施方式
本发明提供了一种降血糖、降血脂、增强免疫力的富硒口服液,包括功能原料和硒蛋白,所述的功能原料包括青钱柳、湖北海棠、玉竹、皱皮木瓜。
本发明提供的一种具有降血糖、降血脂、增强免疫力功效的富硒口服液的功能原料包括青钱柳。所述青钱柳的重量百分比优选为10~60%,更优选为20~50%。青钱柳可显著增强四氧嘧啶糖尿病小鼠的葡萄糖耐受能力并促进病变胰岛结构功能恢复,降低空腹血糖。同时,青钱柳还可抑制高脂血症小鼠FAS基因和蛋白质表达,明显的改善血脂代谢和提高机体抗氧化能力。
本发明提供的一种具有降血糖、降血脂、增强免疫力功效的富硒口服液的功能原料包括湖北海棠。所述湖北海棠的重量百分比优选为10~60%,更优选为20~50%。湖北海棠提取物可竞争性抑制葡萄糖在肾脏附近的重吸收以及在肠胃道的摄取,进而发挥降血糖的作用,同时可以明显抑制糖尿病小鼠的血清甘油三酯、总胆固醇、丙二醇水平,并能增强超氧化物岐化酶、谷胱甘肽过氧化物酶的活性,从而缓慢降低血脂。
本发明提供的一种具有降血糖、降血脂、增强免疫力功效的富硒口服液的功能原料包括玉竹。所述玉竹的重量百分比优选为5~30%,更优选为10~25%。玉竹用于治疗糖尿病已经有几千年的历史。玉竹提取物可以降低糖尿病大鼠的餐后血糖值,改善葡萄糖耐受量,减少饮食及饮水量,并延缓体重的降低。
本发明提供的一种具有降血糖、降血脂、增强免疫力功效的口服液的功能原料包括皱皮木瓜。所述皱皮木瓜的重量百分比优选为5~30%,更优选为10~25%。皱皮木瓜可显著的抑制α-葡糖糖苷酶、β-葡萄糖苷酶活性,同时降低高脂小鼠血清总胆固醇、甘油三酯、低密度脂蛋白胆固醇含量和动脉粥样硬化指数,提高高密度脂蛋白胆固醇含量,达到降血脂作用。
本发明提供的一种具有降血糖、降血脂、增强免疫力功效的富硒口服液的功能原料包括硒蛋白。所述硒蛋白的重量百分比优选为0.1~5%,更优选为0.5~3%。所述硒蛋白中硒含量为500~4000mg/kg。硒蛋白能有效刺激脂肪细胞膜上葡萄糖载体的转运过程,促进脂肪组织对葡萄糖的摄取,加大葡萄糖吸收利用效率,进而减低机体中血糖水平。硒能使血液中免疫球蛋白水平升高,增强机体细胞免疫功能,增强淋巴细胞转化能力,进而增强机体免疫力
上述5种物质形成的富硒口服液通过降低糖苷水解酶活性,减少机体葡糖糖摄入量,促进恢复病变胰岛功能恢复,改善葡萄糖耐受量,协同降低血糖水平。植物组合物通过降低甘油三酯、总胆固醇水平,达到降血脂作用。同时,通过补硒增加机体细胞免疫能力,进而增强机体免疫力。
本发明还提供了所述口服液的制备方法,包括以下步骤:
1)将青钱柳、湖北海棠、玉竹和皱皮木瓜分别或混合后粉碎,得到4种原料粉末或混合原料粉末;
2)将所述步骤1)得到的4种原料粉末分别与水混合,加热回流,得到4种滤液或所述步骤1)得到的混合原料粉末与水混合加热回流,得到混合滤液;
3)将所述步骤2)得到的4种滤液合并后或所述步骤2)得到的混合滤液与絮凝剂混合进行絮凝,加热,固液分离,得到的液体部分为澄清液;
4)将所述步骤3)得到的澄清液浓缩,添加硒蛋白,调味,灭菌,灌装得到口服液。
本发明将将青钱柳、湖北海棠、玉竹和皱皮木瓜分别或混合后粉碎,得到4种原料粉末或混合原料粉末。
本发明中,将青钱柳、湖北海棠、玉竹和皱皮木瓜粉碎之前优选分别挑选青钱柳、湖北海棠、玉竹和皱皮木瓜原料,清洗晾干后混合。
本发明中,所述挑选的方法优选挑选无霉变虫害的原料。
本发明中,所述清洗的方法没有特殊限制,采用本领域技术人员所述熟知的清洗方法即可。
本发明中,所述粉碎的方法没有特殊限制,采用本领域技术人员所熟知的粉碎方法即可。所述粉碎后原料的粒径优选为10~200目,更优选为30~100目。
得到原料粉末后,本发明将将所述步骤1)得到的4种原料粉末分别与水混合,加热回流,得到4种滤液或所述步骤1)得到的混合原料粉末与水混合加热回流,得到混合滤液。
本发明中,所述原料粉末与水的质量体积比优选为1:(4~100),更优选为1:(10~50)。
本发明中,所述加热的温度优选为30~100℃,更优选为50~90℃;所述加热时间优选为0.1~5h,更优选为0.5~3h。
本发明中,所述加热回流重复的次数优选为1~10次,更优选为1~3次。
得到滤液后,本发明将将所述步骤2)得到的4种滤液合并后或所述步骤2)得到的混合滤液与絮凝剂混合进行絮凝,加热,固液分离,得到的液体部分为澄清液。
本发明中,所述混合的方法没有特殊限制,采用本领域技术人员所熟知的混合的技术方案即可。
本发明中,所述絮凝剂与所述原料粉末的质量比优选为(0.1~1):100,更优选为(0.2~0.5):100。
本发明中,所述絮凝剂的种类优选为壳聚糖、羧甲基壳聚糖、壳聚糖季铵盐、明胶和ZTC1+1澄清剂中的一种或多种。所述的ZTC1+1澄清剂为本处壳聚糖与碳酸钙的混合物。所述絮凝剂的来源没有特殊限制,采用本领域技术人员所熟知的絮凝剂的来源即可。本发明实施例中所述絮凝剂的来源为市售获得。
本发明中,所述加热的温度为40~80℃,所述加热的时间优选为5~60min,更优选为10~40min。
本发明中,所述固液分离的方法没有特殊限制,采用本领域技术人员所熟知的固液分离的技术方案即可。本发明实施例中,所述固液分离采用过滤的方法实现。
本发明中,所述固液分离后还优选包括浓缩,添加硒蛋白,调味,溶解,灭菌,灌装,得到口服液。
本发明中,所述浓缩包括减压浓缩,超滤浓缩,冷冻浓缩;浓缩的倍数优选为1~10。所述减压浓缩的真空度优选为0.07~0.1MPa,更优选为0.08MPa;所述减压浓缩的温度优选为50~75℃,更优选为60℃。所述超滤膜浓缩的超滤膜截留分子质量优选为15000~500000u,更优选为30000~40000u;超滤压力优选为0.1~0.3MPa,更优选为0.2MPa;超滤温度优选为10~35℃,更优选为20℃。所述冷冻浓缩的冷冻温度优选为-4~-20℃,更优选为-8~-15℃,最优选为-10℃。
本发明中,所述风味调节剂的添加量优选添加的风味调节剂占浓缩液的质量分数为0.1%~11%,使添加风味调节剂后的浓缩液的pH为5.0~9.0。
本发明中,添加所述风味调味剂得到的溶液颜色均一稳定,具有植物口服液特有的天然清香,外观无明显沉淀,不分层,具有明显的降血糖、降血脂、增强免疫力功效。
本发明中,所述风味调味剂的种类优选包括酸度调节剂,多糖类包埋剂、苦味抑制剂、甜味剂、抗氧化剂、稳定剂中的一种或多种。所述酸度调节剂包括碳酸钾、碳酸氢钾、碳酸钠、碳酸氢钠;所述苦味抑制剂包括新甲基陈皮苷二氢查耳酮、腺苷-5′-磷酸、阿魏酸、磷脂酸、单磷酸中的一种或几种;所述多糖类包埋物包括α-环糊精、β-环糊精、γ-环糊精、羟丙基环糊精中的一种或多种。所述甜味剂包括纽甜、甜蜜素、三氯蔗糖、麦芽糖醇、山梨糖醇、阿力甜、阿巴斯甜、甜菊糖苷、安赛蜜、赤藓糖醇、罗汉果甜苷中的一种或多种。所述抗氧化剂包括抗坏血酸、抗坏血酸钙、抗坏血酸钠、D-异抗坏血酸、D-异坏血酸钠中的一种或几种。所述稳定剂包括六偏磷酸钠、磷酸氢二钾、焦磷酸二氢二钠、三聚磷酸钠中的一种或几种。所述风味调味剂的来源没有特殊限制,采用本领域技术人员所熟知的风味调节剂的来源即可。
本发明中,溶解的方法没有特殊限制,采用本领域技术人员所熟知的溶解的技术方案即可。本发明实施例中溶解的方法为加热搅拌,加热的温度为30~80℃。
所述溶解后,本发明将所述溶解得到的物料灭菌和灌装,得到口服液。本发明中,所述灭菌的方法优选高压蒸汽灭菌,超高温瞬时灭菌,膜过滤除菌,微波灭菌,辐射灭菌中的一种或几种。
本发明中,所述灌装的容器优选玻璃瓶,PET塑料瓶,金属罐中的一种或几种。
基于所述口服液具有明显降血糖、降血脂、增强免疫力的功效,本发明还提供了所述的口服液或所述的方法制备的口服液在制备降血糖和/或降血脂和/或增强免疫力的食品或药品中的应用。
本发明中,所述药品的种类优选为片剂、胶囊剂、颗粒剂、滴丸剂和口服液。
本发明中,所述食品的种类优选为口服液、饼干、食品添加剂等。
下面结合实施例对本发明提供的一种降血糖、降血脂、增强免疫力的口服液及其制备方法和应用进行详细的说明,但是不能把它们理解为对本发明保护范围的限定。
实施例1
准确称取一定量功能原料,按重量百分比为,青钱柳10%,湖北海棠40%,玉竹30%,皱皮木瓜15%,经除杂、清洗后分别粉碎过200目筛,得原料粉末。按照原料粉末与水的质量比为1:4的量分别加入水,在100℃的温度下回流提取0.5h,提取10次,过滤,合并滤液。向滤液中加入原料药质量比为0.5%的壳聚糖进行絮凝,在40℃的温度下搅拌60min,过滤,收集澄清液。将澄清液在真空度为0.1Mpa,温度为50℃条件下进行减压浓缩,浓缩达到8倍时停止浓缩。向浓缩液中加入硒蛋白5%,其中硒含量为500mg/kg。再加入碳酸钾至pH为5,再加入占澄清液质量百分比的1%的α-环糊精,0.003%的纽甜,0.01%的甜菊糖苷,0.005%的腺酸苷,0.5%的抗坏血酸,0.5%的六偏磷酸钠,加热至30℃溶解后,在121℃条件下灭菌10min进行高压蒸汽灭菌,得到的口服液灌装进玻璃瓶。
实施例2
准确称取一定量功能原料,按重量百分比为,青钱柳20%,湖北海棠60%,玉竹14.9%,皱皮木瓜5%,经除杂、清洗后分别粉碎过10目筛,得原料粉末。按照原料粉末与水的质量比为1:100的量分别加入水,在30℃的温度下回流提取5h,提取1次,过滤,合并滤液。向滤液中加入原料药质量比为1%的羧甲基壳聚糖进行絮凝,在80℃的温度下搅拌5min,过滤,收集澄清液。将澄清液在真空度为0.07Mpa,温度为75℃条件下进行减压浓缩,浓缩达到1.5倍时停止浓缩。向浓缩液中加入硒蛋白0.1%,其中硒含量为4000mg/kg。再加入碳酸氢钾至pH为6后加入占澄清液质量百分比的2%的β-环糊精,0.05%的甜蜜素,0.1%的腺苷-5′-磷酸,1.2%的抗坏血酸钙,0.3%的磷酸氢二钾,加热至80℃溶解后,在135℃条件下灭菌10s条件下超高温瞬时灭菌,得到的口服液灌装进玻璃瓶。
实施例3
准确称取一定量功能原料,按重量百分比为,青钱柳48.5%,湖北海棠23.5%,玉竹15%,皱皮木瓜5g,经除杂、清洗后分别粉碎过30目筛,得原料粉末。按照原料粉末与水的质量比为1:10的量分别加入水,在90℃的温度下回流提取1h,提取5次,过滤,合并滤液。向滤液中加入原料药质量比为0.4%的壳聚糖季铵盐进行絮凝,在55℃的温度下搅拌50min,过滤,收集澄清液。将澄清液在超滤膜截留分子质量为45000u,超滤压力为0.2MPa,超滤温度为25℃的条件下进行超滤膜浓缩,浓缩达到5倍时停止浓缩。向浓缩液中加入硒蛋白3%,其中硒含量为800mg/kg。再加入碳酸钠至pH为7后加入占澄清液质量百分比的0.5%的γ-环糊精,0.022%的三氯蔗糖,0.2%的阿魏酸,2.3%的抗坏血酸钠,0.2%的焦磷酸二氢二钠,加热至50℃溶解后,膜过滤灭菌,得到的口服液灌装进金属瓶。
实施例4
准确称取一定量功能原料,按重量百分比为,青钱柳60%,湖北海棠10%,玉竹5%,皱皮木瓜24.2%,经除杂、清洗后分别粉碎过100目筛,得原料粉末。按照原料粉末与水的质量比为1:100的量分别加入水,在50℃的温度下回流提取0.1h,提取1次,过滤,合并滤液。向滤液中加入原料药质量比为0.5%的明胶进行絮凝,在65℃的温度下搅拌15min,过滤,收集澄清液。将澄清液在超滤膜截留分子质量为500000u,超滤压力为0.1MPa,超滤温度为10℃条件下进行超滤膜浓缩,浓缩达到2倍时停止浓缩。向浓缩液中加入硒蛋白0.8%,其中硒含量为1000mg/kg。再加入碳酸氢钠至pH为9,再加入占澄清液质量百分比的0.75%的麦芽糊精,3%的麦芽糖醇,0.3%的磷脂酸,5.5%的D-异抗坏血酸,0.1%的三聚磷酸钠,加热至45℃溶解后,微波灭菌,得到的口服液灌装进玻璃瓶。
实施例5
准确称取一定量功能原料,按重量百分比为,青钱柳29.5%,湖北海棠29.5%,玉竹10%,皱皮木瓜30%,经除杂、清洗后分别粉碎过80目筛,得原料粉末。按照原料粉末与水的质量比为1:20的量分别加入水,在70℃的温度下回流提取3h,提取1次,过滤,合并滤液。向滤液中加入原料药质量比为0.8%的ZTC1+1进行絮凝,在70℃的温度下搅拌10min,过滤,收集澄清液。将澄清液浓缩,浓缩达到1倍时停止浓缩。向浓缩液中加入硒蛋白1%,其中硒含量为1200mg/kg。再加入碳酸氢钠至pH为7.5,再加入占澄清液质量百分比的0.05%的羟丙基环糊精,5%的山梨糖醇,0.3%的腺苷-5′-磷酸,6%的D-异抗坏血酸钠,0.05%的六偏磷酸钠,加热至70℃溶解后,辐射灭菌,得到的口服液灌装进PET瓶。
实施例6
准确称取一定量功能原料,按重量百分比为,青钱柳31.5%,湖北海棠32%,玉竹25.5%,皱皮木瓜9.5%,经除杂、清洗后分别粉碎过40目筛,得原料粉末。按照原料粉末与水的质量比为1:60的量分别加入水,在70℃的温度下回流提取4h,提取1次,过滤,合并滤液。向滤液中加入原料药质量比为0.1%的壳聚糖进行絮凝,在60℃的温度下搅拌40min,过滤,收集澄清液。将澄清液在真空度为0.09Mpa,温度为60℃条件下进行减压浓缩,浓缩达到3倍时停止浓缩。向浓缩液中加入硒蛋白1.5%,其中硒含量为2300mg/kg。再加入碳酸钠至pH为5.5后加入占澄清液质量百分比的0.01%的α-环糊精,0.003%的阿力甜,0.002%的新甲基陈皮苷二氢查耳酮,5%的抗坏血酸钠,0.25%的磷酸氢二钾,加热至55℃溶解后,在117℃条件下灭菌20min进行高压蒸汽灭菌,得到的口服液灌装进金属瓶。
实施例7
准确称取一定量功能原料,按重量百分比为,青钱柳38%,湖北海棠34.5%,玉竹15%,皱皮木瓜10%,经除杂、清洗后分别粉碎过80目筛,得原料粉末。按照原料粉末与水的质量比为1:40的量分别加入水,在70℃的温度下回流提取3h,提取2次,过滤,合并滤液。向滤液中加入原料药质量比为0.2%的羟丙基壳聚糖进行絮凝,在65℃的温度下搅拌35min,过滤,收集澄清液。将澄清液在超滤膜截留分子质量为40000u,超滤压力为0.3MPa,超滤温度为35℃条件下进行超滤膜浓缩,浓缩达到3.5倍时停止浓缩。向浓缩液中加入硒蛋白2.5%,其中硒含量为650mg/kg。再加入碳酸氢钾至pH为7后加入占澄清液质量百分比的0.5%的β-环糊精,0.003%的阿力甜,5%的赤藓糖醇,0.02%的单磷酸,4.5%的抗坏血酸钙,0.33%的焦磷酸二氢二钠,加热至60℃溶解后,在135℃条件下灭菌8s进行超高温瞬时灭菌,得到的口服液灌装进玻璃瓶。
实施例8
准确称取一定量功能原料,按重量百分比为,青钱柳40%,湖北海棠35%,玉竹13%,皱皮木瓜8%,经除杂、清洗后分别粉碎过50目筛,得原料粉末。按照原料粉末与水的质量比为1:40的量分别加入水,在50℃的温度下回流提取2h,提取2次,过滤,合并滤液。向滤液中加入原料药质量比为0.4%的壳聚糖季铵盐进行絮凝,在45℃的温度下搅拌20min,过滤,收集澄清液。将澄清液在冷冻温度为-20℃条件下进行冷冻浓缩,浓缩达到2倍时停止浓缩。向浓缩液中加入硒蛋白4%,其中硒含量为3500mg/kg。再加入碳酸钾至pH为6.3后加入占澄清液质量百分比的0.03%的γ-环糊精,0.02%的赤藓糖醇,0.05%的单磷酸,1.5%的抗坏血酸钠,0.33%的三聚磷酸钠,加热至75℃溶解后,进行膜过滤灭菌,得到的口服液灌装进PET瓶。
实施例9
准确称取一定量功能原料,按重量百分比为,青钱柳25.5%,湖北海棠27.5%,玉竹17.5%,皱皮木瓜27%,经除杂、清洗后分别粉碎过40目筛,得原料粉末。按照原料粉末与水的质量比为1:30的量分别加入水,在60℃的温度下回流提取1h,提取3次,过滤,合并滤液。向滤液中加入原料药质量比为0.3%的明胶进行絮凝,在55℃的温度下搅拌30min,过滤,收集澄清液。将澄清液在冷冻温度为-10℃条件下进行冷冻浓缩,浓缩达到2倍时停止浓缩。向浓缩液中加入硒蛋白2.5%,其中硒含量为2500mg/kg。再加入碳酸氢钾至pH=7.8后加入占澄清液质量百分比的0.03%的β-环糊精,0.02%的安赛蜜,2%的木糖醇,0.007%的新甲基陈皮苷二氢查耳酮,3%的D-抗坏血酸,0.2%的六偏磷酸钠,加热至45℃溶解后,进行微波灭菌,得到的口服液灌装进金属瓶。
实施例10
准确称取一定量功能原料,按重量百分比为青钱柳35%,湖北海棠23.5%,玉竹20%,皱皮木瓜20%,经除杂、清洗后分别粉碎过40目筛,得原料粉末。按照原料粉末与水的质量比为1:30的量分别加入水,在80℃的温度下回流提取2h,提取1次,过滤,合并滤液。向滤液中加入原料药质量比为0.5%的ZTC1+1进行絮凝,在60℃的温度下搅拌25min,过滤,收集澄清液。将澄清液在真空度为0.09Mpa,温度为55℃条件下进行减压浓缩,浓缩达到2.5倍时停止浓缩。向浓缩液中加入硒蛋白1.5%,其中硒含量为2000mg/kg。再加入碳酸氢钠至pH=7后加入占澄清液质量百分比的1.2%的羟丙基环糊精,0.015%的安赛蜜,2%的三氯蔗糖,0.5%的罗汉果甜苷,0.1%的腺苷-5′-磷酸,3.5%的D-抗坏血酸钠,0.35%的磷酸氢二钾,加热至55℃溶解后,进行辐射灭菌,得到的口服液灌装进PET瓶。
实施例11-20
以实施例1-10制备的富硒口服液干燥后进行小鼠长期毒性试验分别为实施例11-20。
取健康Wistar大鼠400只,雌雄各半,随机分为4组,每组10只,分别为将实施例6制备的口服液的灌胃剂量调整为高剂量组(2.7g/kg)、中剂量组(0.9g/kg)、低剂量组(0.3g/kg)另设空白组作为对照。各剂量组进行富硒口服液灌胃,每日灌胃2次,每周灌胃6天(第七天停止灌胃一天),连续十二周。空白组给予同等量蒸馏水。实验过程中每周称重,并观察各组大鼠活动、毛色、进食饮水、精神状态等。实验结束后对大鼠进行血液学、血液生化学指标检查以分析可能出现的毒性反应,同时处死并解剖大鼠,取主要脏器称重,计算脏器系数,并对主要脏器作病理组织学检查。
实验结果显示,在灌胃给药期间,各组大鼠的活动、毛色、进食饮水、精神状态等未见明显的异常变化,各给药剂量组的体重、进食量以及血液学、血液生化学指标和脏器系数与空白组相比均未见明显变化,大鼠主要脏器的病理组织学检查未见任何异常。
实施例21
以实施例6制备的富硒口服液干燥后得到的干燥粉末进行小鼠降血糖对比实验得到实施例21。
取健康雄性C57小鼠70只,普通维持饲料适应喂养5天,禁食不禁水过夜,取尾血,测定空腹即给葡萄糖前(0小时)血糖值,给2.5g/kgBW葡萄糖后测定0.5、2小时血糖值,作为该批次动物基础值。以0小时血糖水平分5个组,即1个空白对照组、1个模型对照组、1个阳性药物组(对照药物:消渴丸)、实验组(其中将实施例6制备的口服液的干燥粉末剂量调整为高剂量组(2.7g/kg)、中剂量组(0.9g/kg)、低剂量组(0.3g/kg)。各剂量组分别灌胃给予不同剂量的的受试样品,阳药组给予51.4mg/100g的消渴丸,模型对照组给予同体积溶剂,连续42天。空白组给予维持料饲养,其他组均给以高脂饲料。4周后,阳药组、模型对照组、实验组在高脂饲料基础上分别给予链尿佐菌素40mg/kg腹腔注射,空白组给予同体积的柠檬酸盐溶液,间隔三天后,测空腹血糖值,再注射一次。各组小鼠禁食不禁水过夜,测定空腹血糖即给葡萄糖前(0小时)血糖值,实验组给予不同浓度受试样品,模型对照组给予同体积溶剂,空白对照组不做处理,15分钟后各组经口给予葡萄糖2.5g/kgBW,测定给葡萄糖后各组0.5、2小时的血糖值,计算血糖曲线下面积(AUC)。末次给药后,所有小鼠普通维持料喂养2d后禁食12h。摘眼球取血,血液离心分离血清,检测血清中糖化血清蛋白(GSP)含量。处死小鼠后剪取小鼠肝脏组织,检测小鼠肝糖原含量。
高、中、低剂量组小鼠的血糖曲线下面积、糖化血清蛋白含量、肝糖原含量分别检测结果见图1,图2,图3(*与空白组比较,p<0.05;**与空白组比较,p<0.01;#与模型组比较,p<0.05;##与模型组比较,p<0.01;)。由图可知,小鼠血糖曲线下面积(AUC)、糖化血清蛋白(GSP)含量、肝糖原含量均表明富硒口服液具有良好的降血糖功效,其中,高剂量口服液与对照药物消渴丸降血糖效果相当,中剂量口服液与高剂量口服液降血糖效果相当。同时,随着剂量的不断增加,其降血糖效果也随之增强。
实施例22-31
将实施例1-10制备的富硒口服液的干燥粉末剂量均调整为0.9g/kg,按照实施例21中实验方法得到实施例22~31,检测各组小鼠血糖曲线下面积、糖化血清蛋白含量、肝糖原含量。
各组小鼠血糖曲线下面积、糖化血清蛋白含量、肝糖原含量分别见表1。
表1实施例22~31的小鼠降血糖实验结果
由表1可知,小鼠血糖曲线下面积、GSP含量、肝糖原含量均表明实施例1-10得到的富硒口服液具有良好的降血糖功效。
实施例32
以实施例6制备的富硒口服液干燥后得到的干燥粉末进行小鼠降血脂对比实验得到实施例32。
参照实施例21-30对小鼠的喂养方式进行试验。其中将实施例6制备的口服液的干燥粉末剂量调整为高剂量组(2.7g/kg)、中剂量组(0.9g/kg)、低剂量组(0.3g/kg),检测各组小鼠血清中总胆固醇(TC)、甘油三酯(TG)、高密度脂蛋白胆固醇(HDL-C)、低密度脂蛋白胆固醇(LDL-C)含量,实验结果见图4,图5,图6,图7(*与空白组比较,p<0.05;**与空白组比较,p<0.01;#与模型组比较,p<0.05;##与模型组比较,p<0.01;)。
由图可知,小鼠血清中总胆固醇(TC)、甘油三酯(TG)、高密度脂蛋白胆固醇(HDL-C)、低密度脂蛋白胆固醇(LDL-C)含量均表明富硒口服液具有良好的降血脂功效。随着剂量的不断增加,其降血脂效果也随之增强。
实施例33-42
将实施例1-10制备的富硒口服液的干燥粉末剂量均调整为0.9g/kg,按照实施例32中实验方法检测得到实施例33~42,检测各组小鼠血清中总胆固醇(TC)、甘油三酯(TG)、高密度脂蛋白胆固醇(HDL-C)、低密度脂蛋白胆固醇(LDL-C)含量,实验结果见表2。
表2实施例33~42的小鼠降血脂实验结果
由表2可知,TC、TG、HDL-C、LDL-C含量均表明,实施例1-10得到富硒口服液均有明显降血脂效果。
实施例43
以实施例6制备的富硒口服液干燥后得到的干燥粉末进行小鼠增强免疫力对比实验得到实施例43。
参照实施例21-30对小鼠的喂养方式进行试验。其中将实施例6制备的口服液的干燥粉末剂量调整为高剂量组(2.7g/kg)、中剂量组(0.9g/kg)、低剂量组(0.3g/kg),取各组小鼠脾脏采用MTT法进行免疫细胞增殖试验,检测刺激指数值(SI),实验结果见图8。
由图8可知,小鼠脾脏免疫细胞MTT转化实验刺激指数(SI)表明富硒口服液具有良好的增强免疫力功效。随着剂量的不断增加,其增强免疫力效果也随之增强。
实施例44~42
将实施例1~10制备的富硒口服液的干燥粉末剂量均调整为0.9g/kg,按照实施例43中实验方法检测得到实施例44~53,检测各组小鼠脾脏免疫细胞MTT转化实验刺激指数(SI),实验结果见表4。
表4实施例44~53的小鼠增强免疫力实验结果
由表3可知,刺激指数(SI)均表明,实施例1~10得到富硒口服液均有明显增强免疫力效果。
由以上实施例可知,本发明提供的一种降血糖、降血脂、增强免疫力的富硒口服液,有明显地降血糖、降血脂、增强免疫力效果。并且实验证明本发明提供的口服液对小鼠无毒副作用,适合长期服用。
以上所述仅是本发明的优选实施方式,应当指出,对于本技术领域的普通技术人员来说,在不脱离本发明原理的前提下,还可以做出若干改进和润饰,这些改进和润饰也应视为本发明的保护范围。
- 还没有人留言评论。精彩留言会获得点赞!