一种反向温敏技术制备人工硬脑膜的方法与流程
本发明涉及医用生物材料技术领域,采用反向温敏的方式进行制备,采用该技术制备的生物材料可应用于硬脑膜、硬脊膜及周围神经的修复。
背景技术:
硬脑膜是位于脑组织表面和颅骨内侧面之间的双层膜性组织结构,保持硬脑膜完整性是其发挥保护和支持作用的基础。在临床上,肿瘤侵蚀、炎症破坏、先天性发育不良或开放性的颅脑损伤、手术等因素可导致硬脑膜缺损。当硬脑膜缺损时,易形成皮下积液和脑脊液漏,导致感染可引发脑炎、脑膜炎,且脑损伤及手术后脑组织可与头皮下组织直接粘连愈合,增加癫痫发生的机会,手术后头皮或肌肉层的渗血可弥漫至蛛网膜下腔,引发术后发热,头痛、无菌性炎症或脑膜刺激征。因此,手术修补硬脑膜缺损恢复其正常的解剖结构,可为脑组织提供保护作用,并能减少术后大脑与周围组织的粘连,降低癫痫、颅内感染,皮下积液、脑脊液漏等并发症的发生率。
人工硬脑膜(Artificial Dura Mater)是用生物材料制成人体脑膜的替代物,用于因颅脑、脊髓损伤、肿瘤及其他颅脑疾病引起的硬脑膜或脊膜缺损的修补,防止脑脊液外漏、颅内感染、脑膨出、脑粘连和疤痕等严重并发症,以恢复其完整性。理想的硬脑膜替代物材料具有以下特点:①安全性,无毒性,无炎症反应、不传播病毒性疾病;②组织相容性好,无免疫反应;③柔顺性好,细胞粘附性能好;④防渗漏性好;⑤无脑组织粘连;⑥可吸收性,新生脑组织形成的同时,人工硬脑膜应逐渐降解吸收;⑦便于手术操作。
临床上使用的硬脑膜替代材料有各自的优缺点,主要分为以下四个大类:①自体筋膜:其优点是是排异反应较少且组织相容性良好,缺点是不宜取材,且增加自体损伤,易与脑组织发生粘连引起癫痫。②同种异体组织,如冻干人硬脑膜:其优点是具有正常人体硬脑膜的解剖结构,能够起到一定的支撑和保护脑组织的作用,缺点是材料来源有限,并受到伦理道德的限制,而且具有潜在感染病毒性疾病的可能,现已禁用。③异种生物材料,如猪腹膜、牛心包等:是目前临床上使用较多的人工硬膜材料。其优点是材料来源充足,无伦理学限制;具有良好的致密性,修补后能基本恢复硬脑膜的解剖结构,可有效防止脑脊液漏;生物相容性好,炎症反应轻微;具有一定的韧性和弹性;表面光滑,不易与周围组织发生粘连。缺点是在去除异种蛋白抗原时使用的戊二醛可在材料中残留部分醛基,不易彻底清除,有碍于成纤维细胞长入替代材料内部,且存在一定的毒性,并具有潜在的异物反应可能。④人工合成替代材料,如丝素蛋白、高分子聚合材料等。这类材料的优点是制作方便,价格低廉,其缺点是作为永久性异物,有发生排异反应的可能,易导致无菌性炎症的发生形成肉芽肿等。
天然高分子材料应用于人工硬脑膜是当今医用生物材料发展的趋势之一,最为常见的材料是Ⅰ型胶原蛋白,通过冻干等技术制备而成。北京天新福公司采用Ⅰ型胶原蛋白制备人工硬脑膜并投入到了临床使用,因其无毒副作用、无免疫排斥反应且能够自行降解等优点得到了广泛的应用。但胶原蛋白制备的生物材料力学性能和抗水性能相对较差,在液体环境中不能保持一定的韧性强度,且在体内降解速度过快,从而限制了其在某些医疗领域的应用。此外,在国内公开的专利中,有很多采用壳聚糖作为制备材料的先例,但壳聚糖在支撑组织细胞方面的力学性能不好,一般是与其它材料进行复合使用才能满足临床需求。在国内专利《一种胸膜/脑膜及其制备方法》(申请号201510511365.5)中提出了一种旋转涂膜的方式制备壳聚糖膜的方法,通过这种方法制备的胸膜/脑膜是致密的、无孔结构薄膜,虽然在防渗性能上有所提高,但它不能吸收渗出的脑脊液,且这种无孔结构不利于组织细胞的粘附生长,另外,这一薄膜的厚度相对较薄,与人体中硬脑膜的实际厚度有一定的差异。本发明的目的是制备出一种具有相对较高机械性能、具有多孔结构、厚度易控、且能够在液体环境中保持材料形状和韧性的新型硬脑膜产品,以丰富硬脑膜产品市场,满足临床上对硬脑膜、硬脊膜及周围神经修复材料的需求。
温敏性几丁糖水凝胶在室温及更高温度下可以由流动的液体状态转化为不流动的凝胶状态,但这一凝胶状态极易与玻璃、金属、聚四氟乙烯等材质的容器发生牢固的粘连,使其很难从这些器具中光滑、完整的脱离下来,本发明中利用明胶与温敏性几丁糖反向温敏特性,采用明胶相变涂层的方式进行脱膜,明胶在高温下溶解后可形成极小的空腔,盐溶液占据这些空腔后便可使凝胶与器皿有效的分离开来,示意图如图1所示。
技术实现要素:
本发明涉及一种反向温敏技术制备人工硬脑膜的制备方法,该方法制备的人工硬脑膜具有高韧性、多孔结构、可在生理缓冲溶液中保存等特点。在制备过程中,巧妙的利用两种不同温度响应的天然高分子材料,首先利用生理温度下温敏性几丁糖材料本身的溶液-凝胶温度响应固化成型,然后利用生理缓冲液的相变响应进行固化,随后利用明胶材料本身生理温度下的凝胶-溶液的温度响应将其与模具基地脱离,然后通过浸泡、漂洗、冷冻干燥、灭菌等过程得到人工硬脑膜,其大致步骤如下:
在选定的模具底部及周边区域,用一定浓度的明胶溶液进行涂膜,在0-30℃温度条件下静置一段时间,向该模具中注入一定体积的温敏性几丁糖溶液(注入前温敏性几丁糖溶液应在冰箱中保存或预冷),15-30℃条件下静置使固化成凝胶状态。随后将该水凝胶连同模具一同放入20-60℃盐溶液中,利用二者对温度双向响应特性使凝胶从模具中脱离。将凝胶转移至新鲜的盐溶液中密封,20-60℃水浴放置12-96h,使凝胶充分进行相转变,而后取膜、去离子水漂洗、冷冻干燥、裁剪后用PBS浸润、最后灭菌即得。
本发明的优点:
1.制备工艺简单,不需要经过任何化学交联剂的参与便能制备出高韧性、高机械强度的薄膜;
2.本产品具有多孔结构,利于细胞粘附生长;
3.经本方法制得的硬脑膜补片可保存在生理缓冲液中,可采用高温高压湿热灭菌的方式对产品进行终端灭菌;
4.本产品为可降解生物高分子材料,使用后无需再次手术取出。
附图说明
图1反向温敏技术示意图;
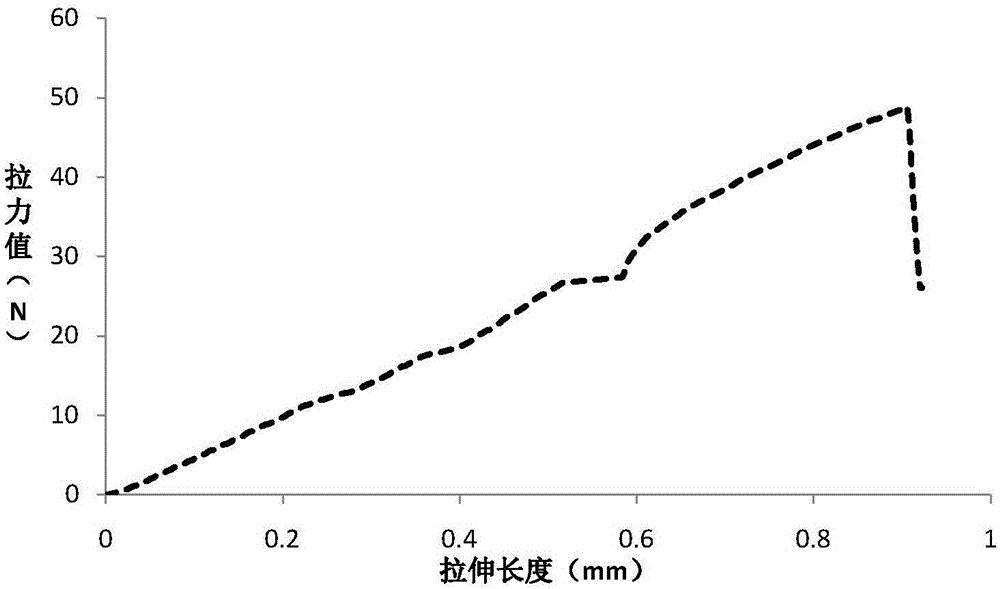
图2温敏性几丁糖人工硬脑膜拉力测试结果(干态);
图3温敏性几丁糖人工硬脑膜拉力测试结果(湿态);
图4温敏性几丁糖硬脑膜补片横切面结构(SEM);
图5温敏性几丁糖硬脑膜补片纵切面结构(SEM) 。
具体实施方式
现结合实施例,对本发明作详细描述,但本发明的实施不仅限于此。
实施例一
在选定的模具底部及周边区域,用一定浓度的明胶溶液进行涂膜,低温或室温条件下放置待凝,向该模具中注入一定体积的温敏性几丁糖溶液(注入前温敏性几丁糖溶液应在冰箱中保存或预冷),室温或40℃左右烘箱中静置待凝,将该水凝胶连同模具一同放入预先加热好的PBS水浴中进行脱胶。将凝胶转移至新鲜的PBS溶液中密封,水浴放置24小时,使凝胶充分进行相转变。第二天,取膜,去离子水漂洗30min,放入特定模具中,铺平,进行冷冻干燥。
将冻干后的海绵裁剪后用PBS浸润,放入装有PBS的西林瓶中,密封后121℃高压灭菌15min,即得。
实施例二
在选定的模具底部及周边区域,用一定浓度的明胶溶液进行涂膜,低温或室温条件下放置待凝,向该模具中注入一定体积的温敏性几丁糖溶液(注入前温敏性几丁糖溶液应在冰箱中保存或预冷),室温或40℃左右烘箱中静置待凝,将该水凝胶连同模具一同放入预先加热好的PBS水浴中进行脱胶。将凝胶转移至新鲜的PBS溶液中密封,水浴放置48小时,使凝胶充分进行相转变。第二天,取膜,去离子水漂洗30min,放入特定模具中,铺平,进行冷冻干燥。
将冻干后的海绵裁剪后用PBS浸润,放入装有PBS的西林瓶中,密封后121℃高压灭菌15min,即得。
实施例三
在选定的模具底部及周边区域,用一定浓度的明胶溶液进行涂膜,低温或室温条件下放置待凝,向该模具中注入一定体积的温敏性几丁糖溶液(注入前温敏性几丁糖溶液应在冰箱中保存或预冷),室温或40℃左右烘箱中静置待凝,将该水凝胶连同模具一同放入预先加热好的PBS水浴中进行脱胶。将凝胶转移至新鲜的PBS溶液中密封,水浴放置48小时,使凝胶充分进行相转变。第二天,取膜,去离子水漂洗10min,放入特定模具中,铺平,进行冷冻干燥。
将冻干后的海绵裁剪后用PBS浸润,放入装有PBS的西林瓶中,密封后121℃高压灭菌15min,即得。
实施例四
将由实施例所得的冻干温敏性几丁糖海绵样品及经高温高压灭菌后的最终制品于万能拉力机上进行拉伸性能测试。测试条件:拉伸速率10mm/min,断裂敏感度为35%,即当拉力降为最大拉力的75%时即视为产品断裂。测试结果见图2、图3,可以看出温敏性几丁糖薄膜在干态下的拉伸强度非常好,在湿态下的薄膜拉伸伸长率有着显著的提升。
实施例五
将由实施例所得的冻干温敏性几丁糖海绵样品,横切面(图4)及纵切面(图5)通过SEM电镜扫描,结果表明,制品具有多孔结构,且制品表面的多孔结构较中间部分的多孔结构要致密,这一结构不仅有利于防止脑脊液渗漏,还有利于将吸收的渗漏液牢牢地锁在制品中,防止二次感染。
- 还没有人留言评论。精彩留言会获得点赞!