一种肌腱‑骨组织骨性复合体的构建方法与流程
本发明涉及组织工程领域,具体涉及通过组织工程技术干预促使软组织广泛骨化、并与宿主骨组织之间形成牢固的骨性复合体,提高软组织与骨组织之间愈合能力的技术。
背景技术:
前交叉韧带(Anterior Cruciate Ligament,ACL)损伤是膝关节常见的损伤。随着人们社会活动增加,生产劳动、交通事故、体育运动和日常意外中ACL损伤经常发生。研究显示每年新增ACL损伤患者约175000例,其中包括38000例青少年患者。ACL损伤严重影响膝关节运动功能,如果损伤未得到及时治疗,还将继发关节内其它重要结构损伤(如半月板、关节软骨等),远期膝关节发生退变。
ACL为膝关节内韧带,被滑膜组织包绕,在维持膝关节稳定性上发挥着至关重要的作用。ACL损伤后其自身愈合功能差,即便是采用缝合治疗,ACL损伤的愈合失败率和再松弛发生率仍很高。由于ACL损伤后自发愈合和缝合治疗收效甚微,临床上通常采用手术重建方式治疗ACL损伤。临床和基础研究均表明韧带重建手术能够在一定程度上恢复ACL功能、提高膝关节稳定性。然而,由于肌腱与骨隧道愈合、止点结构异常、移植物重塑及手术方式等因素的影响,目前重建术后ACL的功能与正常ACL之间尚有不少差距。其中,肌腱与骨隧道愈合及止点结构形成是影响重建ACL功能的关键。
研究表明,重建术后肌腱移植物与骨隧道(以下简称腱-骨)之间愈合是不彻底的,肌腱移植物与骨隧道之间主要以纤维组织连接,未能形成正常的直接止点结构。重建韧带的生物力学性能也仅为正常韧带的50%左右。正常ACL的止点为直接止点,由连续的四层结构组成,即纤维组织、未钙化纤维软骨层、钙化纤维软骨层及骨组织。这种特化的止点结构有效地将负荷从肌腱组织(软组织)传递到骨组织(硬组织)。目前,无论采用何种方式重建固定,肌腱与骨隧道之间均不能形成正常止点结构。腱-骨之间不彻底的愈合影响着重建ACL的功能发挥。远期随访发现重建的骨隧道持续可见,还发现隧道存在扩大的变化。目前,ACL重建术后肌腱移植物与骨隧道之间愈合是不完全、不彻底的,不能恢复正常止点结构,影响了重建后ACL功能恢复和远期疗效。
研究者们分析了各种影响腱-骨组织愈合的因素,并针对性地采用干预手段促进重建术后肌腱移植物与骨隧道之间的愈合。目前,这些方法主要采用生长因子、细胞因子、细胞移植、生物材料、物理干预及基因治疗等方法促进腱-骨愈合。研究显示,骨组织的形成对于肌腱移植物与骨隧道之间的愈合至关重要。许多生长因子(如TGF-beta1、EGF、BMP、骨生长因子及粒细胞集落刺激因子等)先后被应用到肌腱移植物与骨隧道界面之间,它们在不同程度上改善了腱-骨界面愈合、提高了其生物力学性能。磷酸钙及类似材料也被用于促进重建术后腱-骨愈合。可注射性磷酸钙、羟磷石灰、钙磷骨水泥及镁盐基质骨诱导物等均表现出促进重建术后腱-骨愈合的作用,在一定程度上改善了组织界面愈合,提高了生物力学性能。此外,还有研究者通过抑制MMP、调节巨噬细胞、抑制破骨细胞及加速血管重构等生物学方法干预,均在一定程度上起到改善腱-骨界面组织结构、提高生物力学性能的作用。还有研究显示不同组织来源的间充质干细胞、骨膜组织或其前体细胞、骨髓衍生物等移植治疗能够在一定程度上加速肌腱移植物与骨隧道的愈合过程。此外,还有学者利用体外冲击波、低强频谱超声波等物理方法干预,均在一定程度上起到促进腱-骨愈合,提高重建ACL生物力学性能的作用。
上述各种方法主要针对肌腱移植物与骨隧道界面的愈合进行干预处理。虽然这些方法能够在一定程度上改善重建术后腱-骨界面愈合,但是这种腱-骨界面愈合与正常ACL止点结构或骨-骨愈合(如骨-腱-骨移植物进行ACL重建)之间仍存在较大差异。骨-骨愈合不仅较腱-骨愈合更牢固,同时还有利于直接止点结构形成。从骨-骨愈合的优势来考虑,我们能否进一步通过现代生物学技术将腱-骨愈合(肌腱移植物重建)转变为骨-骨愈合?通过有效干预促使肌腱移植物发生广泛骨化,再与(宿主)骨隧道之间形成骨-骨连接、愈合,这种移植物与骨隧道之间广泛成骨化、相互骨性连接,促进肌腱移植物与骨隧道之间愈合更彻底、更牢固,有利于重建术后ACL直接止点结构形成,进而降低移植物、骨隧道相关并发症,最终提高ACL重建手术治疗效果。
骨形态发生蛋白(Bone Morphogenetic Protein,BMP)具有高效的诱导成骨作用。大量研究表明,BMP能诱导骨长入和新骨形成,促进原位或异位成骨的作用。作为重要的骨诱导因子,BMP被广泛应用于现代骨科领域(如骨不连、脊柱融合等治疗),并获得了良好的临床疗效。目前,也有研究者在腱-骨界面之间引入BMP及相关复合物,用以促进腱-骨界面愈合。Rodeo等将BMP/胶原海绵植入肌腱移植物周围,观察到腱-骨界面之间骨组织形成增多,最大牵出力高于对照组。还有研究者通过基因技术转染表达BMP的病毒载体,结果显示BMP组腱-骨界面之间骨组织形成,对照组仅有纤维结缔组织和类Sharpey纤维形成,两者之间生物力学性能差异明显。另外,Pan等采用钙磷化合物和纤维蛋白作为载体,联合BMP移植促进ACL重建术后腱-骨愈合。研究显示腱-骨界面之间均可见新生软骨组织和骨组织形成。上述研究表明,BMP具有高效的诱导成骨活性,能够起到改善腱-骨界面愈合、提高重建ACL生物力学性能的作用。
肌腱移植物与骨隧道愈合过程离不开骨组织形成及长入。根据上述研究背景,如果我们进一步利用BMP诱导肌腱移植物内部和腱-骨界面之间广泛成骨,肌腱移植物与骨隧道之间形成骨性连接,构建骨性腱-骨组织复合体,进而促进重建术后腱-骨愈合、提高重建ACL生物力学性能,可以克服目前肌腱-骨隧道之间界面愈合所存在的缺陷。
技术实现要素:
本发明针对目前肌腱-骨隧道之间界面愈合所存在的缺陷,提出一种肌腱-骨组织骨性复合体的构建方法,采用骨形成发生蛋白与纤维蛋白凝胶制备骨诱导复合生物制剂,通过特定的处理程序,在活体条件下促使骨隧道内移植肌腱(内、外部)广泛形成骨组织,与宿主骨组织(隧道)相互交联构建新型肌腱-骨组织骨性复合体,形成直接止点样结构,从而促进移植肌腱在骨隧道内更加牢固地愈合。
本发明的技术方案如下:
一种肌腱-骨组织骨性复合体的构建方法,包括以下步骤:
(1)骨诱导原液制备
以BMP为原料,在特定条件下充分溶解,制备最终浓度为0.8~1.0g/L的骨诱导原液;
(2)初始骨诱导复合制剂的合成
以生物凝胶作为载体,将步骤(1)中制备的骨诱导原液按照一定比例与生物凝胶原液进行充分混合,形成初始(状态)的骨诱导复合制剂,用于后续步骤的处理。
(3)体内骨隧道的建立
在活体条件下动物体内建立一定直径大小的受体骨性隧道。
(4)游离移植物预处理
在活体条件下动物体内选择合适肌腱作为移植物,并用步骤(1)中制备的骨诱导原液处理肌腱移植段。
(5)移植物植入
将肌腱移植物通过合适的方式植入骨隧道内,并采用物理方法予以固定移植物。
(6)腱-骨组织界面处理
将步骤(2)中制备的初始(状态)的骨诱导复合制剂进一步转变为活性(状态)的骨诱导复合制剂,同时对肌腱移植物和骨隧道之间界面进行诱导处理。
(7)腱-骨复合体的检测
在活体内作用一定时间后,获取标本进行检测,观察腱-骨复合体大体解剖,检测肌腱移植物骨化、腱-骨组织骨性连接、直接止点形成情况。
本发明提供的腱-骨组织骨性复合体构建方法与目前腱-骨愈合常用方法不同之处在于,该方法采用BMP联合纤维蛋白胶诱导肌腱移植物内、外以及腱-骨界面之间广泛形成骨组织,并与宿主骨组织(隧道)之间形成骨性连接,构建一种牢固的腱-骨组织骨性复合体,进而促进肌腱移植物在骨隧道内的愈合。这种愈合方式较常规的肌腱-骨隧道界面愈合更加地牢固、彻底,并且组织形态上更加接近正常止点结构,为临床上ACL重建术后腱-骨愈合提供新的方法。
附图说明
图1是骨隧道内肌腱移植段广泛骨化后的横断面CT扫描图;
图2是骨隧道内肌腱移植段广泛骨化后的冠状面CT扫描图;
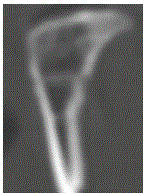
图3是骨隧道内肌腱移植段广泛骨化后的矢状面CT扫描图;
图4是骨隧道内肌腱移植段发生成骨化改变的大体解剖图;
图5是腱-骨复合体形成骨性连接的大体解剖图;
图6是肌腱内新生骨组织图;
图7是直接止点样的四层移行结构图;
图8是肌腱移植物内部及肌腱-骨隧道界面之间的类软骨样细胞图。
具体实施方式
实施例1:骨诱导原液制备
精确称取纯化rh-BMP固体粉末(上海瑞邦)1mg,将其充分溶解于1.2ml浓度为0.01mol/L的PBS(pH7.2~7.4)溶液中,至最终浓度为0.833g/L。进一步采用φ0.22μm滤膜无菌化处理,制备骨诱导原液,并在4℃环境中保存。
实施例2:初始骨诱导复合制剂的合成
在室温环境下制备纤维蛋白胶载体。取猪源纤维蛋白粘合剂(广州倍秀),按照要求在无菌操作下将主体胶溶解液与主体胶干粉充分混合,形成主体胶溶液(A液);再将催化剂溶解液与催化剂干粉充分混合,形成催化剂溶液(B液)。
取实施例1中所获得的骨诱导原液20μl,充分溶解于催化剂溶液(B液)中,形成初始(状态)的骨诱导复合制剂,以备后用(使用时,初始状态的A液和B液充分混匀)。
实施例3:骨组织隧道建立
取成年新西兰大白兔(雌雄不限,体重2.5kg左右),使用2%戊巴比妥钠(30mg/kg)通过耳缘静脉进行全身麻醉。麻醉起效后,将大白兔固定在专用手术台上,下肢进行备皮、术区消毒、铺无菌敷料。取膝关节前正中切口,逐层显露胫骨近端。然后,在胫骨结节水平采用φ1.5~2.0mm钻头由外向内建立1.5~2.0cm的胫骨近端骨隧道,备用。
实施例4:游离移植物预处理
沿髌腱外侧缘作1cm左右的关节切口,进入关节腔、寻找趾长伸肌腱。于肌腱股骨髁止点处将其横断,然后在胫骨结节水平寻找肌腱断端,并将其游离端编织缝合,尾线留作牵引线。在肌腱移植段内注入实施例1中制备的骨诱导原液。用微量注射器取15μl骨诱导原液,分别在肌腱移植段内3个不同位置的注射点缓慢注入液体,每处注射持续时间约3min,期间避免液体外渗。
实施例5:移植物的植入
将实施例4中编织、处理后的肌腱移植物通过尾线牵引,由外向内地通过实施例3中建立的胫骨骨隧道,并使肌腱移植段与骨隧道紧密接触。同时,在骨隧道内、外入口处,以缝合方式将肌腱移植物牢固固定在隧道口处。
实施例6:腱-骨组织界面处理
在肌腱移植物与骨隧道之间的间隙内(即界面)、在肌腱移植段四周(上、下、前、后,共4处界面)注射实施例2中所配制的初始(状态)的骨诱导复合制剂(即预处理的A液和B液)。在界面间隙每处注射部位内,通过双腔导管同时缓慢注射入A液和B液各约0.5ml,待A液和B液充分反应后再进行下一处的界面注射。
实施例7:腱-骨复合体的检测
术后大白兔常规抗感染,正常饲养、不限活动。术后3个月时处死大白兔,进行大体解剖观察、影像学检测、H.E染色及特殊染色等组织学检测,观察腱-骨复合体形成情况,肌腱与骨隧道之间愈合等情况。CT检测可见骨隧道内肌腱移植段广泛骨化,其密度明显增高,与骨组织密度相近(图1,横断面),新生骨组织主要沿肌腱移植物分布(图2,冠状面),并且诱导肌腱内外、骨隧道界面广泛骨化(图3,矢状面)。进一步取腱-骨复合体进行大体解剖观察,可见骨隧道内肌腱移植段质地明显变硬,与骨组织硬度相近,参见图4。肌腱移植物与骨隧道之间界面消失,肌腱内外与界面之间可见骨组织广泛形成,肌腱与骨隧道骨性融合,形成牢固的腱-骨复合体,参见图5。H.E染色可见骨隧道内肌腱组织与骨隧道之间界面消失,肌腱内新生骨组织形成,参见图6,肌腱与骨隧道之间形成类似直接止点样的四层移行结构,参见图7。Masson特殊染色可见肌腱移植物内部及肌腱-骨隧道界面之间均可见大量类软骨样细胞形成,提示腱-骨复合体形成可能与软骨内骨化有关,参见图8。
- 还没有人留言评论。精彩留言会获得点赞!