一种预防或治疗糖尿病性神经损伤及其相关病症的方法与流程
本发明涉及纤溶酶原或纤溶酶修复神经组织损伤、预防和/或治疗糖尿病性神经损伤相关病症的作用。
发明背景
糖尿病(diabetes mellitus)是一种体内胰岛素相对或绝对不足或靶细胞对胰岛素敏感性降低,或胰岛素本身存在结构上的缺陷而引起的碳水化合物、脂肪和蛋白质代谢紊乱的一种慢性疾病[1]。美国每年用于糖尿病治疗的花费为有1760亿美元(176billion),因糖尿病间接造成的损失也高达690(69billion)亿美元[2]。糖尿病神经病变是一种以糖尿病高血糖为特征的机体代谢障碍而累及神经系统的疾病,同时也是糖尿病最常见的慢性并发症之一[3]。其中有60-75%的糖尿病患者最终会发展成糖尿病神经病变[4]。糖尿病神经病变是非创伤性下肢截肢的最主要因素。糖尿病神经病变主要包括糖尿病中枢神经病变和周围神经病变(Diabetic Peripheral Neuropathy,DNP),尤以后者多见。糖尿病中枢神经病变是指在糖尿病背景下,大脑、小脑、脑干神经元和神经纤维及脊髓的神经元受损伤而造成的病变。糖尿病周围神经病变是指在排除其他原因的情况下,糖尿病患者出现周围神经功能障碍相关的症状和/或体征,主要由周围感觉神经的损伤或感染引起。
疼痛是糖尿病神经病变的主要症状之一,主要由糖尿病神经损伤引起。如上文所述,糖尿病神经疼痛相应地分为糖尿病中枢神经性疼痛和糖尿病周围神经性疼痛,以后者更为常见,且严重影响患者的生活质量,特别是损害睡眠和降低生活享受程度,长期慢性疼痛症状改变患者精神和情绪等方面,同时令其生活和社交能力下降。
对于糖尿病神经病变,在不同阶段中疼痛产生的具体发病机制尚未完全明确。目前临床上用于治疗糖尿病神经疼痛的药物主要包括如下几类:(1)抗癫痫药物,例如加巴喷丁、普瑞巴林等;(2)阿片类镇痛药物,例如曲马多、吗啡类、羟考酮等;(3)局部麻醉药物,例如利多卡因;(4)抗抑郁剂,例如阿米替林、帕罗西汀、文拉法辛等;(5)非甾体抗炎药(NSAID),如萘普生、萘普酮等。然而传统的药物依然存在多种缺陷,如加巴喷丁等抗癫痫药物副作用和不良反应几率较高且成本昂贵,而阿片类和非甾体抗炎药对周围和中枢神经性疼痛的效力有限或不足,而帕罗西汀和文拉法辛等抗抑郁药则容易出现中枢五羟色胺综合征,用药禁忌较多等。因此,尽管近年来在缓解糖尿病神经疼痛的药物开发方面已经取得了一定进步,仍然亟需一种有效的修复糖尿病神经损伤、防止糖尿病糖尿病神经损伤相关病症的药物。
纤溶酶是纤溶酶原激活系统(PA系统)的关键组分。它是一种广谱的蛋白酶,能够水解细胞外基质(ECM)的几个组分,包括纤维蛋白、明胶、纤连蛋白、层粘连蛋白和蛋白聚糖[5],此外,纤溶酶能将一些金属蛋白酶前体(pro-MMP)激活形成具有活性的金属蛋白酶(MMP)。因此纤溶酶被认为是胞外蛋白水解作用的一个重要的上游调节物[6,7]。纤溶酶是由纤溶酶原通过两种生理性的PA:组织型纤溶酶原激活剂(tPA)或尿激酶型纤溶酶原激活剂(uPA)蛋白水解形成的。由于纤溶酶原在血浆和其他体液中相对水平较高,传统上认为PA系统的调节主要通过PA的合成和活性水平实现。PA系统组分的合成受不同因素严格调节,如激素、生长因子和细胞因子。此外,还存在纤溶酶和PA的特定生理抑制剂。纤溶酶的主要抑制剂是α2-抗纤溶酶(α2-antiplasmin)。某些细胞表面具有直接水解活性的uPA特异性细胞表面受体(uPAR)[8,9]。
纤溶酶原(plasminogen,plg)是一个单链糖蛋白,由791个氨基酸组成,分子量约为92kDa[10,11]。纤溶酶原主要在肝脏合成,大量存在于胞外液中。血浆中纤溶酶原含量约为2μM。因此纤溶酶原是组织和体液中蛋白质水解活性的一个巨大的潜在来源[12,13]。纤溶酶原存在两种分子形式:谷氨酸-纤溶酶原(Glu-plasminogen)和赖氨酸-纤溶酶原(Lys-plasminogen)。天然分泌和未裂解形式的纤溶酶原具有一个氨基末端(N-末端)谷氨酸,因此被称为谷氨酸-纤溶酶原。然而,在纤溶酶存在时,谷氨酸-纤溶酶原在Lys76-Lys77处水解成为赖氨酸-纤溶酶原。与谷氨酸-纤溶酶原相比,赖氨酸-纤溶酶原与纤维蛋白具有更高的亲和力,并可以更高的速率被PA激活。这两种形式的纤溶酶原的Arg560-Val561肽键可被uPA或tPA切割,导致二硫键连接的双链蛋白酶纤溶酶的形成[14]。纤溶酶原的氨基末端部分包含五个同源三环,即所谓的kringle,羧基末端部分包含蛋白酶结构域。一些kringle含有介导纤溶酶原与纤维蛋白及其抑制剂α2-AP特异性相互作用的赖氨酸结合位点。最新发现一个为38kDa的纤维蛋白溶酶原片段,其中包括kringle1-4,是血管生成的有效抑制剂。这个片段被命名为血管抑素,可通过几个蛋白酶水解纤溶酶原产生。
纤溶酶的主要底物是纤维蛋白,纤维蛋白的溶解是预防病理性血栓形成的关键[15]。纤溶酶还具有对ECM几个组分的底物特异性,包括层粘连蛋白、纤连蛋白、蛋白聚糖和明胶,表明纤溶酶在ECM重建中也起着重要作用[12,16,17]。间接地,纤溶酶还可以通过将某些蛋白酶前体转化为活性蛋白酶来降解ECM的其他组分,包括MMP-1、MMP-2、MMP-3和MMP-9。因此,有人提出,纤溶酶可能是细胞外蛋白水解的一个重要的上游调节器[18]。此外,纤溶酶具有激活某些潜在形式的生长因子的能力[19-21]。在体外,纤溶酶还能水解补体系统的组分并释放趋化补体片段。
db/db小鼠是最为广泛应用的糖尿病实验动物模型之一,其在糖尿病神经痛的发病过程,发病机理等方面高度与人的糖尿病神经痛发病情况类似。因此,使用db/db小鼠进行相关研究,其结果具有代表性。db/db鼠在4-6周时发展成糖尿病鼠,8-12周时痛觉超敏,12周以后则痛觉减退。[22-26]
通过研究,本发明令人惊讶地发现,纤溶酶原具有显著的神经修复作用和治疗糖尿病神经损伤及其相关病症的作用,且安全性好。因此,纤溶酶原可能是一种新的修复糖尿病神经组织损伤、以及治疗和/或预防其相关病症的策略。
发明概述
一方面,本发明涉及一种预防和/或修复糖尿病性神经损伤的方法,包括给药受试者治疗有效量的纤溶酶原或纤溶酶。一方面本发明涉及纤溶酶原或纤溶酶用于预防和/或修复糖尿病性神经损伤的用途,包括给药受试者治疗有效量的纤溶酶原或纤溶酶。
在一个实施方案中,所述糖尿病性神经损伤包括神经组织损伤,神经的炎症。本发明还涉及一种治疗和/或预防糖尿病性神经损伤相关病症的方法,包括给药受试者治疗有效量的纤溶酶原或纤溶酶。在一个实施方案中,所述糖尿病性神经损伤相关病症包括肢体疼痛、感觉减退、麻木、灼热、冰凉,以及糖尿病神经性疼痛,包括但不限于糖尿病并发症引发的自发性疼痛、痛觉减退(hypoalgesia)、痛觉超敏(hyperalgesia)等。在一个实施方案中,所述纤维蛋白溶酶原与序列2、6、8、10或12具有至少80%、85%、90%、95%、96%、97%、98%或99%的序列同一性,并且仍然具有纤维蛋白溶酶原活性。在一个实施方案中,所述纤维蛋白溶酶原是包含纤溶酶原活性片段、并且仍然具有纤维蛋白溶酶原活性的蛋白质。在一个实施方案中,所述纤溶酶原选自Glu-纤维蛋白溶酶原、Lys-纤维蛋白溶酶原、小纤维蛋白溶酶原、微纤维蛋白溶酶原、δ-纤溶酶原或其任意组合。在一个实施方案中,所述纤维蛋白溶酶原全身或局部施用,例如,通过表面、静脉内、肌内、皮下、吸入、椎管内、局部注射、关节内注射或直肠施用。在一个实施方案中,所述纤维蛋白溶酶原可与其它药物或疗法联合施用。在一个实施方案中,所述其它药物或疗法包括神经营养药物、镇痛类药物、糖尿病治疗药物、抗感染药物、抗高血压药物、抗高血脂药物、物理疗法,例如,电磁疗法、红外线疗法。
在一个实施方案中,所述所述受试者为哺乳动物,优选为人。
在一个实施方案中,所述受试者纤维蛋白溶酶或者纤维蛋白溶酶原低下。具体地,所述低下是先天的、继发的和/或局部的。
在一个实施方案中,纤维蛋白溶酶原与序列2、6、8、10或12具有至少80%、85%、90%、95%、96%、97%、98%或99%的序列同一性,并且仍然具有纤维蛋白溶酶原活性。在一个实施方案中,纤维蛋白溶酶原是在序列2、6、8、10或12的基础上,添加、删除和/或取代1-100、1-90、1-80、1-70、1-60、1-50、1-45、1-40、1-35、1-30、1-25、1-20、1-15、1-10、1-5、1-4、1-3、1-2、1个氨基酸,并且仍然具有纤维蛋白溶酶原活性的蛋白质。在一个实施方案中,纤溶酶原是包含纤溶酶原活性片段、并且仍然具有纤维蛋白溶酶原活性的蛋白质。在一个实施方案中,纤溶酶原选自Glu-纤维蛋白溶酶原、Lys-纤维蛋白溶酶原、小纤维蛋白溶酶原、微纤维蛋白溶酶原、δ-纤溶酶原或其任意组合。在一个实施方案中,纤溶酶原是选自如下的保守取代变体:Glu-纤维蛋白溶酶原、Lys-纤维蛋白溶酶原、小纤维蛋白溶酶原、δ-纤溶酶原或微纤维蛋白溶酶原。在一个实施方案中,纤维蛋白溶酶原为人天然纤维蛋白溶酶原,例如序列2所示的纤溶酶原的直向同系物,例如,来自灵长类动物或啮齿类动物的纤维蛋白溶酶原直向同系物,例如来自大猩猩、恒河猴、鼠、牛、马、狗的纤维蛋白溶酶原直向同系物。最优选,本发明的纤维蛋白溶酶原的氨基酸序列如序列2、6、8、10或12所示。
在一个实施方案中,所述纤溶酶原与适当的多肽载体或稳定剂组合施用。在一个实施方案中,所述纤溶酶原以每天0.0001-2000mg/kg、0.001-800mg/kg、0.01-600mg/kg、0.1-400mg/kg、1-200mg/kg、1-100mg/kg、10-100mg/kg(以每公斤体重计算)或0.0001-2000mg/cm2、0.001-800mg/cm2、0.01-600mg/cm2、0.1-400mg/cm2、1-200mg/cm2、1-100mg/cm2、10-100mg/cm2(以每平方厘米体表面积计算)的剂量施用,优选至少重复一次,优选至少每天施用。在局部施用的情况下,上述剂量还可以根据情况进一步调整。
另一方面,本发明涉及纤溶酶原或纤溶酶在制备预防和/或修复糖尿病性神经损伤的药物中的用途。一方面,本发明涉及一种制药方法,包括将纤溶酶原或纤溶酶和药学可接受的载体一起制备成预防和/或修复糖尿病性神经损伤的药物。
在一个实施方案中,所述糖尿病性神经损伤包括神经组织损伤,神经的炎症。本发明还涉及纤溶酶原或纤溶酶在制备治疗和/或预防糖尿病性神经损伤相关病症的药物中的用途。在一个实施方案中,所述糖尿病性神经损伤相关病症包括肢体疼痛、感觉减退、麻木、灼热、冰凉,以及糖尿病神经性疼痛,包括但不限于糖尿病并发症引发的自发性疼痛、痛觉减退、痛觉超敏。在一个实施方案中,所述纤维蛋白溶酶原与序列2、6、8、10或12具有至少80%、85%、90%、95%、96%、97%、98%或99%的序列同一性,并且仍然具有纤维蛋白溶酶原活性。在一个实施方案中,所述纤维蛋白溶酶原是包含纤溶酶原活性片段、并且仍然具有纤维蛋白溶酶原活性的蛋白质。在一个实施方案中,所述纤溶酶原选自Glu-纤维蛋白溶酶原、Lys-纤维蛋白溶酶原、小纤维蛋白溶酶原、微纤维蛋白溶酶原、δ-纤溶酶原或其任意组合。在一个实施方案中,所述纤维蛋白溶酶原全身或局部施用,例如,通过表面、静脉内、肌内、皮下、吸入、椎管内、局部注射、关节内注射或直肠施用。在一个实施方案中,所述纤维蛋白溶酶原可与其它药物或疗法联合施用。在一个实施方案中,所述其它药物或疗法包括神经营养药物,镇痛类药物,糖尿病治疗药物,抗感染药物,抗高血压药物、抗高血脂药物、物理疗法,例如,电磁疗法、红外线疗法。
在一个实施方案中,所述所述受试者为哺乳动物,优选为人。
在一个实施方案中,所述受试者纤维蛋白溶酶或者纤维蛋白溶酶原低下。具体地,所述低下是先天的、继发的和/或局部的。
在一个实施方案中,纤维蛋白溶酶原与序列2、6、8、10或12具有至少80%、85%、90%、95%、96%、97%、98%或99%的序列同一性,并且仍然具有纤维蛋白溶酶原活性。在一个实施方案中,纤维蛋白溶酶原是在序列2、6、8、10或12的基础上,添加、删除和/或取代1-100、1-90、1-80、1-70、1-60、1-50、1-45、1-40、1-35、1-30、1-25、1-20、1-15、1-10、1-5、1-4、1-3、1-2、1个氨基酸,并且仍然具有纤维蛋白溶酶原活性的蛋白质。在一个实施方案中,纤溶酶原是包含纤溶酶原活性片段、并且仍然具有纤维蛋白溶酶原活性的蛋白质。在一个实施方案中,纤溶酶原选自Glu-纤维蛋白溶酶原、Lys-纤维蛋白溶酶原、小纤维蛋白溶酶原、微纤维蛋白溶酶原、δ-纤溶酶原或其任意组合。在一个实施方案中,纤溶酶原是选自如下的保守取代变体:Glu-纤维蛋白溶酶原、Lys-纤维蛋白溶酶原、小纤维蛋白溶酶原、δ-纤溶酶原或微纤维蛋白溶酶原。在一个实施方案中,纤维蛋白溶酶原为人天然纤维蛋白溶酶原,例如序列2所示的纤溶酶原的直向同系物,例如,来自灵长类动物或啮齿类动物的纤维蛋白溶酶原直向同系物,例如来自大猩猩,恒河猴、鼠、牛、马,狗的纤维蛋白溶酶原直向同系物。最优选,本发明的纤维蛋白溶酶原的氨基酸序列如序列2、6、8、10或12所示。
在一个实施方案中,所述纤溶酶原与适当的多肽载体或稳定剂组合施用。在一个实施方案中,所述纤溶酶原以每天0.0001-2000mg/kg、0.001-800mg/kg、0.01-600mg/kg、0.1-400mg/kg、1-200mg/kg、1-100mg/kg、10-100mg/kg(以每公斤体重计算)或0.0001-2000mg/cm2、0.001-800mg/cm2、0.01-600mg/cm2、0.1-400mg/cm2、1-200mg/cm2、1-100mg/cm2、10-100mg/cm2(以每平方厘米体表面积计算)的剂量施用,优选至少重复一次,优选至少每天施用。在局部施用的情况下,上述剂量还可以根据情况进一步调整。
另一方面,本发明涉及用于预防和/或修复受试者糖尿病性神经损伤的纤溶酶原,以及用于预防和/或修复受试者糖尿病性神经损伤的、包含纤溶酶原或纤溶酶的药物组合物。在一个实施方案中,所述糖尿病性神经损伤包括神经组织损伤,神经的炎症。本发明还涉及用于治疗和/或预防受试者糖尿病性神经损伤相关病症的纤溶酶原,以及用于治疗和/或预防受试者糖尿病性神经损伤相关病症的、包含纤溶酶原的药物组合物。在一个实施方案中,所述糖尿病性神经损伤相关病症包括肢体疼痛、感觉减退、麻木、灼热、冰凉,以及糖尿病神经性疼痛,包括但不限于糖尿病并发症引发的自发性疼痛、痛觉减退、痛觉超敏。在一个实施方案中,所述纤维蛋白溶酶原与序列2、6、8、10或12具有至少80%、85%、90%、95%、96%、97%、98%或99%的序列同一性,并且仍然具有纤维蛋白溶酶原活性。在一个实施方案中,所述纤维蛋白溶酶原是包含纤溶酶原活性片段、并且仍然具有纤维蛋白溶酶原活性的蛋白质。在一个实施方案中,所述纤溶酶原选自Glu-纤维蛋白溶酶原、Lys-纤维蛋白溶酶原、小纤维蛋白溶酶原、微纤维蛋白溶酶原、δ-纤溶酶原或其任意组合。在一个实施方案中,所述纤维蛋白溶酶原全身或局部施用,例如,通过表面、静脉内、肌内、皮下、吸入、椎管内、局部注射、关节内注射或直肠施用。在一个实施方案中,所述纤维蛋白溶酶原可与其它药物或疗法联合施用。在一个实施方案中,所述其它药物或疗法包括神经营养药物,镇痛类药物,糖尿病治疗药物,抗感染药物,抗高血压药物、抗高血脂药物、物理疗法,例如,电磁疗法、红外线疗法。
在一个实施方案中,所述所述受试者为哺乳动物,优选为人。
在一个实施方案中,所述受试者纤维蛋白溶酶或者纤维蛋白溶酶原低下。具体地,所述低下是先天的、继发的和/或局部的。
在一个实施方案中,纤维蛋白溶酶原与序列2、6、8、10或12具有至少80%、85%、90%、95%、96%、97%、98%或99%的序列同一性,并且仍然具有纤维蛋白溶酶原活性。在一个实施方案中,纤维蛋白溶酶原是在序列2、6、8、10或12的基础上,添加、删除和/或取代1-100、1-90、1-80、1-70、1-60、1-50、1-45、1-40、1-35、1-30、1-25、1-20、1-15、1-10、1-5、1-4、1-3、1-2、1个氨基酸,并且仍然具有纤维蛋白溶酶原活性的蛋白质。在一个实施方案中,纤溶酶原是包含纤溶酶原活性片段、并且仍然具有纤维蛋白溶酶原活性的蛋白质。在一个实施方案中,纤溶酶原选自Glu-纤维蛋白溶酶原、Lys-纤维蛋白溶酶原、小纤维蛋白溶酶原、微纤维蛋白溶酶原、δ-纤溶酶原或其任意组合。在一个实施方案中,纤溶酶原是选自如下的保守取代变体:Glu-纤维蛋白溶酶原、Lys-纤维蛋白溶酶原、小纤维蛋白溶酶原、δ-纤溶酶原或微纤维蛋白溶酶原。在一个实施方案中,纤维蛋白溶酶原为人天然纤维蛋白溶酶原,例如序列2所示的纤溶酶原的直向同系物,例如,来自灵长类动物或啮齿类动物的纤维蛋白溶酶原直向同系物,例如来自大猩猩,恒河猴、鼠、牛、马,狗的纤维蛋白溶酶原直向同系物。最优选,本发明的纤维蛋白溶酶原的氨基酸序列如序列2、6、8、10或12所示。
在一个实施方案中,所述纤溶酶原与适当的多肽载体或稳定剂组合施用。在一个实施方案中,所述纤溶酶原以每天0.0001-2000mg/kg、0.001-800mg/kg、0.01-600mg/kg、0.1-400mg/kg、1-200mg/kg、1-100mg/kg、10-100mg/kg(以每公斤体重计算)或0.0001-2000mg/cm2、0.001-800mg/cm2、0.01-600mg/cm2、0.1-400mg/cm2、1-200mg/cm2、1-100mg/cm2、10-100mg/cm2(以每平方厘米体表面积计算)的剂量施用,优选至少重复一次,优选至少每天施用。在局部施用的情况下,上述剂量还可以根据情况进一步调整。
另一个方面,本发明涉及用于预防和/或修复受试者糖尿病性神经损伤的、包含纤溶酶原或纤溶酶的药物组合物的制品或药盒。在一个实施方案中,所述糖尿病性神经损伤包括神经组织损伤,神经的炎症。本发明还涉及用于治疗和/或预防受试者糖尿病性神经损伤相关病症的、包含纤溶酶原或纤溶酶的药物组合物的制品或药盒。在一个实施方案中,所述糖尿病性神经损伤相关病症包括肢体疼痛、感觉减退、麻木、灼热、冰凉,以及糖尿病神经性疼痛,包括但不限于糖尿病并发症引发的自发性疼痛、痛觉减退、痛觉超敏。在一个实施方案中,所述纤维蛋白溶酶原与序列2、6、8、10或12具有至少80%、85%、90%、95%、96%、97%、98%或99%的序列同一性,并且仍然具有纤维蛋白溶酶原活性。在一个实施方案中,所述纤维蛋白溶酶原是包含纤溶酶原活性片段、并且仍然具有纤维蛋白溶酶原活性的蛋白质。在一个实施方案中,所述纤溶酶原选自Glu-纤维蛋白溶酶原、Lys-纤维蛋白溶酶原、小纤维蛋白溶酶原、微纤维蛋白溶酶原、δ-纤溶酶原或其任意组合。在一个实施方案中,所述纤维蛋白溶酶原全身或局部施用,例如,通过表面、静脉内、肌内、皮下、吸入、椎管内、局部注射、关节内注射或直肠施用。在一个实施方案中,所述纤维蛋白溶酶原可与其它药物或疗法联合施用。在一个实施方案中,所述其它药物或疗法包括神经营养药物、镇痛类药物、糖尿病治疗药物、抗感染药物、抗高血压药物、抗高血脂药物、物理疗法,例如,电磁疗法、红外线疗法。
在一个实施方案中,所述所述受试者为哺乳动物,优选为人。
在一个实施方案中,所述受试者纤维蛋白溶酶或者纤维蛋白溶酶原低下。具体地,所述低下是先天的、继发的和/或局部的。
在一个实施方案中,纤维蛋白溶酶原与序列2、6、8、10或12具有至少80%、85%、90%、95%、96%、97%、98%或99%的序列同一性,并且仍然具有纤维蛋白溶酶原活性。在一个实施方案中,纤维蛋白溶酶原是在序列2、6、8、10或12的基础上,添加、删除和/或取代1-100、1-90、1-80、1-70、1-60、1-50、1-45、1-40、1-35、1-30、1-25、1-20、1-15、1-10、1-5、1-4、1-3、1-2、1个氨基酸,并且仍然具有纤维蛋白溶酶原活性的蛋白质。在一个实施方案中,纤溶酶原是包含纤溶酶原活性片段、并且仍然具有纤维蛋白溶酶原活性的蛋白质。在一个实施方案中,纤溶酶原选自Glu-纤维蛋白溶酶原、Lys-纤维蛋白溶酶原、小纤维蛋白溶酶原、微纤维蛋白溶酶原、δ-纤溶酶原或其任意组合。在一个实施方案中,纤溶酶原是选自如下的保守取代变体:Glu-纤维蛋白溶酶原、Lys-纤维蛋白溶酶原、小纤维蛋白溶酶原、δ-纤溶酶原或微纤维蛋白溶酶原。在一个实施方案中,纤维蛋白溶酶原为人天然纤维蛋白溶酶原,例如序列2所示的纤溶酶原的直向同系物,例如,来自灵长类动物或啮齿类动物的纤维蛋白溶酶原直向同系物,例如来自大猩猩,恒河猴、鼠、牛、马,狗的纤维蛋白溶酶原直向同系物。最优选,本发明的纤维蛋白溶酶原的氨基酸序列如序列2、6、8、10或12所示。
在一个实施方案中,所述制品或药盒包含含有有效剂量的纤溶酶原的容器。优选,该制品或药盒进一步包含含有一种或多种其它药物的容器。该药盒还可包含使用说明书,说明所述纤溶酶原可以用于治疗所述由糖尿病引起的神经损伤及其相关病症,并且可以进一步说明,所述纤溶酶原可以在其它药物或疗法施用之前,同时,和/或之后施用。
一方面,本发明涉及纤溶酶原或纤溶酶在制备预防和/或治疗受试者的糖尿病性血管病变导致的机体组织和内脏器官损伤(损害)的药物、制品、药盒中的用途。在一个实施方案中,所述组织和内脏器官损伤(损害)包括对大脑、心脏、肝脏、肺脏、肾脏、神经、视网膜、皮肤、胃肠道的损伤(损害)。一方面,本发明涉及纤溶酶原或纤溶酶在制备预防和/或治疗受试者的糖尿病并发症的药物、制品、药盒中的用途。在一个实施方案中,所述糖尿病并发症为糖尿病引发的糖尿病性大脑病变、糖尿病性心脏病变、糖尿病性肝脏病变、糖尿病性肾脏病变、糖尿病性肺脏病变、糖尿病性神经病变,糖尿病性血管病变、糖尿病性视网膜病变、糖尿病性皮肤病变。
一方面,本发明涉及一种制药方法,包括将纤溶酶原或纤溶酶与药学可接受的载体制备成用于预防和/或治疗受试者的糖尿病性血管病变导致的机体组织和内脏器官损伤(损害)的药物、制品、药盒。在一个实施方案中,所述组织和内脏器官损伤(损害)包括对大脑、心脏、肝脏、肺脏、肾脏、神经、视网膜、皮肤、胃肠道的损伤(损害)。一方面,本发明涉及一种制药方法,包括将纤溶酶原或纤溶酶与药学可接受载体制备成预防和/或治疗受试者的糖尿病并发症的药物、制品或药盒。在一个实施方案中,所述糖尿病并发症为糖尿病引发的糖尿病性大脑病变、糖尿病性心脏病变、糖尿病性肝脏病变、糖尿病性肾脏病变、糖尿病性肺脏病变、糖尿病性神经病变,糖尿病性血管病变、糖尿病性视网膜病变、糖尿病性皮肤病变。
一方面,本发明涉及用于预防和/或治疗受试者的糖尿病性血管病变导致的机体组织和内脏器官损伤(损害)的纤溶酶原或纤溶酶、包含纤溶酶原或纤溶酶的药物组合物、制品、药盒。在一个实施方案中,所述组织和内脏器官损伤(损害)包括对大脑、心脏、肝脏、肾脏、肺脏、神经、视网膜、胃肠道、皮肤的损伤(损害)。一方面,本发明涉及用于预防和/或治疗受试者的糖尿病并发症的纤溶酶原、包含纤溶酶原的药物组合物、制品或药盒。在一个实施方案中,所述糖尿病并发症为糖尿病引发的糖尿病性大脑病变、糖尿病性心脏病变、糖尿病性肝脏病变、糖尿病性肺脏病变糖尿病性肾脏病变、糖尿病性神经病变,糖尿病性血管病变、糖尿病性视网膜病变、糖尿病性皮肤病变。
一方面,本发明涉及一种预防和/或治疗受试者的糖尿病性血管病变导致的机体组织和内脏器官损伤(损害)的方法,包括给药受试者纤溶酶原或纤溶酶、包含纤溶酶原或纤溶酶的药物组合物、制品、药盒。本发明还涉及纤溶酶原或纤溶酶、包含纤溶酶原或纤溶酶的药物组合物、制品、药盒用于预防和/或治疗受试者的糖尿病性血管病变导致的机体组织和内脏器官损伤(损害)的用途。在一个实施方案中,所述组织和内脏器官损伤(损害)包括对大脑、心脏、肝脏、肺脏、肾脏、神经、视网膜、胃肠道、皮肤的损伤(损害)。一方面,本发明涉及一种预防和/或治疗受试者的糖尿病并发症的方法,包括给药受试者纤溶酶原或纤溶酶、包含纤溶酶原或纤溶酶的药物组合物、制品或药盒。本发明还包括纤溶酶原或纤溶酶、包含纤溶酶原或纤溶酶的药物组合物、制品或药盒用于预防和/或治疗受试者的糖尿病并发症的用途。在一个实施方案中,所述糖尿病并发症为糖尿病引发的糖尿病性大脑病变、糖尿病性心脏病变、糖尿病性肝脏病变、糖尿病性肺脏病变、糖尿病性肾脏病变、糖尿病性神经病变,糖尿病性血管病变、糖尿病性视网膜病变、糖尿病性皮肤病变。
在一个实施方案中,所述纤维蛋白溶酶原与序列2、6、8、10或12具有至少80%、85%、90%、95%、96%、97%、98%或99%的序列同一性,并且仍然具有纤维蛋白溶酶原活性。在一个实施方案中,纤维蛋白溶酶原是在序列2、6、8、10或12的基础上,添加、删除和/或取代1-100、1-90、1-80、1-70、1-60、1-50、1-45、1-40、1-35、1-30、1-25、1-20、1-15、1-10、1-5、1-4、1-3、1-2、1个氨基酸,并且仍然具有纤维蛋白溶酶原活性的蛋白质。在一个实施方案中,纤溶酶原是包含纤溶酶原活性片段、并且仍然具有纤维蛋白溶酶原活性的蛋白质。在一个实施方案中,纤溶酶原选自Glu-纤维蛋白溶酶原、Lys-纤维蛋白溶酶原、小纤维蛋白溶酶原、微纤维蛋白溶酶原、δ-纤溶酶原或其任意组合。在一个实施方案中,纤溶酶原是选自如下的保守取代变体:Glu-纤维蛋白溶酶原、Lys-纤维蛋白溶酶原、小纤维蛋白溶酶原、δ-纤溶酶原或微纤维蛋白溶酶原。在一个实施方案中,纤维蛋白溶酶原为人天然纤维蛋白溶酶原,例如序列2所示的纤溶酶原的直向同系物,例如,来自灵长类动物或啮齿类动物的纤维蛋白溶酶原直向同系物,例如来自大猩猩,恒河猴、鼠、牛、马,狗的纤维蛋白溶酶原直向同系物。最优选,本发明的纤维蛋白溶酶原的氨基酸序列如序列2、6、8、10或12所示。
在一个实施方案中,所述受试者纤维蛋白溶酶或者纤维蛋白溶酶原低下。具体地,所述低下是先天的、继发的和/或局部的。
本发明明确涵盖了属于本发明实施方案之间的技术特征的所有组合,并且这些组合后的技术方案在本申请中已经明确公开,就像上述技术方案已经单独且明确公开一样。另外,本发明还明确涵盖各个实施方案及其要素的所有亚组合,并且在本文中公开,就像每一个此类亚组合单独且明确在本文中公开一样。
发明详述
1.定义
“糖尿病”是由遗传因素、免疫功能紊乱、微生物感染及其毒素、自由基毒素、精神因素等等各种致病因子作用于机体导致胰岛功能减退、胰岛素抵抗等而引发的糖、蛋白质、脂肪、水和电解质等一系列代谢紊乱综合征,临床上以高血糖为主要特点。
“糖尿病并发症”是由糖尿病过程中血糖控制不良导致的身体其他器官或组织的损害或功能障碍,其中包括肝脏、肾脏、心脏、视网膜、神经系统的损害或功能障碍等。据世界卫生组织统计,糖尿病并发症高达100多种,是目前已知并发症最多的一种疾病。
“糖尿病性微血管病变”指糖尿病患者机体各器官或组织微循环不同程度的异常导致的微血管病变。微血管病变形成的过程大致为:微循环功能性改变,内皮损伤,基膜增厚,血粘度增高,红细胞聚集,血小板粘附和聚集,最后导致微血栓形成和/或微血管闭塞。
上述“糖尿病性微血管病变”导致组织或器官局部血管损伤、血流不畅、细胞缺氧、形成血凝块、血栓和炎症,并进一步影响周边的组织及器官功能,进而导致“糖尿病并发症”。因此,本发明权利要求技术方案中提到“糖尿病性血管病变”和“糖尿病并发症”术语时,都涵盖了糖尿病引发的血栓。
“糖尿病性神经病变”或称为“糖尿病性神经病”是一种以糖尿病高血糖为特征的机体代谢障碍而累及神经系统的疾病,其由糖尿病引起的神经系统损伤造成。
“糖尿病性神经损伤”包括感觉神经受损、运动神经受损和自主神经受损。其中感觉神经受损通常较为严重,常见症状为疼痛,包括灼烧样疼痛、电极样疼痛、针扎样疼痛及各种不同的患者体验等。
“糖尿病性神经损伤相关病症”是一种以糖尿病高血糖为特征的机体代谢障碍而累及神经系统所引起的一系列病症,由糖尿病引起的神经系统损伤造成,包括但不限于:肢体疼痛、感觉减退、麻木、灼热、冰凉,以及糖尿病神经性疼痛,包括但不限于糖尿病并发症引发的自发性疼痛、痛觉减退(hypoalgesia)、痛觉超敏(hyperalgesia)等等。
“糖尿病性神经疼痛”是糖尿病神经病变的最常见形式,通常由糖尿病感觉神经受损所致。主要的疼痛通常伴有温度和触觉丧失,疼痛发生以下肢感觉居多,同时也发生在上肢和躯干。一般可分为周围和中枢神经疼痛。周围神经疼痛通过周围神经的损伤引起,而中枢神经疼痛通过中枢神经系统和/或脊髓损伤引起。
“纤溶酶”是存在于血液中的一种非常重要的酶,能将纤维蛋白凝块水解为纤维蛋白降解产物和D-二聚体。
“纤溶酶原”是纤溶酶的酶原形式,根据swiss prot中的序列,按含有信号肽的天然人源纤溶酶原氨基酸序列(序列4)计算由810个氨基酸组成,分子量约为90kD,主要在肝脏中合成并能够在血液中循环的糖蛋白,编码该氨基酸序列的cDNA序列如序列3所示。全长的纤溶酶原包含七个结构域:位于C末端的丝氨酸蛋白酶结构域、N末端的Pan Apple(PAp)结构域以及5个Kringle结构域(Kringle1-5)。参照swiss prot中的序列,其信号肽包括残基Met1-Gly19,PAp包括残基Glu20-Val98,Kringle1包括残基Cys103-Cys181,Kringle2包括残基Glu184-Cys262,Kringle3包括残基Cys275-Cys352,Kringle4包括残基Cys377-Cys454,Kringle5包括残基Cys481-Cys560。根据NCBI数据,丝氨酸蛋白酶域包括残基Val581-Arg804。
Glu-纤溶酶原是天然全长的纤溶酶原,由791个氨基酸组成(不含有19个氨基酸的信号肽),编码该序列的cDNA序列如序列1所示,其氨基酸序列如序列2所示。在体内,还存在一种是从Glu-纤溶酶原的第76-77位氨基酸处水解从而形成的Lys-纤溶酶原,如序列6所示,编码该氨基酸序列的cDNA序列如序列5所示。δ-纤溶酶原(δ-plasminogen)是全长纤溶酶原缺失了Kringle2-Kringle5结构的片段,仅含有Kringle1和丝氨酸蛋白酶域[27,30],有文献报道了δ-纤溶酶原的氨基酸序列(序列8)[30],编码该氨基酸序列的cDNA序列如序列7。小纤溶酶原(Mini-plasminogen)由Kringle5和丝氨酸蛋白酶域组成,有文献报道其包括残基Val443-Asn791(以不含有信号肽的Glu-纤溶酶原序列的Glu残基为起始氨基酸)[28],其氨基酸序列如序列10所示,编码该氨基酸序列的cDNA序列如序列9所示。而微纤溶酶原(Micro-plasminogen)仅含有丝氨酸蛋白酶结构域,有文献报道其氨基酸序列包括残基Ala543-Asn791(以不含有信号肽的Glu-纤溶酶原序列的Glu残基为起始氨基酸)[29],也有专利文献CN102154253A报道其序列包括残基Lys531-Asn791(以不含有信号肽的Glu-纤溶酶原序列的Glu残基为起始氨基酸),本专利序列参考专利文献CN102154253A,其氨基酸序列如序列12所示,编码该氨基酸序列的cDNA序列如序列11所示。
本发明的“纤溶酶”与“纤维蛋白溶酶”、“纤维蛋白溶解酶”可互换使用,含义相同;“纤溶酶原”与“纤维蛋白溶酶原”、“纤维蛋白溶解酶原”可互换使用,含义相同。
在循环过程中,纤溶酶原采用封闭的非活性构象,但当结合至血栓或细胞表面时,在纤溶酶原激活剂(plasminogen activator,PA)的介导下,其转变为呈开放性构象的活性纤溶酶。具有活性的纤溶酶可进一步将纤维蛋白凝块水解为纤维蛋白降解产物和D-二聚体,进而溶解血栓。其中纤溶酶原的PAp结构域包含维持纤溶酶原处于非活性封闭构象的重要决定簇,而KR结构域则能够与存在于受体和底物上的赖氨酸残基结合。已知多种能够作为纤溶酶原激活剂的酶,包括:组织纤溶酶原激活剂(tPA)、尿激酶纤溶酶原激活剂(uPA)、激肽释放酶和凝血因子XII(哈格曼因子)等。
“纤溶酶原活性片段”是指在纤溶酶原蛋白中,能够与底物中的靶序列结合并发挥蛋白水解功能的活性片段。本发明涉及纤溶酶原的技术方案涵盖了用纤溶酶原活性片段代替纤溶酶原的技术方案。本发明所述的纤溶酶原活性片段为包含纤溶酶原的丝氨酸蛋白酶域的蛋白质,优选,本发明所述的纤溶酶原活性片段包含序列14、与序列14具有至少80%、90%、95%、96%、97%、98%、99%同源性的氨基酸序列的蛋白质。因此,本发明所述的纤溶酶原包括含有该纤溶酶原活性片段、并且仍然保持该纤溶酶原活性的蛋白。
目前,对于血液中纤维蛋白溶酶原及其活性测定方法包括:对组织纤维蛋白溶酶原激活剂活性的检测(t-PAA)、血浆组织纤维蛋白溶酶原激活剂抗原的检测(t-PAAg)、对血浆组织纤溶酶原活性的检测(plgA)、血浆组织纤溶酶原抗原的检测(plgAg)、血浆组织纤维蛋白溶酶原激活剂抑制物活性的检测、血浆组织纤维蛋白溶酶原激活剂抑制物抗原的检测、血浆纤维蛋白溶酶-抗纤维蛋白溶酶复合物检测(PAP)。其中最常用的检测方法为发色底物法:向受检血浆中加链激酶(SK)和发色底物,受检血浆中的纤溶酶原在SK的作用下,转变成PLM,后者作用于发色底物,随后用分光光度计测定,吸光度增加与纤维蛋白溶酶原活性成正比。此外也可采用免疫化学法、凝胶电泳、免疫比浊法、放射免疫扩散法等对血液中的纤维蛋白溶酶原活性进行测定。
“直系同源物或直系同系物(ortholog)”指不同物种之间的同源物,既包括蛋白同源物也包括DNA同源物,也称为直向同源物、垂直同源物。其具体指不同物种中由同一祖先基因进化而来的蛋白或基因。本发明的纤溶酶原包括人的天然纤溶酶原,还包括来源于不同物种的、具有纤溶酶原活性的纤溶酶原直系同源物或直系同系物。
“保守取代变体”是指其中一个给定的氨基酸残基改变但不改变蛋白质或酶的整体构象和功能,这包括但不限于以相似特性(如酸性,碱性,疏水性,等)的氨基酸取代亲本蛋白质中氨基酸序列中的氨基酸。具有类似性质的氨基酸是众所周知的。例如,精氨酸、组氨酸和赖氨酸是亲水性的碱性氨基酸并可以互换。同样,异亮氨酸是疏水氨基酸,则可被亮氨酸,蛋氨酸或缬氨酸替换。因此,相似功能的两个蛋白或氨基酸序列的相似性可能会不同。例如,基于MEGALIGN算法的70%至99%的相似度(同一性)。“保守取代变体”还包括通过BLAST或FASTA算法确定具有60%以上的氨基酸同一性的多肽或酶,若能达75%以上更好,最好能达85%以上,甚至达90%以上为最佳,并且与天然或亲本蛋白质或酶相比具有相同或基本相似的性质或功能。
“分离的”纤溶酶原是指从其天然环境分离和/或回收的纤溶酶原蛋白。在一些实施方案中,所述纤溶酶原会纯化(1)至大于90%、大于95%、或大于98%的纯度(按重量计),如通过Lowry法所确定的,例如超过99%(按重量计),(2)至足以通过使用旋转杯序列分析仪获得N端或内部氨基酸序列的至少15个残基的程度,或(3)至同质性,该同质性是通过使用考马斯蓝或银染在还原性或非还原性条件下的十二烷基硫酸钠-聚丙烯酰胺凝胶电泳(SDS-PAGE)确定的。分离的纤溶酶原也包括通过生物工程技术从重组细胞制备,并通过至少一个纯化步骤分离的纤溶酶原。
术语“多肽”、“肽”和“蛋白质”在本文中可互换使用,指任何长度的氨基酸的聚合形式,其可以包括遗传编码的和非遗传编码的氨基酸,化学或生物化学修饰的或衍生化的氨基酸,和具有经修饰的肽主链的多肽。该术语包括融合蛋白,包括但不限于具有异源氨基酸序列的融合蛋白,具有异源和同源前导序列(具有或没有N端甲硫氨酸残基)的融合物;等等。
关于参照多肽序列的“氨基酸序列同一性百分数(%)”定义为在必要时引入缺口以实现最大百分比序列同一性后,且不将任何保守替代视为序列同一性的一部分时,候选序列中与参照多肽序列中的氨基酸残基相同的氨基酸残基的百分率。为测定百分比氨基酸序列同一性目的的对比可以以本领域技术范围内的多种方式实现,例如使用公众可得到的计算机软件,诸如BLAST、BLAST-2、ALIGN或Megalign(DNASTAR)软件。本领域技术人员能决定用于比对序列的适宜参数,包括对所比较序列全长实现最大对比需要的任何算法。然而,为了本发明的目的,氨基酸序列同一性百分数值是使用序列比较计算机程序ALIGN-2产生的。
在采用ALIGN-2来比较氨基酸序列的情况中,给定氨基酸序列A相对于给定氨基酸序列B的%氨基酸序列同一性(或者可表述为具有或包含相对于、与、或针对给定氨基酸序列B的某一%氨基酸序列同一性的给定氨基酸序列A)如下计算:
分数X/Y乘100
其中X是由序列比对程序ALIGN-2在该程序的A和B比对中评分为相同匹配的氨基酸残基的数目,且其中Y是B中的氨基酸残基的总数。应当领会,在氨基酸序列A的长度与氨基酸序列B的长度不相等的情况下,A相对于B的%氨基酸序列同一性会不等于B相对于A的%氨基酸序列同一性。除非另有明确说明,本文中使用的所有%氨基酸序列同一性值都是依照上一段所述,使用ALIGN-2计算机程序获得的。
如本文中使用的,术语“治疗”和“处理”指获得期望的药理和/或生理效果。所述效果可以是完全或部分预防疾病或其症状,和/或部分或完全治愈疾病和/或其症状,并且包括:(a)预防疾病在受试者体内发生,所述受试者可以具有疾病的素因,但是尚未诊断为具有疾病;(b)抑制疾病,即阻滞其形成;和(c)减轻疾病和/或其症状,即引起疾病和/或其症状消退。
术语“个体”、“受试者”和“患者”在本文中可互换使用,指哺乳动物,包括但不限于鼠(大鼠,小鼠)、非人灵长类、人、犬、猫、有蹄动物(例如马、牛、绵羊、猪、山羊)等。
“治疗有效量”或“有效量”指在对哺乳动物或其它受试者施用以治疗疾病时足以实现对疾病的所述预防和/或治疗的纤溶酶原的量。“治疗有效量”会根据所使用的纤溶酶原、要治疗的受试者的疾病和/或其症状的严重程度以及年龄、体重等而变化。
2.本发明纤溶酶原的制备
纤溶酶原可以从自然界分离并纯化用于进一步的治疗用途,也可以通过标准的化学肽合成技术来合成。当通过化学合成多肽时,可以经液相或固相进行合成。固相多肽合成(SPPS)(其中将序列的C末端氨基酸附接于不溶性支持物,接着序贯添加序列中剩余的氨基酸)是适合纤溶酶原化学合成的方法。各种形式的SPPS,诸如Fmoc和Boc可用于合成纤溶酶原。用于固相合成的技术描述于Barany和Solid-Phase Peptide Synthesis;第3-284页于The Peptides:Analysis,Synthesis,Biology.第2卷:Special Methods in Peptide Synthesis,Part A.,Merrifield,等J.Am.Chem.Soc.,85:2149-2156(1963);Stewart等,Solid Phase Peptide Synthesis,2nd ed.Pierce Chem.Co.,Rockford,Ill.(1984);和Ganesan A.2006Mini Rev.Med Chem.6:3-10和Camarero JA等2005Protein Pept Lett.12:723-8中。简言之,用其上构建有肽链的功能性单元处理小的不溶性多孔珠。在偶联/去保护的重复循环后,将附接的固相游离N末端胺与单个受N保护的氨基酸单元偶联。然后,将此单元去保护,露出可以与别的氨基酸附接的新的N末端胺。肽保持固定在固相上,之后将其切掉。
可以使用标准重组方法来生产本发明的纤溶酶原。例如,将编码纤溶酶原的核酸插入表达载体中,使其与表达载体中的调控序列可操作连接。表达调控序列包括但不限于启动子(例如天然关联的或异源的启动子)、信号序列、增强子元件、和转录终止序列。表达调控可以是载体中的真核启动子系统,所述载体能够转化或转染真核宿主细胞(例如COS或CHO细胞)。一旦将载体掺入合适的宿主中,在适合于核苷酸序列的高水平表达及纤溶酶原的收集和纯化的条件下维持宿主。
合适的表达载体通常在宿主生物体中作为附加体或作为宿主染色体DNA的整合部分复制。通常,表达载体含有选择标志物(例如氨苄青霉素抗性、潮霉素抗性、四环素抗性、卡那霉素抗性或新霉素抗性)以有助于对外源用期望的DNA序列转化的那些细胞进行检测。
大肠杆菌(Escherichia coli)是可以用于克隆主题抗体编码多核苷酸的原核宿主细胞的例子。适合于使用的其它微生物宿主包括杆菌,诸如枯草芽孢杆菌(Bacillus subtilis)和其他肠杆菌科(enterobacteriaceae),诸如沙门氏菌属(Salmonella)、沙雷氏菌属(Serratia)、和各种假单胞菌属(Pseudomonas)物种。在这些原核宿主中,也可以生成表达载体,其通常会含有与宿主细胞相容的表达控制序列(例如复制起点)。另外,会存在许多公知的启动子,诸如乳糖启动子系统,色氨酸(trp)启动子系统,β-内酰胺酶启动子系统,或来自噬菌体λ的启动子系统。启动子通常会控制表达,任选在操纵基因序列的情况中,并且具有核糖体结合位点序列等,以启动并完成转录和翻译。
其他微生物,诸如酵母也可用于表达。酵母(例如酿酒酵母(S.cerevisiae))和毕赤酵母(Pichia)是合适的酵母宿主细胞的例子,其中合适的载体根据需要具有表达控制序列(例如启动子)、复制起点、终止序列等。典型的启动子包含3-磷酸甘油酸激酶和其它糖分解酶。诱导型酵母启动于特别包括来自醇脱氢酶、异细胞色素C、和负责麦芽糖和半乳糖利用的酶的启动子。
在微生物外,哺乳动物细胞(例如在体外细胞培养物中培养的哺乳动物细胞)也可以用于表达并生成本发明的纤溶酶原(例如编码主题抗-Tau抗体的多核苷酸)。参见Winnacker,From Genes to Clones,VCH Publishers,N.Y.,N.Y.(1987)。合适的哺乳动物宿主细胞包括CHO细胞系、各种Cos细胞系、HeLa细胞、骨髓瘤细胞系、和经转化的B细胞或杂交瘤。用于这些细胞的表达载体可以包含表达控制序列,如复制起点,启动子和增强子(Queen等,Immunol.Rev.89:49(1986)),以及必需的加工信息位点,诸如核糖体结合位点、RNA剪接位点、多聚腺苷酸化位点,和转录终止子序列。合适的表达控制序列的例子是白免疫球蛋白基因、SV40、腺病毒、牛乳头瘤病毒、巨细胞病毒等衍生的启动子。参见Co等,J.Immunol.148:1149(1992)。
一旦合成(化学或重组方式),可以依照本领域的标准规程,包括硫酸铵沉淀、亲和柱、柱层析、高效液相层析(HPLC)、凝胶电泳等来纯化本发明所述的纤溶酶原。该纤溶酶原是基本上纯的,例如至少约80%至85%纯的,至少约85%至90%纯的,至少约90%至95%纯的,或98%至99%纯的或更纯的,例如不含污染物,所述污染物如细胞碎片,除主题抗体以外的大分子,等等。
3.药物配制剂
可以通过将具有所需纯度的纤溶酶原与可选的药用载体、赋形剂,或稳定剂(Remington's Pharmaceutical Sciences,16版,Osol,A.ed.(1980))混合形成冻干制剂或水溶液制备治疗配制剂。可接受的载体、赋形剂、稳定剂在所用剂量及浓度下对受者无毒性,并包括缓冲剂例如磷酸盐、柠檬酸盐及其它有机酸;抗氧化剂包括抗坏血酸和蛋氨酸;防腐剂(例如十八烷基二甲基苄基氯化铵;氯化己烷双胺;氯化苄烷铵(benzalkonium chloride),苯索氯铵;酚、丁醇或苯甲醇;烷基对羟基苯甲酸酯如甲基或丙基对羟基苯甲酸酯;邻苯二酚;间苯二酚;环己醇;3-戊醇;间甲酚);低分子量多肽(少于约10个残基);蛋白质如血清白蛋白、明胶或免疫球蛋白;亲水聚合物如聚乙烯吡咯烷酮;氨基酸如甘氨酸、谷氨酰胺、天冬酰胺、组氨酸、精氨酸或赖氨酸;单糖、二糖及其它碳水化合物包括葡萄糖、甘露糖,或糊精;螯合剂如EDTA;糖类如蔗糖、甘露醇、岩藻糖或山梨醇;成盐反离子如钠;金属复合物(例如锌-蛋白复合物);和/或非离子表面活性剂,例如TWEENTM,PLURONICSTM或聚乙二醇(PEG)。优选冻干的抗-VEGF抗体配制剂在WO 97/04801中描述,其包含在本文中作为参考。
本发明的配制剂也可含有需治疗的具体病症所需的一种以上的活性化合物,优选活性互补并且相互之间没有副作用的那些。例如,抗高血压的药物、抗心律失常的药物、治疗糖尿病的药物等。
本发明的纤溶酶原可包裹在通过诸如凝聚技术或界面聚合而制备的微胶囊中,例如,可置入在胶质药物传送系统(例如,脂质体,白蛋白微球,微乳剂,纳米颗粒和纳米胶囊)中或置入粗滴乳状液中的羟甲基纤维素或凝胶-微胶囊和聚-(甲基丙烯酸甲酯)微胶囊中。这些技术公开于Remington's Pharmaceutical Sciences 16th edition,Osol,A.Ed.(1980)。
用于体内给药的本发明的纤溶酶原必需是无菌的。这可以通过在冷冻干燥和重新配制之前或之后通过除菌滤膜过滤而轻易实现。
本发明的纤溶酶原可制备缓释制剂。缓释制剂的适当实例包括具有一定形状且含有糖蛋白的固体疏水聚合物半通透基质,例如膜或微胶囊。缓释基质实例包括聚酯、水凝胶(如聚(2-羟基乙基-异丁烯酸酯)(Langer等,J.Biomed.Mater.Res.,15:167-277(1981);Langer,Chem.Tech.,12:98-105(1982))或聚(乙烯醇)、聚交酯(美国专利3773919,EP 58,481)、L-谷氨酸与乙基-L-谷氨酸的共聚物(Sidman,等,Biopolymers 22:547(1983))、不可降解的乙烯-乙烯乙酸酯(ethylene-vinyl acetate)(Langer,等,出处同上)、或可降解的乳酸-羟基乙酸共聚物如Lupron DepotTM(由乳酸-羟基乙酸共聚物和亮氨酰脯氨酸(leuprolide)乙酸酯组成的可注射的微球体),以及聚D-(-)-3-羟丁酸。聚合物如乙烯-乙酸乙烯酯和乳酸-羟基乙酸能持续释放分子100天以上,而一些水凝胶释放蛋白的时间却较短。可以根据相关机理来设计使蛋白稳定的合理策略。例如,如果发现凝聚的机理是通过硫代二硫键互换而形成分子间S-S键,则可通过修饰巯基残基、从酸性溶液中冻干、控制湿度、采用合适的添加剂、和开发特定的聚合物基质组合物来实现稳定。
4.给药和剂量
可以通过不同方式,例如通过静脉内、腹膜内、皮下、颅内、鞘内、动脉内(例如经由颈动脉)、肌内、鼻内、表面或皮内施用或脊髓或脑投递来实现本发明药物组合物的施用。气溶胶制剂如鼻喷雾制剂包含活性剂的纯化的水性或其它溶液及防腐剂和等渗剂。将此类制剂调节至与鼻粘膜相容的pH和等渗状态。
在一些情况中,可以以下方式修饰或配制本发明的纤溶酶原药物组合物,从而提供其穿过血脑屏障的能力。可以通过各种肠内和胃肠外施用路径,包括口服,静脉内等对患有血栓和/或血栓相关疾病的个体施用此类纤溶酶原的组合物。
用于胃肠外施用的制备物包括无菌水性或非水性溶液、悬浮液和乳剂。非水性溶剂的例子是丙二醇、聚乙二醇、植物油如橄榄油,和可注射有机酯,如油酸乙酯。水性载体包括水、醇性/水性溶液、乳剂或悬浮液,包括盐水和缓冲介质。胃肠外媒介物包含氯化钠溶液、林格氏右旋糖、右旋糖和氯化钠、或固定油。静脉内媒介物包含液体和营养补充物、电解质补充物,等等。也可以存在防腐剂和其他添加剂,诸如例如,抗微生物剂、抗氧化剂、螯合剂、和惰性气体,等等。
在一些实施方案中,本发明的纤溶酶原与促进穿过血脑屏障的药剂配制在一起。在一些情况中,本发明的纤溶酶原直接或经接头与促进穿过血脑屏障的载体分子、肽或蛋白质融合。在一些实施方案中,本发明的纤溶酶原与结合内源血脑屏障(BBB)受体的多肽融合。连接纤溶酶原与结合内源BBB受体的多肽,促进穿过BBB。结合内源BBB受体的合适的多肽包括抗体,例如单克隆抗体,或其抗原结合片段,其特异性结合内源BBB受体。合适的内源BBB受体包括但不限于胰岛素受在一些情况中,抗体是囊封于脂质体中的。参见例如美国专利公开文本No.2009/0156498。
医务人员会基于各种临床因素确定剂量方案。如医学领域中公知的,任一患者的剂量取决于多种因素,包括患者的体型、体表面积、年龄、要施用的具体化合物、性别、施用次数和路径、总体健康、和同时施用的其它药物。本发明包含纤溶酶原的药物组合物的剂量范围可以例如为每天约0.0001至2000mg/kg,或约0.001至500mg/kg(例如0.02mg/kg,0.25mg/kg,0.5mg/kg,0.75mg/kg,10mg/kg,50mg/kg等等)受试者体重。例如,剂量可以是1mg/kg体重或50mg/kg体重或在1-50mg/kg的范围,或至少1mg/kg。高于或低于此例示性范围的剂量也涵盖在内,特别是考虑到上述的因素。上述范围中的中间剂量也包含在本发明的范围内。受试者可以每天、隔天、每周或根据通过经验分析确定的任何其它日程表施用此类剂量。例示性的剂量日程表包括连续几天1-10mg/kg。在本发明的药物施用过程中需要实时评估、定期评估血栓和血栓相关疾病的治疗效果和安全性。
5.治疗效力和治疗安全性
本发明的一个实施方案涉及使用纤溶酶原治疗受试者后,对治疗效力和治疗安全性的判断。
治疗效力评估:从治疗开始周(基线周)到预设的治疗阶段之间对受试者进行日常平均疼痛评价,所述评价可以例如使用11点VAS量表疼痛评分、LANSS量表、神经病理性疼痛量表(NPS)或Likert量表(按照0-10分进行等级评分)等来进行。例如VAS量表,0表示无疼痛,11代表疼痛无法忍受。其中:
0分:无疼痛;
3分以下:有轻微的疼痛,能忍受;
4-6分:受试者疼痛并影响睡眠,尚能忍受;
7-10分:受试者有渐强烈的疼痛,疼痛难忍,影响食欲与睡眠。
也可以采用更精细的VAS量表进行评分,例如以100-毫米刻度评价疼痛。
还可将疼痛指数作为主要评价指标,同时设置次要评价指标,如关节活动度、功能状态、生活质量等。
安全性评估:此外,本发明还涉及使用纤溶酶原及其变体对受试者进行治疗过程中和治疗后,对所述治疗方案安全性的判断,包括但不限于不良事件监测、临床实验室评价、心电图(ECG)、生命体征测量,以及物理和神经检查等,并对受试者中药物的血清半衰期、治疗半衰期、半数中毒量(TD50)、半数致死量(LD50)进行统计。不良事件定义为被给予药物的患者或临床试验受试者中任何不利的医学事件,所述事件不必与该治疗具有因果关系。其中不良事件通常包括但不限于头痛、头晕、上呼吸道感染、恶心等。
6.制品或药盒
本发明的一个实施方案涉及一种制品或药盒,其包含本发明的纤溶酶原/纤溶酶。所述制品优选包括一个容器,标签或包装插页。适当的容器有瓶子、小瓶、注射器等。容器可由各种材料如玻璃或塑料制成。所述容器含有组合物,所述组合物可有效治疗本发明的疾病或病症并具有无菌入口(例如所述容器可为静脉内溶液包或小瓶,其含有可被皮下注射针穿透的塞子的)。所述组合物中至少一种活性剂为纤溶酶原/纤溶酶。所述容器上或所附的标签说明所述组合物用于治疗本发明所述糖尿病性神经病变。所述制品可进一步包含含有可药用缓冲液的第二容器,诸如磷酸盐缓冲的盐水,林格氏溶液以及葡萄糖溶液。其可进一步包含从商业和使用者角度来看所需的其它物质,包括其它缓冲液、稀释剂、过滤物、针和注射器。此外,所述制品包含带有使用说明的包装插页,包括例如指示所述组合物的使用者将纤溶酶原组合物以及治疗伴随的疾病的其它药物给药患者。
附图说明:
图1显示14-15周龄的糖尿病小鼠给予纤溶酶原后体重的变化。
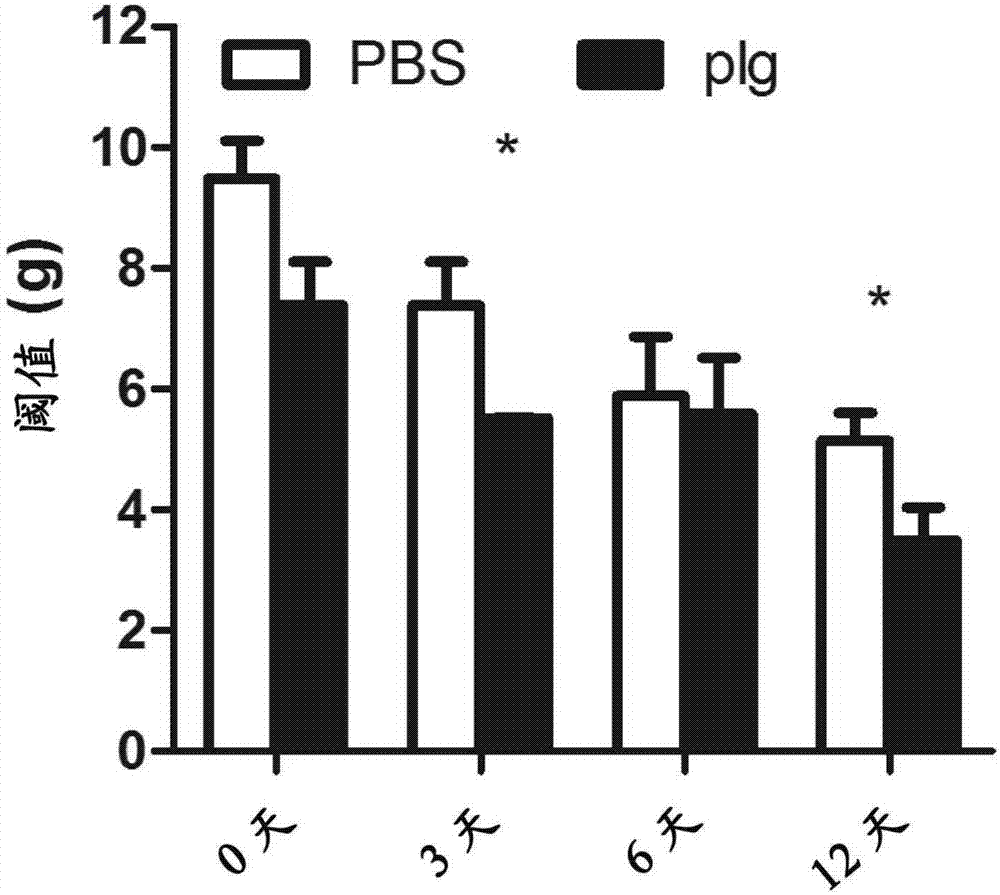
图2显示14-15周龄的糖尿病小鼠给予纤溶酶原后机械触诱发痛感应能力的变化。
图3显示14-15周龄的糖尿病小鼠在给药纤溶酶原后第0、3、6、12天检测冷刺激感应能力的结果。
图4显示14-15周龄的糖尿病小鼠在给药纤溶酶原后第0、3、6、12天检测机械痛敏感应能力的结果。
图5显示24-25周龄的糖尿病小鼠在给药纤溶酶原后体重的变化。
图6显示24-25周龄的糖尿病小鼠在给药纤溶酶原后第0、4、7、11、16天检测机械触诱发痛感应能力的结果。
图7显示24-25周龄的糖尿病小鼠在给药纤溶酶原后第0、4、7、11、16天检测冷刺激感应能力的结果。
图8显示24-25周龄的糖尿病小鼠在给纤溶酶原后第0、4、7、11、16天检测机械痛敏感应能力的结果。
图9显示24-25周龄的糖尿病小鼠在连续15天给药纤溶酶原后坐骨神经HE染色观察结果。
图10显示24-25周龄的糖尿病小鼠在连续15天给药纤溶酶原后坐骨神经纤维蛋白免疫染色观察结果。
图11显示24-25周龄的糖尿病小鼠在连续31天给药纤溶酶原后肝脏纤维蛋白免疫染色观察结果。
图12显示24-25周龄的糖尿病小鼠在连续31天给药纤溶酶原后肝脏F4/80免疫染色观察结果。
图13显示24-25周龄的糖尿病小鼠在连续31天给药纤溶酶原后肾脏纤维蛋白免疫染色观察结果。
图14显示24-25周龄的糖尿病小鼠在连续31天给药纤溶酶原后肾脏Bcl-2免疫染色观察结果。
图15显示24-25周龄的糖尿病小鼠在连续31天给药纤溶酶原后视网膜PAS染色观察结果。
图16显示24-25周龄的糖尿病小鼠在连续15天给药纤溶酶原后血清中D-二聚体的含量检测结果。
图17显示24-25周龄的糖尿病小鼠在给药纤溶酶原31天后血清心肌肌钙蛋白I浓度检测结果。
图18显示24-25周糖尿病小鼠给予纤溶酶原31天肾脏IgM免疫染色观察结果。
图19显示24-25周糖尿病小鼠给予纤溶酶原31天后血清谷丙转氨酶(ALT)检测结果。
图20显示8周龄糖尿病小鼠给予纤溶酶原9天机械触诱发痛感应能力的变化。
实施例
实施例1纤溶酶原对实验动物体重的影响
14-15周龄db/db雄鼠10只,随机分为两组,给溶媒PBS对照组和给纤溶酶原组各5只。实验开始当天记为第0天称重分组,实验第二天开始给纤溶酶原或PBS,并记为第1天。给纤溶酶原组小鼠按1mg/0.1mL/只/天尾静脉注射纤溶酶原,给溶媒PBS对照组给予相同体积的PBS。在第0、3、6、12天分别称体重。结果显示给纤溶酶原组和给溶媒PBS对照组在第0、3、6、12天体重无显著差异(图1),说明纤溶酶原对动物体重影响不大。
实施例2纤溶酶原促进糖尿病小鼠对痛觉感应能力的修复
14-15周龄db/db雄鼠10只,随机分为两组,溶媒PBS对照组和给纤溶酶原组,每组各5只。实验开始当天记为第0天称重分组,实验第二天开始给纤溶酶原或PBS并记为第1天。给纤溶酶原组小鼠按1mg/0.1mL/只/天尾静脉注射纤溶酶原,给溶媒PBS对照组给予相同体积的PBS。在给纤溶酶原后第0,3,6,12天用Von-Frey纤维丝(Stoelting,USA)检测动物对机械性损伤的敏感程度。以2.0g力为起始力,先检测其左脚。若5次刺激有4次有缩爪反应即为阳性,记为该动物对机械损伤的阈值。若2.0g力刺激反应为阴性则以大一级的力刺激其右脚,若为阳性则计为其阈值,若为阴性则继续以大一级的力刺激其左脚,如此交替刺激糖尿病鼠左右脚直到出现阳性反应[31]。Von Frey纤维丝实验统计结果显示,给药3天和给药11天后均观察到其50%痛觉阈值显著低于给溶媒PBS对照组(图2),说明纤溶酶原修复了糖尿病小鼠对机械触诱发痛(mechanical allodynia)的感应能力。
实施例3纤溶酶原恢复糖尿病小鼠对冷刺激的神经感应
14-15周龄db/db雄鼠10只,随机分为两组,给溶媒PBS对照组和给纤溶酶原组,每组各5只。实验开始当天记为第0天称重分组,实验第二天开始给纤溶酶原或PBS并记为第1天。给纤溶酶原组小鼠按1mg/0.1mL/只/天尾静脉注射纤溶酶原,给溶媒PBS对照组给予相同体积的PBS。在给纤溶酶原后第0,3,6,12天用去针头注射器挤出一滴丙酮液珠并轻触糖尿病鼠足底,使其覆盖整个足底。从左脚开始,每隔3分钟轮流刺激其左右脚,共刺激10次,并统计缩爪反应次数。反应百分比=缩爪次数/刺激次数×100%。
实验结果显示,在第0和第3天时,给纤溶酶原组和对照组对丙酮刺激无显著差异,而第6天开始观察到显著差异,在第12天则观察到极显著差异(图3)。这些结果表明,给纤溶酶原6天后显示出了对冷觉显著敏感,而在12天时出现极显著的反应差异,说明纤溶酶原极显著地修复了糖尿病小鼠对冷刺激的神经感应损伤。
实施例4纤溶酶原对糖尿病小鼠机械性痛敏感应的修复
14-15周龄db/db雄鼠10只,随机分为两组,给溶媒PBS对照组和给纤溶酶原组,每组各5只。实验开始当天记为第0天称重分组,实验第二天开始给纤溶酶原或PBS并记为第1天。给纤溶酶原组小鼠按1mg/0.1mL/只/天尾静脉注射纤溶酶原,给溶媒PBS对照组给予相同体积的PBS。在给纤溶酶原后第0,3,6,12天用美标27号针头(27gauge-needle)以轻触小鼠足底但不能刺穿其真皮层的力度刺激db/db鼠足底,从左脚开始,每隔3分钟轮流刺激其左右脚,共刺激10次,并统计缩爪反应次数。反应百分比=缩爪次数/刺激次数×100%。给纤溶酶原组和给溶媒PBS对照组对针刺反应差异极显著,P值小于0.0001(图4),说明纤溶酶原极显著地修复了糖尿病导致的神经机械性痛敏感应的损伤。
实施例5纤溶酶原对糖尿病后期神经损伤小鼠体重的影响
24-25周龄db/db雄鼠10只,随机分为两组,给溶媒PBS对照组和给纤溶酶原组,每组各5只。实验开始当天记为第0天称重分组,实验第二天开始给纤溶酶原或PBS并记为第1天,连续给药15天。给纤溶酶原组小鼠按2mg/0.2mL/只/天尾静脉注射纤溶酶原,给溶媒PBS对照组给予相同体积的PBS。在给纤溶酶原第0、4、7、11、16天分别称体重。结果显示给纤溶酶原组和给溶媒PBS对照组在第0、4、7、11、16天体重(图5)无显著差异,说明纤溶酶原对动物体重影响不大。
实施例6纤溶酶原促进糖尿病后期神经损伤小鼠对机械触诱发痛感应能力的修复
24-25周龄db/db雄鼠10只,随机分为两组,给溶媒PBS对照组和给纤溶酶原组,每组各5只。实验开始当天记为第0天称重分组,实验第二天开始给纤溶酶原或PBS并记为第1天,连续给药15天。给纤溶酶原组小鼠按2mg/0.2mL/只/天尾静脉注射纤溶酶原,给溶媒PBS对照组给予相同体积的PBS。在给纤溶酶原后第0、4、7、11、16天用Von-Frey纤维丝(Stoelting,USA)检测动物对机械性损伤的敏感程度。以2.0g力为起始力,先检测其左脚。若5次刺激有2次有缩爪反应即为阳性,若为阳性即用小一级的力再对其右脚进行刺激;若为阴性,则用大一级的力对其右脚进行刺激,如此左右脚交替刺激,刺激间隔为5分钟,总共刺激6次,然后根据S.R.Chaplan et.al.(1994)[32]介绍的方法计算其50%缩爪的阈值。
研究发现,与给溶媒PBS对照组相比,给纤溶酶原组的糖尿病小鼠机械触诱发痛反应均一性增加,且在第16天检测时发现与给溶媒PBS对照组相比出现了极显著差异(图6),说明纤溶酶原修复了神经损伤晚期的糖尿病小鼠对机械触诱发痛(mechanical allodynia)的感应能力。
实施例7纤溶酶原对糖尿病后期神经损伤小鼠冷刺激感应的修复
24-25周龄db/db雄鼠10只,随机分为两组,给溶媒PBS对照组和给纤溶酶原组,每组各5只。实验开始当天记为第0天称重分组,实验第二天开始给纤溶酶原或PBS并记为第1天,连续给药15天。给纤溶酶原组小鼠按2mg/0.2mL/只/天尾静脉注射纤溶酶原,给溶媒PBS对照组给予相同体积的PBS。在给药后第0、4、7、11、16天用去针头注射器挤出一滴丙酮液珠并轻触db/db鼠足底,使其覆盖整个足底。从左脚开始,每隔3分钟轮流刺激其左右脚,共刺激10次,并统计缩爪反应次数。反应百分比=缩爪次数/刺激次数×100%。
实验结果显示,在第0和第4天时,给纤溶酶原组和给溶媒PBS对照组对丙酮刺激并无显著差异,而第7天开始观察到显著差异,在第16天则观察到极显著差异,P值<0.0001(图7),说明给药15天后,糖尿病小鼠几乎完全恢复了对冷刺激的反应,表明纤溶酶原极显著地修复了晚期糖尿病的神经冷刺激损伤。
实施例8纤溶酶原对糖尿病后期神经损伤小鼠机械痛敏感应的修复
24-25周龄db/db雄鼠10只,随机分为两组,给溶媒PBS对照组和给纤溶酶原,每组各5只。实验开始当天记为第0天称重分组,实验第二天开始给纤溶酶原或PBS并记为第1天,连续给药15天。给纤溶酶原组小鼠按2mg/0.2mL/只/天尾静脉注射纤溶酶原,给溶媒PBS对照组给予相同体积的PBS。在给纤溶酶原后第0、4、7、11、16天用27号针头(27-gauge needle)以轻触小鼠足底但不能刺穿其真皮层的力度刺激db/db鼠足底,从左脚开始,每隔3分钟轮流刺激其左右脚,共刺激10次,并统计缩爪反应次数。反应百分比=缩爪次数/刺激次数×100%。
实验结果显示,在给纤溶酶原第7天或更早便可观察到糖尿病后期神经损伤小鼠对针刺刺激感应的不同程度的恢复,在第11和16天观察到给纤溶酶原组和给溶媒PBS对照组小鼠对针刺刺激反应有极显著差异和显著差异(图8),说明纤溶酶原极显著地修复了糖尿病后期小鼠的机械痛敏感应。
实施例9纤溶酶原对糖尿病后期神经损伤小鼠神经组织损伤的保护作用
24-25周龄db/db雄鼠10只,随机分为两组,给溶媒PBS对照组和给纤溶酶原组,每组各5只。实验开始当天记为第0天称重分组,实验第二天开始给纤溶酶原或PBS并记为第1天,连续给药15天。给纤溶酶原组小鼠按2mg/0.2mL/只/天尾静脉注射纤溶酶原,给溶媒PBS对照组给予相同体积的PBS。在第16天处死小鼠并取坐骨神经在10%中性福尔马林固定液中固定24小时。固定后的坐骨神经经酒精梯度脱水和二甲苯透明后进行石蜡包埋。组织切片厚度为5μm,切片脱蜡复水并用苏木素和伊红染色(HE染色),1%盐酸酒精分化,氨水返蓝,并酒精梯度脱水封片,切片在显微镜下400倍下观察。
实验结果显示,给溶媒PBS对照组坐骨神经纤维间隙增宽,较大数量的髓鞘轴索肿胀(↑),少数轴索崩解(▲)(图9A)。而纤溶酶原组神经纤维排列紧密,仅可见少量髓鞘轴索肿胀,崩解(图9B)。说明纤溶酶原对糖尿病后期小鼠的神经组织损伤具有一定的修复作用。
实施例10纤溶酶原减少糖尿病后期神经损伤小鼠神经组织纤维蛋白水平
24-25周龄db/db雄鼠10只,随机分为两组,给溶媒PBS对照组和给纤溶酶原组,每组各5只。实验开始当天记为第0天称重分组,实验第二天开始给纤溶酶原或PBS并记为第1天,连续给药15天。给纤溶酶原组小鼠按2mg/0.2mL/只/天尾静脉注射纤溶酶原,给溶媒PBS对照组给予相同体积的PBS。在第16天处死小鼠并取坐骨神经在10%中性福尔马林固定液中固定24小时。固定后的坐骨神经经酒精梯度脱水和二甲苯透明后进行石蜡包埋。组织切片厚度为5μm,切片脱蜡复水后水洗1次,然后用PAP笔圈出组织。以3%TBS稀释的双氧水孵育15分钟,水洗3次。10%正常羊血清(Vector laboratories,Inc.,USA)封闭1小时,吸走多余血清。兔抗小鼠纤维蛋白(原)抗体(Abcam)室温孵育1小时或4℃孵育过夜,TBS洗3次。山羊抗兔IgG(HRP)抗体(Abcam)二抗室温孵育1小时,TBS洗3次。按DAB试剂盒(Vector laboratories,Inc.,USA)显色,水洗3次后苏木素复染30秒,流水冲洗5分钟。梯度脱水透明并封片,切片在显微镜下400倍下观察。
纤维蛋白原是纤维蛋白的前体,在组织存在损伤的情况下,作为机体对损伤的一种应激反应,纤维蛋白原水解成纤维蛋白[33-35]。因此可将纤维蛋白原水平作为损伤程度的一个标志。
研究发现,与给溶媒PBS对照组(图10A)相比,给纤溶酶原组(图10B)的小鼠其坐骨神经纤维蛋白的水平降低,说明纤溶酶原使神经组织的损伤得到了一定程度的修复。
实施例11纤溶酶原减少糖尿病晚期肝组织纤维蛋白水平
24-25周龄db/db雄鼠10只,随机分为两组,给溶媒PBS对照组和给纤溶酶原组,每组各5只。实验开始当天记为第0天称重分组,实验第二天开始给纤溶酶原或PBS并记为第1天,连续给药31天。给纤溶酶原组小鼠按2mg/0.2mL/只/天尾静脉注射纤溶酶原,给溶媒PBS对照组给予相同体积的PBS。在第32天处死小鼠并取肝脏组织在10%中性福尔马林固定液中固定24小时。固定后的肝脏组织经酒精梯度脱水和二甲苯透明后进行石蜡包埋。组织切片厚度为5μm,切片脱蜡复水后水洗1次。以3%双氧水孵育15分钟,水洗2次,每次5分钟。10%的正常羊血清液(Vector laboratories,Inc.,USA)封闭1小时;时间到后,弃除羊血清液,用PAP笔圈出组织。兔抗小鼠纤维蛋白(原)抗体(Abcam)4℃孵育过夜,TBS洗2次,每次5分钟。山羊抗兔IgG(HRP)抗体(Abcam)二抗室温孵育1小时,TBS洗2次,每次5分钟。按DAB试剂盒(Vector laboratories,Inc.,USA)显色,水洗3次后苏木素复染30秒,流水冲洗5分钟。梯度脱水透明并封片,切片在显微镜下200倍下观察。
纤维蛋白原是纤维蛋白的前体,在组织存在损伤的情况下,作为机体对损伤的一种应激反应,纤维蛋白原水解成纤维蛋白[33-35]。因此可将纤维蛋白水平作为损伤程度的一个标志。
研究发现,与给溶媒PBS对照组(图11A)相比,给纤溶酶原组(图11B)的小鼠其肝脏组织纤维蛋白阳性着色浅,说明注射纤溶酶原能使糖尿病小鼠肝脏组织沉积的纤维蛋白显著降低,反映出纤溶酶原对糖尿病小鼠的肝脏组织损伤有显著修复作用。
实施例12纤溶酶原减轻糖尿病晚期小鼠肝脏组织的炎症
24-25周龄db/db雄鼠10只,随机分为两组,给溶媒PBS对照组和给纤溶酶原组,每组各5只。实验开始当天记为第0天称重分组,实验第二天开始给纤溶酶原或PBS并记为第1天,连续给药31天。给纤溶酶原组小鼠按2mg/0.2mL/只/天尾静脉注射纤溶酶原,给溶媒PBS对照组给予相同体积的PBS。给纤溶酶原31天后处死小鼠并取肝脏组织在10%中性福尔马林固定液中固定24小时。固定后的肝脏组织经酒精梯度脱水和二甲苯透明后进行石蜡包埋。组织切片厚度为5μm,切片脱蜡复水后水洗1次。以3%双氧水孵育15分钟,水洗2次,每次5分钟。10%正常羊血清(Vector laboratories,Inc.,USA)封闭1小时,时间到后甩去血清,用PAP笔圈出组织。针对F4/80的兔多克隆抗体(Abcam)4℃孵育过夜,TBS洗2次,每次5分钟。山羊抗兔IgG(HRP)抗体(Abcam)二抗室温孵育1小时,TBS洗2次。按DAB试剂盒(Vector laboratories,Inc.,USA)显色,水洗3次后苏木素复染30秒,流水冲洗5分钟。梯度脱水透明并封片,切片在显微镜下400倍下观察。
F4/80为巨噬细胞标志物,可以表示炎症反应的程度和阶段。结果显示,给纤溶酶原组(图12B)与给溶媒PBS对照组(图12A)相比,给纤溶酶原组小鼠的F4/80阳性表达明显降低,说明给纤溶酶原后肝脏组织炎症减少。图12C为F4/80免疫组化阳性表达数定量分析结果,给纤溶酶原组F4/80表达量显著减少,且具有统计学差异,说明注射纤溶酶原能够显著减轻糖尿病小鼠肝脏的炎症。
实施例13纤溶酶原促进糖尿病晚期小鼠肾脏纤维蛋白水解
24-25周龄db/db雄鼠20只,随机分为两组,给溶媒PBS对照组和给纤溶酶原组,每组各10只。实验开始当天记为第0天称重分组,实验第二天开始给纤溶酶原或PBS并记为第1天,连续给药31天。给纤溶酶原组小鼠按2mg/0.2mL/只/天尾静脉注射纤溶酶原,给溶媒PBS对照组给予相同体积的PBS。在第32天处死小鼠并取肾脏在10%中性福尔马林固定液中固定24小时。固定后的肾脏组织经酒精梯度脱水和二甲苯透明后进行石蜡包埋。组织切片厚度为5μm,切片脱蜡复水后水洗1次。以3%双氧水孵育15分钟,水洗2次,每次5分钟。10%的正常羊血清液(Vector laboratories,Inc.,USA)封闭1小时;时间到后,弃除羊血清液,用PAP笔圈出组织。兔抗小鼠纤维蛋白(原)抗体(Abcam)4℃孵育过夜,TBS洗2次,每次5分钟。山羊抗兔IgG(HRP)抗体(Abcam)二抗室温孵育1小时,TBS洗2次,每次5分钟。按DAB试剂盒(Vector laboratories,Inc.,USA)显色,水洗3次后苏木素复染30秒,流水冲洗5分钟。梯度脱水透明并封片,切片在显微镜下200倍下观察。
纤维蛋白原是纤维蛋白的前体,在组织存在损伤的情况下,作为机体对损伤的一种应激反应,纤维蛋白原水解成纤维蛋白沉积在损伤部位[33-35]。因此,可将纤维蛋白水平作为损伤程度的一个标志。
结果显示,给纤溶酶原组(图13B)比给溶媒PBS对照组(图13A)纤维蛋白原阳性着色浅,说明注射纤溶酶原能够显著降低糖尿病小鼠肾脏沉积的纤维蛋白,反映出纤溶酶原对糖尿病小鼠的机体损伤有显著修复作用。
实施例14纤溶酶原促进糖尿病晚期小鼠肾脏细胞凋亡抑制蛋白Bcl-2的表达
24-25周龄db/db雄鼠20只,随机分为两组,给溶媒PBS对照组和给纤溶酶原组,每组各10只。实验开始当天记为第0天称重分组,实验第二天开始给纤溶酶原或PBS并记为第1天,连续给药31天。给纤溶酶原组小鼠按2mg/0.2mL/只/天尾静脉注射纤溶酶原,给溶媒PBS对照组给予相同体积的PBS。在第32天处死小鼠并取肾脏在10%中性福尔马林固定液中固定24小时。固定后的肾脏组织经酒精梯度脱水和二甲苯透明后进行石蜡包埋。组织切片厚度为5μm,切片脱蜡复水后水洗1次。以3%双氧水孵育15分钟,水洗2次,每次5分钟。10%的正常羊血清液(Vector laboratories,Inc.,USA)封闭1小时;时间到后,弃除羊血清液,用PAP笔圈出组织。兔抗小鼠Bcl-2抗体(Abcam)4℃孵育过夜,TBS洗2次,每次5分钟。山羊抗兔IgG(HRP)抗体(Abcam)二抗室温孵育1小时,TBS洗2次,每次5分钟。按DAB试剂盒(Vector laboratories,Inc.,USA)显色,水洗3次后苏木素复染30秒,流水冲洗5分钟。梯度脱水透明并封片,切片在显微镜下200倍下观察。
Bcl-2为细胞凋亡抑制蛋白,在凋亡刺激因子作用下会下调表达[36,37]。Bcl-2免疫组化结果显示,给纤溶酶原组(图14B)肾小管上皮细胞阳性表达着色要明显深于给溶媒PBS对照组(图14A),且前者的着色范围更广。定量分析结果与观察结果一致,且具有显著差异(如图14C)。这表明纤溶酶原能够促进糖尿病小鼠肾脏细胞凋亡抑制分子Bcl-2的表达,从而能够抑制糖尿病小鼠肾脏组织细胞的凋亡。
实施例15纤溶酶原改善糖尿病晚期小鼠视网膜的损伤
24-25周龄db/db雄鼠20只,随机分为两组,给溶媒PBS对照组和给纤溶酶原组,每组各10只。实验开始当天记为第0天称重分组,实验第二天开始给纤溶酶原或PBS并记为第1天,连续给药31天。给纤溶酶原组小鼠按2mg/0.2mL/只/天尾静脉注射纤溶酶原,给溶媒PBS对照组给予相同体积的PBS。在第32天处死小鼠并取左侧眼球在多聚甲醛固定液中固定24小时。固定后的眼球剥离出视网膜后,置于1mL 3%胰酶(Solarbio)的EP管中,在摇床中37℃震荡消化2-3h。待视网膜出现软化、脱落的现象后小心的将视网膜移入装有蒸馏水的EP管中,于摇床中37℃震荡2-3h,使视网膜上多余的组织脱落。轻柔的吹打视网膜,使其只剩血管层后在玻片上铺片,自然风干。视网膜于Schiff氏液染色(PAS染色),1%盐酸酒精分化,氨水返蓝,并酒精梯度脱水二甲苯透明后封片,在显微镜下400倍下观察。
从实验结果可以看出,与纤溶酶原组(图15B)相比,给溶媒PBS对照组(图15A)db/db鼠视网膜毛细血管管径粗细不一,血管管壁增厚深染,血管内皮细胞(Δ)增生,周细胞(↓)明显减少,而给纤溶酶原组病理改变明显减轻;定量分析发现给纤溶酶原组与给溶媒PBS对照组相比无细胞血管长度(图15C)显著减少,并且统计学分析结果显示显著差异。说明纤溶酶原能够显著促进糖尿病后期小鼠视网膜损伤的修复。
实施例16纤溶酶原促进糖尿病造成的微血栓的溶解
24-25周龄db/db雄鼠10只,随机分为两组,给溶媒PBS对照组和给纤溶酶原组,每组各5只。实验开始当天记为第0天称重分组,实验第二天开始给纤溶酶原或PBS并记为第1天,连续给药15天。给纤溶酶原组小鼠按2mg/0.2mL/只/天尾静脉注射纤溶酶原,给溶媒PBS对照组给予相同体积的PBS。在第16天摘眼球取血,全血静置后血清用于检测血液中D-二聚体含量。
结果显示,给药15天后,给纤溶酶原组血清中D-二聚体含量显著上升(图16),说明给纤溶酶原后,由于糖尿病造成的微血栓显著溶解。
实施例17纤溶酶原促进糖尿病晚期心肌损伤的修复
24-25周龄db/db雄鼠28只,随机分为两组,给溶媒PBS对照组12只,给纤溶酶原组16只。实验开始当天记为第0天称重分组,实验第二天开始给纤溶酶原或PBS并记为第1天,连续给药31天。给纤溶酶原组小鼠按2mg/0.2mL/只/天尾静脉注射纤溶酶原,给溶媒PBS对照组给予相同体积的PBS。第32天摘除眼球取血,以3500r/min离心15-20分钟,并取心取上清进行心肌肌钙蛋白I的浓度测定。
心肌肌钙蛋白I(cardiac troponin,CTNI)是心肌损伤的重要标志物,其血清浓度能够反映心肌损伤的程度[38]。结果显示,给纤溶酶原组心肌肌钙蛋白I的浓度要明显的低于给溶媒PBS对照组,且具有极显著的统计学差异(图17)。说明纤溶酶原能够极显著促进糖尿病后期小鼠心肌损伤的修复。
实施例18纤溶酶原降低糖尿病晚期小鼠肾脏的损伤
24-25周龄db/db雄鼠8只,随机分为两组,给溶媒PBS对照组和给纤溶酶原组,每组各4只。实验开始当天记为第0天称重分组,实验第二天开始给纤溶酶原或PBS并记为第1天,连续给药31天。给纤溶酶原组小鼠按2mg/0.2mL/只/天尾静脉注射纤溶酶原,给溶媒PBS对照组给予相同体积的PBS。在第32天检测生理指标结束,处死小鼠并取肾脏在10%中性福尔马林固定液中固定24小时。固定后的肾脏组织经酒精梯度脱水和二甲苯透明后进行石蜡包埋。组织切片厚度为5μm,切片脱蜡复水后水洗1次。以3%双氧水孵育15分钟,水洗2次,每次5分钟。山羊抗鼠IgM(HRP)抗体(Abcam)室温孵育1小时,TBS洗2次,每次5分钟。按DAB试剂盒(Vector laboratories,Inc.,USA)显色,水洗3次后苏木素复染30秒,流水冲洗5分钟。梯度脱水透明并封片,切片在显微镜下400倍下观察。
IgM抗体在清除凋亡和坏死细胞过程中发挥着重要作用[39-41]。因此,其表达能够反映组织器官的损伤情况。
结果显示,给纤溶酶原组(图18B)小鼠肾小球IgM的阳性着色浅于给溶媒PBS对照组(图18A),并且范围也较小,统计分析结果与观察结果一致(图18C),这表明注射纤溶酶原后肾小球的损伤明显的改善,反映出纤溶酶原对糖尿病小鼠的机体损伤有显著修复功能。
实施例19纤溶酶原促进糖尿病小鼠肝脏损的修复
25-28周龄db/db雄鼠9只,随机分为两组,给溶媒PBS对照组3只,给纤溶酶原组6只。实验开始当天记为第0天称重分组,实验第二天开始给纤溶酶原或PBS并记为第1天,连续给药31天。给纤溶酶原组小鼠按2mg/0.2mL/只/天尾静脉注射纤溶酶原,给溶媒PBS对照组给予相同体积的PBS。给纤溶酶原31天后摘眼球采全血,待血清析出后4℃3500r/min离心10分钟,取上清液进行检测。本实验使用谷丙转氨酶检测试剂盒(南京建成生物工程研究所,货号C009-2),运用赖氏比色法(Reitman-Frankel)检测血清中谷丙转氨酶(ALT)的含量。
谷丙转氨酶是肝脏健康状态的一个重要指标[42,43],谷丙转氨酶的正常参考值区间为9~50U/L。检测结果显示,给溶媒PBS对照组血清中ALT的含量显著高于正常生理指标,而给纤溶酶原组已经恢复到体内的正常水平,并且给纤溶酶原组要显著低于给溶媒PBS对照组,且具有统计学差异(图19)。说明在糖尿病晚期模型小鼠中,注射纤溶酶原能有效地修复肝损伤。
实施例20纤溶酶原促进糖尿病小鼠对痛觉感应能力的修复
8周龄db/db雄鼠8只,随机分为两组,给溶媒PBS对照组和给纤溶酶原组,每组4只。实验开始当天记为第0天称重分组,实验第二天开始给纤溶酶原或PBS并记为第1天,连续给药8天。给纤溶酶原组小鼠按2mg/0.2mL/只/天尾静脉注射纤溶酶原,给溶媒PBS对照组给予相同体积的PBS。在给纤溶酶原后第0,3,6、9天用Von-Frey纤维丝(Stoelting,USA)检测动物对机械性损伤的敏感程度。以2.0g力为起始力,先检测其左脚。若5次刺激有2次有缩爪反应即为阳性,若为阳性即用小一级的力再对其右脚进行刺激;若为阴性,则用大一级的力对其右脚进行刺激,如此左右脚交替刺激,刺激间隔为5分钟,总共刺激6次,然后根据S.R.Chaplan et.al.(1994)[32]介绍的方法计算其50%缩爪的阈值。
db/db鼠在4周左右时发展成糖尿病鼠,8-12周时痛觉超敏,12周以后则痛觉脱敏[45,46]。因此,我们选择8周龄超敏期的db/db鼠来进行实验。
结果显示,与给溶酶PBS对照组相比,给纤溶酶原组小鼠的痛觉阈值显著升高(图20)。说明纤溶酶原能够显著减轻糖尿病早期神经损伤所致的痛觉超敏(过度敏感)。
参考文献:
[1]Md.Shahidul Islam,2013.Animal Models of Diabetic Neuropathy:Progress Since 1960s.Journal of Diabetes Research.
[2]Eizirik DL,Miani M,Cardozo AK.2013.Signalling danger:Endoplasmic reticulum stress and the unfolded protein response in pancreatic islet inflammation.Diabetologia 56:234–241.
[3]Said G.Diabetic neuropathy.Nat Clin Pract Neurol 2007;3:331-40.
[4]Vincent AM,Callaghan BC,Smith AL,Feldman EL.2011.Diabetic neuropathy:Cellular mechanisms as therapeutic targets.Nat Rev Neurol 7:573–583.
[5]Alexander CM and Werb,Z.(1991).Extracellular matrix degradation.In Cell Biology of Extracellular Matrix,Hay ED,ed.(New York:Plenum Press),pp.255-302.
[6]Werb,Z.,Mainardi,C.L.,Vater,C.A.,and Harris,E.D.,Jr.(1977).Endogenous activiation of latent collagenase by rheumatoid synovial cells.Evidence for a role of plasminogen activator.N.Engl.J.Med.296,1017-1023.
[7]He,C.S.,Wilhelm,S.M.,Pentland,A.P.,Marmer,B.L.,Grant,G.A.,Eisen,A.Z.,and Goldberg,G.I.(1989).Tissue cooperation in a proteolytic cascade activating human interstitial collagenase.Proc.Natl.Acad.Sci.U.S.A 86,2632-2636.
[8]Stoppelli,M.P.,Corti,A.,Soffientini,A.,Cassani,G.,Blasi,F.,and Assoian,R.K.(1985).Differentiation-enhanced binding of the amino-terminal fragment of human urokinase plasminogen activator to a specific receptor on U937monocytes.Proc.Natl.Acad.Sci.U.S.A 82,4939-4943.
[9]Vassalli,J.D.,Baccino,D.,and Belin,D.(1985).A cellular binding site for the Mr 55,000 form of the human plasminogen activator,urokinase.J.Cell Biol.100,86-92.
[10]Wiman,B.and Wallen,P.(1975).Structural relationship between"glutamic acid"and "lysine"forms of human plasminogen and their interaction with the NH2-terminal activation peptide as studied by affinity chromatography.Eur.J.Biochem.50,489-494.
[11]Saksela,O.and Rifkin,D.B.(1988).Cell-associated plasminogen activation:regulation and physiological functions.Annu.Rev.Cell Biol.4,93-126.
[12]Raum,D.,Marcus,D.,Alper,C.A.,Levey,R.,Taylor,P.D.,and Starzl,T.E.(1980).Synthesis of human plasminogen by the liver.Science 208,1036-1037
[13]Wallén P(1980).Biochemistry of plasminogen.In Fibrinolysis,Kline DL and Reddy KKN,eds.(Florida:CRC
[14]Sottrup-Jensen,L.,Zajdel,M.,Claeys,H.,Petersen,T.E.,and Magnusson,S.(1975).Amino-acid sequence of activation cleavage site in plasminogen:homology with"pro"part of prothrombin.Proc.Natl.Acad.Sci.U.S.A 72,2577-2581.
[15]Collen,D.and Lijnen,H.R.(1991).Basic and clinical aspects of fibrinolysis and thrombolysis.Blood 78,3114-3124.
[16]Alexander,C.M.and Werb,Z.(1989).Proteinases and extracellular matrix remodeling.Curr.Opin.Cell Biol.1,974-982.
[17]Mignatti,P.and Rifkin,D.B.(1993).Biology and biochemistry of proteinases in tumor invasion.Physiol Rev.73,161-195.
[18]Collen,D.(2001).Ham-Wasserman lecture:role of the plasminogen system in fibrin-homeostasis and tissue remodeling.Hematology.(Am.Soc.Hematol.Educ.Program.)1-9.
[19]Rifkin,D.B.,Moscatelli,D.,Bizik,J.,Quarto,N.,Blei,F.,Dennis,P.,Flaumenhaft,R.,and Mignatti,P.(1990).Growth factor control of extracellular proteolysis.Cell Differ.Dev.32,313-318.
[20]Andreasen,P.A.,Kjoller,L.,Christensen,L.,and Duffy,M.J.(1997).The urokinase-type plasminogen activator system in cancer metastasis:a review.Int.J.Cancer 72,1-22.
[21]Rifkin,D.B.,Mazzieri,R.,Munger,J.S.,Noguera,I.,and Sung,J.(1999).Proteolytic control of growth factor availability.APMIS 107,80-85.
[22]Cheng HT,Dauch JR,Hayes JM,Hong Y,Feldman EL.2009.Nerve growth factor mediates mechanical allodynia in a mouse model of type 2 diabetes.J Neuropathol Exp Neurol 68:1229–1243.
[23]Ii M,Nishimura H,Kusano KF,Qin G,Yoon YS,Wecker A,Asahara T,Losordo DW.2005.Neuronal nitric oxide synthase mediates statin-induced restoration of vasa nervorum and reversal of diabetic neuropathy.Circulation 112:93–102.
[24]Kan M,Guo G,Singh B,Singh V,Zochodne DW.2012.Glucagon-like peptide 1,insulin,sensory neurons,and diabetic neuropathy.J Neuropathol Exp Neurol 71:494–510.
[25]Sullivan KA,Hayes JM,Wiggin TD,Backus C,Su Oh S,Lentz SI,Brosius F 3rd,Feldman EL.2007.Mouse models of diabetic neuropathy.Neurobiol Dis 28:276–285.
[26]Wang L,Chopp M,Szalad A,Liu Z,Bolz M,Alvarez FM,Lu M,Zhang L,Cui Y,Zhang RL,Zhang ZG.2011.Phosphodiesterase-5 is a therapeutic target for peripheral neuropathy in diabetic mice.Neuroscience 193:399–410.
[27]Marder V J,Novokhatny V.Direct fibrinolytic agents:biochemical attributes,preclinical foundation and clinical potential[J].Journal of Thrombosis and Haemostasis,2010,8(3):433-444.
[28]Sottrup-Jensen L,Claeys H,Zajdel M,et al.The primary structure of human plasminogen:Isolation of two lysine-binding fragments and one“mini”-plasminogen(MW,38,000)by elastase-catalyzed-specific limited proteolysis[J].Progress in chemical fibrinolysis and thrombolysis,1978,3:191-209.
[29]Nagai N,Demarsin E,Van Hoef B,et al.Recombinant human microplasmin:production and potential therapeutic properties[J].Journal of Thrombosis and Haemostasis,2003,1(2):307-313.
[30]Hunt J A,Petteway Jr S R,Scuderi P,et al.Simplified recombinant plasmin:production and fu-nctional comparison of a novel thrombolytic molecule with plasma-derived plasmin[J].Thromb Haemost,2008,100(3):413-419.
[31]Yoon Choi a,Young Wook Yoon a,Heung Sik Na,Sun Ho Kim,Jin MO Chung.Behavioral signs of ongoing pain and cold allodynia in a rat model of neuropathic pain,Pain,59(1994)369-376.
[32]S.R.Chaplan,et al.,Quantitative assessment of tactile allodynia in the rat paw,Journal of Neuroscience Methods 53(1994)55-63.
[33]Jae Kyu Ryu,Mark A.Petersen,Sara G.Murray et al.Blood coagulation protein fibrinogen promotes autoimmunity and demyelination via chemokine release and antigen presentation.NATURE COMMUNICATIONS,2015,6:8164.
[34]Dimitrios Davalos,Katerina Akassoglou.Fibrinogen as a key regulator of inflammation in disease.Seminars in Immunopathology,2012.34(1):43-62.
[35]Valvi D,Mannino DM,Mullerova H,et al.Fibrinogen,chronic obstructive pulmonary disease(COPD)and outcomes in two United States cohorts.Int J Chron Obstruct Pulmon Dis 2012;7:173–82.
[36]Moungj aroen J,Nimmannit U,Callery PS,Wang L,Azad N,Lipipun V,Chanvorachote P,Rojanasakul Y(2006).Reactive oxygen species mediate caspase activation and apoptosis induced by lipoic acid in human lung epithelial cancer cells through Bcl-2 downregulation.J Pharmacol Exp Ther 319,1062–1069.
[37]Wang L,Chanvorachote P,Toledo D,Stehlik C,Mercer RR,Castranova V,Rojanasakul Y (2008).Peroxide is a key mediator of Bcl-2 down-regulation and apoptosis induction by cisplatinin human lung cancer cells.Mol Pharmacol 73,119–127.
[38]R.Langhorn and J.L.Willesen.Cardiac Troponins in Dogs and Cats.J Vet Intern Med 2016;30:36–50.
[39]Zwart B,Ciurana C,Rensink I,Manoe R,Hack CE,et al.(2004)Complement activation by apoptotic cells occurs predominantly via IgM and is limited to late apoptotic(secondary necrotic)cells.Autoimmunity 37:95–102.
[40]Zhang M,Takahashi K,Alicot EM,Vorup-Jensen T,Kessler B,et al.(2006)Activation of the lectin pathway by natural IgM in a model of ischemia/reperfusion injury.J Immunol 177:4727–4734.
[41]Kim SJ,Gershov D,Ma X,Brot N,Elkon KB(2002)I-PLA2 Activation during Apoptosis Promotes the Exposure of Membrane Lysophosphatidylcholine Leading to Binding by Natural Immunoglobulin M Antibodies and Complement Activation.The Journal of Experimental Medicine 196:655–665.
[42]Karmen A,Wroblewski F,Ladue JS(Jan 1955).Transaminase activity in human blood.The Journal of Clinical Investigation.34(1):126–31
[43]Wang CS,Chang TT,Yao WJ,Wang ST,Chou P(Apr 2012).Impact of increasing alanine aminotransferase levels within normal range on incident diabetes.Journal of the Formosan Medical Association=Taiwan Yi Zhi.111(4):201–8.
[44]Roy S,Sato T,Paryani G,Kao R:Downregulation of fibronectin overexpression reduces basement membrane thickening and vascular lesions in retinas of galactose-fed rats.Diabetes 2003,52:1229–1234.
[45]Cheng HT,Dauch JR,Hayes JM,Hong Y,Feldman EL.2009.Nerve growthfactor mediates mechanical allodynia in a mouse model of type 2 diabetes.J Neuropathol Exp Neurol 68:1229–1243.
[46]Ii M,Nishimura H,Kusano KF,Qin G,Yoon YS,Wecker A,Asahara T,Losordo DW.2005.Neuronal nitric oxide synthase mediatesstatin-induced restoration of vasa nervorum and reversal of diabetic neuropathy.Circulation 112:93–102。
序列表
<110> 深圳瑞健生命科学研究院有限公司
<120> 一种预防或治疗糖尿病性神经损伤及其相关病症的方法
<130> PCK02771
<160> 14
<170> PatentIn version 3.5
<210> 1
<211> 2376
<212> DNA
<213> 不含有信号肽的天然纤溶酶原(Glu-PLG,Glu-纤维蛋白溶酶原)核酸序列
<400> 1
gagcctctgg atgactatgt gaatacccag ggggcttcac tgttcagtgt cactaagaag 60
cagctgggag caggaagtat agaagaatgt gcagcaaaat gtgaggagga cgaagaattc 120
acctgcaggg cattccaata tcacagtaaa gagcaacaat gtgtgataat ggctgaaaac 180
aggaagtcct ccataatcat taggatgaga gatgtagttt tatttgaaaa gaaagtgtat 240
ctctcagagt gcaagactgg gaatggaaag aactacagag ggacgatgtc caaaacaaaa 300
aatggcatca cctgtcaaaa atggagttcc acttctcccc acagacctag attctcacct 360
gctacacacc cctcagaggg actggaggag aactactgca ggaatccaga caacgatccg 420
caggggccct ggtgctatac tactgatcca gaaaagagat atgactactg cgacattctt 480
gagtgtgaag aggaatgtat gcattgcagt ggagaaaact atgacggcaa aatttccaag 540
accatgtctg gactggaatg ccaggcctgg gactctcaga gcccacacgc tcatggatac 600
attccttcca aatttccaaa caagaacctg aagaagaatt actgtcgtaa ccccgatagg 660
gagctgcggc cttggtgttt caccaccgac cccaacaagc gctgggaact ttgtgacatc 720
ccccgctgca caacacctcc accatcttct ggtcccacct accagtgtct gaagggaaca 780
ggtgaaaact atcgcgggaa tgtggctgtt accgtgtccg ggcacacctg tcagcactgg 840
agtgcacaga cccctcacac acataacagg acaccagaaa acttcccctg caaaaatttg 900
gatgaaaact actgccgcaa tcctgacgga aaaagggccc catggtgcca tacaaccaac 960
agccaagtgc ggtgggagta ctgtaagata ccgtcctgtg actcctcccc agtatccacg 1020
gaacaattgg ctcccacagc accacctgag ctaacccctg tggtccagga ctgctaccat 1080
ggtgatggac agagctaccg aggcacatcc tccaccacca ccacaggaaa gaagtgtcag 1140
tcttggtcat ctatgacacc acaccggcac cagaagaccc cagaaaacta cccaaatgct 1200
ggcctgacaa tgaactactg caggaatcca gatgccgata aaggcccctg gtgttttacc 1260
acagacccca gcgtcaggtg ggagtactgc aacctgaaaa aatgctcagg aacagaagcg 1320
agtgttgtag cacctccgcc tgttgtcctg cttccagatg tagagactcc ttccgaagaa 1380
gactgtatgt ttgggaatgg gaaaggatac cgaggcaaga gggcgaccac tgttactggg 1440
acgccatgcc aggactgggc tgcccaggag ccccatagac acagcatttt cactccagag 1500
acaaatccac gggcgggtct ggaaaaaaat tactgccgta accctgatgg tgatgtaggt 1560
ggtccctggt gctacacgac aaatccaaga aaactttacg actactgtga tgtccctcag 1620
tgtgcggccc cttcatttga ttgtgggaag cctcaagtgg agccgaagaa atgtcctgga 1680
agggttgtag gggggtgtgt ggcccaccca cattcctggc cctggcaagt cagtcttaga 1740
acaaggtttg gaatgcactt ctgtggaggc accttgatat ccccagagtg ggtgttgact 1800
gctgcccact gcttggagaa gtccccaagg ccttcatcct acaaggtcat cctgggtgca 1860
caccaagaag tgaatctcga accgcatgtt caggaaatag aagtgtctag gctgttcttg 1920
gagcccacac gaaaagatat tgccttgcta aagctaagca gtcctgccgt catcactgac 1980
aaagtaatcc cagcttgtct gccatcccca aattatgtgg tcgctgaccg gaccgaatgt 2040
ttcatcactg gctggggaga aacccaaggt acttttggag ctggccttct caaggaagcc 2100
cagctccctg tgattgagaa taaagtgtgc aatcgctatg agtttctgaa tggaagagtc 2160
caatccaccg aactctgtgc tgggcatttg gccggaggca ctgacagttg ccagggtgac 2220
agtggaggtc ctctggtttg cttcgagaag gacaaataca ttttacaagg agtcacttct 2280
tggggtcttg gctgtgcacg ccccaataag cctggtgtct atgttcgtgt ttcaaggttt 2340
gttacttgga ttgagggagt gatgagaaat aattaa 2376
<210> 2
<211> 791
<212> PRT
<213> 不含有信号肽的天然纤溶酶原(Glu-PLG,Glu-纤维蛋白溶酶原)氨基酸序列
<400> 2
Glu Pro Leu Asp Asp Tyr Val Asn Thr Gln Gly Ala Ser Leu Phe Ser
1 5 10 15
Val Thr Lys Lys Gln Leu Gly Ala Gly Ser Ile Glu Glu Cys Ala Ala
20 25 30
Lys Cys Glu Glu Asp Glu Glu Phe Thr Cys Arg Ala Phe Gln Tyr His
35 40 45
Ser Lys Glu Gln Gln Cys Val Ile Met Ala Glu Asn Arg Lys Ser Ser
50 55 60
Ile Ile Ile Arg Met Arg Asp Val Val Leu Phe Glu Lys Lys Val Tyr
65 70 75 80
Leu Ser Glu Cys Lys Thr Gly Asn Gly Lys Asn Tyr Arg Gly Thr Met
85 90 95
Ser Lys Thr Lys Asn Gly Ile Thr Cys Gln Lys Trp Ser Ser Thr Ser
100 105 110
Pro His Arg Pro Arg Phe Ser Pro Ala Thr His Pro Ser Glu Gly Leu
115 120 125
Glu Glu Asn Tyr Cys Arg Asn Pro Asp Asn Asp Pro Gln Gly Pro Trp
130 135 140
Cys Tyr Thr Thr Asp Pro Glu Lys Arg Tyr Asp Tyr Cys Asp Ile Leu
145 150 155 160
Glu Cys Glu Glu Glu Cys Met His Cys Ser Gly Glu Asn Tyr Asp Gly
165 170 175
Lys Ile Ser Lys Thr Met Ser Gly Leu Glu Cys Gln Ala Trp Asp Ser
180 185 190
Gln Ser Pro His Ala His Gly Tyr Ile Pro Ser Lys Phe Pro Asn Lys
195 200 205
Asn Leu Lys Lys Asn Tyr Cys Arg Asn Pro Asp Arg Glu Leu Arg Pro
210 215 220
Trp Cys Phe Thr Thr Asp Pro Asn Lys Arg Trp Glu Leu Cys Asp Ile
225 230 235 240
Pro Arg Cys Thr Thr Pro Pro Pro Ser Ser Gly Pro Thr Tyr Gln Cys
245 250 255
Leu Lys Gly Thr Gly Glu Asn Tyr Arg Gly Asn Val Ala Val Thr Val
260 265 270
Ser Gly His Thr Cys Gln His Trp Ser Ala Gln Thr Pro His Thr His
275 280 285
Asn Arg Thr Pro Glu Asn Phe Pro Cys Lys Asn Leu Asp Glu Asn Tyr
290 295 300
Cys Arg Asn Pro Asp Gly Lys Arg Ala Pro Trp Cys His Thr Thr Asn
305 310 315 320
Ser Gln Val Arg Trp Glu Tyr Cys Lys Ile Pro Ser Cys Asp Ser Ser
325 330 335
Pro Val Ser Thr Glu Gln Leu Ala Pro Thr Ala Pro Pro Glu Leu Thr
340 345 350
Pro Val Val Gln Asp Cys Tyr His Gly Asp Gly Gln Ser Tyr Arg Gly
355 360 365
Thr Ser Ser Thr Thr Thr Thr Gly Lys Lys Cys Gln Ser Trp Ser Ser
370 375 380
Met Thr Pro His Arg His Gln Lys Thr Pro Glu Asn Tyr Pro Asn Ala
385 390 395 400
Gly Leu Thr Met Asn Tyr Cys Arg Asn Pro Asp Ala Asp Lys Gly Pro
405 410 415
Trp Cys Phe Thr Thr Asp Pro Ser Val Arg Trp Glu Tyr Cys Asn Leu
420 425 430
Lys Lys Cys Ser Gly Thr Glu Ala Ser Val Val Ala Pro Pro Pro Val
435 440 445
Val Leu Leu Pro Asp Val Glu Thr Pro Ser Glu Glu Asp Cys Met Phe
450 455 460
Gly Asn Gly Lys Gly Tyr Arg Gly Lys Arg Ala Thr Thr Val Thr Gly
465 470 475 480
Thr Pro Cys Gln Asp Trp Ala Ala Gln Glu Pro His Arg His Ser Ile
485 490 495
Phe Thr Pro Glu Thr Asn Pro Arg Ala Gly Leu Glu Lys Asn Tyr Cys
500 505 510
Arg Asn Pro Asp Gly Asp Val Gly Gly Pro Trp Cys Tyr Thr Thr Asn
515 520 525
Pro Arg Lys Leu Tyr Asp Tyr Cys Asp Val Pro Gln Cys Ala Ala Pro
530 535 540
Ser Phe Asp Cys Gly Lys Pro Gln Val Glu Pro Lys Lys Cys Pro Gly
545 550 555 560
Arg Val Val Gly Gly Cys Val Ala His Pro His Ser Trp Pro Trp Gln
565 570 575
Val Ser Leu Arg Thr Arg Phe Gly Met His Phe Cys Gly Gly Thr Leu
580 585 590
Ile Ser Pro Glu Trp Val Leu Thr Ala Ala His Cys Leu Glu Lys Ser
595 600 605
Pro Arg Pro Ser Ser Tyr Lys Val Ile Leu Gly Ala His Gln Glu Val
610 615 620
Asn Leu Glu Pro His Val Gln Glu Ile Glu Val Ser Arg Leu Phe Leu
625 630 635 640
Glu Pro Thr Arg Lys Asp Ile Ala Leu Leu Lys Leu Ser Ser Pro Ala
645 650 655
Val Ile Thr Asp Lys Val Ile Pro Ala Cys Leu Pro Ser Pro Asn Tyr
660 665 670
Val Val Ala Asp Arg Thr Glu Cys Phe Ile Thr Gly Trp Gly Glu Thr
675 680 685
Gln Gly Thr Phe Gly Ala Gly Leu Leu Lys Glu Ala Gln Leu Pro Val
690 695 700
Ile Glu Asn Lys Val Cys Asn Arg Tyr Glu Phe Leu Asn Gly Arg Val
705 710 715 720
Gln Ser Thr Glu Leu Cys Ala Gly His Leu Ala Gly Gly Thr Asp Ser
725 730 735
Cys Gln Gly Asp Ser Gly Gly Pro Leu Val Cys Phe Glu Lys Asp Lys
740 745 750
Tyr Ile Leu Gln Gly Val Thr Ser Trp Gly Leu Gly Cys Ala Arg Pro
755 760 765
Asn Lys Pro Gly Val Tyr Val Arg Val Ser Arg Phe Val Thr Trp Ile
770 775 780
Glu Gly Val Met Arg Asn Asn
785 790
<210> 3
<211> 2433
<212> DNA
<213> 含有信号肽的天然纤溶酶原(来源于swiss prot)的核酸序列
<400> 3
atggaacata aggaagtggt tcttctactt cttttatttc tgaaatcagg tcaaggagag 60
cctctggatg actatgtgaa tacccagggg gcttcactgt tcagtgtcac taagaagcag 120
ctgggagcag gaagtataga agaatgtgca gcaaaatgtg aggaggacga agaattcacc 180
tgcagggcat tccaatatca cagtaaagag caacaatgtg tgataatggc tgaaaacagg 240
aagtcctcca taatcattag gatgagagat gtagttttat ttgaaaagaa agtgtatctc 300
tcagagtgca agactgggaa tggaaagaac tacagaggga cgatgtccaa aacaaaaaat 360
ggcatcacct gtcaaaaatg gagttccact tctccccaca gacctagatt ctcacctgct 420
acacacccct cagagggact ggaggagaac tactgcagga atccagacaa cgatccgcag 480
gggccctggt gctatactac tgatccagaa aagagatatg actactgcga cattcttgag 540
tgtgaagagg aatgtatgca ttgcagtgga gaaaactatg acggcaaaat ttccaagacc 600
atgtctggac tggaatgcca ggcctgggac tctcagagcc cacacgctca tggatacatt 660
ccttccaaat ttccaaacaa gaacctgaag aagaattact gtcgtaaccc cgatagggag 720
ctgcggcctt ggtgtttcac caccgacccc aacaagcgct gggaactttg tgacatcccc 780
cgctgcacaa cacctccacc atcttctggt cccacctacc agtgtctgaa gggaacaggt 840
gaaaactatc gcgggaatgt ggctgttacc gtgtccgggc acacctgtca gcactggagt 900
gcacagaccc ctcacacaca taacaggaca ccagaaaact tcccctgcaa aaatttggat 960
gaaaactact gccgcaatcc tgacggaaaa agggccccat ggtgccatac aaccaacagc 1020
caagtgcggt gggagtactg taagataccg tcctgtgact cctccccagt atccacggaa 1080
caattggctc ccacagcacc acctgagcta acccctgtgg tccaggactg ctaccatggt 1140
gatggacaga gctaccgagg cacatcctcc accaccacca caggaaagaa gtgtcagtct 1200
tggtcatcta tgacaccaca ccggcaccag aagaccccag aaaactaccc aaatgctggc 1260
ctgacaatga actactgcag gaatccagat gccgataaag gcccctggtg ttttaccaca 1320
gaccccagcg tcaggtggga gtactgcaac ctgaaaaaat gctcaggaac agaagcgagt 1380
gttgtagcac ctccgcctgt tgtcctgctt ccagatgtag agactccttc cgaagaagac 1440
tgtatgtttg ggaatgggaa aggataccga ggcaagaggg cgaccactgt tactgggacg 1500
ccatgccagg actgggctgc ccaggagccc catagacaca gcattttcac tccagagaca 1560
aatccacggg cgggtctgga aaaaaattac tgccgtaacc ctgatggtga tgtaggtggt 1620
ccctggtgct acacgacaaa tccaagaaaa ctttacgact actgtgatgt ccctcagtgt 1680
gcggcccctt catttgattg tgggaagcct caagtggagc cgaagaaatg tcctggaagg 1740
gttgtagggg ggtgtgtggc ccacccacat tcctggccct ggcaagtcag tcttagaaca 1800
aggtttggaa tgcacttctg tggaggcacc ttgatatccc cagagtgggt gttgactgct 1860
gcccactgct tggagaagtc cccaaggcct tcatcctaca aggtcatcct gggtgcacac 1920
caagaagtga atctcgaacc gcatgttcag gaaatagaag tgtctaggct gttcttggag 1980
cccacacgaa aagatattgc cttgctaaag ctaagcagtc ctgccgtcat cactgacaaa 2040
gtaatcccag cttgtctgcc atccccaaat tatgtggtcg ctgaccggac cgaatgtttc 2100
atcactggct ggggagaaac ccaaggtact tttggagctg gccttctcaa ggaagcccag 2160
ctccctgtga ttgagaataa agtgtgcaat cgctatgagt ttctgaatgg aagagtccaa 2220
tccaccgaac tctgtgctgg gcatttggcc ggaggcactg acagttgcca gggtgacagt 2280
ggaggtcctc tggtttgctt cgagaaggac aaatacattt tacaaggagt cacttcttgg 2340
ggtcttggct gtgcacgccc caataagcct ggtgtctatg ttcgtgtttc aaggtttgtt 2400
acttggattg agggagtgat gagaaataat taa 2433
<210> 4
<211> 810
<212> PRT
<213> 含有信号肽的天然纤溶酶原(来源于swiss prot)的氨基酸序列
<400> 4
Met Glu His Lys Glu Val Val Leu Leu Leu Leu Leu Phe Leu Lys Ser
1 5 10 15
Gly Gln Gly Glu Pro Leu Asp Asp Tyr Val Asn Thr Gln Gly Ala Ser
20 25 30
Leu Phe Ser Val Thr Lys Lys Gln Leu Gly Ala Gly Ser Ile Glu Glu
35 40 45
Cys Ala Ala Lys Cys Glu Glu Asp Glu Glu Phe Thr Cys Arg Ala Phe
50 55 60
Gln Tyr His Ser Lys Glu Gln Gln Cys Val Ile Met Ala Glu Asn Arg
65 70 75 80
Lys Ser Ser Ile Ile Ile Arg Met Arg Asp Val Val Leu Phe Glu Lys
85 90 95
Lys Val Tyr Leu Ser Glu Cys Lys Thr Gly Asn Gly Lys Asn Tyr Arg
100 105 110
Gly Thr Met Ser Lys Thr Lys Asn Gly Ile Thr Cys Gln Lys Trp Ser
115 120 125
Ser Thr Ser Pro His Arg Pro Arg Phe Ser Pro Ala Thr His Pro Ser
130 135 140
Glu Gly Leu Glu Glu Asn Tyr Cys Arg Asn Pro Asp Asn Asp Pro Gln
145 150 155 160
Gly Pro Trp Cys Tyr Thr Thr Asp Pro Glu Lys Arg Tyr Asp Tyr Cys
165 170 175
Asp Ile Leu Glu Cys Glu Glu Glu Cys Met His Cys Ser Gly Glu Asn
180 185 190
Tyr Asp Gly Lys Ile Ser Lys Thr Met Ser Gly Leu Glu Cys Gln Ala
195 200 205
Trp Asp Ser Gln Ser Pro His Ala His Gly Tyr Ile Pro Ser Lys Phe
210 215 220
Pro Asn Lys Asn Leu Lys Lys Asn Tyr Cys Arg Asn Pro Asp Arg Glu
225 230 235 240
Leu Arg Pro Trp Cys Phe Thr Thr Asp Pro Asn Lys Arg Trp Glu Leu
245 250 255
Cys Asp Ile Pro Arg Cys Thr Thr Pro Pro Pro Ser Ser Gly Pro Thr
260 265 270
Tyr Gln Cys Leu Lys Gly Thr Gly Glu Asn Tyr Arg Gly Asn Val Ala
275 280 285
Val Thr Val Ser Gly His Thr Cys Gln His Trp Ser Ala Gln Thr Pro
290 295 300
His Thr His Asn Arg Thr Pro Glu Asn Phe Pro Cys Lys Asn Leu Asp
305 310 315 320
Glu Asn Tyr Cys Arg Asn Pro Asp Gly Lys Arg Ala Pro Trp Cys His
325 330 335
Thr Thr Asn Ser Gln Val Arg Trp Glu Tyr Cys Lys Ile Pro Ser Cys
340 345 350
Asp Ser Ser Pro Val Ser Thr Glu Gln Leu Ala Pro Thr Ala Pro Pro
355 360 365
Glu Leu Thr Pro Val Val Gln Asp Cys Tyr His Gly Asp Gly Gln Ser
370 375 380
Tyr Arg Gly Thr Ser Ser Thr Thr Thr Thr Gly Lys Lys Cys Gln Ser
385 390 395 400
Trp Ser Ser Met Thr Pro His Arg His Gln Lys Thr Pro Glu Asn Tyr
405 410 415
Pro Asn Ala Gly Leu Thr Met Asn Tyr Cys Arg Asn Pro Asp Ala Asp
420 425 430
Lys Gly Pro Trp Cys Phe Thr Thr Asp Pro Ser Val Arg Trp Glu Tyr
435 440 445
Cys Asn Leu Lys Lys Cys Ser Gly Thr Glu Ala Ser Val Val Ala Pro
450 455 460
Pro Pro Val Val Leu Leu Pro Asp Val Glu Thr Pro Ser Glu Glu Asp
465 470 475 480
Cys Met Phe Gly Asn Gly Lys Gly Tyr Arg Gly Lys Arg Ala Thr Thr
485 490 495
Val Thr Gly Thr Pro Cys Gln Asp Trp Ala Ala Gln Glu Pro His Arg
500 505 510
His Ser Ile Phe Thr Pro Glu Thr Asn Pro Arg Ala Gly Leu Glu Lys
515 520 525
Asn Tyr Cys Arg Asn Pro Asp Gly Asp Val Gly Gly Pro Trp Cys Tyr
530 535 540
Thr Thr Asn Pro Arg Lys Leu Tyr Asp Tyr Cys Asp Val Pro Gln Cys
545 550 555 560
Ala Ala Pro Ser Phe Asp Cys Gly Lys Pro Gln Val Glu Pro Lys Lys
565 570 575
Cys Pro Gly Arg Val Val Gly Gly Cys Val Ala His Pro His Ser Trp
580 585 590
Pro Trp Gln Val Ser Leu Arg Thr Arg Phe Gly Met His Phe Cys Gly
595 600 605
Gly Thr Leu Ile Ser Pro Glu Trp Val Leu Thr Ala Ala His Cys Leu
610 615 620
Glu Lys Ser Pro Arg Pro Ser Ser Tyr Lys Val Ile Leu Gly Ala His
625 630 635 640
Gln Glu Val Asn Leu Glu Pro His Val Gln Glu Ile Glu Val Ser Arg
645 650 655
Leu Phe Leu Glu Pro Thr Arg Lys Asp Ile Ala Leu Leu Lys Leu Ser
660 665 670
Ser Pro Ala Val Ile Thr Asp Lys Val Ile Pro Ala Cys Leu Pro Ser
675 680 685
Pro Asn Tyr Val Val Ala Asp Arg Thr Glu Cys Phe Ile Thr Gly Trp
690 695 700
Gly Glu Thr Gln Gly Thr Phe Gly Ala Gly Leu Leu Lys Glu Ala Gln
705 710 715 720
Leu Pro Val Ile Glu Asn Lys Val Cys Asn Arg Tyr Glu Phe Leu Asn
725 730 735
Gly Arg Val Gln Ser Thr Glu Leu Cys Ala Gly His Leu Ala Gly Gly
740 745 750
Thr Asp Ser Cys Gln Gly Asp Ser Gly Gly Pro Leu Val Cys Phe Glu
755 760 765
Lys Asp Lys Tyr Ile Leu Gln Gly Val Thr Ser Trp Gly Leu Gly Cys
770 775 780
Ala Arg Pro Asn Lys Pro Gly Val Tyr Val Arg Val Ser Arg Phe Val
785 790 795 800
Thr Trp Ile Glu Gly Val Met Arg Asn Asn
805 810
<210> 5
<211> 2145
<212> DNA
<213> LYS77-PLG(Lys-纤溶酶原)核酸序列
<400> 5
aaagtgtatc tctcagagtg caagactggg aatggaaaga actacagagg gacgatgtcc 60
aaaacaaaaa atggcatcac ctgtcaaaaa tggagttcca cttctcccca cagacctaga 120
ttctcacctg ctacacaccc ctcagaggga ctggaggaga actactgcag gaatccagac 180
aacgatccgc aggggccctg gtgctatact actgatccag aaaagagata tgactactgc 240
gacattcttg agtgtgaaga ggaatgtatg cattgcagtg gagaaaacta tgacggcaaa 300
atttccaaga ccatgtctgg actggaatgc caggcctggg actctcagag cccacacgct 360
catggataca ttccttccaa atttccaaac aagaacctga agaagaatta ctgtcgtaac 420
cccgataggg agctgcggcc ttggtgtttc accaccgacc ccaacaagcg ctgggaactt 480
tgtgacatcc cccgctgcac aacacctcca ccatcttctg gtcccaccta ccagtgtctg 540
aagggaacag gtgaaaacta tcgcgggaat gtggctgtta ccgtgtccgg gcacacctgt 600
cagcactgga gtgcacagac ccctcacaca cataacagga caccagaaaa cttcccctgc 660
aaaaatttgg atgaaaacta ctgccgcaat cctgacggaa aaagggcccc atggtgccat 720
acaaccaaca gccaagtgcg gtgggagtac tgtaagatac cgtcctgtga ctcctcccca 780
gtatccacgg aacaattggc tcccacagca ccacctgagc taacccctgt ggtccaggac 840
tgctaccatg gtgatggaca gagctaccga ggcacatcct ccaccaccac cacaggaaag 900
aagtgtcagt cttggtcatc tatgacacca caccggcacc agaagacccc agaaaactac 960
ccaaatgctg gcctgacaat gaactactgc aggaatccag atgccgataa aggcccctgg 1020
tgttttacca cagaccccag cgtcaggtgg gagtactgca acctgaaaaa atgctcagga 1080
acagaagcga gtgttgtagc acctccgcct gttgtcctgc ttccagatgt agagactcct 1140
tccgaagaag actgtatgtt tgggaatggg aaaggatacc gaggcaagag ggcgaccact 1200
gttactggga cgccatgcca ggactgggct gcccaggagc cccatagaca cagcattttc 1260
actccagaga caaatccacg ggcgggtctg gaaaaaaatt actgccgtaa ccctgatggt 1320
gatgtaggtg gtccctggtg ctacacgaca aatccaagaa aactttacga ctactgtgat 1380
gtccctcagt gtgcggcccc ttcatttgat tgtgggaagc ctcaagtgga gccgaagaaa 1440
tgtcctggaa gggttgtagg ggggtgtgtg gcccacccac attcctggcc ctggcaagtc 1500
agtcttagaa caaggtttgg aatgcacttc tgtggaggca ccttgatatc cccagagtgg 1560
gtgttgactg ctgcccactg cttggagaag tccccaaggc cttcatccta caaggtcatc 1620
ctgggtgcac accaagaagt gaatctcgaa ccgcatgttc aggaaataga agtgtctagg 1680
ctgttcttgg agcccacacg aaaagatatt gccttgctaa agctaagcag tcctgccgtc 1740
atcactgaca aagtaatccc agcttgtctg ccatccccaa attatgtggt cgctgaccgg 1800
accgaatgtt tcatcactgg ctggggagaa acccaaggta cttttggagc tggccttctc 1860
aaggaagccc agctccctgt gattgagaat aaagtgtgca atcgctatga gtttctgaat 1920
ggaagagtcc aatccaccga actctgtgct gggcatttgg ccggaggcac tgacagttgc 1980
cagggtgaca gtggaggtcc tctggtttgc ttcgagaagg acaaatacat tttacaagga 2040
gtcacttctt ggggtcttgg ctgtgcacgc cccaataagc ctggtgtcta tgttcgtgtt 2100
tcaaggtttg ttacttggat tgagggagtg atgagaaata attaa 2145
<210> 6
<211> 714
<212> PRT
<213> LYS77-PLG(Lys-纤溶酶原)氨基酸序列
<400> 6
Lys Val Tyr Leu Ser Glu Cys Lys Thr Gly Asn Gly Lys Asn Tyr Arg
1 5 10 15
Gly Thr Met Ser Lys Thr Lys Asn Gly Ile Thr Cys Gln Lys Trp Ser
20 25 30
Ser Thr Ser Pro His Arg Pro Arg Phe Ser Pro Ala Thr His Pro Ser
35 40 45
Glu Gly Leu Glu Glu Asn Tyr Cys Arg Asn Pro Asp Asn Asp Pro Gln
50 55 60
Gly Pro Trp Cys Tyr Thr Thr Asp Pro Glu Lys Arg Tyr Asp Tyr Cys
65 70 75 80
Asp Ile Leu Glu Cys Glu Glu Glu Cys Met His Cys Ser Gly Glu Asn
85 90 95
Tyr Asp Gly Lys Ile Ser Lys Thr Met Ser Gly Leu Glu Cys Gln Ala
100 105 110
Trp Asp Ser Gln Ser Pro His Ala His Gly Tyr Ile Pro Ser Lys Phe
115 120 125
Pro Asn Lys Asn Leu Lys Lys Asn Tyr Cys Arg Asn Pro Asp Arg Glu
130 135 140
Leu Arg Pro Trp Cys Phe Thr Thr Asp Pro Asn Lys Arg Trp Glu Leu
145 150 155 160
Cys Asp Ile Pro Arg Cys Thr Thr Pro Pro Pro Ser Ser Gly Pro Thr
165 170 175
Tyr Gln Cys Leu Lys Gly Thr Gly Glu Asn Tyr Arg Gly Asn Val Ala
180 185 190
Val Thr Val Ser Gly His Thr Cys Gln His Trp Ser Ala Gln Thr Pro
195 200 205
His Thr His Asn Arg Thr Pro Glu Asn Phe Pro Cys Lys Asn Leu Asp
210 215 220
Glu Asn Tyr Cys Arg Asn Pro Asp Gly Lys Arg Ala Pro Trp Cys His
225 230 235 240
Thr Thr Asn Ser Gln Val Arg Trp Glu Tyr Cys Lys Ile Pro Ser Cys
245 250 255
Asp Ser Ser Pro Val Ser Thr Glu Gln Leu Ala Pro Thr Ala Pro Pro
260 265 270
Glu Leu Thr Pro Val Val Gln Asp Cys Tyr His Gly Asp Gly Gln Ser
275 280 285
Tyr Arg Gly Thr Ser Ser Thr Thr Thr Thr Gly Lys Lys Cys Gln Ser
290 295 300
Trp Ser Ser Met Thr Pro His Arg His Gln Lys Thr Pro Glu Asn Tyr
305 310 315 320
Pro Asn Ala Gly Leu Thr Met Asn Tyr Cys Arg Asn Pro Asp Ala Asp
325 330 335
Lys Gly Pro Trp Cys Phe Thr Thr Asp Pro Ser Val Arg Trp Glu Tyr
340 345 350
Cys Asn Leu Lys Lys Cys Ser Gly Thr Glu Ala Ser Val Val Ala Pro
355 360 365
Pro Pro Val Val Leu Leu Pro Asp Val Glu Thr Pro Ser Glu Glu Asp
370 375 380
Cys Met Phe Gly Asn Gly Lys Gly Tyr Arg Gly Lys Arg Ala Thr Thr
385 390 395 400
Val Thr Gly Thr Pro Cys Gln Asp Trp Ala Ala Gln Glu Pro His Arg
405 410 415
His Ser Ile Phe Thr Pro Glu Thr Asn Pro Arg Ala Gly Leu Glu Lys
420 425 430
Asn Tyr Cys Arg Asn Pro Asp Gly Asp Val Gly Gly Pro Trp Cys Tyr
435 440 445
Thr Thr Asn Pro Arg Lys Leu Tyr Asp Tyr Cys Asp Val Pro Gln Cys
450 455 460
Ala Ala Pro Ser Phe Asp Cys Gly Lys Pro Gln Val Glu Pro Lys Lys
465 470 475 480
Cys Pro Gly Arg Val Val Gly Gly Cys Val Ala His Pro His Ser Trp
485 490 495
Pro Trp Gln Val Ser Leu Arg Thr Arg Phe Gly Met His Phe Cys Gly
500 505 510
Gly Thr Leu Ile Ser Pro Glu Trp Val Leu Thr Ala Ala His Cys Leu
515 520 525
Glu Lys Ser Pro Arg Pro Ser Ser Tyr Lys Val Ile Leu Gly Ala His
530 535 540
Gln Glu Val Asn Leu Glu Pro His Val Gln Glu Ile Glu Val Ser Arg
545 550 555 560
Leu Phe Leu Glu Pro Thr Arg Lys Asp Ile Ala Leu Leu Lys Leu Ser
565 570 575
Ser Pro Ala Val Ile Thr Asp Lys Val Ile Pro Ala Cys Leu Pro Ser
580 585 590
Pro Asn Tyr Val Val Ala Asp Arg Thr Glu Cys Phe Ile Thr Gly Trp
595 600 605
Gly Glu Thr Gln Gly Thr Phe Gly Ala Gly Leu Leu Lys Glu Ala Gln
610 615 620
Leu Pro Val Ile Glu Asn Lys Val Cys Asn Arg Tyr Glu Phe Leu Asn
625 630 635 640
Gly Arg Val Gln Ser Thr Glu Leu Cys Ala Gly His Leu Ala Gly Gly
645 650 655
Thr Asp Ser Cys Gln Gly Asp Ser Gly Gly Pro Leu Val Cys Phe Glu
660 665 670
Lys Asp Lys Tyr Ile Leu Gln Gly Val Thr Ser Trp Gly Leu Gly Cys
675 680 685
Ala Arg Pro Asn Lys Pro Gly Val Tyr Val Arg Val Ser Arg Phe Val
690 695 700
Thr Trp Ile Glu Gly Val Met Arg Asn Asn
705 710
<210> 7
<211> 1245
<212> DNA
<213> delta-plg(delta-纤溶酶原)核酸序列
<400> 7
gagcctctgg atgactatgt gaatacccag ggggcttcac tgttcagtgt cactaagaag 60
cagctgggag caggaagtat agaagaatgt gcagcaaaat gtgaggagga cgaagaattc 120
acctgcaggg cattccaata tcacagtaaa gagcaacaat gtgtgataat ggctgaaaac 180
aggaagtcct ccataatcat taggatgaga gatgtagttt tatttgaaaa gaaagtgtat 240
ctctcagagt gcaagactgg gaatggaaag aactacagag ggacgatgtc caaaacaaaa 300
aatggcatca cctgtcaaaa atggagttcc acttctcccc acagacctag attctcacct 360
gctacacacc cctcagaggg actggaggag aactactgca ggaatccaga caacgatccg 420
caggggccct ggtgctatac tactgatcca gaaaagagat atgactactg cgacattctt 480
gagtgtgaag aggcggcccc ttcatttgat tgtgggaagc ctcaagtgga gccgaagaaa 540
tgtcctggaa gggttgtagg ggggtgtgtg gcccacccac attcctggcc ctggcaagtc 600
agtcttagaa caaggtttgg aatgcacttc tgtggaggca ccttgatatc cccagagtgg 660
gtgttgactg ctgcccactg cttggagaag tccccaaggc cttcatccta caaggtcatc 720
ctgggtgcac accaagaagt gaatctcgaa ccgcatgttc aggaaataga agtgtctagg 780
ctgttcttgg agcccacacg aaaagatatt gccttgctaa agctaagcag tcctgccgtc 840
atcactgaca aagtaatccc agcttgtctg ccatccccaa attatgtggt cgctgaccgg 900
accgaatgtt tcatcactgg ctggggagaa acccaaggta cttttggagc tggccttctc 960
aaggaagccc agctccctgt gattgagaat aaagtgtgca atcgctatga gtttctgaat 1020
ggaagagtcc aatccaccga actctgtgct gggcatttgg ccggaggcac tgacagttgc 1080
cagggtgaca gtggaggtcc tctggtttgc ttcgagaagg acaaatacat tttacaagga 1140
gtcacttctt ggggtcttgg ctgtgcacgc cccaataagc ctggtgtcta tgttcgtgtt 1200
tcaaggtttg ttacttggat tgagggagtg atgagaaata attaa 1245
<210> 8
<211> 414
<212> PRT
<213> delta-plg(delta-纤溶酶原)氨基酸序列
<400> 8
Glu Pro Leu Asp Asp Tyr Val Asn Thr Gln Gly Ala Ser Leu Phe Ser
1 5 10 15
Val Thr Lys Lys Gln Leu Gly Ala Gly Ser Ile Glu Glu Cys Ala Ala
20 25 30
Lys Cys Glu Glu Asp Glu Glu Phe Thr Cys Arg Ala Phe Gln Tyr His
35 40 45
Ser Lys Glu Gln Gln Cys Val Ile Met Ala Glu Asn Arg Lys Ser Ser
50 55 60
Ile Ile Ile Arg Met Arg Asp Val Val Leu Phe Glu Lys Lys Val Tyr
65 70 75 80
Leu Ser Glu Cys Lys Thr Gly Asn Gly Lys Asn Tyr Arg Gly Thr Met
85 90 95
Ser Lys Thr Lys Asn Gly Ile Thr Cys Gln Lys Trp Ser Ser Thr Ser
100 105 110
Pro His Arg Pro Arg Phe Ser Pro Ala Thr His Pro Ser Glu Gly Leu
115 120 125
Glu Glu Asn Tyr Cys Arg Asn Pro Asp Asn Asp Pro Gln Gly Pro Trp
130 135 140
Cys Tyr Thr Thr Asp Pro Glu Lys Arg Tyr Asp Tyr Cys Asp Ile Leu
145 150 155 160
Glu Cys Glu Glu Ala Ala Pro Ser Phe Asp Cys Gly Lys Pro Gln Val
165 170 175
Glu Pro Lys Lys Cys Pro Gly Arg Val Val Gly Gly Cys Val Ala His
180 185 190
Pro His Ser Trp Pro Trp Gln Val Ser Leu Arg Thr Arg Phe Gly Met
195 200 205
His Phe Cys Gly Gly Thr Leu Ile Ser Pro Glu Trp Val Leu Thr Ala
210 215 220
Ala His Cys Leu Glu Lys Ser Pro Arg Pro Ser Ser Tyr Lys Val Ile
225 230 235 240
Leu Gly Ala His Gln Glu Val Asn Leu Glu Pro His Val Gln Glu Ile
245 250 255
Glu Val Ser Arg Leu Phe Leu Glu Pro Thr Arg Lys Asp Ile Ala Leu
260 265 270
Leu Lys Leu Ser Ser Pro Ala Val Ile Thr Asp Lys Val Ile Pro Ala
275 280 285
Cys Leu Pro Ser Pro Asn Tyr Val Val Ala Asp Arg Thr Glu Cys Phe
290 295 300
Ile Thr Gly Trp Gly Glu Thr Gln Gly Thr Phe Gly Ala Gly Leu Leu
305 310 315 320
Lys Glu Ala Gln Leu Pro Val Ile Glu Asn Lys Val Cys Asn Arg Tyr
325 330 335
Glu Phe Leu Asn Gly Arg Val Gln Ser Thr Glu Leu Cys Ala Gly His
340 345 350
Leu Ala Gly Gly Thr Asp Ser Cys Gln Gly Asp Ser Gly Gly Pro Leu
355 360 365
Val Cys Phe Glu Lys Asp Lys Tyr Ile Leu Gln Gly Val Thr Ser Trp
370 375 380
Gly Leu Gly Cys Ala Arg Pro Asn Lys Pro Gly Val Tyr Val Arg Val
385 390 395 400
Ser Arg Phe Val Thr Trp Ile Glu Gly Val Met Arg Asn Asn
405 410
<210> 9
<211> 1104
<212> DNA
<213> Mini-plg(小纤维蛋白溶酶原)核酸序列
<400> 9
gtcaggtggg agtactgcaa cctgaaaaaa tgctcaggaa cagaagcgag tgttgtagca 60
cctccgcctg ttgtcctgct tccagatgta gagactcctt ccgaagaaga ctgtatgttt 120
gggaatggga aaggataccg aggcaagagg gcgaccactg ttactgggac gccatgccag 180
gactgggctg cccaggagcc ccatagacac agcattttca ctccagagac aaatccacgg 240
gcgggtctgg aaaaaaatta ctgccgtaac cctgatggtg atgtaggtgg tccctggtgc 300
tacacgacaa atccaagaaa actttacgac tactgtgatg tccctcagtg tgcggcccct 360
tcatttgatt gtgggaagcc tcaagtggag ccgaagaaat gtcctggaag ggttgtaggg 420
gggtgtgtgg cccacccaca ttcctggccc tggcaagtca gtcttagaac aaggtttgga 480
atgcacttct gtggaggcac cttgatatcc ccagagtggg tgttgactgc tgcccactgc 540
ttggagaagt ccccaaggcc ttcatcctac aaggtcatcc tgggtgcaca ccaagaagtg 600
aatctcgaac cgcatgttca ggaaatagaa gtgtctaggc tgttcttgga gcccacacga 660
aaagatattg ccttgctaaa gctaagcagt cctgccgtca tcactgacaa agtaatccca 720
gcttgtctgc catccccaaa ttatgtggtc gctgaccgga ccgaatgttt catcactggc 780
tggggagaaa cccaaggtac ttttggagct ggccttctca aggaagccca gctccctgtg 840
attgagaata aagtgtgcaa tcgctatgag tttctgaatg gaagagtcca atccaccgaa 900
ctctgtgctg ggcatttggc cggaggcact gacagttgcc agggtgacag tggaggtcct 960
ctggtttgct tcgagaagga caaatacatt ttacaaggag tcacttcttg gggtcttggc 1020
tgtgcacgcc ccaataagcc tggtgtctat gttcgtgttt caaggtttgt tacttggatt 1080
gagggagtga tgagaaataa ttaa 1104
<210> 10
<211> 367
<212> PRT
<213> Mini-plg(小纤维蛋白溶酶原)氨基酸序列
<400> 10
Val Arg Trp Glu Tyr Cys Asn Leu Lys Lys Cys Ser Gly Thr Glu Ala
1 5 10 15
Ser Val Val Ala Pro Pro Pro Val Val Leu Leu Pro Asp Val Glu Thr
20 25 30
Pro Ser Glu Glu Asp Cys Met Phe Gly Asn Gly Lys Gly Tyr Arg Gly
35 40 45
Lys Arg Ala Thr Thr Val Thr Gly Thr Pro Cys Gln Asp Trp Ala Ala
50 55 60
Gln Glu Pro His Arg His Ser Ile Phe Thr Pro Glu Thr Asn Pro Arg
65 70 75 80
Ala Gly Leu Glu Lys Asn Tyr Cys Arg Asn Pro Asp Gly Asp Val Gly
85 90 95
Gly Pro Trp Cys Tyr Thr Thr Asn Pro Arg Lys Leu Tyr Asp Tyr Cys
100 105 110
Asp Val Pro Gln Cys Ala Ala Pro Ser Phe Asp Cys Gly Lys Pro Gln
115 120 125
Val Glu Pro Lys Lys Cys Pro Gly Arg Val Val Gly Gly Cys Val Ala
130 135 140
His Pro His Ser Trp Pro Trp Gln Val Ser Leu Arg Thr Arg Phe Gly
145 150 155 160
Met His Phe Cys Gly Gly Thr Leu Ile Ser Pro Glu Trp Val Leu Thr
165 170 175
Ala Ala His Cys Leu Glu Lys Ser Pro Arg Pro Ser Ser Tyr Lys Val
180 185 190
Ile Leu Gly Ala His Gln Glu Val Asn Leu Glu Pro His Val Gln Glu
195 200 205
Ile Glu Val Ser Arg Leu Phe Leu Glu Pro Thr Arg Lys Asp Ile Ala
210 215 220
Leu Leu Lys Leu Ser Ser Pro Ala Val Ile Thr Asp Lys Val Ile Pro
225 230 235 240
Ala Cys Leu Pro Ser Pro Asn Tyr Val Val Ala Asp Arg Thr Glu Cys
245 250 255
Phe Ile Thr Gly Trp Gly Glu Thr Gln Gly Thr Phe Gly Ala Gly Leu
260 265 270
Leu Lys Glu Ala Gln Leu Pro Val Ile Glu Asn Lys Val Cys Asn Arg
275 280 285
Tyr Glu Phe Leu Asn Gly Arg Val Gln Ser Thr Glu Leu Cys Ala Gly
290 295 300
His Leu Ala Gly Gly Thr Asp Ser Cys Gln Gly Asp Ser Gly Gly Pro
305 310 315 320
Leu Val Cys Phe Glu Lys Asp Lys Tyr Ile Leu Gln Gly Val Thr Ser
325 330 335
Trp Gly Leu Gly Cys Ala Arg Pro Asn Lys Pro Gly Val Tyr Val Arg
340 345 350
Val Ser Arg Phe Val Thr Trp Ile Glu Gly Val Met Arg Asn Asn
355 360 365
<210> 11
<211> 750
<212> DNA
<213> Micro-plg(微纤维蛋白溶酶原)核酸序列
<400> 11
gccccttcat ttgattgtgg gaagcctcaa gtggagccga agaaatgtcc tggaagggtt 60
gtaggggggt gtgtggccca cccacattcc tggccctggc aagtcagtct tagaacaagg 120
tttggaatgc acttctgtgg aggcaccttg atatccccag agtgggtgtt gactgctgcc 180
cactgcttgg agaagtcccc aaggccttca tcctacaagg tcatcctggg tgcacaccaa 240
gaagtgaatc tcgaaccgca tgttcaggaa atagaagtgt ctaggctgtt cttggagccc 300
acacgaaaag atattgcctt gctaaagcta agcagtcctg ccgtcatcac tgacaaagta 360
atcccagctt gtctgccatc cccaaattat gtggtcgctg accggaccga atgtttcatc 420
actggctggg gagaaaccca aggtactttt ggagctggcc ttctcaagga agcccagctc 480
cctgtgattg agaataaagt gtgcaatcgc tatgagtttc tgaatggaag agtccaatcc 540
accgaactct gtgctgggca tttggccgga ggcactgaca gttgccaggg tgacagtgga 600
ggtcctctgg tttgcttcga gaaggacaaa tacattttac aaggagtcac ttcttggggt 660
cttggctgtg cacgccccaa taagcctggt gtctatgttc gtgtttcaag gtttgttact 720
tggattgagg gagtgatgag aaataattaa 750
<210> 12
<211> 249
<212> PRT
<213> Micro-plg(微纤维蛋白溶酶原)氨基酸序列
<400> 12
Ala Pro Ser Phe Asp Cys Gly Lys Pro Gln Val Glu Pro Lys Lys Cys
1 5 10 15
Pro Gly Arg Val Val Gly Gly Cys Val Ala His Pro His Ser Trp Pro
20 25 30
Trp Gln Val Ser Leu Arg Thr Arg Phe Gly Met His Phe Cys Gly Gly
35 40 45
Thr Leu Ile Ser Pro Glu Trp Val Leu Thr Ala Ala His Cys Leu Glu
50 55 60
Lys Ser Pro Arg Pro Ser Ser Tyr Lys Val Ile Leu Gly Ala His Gln
65 70 75 80
Glu Val Asn Leu Glu Pro His Val Gln Glu Ile Glu Val Ser Arg Leu
85 90 95
Phe Leu Glu Pro Thr Arg Lys Asp Ile Ala Leu Leu Lys Leu Ser Ser
100 105 110
Pro Ala Val Ile Thr Asp Lys Val Ile Pro Ala Cys Leu Pro Ser Pro
115 120 125
Asn Tyr Val Val Ala Asp Arg Thr Glu Cys Phe Ile Thr Gly Trp Gly
130 135 140
Glu Thr Gln Gly Thr Phe Gly Ala Gly Leu Leu Lys Glu Ala Gln Leu
145 150 155 160
Pro Val Ile Glu Asn Lys Val Cys Asn Arg Tyr Glu Phe Leu Asn Gly
165 170 175
Arg Val Gln Ser Thr Glu Leu Cys Ala Gly His Leu Ala Gly Gly Thr
180 185 190
Asp Ser Cys Gln Gly Asp Ser Gly Gly Pro Leu Val Cys Phe Glu Lys
195 200 205
Asp Lys Tyr Ile Leu Gln Gly Val Thr Ser Trp Gly Leu Gly Cys Ala
210 215 220
Arg Pro Asn Lys Pro Gly Val Tyr Val Arg Val Ser Arg Phe Val Thr
225 230 235 240
Trp Ile Glu Gly Val Met Arg Asn Asn
245
<210> 13
<211> 684
<212> DNA
<213> 丝氨酸蛋白酶(结构)域的核酸序列
<400> 13
gttgtagggg ggtgtgtggc ccacccacat tcctggccct ggcaagtcag tcttagaaca 60
aggtttggaa tgcacttctg tggaggcacc ttgatatccc cagagtgggt gttgactgct 120
gcccactgct tggagaagtc cccaaggcct tcatcctaca aggtcatcct gggtgcacac 180
caagaagtga atctcgaacc gcatgttcag gaaatagaag tgtctaggct gttcttggag 240
cccacacgaa aagatattgc cttgctaaag ctaagcagtc ctgccgtcat cactgacaaa 300
gtaatcccag cttgtctgcc atccccaaat tatgtggtcg ctgaccggac cgaatgtttc 360
atcactggct ggggagaaac ccaaggtact tttggagctg gccttctcaa ggaagcccag 420
ctccctgtga ttgagaataa agtgtgcaat cgctatgagt ttctgaatgg aagagtccaa 480
tccaccgaac tctgtgctgg gcatttggcc ggaggcactg acagttgcca gggtgacagt 540
ggaggtcctc tggtttgctt cgagaaggac aaatacattt tacaaggagt cacttcttgg 600
ggtcttggct gtgcacgccc caataagcct ggtgtctatg ttcgtgtttc aaggtttgtt 660
acttggattg agggagtgat gaga 684
<210> 14
<211> 228
<212> PRT
<213> 丝氨酸蛋白酶(结构)域的氨基酸序列
<400> 14
Val Val Gly Gly Cys Val Ala His Pro His Ser Trp Pro Trp Gln Val
1 5 10 15
Ser Leu Arg Thr Arg Phe Gly Met His Phe Cys Gly Gly Thr Leu Ile
20 25 30
Ser Pro Glu Trp Val Leu Thr Ala Ala His Cys Leu Glu Lys Ser Pro
35 40 45
Arg Pro Ser Ser Tyr Lys Val Ile Leu Gly Ala His Gln Glu Val Asn
50 55 60
Leu Glu Pro His Val Gln Glu Ile Glu Val Ser Arg Leu Phe Leu Glu
65 70 75 80
Pro Thr Arg Lys Asp Ile Ala Leu Leu Lys Leu Ser Ser Pro Ala Val
85 90 95
Ile Thr Asp Lys Val Ile Pro Ala Cys Leu Pro Ser Pro Asn Tyr Val
100 105 110
Val Ala Asp Arg Thr Glu Cys Phe Ile Thr Gly Trp Gly Glu Thr Gln
115 120 125
Gly Thr Phe Gly Ala Gly Leu Leu Lys Glu Ala Gln Leu Pro Val Ile
130 135 140
Glu Asn Lys Val Cys Asn Arg Tyr Glu Phe Leu Asn Gly Arg Val Gln
145 150 155 160
Ser Thr Glu Leu Cys Ala Gly His Leu Ala Gly Gly Thr Asp Ser Cys
165 170 175
Gln Gly Asp Ser Gly Gly Pro Leu Val Cys Phe Glu Lys Asp Lys Tyr
180 185 190
Ile Leu Gln Gly Val Thr Ser Trp Gly Leu Gly Cys Ala Arg Pro Asn
195 200 205
Lys Pro Gly Val Tyr Val Arg Val Ser Arg Phe Val Thr Trp Ile Glu
210 215 220
Gly Val Met Arg
225
- 还没有人留言评论。精彩留言会获得点赞!