一种可注射骨水泥及其制备方法与流程
本发明属于生物医用材料技术领域,尤其涉及一种可注射骨水泥及其制备方法。
背景技术:
可注射骨水泥由于特别适用于操作空间小或窄间隙的骨缺损修复而引起很大关注。目前用于可注射骨水泥的材料包括生物相容性较差的聚甲基丙烯酸甲酯(PMMA)骨水泥及具有良好生物相容性的磷酸钙(CPC)和磷酸镁基骨水泥(MPC)。
可生物降解性是骨水泥性能中的重要方面。PMMA骨水泥由于其不可降解,造成缺损部分难以完全修复;磷酸钙骨水泥的固化产物为类羟基磷灰石结构,仅产生有限的降解。
可注射性是衡量可注射骨水泥的重要指标。而磷酸钙骨水泥即使在很小的压力下也会发生压滤现象,表现出差的注射性。通常采用如下方法改善其注射性:改变颗粒尺寸及形状;增大骨水泥混合物的粘度;增大液固比;改善流变性和加入其他改善剂。通常增大固液比可以有效提高可注射性,如2008年刘昌胜等报道的磷酸钙-磷酸镁复合骨水泥,增大液固比极大地提高了注射性,但是使其力学强度下降,凝固时间延长。
技术实现要素:
针对现有技术中的上述问题,本发明的主要目的在于提供一种可注射骨水泥及其制备方法,所述骨水泥生物降解性优良,且具有在良好可注射性下较高的力学强度以及合适的固化时间的优点。
为了达到上述目的,本发明采用如下技术方案:一种可注射骨水泥,包括如下原料:微球及固化液,所述微球的成分包括50-60%重量百分比的氧化镁和30-40%重量百分比的Ca7Mg2P6O24;所述固化液选自磷酸二氢氨、磷酸二氢钠及磷酸二氢钾中的一种或其混合物的生理盐水或去离子水溶液;所述固化液和微球的固液比为1.2~2.0mL/g。
作为进一步的优选,所述固化液和微球的固液比为1.41~1.73mL/g。
作为进一步的优选,所述微球的直径为300-500μm。
作为进一步的优选,制备所述微球的原料包括:碱式碳酸镁和非晶磷酸三钙,所述碱式碳酸镁和非晶磷酸三钙的质量比3~5:1。
作为进一步的优选,制备所述微球的原料还包括::含硅元素、锌元素或锶元素的有机或无机物。
作为进一步的优选,制备所述微球的原料还包括:正硅酸四乙基酯、硝酸锌或硝酸锶。
作为进一步的优选,制备所述微球的方法包括:
(1)将无机粉末混匀后加入水混合均匀,再加入明胶混合均匀,得到浆料;
(2)将所述浆料滴加入搅拌的油中,所述明胶质量占无机粉末质量的20-40%,所述油的温度为-6~4℃,所述搅拌速度为200~350转/分;
(3)静置得到微球,除去油,固化;
(4)洗涤,干燥,得到无机明胶复合微球;
(5)将所述无机明胶复合微球于高温炉中烧结,所述烧结温度为1100-1200℃,烧结时间为1-3小时,得到微球;
所述无机粉末包括质量比3~5:1的碱式碳酸镁和非晶磷酸三钙。
作为进一步的优选,在步骤(1)中还可加入微球改性剂,所述微球改性剂质量占无机粉末质量的10-40%。
作为进一步的优选,所述的微球改性剂是水溶性高分子。
作为进一步的优选,所述的微球改性剂选自聚乙烯醇、聚丙烯酰胺、聚丙烯酸、聚乙烯吡咯烷酮、聚马来酸酐、聚季胺盐和聚乙二醇。
作为进一步的优选,步骤(2)中所述的油选自二甲基硅油、苯甲基硅油和橄榄油。
作为进一步的优选,步骤(2)中所述浆料在滴加时的温度为40~80℃。
作为进一步的优选,步骤(2)中,所述浆料在滴加时的温度为60-70℃,所述搅拌的速度为300-320转/分,所述搅拌的时间为2-4min。
作为进一步的优选,步骤(3)中,所述固化为加入戊二醛溶液固化,所述固化时间为2.5-3.5小时。
作为进一步的优选,所述无机粉末中还包括:含硅元素、锌元素或锶元素的有机或无机物。
作为进一步的优选,所述无机粉末中还包括:正硅酸四乙基酯、硝酸锌或硝酸锶。
一种可注射骨水泥的制备方法,所述制备方法包括:
将所述微球预先装入注射器;
将所述固化液加入装有所述微球的注射器中,混合约1~2min,注入模具或缺损部位,于37℃下,8-12min自然固化。
本发明的有益效果是:本发明利用氧化镁和固化液之间的快速反应实现骨水泥快速固化及良好填充,本发明使用主成分为氧化镁和Ca7Mg2P6O24的微球作为骨水泥的固相,相较以粉末或小颗粒为固相的传统骨水泥具有更好的可注射性及较短的固化时间,同时以微球形态固化的骨水泥能产生比粉末固化的骨水泥更大的间隙便于新生骨长入及营养输送;与传统磷酸钙骨水泥相比,本发明中的可注射骨水泥具有更优的生物降解性和促骨生成的性能,并且在满足良好可注射性的要求下不损害骨水泥的力学强度及固化时间,故在骨修复领域具有重要应用价值。
附图说明
图1为本发明实施例可注射骨水泥的制备方法流程示意图。
图2a-2d为本发明实施例1骨水泥的扫描电镜图片。
图2e-2f为本发明实施例1骨水泥的能谱线扫描结果示意图。
图2g为本发明实施例1骨水泥的XRD图片。
图3为本发明实施例骨水泥与CPC骨水泥的固化时间对比示意图。
图4为本发明实施例骨水泥与CPC骨水泥的力学强度的对比示意图。
图5为将本发明实施例骨水泥与CPC骨水泥分别注入大鼠颅骨模型缺损处的恢复效果对比图。
具体实施方式
本发明通过提供一种可注射骨水泥及其制备方法,解决了传统磷酸钙骨水泥生物降解性能差、良好可注射性下的力学强度较低以及固化时间过长等缺陷。
为了解决上述缺陷,本发明实施例的主要思路是:
本发明实施例可注射骨水泥,包括如下原料:微球及固化液,所述微球的成分包括50-60%重量百分比的氧化镁和30-40%重量百分比的Ca7Mg2P6O24;所述固化液选自磷酸二氢氨、磷酸二氢钠及磷酸二氢钾中的一种或其混合物的生理盐水或去离子水溶液;所述固化液和微球的固液比为1.3~2.0mL/g。
本发明实施例可注射骨水泥的制备方法,所述制备方法包括:
将所述微球预先装入注射器;
将所述固化液加入装有所述微球的注射器中,混合约1~2min,注入模具或缺损部位,于37℃下,8-12min自然固化。
本发明实施例骨水泥固化过程包括两个阶段:一是初混阶段,骨水泥微球与固化液在注射器中混合1-2min。此阶段微球表面的氧化镁与固化液成分发生反应,形成磷酸镁氨。推动注射器活塞的过程中,微球随着滚动,微球之间不能形成由磷酸镁氨构成的稳定结晶,故不会凝固。二是注射阶段,将混合好的微球连同固化液注入缺损部位,微球立即以最紧密堆积的方式填满缺损。此时微球之间的位置稳定,磷酸镁氨结晶立即在微球之间形成,达到初步固化,随后微球间的空隙也被磷酸镁氨充满,达到最终的固化,整个过程约8-12min完成。
本发明实施例骨水泥固化产物磷酸镁氨具有良好的生物降解性,本发明实施例使用主成分为氧化镁和Ca7Mg2P6O24的微球作为骨水泥的固相,降低了氧化镁的用量及占比浓度,进而克服了氧化镁由于碱性强而易损害周围骨组织的缺陷;而Ca7Mg2P6O24作为人体牙齿的组成成分,也同时存在于其他动物牙齿中,含有Ca7Mg2P6O24组分的羟基磷灰石支架亦被证明具有良好的生物相容性及一定的降解性。
本发明实施例骨水泥固化时间要短于传统磷酸钙骨水泥,整个固化过程约8-12min完成。
而本发明实施例微球可采用如下方法制备:
(1)将无机粉末混匀后加入水混合均匀,再加入明胶混合均匀,得到浆料;
(2)将所述浆料滴加入搅拌的油中,所述明胶质量占无机粉末质量的20-40%,所述油的温度为-6~4℃,所述搅拌速度为200~350转/分;
(3)静置得到微球,除去油,固化;
(4)洗涤,干燥,得到无机明胶复合微球;
(5)将所述无机明胶复合微球于高温炉中烧结,所述烧结温度为1100-1200℃,烧结时间为1-3小时,得到微球;
所述无机粉末包括碱式碳酸镁(又名四水碳酸镁)和非晶磷酸三钙(Amorphous Calcium Phosphate,简称ACP)。
本发明实施例微球制备方法采用明胶为微球模板,控制成球温度和球径,将无机粉末制成无机/明胶复合微球,烧结去除明胶,得到无机微球。明胶为有机成分,在成球过程中主要起到载体的作用。
在步骤(1)中还可加入微球改性剂,以改变无机微球的间隙度;微球改性剂加入后形成一有机相,占用一定的空间,当高温烧结掉所述有机相后,形成一定的空隙,以便后续微球应用时与其它物质更好的接触及反应,所述微球改性剂质量占无机粉末质量的10-40%。所述的微球改性剂选自聚乙烯醇、聚丙烯酰胺、聚丙烯酸、聚乙烯吡咯烷酮、聚马来酸酐、聚季胺盐或聚乙二醇等水溶性高分子。
步骤(2)中,所述浆料在滴加前,将所述浆料吸入注射器中再行滴加,为了进一步保证其温度的稳定性,可将注射器放入恒温装置,例如水浴中。所述浆料滴加温度和油温的控制可影响成球的效率,同时浆料的温度选择也应考虑对明胶硬度的影响。所述浆料在滴加时的温度为40~80℃。
步骤(2)中,所述搅拌的速度为300-320转/分。搅拌速度的调节可控制微球成球时的粒径。
所述制备方法还包括步骤(6):经过过筛,得到不同直径范围的无机微球。
所述制备方法保证得到的氧化镁和Ca7Mg2P6O24成分均匀混合,而且球的直径均一。
微球中添加微量的硅、锌等元素可以调节微球的抗水崩解性及改善微球骨水泥的生物相容性。其可在微球制备过程中在碱式碳酸镁和非晶磷酸三钙粉末中掺入上述元素。
为了让本发明之上述和其它目的、特征、和优点能更明显易懂,下文特举数实施例,来说明本发明所述之可注射骨水泥及其制备方法。
实施例1
本发明实施例1微球由下述方法制备:
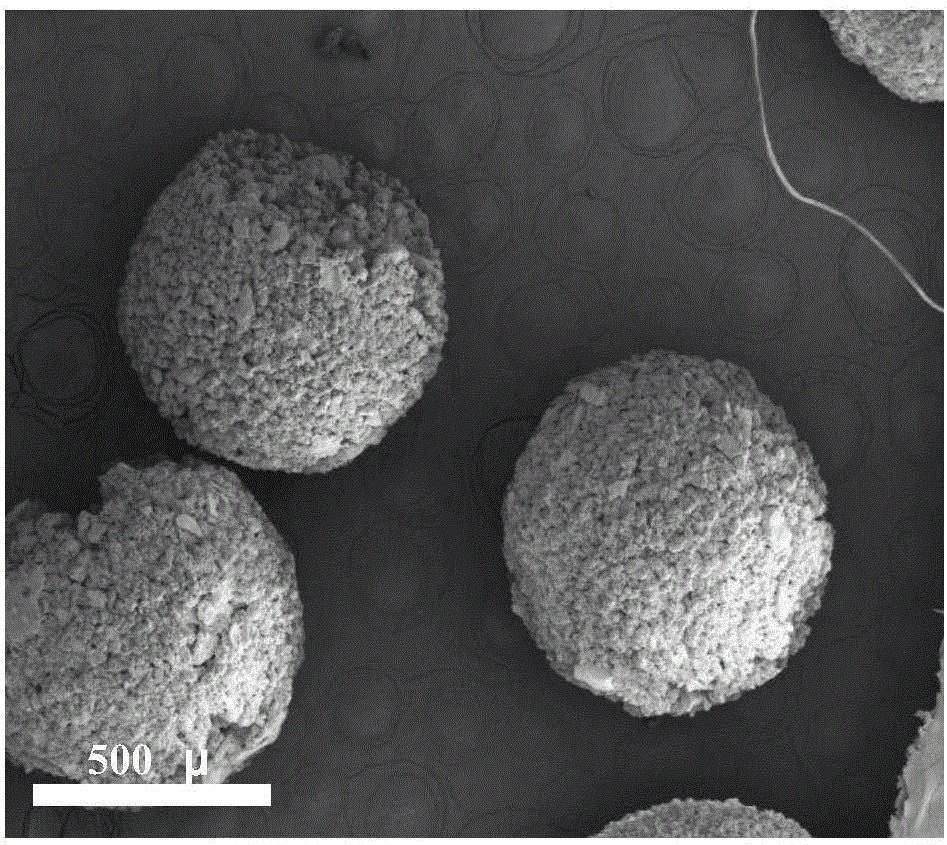
配制质量分数15%的明胶溶液;于500mL烧杯中加入250mL二甲基硅油置于-20℃冰箱中预冷;加装机械搅拌器。取5mL离心管,加入0.05g非晶磷酸钙及0.15g碱式碳酸镁,混合均匀,加入1024μL去离子水,搅拌均匀;加入226μL明胶溶液,搅拌均匀,于70℃水浴下吸入1mL注射器中,并将注射器放入70℃水浴中保温。将预冷二甲基硅油的烧杯取出,置于机械搅拌器下方,机械搅拌棒深入烧杯底部,使二甲基硅油温度升到-4℃,开启搅拌,转速300rpm。取出注射器,缓慢滴入二甲基硅油中,搅拌约3min,静置1h。移出二甲基硅油,用丙酮洗涤两遍,加入质量分数2.5%的戊二醛溶液,3h后,移出戊二醛溶液,无水乙醇洗涤两遍,将微球于60℃烘箱中烘干,即得到无机/明胶微球。将微球于高温炉中于1200℃烧结2h迅速取出冷至室温,即得到MgO/Ca7Mg2P6O24/Mg2SiO4微球。过筛,得到不同直径范围的微球。所述微球中成分包含50%重量百分比的氧化镁和40%重量百分比的Ca7Mg2P6O24。所述微球的直径为300-500μm。
取上述制备的0.1476g MgO/Ca7Mg2P6O24/Mg2SiO4(CaPMgSi)微球,装入1mL注射器中,加入含质量分数37%的磷酸二氢氨的水溶液208.1μL,反复推动注射器,使固液混合均匀,约2min后注入含有200微升PBS缓冲溶液(PH=7.4)的5mL离心管,置于37℃水浴下,12h后取样,用去离子水洗涤,真空干燥,扫描电镜表征。如图2所示。图2a-2d为骨水泥微球的扫描电镜图片,可以看出其表面及内部含有大量的微孔结构。图2b-2d为图2a中各部位的放大图。图2e为能谱线扫描结果,显示微球链接部分的元素组成为镁磷硅,而无钙元素。图2f的XRD表征说明,骨水泥固化后形成新的组分(磷酸镁氨),结合图2(e、f),说明本发明实施力可注射微球骨水泥的固化过程为微球形成的磷酸镁氨结晶的形成。
实施例2
本发明实施例2微球由下述方法制备:
配制质量分数15%的明胶溶液;于500mL烧杯中加入250mL橄榄油置于-20℃冰箱中预冷;加装机械搅拌器。取5mL离心管,加入0.04g含质量分数3.08%二氧化硅的非晶磷酸钙及0.16g碱式碳酸镁中,混合均匀,加入824μL去离子水,搅拌均匀;加入200μL聚丙烯酰胺溶液,搅拌均匀;加入226μL明胶溶液,搅拌均匀,于60℃水浴下吸入1mL注射器中,并将注射器放入60℃水浴中保温。将预冷橄榄油的烧杯取出,置于机械搅拌器下方,机械搅拌棒深入烧杯底部,使橄榄油温度升到-2℃,开启搅拌,转速320rpm。取出注射器,缓慢滴入橄榄油中,搅拌约3min,静置1h。移出橄榄油,用丙酮洗涤两遍,加入质量分数2.5%的戊二醛溶液,3h后,移出戊二醛溶液,无水乙醇洗涤两遍,将微球于60℃烘箱中烘干,即得到无机/明胶微球。将微球于高温炉中于1100℃烧结3h,迅速取出冷至室温,即得到MgO/Ca7Mg2P6O24/Mg2SiO4微球。过筛,得到不同直径范围的微球。所述微球中成分包含55%重量百分比的氧化镁和35%重量百分比的Ca7Mg2P6O24。所述微球的直径为300-500μm。
取上述制备的成分为MgO/Ca7Mg2P6O24/Mg2SiO4的骨水泥微球0.1476g,装入1mL注射器中,加入含质量分数37%的磷酸二氢钠的水溶液265.6μL,混合后注入圆柱形模具(内径6mm,高12mm),并置于37℃环境下,利用水泥稠度测定仪测其固化时间。每组测3个平行样。如图3所示,相比传统CPC骨水泥,本发明实施例骨水泥固化时间更短。
实施例3
本发明实施例3微球由下述方法制备:
配制质量分数15%的明胶溶液;于500mL烧杯中加入250mL苯甲基硅油置于-20℃冰箱中预冷;加装机械搅拌器。将0.035g非晶磷酸钙及0.165g碱式碳酸镁混合均匀,加入210.5μL离子水,搅拌均匀;搅拌均匀;加入169.5μL明胶溶液,搅拌均匀,于50℃水浴下吸入1mL注射器中,并将注射器放入50℃水浴中保温。将预冷苯甲基硅油的烧杯取出,置于机械搅拌器下方,机械搅拌棒深入烧杯底部,使苯甲基硅油温度升到2℃,开启搅拌,转速350rpm。取出注射器,缓慢滴入苯甲基硅油中,搅拌约3min,静置1h。移出苯甲基硅油,用丙酮洗涤两遍,加入质量分数2.5%的戊二醛溶液,3h后,移出戊二醛溶液,无水乙醇洗涤两遍,将微球于60℃烘箱中烘干,即得到无机/明胶微球。将微球于高温炉中于1200℃烧结1h,于高温炉冷至室温,即得到MgO/Ca7Mg2P6O24/Mg2SiO4微球。过筛,得到不同直径范围的微球。所述微球中成分包含58%重量百分比的氧化镁和35%重量百分比的Ca7Mg2P6O24。所述微球的直径为300-500μm。
取上述制备的成分为MgO/Ca7Mg2P6O24/Mg2SiO4的骨水泥微球0.1476g,装入1mL注射器中,加入含质量分数37%的磷酸二氢氨的水溶液255.6μL(液固比1.73mL/g),混合后注入圆柱形模具(内径6mm,高12mm),待其固化后,脱模,并置于37℃,林氏溶液(0.15M氯化钠溶液)中,1h、1d后用万能力学测定仪测其压缩强度(测试速度1mm/min),每组测3个平行样。如图4所示,本发明实施例可注射微球骨水泥在固化1h内,力学强度要远大于传统CPC骨水泥(**p<0.01),且随固化时间增加,力学强度无明显变化。
实施例4
本发明实施例4微球由下述方法制备:
配制质量分数15%的明胶溶液;于500mL烧杯中加入250mL苯甲基硅油置于-20℃冰箱中预冷;加装机械搅拌器。取5mL离心管,加入0.044g非晶磷酸钙及0.155g碱式碳酸镁、0.001g正硅酸四乙基酯,混合均匀,加入874μL去离子水,搅拌均匀;加入150μL聚乙烯醇溶液(含0.02g聚乙烯醇),搅拌均匀;加入226μL明胶溶液,搅拌均匀,于80℃水浴下吸入1mL注射器中,并将注射器放入80℃水浴中保温。将预冷二甲基硅油的烧杯取出,置于机械搅拌器下方,机械搅拌棒深入烧杯底部,使二甲基硅油温度升到4℃,开启搅拌,转速300rpm。取出注射器,缓慢滴入二甲基硅油中,搅拌约3min,静置1h。移出二甲基硅油,用丙酮洗涤两遍,加入质量分数2.5%的戊二醛溶液,3h后,移出戊二醛溶液,无水乙醇洗涤两遍,将微球于60℃烘箱中烘干,即得到非晶磷酸钙/明胶微球。将微球于高温炉中于1100℃烧结1h,迅速取出冷至室温,即得到微球。过筛,得到不同直径范围的微球。所述微球中成分包含55%重量百分比的氧化镁和40%重量百分比的Ca7Mg2P6O24。所述微球的直径为300-500μm。
实施例5
本发明实施例5微球由下述方法制备:
配制质量分数15%的明胶溶液;于500mL烧杯中加入250mL橄榄油置于-20℃冰箱中预冷;加装机械搅拌器。取5mL离心管,加入0.043g非晶磷酸钙及0.155g碱式碳酸镁、0.002g硝酸锌,混合均匀,加入824μL去离子水,搅拌均匀;加入200μL聚马来酸酐溶液,搅拌均匀;加入226μL明胶溶液,搅拌均匀,于60℃水浴下吸入1mL注射器中,并将注射器放入60℃水浴中保温。将预冷橄榄油的烧杯取出,置于机械搅拌器下方,机械搅拌棒深入烧杯底部,使橄榄油温度升到-6℃,开启搅拌,转速220rpm。取出注射器,缓慢滴入橄榄油中,搅拌约3min,静置1h。移出橄榄油,用丙酮洗涤两遍,加入质量分数2.5%的戊二醛溶液,3h后,移出戊二醛溶液,无水乙醇洗涤两遍,将微球于60℃烘箱中烘干,即得到非晶磷酸钙/明胶微球。将微球于高温炉中于1200℃烧结60min,迅速取出冷至室温,即得到微球。过筛,得到不同直径范围的微球。所述微球中成分包含52%重量百分比的氧化镁和40%重量百分比的Ca7Mg2P6O24。所述微球的直径为300-500μm。
实施例6
本发明实施例6微球由下述方法制备:
配制质量分数15%的明胶溶液;于500mL烧杯中加入250mL苯甲基硅油置于-20℃冰箱中预冷;加装机械搅拌器。加入0.05g非晶磷酸钙及0.148g碱式碳酸镁(CAS:39409-82-0)、0.002g硝酸锶,混合均匀,加入267μL离子水,搅拌均匀;加入113μL明胶溶液,搅拌均匀,于50℃水浴下吸入1mL注射器中,并将注射器放入50℃水浴中保温。将预冷苯甲基硅油的烧杯取出,置于机械搅拌器下方,机械搅拌棒深入烧杯底部,使苯甲基硅油温度升到1℃,开启搅拌,转速300rpm。取出注射器,缓慢滴入苯甲基硅油中,搅拌约3min,静置1h。移出苯甲基硅油,用丙酮洗涤两遍,加入质量分数2.5%的戊二醛溶液,3h后,移出戊二醛溶液,无水乙醇洗涤两遍,将微球于60℃烘箱中烘干,即得到无机/明胶微球。将微球于高温炉中于1100℃烧结2h,于高温炉冷至室温,即得到微球。过筛,得到不同直径范围的微球。所述微球中成分包含50%重量百分比的氧化镁和40%重量百分比的Ca7Mg2P6O24。所述微球的直径为300-500μm。
将实施例1-6中制备的微球用于制备可注射骨水泥,所述制备方法包括:
将所述微球预先装入注射器;
将所述固化液加入装有所述微球的注射器中,混合约1~2min,注入模具或缺损部位,于37℃下,8-12min自然固化。
取4个月大的SD大鼠,做直径5mm的颅骨缺损,将上述混合后的骨水泥填充入缺损处,待其凝固,缝合皮肤。4W后,microCT检测颅骨修复效果。对照组用传统磷酸钙骨水泥(CPC)。结果如图5所示,植入本发明实施例可注射微球骨水泥的骨缺损区,材料很好的填充骨缺损,且新生骨明显生成。另外骨缺损边缘,微球形状不能保持,而缺损中央可见明显微球形状,说明微球可以在体内逐步降解,且微球在骨缺损边缘降解速度要高于中间部分。图5中,Top指颅骨顶部,Bottom指颅骨下部。
上述本申请实施例中的技术方案,至少具有如下的技术效果或优点:
本发明利用氧化镁和固化液之间的快速反应实现骨水泥快速固化及良好填充,本发明使用主成分为氧化镁和Ca7Mg2P6O24的微球作为骨水泥的固相,相较以粉末或小颗粒为固相的传统骨水泥具有更好的可注射性及较短的固化时间,同时以微球形态固化的骨水泥能产生比粉末固化的骨水泥更大的间隙便于新生骨长入及营养输送;与传统磷酸钙骨水泥相比,本发明中的可注射骨水泥具有更优的生物降解性和促骨生成的性能,并且在满足良好可注射性的要求下不损害骨水泥的力学强度及固化时间,故在骨修复领域具有重要应用价值。
尽管已描述了本发明的优选实施例,但本领域内的技术人员一旦得知了基本创造性概念,则可对这些实施例作出另外的变更和修改。所以,所附权利要求意欲解释为包括优选实施例以及落入本发明范围的所有变更和修改。显然,本领域的技术人员可以对本发明进行各种改动和变型而不脱离本发明的精神和范围。这样,倘若本发明的这些修改和变型属于本发明权利要求及其等同技术的范围之内,则本发明也意图包含这些改动和变型在内。
- 还没有人留言评论。精彩留言会获得点赞!