在CNS神经性损伤后非‑急性期间处理的组合物及方法与流程
本申请是申请日为2009年8月17日、申请号为200980136712.3的同名申请的分案申请。【
技术领域:
】发明领域涉及治疗中枢神经系统神经损伤。更特别是,本发明针对在创伤性神经损伤后非-急性或慢性期间给受试者施用神经调节蛋白[例如,神经胶质生长因子2(ggf2)]。
背景技术:
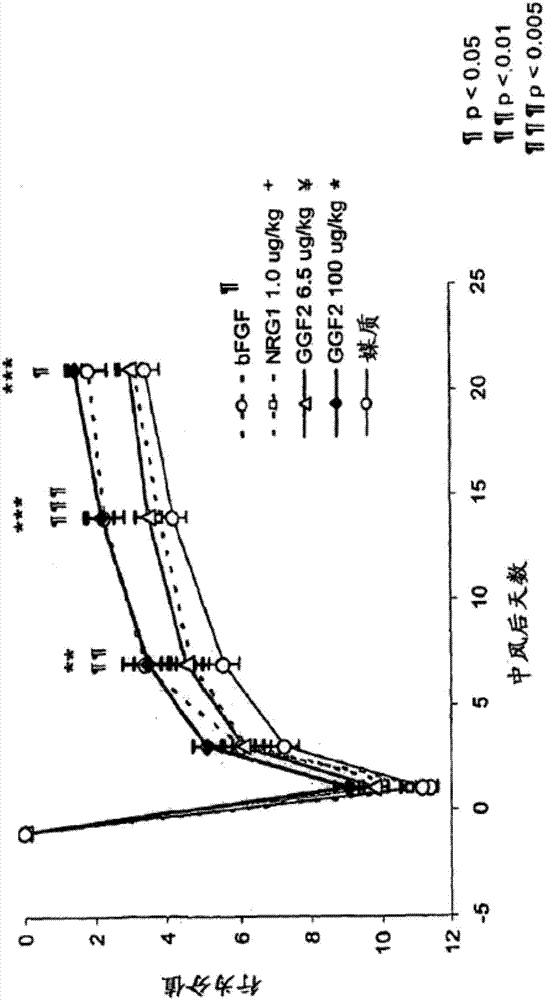
:中枢神经系统(cns)损伤是严重的健康问题。此类别的损伤包括事件,例如缺血性损伤,出血性损伤,穿透性创伤及非-穿透性创伤。cns损伤通常不完全痊愈,留给受试者变动于极其弱到死亡的一些程度的永久的功能障碍。残留的功能障碍可包括:运动,感觉,认知,情绪及自主异常。关键类别的cns神经损伤包括脑损伤。脑损伤是导致一些程度的永久的残疾包括运动,感觉及认知缺乏及情绪不稳定性(例如创伤后应激障碍,注意力缺乏病症,抑郁症及情绪不稳定性)的破坏性病情。脑损伤的常见原因包括:缺血性中风,出血性中风,硬膜下血肿,硬膜上血肿,闭合性头损伤(加速/减速,脑震荡及旋转),穿透性脑损伤(枪伤及其他投射物伤)。中风是死亡的第三-主导原因,及是西方世界中残疾的主要原因。因此,中风造成大的社会经济学负担。中风的病因学可为缺血性中风(其为大部分中风的情形)或出血性中风。缺血性中风可由在体内别处形成凝块及经血流行进到脑导致(栓塞性中风),或由脑动脉内侧形成的血凝块导致(血栓性中风)。在由于缺失葡萄糖及氧而立即梗塞核心内大量细胞死亡后,由于第二机理(例如谷氨酸盐兴奋性中毒,凋亡性机理,及自由基产生),梗塞区扩展数天。神经损伤后(例如缺血性事件)动物及人可经几天,几周及几个月不用任何治疗剂而恢复功能。但是,时常,此恢复仅为部分,及动物及人患有可包括运动,感觉及认知缺乏的永久的残疾。熟知增加个体患中风的可能性的危险因素。这些包括,及不限于,不可变化的危险因素:老年,遗传,ace,性别,中风或心脏病的之前历史;及可变化,治疗或控制的危险因素:高血压,吸烟,糖尿病,颈动脉或其他动脉疾病,心房颤动,其他心脏病,镰形细胞病,高血胆甾醇,差的摄食,及身体不活动及肥胖症。至今,缺血性中风的非-减轻性治疗限于在中风后急性期施用治疗剂。急性期跨神经损伤(例如,中风)的起始时间到神经损伤后大致6小时。急性期之后是半-急性期,其跨神经损伤后大致6小时~2天。因此,使用当前非-减轻性治疗剂力图反转血流阻塞,恢复脑的氧合作用及限制丧失脑结构的程度。不同于用于急性使用的tpa,无用于治疗中风的药物获得批准。患者保留一些水平的功能障碍,其最佳可多少内源性地改善大致60天。此恢复可仅通过物理治疗增加。不幸的是,许多患者被留下有少的改善希望的永久的残疾。目前,被食品和药物管理局(fda)批准的用于治疗缺血性中风的药物仅有组织纤溶酶原活化子(tpa)。tpa是将纤溶酶原转变为纤溶酶的丝氨酸蛋白酶。纤溶酶然后断裂纤维蛋白,其是阻塞脑中血管及导致中风的凝块的成分。其在理想情况下在自症状起始的3小时内施用。一般而言,认为仅3%~5%的患中风的个体及时达到医院得到此治疗。理想情况下,阻塞后头3小时内施用tpa,但可在晚至阻塞后6小时由一些临床医师施用。不幸的是,对于此治疗认为绝大部分经历中风的患者未及时达到医院。对于那些在有效的时间窗内到达医院的患者,tpa施用力图反转血流阻塞,恢复脑的氧合作用及限制丧失脑结构的程度。但是,有一些限制tpa持续使用的显著的禁忌症。在约3~6小时的初始时期后,至多,tpa可导致脑内出血及出血性中风。由于所述理由,tpa限于急性期期间施用,以便实现任何治疗性功效。至今无其他用于治疗中风的治疗已获得批准。其他实验治疗(例如动脉递送的促尿激酶)处于研究中作为用于破裂凝块及恢复血流的潜在手段。但是,科学文献已描述许多被证明对于保护脑质有益及在中风实验动物模型中恢复功能的试剂。全部这些试剂致力于降低急性细胞死亡,发炎,及凋亡及因此,必需在缺血性事件后几小时内(一些达24小时)递送。迄今,都知道急切需要cns损伤(例如中风)的治疗手段。(abe等人,2008年,jcerebbloodflowmetab.7月23日,电子公开首页,sun等人,2008年,stroke,7月10日,电子公开首页(页码还不可用);dohare等人,2008年,behavbrainres.193(2):289~97;belayev等人,2001年,stroke,32(2):553~60)。但是,所述试剂尚未显示当在几小时的滞后时间后,至多在一些实验动物模型中约在中风后一天时施用时限制中风后对脑的损伤,恢复功能或增强恢复。仅知的对于中风后显示功效数天及数周的治疗是减轻性或康复性的,例如职业性或物理治疗。的确,本发明人未发现任何已显示在中风后增强恢复数天或数周的试剂或药物。急性阻塞后,常有毁坏的脑质的局限区,其被半影区域围绕,其如果不恢复循环,将在数小时内死。此半影区域的至死亡的时间可用神经保护剂(例如nmda拮抗剂,钙通道阻断剂,自由基清除剂及捕获剂,抗-凋亡剂,胱天蛋白酶抑制剂,parp抑制剂,等)在实验模型中延长几小时。为此目的,“神经保护剂”可在它们死于在急性期呈于它们的各种损伤之前解救神经元。24~48小时后,但是,有少的希望从坏死性死亡及凋亡性死亡保护细胞持续几天(见图1,用于抗-凋亡性治疗的治疗性窗未证明相比急性保护治疗宽得多[schulzetal.,1998,celldeathdiffer.5(10):847-57;komjatietal.,2004,intjmolmed.13(3):373-82]。神经调节蛋白呈现神经保护性质,如上述其他试剂,其显示降低中风后数小时内递送到动物见到的残疾的益处。见美国申请系列号09/530,884,将其整个内容通过引用并入本文。从神经损伤的发病率来看,特别关于中风,有可有效施用给受试者以限制神经损伤后对脑的损伤,恢复功能和/或增强恢复的治疗剂的需求。神经调节蛋白(nrg)及nrg受体包括用于涉及神经,肌肉,上皮,及其他组织中器官发生的细胞间信号转导的生长因子-受体酪氨酸激酶系统(lemke,mol.cell.neurosci.7:247-262,1996andburdenetal.,neuron18:847-855,1997)。nrg家族由编码多种含表皮生长因子(egf)-样,免疫球蛋白(ig),及其他可识别结构域的配体的4种基因构成。多种分泌的及膜-附接的异构体发挥此信号转导系统中配体的作用。nrg配体的受体是egf受体(egfr)家族的全部成员,及包括egfr(或erbb1),erbb2,erbb3,及erbb4,在人中也分别被称为her1~her4(meyeretal.,development124:3575-3586,1997;orr-urtregeretal.,proc.natl.acad.sci.usa90:1867-71,1993;marchionnietal.,nature362:312-8,1993;chenetal.,j.comp.neurol.349:389-400,1994;corfasetal.,neuron14:103-115,1995;meyeretal.,proc.natl.acad.sci.usa91:1064-1068,1994;andpinkas-kramarskietal.,oncogene15:2803-2815,1997)。4种nrg基因,nrg-1,nrg-2,nrg-3,及nrg-4,定位于不同的染色体座位(pinkas-kramarskietal.,proc.natl.acad.sci.usa91:9387-91,1994;carrawayetal.,nature387:512-516,1997;changetal.,nature387:509-511,1997;andzhangetal.,proc.natl.acad.sci.usa94:9562-9567,1997),及共同编码多种nrg蛋白。nrg-1的基因产物,例如,包括一组大致15种不同的结构上-相关的异构体(lemke,mol.cell.neurosci.7:247-262,1996andpelesandyarden,bioessays15:815-824,1993)。首先鉴定的nrg-1的亚型包括neu分化因子(ndf;pelesetal.,cell69,205-216,1992andwenetal.,cell69,559-572,1992),神经生长因子(hrg;holmesetal.,science256:1205-1210,1992),乙酰胆碱受体诱导活性(aria;fallsetal.,cell72:801-815,1993),及神经胶质生长因子ggf1,ggf2,及ggf3(marchionnietal.nature362:312-8,1993)。nrg-2基因通过同源性克隆(changetal.,nature387:509-512,1997;carrawayetal.,nature387:512-516,1997;andhigashiyamaetal.,j.biochem.122:675-680,1997)及通过基因组方法(busfieldetal.,mol.cell.biol.17:4007-4014,1997)鉴定。nrg-2cdna也已知为erbb激酶(ntak;genbank登录号no.ab005060)的神经-及胸腺-来源的活化子,神经调节蛋白(don-1)的趋异剂,及小脑-来源的生长因子(cdgf;pct申请wo97/09425)。实验证据显示,表达erbb4或erbb2/erbb4组合的细胞可能显示对nrg-2的特别稳健的应答(pinkas-kramarskietal.,mol.cell.biol.18:6090-6101,1998)。nrg-3基因产物(zhang等人,supra)也已知结合及活化erbb4受体(hijazietal.,int.j.oncol.13:1061-1067,1998)。egf-样结构域以全部形式的nrg的核心存在,及需要结合及活化erbb受体。3种基因中编码的egf-样结构域的推断的氨基酸序列大致30~40%相同(比对)。而且,nrg-1及nrg-2中似乎有至少2种亚型的egf-样结构域,其可赋予不同的生物活性及组织-特异性潜力。对nrg的细胞应答通过表皮生长因子受体家族的nrg受体酪氨酸激酶egfr,erbb2,erbb3,及erbb4介导。全部nrg的高-亲和力结合主要经erbb3或erbb4介导。nrg配体的结合导致与其他erbb亚基的二聚化,及通过对特异性酪氨酸残基的磷酸化的反式激活。在某些实验环境中,erbb受体的几乎全部组合似乎能响应nrg-1异构体的结合形成二聚体。但是,看起来erbb2是可在稳定配体-受体复合物中起重要的作用的优选的二聚化偶体。erbb2不结合其自身的配体,但必需与其他受体亚型之一异源配对。erbb3不具有酪氨酸激酶活性,但是其他受体的磷酸化的靶。nrg-1,erbb2,及erbb4的表达已知必要于小鼠发育期间心室心肌小梁形成。【发明概述】本发明提供用于治疗哺乳动物神经损伤后的新方法。方法基于可通过给哺乳动物施用治疗有效量的多肽来实现含表皮生长因子-样(egf-样)结构域的多肽的治疗性益处的观察;在某些实施方式中,在神经损伤后第1小时,第2小时,第8小时,第12小时,第24小时,第30小时,第36小时、第42小时,第2天或更久时或后进行治疗。在本发明的一个实施方式中在急性窗损伤后之后起始治疗。在本发明的一个实施方式中在半-急性窗损伤后之后起始治疗。在本发明的一个实施方式中期间及仍持续在急性窗损伤后之后起始治疗。在本发明的一个实施方式中治疗在半-急性窗损伤后期间起始及在半-急性窗损伤后之后仍持续。因此,本发明包括给哺乳动物施用含egf-样结构域的多肽(或编码多肽的核酸),其在神经损伤后第1,2或3天甚至达及包括第4,5,6,7,8,9,10,11,12,13,14天;在神经损伤后一周或多于一周,2周或多于2周;在神经损伤后3周或多于3周;在神经损伤后4周或多于4周;在神经损伤后1个月或多于一个月;在神经损伤后2个月或多于2个月;在神经损伤后3个月或多于3个月;在神经损伤后4个月或多于4个月;在神经损伤后5个月或多于5个月;在神经损伤后6个月或多于6个月起始。根据本发明,egf-样结构域由神经调节蛋白基因编码。根据本发明的施用包括以对于治疗哺乳动物的神经损伤后慢性期有效的量施用包括egf-样结构域的肽,或编码所述多肽的核酸分子。根据本发明的另一方面,提供哺乳动物缺血性事件后急性或半-急性期外期间促进神经恢复的方法。本发明的治疗可在急性或半-急性时期内开始,但包括超过急性或半-急性时期分别至少1次,2次,3次,4次,5次,6次或多于6次治疗。本发明的方法包括给所述哺乳动物施用包括表皮生长因子-样(egf-样)结构域的多肽,其中所述egf-样结构域由神经调节蛋白(nrg)-1基因编码,及所述施用在缺血性事件后进行至少2或3或4天,尽管治疗可在急性或半急性时间框架内开始,及以足以在所述哺乳动物缺血性事件后慢性期期间促进神经恢复的有效量治疗。在本发明的特定实施方式中,神经调节蛋白基因可为nrg-1基因,nrg-2基因,nrg-3基因或nrg-4基因。本发明的神经调节蛋白多肽可,进而,由这4种神经调节蛋白基因任之一编码;本发明的神经调节蛋白多肽可,进而,由这4种神经调节蛋白基因任之一的变体或同系物编码。见图6a~6d是全长人ggf2(nrg-1的亚型)的氨基酸及核酸序列。在本发明的一个方面,适宜哺乳动物包括但不限于,小鼠,大鼠,兔,狗,猴或猪。在本发明的更特定的实施方式中,哺乳动物是人。【定义】本文中的术语‘约”包括指定的值±1,2,3,4,5,6,7,8,9,10,11,12,13,14,15%的指定的值。在一实施方式中“约”表示98~102%的指定的值。在一实施方式中“约”表示95~105%的指定的值。损伤后,“急性期”跨神经损伤(例如,中风)起始时间到神经损伤后大致6小时。急性期之后是“半-急性期”,其跨神经损伤后大致6小时~2天。在一实施方式中,“半-急性期”跨神经损伤后大致6小时~3天。半-急性期之后时期称为神经损伤后“慢性期”。后-急性期包括半-急性及慢性损伤后时期。通过"表皮生长因子-样结构域"或"egf-样结构域"是指结合及活化erbb2,erbb3,erbb4,或其组合,及与如公开于holmes等人,science256:1205~1210,1992年;美国专利no.5,530,109;美国专利no.5,716,930;美国专利no.7,037,888;hijazi等人,int.j.oncol.13:1061~1067,1998年;chang等人,nature387:509~512,1997年;carraway等人,nature387:512~516,1997年;higashiyama等人,jbiochem.122:675~680,1997年;及wo97/09425)的egf受体-结合结构域带有结构相似性的由nrg-1,nrg-2,或nrg-3基因编码的多肽基序。对于对应于由nrg-1基因编码的egfl结构域1~6的核酸及氨基酸序列见图7~12。"表达载体"是指源于,例如,噬菌体,腺病毒,反转录病毒,痘病毒,疱疹病毒,或人工染色体的,用于转移,运作性连接到启动子的多肽(例如,神经调节蛋白)编码序列到宿主细胞,以至于编码的肽或多肽在宿主细胞内表达的遗传加工的质粒或病毒。术语“神经损伤”及“损伤”常在本文中互换使用。“神经创伤”是“神经损伤”的一实施方式及可通常认为是同义词。“神经损伤”是导致神经组织的一些破坏或死亡的损伤。神经损伤通常作为后遗症具有一些损失,例如,心理,感觉或肌肉功能减少。“神经保护剂”可在它们死于在急性或半-急性损伤后期呈于它们的各种损伤之前解救神经元。急性阻塞后,常有被半影区域围绕的毁坏的脑质的局限区,所述半影区如果不恢复循环将在数小时内死。此半影区域至死亡的时间可用“神经保护剂”(例如nmda拮抗剂,钙通道阻断剂,自由基清除剂及捕获剂,抗-凋亡剂,胱天蛋白酶抑制剂,parp抑制剂,等),在实验模型中延长几小时。为此目的“神经保护剂”可在它们死于在急性期呈于它们的各种损伤之前解救神经元。"神经调节蛋白"或"nrg"是指由nrg-1,nrg-2,nrg-3或nrg-4基因或核酸(例如,cdna)编码,及结合及活化egfr,erbb1,erbb2,erbb3,或erbb4受体,或其组合的多肽。"神经调节蛋白-1”,"nrg-1”,"神经生长因子”,"ggf2”,或"p185erbb2配体"是指结合erbb2受体及由描述于美国专利no.5,530,109;美国专利no.5,716,930;及美国专利no.7,037,888(将各均通过引用整体并入本文)的p185erbb2配体基因编码的多肽。结合到erbb2受体可为通过erbb2受体与erbb1,erbb3或erbb4的异源配对的间接结合。"神经调节蛋白-样多肽"是指具有由神经调节蛋白基因编码的egf-样结构域,以及结合及活化egfr,erbb1,erbb-2,erbb-3,erbb-4,或它们的组合的多肽。结合到erbb2受体可为通过erbb2受体与erbb1,erbb3或erbb4的异源配对的间接结合。本文中的术语“神经恢复”用于指在损伤,疾病,感染或其他神经系统分裂后,脑,脊髓或外周神经的神经系统向正常状态恢复其功能的过程。"运作性连接的"是指编码多肽(例如,cdna)与一或多个调控序列的核酸以当适当的分子(例如,转录活化子蛋白)结合到调控序列时使基因表达的方式连接。本文所用的“肽”包括约625,600,575,550,525,500,475,450,425,400,375,350,325,300,275,250,225,200,175,150,125,100,75,50或少于50个氨基酸,或者基本上由其构成或由其构成的肽。"启动子"是指足以指导转录的最小的序列。本发明也包括足以致使启动子-依赖性基因表达基于细胞类型或生理状态(例如,含氧量低的对比含氧量正常的条件)可控制的,或可被外部信号或试剂诱导的启动子元件;所述元件可位于天然的基因的5'或3'或内部区中。术语"治疗有效量"旨在表示引起由研究者,兽医,医学医生或其他临床医师观察的组织,系统,动物或人的生物或医学应答的药物或药学试剂的量。治疗性变化是以期望减轻疾病或解决病情的方向所测的生物化学特征性中的变化。更具体而言,"治疗有效量"是足以降低与医学病情或虚弱相关的症状,以标准化导致特异性身体功能损伤的疾病或病症中的身体功能,或提供改善in一或多种临床上所测的疾病参数的量。本文中的术语“治疗”指神经损伤后获得至无损伤的恢复;加速神经损伤后自然恢复的速度;或促进恢复到更高功能水平。不被理论束缚,在慢性损伤后窗中,其未含盖将有能力减少任何进一步神经性死亡,即,已知在慢性窗发生时神经死亡。但是,本发明的治疗包括,在慢性时期期间,例如,减少组织(例如,肌肉或骨)的将由包括的神经提供的组织中别样发生的降低功能或活力。此外,本发明的治疗包括,在慢性时期期间,例如,减少由包括的神经提供的组织中别样发生的萎缩(例如,肌肉或骨)。通过"转化的细胞"是指已利用重组dna技术或已知的基因治疗技术导入编码神经调节蛋白或具有神经调节蛋白egf-样结构域的多肽的dna分子的细胞(或细胞后代)。除非另有定义,本文所用的全部技术及科学术语具有与被本发明所属领域的普通技术人员通常理解的相同含义。【附图说明】图1显示中风/缺血后进行期的示意图。图中“ot”表示职业疗法及“pt”表示物理治疗。图2示中脑动脉的永久的结扎后的前肢行为分值。将大鼠如所示用ggf2,nrg1,fgf,或媒质处理。以100μg/kg的fgf及ggf2在第21天行为测试中展示显著的改善。(+,¥,*表示通过anova及后-tukey显著不同于媒质(对于bfgf,nrg1,ggf2以6.5μg/kg,及对于ggf2以100μg/kg))。图3示中脑动脉的永久的结扎后的后肢行为分值。将大鼠如所示用ggf2,nrg1,fgf,或媒质处理。ggf2以6.5μg/kg及nrg以1.0μg/kg,在第7天及第14天行为测试,但不在第21天的研究终点显著好于媒质。ggf2以100μg/kg及fgf在处理后全部行为时间点显著好于媒质。(+,¥,*表示通过anova及后-tukey显著不同于媒质(对于bfgf,nrg1,ggf2以6.5μg/kg及对于ggf2以100μg/kg))。图4示中脑动脉永久的结扎后的身体摆动行为分值。将大鼠如所示用ggf2,nrg1,fgf,或媒质处理。ggf2以100μg/kg及fgf在第21天相比媒质显著改善。(+,¥,*表示通过重复的测量anova及后-hoctukey显著不同于媒质(对于bfgf,nrg1,ggf2以6.5μg/kg及对于ggf2以100μg/kg))。图5a显示中脑动脉的永久的结扎后前肢行为分值。将大鼠在结扎后起始1,3或7天用ggf2处理。将ggf2每天以0.1mg/kg静脉内递送10天。用全部处理范例在第21天时间点前肢行为分值显著好于媒质。(*,¥,+表示通过重复的测量anova及后-hoctukey,分别在第1,3及7天处理组显著不同于媒质)。图5b显示中脑动脉的永久的结扎后的后肢行为分值。将大鼠在结扎后起始1,3或7天用ggf2处理。将ggf2每天静脉内以0.1mg/kg递送10天。当在结扎后1或7天起始治疗时后肢行为分值显著好于媒质,及相比在第21天时间点结扎后3天起始治疗的媒质改善。(*,¥,+表示通过重复的测量anova及后-hoctukey,分别在第1,3及7天处理组显著不同于媒质)。图5c显示中脑动脉永久的结扎后的身体摆动行为分值。将大鼠在结扎后起始1,3或7天用ggf2处理。将ggf2每天静脉内以0.1mg/kg递送10天。当结扎后1天起始治疗时身体摆动分值显著好于媒质,及相比结扎后3或7天起始治疗的媒质改善。(*,¥,+表示通过重复的测量anova及后-hoctukey,分别在第1,3及7天处理组显著不同于媒质)。图6a~d显示全长ggf2的核酸及氨基酸序列。图7~12显示表皮生长因子样(egfl)结构域1~6的核酸及氨基酸序列。图13显示来自nrg-1基因的表皮生长因子样肽的核酸及氨基酸序列。图14显示来自nrg-1的表皮生长因子样(egfl)β片段的核酸及氨基酸序列。图15显示来自nrg-1的表皮生长因子样(egfl)α片段的核酸及氨基酸序列。图16显示来自nrg-2α的表皮生长因子样(egfl)α片段的核酸及氨基酸序列。图17显示来自nrg-2β的表皮生长因子样(egfl)α片段的核酸及氨基酸序列。图18显示各egf-样肽的氨基酸序列比对。egf-样结构域可定义为nrg的亚结构域,序列比对显示,其与人egf分子(序列p01133|971~1023,在图中比对底部)相比,在氨基酸序列上具有至少25,26,27,28,29,30,31,32,33,34,35,36,37,38,39,40,41,42,43,44或45%同源性。同源氨基酸具有相同的,保守的或半-保守的物理-化学及结构性质,如分别通过符号‘*’,‘:’及‘.’标识。图19显示转染cho(dhfr-)细胞的表达载体(psv-ahsg)。图20显示含人ggf2的编码序列的pcmggf2载体。图21显示为增强转录,将ggf2编码序列放置在ebvbmlf-1干扰序列(mis)后。【发明详述】如所示本文中,缺血性中风的非-减轻性治疗迄今限于在中风后急性期施用治疗剂。急性期期间观察到至少部分由于氧剥夺的立即细胞死亡。此外,如图1中所示,血流阻塞导致细胞内贮存的自由基,谷氨酸盐,及钙及钠释放,这被理解为毁坏脑组织及扩展损伤区。神经损伤后大致6小时~2天(或通过一些定义是3天)的半-急性期的特征在于持续的自由基释放,谷氨酸盐清除,钙及钠释放,阻塞的区的氧剥夺,及立即局限的细胞死亡。至今,无已知的用于人中风后半-急性期期间的临床上获得批准的试剂。如图1中所示,药学神经损伤后治疗的有限的窗至少部分被病理生理学及暂时的损伤进展解释。例如阻塞的数分钟内,在梗塞核心的神经元毁坏。阻塞后数小时时,自由基,兴奋毒性及炎症试剂释放/产生,及这些分子持续毁坏脑组织及扩展损伤区。如上所述,损伤的程度可有限,通过恢复血流(使用临床上获得批准的溶栓剂,即,tpa)从而达到疫区的再-氧合作用。如通过科学文献所示,各化合物似乎在急性及半-急性时期呈现功效。但是,cns神经损伤后24,36或48小时标记后,潜在治疗进行性丧失治疗损伤的能力。实际上,在急性时期具有效应的一些治疗剂模式,例如tpa,随着损伤后时间经过开始具有严重的,威胁生命的禁忌症。缺血性事件后数天,数周或数个月,在中风后慢性期期间,治疗必需旨在促进神经恢复。创伤性事件(例如中枢神经系统中的中风)后神经恢复的促进相比前-慢性窗中所采用的涉及明显不同的生理学现象及治疗性策略。前-慢性治疗通常涉及旨在恢复血流及减少急性细胞死亡的试剂。相反,可在损伤后48小时或更久,或72小时或更久时有效施用的治疗剂通过其不改变缺血性损伤大小而恢复功能的能力从急性期治疗剂分化出。在一实施方式中,本发明的治疗在缺血性cns损伤的基本上完全损伤后死亡后开始;“缺血性cns损伤的基本上完全损伤后死亡”是指直接导致缺血性事件的cns细胞死亡将发生,其他由于年龄或治疗(无关治疗是否设计用于解决缺血)的细胞死亡不在此定义的范围内。如所示本文中,本发明人展示,神经调节蛋白对在神经创伤性损伤的慢性期期间恢复神经性功能有效。在一实施方式中,神经创伤性损伤是缺血性中风。如本文所述,本发明人作出惊人的发现,神经调节蛋白在缺血性事件后慢性期期间起始施剂时有效。甚至更惊人的是发现神经调节蛋白甚至当晚至在缺血性事件后7天时起始施剂时有效。本数据显示,达到的有利的结果不通过与发现在立即缺血后治疗中有效的机理相同的机理发生。中风后慢性期期间的神经调节蛋白处理不改变缺血性损伤的大小(见表1)。此明显显示,病理生理学的急性及半-急性期完全在这些期,及慢性期期间施用的神经调节蛋白促进神经恢复,而非建立再灌注及保护神经元。表1:梗塞体积(%)bfgf21.3±3.3nrg1.0μg/kg26.8±3.0ggf26.5μg/kg27.1±3.7ggf2100μg/kg26.3±3.5媒质25.0±3.5【本发明的组合物】如上所述,神经调节蛋白是由nrg-1,nrg-2,nrg-3或nrg-4基因编码的多肽及具有使它们结合及活化erbb受体的egf-样结构域。holmes等人(science256:1205~1210,1992)显示,egf-样结构域单独足以结合及活化p185erbb2受体。因此,由nrg-1,nrg-2,nrg-3或nrg-4基因编码的任何多肽产物,或任何神经调节蛋白-样多肽,例如,具有由神经调节蛋白基因或cdna编码的egf-样结构域(例如,含nrg-1肽亚结构域c-c/d或c-c/d'的egf-样结构域,如uspn5,530,109,uspn5,716,930,及uspn7,037,888中所述;或如公开于wo97/09425的egf-样结构域)的多肽可用于本发明的方法。本发明的组合物可为单元剂型。包括本发明的组合物和/或根据本发明的使用说明的试剂盒也在本发明的范围内。可将本发明的组合物与药学-可接受的稀释剂,载质,或赋形剂一同施用于的患者。采用常规药学实践提供制剂或组合物以将所述组合物施用给患者或实验动物。尽管静脉内施用是优选的,可采用任何适当的施用途径,例如,肠胃外,皮下,肌内,颅内,眶内,眼,心室内,囊内,脊柱内,脑池内,腹膜内,鼻内,气雾剂,口服,或经皮(例如,通过施加带制剂的粘合贴剂能交叉真皮及进入血流)或局部施用。治疗性制剂可取液体溶液或悬浮液形式;对于口服施用,制剂可取片剂或胶囊形式;及对于鼻内制剂,以粉末,鼻滴液,或气雾剂的形式。本领域中熟知的用于制备制剂的方法见于,例如,"remington'spharmaceuticalsciences”。用于肠胃外施用的制剂可,例如,含赋形剂,无菌水,或盐水,聚烯基甘醇(例如聚乙二醇),蔬菜来源的油,或氢化萘。用于施用本发明的分子的其他潜在地有用的肠胃外递送系统包括乙烯-乙酸乙烯酯共聚物粒子,渗透泵,可植入的输注系统,及脂质体。用于吸入的制剂可含赋形剂,例如,乳糖,或可为含,例如,聚氧乙烯-9-月桂醚,甘胆酸盐及脱氧胆酸盐的水溶液,或可为用于以鼻滴液的形式施用的油性溶液,或作为凝胶。本发明的其他方面提供了将本化合物用作尤其是治疗或预防前述病情及疾病的药物。本文也提供本化合物在制备用于治疗或预防前述病情及疾病之一的药物中的用途。关于静脉内注射,剂量水平通常在从以下列表中的一个值到列表中的更高值的范围内:约0.001mg/kg,约0.01mg/kg,约0.1mg/kg,约1mg/kg,及约10mg/kg。施剂周期性通常在从约每24,48,72,或96小时的规则的时间间隔内。在替代性实施方式中,施剂周期性通常在从约每1,2,3,4,5,6,7,数天的规则的时间间隔内。在替代性实施方式中,施剂周期性通常在从约每1,2,3,4,或5周的规则的时间间隔内。所述施剂时期后,可采用欠频繁的施剂,例如每月,每3个月,每4个月,或每年。选择经皮剂量来提供相比使用注射剂量实现的基本上相同的,类似或更低生理学水平(血浆,组织,csf)。可将本发明的化合物作为单独的活性剂施用,或它们可与其他试剂(包括可发现展示相同的或类似治疗性活性及测定为对于所述组合的施用安全的及有效的其他化合物)组合施用。含盖的用于治疗急性或半-急性神经损伤的其他所述化合物包括造血因子(例如,g-csf和/或gm-csf);具有溶血栓活性的物质,例如,tpa,链激酶,尿激酶,和/或安克洛酶;抗血小板剂,例如乙酰水杨酸(阿司匹林),氯吡格雷(plavix),与缓释双嘧达莫(aggrenox)组合的阿司匹林;抗凝剂,例如杀鼠灵(coumadin)或肝素;和/或干扰凋亡性信号转导的物质(例如胱天蛋白酶抑制剂)或孕酮。但是,已知以预防中风发展的目的(例如,用于抗血小板剂或抗凝剂),或在中风后急性期期间(tpa)施用以上化合物。为了评估根据本发明有效治疗的运动,感觉或认知缺乏,本领域中可用几种工具。熟知的监控治疗功效的标志包括:细微精神状态检查(mmse),改良的细微精神状态检查(3ms),功能损伤测量(fim,barthel测试,fugl-meyer运动分值,wolf运动功能测试,jebsen-taylor手功能测试,nottingham健康特征部分1及运动评定标尺(mas),运动评估标尺(smes),berg平衡标尺(bbs)及日常生活barthel活性(adl),及其他临床测试,例如影响,语言,吞咽,认知,运动协调,强度,感觉及自主功能测量,以及存活率及住院率可用于评定疾病进展。损伤后,疾病,感染或其他神经系统分裂,脑,脊髓或外周神经由于任何的组合总破坏,凋亡,分裂的通路及突触,发炎,改变的化学环境,细胞代谢变化及细胞转录及翻译变化而不恰当地起作用。本文中的术语“神经恢复”用于指神经系统向正常状态恢复其功能的过程。此过程可通过修正,防止,反转或消除以上提及的任何原因来发生。此外,目前已知显著的神经恢复可通过称为‘可塑性’的处理发生,其中神经系统形成新联系以补偿或适应于其他变化。cns损伤导致造成分裂的功能及残疾的局部及长-范围联系的分裂。可塑性是既有的神经元之间形成新联系的事件。可塑性已显示是包括视觉系统(pizzorusso等人)及脊髓(fawcettjw(2009)brain132:1417-1418)的cns系统中的神经恢复机理。在可塑性中,新突触形成或既有的突触加强,减弱或去除,以使既有的结构及系统补偿已在损伤中毁坏或分裂的那些。其他形式的可塑性可包括改变既有的细胞的神经化学,以变化直接突触信号转导及旁分泌信号转导。可塑性也可取改变受体水平的形式,以使神经元及其他细胞更或欠敏感于直接的突触或旁分泌信号转导。这些过程良好被接受为学习及记忆的机理。文献,行为,材料,装置,物品等的讨论包括在此说明书中仅旨在提供本发明的背景。不推荐或代表,任何或全部这些东西形成部分现有技术基础或是本申请的各权利要求的优先权日之前本发明领域相关中的公知常识。本发明已联系其特定实施方式描述,需知,能进一步改良及本申请,一般而言,旨在覆盖遵循本发明的原理的本发明的任何变化,使用,或适应,及包括在本发明所属领域中已知的或习惯的实践内从本公开内容脱离,及可将应用于前述必要的特征,及落入随附的权利要求的范围。以下实施例将辅助本领域技术人员更佳了解本发明及其原理及优点。期望这些实施例为阐明本发明及不限制其范围。【实施例】【实施例1:材料及方法】【动物准备】将50只,成年,雄性sprague-dawley用于研究(定购10只额外的动物)。全部大鼠笼养及进行用于以适应环境目的在手术之前7天行为评定的操作。操作时期末,大鼠随机化及分配到不同的组。大鼠通过尾标记给予唯一的识别号。10只额外的大鼠也操作。【手术准备】【中脑动脉阻塞(mcao),tamura模型】此大鼠手术损伤模型是本领域中良好接受的中风模型(tamuraetal,1981,jcerebbloodflowmetab.1(1):53-60;tamuraetal,1981,jcerebbloodflowmetab.1(1):61-9)。通过使用tamura等人方法的改良方法的近端右中脑动脉(mca)永久的阻塞来制备病灶脑梗塞。用在n2o:o2(2:1)的混合物中的2~3%氟烷麻醉雄性sprague-dawley大鼠(在手术时300~400g),及用在n2o:o2(2:1)的混合物中的1~1.5%氟烷维持。两断颞肌,及通过在眼及耳道之间中位切开来呈现。通过颞下颅骨切除术不去除髋弓及不横断面神经地暴露近端mca。然后通过从刚好接近嗅觉通路到大脑下静脉的显微双极性凝固阻塞动脉,及横断。贯穿整个过程于37.5℃±0.5℃体温维持。在mcao前一天及mcao刚后腹膜内(i.p.)给予头孢唑林(40mg/kg;baxter,lot06014.1,exp。1月2009年),以阻止感染。在mcao手术之前作为镇痛剂皮下(0.05~0.1mg/kg)给予丁丙诺啡(ndc12496-0757-1,lot#700y02,exp:1月1日2010年)。【化合物制备及施剂】【ggf2及nrg-1(nrg-egf)】在acordatherapeutics制备浓储物溶液及保存于0~5℃。如下述制成剂量:【nrg-1[nrg1b2egf结构域(156q)]的克隆,表达及纯化】dna:从人脑cdna克隆nrg1b2egf结构域及使用nde1及bamh1限制性位点克隆进pet15b载体(novagencat#69661~3)。得到的蛋白是6.92kda+~3kdahis标签(=9.35kda)。【nrg1b2egfpet15克隆的dna序列】有下划线的序列是克隆位点(nde1及bamh1)从pet15b载体最终翻译的蛋白示于下。egf结构域加了下划线。理论pi/mw:7.69/9349.58【蛋白表达】使用过夜表达自动诱导系统(novagen)在lb培养基中于25℃将克隆转化进用于蛋白表达的bl21细胞24小时。表达主要在不溶性包含体中。蛋白再折叠:从novagen蛋白再折叠试剂盒改造,70123-3。蛋白纯化:将蛋白以2.5ml/分钟装在阴离子交换柱deae。nrg-1片段仍在流通中,然而混入物结合及以更高盐洗脱。装载及洗涤缓冲液是50mmtrisph7.9,及洗脱缓冲液是含1mnacl的50mmtrisph7.9。将流通液合并,及用来自millipore的centriprepym-3浓缩。蛋白印迹:通过蛋白印迹评定蛋白表达。得到的条带以约10kd运行。将4~20%标准凝胶(biorad)用于蛋白解析,然后转移到protran硝酸纤维素纸(来自schliecher及schull的0.1μm孔径)。印迹在tbs-t(0.1%)中的5%乳中封闭。在tbs-t中的5%乳中的1:1000稀释的第一抗体(来自r&d系统的抗egf人nrg1-α/hrg1-α亲和力纯化的多克隆抗体cat#af-296-na)-于室温1小时(也于4℃工作过夜)。以tbs-t中的5%乳中的1:10,000稀释液使用兔抗山羊hrp第二抗体,于室温1小时。全部在tbs-t中进行洗涤。【nrg-1的纯化流程】将培养物于25℃在来自novagen的过夜表达自动诱导系统1(cat#71300-4)中生长。有非常少的可溶性nrg-1存在。将培养物离心沉降及将沉淀提取,溶解及在纯化可发生之前再折叠以获取nrg-1。【用于提取,增溶及再折叠的物质】10×洗涤缓冲液:200mmtris-hcl,ph7.5,100mmedta,10%tritonx-10010×增溶缓冲液:500mmcaps,ph11.050×透析缓冲液:1mtris-hcl,ph8.530%n-月桂基肌氨酸-作为粉末添加(sigma61739-5g)1mdtt还原的谷胱甘肽(novagen3541)氧化的谷胱甘肽(novagen3542)【a.细胞裂解及包含体的制备】-解冻及在30ml1×洗涤缓冲液中重悬浮细胞沉淀。根据需要,为完全重悬浮而混合。-将蛋白酶抑制剂(25μl的10×/50ml),dna酶(200μl的1mg/ml/50ml)及mgcl2(500μl的1m/50ml)添加到悬浮液。-通过超声处理裂解细胞。a.贯穿此步骤在冰上冷却细胞。b.使用方形端,以6,10次水平超声处理30秒钟,直到悬浮液粘性减小。各超声处理之间使悬浮液在冰上冷却60秒钟。当超声处理时,保持50ml圆锥形管内的体积不高于40ml。-当完成时,将各悬浮液转移到用于以f-16/250转子使用的250ml曲颈离心瓶。-通过以10000×g离心12分钟来收集包含体。-去除上清(留下用于可溶性蛋白分析的样品)及在30ml的1×洗涤缓冲液中充分重悬浮沉淀。-如在步骤4中重复离心及留下沉淀。-再次,在30ml的1×洗涤缓冲液中充分重悬浮沉淀。-通过以10000×g离心10分钟来收集包含体。倒出上清及通过在纸巾上敲打颠倒的管来去除最后痕量的液体。【b.增溶及再折叠】-从待处理的包含体湿重,计算对于以10~15mg/ml浓度重悬浮包含体必需的1×增溶缓冲液的量。如果计算的体积大于250ml,使用250ml。-于室温,制备计算的体积的补充了0.3%n-月桂基肌氨酸(可使用达2%,如果进一步优化中需要)(300mg/100ml缓冲液)及1mmdtt的1×增溶缓冲液。-将计算的量的1×增溶缓冲液来自步骤2的添加到包含体及轻轻混合。可将大的碎片通过重复的移液打碎。-在冰箱摇床中于25℃,以50~100rpm温育4~5小时。-通过于室温以10000×g离心10分钟来澄清。【c.蛋白再折叠的透析流程】-制备所需的体积的用于溶解的蛋白透析的缓冲液。透析应以至少2次大于样品体积50倍的缓冲液变更进行。-将50×透析缓冲液稀释到期望的体积的1×,及补充0.1mmdtt。-于4℃透析至少4小时。更换缓冲液及持续。透析额外的4或更多小时。-制备额外的如在步骤1中测定的透析缓冲液,但省略dtt。-通过2次额外的变更(分钟。各4hr),用缺少dtt的透析缓冲液持续透析。【d.促进二硫键形成的氧化还原再折叠缓冲液】-制备在1×透析缓冲液中含1mm还原的谷胱甘肽(1.2g/4l)及0.2mm氧化的谷胱甘肽(0.48g/4l)的透析缓冲液。体积应25倍大于溶解的蛋白样品体积。冷却至4℃。-透析来自步骤1的再折叠的蛋白于4℃过夜。【纯化】全部过程于4℃进行。化学品:氨基丁三醇盐酸盐(sigmat5941-500g)氯化钠5m溶液(sigmas6546-4l)氢氧化钠10n(jtbaker5674-02)【e.在deaehiprep16/10阴离子柱-20ml(gehealthcare)上的纯化】缓冲液a:50mmtris-hclph8.0缓冲液b:含1mnaclph8.0的50mmtris-hcl柱平衡:缓冲液a-5cv,缓冲液b-5cv,缓冲液a-10cv-每次运行以2.0ml/分钟负荷50ml的样品到20ml柱(nrg-1在流通中)。-用5cv的缓冲液a洗涤20ml柱20ml柱用至100%b的梯度用5cv。这是为洗脱下混入物。-用10cv的100%缓冲液b清洁。-用15cv的缓冲液a平衡-用sds-page银染色分析级分-用nrg-1(10kda)合并级分【f.nrg-1的浓度】-用milliporecentriprep3000mwco15ml浓缩机(ultracelym-3,4320)浓缩-使用改良的lowry蛋白测定来测定浓度。【g.his-标签去除】用来自novagen(cat#69022-3)的a凝血酶切割捕获试剂盒进行his-标签去除。基于之前测试,最佳条件对于每10μg的nrg-1蛋白是于室温以0.005u的酶/μl的凝血酶4小时。温育4小时后,添加16μl的链霉亲和素琼脂糖浆/单元的凝血酶。于室温摇动样品30分钟。通过自旋-过滤或无菌过滤(取决于体积)回收nrg-1。用egf及抗-his蛋白印迹确定完全切割。【h.最终缓冲液中的储存】于4℃储存在含0.2%bsa的1×pbs中。【ggf2的表达及纯化】对于ggf2的克隆及背景信息,见uspn5,530,109。细胞系描述于uspn6,051,401。将各uspn5,530,109及uspn6,051,401的整个内容均通过引用整体并入本文。cho-(alpha2hsg)-ggf细胞系:此细胞系设计来产生足够的量的胎球蛋白(人alpha2hsg),以支持在无血清条件下rhggf2的高产生速度。用如图19显示的表达载体(psv-ahsg)转染cho(dhfr-)细胞。在氨苄西林压力下稳定的细胞生长。细胞系标识为(dhfr-/α2hsgp)。然后将dhfr-/α2hsgp细胞使用阳离子脂质dmrie-c试剂(lifetechnologies#10459-014)用如图20显示的含人ggf2的编码序列的pcmggf2载体转染。根据标准流程使用甲氨喋呤(100nm,200nm,400nm,1μm)以4~6周间隔衍生稳定的及高产的细胞系。使细胞逐渐从含血清的培养基脱离。克隆通过标准限制稀释方法分离。培养基要求之细节见于上述报道。为增强转录,将ggf2编码序列放置在ebvbmlf-1干扰序列(mis)后。见图21。mis序列ggat[aactagcagcatttcctccaacgaggatcccgcag(gtaagaagctacaccggccagtggccggggcccgataactagcagcatttcctccaacgaggatcccgcag(gtaagaagctacaccggccagtggccggggccgtggagccgggggcatccggtgcctgagacagaggtgctcaaggcagtctccaccttttgtctcccctctgcag)agagccacattctggaa]gtt【ggf2编码序列】【ggf2蛋白序列】mrwrraprrsgrpgpraqrpgsaarsspplpllplllllgtaalapgaaagneaapagasvcyssppsvgsvqelaqraavviegkvhpqrrqqgaldrkaaaaageagawggdreppaagpralgppaeepllaangtvpswptapvpsagepgeeapylvkvhqvwavkagglkkdslltvrlgtwghpafpscgrlkedsryiffmepdanstsrapaafrasfppletgrnlkkevsrvlckrcalppqlkemksqesaagsklvlrcetsseysslrfkwfkngnelnrknkpqnikiqkkpgkselrinkasladsgeymckvisklgndsasanitivesnatststtgtshlvkcaekektfcvnggecfmvkdlsnpsrylckcpneftgdrcqnyvmasfyststpflslpeggf2产生:将一瓶2.2×106细胞/ml的ggf2解冻到100ml的acorda培养基1(见表2),及扩展直到达到足够数,以接种产生容器。将细胞在2l通气的滚瓶中以1.0×105细胞/ml接种于生产培养基acorda培养基2(见表3)。将滚瓶维持于37℃5天,然后降低到27℃26天。监控滚瓶的细胞计数及总体外观,但它们不进料。一旦活力到10%以下,将细胞旋转出,及收获条件培养基及无菌过滤。表2:培养基1表3:培养基2【ggf2的纯化流程】全部过程于4℃进行。化学品:乙酸钠冰醋酸(用于ph调节)10nnaoh(用于ph调节)nacl硫酸钠l-精氨酸(jtbakercat#:2066-06)甘露糖醇(jtbakercat#:2553-01)原材料:条件培养基上清。调整ph到6.5。【步骤1】捕获-阳离子交换层析hiprepsp16/10(amershambiosciences)柱平衡:缓冲液a-5cv,缓冲液b-5cv,缓冲液15%b-5cv缓冲液a:20mm乙酸钠,ph6.0缓冲液b:20mm乙酸钠,ph6.0,1mnacl以2ml/分钟负荷样品(如果可能,用连续的负荷)过夜。用连续的装载结合更佳。用于起始样品的最大容量:5mgggf2/ml培养基流速:3ml/分钟首次洗涤:15%b,10cv第二次洗涤:35%b,10cvggf2洗脱:60%b,8cv柱洗涤:100%b,8cv【步骤2】精制-凝胶过滤层析聚丙烯酰胺葡聚糖s20026/60洗脱缓冲液:20mm乙酸钠,100mm硫酸钠,1%甘露糖醇,10mml-精氨酸,ph6.5缓冲液导电性:样品:spggf2洗脱合并浓缩达~au2801.0流速:1.3ml/分钟峰洗脱:从注射开始,在~0.36cv【步骤3】dna及内毒素去除-通过interceptq膜过滤。预平衡缓冲液:20mm乙酸钠,100mm硫酸钠,1%甘露糖醇,10mml-精氨酸,ph6.5收集流通物【步骤4】最终制剂及样品制备将额外的90mml-精氨酸添加到样品浓缩无菌过滤器本文所用的媒质/对照物品是如所示的0.2%牛血清白蛋白(bsa),0.1m磷酸钠,ph7.6或0.1m磷酸钠,ph7.6。【碱性fgf】如peprotech的指导将bfgf(peprotechinc.,100-18b,lot1206cy08g2407)复原到0.1mg/ml的浓储物溶液及使用之前保存于-20℃。在注射日,将100μg/ml的bsa(rochediagnostics,lot12403328exp.mar31,2008)溶液制成为稀释剂,以使最终bfgf浓度为20μg/ml(1μg/50ul)。此物质仅用于研究1。【随机化及盲试】5只动物每天操作。研究者进行手术及使行为评定对于各动物的处理分配(除了bfgf处理的组之外)盲,直到收集全部数据。【行为测试】感觉运动功能活性使用前肢及后肢放置,及身体摆动行为测试评价。这些测试在手术前一天,手术后1天及在mcao后3,7,14及21天时进行。【1.肢放置】肢放置测试分为前肢及后肢测试。对于前肢放置测试,检查者保持大鼠接近于的桌面,及评分大鼠响应须,视觉,触觉,或本体感受性刺激将前肢放置到桌面的能力。类似地,对于后肢放置测试,检查者评定大鼠响应触觉及本体感受性刺激将后肢放置到桌面的能力。对感觉输入的各模式得到分离的亚-分值(半点指定可能的),及加入,以给出总分值(对于前肢放置测试:0=正常,12=最大程度地损伤的;对于后肢放置测试:0=正常;6=最大程度地损伤的)。【2.身体摆动测试】将大鼠从其尾基部大致1英寸拿住。其然后升高到桌面以上1英寸。大鼠以垂直轴保持,限定为向左或右侧不多于10°。只要大鼠动其头出垂直轴到任意侧就记录摆动。大鼠必需返回垂直位置,才计数下一次摆动。总计数30次摆动。正常大鼠一般具有向两侧的等数的摆动。病灶缺血后,大鼠倾向于摆动到对侧(左)侧。在行为测试的全部天,动物在药物施用之前测试。以手术日(第0天)作为参照指定时间点。【处死及梗塞体积】在mcao后21天时行为评估后,将大鼠用氯胺酮(50~100mg/kg)及赛拉嗪(5~10mg/kg)混合物,腹膜内深度麻醉。将动物用正常盐水(含肝素,2单元/ml)然后是10%福尔马林经贲门灌注。然后移出脑,及储存于10%福尔马林。然后将固定的脑用石蜡包埋,及使用切片机切成5μm冠切片。然后将切片用苏木素及伊红(h&e)染色。将来自各脑的7个切片(相比前囟点分别+4.7,+2.7,+0.7,-1.3,-3.3,-5.3及-7.3)通过数码照相机拍摄,及将各切片上的梗塞区通过nih图像(图像j)使用"间接方法"(完整的对侧[左]半球面积-同侧[右]半球的完整的区面积)测定,以修正脑水肿。然后总和众切片的梗塞面积及乘以切片厚度,以给出总梗塞体积,其表示为完整的对侧半球体积的百分率。【实施例2:ggf2(nrg-1)in在大鼠永久的中脑动脉阻塞(mcao)模型中增强神经性恢复的效应–在急性期期间起始治疗及然后持续】【ggf2及nrg-1的效应:大鼠中mca阻塞(mcao)后功能恢复】研究1实验组(n=10):nrg-1,1.0μg/kg,1ml/kg静脉内;1小时后,&一次/天(q24)mcao后持续10天ggf2,6.5μg/kg,1ml/kg静脉内;1小时后,&q24mcao后持续10天ggf2,100μg/kg,1ml/kg静脉内;1小时后,&q24mcao后持续10天bfgf,脑池内,1μg/50μl;mcao后第1天及第3天(阳性对照)媒质,1ml/kg静脉内;1小时后,&q24mcao后持续10天(媒质=0.2%bsa/0.1m磷酸钠ph7.6)全部数据表示为平均值±标准误差。除非别有指定,行为及体重数据通过重复的anova测量(处理x时间)分析。包括全部组的总体anova的阳性f-值致使组之间配对anova。梗塞体积数据通过单因素anova分析。【结果】【前肢放置测试】ggf2中的恢复,100μg/kg组高于媒质组(p<0.001)。bfgf组中的恢复高于媒质组(p<0.05)。ggf2,6.5μg/kg或nrg,1.0μg/kg组的恢复相比媒质组无显著的差异。见图2。【后肢放置测试】bfgf及ggf2中的恢复,在全部行为测试天100μg/kg组显著好于媒质组(p<0.001)。ggf2中的恢复,在行为测试第7天及第14天,6.5μg/kg组及nrg,1.0μg/kg组相比媒质显著改善,但此效应未维持到21天端点。见图3。【身体摆动测试】bfgf组及ggf2中的恢复,在行为测试第21天端点,100μg/kg组相比媒质显著改善(p<0.05)。nrg的恢复,1.0μg/kg组,或ggf2,6.5μg/kg组相比媒质组无显著的差异。见图4。【重量变化】组间无显著的差异。梗塞体积:组间无显著的差异。见以上表1。【总结】这些结果证实,ggf2以剂量应答性方式作用,及促进此永久的中风模型中的功能恢复。使用更低剂量的神经调节蛋白的后肢数据显示,持续的处理可导致持续的改善。【实施例3:ggf2剂量施用(损伤后延缓)时机(包括慢性时期施剂)在大鼠永久的中脑动脉阻塞(mcao)中增强神经性恢复中的效应】ggf2对大鼠中mcao后功能恢复的效应实验组(n=10):ggf2,0.1mg/kg,(1ml/kg)静脉内;10日每天注射,在mcao后第1天起始ggf2,0.1mg/kg,(1ml/kg)静脉内;10日每天注射,在mcao后第3天起始ggf2,0.1mg/kg,(1ml/kg)静脉内;10日每天注射,在mcao后第7天起始媒质,1ml/kg静脉内;10日每天注射,在mcao后第1天起始(媒质=0.1m磷酸钠ph7.6)动物开始在mcao后第1天,第3天或第7天静脉内接受ggf2或媒质持续10天。全部溶液每天新鲜制备。【结果】【前肢放置】第1天ggf2处理组中的恢复在处理后测试的全部时间点(在第3天(p<0.0001),在第7天(p<0.005),在第14天(p<0.0001)及在第21天(p<0.0001))相比媒质组显著改善。第3天ggf2处理组展示相比媒质显著的改善,在第7天(p<0.05)及第21天(p<0.05)第7天ggf2处理组展示相比媒质恢复斜率的清楚的偏转,从第7天(处理开始)~第14天,此差异变得显著的至第21天(p<0.05)。这些数据表明在损伤后晚至3及甚至7天处理可产生显著的神经性功能的改善。更延长的处理可有益及导致更大及更持续的效应。见图5a。【后肢放置】第1天ggf2处理组中的恢复在处理后测试的全部时间点(在第3天(p<0.05)及在第7,14及21天(p<0.0001))相比媒质组显著改善。第3天ggf2处理组在测试第7天的(p<0.001)及第14天(p<0.05,处理结束后的天)展示显著好于媒质的改善,及在第21天趋向显著(p<0.065)。第7天ggf2处理组在测试第21天研究端点相比媒质显著改善(p<0.05)。图5b。身体摆动:第1天ggf2处理组的恢复显著好于媒质组(p<0.001)。在第3天ggf2组及第7天ggf2组,相比媒质组有向恢复的趋势图,5c。组之间无显著的体重差异。梗塞体积:如表4中所示的,全部组间无显著的差异。表4:组%梗塞体积第1天媒质32.89±2.63ggf2第1天27.62±2.48ggf2第3天33.31±3.84ggf2第7天27.30±2.87【总结】至第21天研究终点,发现于mcao后第1天,第3天或第7天起始治疗导致相比媒质处理的动物显著的前肢功能的改善。于mcao后第1天,第3天或第7天起始治疗导致在与处理时间相关的特异性行为测试点期间相比媒质处理显著的后肢功能的改善,表明持续的处理可确保有益。用在此损伤后后期时间点给予的干扰的功能恢复消除效应是由于急性神经保护的可能性。的确,此与梗塞体积缺乏显著的变化偶联的数据显示,改善是由于用ggf2治疗的神经恢复的促进。此显示,在可施用ggf2作为中风慢性期的有效治疗剂期间存在(急性后及半急性后)长时间窗。值得注意,在mcao后3及7天施用ggf2后观察的显著的(根据anova统计学)改善代表由在之前的治疗中风急性期可用的策略提供的治疗性窗的显著扩展。本领域中首次,本文呈现的数据展示,ggf2施用甚至在中风慢性期期间有效。本文呈现的数据还提示,ggf2贡献于神经损伤后神经恢复。【实施例4:缺血性中风的治疗】将有缺血性中风的迹象及症状的患者呈于医学设备。将患者用tpa或其他治疗重血管化,以恢复血流。尽管血流已恢复,一些水平的脑损伤已发生。损伤后3天神经学评定患者,及显示具有可测量的感觉和/或运动缺乏。于第4天开始,在第2天后及第3天后,将此患者以0.01和1.0mg/kg/剂量之间的剂量用神经调节蛋白静脉内处理10天~3个月。患者无伴随的使用职业性或物理治疗地成功地重获感觉及运动功能。此恢复好于临床上会预测到的无神经调节蛋白治疗的恢复。此恢复好于临床上会预测到的不使用职业性或物理治疗的恢复。【实施例5:中风治疗及得到的右手麻痹】将患右手麻痹的患者呈于急诊部。评估及成像后确定患者患缺血性中风。患者根据获得批准的方法接受tpa,及血流通过血栓形成恢复。但是,tpa处理后一周,患者右手具有通过手运动活性的标准神经性测量所测的残留的麻痹。此患者用神经调节蛋白(0.01~1.0mg/kg,静脉内)一次/周处理4周。手功能改善由神经学家或其他医师用标准神经性测试(包括动力仪)及其他强度测试周期性地测量。患者成功地不伴随使用职业性或物理治疗地重获右手感觉及运动功能。此恢复好于临床上会预测到的无神经调节蛋白治疗的恢复。此恢复好于临床上会预测到的不使用职业性或物理治疗的恢复。【实施例6:缺血性中风的治疗】将有缺血性中风的迹象及症状的患者呈于医学设备。它们发现具有左侧麻痹。患者不及时到达重血管化治疗。临床评估之后发现,一些脑损伤已发生。损伤后3天神经学评定患者,及显示具有可测量的感觉及运动缺乏。此患者用神经调节蛋白以0.01和1.0mg/kg/剂量之间的剂量每天静脉内处理4周;然后接受每周剂量6个月。也接受物理治疗。注意到早至治疗第二周的改善;恢复持续贯穿神经调节蛋白治疗时期。患者成功地重获左侧感觉及运动功能。此恢复观察到同样优良;及相比临床上会预测到的不单独利用物理治疗的恢复好得多。【实施例7:缺血性中风的治疗】将患左手麻痹的患者呈于急诊部。患者报道手出问题开始“超过一周前”。评估及成像后确定患者患缺血性中风。患者不接受tpa。神经性检查之后发现患者具有通过手运动活性的标准神经性测量所测的残留的左手麻痹;患者还具有感觉缺乏。患者拒绝参与物理或职业疗法。此患者用神经调节蛋白(0.01~1.0mg/kg,静脉内)一次/周治疗12周。由神经学家或其他医师用标准神经性测试(包括动力仪)及其他强度测试周期性地测量手功能的改善。注意到早至治疗第二周的改善;恢复持续贯穿神经调节蛋白治疗时期。患者成功地不伴随使用职业性或物理治疗地重获左手感觉及运动功能。此恢复好于临床上会预测到的无神经调节蛋白治疗的恢复。此恢复好于临床上会预测到的不使用职业性或物理治疗的恢复。【实施例8:创伤性脑损伤】将创伤性事件后有头损伤及由此造成的脑损伤的迹象及症状的患者呈于医学设备。一些水平的脑损伤已发生,如通过成像及神经性测试(包括glasgowcoma标尺及更详细的神经认知测试)评定。损伤后5天,神经学评定患者,及显示具有可测量的感觉及运动缺乏。此患者用神经调节蛋白以0.01和1.0mg/kg/剂量之间的剂量静脉内处理3个月。起初患者不愿意参与物理治疗。在早至治疗第一周注意到脑功能改善;恢复持续贯穿神经调节蛋白治疗时期。此恢复好于临床上会预测到的无神经调节蛋白治疗的恢复。在3个月开始,患者开始一次/周接受神经调节蛋白,及它们也开始接受物理治疗。伴随的治疗从原损伤日持续直到一年。在患者的损伤一周年,恢复效果非凡。临床上相比无任何治疗的情况下预期的更佳,及也好于使用物理治疗预期的。【实施例9:脑出血的治疗】将有与缺血性中风或脑出血一致的迹象及症状的患者呈于医学设备。稳定患者。神经性评定之后发现一些水平的脑损伤已发生。损伤后一周,患者再次神经学评定,及显示具有可测量的感觉和/或运动缺乏。此患者用神经调节蛋白以0.01和1.0mg/kg之间的剂量每天静脉内处理10天,然后是每周施用此剂量2个月,在该点全部处理将中止。早至处理第一周注意到脑功能的改善;恢复持续贯穿神经调节蛋白治疗时期。神经调节蛋白治疗停止之后,患者恢复被认为临床上优良。患者从初始损伤之日起6个月,然后12个月返回评估;在各评定,患者的恢复被认为临床上优良。【实施例10:包括在半-急性及慢性时期治疗的损伤的nrg治疗】对于综合试验,包含标准包括:成年者,雄性及雌性,有神经损伤的临床证据。【探究的适应症】缺血性中风,用溶血栓剂,缺血性中风,不用溶血栓剂,出血性中风,闭合的头部创伤性脑损伤,穿透性创伤性脑损伤【探究的剂量范围】0.001mg/kg~10.0mg/kg/剂量【探究的剂量频度】每天每隔一天每第四天一次/周每隔一周一次一次/个月【混合的周期性方案】-对于1或2周每天,然后对于之后研究每周,每两周,或每月-对于1或2周每隔一天,然后每周,每两周或然后每月【探究的治疗起始】损伤后尽早在损伤后6,12,24及48小时内在损伤后72小时后在损伤后7,14,30,60,90,120天【探究的处理持续时间】处理1,2,4,10,30周。处理1,2,3,4,5,6,7,8,9,10,11,12个月【探究的功能】手运动功能,面运动功能,语言认知功能存活返回工作的时间通过标准神经性测量测量恢复。不利的事件弱及良好-耐受。结果:如通过本领域中已知的方法所测,用神经调节蛋白处理的患者相比用安慰剂处理的患者,在心理,感觉或肌肉功能显示统计学更大的改善。在替代性实施方式中探究小于全部以上参数的组合。【实施例11:有单侧手虚弱和/或麻痹的缺血性中风的nrg治疗(不血栓溶解)】包含标准包括:成年者,雄性及雌性,基于损失意识,定向障碍,语言障碍,面或肢麻痹的中风证据。缺血性中风用放射摄影成像确证。选择不是tpa(或其他溶血栓剂)的候选体的或由于任何原因之前未接受tpa的单侧手虚弱和/或麻痹的患者。得到患者和/或某些有权为患者签字的人的同意。患者募集及随机化至接受的神经调节蛋白或安慰剂起始快至它们呈于医学设备(包括医院或医师的办公室),诊断,得到成像。对此试验,在损伤后1小时和7天之间起始治疗。处理持续3个月,对于1周是每隔一天施剂,然后对于其余处理时期是每周施剂。患者用0.0001~1.0mg/kg,静脉内,im或皮下施剂。通过每隔一周手运动活性的标准神经性测量经研究的持续时间来测量恢复。不利的事件弱及良好-耐受。结果:如通过本领域中已知的方法所测,用神经调节蛋白处理的患者相比用安慰剂处理的患者,手功能显示统计学更大的改善。【实施例12:不用溶血栓剂的单侧面部麻痹的nrg治疗】选择未或不可接受溶血栓剂的患单侧面部麻痹的患者。功能在3个月施剂时期期间每隔一周通过本领域中已知的方法评定。得到患者和/或某些有权为患者签字的人的同意。患者募集及随机化至接受的神经调节蛋白或安慰剂。在损伤后1小时和7天之间起始治疗。处理持续3个月,对于1周是每隔一天施剂,然后对于其余处理时期是每周施剂。患者用0.0001~1.0mg/kg,静脉内,im或皮下施剂。不利的事件弱及良好-耐受。结果:用神经调节蛋白处理的患者在面部运动相比用安慰剂处理的患者显示统计学更大的改善。【实施例13:不用溶血栓剂的失语症或构音困难的nrg治疗】选择未或不可接受溶血栓剂的患失语症或构音困难的患者。功能在3个月施剂时期期间每隔一周通过本领域中已知的方法评定。得到患者和/或某些有权为患者签字的人的同意。患者募集及随机化至接受的神经调节蛋白或安慰剂。在损伤后1小时和7天之间起始治疗。处理持续3个月,对于1周是每隔一天施剂,然后对于其余处理时期是每周施剂。患者用0.0001~1.0mg/kg,静脉内,im或皮下施剂。不利的事件弱及良好-耐受。结果:用神经调节蛋白处理的患者相比用安慰剂处理的患者语言能力显示统计学更大的改善。【实施例14:缺血性中风的nrg治疗(用血栓溶解)】包含标准包括:成年者,雄性及雌性,基于损失意识,定向障碍,语言障碍,面或肢麻痹的中风证据。缺血性中风用放射摄影成像确认。选择成功地用tpa或其他溶血栓剂处理的单侧手虚弱和/或麻痹的患者。得到患者和/或某些有权为患者签字的人的同意患者募集及随机化至接受的神经调节蛋白或安慰剂起始快至它们呈于医学设备,诊断,及成像完成。在损伤后1小时和7天之间起始治疗。处理持续3个月,对于1周是每隔一天施剂,然后对于其余处理时期是每周施剂。患者用0.0001~1.0mg/kg,静脉内,im或皮下施剂。通过每隔一周手运动活性的标准神经性测量经研究的持续时间来测量恢复。不利的事件通常弱及良好耐受的。结果:如通过本领域中已知的方法所测,用神经调节蛋白处理的患者相比用安慰剂处理的患者,手功能显示统计学更大的改善。【实施例15:患单侧面部麻痹的患者的nrg治疗(用溶血栓剂)】包含标准包括:成年者,雄性及雌性,基于损失意识,定向障碍,语言障碍,面或肢麻痹的中风证据。缺血性中风用放射摄影成像确认。选择患失语症或构音困难及接受溶血栓剂的患者。在损伤后1小时和7天之间起始治疗。处理持续3个月,对于1周是每隔一天施剂,然后对于其余处理时期是每周施剂。患者用0.0001~1.0mg/kg,静脉内,im或皮下施剂。功能在3个月施剂时期期间每隔一周通过本领域中已知的方法评定。不利的事件弱及良好-耐受。结果:用神经调节蛋白处理的患者相比用安慰剂处理的患者语言能力显示统计学更大的改善。【实施例16:患创伤性脑损伤的患者的nrg治疗】包含标准包括:成年者,雄性及雌性,有损失意识,定向障碍,语言障碍,面或肢麻痹的创伤性脑损伤证据,有创伤历史证据。排除有穿透损伤证据的患者。得到患者和/或某些有权为患者签字的人的同意。患者募集及随机化至接受的神经调节蛋白或安慰剂起始快至它们呈于医学设备(包括医院或医师的办公室),诊断,成像及得到同意。对此试验,在损伤后1小时和7天之间起始治疗。处理持续3个月,对于1周是每隔一天施剂,然后对于其余处理时期是每周施剂。患者用0.0001~1.0mg/kg,静脉内,im或皮下施剂。功能恢复通过本领域中已知的方法评定。不利的事件弱及良好-耐受。结果:用神经调节蛋白处理的患者相比用安慰剂处理的患者显示统计学更大的改善。【实施例17:患穿透性脑损伤的患者的nrg治疗】包含标准包括:成年者,雄性及雌性,有损失意识,定向障碍,语言障碍,面或肢麻痹的创伤性脑损伤证据,有创伤历史证据。得到患者和/或某些有权为患者签字的人的同意。患者手术或通过其他测量稳定。诊断及得到成像。患者募集及随机化至接受的神经调节蛋白或安慰剂起始快至它们呈于医学设备(包括医院或医师办公室)。在损伤后1小时和7天之间起始治疗。处理持续3个月,对于1周是每隔一天施剂,然后对于其余处理时期是每周施剂。患者用0.0001~1.0mg/kg,静脉内,im或皮下施剂。功能恢复通过本领域中已知的方法评定。不利的事件弱及良好-耐受。结果:用神经调节蛋白处理的患者相比用安慰剂处理的患者,语言能力显示统计学更大的改善。【实施例18:患出血性中风的患者的nrg治疗】包含标准包括:成年者,雄性及雌性,基于损失意识,定向障碍,语言障碍,面或肢麻痹的中风证据。出血性中风用放射摄影成像确证。得到患者和/或某些有权为患者签字的人的同意。选择患单侧手虚弱的患者。患者募集及随机化至接受的神经调节蛋白或安慰剂起始快至它们呈于医学设备(包括医院或医师的办公室),诊断,成像及得到同意。在损伤后1小时和7天之间起始治疗。处理持续3个月,对于1周是每隔一天施剂,然后对于其余处理时期是每周施剂。患者用0.0001~1.0mg/kg,静脉内,im或皮下施剂。通过每隔一周手运动活性的标准神经性测量经研究的持续时间来测量恢复。不利的事件弱及良好-耐受。结果:如通过本领域中已知的方法所测,用神经调节蛋白处理的患者相比用安慰剂处理的患者,显示统计学更大的手功能改善。【实施例19:试剂盒】试剂盒包括本发明的例示实施方式。试剂盒可包括外部容具或容器,其配置为接受一或多个内部容具/容器,器具和/或使用说明。器具可包括施用药物的物品,例如罩,吸入设备,注射器或针。本发明的组合物可包括在本发明的容具内。本发明的容具可含足够的量的本发明的组合物,以对于多个剂量有用,或可取单元或单个剂量形式。本发明的试剂盒通常包括根据本发明施用的使用说明。任何本文中所示或支持的施用模式可构成使用说明的一些部分。在一实施方式中,使用说明表明本发明的组合物旨在在损伤后时期半-急性期间采取一或多于一次。在一实施方式中,使用说明表明本发明的组合物旨在在损伤后时期慢性期间采取一或多于一次。使用说明可附于本发明的任何容器/容具。或者,使用说明可打印在或雕刻于本发明的容具,或作为本发明的容具的成分形成。本申请中参考几个出版物及专利文献,以便更完全说明本发明涉及的现有技术。此说明书提及的全部出版物及专利申请中通过引用并入本文,如同各独立性出版物或专利申请特异性地及个别通过引用并入本文。序列表<110>acordatherapeutics,inc.<120>在cns神经性损伤后非-急性期间处理的组合物及方法<130>61/189,191<140>pct/us2009/004692<141>2009-08-17<160>5<170>patentinversion3.5<210>1<211>198<212>dna<213>智人(homosapiens)<220><223>nrg1b2egf结构域cdna<400>1catatgagccatcttgtaaaatgtgcggagaaggagaaaactttctgtgtgaatggaggg60gagtgcttcatggtgaaagacctttcaaacccctcgagatacttgtgcaagtgcccaaat120gagtttactggtgatcgctgccaaaactacgtaatggccagcttctacaaggcggaggag180ctgtaccagtaaggatcc198<210>2<211>82<212>prt<213>智人(homosapiens)<220><223>nrg1b2egf结构域肽<400>2metglyserserhishishishishishisserserglyleuvalpro151015argglyserhismetserhisleuvallyscysalaglulysglulys202530thrphecysvalasnglyglyglucysphemetvallysaspleuser354045asnproserargtyrleucyslyscysproasngluphethrglyasp505560argcysglnasntyrvalmetalaserphetyrlysalaglugluleu65707580tyrgln<210>3<211>236<212>dna<213>epstein-barr病毒<220><223>mis序列<400>3cgataactagcagcatttcctccaacgaggatcccgcaggtaagaagctacaccggccag60tggccggggcccgataactagcagcatttcctccaacgaggatcccgcaggtaagaagct120acaccggccagtggccggggccgtggagccgggggcatccggtgcctgagacagaggtgc180tcaaggcagtctccaccttttgtctcccctctgcagagagccacattctggaagtt236<210>4<211>1269<212>dna<213>智人(homosapiens)<220><223>ggf2编码序列<400>4atgagatggcgacgcgccccgcgccgctccgggcgtcccggcccccgggcccagcgcccc60ggctccgccgcccgctcgtcgccgccgctgccgctgctgccactactgctgctgctgggg120accgcggccctggcgccgggggcggcggccggcaacgaggcggctcccgcgggggcctcg180gtgtgctactcgtccccgcccagcgtgggatcggtgcaggagctagctcagcgcgccgcg240gtggtgatcgagggaaaggtgcacccgcagcggcggcagcagggggcactcgacaggaag300gcggcggcggcggcgggcgaggcaggggcgtggggcggcgatcgcgagccgccagccgcg360ggcccacgggcgctggggccgcccgccgaggagccgctgctcgccgccaacgggaccgtg420ccctcttggcccaccgccccggtgcccagcgccggcgagcccggggaggaggcgccctat480ctggtgaaggtgcaccaggtgtgggcggtgaaagccgggggcttgaagaaggactcgctg540ctcaccgtgcgcctggggacctggggccaccccgccttcccctcctgcgggaggctcaag600gaggacagcaggtacatcttcttcatggagcccgacgccaacagcaccagccgcgcgccg660gccgccttccgagcctctttcccccctctggagacgggccggaacctcaagaaggaggtc720agccgggtgctgtgcaagcggtgcgccttgcctccccaattgaaagagatgaaaagccag780gaatcggctgcaggttccaaactagtccttcggtgtgaaaccagttctgaatactcctct840ctcagattcaagtggttcaagaatgggaatgaattgaatcgaaaaaacaaaccacaaaat900atcaagatacaaaaaaagccagggaagtcagaacttcgcattaacaaagcatcactggct960gattctggagagtatatgtgcaaagtgatcagcaaattaggaaatgacagtgcctctgcc1020aatatcaccatcgtggaatcaaacgctacatctacatccaccactgggacaagccatctt1080gtaaaatgtgcggagaaggagaaaactttctgtgtgaatggaggggagtgcttcatggtg1140aaagacctttcaaacccctcgagatacttgtgcaagtgcccaaatgagtttactggtgat1200cgctgccaaaactacgtaatggccagcttctacagtacgtccactccctttctgtctctg1260cctgaatag1269<210>5<211>422<212>prt<213>智人(homosapiens)<220><223>ggf2蛋白序列<400>5metargtrpargargalaproargargserglyargproglyproarg151015alaglnargproglyseralaalaargserserproproleuproleu202530leuproleuleuleuleuleuglythralaalaleualaproglyala354045alaalaglyasnglualaalaproalaglyalaservalcystyrser505560serproproservalglyservalglngluleualaglnargalaala65707580valvalilegluglylysvalhisproglnargargglnglnglyala859095leuasparglysalaalaalaalaalaglyglualaglyalatrpgly100105110glyasparggluproproalaalaglyproargalaleuglypropro115120125alaglugluproleuleualaalaasnglythrvalprosertrppro130135140thralaprovalproseralaglygluproglygluglualaprotyr145150155160leuvallysvalhisglnvaltrpalavallysalaglyglyleulys165170175lysaspserleuleuthrvalargleuglythrtrpglyhisproala180185190pheprosercysglyargleulysgluaspserargtyrilephephe195200205metgluproaspalaasnserthrserargalaproalaalaphearg210215220alaserpheproproleugluthrglyargasnleulyslysgluval225230235240serargvalleucyslysargcysalaleuproproglnleulysglu245250255metlysserglngluseralaalaglyserlysleuvalleuargcys260265270gluthrserserglutyrserserleuargphelystrpphelysasn275280285glyasngluleuasnarglysasnlysproglnasnilelysilegln290295300lyslysproglylyssergluleuargileasnlysalaserleuala305310315320aspserglyglutyrmetcyslysvalileserlysleuglyasnasp325330335seralaseralaasnilethrilevalgluserasnalathrserthr340345350serthrthrglythrserhisleuvallyscysalaglulysglulys355360365thrphecysvalasnglyglyglucysphemetvallysaspleuser370375380asnproserargtyrleucyslyscysproasngluphethrglyasp385390395400argcysglnasntyrvalmetalaserphetyrserthrserthrpro405410415pheleuserleuproglu420当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1