一种靶位点的精确定位及处置方法和辅助装置与流程
本发明涉及一种靶位点的精确定位及处置方法,具体涉及一种靶位点的体内和体外精确定位及处置方法,还涉及一种基于该精确定位及处置方法的体外辅助装置及其制备方法。
背景技术:
包括肺部磨玻璃结节(GGO)在内的各种肺部结节,是胸腔镜下肺手术的手术指证之一。而对于结节太小、位置较深的情况,常因在手术中不能直接看到结节位置,而影响对于切除部位的判断。目前,解决这一临床问题,确定肺部结节位置的方法主要有三种:1.术中探查定位:术中根据胸部CT在肺结节大致范围利用手触法触摸,以确定肺结节部位;2.术前CT引导下经胸壁hook-wire定位针定位肺结节:术前在CT引导下,利用hook-wire定位针经胸壁行肺穿刺。通过反复调整和摸索,使针头逐渐接近肺部肿块位置,释放“钩形”金属材质hook-wire细丝,使之停留在肿块附近定位肺部肿块位置。术中只要通过寻找hook-wire的钩针位置,便可辅助确定肿块位置,进而决定切除的肺组织范围;3.术前CT引导下经胸壁micro-coil微弹簧圈定位肺结节:与前述hook-wire法相似,术前在CT引导下利用micro-coil微弹簧圈经胸壁行肺穿刺,定位肺部结节。主要区别在于穿刺到位后所释放的异物不是金属钩,而是一个微型弹簧圈。术中主刀医生通过触摸弹簧圈所在的位置,确定所需要切除的肺组织的范围。
但现有技术存在以下技术问题:a、术中手触摸法无法探知肿块:术中通过触摸而确认结节位置理论上是最直接、最准确的方法,然而在很多情况下术中因肺部结节的密度低、体积小、位置深在以及医生经验不足等各种原因,会导致手触法失败;b、放射辐射影响:术前经CT经hook-wire定位针或micro-coil微弹簧圈引导穿刺定位,均需短期内接受多次CT,以确定定位部位,对患者造成辐射影响;c、人员配备及费用:术前经CT经hook-wire定位针或micro-coil微弹簧圈引导穿刺定位,需要至少两名有经验的医务人员操作。一方面,医务人员培训的学习曲线平缓、培养周期长;另一方面,加重了医务人员的工作量和医疗费用,增加了患者的经济负担。
现有术前定位方法耗时长,要求患者长时间以固定姿势侧卧于CT床上,经受穿刺针的反复调整和多次穿刺,非常痛苦。而对于意识不清或重症的不能配合的患者,现有技术是完全无法可行的。
技术实现要素:
本发明为解决现有技术中的上述问题,首先提出一种靶位点的精确定位及处置方法,其次提供一种靶位点的体外和体外精确定位及处置方法,还提供一种3D打印的肺部靶病灶定位/活检体外辅助装置及其制备方法,使得靶位点的定位更为精准、处置效果更为优异。
本发明一种靶位点的精确定位及处置方法的技术原理为:根据患者断层影像学数据,利用计算机辅助设计软件,构建患者解剖结构的数字模型;根据此模型,个性化设计靶位点定位导板模型,所述靶位点定位导板模型紧密贴合患者解剖结构的数字模型的体表或脏器表面,并根据靶位点的三维位置,设计定位角度辅助单元模型的定位位置和角度;然后利用3D打印技术打印出具有定位角度辅助单元的靶位点定位板,再利用所述具有定位角度辅助单元的靶位点定位板对患者的靶位点进行相应的处置。本发明的靶位点定位及处置方法可广泛应用于手术前定位、穿刺活检、放疗等领域,所述定位处置是指对靶位点进行标记定位、穿刺活检、穿刺引流、定向穿刺、定位切除、立体定位放射、固定器术中放置以及其它手术前或术中操作等。
为实现上述目的,本发明采用以下技术方案:
本发明的第一个方面是提供一种靶位点的精确定位及处置方法,包括如下步骤:
步骤一,根据患者断层影像学数据,利用计算机建模软件,构建患者的解剖结构的数字模型,并在所述解剖结构的数字模型上确定靶位点的三维位置;
步骤二,根据所述步骤一得到的解剖结构的数字模型,再次利用计算机建模软件设计紧密贴合在所述解剖结构的数字模型的患者体表或脏器表面的靶位点定位导板模型;并根据所述步骤一确定的靶位点的三维位置,在所述靶位点定位导板模型上设计定位角度辅助单元模型,所述定位角度辅助单元模型包括辅助通道,所述辅助通道的相对角度根据靶位点的位置、定位角度辅助单元模型的位置、涉及的重要脏器或组织的位置三者共同决定;
步骤三,将具有定位角度辅助单元模型的靶位点定位导板模型利用3D打印技术打印成型,制得靶位点定位装置;
步骤四,将所述步骤三制得的靶位点定位装置安置于患者体表或脏器表面相应位置上,在定位角度辅助单元的辅助下,利用处置装置对靶位点进行相应的处置。
作为本发明的一个优选的技术方案,在所述靶位点的精确定位及处置方法的步骤二中,所述靶位点定位导板模型的设计方法为:
a、在所述解剖结构的数字模型上设计定位路径,所述定位路径为经过所述靶位点且距离体表或脏器表面的最短距离;沿所述定位路径在体表或脏器表面上的点为穿刺点;并在所述解剖结构的数字模型上以患者的体表标志或脏器表面标志为参考点,设计用于辅助所述靶位点定位装置正确放置和定位的解剖定位点;
b、以所述解剖定位点、定位路径和穿刺点为参考,利用计算机建模软件设计贴合在所述解剖结构的数字模型表面的靶位点定位导板模型。
作为本发明的一个较为优选的技术方案,在所述的靶位点的精确定位及处置方法的步骤二中,所述定位角度辅助单元模型的辅助通道位于所述靶位点与所述穿刺点之间的所述定位路径上,所述定位路径是根据需要避开所述解剖结构的数字模型的血管、神经、骨骼而设置的最短距离。
作为本发明的一个优选的技术方案,在所述的靶位点的精确定位及处置方法的步骤二中,根据临床需求不同,在所述定位角度辅助单元模型上设置有用于配合所述处置装置定位的辅件机构。
作为本发明的一个较为优选的技术方案,在所述的靶位点的精确定位及处置方法中,所述辅件机构包括固定架、消毒孔、导轨钢芯。
作为本发明的一个优选的技术方案,在所述的靶位点的精确定位及处置方法中,所述解剖结构的数字模型包括具有靶位点的头颈部、躯干部、上肢部或下肢部的数字模型。
作为本发明的一个优选的技术方案,在所述的靶位点的精确定位及处置方法的步骤一中,根据患者的断层影像学数据,在所述解剖结构的数字模型上标记并计算所述靶位点的部位、大小、深度和个数。
作为本发明的一个优选的技术方案,在所述的靶位点的精确定位及处置方法的步骤四中,所述处置装置为活检枪、定位针、放射源、电极膜片或采血针。
作为本发明的一个较为优选的技术方案,所述定位针为连接组装活检枪弹射部件或者一次性血糖采血针弹射部件。
作为本发明的一个优选的技术方案,在所述的靶位点的精确定位及处置方法中,所述计算机建模软件选自Mimics、Magics、Geomagic Studio、3Dmax、PROE、UG、AUTOCAD或SOLIDWORK。
本发明的第二个方面是提供一种所述的靶位点的精确定位及处置方法在术前定位、穿刺活检、立体辐射放疗领域中的应用。具体如:在肺部结节术前定位,肺部肿块穿刺活检,肺部肿瘤立体定位放射治疗,颅内血肿定向穿刺,脑深部电刺激术,颅内肿瘤立体定位放射治疗,乳房肿块穿刺活检,乳房脓肿穿刺引流,肝脓肿穿刺引流,肝脏肿瘤射频消融,肾脏穿刺活检,骨科内固定器术中放置等中的应用。
本发明的第三个方面是提供一种靶位点的体内精确定位及处置方法,包括如下步骤:
步骤一,根据患者的断层影像学数据,利用计算机建模软件,构建患者的胸腔/腹腔以及相应脏器的数字模型,并在所述胸腔/腹腔以及相应脏器的数字模型上确定肺部肿块的三维位置;
步骤二,根据所述步骤一得到的胸腔/腹腔以及相应脏器的数字模型,再次利用计算机建模软件设计紧密贴合在所述胸腔/腹腔以及相应脏器的数字模型的胸腔或脏器表面的体内靶位点定位导板模型;并根据所述步骤一确定的靶位点的三维位置,在所述体内靶位点定位导板模型上设计定位角度辅助单元模型,所述定位角度辅助单元模型包括辅助通道,所述辅助通道的相对角度根据靶位点的三维位置、定位角度辅助单元模型的位置、涉及的重要脏器或组织的位置三者共同决定;
步骤三,将具有定位角度辅助单元模型的体内靶位点定位导板模型利用3D 打印技术打印成型,制得具有辅助通道的体内靶位点定位装置;
步骤四,将所述步骤三制得的体内靶位点定位装置通过术中微创切口安置于患者的胸腔或脏器表面的相应位置上,在定位角度辅助单元的辅助下,利用处置装置对靶位点进行相应的处置。
作为本发明的一个优选的技术方案,在所述的靶位点的体内精确定位及处置方法的步骤二中,所述体内靶位点定位导板模型的设计方法为:
a、在所述胸腔/腹腔以及相应脏器的数字模型上设计定位路径,所述定位路径为经过所述靶位点且距离胸腔或脏器表面的最短距离;沿所述定位路径在脏器表面上的点为穿刺点;并在所述胸腔/腹腔以及相应脏器的数字模型上以患者的胸腔或脏器表面标志为参考点,设计用于辅助所述体内靶位点定位装置正确放置和定位的解剖定位点;
b、以所述解剖定位点、定位路径和穿刺点为参考,利用计算机建模软件设计贴合在所述胸腔/腹腔以及相应脏器的数字模型表面的体内靶位点定位导板模型。
作为本发明的一个较为优选的技术方案,在所述的靶位点的体内精确定位及处置方法的步骤二中,所述定位角度辅助单元模型的辅助通道位于所述靶位点与所述穿刺点之间的所述定位路径上,所述定位路径是根据需要避开所述胸腔/腹腔以及相应脏器的数字模型的重要血管、神经、骨骼而设置的最短距离。
作为本发明的一个更为优选的技术方案,在所述的靶位点的体内精确定位及处置方法中,所述胸腔或脏器表面标志包括胸廓内面、肺尖、胸膜顶、胸膜底、横膈表面、肋骨、肋骨头关节、脊柱、胸主动脉中的至少两个。
作为本发明的一个优选的技术方案,在所述的靶位点的体内精确定位及处置方法的步骤一中,根据患者的断层影像学数据,在所述胸腔/腹腔以及相应脏器的数字模型上标记并计算靶位点的部位、大小、深度和个数。
作为本发明的一个优选的技术方案,在所述的靶位点的体内精确定位及处置方法中,所述胸腔/腹腔以及相应脏器的数字模型包括胸腔和具有靶位点的脏部或腑部的数字模型。
作为本发明的一个优选的技术方案,在所述的靶位点的体内精确定位及处置方法的步骤四中,将所述体内靶位点定位装置通过术中微创切口安置于患者胸腔内的脏器表面的相应位置时,在患侧肺萎陷的情况下进行;利用处置装置对靶位点进行相应的处置时,在患侧肺通气复张完全的情况下进行。
作为本发明的一个优选的技术方案,在所述的靶位点的体内精确定位及处置方法的步骤四中,所述处置装置为活检枪、定位针、放射源、电极膜片或采血针。
作为本发明的一个较为优选的技术方案,在所述的靶位点的体内精确定位及处置方法中,所述定位针为连接组装活检枪弹射部件或者一次性血糖采血针弹射部件。
作为本发明的一个优选的技术方案,在所述的靶位点的体内精确定位及处置方法中,所述计算机建模软件选自Mimics、Magics、Geomagic Studio、3Dmax、PROE、UG、AUTOCAD或SOLIDWORK。
本发明的第四个方面是提供一种靶位点的体外精确定位及处置方法,包括如下步骤:
步骤一,根据患者的断层影像学数据,利用计算机建模软件,构建患者体表形貌和骨性解剖结构的数字模型,并在所述体表形貌和骨性解剖结构的数字模型上确定肺部肿块的三维位置;
步骤二,根据所述步骤一得到的体表形貌和骨性解剖结构的数字模型,再次利用计算机建模软件设计紧密贴合在所述体表形貌和骨性解剖结构的数字模型的患者体表的体外靶位点定位导板模型;并根据所述步骤一确定的靶位点的三维位置,在所述体外靶位点定位导板模型上设计定位角度辅助单元模型,所述定位角度辅助单元模型包括辅助通道,所述辅助通道的相对角度根据靶位点的位置、定位角度辅助单元模型的位置、涉及的重要脏器或组织的位置三者共同决定;
步骤三,将具有定位角度辅助单元模型的体外靶位点定位导板模型利用3D打印技术打印成型,制得具有辅助通道的体外靶位点定位装置;
步骤四,将所述步骤三制得的体外靶位点定位装置安置于患者体表相应位置上,在定位角度辅助单元的辅助下,通过术中微创切口利用处置装置对靶位点进行相应的处置。
作为本发明的一个优选的技术方案,所述的靶位点的体外精确定位及处置方法的步骤二中,所述体外靶位点定位导板模型的设计方法为:
a、在所述体表形貌和骨性解剖结构的数字模型上设计定位路径,所述定位路径为经过所述靶位点且距离体表的最短距离;沿所述定位路径在体表上的点为穿刺点;并在所述体表形貌和骨性解剖结构的数字模型上以患者的体表标志为参考点,设计用于辅助所述体外靶位点定位装置正确放置和定位的解剖定位点;
b、以所述解剖定位点、定位路径和穿刺点为参考,利用计算机建模软件设计贴合在所述体表形貌和骨性解剖结构的数字模型表面的体外靶位点定位导板模型。
作为本发明的一个较为优选的技术方案,所述的靶位点的精确定位及处置方法的步骤二中,所述定位角度辅助单元模型的辅助通道位于所述靶位点与所述穿刺点之间的所述定位路径上,所述定位路径是根据需要避开所述体表形貌和骨性解剖结构的数字模型的重要血管、神经、骨骼而设置的最短距离。
作为本发明的一个更为优选的技术方案,所述的靶位点的体外精确定位及处置方法中,所述解剖定位点对应于患者的体表标志,所述体表标志胸廓表面、胸骨上窝、胸锁关节、胸骨角、胸骨体、剑突、前正中线、后正中线、棘突中的至少两个。
作为本发明的一个更为优选的技术方案,所述的靶位点的体外精确定位及处置方法中,所述体外靶位点定位装置的内表面上设有用于与所述体表标志相贴合的固定结构。
作为本发明的一个更为优选的技术方案,所述的靶位点的体外精确定位及处置方法中,所述固定结构为凸起状结构、凹陷状结构、线性镂空状结构和圆形镂空状结构中的至少一种。
作为本发明的一个优选的技术方案,所述的靶位点的体外精确定位及处置方法的步骤四中,所述处置装置为活检枪、定位针、放射源、电极膜片或采血针。
作为本发明的一个更为优选的技术方案,所述定位针为连接组装活检枪弹射部件或者一次性血糖采血针弹射部件。
作为本发明的一个优选的技术方案,所述的靶位点的体外精确定位及处置方法中,所述计算机建模软件选自Mimics、Magics、Geomagic Studio、3Dmax、PROE、UG、AUTOCAD或SOLIDWORK。
本发明的第五个方面是提供一种基于上述靶位点的体外精确定位及处置方法的肺部靶病灶定位/活检体外辅助装置,所述定位/活检辅助装置采用3D打印一体成型,其包括:
肺部靶病灶定位导板,所述肺部靶病灶定位导板为与躯体表面相贴合的三角形结构或蝶形结构,其上开设有若干对应于体表标志的凸起和/或镂空通孔;和
定位角度辅助单元,其由进针导轨、导轨接柱和消毒麻醉孔组成,所述导轨接柱为设置于所述肺部靶病灶定位导板上的圆柱形中空结构,所述消毒麻醉孔开设于所述导轨接柱与所述肺部靶病灶定位导板的连接部上,以及所述进针导轨为中空结构并可拆卸装配于所述导轨接柱上端,使得穿刺针可穿过所述进针导轨和导轨接柱形成的进针通道。
作为本发明的一个优选的技术方案,在所述的3D打印的肺部靶病灶定位/活检体外辅助装置上,所述镂空通孔包括位于所述肺部靶病灶定位导板的边框上且分别对应于躯体胸锁关节上缘连线、前正中线或后正中线的镂空线,和位于所述肺部靶病灶定位导板的一顶点位置对应于躯体剑突的圆形镂空;对应于躯体胸骨上凹的所述凸起设置于所述肺部靶病灶定位导板的另一顶点位置上。
作为本发明的一个优选的技术方案,在所述的3D打印的肺部靶病灶定位/活检体外辅助装置上,所述定位角度辅助单元设置于所述肺部靶病灶定位导板的水平延伸部上。
作为本发明的一个优选的技术方案,在所述的3D打印的肺部靶病灶定位/活检体外辅助装置上,所述消毒麻醉孔开设于所述导轨接柱侧面及底部周围并呈半月形开口状结构。
作为本发明的一个优选的技术方案,在所述的3D打印的肺部靶病灶定位/活检体外辅助装置上,所述进针导轨呈中空的螺栓状结构,所述进针导轨的下端可置入所述导轨接柱的中空腔体内;所述进针导轨上端的帽状结构防止其滑入所述导轨接柱的中空腔体内。
本发明的第六个方面是提供一种上述3D打印的肺部靶病灶定位/活检体外辅助装置的制备方法,包括如下步骤:
步骤一,根据预处理得到的具有靶病灶的CT影像序列,利用计算机建模软件,构建体表形貌和骨性解剖结构的数字模型,并在所述体表形貌和骨性解剖结构的数字模型上确定肺部靶病灶的三维位置;
步骤二,根据所述步骤一得到的体表形貌和骨性解剖结构的数字模型,再次利用计算机建模软件设计紧密贴合在所述体表形貌和骨性解剖结构的数字模型的患者体表的肺部靶病灶定位导板模型;并根据所述步骤一确定的肺部靶病灶的三维位置,在所述肺部靶病灶定位导板模型上设计定位角度辅助单元模型,所述定位角度辅助单元模型包括导轨接柱,所述导轨接柱的相对角度根据肺部靶病灶的位置、定位角度辅助单元模型的位置、涉及的重要脏器或组织的位置三者共同决定;
步骤三,由所述肺部靶病灶定位导板模型和定位角度辅助单元模型构成定位/活检辅助装置的数字模型,将所述定位/活检辅助装置的数字模型利用3D打印技术一体打印成型,制得具有辅助通道的定位/活检辅助装置。
作为本发明的一个优选的技术方案,在所述3D打印的肺部靶病灶定位/活检体外辅助装置的制备方法中,所述肺部靶病灶定位导板模型的设计方法为:
a、在所述体表形貌和骨性解剖结构的数字模型上设计定位路径,所述定位路径为经过所述靶位点且距离体表的最短距离;沿所述定位路径在体表上的点为穿刺点;并在所述体表形貌和骨性解剖结构的数字模型上以患者的体表标志为参考点,设计用于辅助所述体外靶位点定位装置正确放置和定位的解剖定位点;
b、以所述解剖定位点、定位路径和穿刺点为参考,利用计算机建模软件设计贴合在所述体表形貌和骨性解剖结构的数字模型表面的肺部靶病灶定位导板模型。
作为本发明的一个优选的技术方案,在所述3D打印的肺部靶病灶定位/活检体外辅助装置的制备方法中,沿所述定位路径在体表的穿刺点作为所述定位角度辅助单元模型的进针点,以所述进针点和所述靶病灶之间的连线为进针角度,以靶病灶中心到进所述针导轨上缘的距离为进针深度。
作为本发明的一个优选的技术方案,在所述3D打印的肺部靶病灶定位/活检体外辅助装置的制备方法的步骤二中,所述定位角度辅助单元模型的辅助通道位于所述靶位点与所述穿刺点之间的所述定位路径上,所述定位路径是根据需要避开所述体表形貌和骨性解剖结构的数字模型的重要血管、神经、骨骼而设置的最短距离。
作为本发明的一个优选的技术方案,在所述3D打印的肺部靶病灶定位/活检体外辅助装置的制备方法中,所述体表标志包括胸骨上凹、胸锁关节上缘连线、胸廓表面、胸骨上窝、胸锁关节、胸骨角、胸骨体、剑突、前正中线、后正中线、棘突中的至少两个。
作为本发明的一个优选的技术方案,在所述3D打印的肺部靶病灶定位/活检体外辅助装置的制备方法的步骤一中,计算机建模软件选自Mimics、Magics、Geomagic Studio、3Dmax、PROE、UG、AUTOCAD或SOLIDWORK。
作为本发明的一个优选的技术方案,在所述3D打印的肺部靶病灶定位/活检体外辅助装置的制备方法的步骤三中对定位/活检辅助装置的数字模型进行3D一体打印的材质选自ABS树脂、聚乳酸、聚乙烯醇和尼龙中的一种或几种。
本发明采用上述技术方案,与现有技术相比,具有如下技术效果:
本发明提供的靶位点的精确定位及处置方法,主要通过患者断层影像学数据个性化设计的靶位点定位装置实现靶位点的精确定位处置,主要用于术前定位、穿刺活检、立体辐射放疗领域中,使用范围广;具体地根据靶位点定位装置的不同,本发明的定位及处置方法可分为靶位点体内或体外精确定位及处置方法,可根据患者靶位点位置,个性化选择最适宜的定位及处置方法。更为具体地,本发明还提供了一种3D打印的肺部靶病灶定位/活检体外辅助装置是根据患者具有肺部肿块的CT影像序列和人体三维扫描仪获得的数据,利用3D打印技术制作个性化的肺部靶病灶定位/活检体外辅助装置,从而做到精确定位;避免了手触法无法触及结节;减少了患者CT的照射量,减轻辐射损害;3D打印根据患者数据量身定做,穿刺精确度提高,操作时间缩短,大大减轻患者痛苦;对患者配合度要求低,可适用于不能很好配合的患者;缩短操作人员的培训时间,有效利用了医疗资源。
附图说明
图1为本发明实施例腔镜术中胸腔内T型定位装置的结构示意图;
图2为本发明实施例腔镜术中胸腔内T型定位装置中竖直段上定位点的截面图;
图3为本发明实施例腔镜术中胸腔内T型定位装置的定位针的结构示意图;
图4为本发明实施例腔镜术中胸腔内T型定位装置的使用状态图;
图5为本发明实施例腔镜术中胸腔内L型定位装置的结构示意图;
图6为本发明实施例腔镜术中胸腔内L型定位装置中横段上定位部的截面图;
图7为本发明实施例腔镜术中胸腔内L型定位装置的定位针的结构示意图;
图8为本发明实施例腔镜术中胸腔内L型定位装置的使用状态图;
图9为本发明实施例腔镜术中V型带膜定位装置的结构示意图;
图10为本发明实施例腔镜术中V型带膜定位装置的局部放大示意图;
图11为本发明实施例腔镜术中V型带膜定位装置中定位点为细针结构的结构示意图;其中,11-a为定位点细节图;11-b为接口细节图;11-c为细针工作示意图;
图12为本发明实施例腔镜术中V型带膜定位装置中定位点为电凝点位点卡槽结构示意图;其中,12-a为俯视图;12-b为剖视图;
图13为本发明实施例肺部肿块体外辅助定位装置的整体结构图;
图14为本发明实施例肺部肿块体外辅助定位装置的使用状态图;
图15为本发明实施例三角形结构的肺部靶病灶定位/活检体外辅助装置的结构示意图;
图16为本发明实施例蝶形结构的肺部靶病灶定位/活检体外辅助装置的结构示意图;
图17为本发明实施例肺部靶病灶定位/活检体外辅助装置中定位角度辅助单元的结构示意图;
图18为本发明实施例肺部靶病灶定位/活检体外辅助装置的针道结构示意图;
图19为本发明实施例三角形结构的定位/活检辅助装置和体表形貌和骨性解剖结构的数字模型示意图;
图20为本发明应用实施例5中复查CT的穿刺效果对比示意图;
图21为本发明应用实施例6三角形结构的定位/活检辅助装置和体表形貌和骨性解剖结构的数字模型示意图;
图22为为本发明应用实施例6中复查CT的穿刺效果对比示意图;
图23为本发明应用实施例7蝶形结构的肺部靶病灶定位/活检体外辅助装置和体表形貌和骨性解剖结构的数字模型示意图。
具体实施方式
本发明的主要技术方案是提供一种靶位点的精确定位及处置方法,其根据患者的断层影像学数据,利用计算机辅助设计软件,构建患者解剖结构的数字模型;据此模型,个性化设计包括靶位点定位导板模型和定位角度辅助单元模型的靶位点定位装置模型,此靶位点定位装置模型紧密贴合患者体表或脏器表面,并根据靶位点的三维位置,个性化设计能够定位处置靶位点的定位位置和角度;然后利用3D打印成型靶位点定位装置,最后再采用所述靶位点定位装置对靶位点进行术前标记定位、穿刺活检以及其它手术中的操作等。
本发明中所述的靶位点是指:患者病灶、靶病灶、肺部肿块、肺结节或肺磨玻璃结节等发生病变的组织,以及包括患者未发生病变的组织或体内特定的组织结构位置,例如,需对患者体内的特定位置进行立体定向放射治疗时,通过本发明的定位处理方法将放射体安放在患者体内的特定位置。
本发明的靶位点的精确定位及处置方法,具体包括如下步骤:
步骤一,根据预处理得到的患者的断层影像学数据,利用计算机建模软件,构建患者的解剖结构的数字模型,并在所述解剖结构的数字模型上确定靶位点的三维位置;
步骤二,根据所述步骤一得到的解剖结构的数字模型,再次利用计算机建模软件个性化设计紧密贴合在所述解剖结构的数字模型的患者体表或脏器表面的靶位点定位导板模型;并根据所述步骤一确定的靶位点的三维位置,在所述靶位点定位导板模型上设计定位角度辅助单元模型,所述定位角度辅助单元模型包括辅助通道,所述辅助通道的相对角度根据靶位点的位置、定位角度辅助单元模型的位置、涉及的重要脏器或组织的位置三者共同决定;
步骤三,将具有定位角度辅助单元模型的靶位点定位导板模型利用3D打印技术打印成型,制得靶位点定位装置;
步骤四,将所述步骤三制得的靶位点定位装置安置于患者体表或脏器表面相应位置上,在定位角度辅助单元的辅助下,利用处置装置对靶位点进行相应的处置。
于上述技术方案的基础上,步骤二中靶位点定位导板模型的设计方法为:
a、在所述解剖结构的数字模型上设计定位路径,所述定位路径为经过所述靶位点且距离体表或脏器表面的最短距离;沿所述定位路径在体表或脏器表面上的点为穿刺点;并在所述解剖结构的数字模型上以患者的体表标志或脏器表面标志为参考点,设计用于辅助所述靶位点定位装置正确放置和定位的解剖定位点;
b、以解剖定位点、定位路径和穿刺点为参考,在所述解剖结构的数字模型表面刻画出靶位点定位板的轮廓;其中,所述轮廓的刻画可分为两种,第一种是当需要从体外对靶位点进行定位处置时,在所述解剖结构的数字模型的体表进行刻画;第二种是当需要从体内对靶位点进行定位处置时,而这种情况下,是在所述解剖结构的数字模型内的器官表面或体腔表面进行刻画;
c、在所述刻画的轮廓的基础上,利用计算机建模软件设计贴合在所述解剖结构的数字模型表面的靶位点定位导板模型。
于上述技术方案的基础上,所述定位角度辅助单元模型的辅助通道位于所述靶位点与所述穿刺点之间的所述定位路径上,所述定位路径是根据需要避开所述解剖结构的数字模型的血管、神经、骨骼而设置的最短距离;具体地,所述定位路径可以为直线形或曲线形或任何根据需要避开重要血管、神经、骨骼等重要组织结的路径。此外,在所述定位路径上形成包含所述辅助通道的标记处置通道,所述处置装置可通过所述标记处置通道对靶位点进行精准定位及处置。
于上述技术方案的基础上,在步骤二中,根据临床需求不同,在所述定位角度辅助单元模型上设置有用于配合所述处置装置定位的辅件机构。所述辅件机构包括固定架、消毒孔、导轨钢芯,如,在手术过程中可通过固定架按一定角度对所述处置装置进行限位,以使所述处置装置对所述靶位点进行精准定向处置;消毒孔开设于辅助通道附近用于对患者体表或脏器表面进行消毒处理,在手术过程中,将靶位点定位装置固定安置于患者体表或脏器表面相应位置上后,所述处置装置在定位角度辅助单元的辅助下,按照一定角度循着辅助通道穿过经消毒处理后的患者体表或脏器表面,精确到达靶位点附近,然后对靶位点进行相应的处置;此外,还可以通过导轨钢芯将所述处置装置通过包含所述辅助通道的标记处置通道送达靶位点附件,然后在体外控制所述处置装置对靶位点进行处置。
于上述技术方案的基础上,本发明中所述解剖结构的数字模型包括具有靶位点的头颈部、躯干部、上肢部或下肢部的数字模型。所述步骤一中,根据患者的断层影像学数据,在构建所述解剖结构的数字模型之前,在所述解剖结构的数字模型上标记并计算靶位点的部位、大小、深度和个数。
于上述技术方案的基础上,在所述的靶位点的精确定位及处置方法的步骤四中,所述处置装置为活检枪、定位针、放射源、电极膜片或采血针。优选地,所述定位针为连接组装活检枪弹射部件或者一次性血糖采血针弹射部件。
于上述技术方案的基础上,所述计算机建模软件选自Mimics、Magics、Geomagic Studio、3Dmax、PROE、UG、AUTOCAD或SOLIDWORK,或其它任何能够根据患者躯体或脏器或重要器官或组织的断层影像学数据构建躯体或脏器或重要器官或组织的数字模型的软件均可。
本发明靶位点的精确定位及处置方法适用范围广泛,如在术前定位、穿刺活检、立体辐射放疗领域中的应用;具体如在肺部结节术前定位,肺部肿块穿刺活检,肺部肿瘤立体定位放射治疗,颅内血肿定向穿刺,脑深部电刺激术,颅内肿瘤立体定位放射治疗,乳房肿块穿刺活检,乳房脓肿穿刺引流,肝脓肿穿刺引流,肝脏肿瘤射频消融,肾脏穿刺活检,骨科内固定器术中放置等的应用。
在本发明的靶位点定位及处置方法的技术方案中,根据靶位点定位操作位置的不同,可具体分为体内精确定位及处置方法或体外精确定位及处置方法。在对患者进行标记处置时,可根据患者靶位点位置,个性化选择最适宜的定位及处置方法。更为具体地,以针对肺部靶病灶的定位处置为例,可分为肺部靶病灶的体内精确定位及处置方法和肺部靶病灶体外精确定位处置两者定位及处置方法,相对而言,在对患者的肺部靶病灶进行标记处置时,采用体外精确定位处置比采用体内精确定位处置更为精准。
作为本发明的一种优选技术方案,本发明提供了一种靶位点的体内精确定位及处置方法,包括如下步骤:
步骤一,根据预处理得到的具有靶位点的CT影像序列,利用计算机建模软件,构建患者胸腔/腹腔以及相应脏器的数字模型,并在所述胸腔/腹腔以及相应脏器的数字模型上确定肺部肿块的三维位置;
步骤二,根据所述步骤一得到的胸腔/腹腔以及相应脏器的数字模型,再次利用计算机建模软件个性化设计紧密贴合在所述胸腔/腹腔以及相应脏器的数字模型的胸腔或脏器表面的体内靶位点定位导板模型;并根据所述步骤一确定的靶位点的三维位置,在所述体内靶位点定位导板模型上设计定位角度辅助单元模型,所述定位角度辅助单元模型包括辅助通道,所述辅助通道的相对角度根据靶位点的三维位置、定位角度辅助单元模型的位置、涉及的重要脏器或组织的位置三者共同决定;
步骤三,将具有定位角度辅助单元模型的体内靶位点定位导板模型利用3D打印技术打印成型,制得具有辅助通道的体内靶位点定位装置;
步骤四,将所述步骤三制得的体内靶位点定位装置通过术中微创切口安置于患者的胸腔或脏器表面的相应位置上,在定位角度辅助单元的辅助下,利用处置装置对靶位点进行相应的处置。
于上述技术方案的基础上,在所述的靶位点的体内精确定位及处置方法的步骤二中,所述肺部靶病灶定位导板模型的设计方法为:
a、在所述胸腔/腹腔以及相应脏器的数字模型上设计定位路径,所述定位路径为经过所述靶位点且距离胸腔或脏器表面的最短距离;沿所述定位路径在脏器表面上的点为穿刺点;并在所述胸腔/腹腔以及相应脏器的数字模型上以患者的胸腔或脏器表面标志为参考点,设计用于辅助所述体内靶位点定位装置正确放置和定位的解剖定位点;
b、以解剖定位点、定位路径和穿刺点为参考,在所述胸腔/腹腔以及相应脏器的数字模型内的器官表面刻画出体内靶位点定位板的轮廓;
c、在所述刻画的轮廓的基础上,利用计算机建模软件设计贴合在所述胸腔/腹腔以及相应脏器的数字模型表面的体内靶位点定位导板模型。
于上述技术方案的基础上,在所述的靶位点的体内精确定位及处置方法的步骤二中,所述定位角度辅助单元模型的辅助通道位于所述靶位点与所述穿刺点之间的所述定位路径上,所述定位路径是根据需要避开所述胸腔/腹腔以及相应脏器的数字模型的重要血管、神经、骨骼而设置的最短距离;具体地,所述定位路径可以为直线形,或曲线形或任何根据需要避开重要血管、神经、骨骼等重要组织结的路径。此外,在所述定位路径上形成包含所述辅助通道的标记处置通道,所述处置装置可通过所述标记处置通道对体内靶位点进行精准定位及处置。
于上述技术方案的基础上,在所述的靶位点的体内精确定位及处置方法中,所述胸腔或脏器表面标志包括胸锁关节上缘连线、胸廓内面、肺尖、胸膜顶、胸膜底、横膈表面、肋骨、肋骨头关节、脊柱、胸主动脉中的至少两个。
于上述技术方案的基础上,在所述的靶位点的体内精确定位及处置方法的步骤一中,根据患者的断层影像学数据,在所述胸腔/腹腔以及相应脏器的数字模型上标记并计算靶位点的部位、大小、深度和个数。
于上述技术方案的基础上,在所述的靶位点的体内精确定位及处置方法中,所述胸腔/腹腔以及相应脏器的数字模型包括胸腔和具有靶位点的脏部或腑部的数字模型。
于上述技术方案的基础上,在所述的靶位点的体内精确定位及处置方法的步骤四中,将所述体内靶位点定位装置通过术中微创切口安置于患者胸腔内的脏器表面的相应位置时,在患侧肺萎陷的情况下进行;利用处置装置对靶位点进行相应的处置时,在患侧肺通气复张完全的情况下进行。
于上述技术方案的基础上,在所述的靶位点的体内精确定位及处置方法的步骤四中,所述处置装置为活检枪、定位针、放射源、电极膜片或采血针。所述定位针为连接组装活检枪弹射部件或者一次性血糖采血针弹射部件。
于上述技术方案的基础上,在所述的靶位点的体内精确定位及处置方法中,所述计算机建模软件选自Mimics、Magics、Geomagic Studio、3Dmax、PROE、UG、AUTOCAD或SOLIDWORK,或其它任何能够根据患者躯体或脏器或重要器官或组织的断层影像学数据构建躯体或脏器或重要器官或组织的数字模型的软件均可。
作为本发明的另一种优选技术方案,本发明提供了还一种靶位点的体外精确定位及处置方法,包括如下步骤:
步骤一,根据预处理得到的具有靶位点的CT影像序列,利用计算机建模软件,构建患者体表形貌和骨性解剖结构的数字模型,并在所述体表形貌和骨性解剖结构的数字模型上确定靶位点的三维位置;
步骤二,根据所述步骤一得到的体表形貌和骨性解剖结构的数字模型,再次利用计算机建模软件个性化设计紧密贴合在所述体表形貌和骨性解剖结构的数字模型的患者体表的体外靶位点定位导板模型;并根据所述步骤一确定的靶位点的三维位置,在所述体外靶位点定位导板模型上设计定位角度辅助单元模型,所述定位角度辅助单元模型包括辅助通道,所述辅助通道的相对角度根据靶位点的位置、定位角度辅助单元模型的位置、涉及的重要脏器或组织的位置三者共同决定;
步骤三,将具有定位角度辅助单元模型的肺部靶病灶定位导板模型利用3D打印技术打印成型,制得具有辅助通道的体外肺部肿块定位装置;
步骤四,将所述步骤三制得的体外靶位点定位装置安置于患者体表相应位置上,在定位角度辅助单元的辅助下,通过术中微创切口利用处置装置对通过术中微创切口进行相应的处置。
于上述技术方案的基础上,所述的靶位点的体外精确定位及处置方法的步骤二中,所述体外靶位点定位导板模型的设计方法为:
a、在所述体表形貌和骨性解剖结构的数字模型上设计定位路径,所述定位路径为经过所述靶位点且距离体表的最短距离;沿所述定位路径在体表上的点为穿刺点;并在所述体表形貌和骨性解剖结构的数字模型上以患者的体表标志为参考点,设计用于辅助所述体外靶位点定位装置正确放置和定位的解剖定位点;
b、以解剖定位点、定位路径和穿刺点为参考,在所述体表形貌和骨性解剖结构的数字模型内的体表刻画出体外靶位点定位板的轮廓;
c、在所述刻画的轮廓的基础上,利用计算机建模软件设计贴合在所述体表形貌和骨性解剖结构的数字模型表面的体外靶位点定位导板模型。
于上述技术方案的基础上,所述的靶位点的体外精确定位及处置方法的步骤二中,所述定位角度辅助单元模型的辅助通道位于所述靶位点与所述穿刺点之间的所述定位路径上,所述定位路径是根据需要避开所述体表形貌和骨性解剖结构的数字模型的重要血管、神经、骨骼而设置的最短距离;具体地,所述定位路径可以为直线形,或为曲线形或任何根据需要避开重要血管、神经、骨骼等重要组织结的路径。此外,在所述定位路径上形成包含所述辅助通道的标记处置通道,所述处置装置可通过所述标记处置通道对靶位点进行精准定位及处置。
于上述技术方案的基础上,所述的靶位点的体外精确定位及处置方法中,所述解剖定位点对应于患者的体表标志,所述体表标志包括胸廓表面、胸骨上窝、胸锁关节、胸骨角、胸骨体、剑突、前正中线、后正中线、棘突中的至少两个。
于上述技术方案的基础上,所述的靶位点的体外精确定位及处置方法中,所述解剖定位点上设有用于与所述体表标志相贴合的固定结构。优选地,所述固定结构为凸起状结构、凹陷状结构、线性镂空状结构和圆形镂空状结构中的至少一种。
于上述技术方案的基础上,所述的靶位点的体外精确定位及处置方法的步骤四中,所述处置装置为活检枪、定位针、放射源、电极膜片或采血针。所述定位针为连接组装活检枪弹射部件或者一次性血糖采血针弹射部件。
作为一个优选的技术方案,所述的靶位点的体外精确定位及处置方法中,所述计算机建模软件选自Mimics、Magics、Geomagic Studio、3Dmax、PROE、UG、AUTOCAD或SOLIDWORK。或其它任何能够根据患者躯体或脏器或重要器官或组织的断层影像学数据构建躯体或脏器或重要器官或组织的数字模型的软件均可。
综上所述,本发明的靶位点的精确定位及处置方法,根据靶位点定位操作位置的不同,可具体分为体内精确定位及处置方法或体外精确定位及处置方法。更为具体地,针对不同的靶位点位置结合相应的体内胸腔或脏器表面或其他组织结构表面,本发明的体内精确定位及处置方法可分别衍生出相应的靶位点定位装置,如针对患者肺部肿块、肺磨玻璃结节的胸腔内T型定位装置、胸腔内L型定位装置、胸腔内V型带膜定位装置,或根据本发明定位及处置方法它衍生而来的其它定位处置装置;同理,本发明的体外精确定位及处置方法也分别衍生出了相应的靶位点定位装置,如针对患者肺部肿块、肺磨玻璃结节的八爪状结构体外辅助定位装置、三角形结构或蝶形结构体外辅助定位装置,或其根据本发明定位及处置方法它衍生而来其它定位处置装置,均在本发明靶位点的精确定位及处置方法的保护范围内。
下面通过具体实施例对本发明进行详细和具体的介绍,以使更好的理解本发明,但是下述实施例并不限制本发明范围。
实施例1 本实施例提供一种肺磨玻璃结节胸腔内腔镜术中T型定位方法,包括以下步骤:
步骤一,对患者的的胸部进行CT扫描,得到胸部断层数据,利用计算机建模软件对患者胸腔和具有肺部肿块的肺部进行电脑模型重建,并在胸腔和具有肺部肿块的肺部的数字模型上确定有肺磨玻璃结节的三维位置;
步骤二,根据所述步骤一得到的胸腔和具有肺部肿块的肺部的模型,再次利用计算机建模软件个性化设计紧密贴合在所述胸腔和具有肺部肿块的肺部的数字模型的胸腔表面的T型定位装置模型;并根据所述步骤一确定的肺磨玻璃结节的三维位置,在所述T型定位装置模型上设计定位角度辅助单元模型,所述定位角度辅助单元模型包括辅助通道,所述辅助通道的相对角度根据肺磨玻璃结节的三维位置、定位角度辅助单元模型的位置、涉及的重要脏器或组织的位置三者共同决定;
步骤三,采用3D打印技术根据三维重建的图像打印出具有辅助通道且符合患者胸腔特点的T型定位装置,所述T型定位装置的竖直段上设有根据定位片图像特别定位的处置装置;
步骤四,将T型定位装置适形地置入患者胸腔内,将横段的上表面于微创切口周围胸廓相贴合,横段的一端指向胸骨上窝,使T型定位装置固定在胸腔内,然后通过处置装置对肺磨玻璃结节处的胸膜表层进行标记处置。
在本实施例中,T型定位装置即为本发明的即体内肺部肿块定位装置,T型定位装置中的横段即为本发明中的靶位点定位板,竖直段即为本发明中的定位角度辅助单元。
在本实施例中,所述步骤一中CT扫描包括标记并计算患者肺部的肺磨玻璃结节的部位、大小、深度和个数。所述步骤二中,所述T型定位装置模型的设计方法为:
a、在所述胸腔/腹腔以及相应脏器的数字模型上设计定位路径,所述定位路径为经过所述肺部肿块且距离胸腔或脏器表面的最短距离;沿所述定位路径在脏器表面上的点为穿刺点,所述穿刺点的位置根据手术微创切口的位置而定;并在所述胸腔/腹腔以及相应脏器的数字模型上以患者的胸腔或脏器表面标志为参考点,设计用于辅助所述体内靶位点定位装置正确放置和定位的解剖定位点,所述解剖定位点对应于患者的微创切口周围胸廓表面、胸骨上窝;
b、以解剖定位点、定位路径和穿刺点为参考,在所述胸腔和具有肿块的肺部的数字模型内的器官表面刻画出T型定位装置模型的轮廓;
c、在所述刻画的轮廓的基础上,利用计算机建模软件设计贴合在所述胸腔和具有肿块的肺部的数字模型表面的T型定位装置模型。
在所述步骤二中,所述竖直段的辅助通道位于肺部肿块与所述穿刺点之间的所述定位路径上,所述定位路径是在手术医生的指导下根据需要避开所述胸腔和具有肿块的肺部的数字模型的重要血管、神经而设置的最短距离。步骤四中所述将T型定位装置适形地置入患者胸腔内在患侧肺萎陷的情况下进行,所述对肺磨玻璃结节处的胸膜表层进行标记定位在患侧通气复张完全的情况下进行,所述处置装置采用染色标记定位或电灼烧标记定位装置。
如图1所示,在本实施例中,所述T型定位装置为采用3D打印的包括横段101和竖直段102的“T”型结构,所述竖直段102上端与横段101的中部以角度α相交,所述竖直段102内设有与横段101表面相通的中空管道103,所述竖直段102的下端封闭且竖直段102上设有与中空管道103相连的处置装置;使用时,将T型定位装置适形地置入患者胸腔内并固定,通过处置装置对肺磨玻璃结节处进行标记。
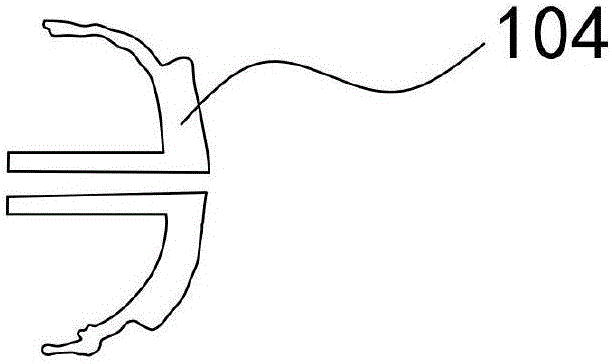
具体地,本实施例的T型定位装置是一种“T”形结构,可分为横段101和竖直段102,竖直段102内设有圆柱形中空管道103,外直径1-3cm,内直径0.5cm,长度依据患者胸腔三维重建模型、肺磨玻璃结节和手术微创切口的位置而设计,竖直段102上端连接接横段101的中部,竖直段102与横段101相交处的角度α是根据患者胸腔三维重建模型、肺磨玻璃结节和手术微创切口的位置而定;可根据患者肺磨玻璃结节(GGO)的部位在竖直段上的定位点104位置上制作处置装置,如图2所示,处置装置与竖直段102的中空管道103相连,处置装置可以是定位针105,如图3所示,定位针105外直径0.5mm,内直径0.4-0.45mm,长度1.5-2cm,定位针105的中空管道中加入医用显色剂,固定位置满意后将定位针105刺入肺磨玻璃结节对应投影的脏层胸膜即可染色定位,定位针105也可以设计为或连接组装活检枪弹射部件或者一次性血糖采血针弹射部件,可以通过扳机控制针座弹射系统将定位针刺入肺磨玻璃结节;处置装置也可以是电极膜片,在T型定位装置的中空管道中可放入电池或者电线,固定位置满意后可触发电流在肺磨玻璃结节对应投影的脏层胸膜上电灼烧标记定位;
在本实施例中,T型定位装置的横段101的上表面为长方形的弧形曲面,中间与竖直段102相连,相连处表面有孔,为竖直段102内的中空管道103出口,弧形曲面的具体形状依据患者在平卧位鼓肺时微创切口周围胸廓表面的三维重建模型设计。横段101两端为A、B端,A端在定位时指向胸骨上窝,如图1和图4所示。
本实施例的T型定位装置采用如下方法制备,包括以下步骤:步骤一,根据预处理得到的具有肺部肿块的定位片图像,利用建模软件对患者胸腔和具有肺部肿块的肺部进行模型重建,并在胸腔和肺部模型上标注肺磨玻璃结节的位置;步骤二,再次利用建模软件在胸腔和肺部模型上根据预设的微创切口构建贴合的“T”型结构模型,其包括横段和竖直段;步骤三,将“T”型结构模型导入打印机并进行3D打印,并在打印的竖直段上相应位置处安装与中空管道相连通的处置装置,制得T型定位装置,其中,所述处置装置为定位针或电极膜片。
其中,所述计算机建模软件选自Mimics、Magics、Geomagic Studio、3Dmax、PROE、UG、AUTOCAD或SOLIDWORK。所述步骤一定位片图像包括肺部的肺磨玻璃结节的部位、大小、深度和个数。步骤三中采用3D打印的横段和竖直段的夹角根据数字模型上的肺磨玻璃结节和将行手术微创切口的位置而定。所述步骤三中处置装置在竖直段上的位置根据数字模型中肺磨玻璃结节的部位在竖直段上的位置而定。打印材料可为ABS(ABS树脂,AcrylonitrileButadieneStyrene)、PLA(聚乳酸,PolyLacticAcid)和PVA(聚乙烯醇,Polyvinylalcohol)或Nylon(尼龙)等。
在使用本实施例的T型定位装置对肺磨玻璃结节进行胸腔定位时,患者在术前行胸部CT,标记并计算患者的肺磨玻璃结节(GGO)部位、大小、深度和个数;结合胸部CT,利用3D打印技术配套软件对患者的胸腔及具有肺磨玻璃结节(GGO)的肺部进行电脑数字模型重建,在电脑模型上确定肺磨玻璃结节(GGO),根据三维重建模型设计如上所述的T型定位装置;术中,患者麻醉后,在单肺通气情况下使患侧肺萎陷,通过胸腔镜手术切口将T型定位装置的竖直段通过微创切口置入胸腔内,贴合胸廓表面横段A端指向胸骨上窝,嘱麻醉师通气鼓肺,肺复张完全,“T”型的竖直段的定位装置即可在确定的位置定位,并在脏层胸膜标记,然后根据脏层胸膜标记,即可确定肺结节部位,用于腔镜下肺楔形切除术。
应用实施例1 实施例1的肺磨玻璃结节胸腔内腔镜术中T型定位方法的临床应用
一男性患者,60岁,身高172cm,体重63kg,体检时胸部CT发现右肺中叶外侧段水平裂下1.5cm,约平齐第6胸椎处,有一磨玻璃结节0.5*0.5cm,消炎治疗2周后随访,复查CT发现病灶未减小反而增大1*1cm,决定行胸腔镜下手术治疗,手术切口在右侧第4肋间隙与腋前线的交点处。根据患者的胸部CT图像,利用3Dmax对患者的胸腔及具有肺磨玻璃结节(GGO)的肺部进行电脑数字模型重建,在电脑模型上确定肺磨玻璃结节(GGO)位置,肺磨玻璃结节与手术切口的空间直线距离约为7cm,根据电脑三维重建的图像设计T型定位装置,然后采用3D打印技术打印成型,制得T型定位装置,T型定位装置是由PLA材料通过3D打印的方式制作。竖直段为圆柱形中空管道,外直径1-3cm,内直径0.5cm,长9cm,距离末端2cm处设有定位点,在横段贴合胸廓表面且A端指向胸骨上窝后,竖直段的定位点的方向指向肺磨玻璃结节的位置。定位点上有定位针,定位针外直径0.5mm,内直径0.4mm,定位针后连一胶管,胶管中装有亚甲蓝染料,胶管长0.6m,一端连定位针,可从T型定位装置的中空管道中伸入,在位置放入固定前,针头可收缩在横段的管腔中。T型定位装置的横段为正面图为长方形的弧形曲面,长15cm,宽4.5cm,弧形曲面的具体形状依据患者在平卧位鼓肺时微创切口周围胸廓表面的三维重建模型设计,可适形地贴合患者的胸廓表面。
在使用T型定位装置对患者的肺磨玻璃结节进行标记处置时,患者麻醉后单肺通气,取平卧位,于患者右侧第4、5肋间用手术刀划3cm刀口,使用腔镜器械建立手术通道,嘱麻醉师将患侧肺萎陷后,现将带有定位针同时装好亚甲蓝染料的胶管从定位器横段中间的小孔中放入,然后将定位器竖直段通过手术切口插入胸腔中,胶管的尾端位于胸部切口外。使T型定位装置的横段贴合胸廓表面,横段A端指向胸骨上窝,嘱麻醉师通气鼓肺,肺复张完全,恢复到三维重建模型的大小,此时将竖直段上的定位点与肺表面胸膜贴合的位置即为病灶标记点;最后,快速向胸腔内推送位于体外的胶管,使另一端的定位针刺出,刺入肺表面并注入染料,然后收回胶管,嘱咐麻醉师将肺萎陷,使用腔镜手术器械将定位器从切口处取出,定位结束。
实施例2 本实施例提供一种肺磨玻璃结节胸腔内腔镜术中L型定位方法,包括以下步骤:
步骤一,对患者的的胸部进行CT扫描,得到胸部断层数据,利用计算机建模软件对患者胸腔和具有肺部肿块的肺部进行电脑模型重建,并在胸腔和具有肺部肿块的肺部的数字模型上确定有肺磨玻璃结节的三维位置;
步骤二,根据所述步骤一得到的胸腔和具有肺部肿块的肺部的模型,再次利用计算机建模软件个性化设计紧密贴合在所述胸腔和具有肺部肿块的肺部的数字模型的胸腔表面的L型定位装置模型;并根据所述步骤一确定的肺磨玻璃结节的三维位置,在所述L型定位装置模型上设计定位角度辅助单元模型,所述定位角度辅助单元模型包括辅助通道,所述辅助通道的相对角度根据肺磨玻璃结节的三维位置、定位角度辅助单元模型的位置、涉及的重要脏器或组织的位置三者共同决定;
步骤三,采用3D打印技术根据三维重建的图像打印出符合患者胸腔特点的L型定位装置,所述L型定位装置上设有根据定位片图像定位的处置装置;
步骤四,将L型定位装置适形地置入患者胸腔内,通过所述处置装置对肺磨玻璃结节处的胸膜表层进行标记处置。
在本实施例中,L型定位装置即为本发明的即体内肺部肿块定位装置,L型定位装置中竖直段、弯角和横段组成本发明中的靶位点定位板和定位角度辅助单元,由中竖直段、弯角和横段形成的中空管道即为本发明中定位角度辅助单元的辅助通道,在中空管道的一端设有与肺结节位置相对应的处置装置。
在本实施例中,所述步骤一中,CT扫描包括标记并计算患者肺部的肺磨玻璃结节的部位、大小、深度和个数。所述步骤二中,所述L型定位装置模型的设计方法为:
a、在所述胸腔和具有肿块的肺部的数字模型上设计定位路径,所述定位路径为经过所述肺部肿块且距离胸腔或脏器表面的最短距离;沿所述定位路径在脏器表面上的点为穿刺点,所述穿刺点的位置根据手术微创切口的位置而定;并在所述胸腔/腹腔以及相应脏器的数字模型上以患者的胸腔或脏器表面标志为参考点,设计用于辅助所述体内靶位点定位装置正确放置和定位的解剖定位点,所述解剖定位点对应于患者的微创切口周围胸廓表面、胸骨上窝,所述中空管道形成的辅助通道位于所述定位路径上;
b、以解剖定位点、定位路径和穿刺点为参考,在所述胸腔和具有肿块的肺部的数字模型内的器官表面刻画出L型定位装置模型的轮廓;
c、在所述刻画的轮廓的基础上,利用计算机建模软件设计贴合在所述胸腔和具有肿块的肺部的数字模型表面的L型定位装置模型。
在所述步骤二中,所述中空管道形成的辅助通道位于肺部肿块与所述穿刺点之间的所述定位路径上,所述定位路径是在手术医生的指导下根据需要避开所述胸腔和具有肿块的肺部的数字模型的重要血管、神经而设置的最短距离。步骤四中所述将L型定位装置适形地置入患者胸腔内在患侧肺萎陷的情况下进行,所述对肺磨玻璃结节处的胸膜表层进行标记定位在患侧通气复张完全的情况下进行。以及步骤四中处置装置采用染色标记定位或电灼烧标记定位。
本实施例中的L型定位装置为采用3D打印的“L”型中空管道,包括竖直段、弯角和横段,竖直段顶部设有与患者胸顶面相贴合的头端,横段的末端封闭且横段上设有与中空管道相连的处置装置;使用时,将定位装置(即本发明的处置装置)适形地置入患者胸腔内并固定,在体外控制处置装置对肺磨玻璃结节处进行标记。
如图5-6所示,具体地,L型定位装置是一种“L”形结构,“L”型结构中有预先设计并打印的中空管道204,其横截面为环形,外直径1-3cm,内直径0.5cm。结构上可分为竖直段201、弯角和横段202,所述竖直段201、弯角和横段202内设有相互连通的中空管道204。该L型定位装置在功能上可分为固定部和定位部205,具体地,L型定位装置的竖直段201、弯角和横段202的圆柱体部为固定部;中空管道204和横段上的处置装置的位置为定位部205。
本实施例L型定位装置的竖直段201的顶部设有与患者胸顶面相贴合的头端203,头端203是根据患者肺三维重建模型的胸顶面形状设计,胸顶面为鼓肺时肺尖对应的位置,位于锁骨内侧段上方2-3cm处,头端203可在肺萎陷时适形的放入并贴合固定在胸顶面;竖直段201为圆柱形中空管道,外直径1-3cm,内直径0.5cm,长度依据患者胸腔三维重建模型设计,上接头端203,下接弯角;竖直段201可倚靠或平行于脊柱放置。
本实施例L型定位装置的弯角为连接结构,弯角中有预先设计并打印的中空管道204,其横截面为环形,外直径1-3cm,内直径0.5cm,上连竖直段201,下连横段202,弯角的弧度和角度依据患者肺部三维重建模型而设计。
本实施例L型定位装置的横段202中有预先设计并打印的中空管道204,该横段202的外直径1-3cm,内直径0.5cm,长度依据患者胸腔三维重建模型设计。横段202的前端连接弯角下端,横段202的末端封闭。可根据患者肺磨玻璃结节(GGO)的部位在横段202上设置定位点,在定位点上设置处置装置,处置装置与L型定位装置的中空管道204相连,处置装置可以是定位针206,如图7所示,定位针外直径0.5mm,内直径0.4-0.45mm,长度1.5-2cm,定位针中空管道中加入医用显色剂,固定位置满意后将定位针刺入肺磨玻璃结节对应投影的脏层胸膜即可染色定位,定位针也可以设计为或连接组装活检枪弹射部件或者一次性血糖采血针弹射部件,可以通过扳机控制针座弹射系统将定位针刺入肺磨玻璃结节。此外,处置装置可以是电极膜片,L型定位装置的中空管道204中可放入电池或者电线,固定位置满意后可触发电流使电极膜片在肺磨玻璃结节对应投影的脏层胸膜上电灼烧标记定位。
本实施例中的L型定位装置的制备方法,包括以下步骤:
步骤一,根据预处理得到的具有肺磨玻璃结节的胸部断层数据,利用建模软件对患者胸腔和具有肺部肿块的肺部进行模型重建,在胸腔和肺部模型上确定肺磨玻璃结节在体表的投影位置;
步骤二,根据预先计算的弯角弧度和角度,弯角的弧度根据数字模型中肺磨玻璃结节与胸顶面的位置而定;再次利用建模软件在上述胸腔和肺部模型上构建贴合的“L”型模型结构,其包括头端、竖直段、弯角和横段;
步骤三,将“L”型模型结构导入打印机并进行3D打印,在所打印的横段上安装与中空管道相连通的处置装置,制得L型定位装置,其中处置装置在横段上的位置根据数字模型中肺磨玻璃结节的部位在横段上的位置而定。
使用所述L型定位装置对肺磨玻璃结节进行胸腔定位时,患者在术前行胸部CT,标记并计算患者的肺磨玻璃结节(GGO)部位、大小、深度和个数;结合胸部CT,利用3D打印技术配套软件,如3Dmax、PROE、UG、AUTOCAD、SOLIDWORK等,对患者的胸腔及具有肺磨玻璃结节(GGO)的肺部进行电脑数字模型重建,在电脑模型上确定肺磨玻璃结节(GGO);然后再根据电脑三维重建的图像设计L型定位装置模型,并采用3D打印技术制作“L型定位装置”。
具体如图8所示,本实施例的L型定位装置的定位处置原理为:术前,患者在鼓肺状态下行胸部CT,利用3D打印技术配套软件对患者的胸腔及具有肺磨玻璃结节(GGO)的肺部进行电脑数字模型重建,在电脑模型上确定肺磨玻璃结节(GGO),根据三维重建模型设计符合患者的L型定位装置;术中,患者麻醉后,在单肺通气情况下使患侧肺萎陷,通过胸腔镜手术切口以旋转方式置入胸腔内,使L型定位装置的头端203贴合固定在肺间对应的位置,即贴合固定在胸顶面位置,或使竖直段201倚靠或平行于胸椎放置,将L型定位装置固定满意后,嘱麻醉师对患侧肺通气鼓肺,使肺复张完全,通过“L”型的横段202中的处置装置,所述处置装置如采用定位针206或电极膜片,即可在已确定的肺磨玻璃结节(GGO)位置或周边定位,并通过染色或电灼烧在脏层胸膜进行标记;根据脏层胸膜标记,即可确定肺结节部位,用于腔镜下肺楔形切除术。
应用实施例2 实施例2的肺磨玻璃结节胸腔内腔镜术中L型定位方法的临床应用
一女性患者,52岁,身高158cm,体重50kg,体检时胸部CT发现右肺中叶内侧段水平裂下1.5cm,约平齐第6胸椎处,有一磨玻璃结节0.5*0.5cm,消炎治疗2周后随访,复查CT发现病灶未减小反而增大1*1cm,决定行胸腔镜下手术治疗。根据患者的胸部CT图像,利用3Dmax对患者的胸腔及具有肺磨玻璃结节(GGO)的肺部进行电脑数字模型重建,在电脑模型上确定肺磨玻璃结节(GGO)位置,根据电脑三维重建的图像设计“L型定位器”,具体包括以下步骤:“L”型定位器是由PLA材料通过3D打印的方式制作。头端依据患者鼓肺时右肺上叶尖段的形状设计,体部长度为第1胸椎到第6胸椎的长度约为13cm,外直径1.5cm,内直径0.5cm;弯角为曲面,为90度直角,横段长8cm,定位点位于距离横段末端2cm处,定位点上有定位针,定位针外直径0.5mm,内直径0.4mm,定位针后连一胶管,胶管中装有亚甲蓝染料,胶管长0.6m,一端连定位针,可从“L”型定位器的中空管道中伸入,在位置放入固定前,针头可收缩在横段的管腔中。
使用所述L型带膜定位装置进行标记处置时,患者麻醉后单肺通气,取平卧位,于患者右侧第4、5肋间用手术刀划3cm刀口,使用腔镜器械建立手术通道,嘱麻醉师将患侧肺萎陷后,现将带有定位针同时装好亚甲蓝染料的胶管从定位器头端放入,然后将定位器通过旋转的方式放入胸腔中,胶管的尾端位于胸部切口外。利用腔镜器械使头端适形的贴住胸顶面,体部倚靠在胸椎上,头端对应第1胸椎,弯角处对应第6胸椎,横段末端指向胸骨;位置固定满意后嘱麻醉师鼓患侧肺,使恢复到三维重建模型的大小,此时将横段上的定位点与肺表面胸膜贴合的位置即为病灶标记点;快速向胸腔内推送位于体外的胶管,使另一端的定位针刺出,刺入肺表面并注入染料,然后收回胶管,嘱咐麻醉师将肺萎陷,使用腔镜手术器械将定位器从切口处取出,定位结束。
实施例3 本实施例提供一种肺磨玻璃结节胸腔内腔镜术中V型定位方法,包括以下步骤:
步骤一,对患者的的胸部进行CT扫描,得到胸部断层数据,根据肺部定位片图像,利用计算机建模软件对患者胸腔和具有肺部肿块的肺部进行电脑模型重建,并在胸腔和具有肺部肿块的肺部的数字模型上确定有肺磨玻璃结节的三维位置;
步骤二,根据所述步骤一得到的胸腔和具有肺部肿块的肺部的模型,再次利用计算机建模软件个性化设计紧密贴合在所述胸腔和具有肺部肿块的肺部的数字模型的胸腔表面的V型带膜定位装置模型;并根据所述步骤一确定的肺磨玻璃结节的三维位置,在所述V型带膜定位装置上设计定位角度辅助单元模型,所述定位角度辅助单元模型包括辅助通道,所述辅助通道的相对角度根据肺磨玻璃结节的三维位置、定位角度辅助单元模型的位置、涉及的重要脏器或组织的位置三者共同决定;
步骤三,采用3D打印技术根据三维重建的图像打印出符合患者胸腔特点的V型带膜定位装置,所述V型带膜定位装置上设有根据定位片图像特别定位的处置装置;
步骤四,术中令患侧肺萎陷,在单肺通气情况下将V型带膜定位装置收起,置入胸腔内使定位臂紧贴预定解剖结构后展开展开臂,微调位置直到固定满意;嘱麻醉师患肺通气鼓肺,肺复张完全后,V型带膜定位装置的膜部应可紧贴肺脏层胸膜上,通过处置装置(注入医用显色剂或按动电极片开关按钮),使得定位点在肺表面留下标记。根据标记,即可确定肺结节部位,用于腔镜下肺楔形切除术。
在本实施例中,V型带膜定位装置即为本发明的即体内肺部肿块定位装置,V型带膜定位装置中可展开设置的展开臂和定位臂组成本发明中的靶位点定位板,膜部即为本发明中的定位角度辅助单元,在所述膜部上一体设有与肺结节位置相对应的处置装置。
在本实施例中,所述步骤一中CT扫描包括标记并计算患者肺部的肺部肿块的部位、大小、深度和个数。所述步骤二中,所述V型带膜定位装置模型的设计方法为:
a、在所述胸腔和具有肿块的肺部的数字模型上设计定位路径,所述定位路径为经过所述肺部肿块且距离胸腔或脏器表面的最短距离;沿所述定位路径在脏器表面上的点为穿刺点,所述穿刺点的位置根据手术微创切口的位置而定;并在所述胸腔/腹腔以及相应脏器的数字模型上以患者的胸腔或脏器表面标志为参考点,设计用于辅助所述体内靶位点定位装置正确放置和定位的解剖定位点,所述解剖定位点对应于患者的微创切口周围胸廓表面、胸骨上窝,所述膜部上的细管形成的辅助通道位于所述定位路径上;
b、以解剖定位点、定位路径和穿刺点为参考,在所述胸腔和具有肿块的肺部的数字模型内的器官表面刻画出V型带膜定位装置模型的轮廓;
c、在所述刻画的轮廓的基础上,利用计算机建模软件设计贴合在所述胸腔和具有肿块的肺部的数字模型表面的V型带膜定位装置模型。
在所述步骤二中,由所述膜部上的细管形成的辅助通道,位于肺部肿块与所述穿刺点之间的所述定位路径上;所述定位路径在医生的指导下根据需要避开所述胸腔和具有肿块的肺部的数字模型的重要血管、神经设置。步骤四中所述将V型带膜定位装置适形地置入患者胸腔内在患侧肺萎陷的情况下进行,所述对肺部肿块处的胸膜表层进行标记定位在患侧通气复张完全的情况下进行。所述步骤四中处置装置采用染色标记定位或电灼烧标记定位。
如图9所示,本实施例中的V型带膜定位装置采用3D打印,其包括:展开臂301,展开臂301在胸腔内展开后可与胸郭内壁相贴合;定位臂302,其一端与展开臂301的一端通过铰链连接,构成可按一定角度开合的“V”型结构,定位臂302能够定位于胸郭内壁并与壁层胸膜紧密相贴;膜部303,设置于展开臂301和定位臂302之间,膜部303与展开臂301和定位臂302固定连接一体打印成型,膜部303展开后可与胸郭内壁和肺部表面相贴合;以及处置装置305,处置装置305设置于膜部303的表面上,用于对肺部肿块的位置进行标记。
为了更好的实现精准定位,如图10所示,定位臂302上与展开臂301铰接的一端设为圆钝形的勺状圆顶304,勺状圆顶304的形状与胸顶部的形状一致,胸顶部为鼓肺时肺尖对应的位置,展开臂301和定位臂302为弯曲状,其弯曲面与胸腔内表面一致。定位臂302上开设有收纳槽306,定位臂302与展开臂301的铰接点位于收纳槽306内。“V”型结构的开合角度为收纳槽边缘与定位臂表面形成的夹角,其中,展开臂与定位臂张开的角度α根据患者肺胸腔和肺部肿块的位置而设定。展开臂301和定位臂302之间通过“V”型的弹簧片307展开,“V”型弹簧片307的两端分别置于展开臂301上的第一凹槽308和定位臂上的第二凹槽309内。处置装置305可选为细针结构或电极膜片结构。本发明定位装置的材质选自ABS(ABS树脂)、PLA(聚乳酸)、PVA(聚乙烯醇)和Nylon(尼龙)中的一种或几种,其中,当处置装置305为电极膜片结构时,膜部303优选为耐热材料。
作为本发明的一个优选地方面,如图11所示,处置装置305为细针结构,该细针结构为3-5mm的细针3051,细针3051通过埋设与膜部303的细管3052经转接头3053与注射装置3054连接,注射装置3054为注射器,使用注射器向肺表面注射医用显色剂,优选的医用显色剂为美兰染液。此外,如图12所示,处置装置为也可以为电极膜片结构,电极膜片结构包括固定于膜部303上的卡槽3055和安装在卡槽3055内的电极片3056,该电极片3056通过电线3057与腔外的电极片开关连接,由电极片开关激发电极片3056从而在肺表面烫出标记。
具体地,本发明的展开臂301和定位臂302均是根据患者胸廓内形状利用3DMax软件三维制作而成,均与患侧胸廓内解剖结构紧密贴合。其中,展开臂301在胸腔内释放后与胸廓侧壁或者前臂的壁层胸膜表面紧密相贴;若患侧为右侧,则该定位臂302沿脊柱与肋骨的夹角与壁层胸膜紧密相贴,若患侧为左侧,则该定位臂302沿主动脉弓、脊柱与肋骨的夹角与壁层胸膜紧密相贴。
规定患者头侧为近端,患者尾侧为远端,定位臂302的近端为一圆钝的勺状圆顶304,该勺状圆顶304的具体形状依据三维数字模型中患者胸顶/肺尖的形状而设计,目的是当定位臂302与胸廓内结构贴合后,该顶点正好顶于胸顶部,保证了定位装置相对位置的稳定。
展开臂301和定位臂302相交于定位臂302近端上一点,由一铰链相连接,并可在一定角度内开合。当折叠时,展开臂301可部分重叠在定位臂302的收纳槽306内,方便将V型带膜定位装置收缩成长条形经微创手术刀口送入体腔内。展开臂301和定位臂302靠近铰链处分别设有第一凹槽308和第二凹槽309用以固定安放弹簧片307,该弹簧片307提供了V型带膜定位装置自动展开的动力。当定位臂302安放到位后,松开展开臂301,V型带膜定位装置便可自行展开。展开臂与定位臂张开的角度α即定位臂302收纳槽近端边缘与定位臂302表面形成的夹角,其大小根据数字模型的数据预先设定好,用以防止展开臂301过度展开。
展开臂301和定位臂302之间的部分为膜部303,其形状是根据数字数字模型上展开臂301和定位臂302夹角之间所包括的肺表面脏层胸膜的三维立体形状而设计,即该三角形薄膜能够紧密贴附在相对应区域的胸廓内壁和肺部表面。在膜部303与肺组织相贴的一面有处置装置305,该处置装置305的位置是肺内肿块于肺表面的垂直投影位置,该处置装置305的结构是3-5mm高的细针结构或电极片结构与耐热材料。若处置装置305为一细针结构,则在膜部303上同时设计一条细管3052埋于膜部303内,并有一转接头3053可与输液装置3054相连,如图11中11-a、11-b所示,通过与细管相连的注射装置向肺表面注射医用显色剂如图11中11-c所示。若处置装置305为电极片结构,则该点在打印材质上设置为耐热材料,并有一卡槽装置,如图12中12-a、12-b所示,可在术中将电刀的电极片3056拆下安装在该卡槽3055内,通过电线3057在腔外激发电极片3056从而在肺表面烫出标记。
本实施例中的V型带膜定位装置的制备方法,包括以下步骤:
步骤一,根据预处理得到的胸部CT数据,利用建模软件对患者胸腔和具有肿块的肺部进行模型重建,并在胸腔和肺部模型上标注肿块的位置;
步骤二,再次利用建模软件在上述胸腔和肺部模型内重建贴合的“V”型结构模型,其包括展开臂301、定位臂302和膜部303;
步骤三,将“V”型结构模型导入打印机并进行3D打印,并在打印的展开臂301和定位臂302之间安装弹簧片307、在膜部303的相应位置处安装处置装置305,制得V型带膜定位装置。
在所述制备方法中,步骤二中“V”型结构模型的展开臂301可与模型的胸郭内壁相贴合,“V”型结构模型的定位臂302可与模型的壁层胸膜紧密相贴,“V”型结构模型的膜部303可与模型的胸郭内壁和肺部表面相贴合。步骤三中处置装置305在膜部303上的位置为“V”型结构模型中肺部肿块的部位在膜部303表面的垂直投影位置。
本实施例的V型带膜定位装置的定位处置方法为:在腔镜术中令患侧肺萎陷,在单肺通气情况下将V型带膜定位装置收起,置入胸腔内使定位臂302紧贴预定解剖结构后展开展开臂301,微调位置直到固定满意;嘱麻醉师患肺通气鼓肺,肺复张完全后,V型带膜定位装置的膜部303应可紧贴肺脏层胸膜上,医师通过处置装置305注入医用显色剂或按动电极片开关按钮,使得处置装置305在肺表面留下标记;根据标记,即可确定肺结节部位,用于腔镜下肺楔形切除术。
应用实施例3 实施例3的肺磨玻璃结节胸腔内腔镜术中V型定位方法的临床应用
患者男性67岁,体检CT发现右肺上叶有磨玻璃结节影(GGO)一个。将CT影像数据导入计算机软件中,重建患者右肺和胸廓内表面数字数字模型。在数字数字模型上确定结节在肺表面的垂直投影。利用3DMax软件,根据三维数字模型所反映的患者胸顶、脊柱和右肺的解剖结构,绘制出定位臂302的三维数字模型,其中圆顶的上表面与胸顶相贴合、下表面与肺尖相贴合,长臂部与肺表面、脊柱和肋骨三者的夹角相贴合。定位臂302上预留有收纳槽、铰链孔和弹簧片卡槽。
类似地,用计算机建模软件沿肺数字数字模型的表面画出展开臂301,使得展开臂301和定位臂302中间覆盖的区域包括结节的肺表面投影。选中右肺数字数字模型的表面展开臂301和定位臂302之间的三角形区域,将该表面单独提取出来,将厚度增加到3mm,在穿刺点上用软件画一3mm长直径0.5mm的空心细针,并在膜内设计埋藏一条直径1mm的空心管道,在膜的边缘处设计一接口,方便与输液管道相连。将设计好的模型导入打印机驱动程序,将展开臂301和定位臂302的材料赋值为硬质塑料,膜部的主体和细管的材料赋值为硅胶,细针的材料赋值为硬质塑料。分别上机打印三部分原件。将打印好展开臂301插入定位臂302收纳槽的相应位置,安装不锈钢弹簧片后,将膜边缘部用胶水黏贴在两臂上。检查各部链接情况和牢固程度,确保没有产品缺陷后送供应室消毒包装备用。
手术开始后,从无菌包装中取出定位器。术中令患侧肺萎陷,先将定位器折叠收起,在单肺通气情况下经微创刀口送入胸腔内,使定位臂302紧贴预定解剖结构后,释放展开臂301是指展开到位,微调定位器位置直到固定满意。嘱麻醉师向患侧肺通气鼓肺,待肺复张完全后,定位器的膜部紧贴于肺脏层胸膜上,细针刺破脏胸膜表面。医师通过注射器注入少量美兰染液,使得定位点在肺表面留下蓝色标记。令患侧肺重新萎陷,检查肺表面标记情况。结合术前CT辅助估计标记准确情况。确认无误后根据标记,即可确定肺结节部位,于腔镜下对该部分肺组织行肺楔形切除术。
实施例4 本实施例提供一种基于3D打印的肺部肿块体外辅助定位方法,包括以下步骤:
步骤一,对患者的的胸部进行CT扫描,得到胸部断层数据,利用计算机建模软件重建患者的体表形貌和骨性解剖结构的数字模型,并在所述体表形貌和骨性解剖结构的数字模型上确定肺部肿块在患者体表的穿刺点;
步骤二,根据所述步骤一得到的体表形貌和骨性解剖结构的数字模型,再次利用计算机建模软件个性化设计紧密贴合在所述体表形貌和骨性解剖结构的数字模型的伞状结构定位板模型;并根据所述步骤一确定的肺部肿块的三维位置,在所述伞状结构定位板模型上设计中心定位模块模型,所述中心定位模块模型包括辅助通道,所述辅助通道的相对角度根据肺部肿块的位置、中心定位模块模型的位置、涉及的重要脏器或组织的位置三者共同决定,依此来设计定位针的进针角度和深度;
步骤三,将具有中心定位模块模型的伞状结构定位板模型利用3D打印技术打印成型,制得具有辅助通道的体外肺部肿块定位装置;
步骤四,将所述步骤三制得的体外肺部肿块定位装置安置于患者体表相应位置上,在中心定位模块的辅助下,利用处置装置对肺部肿块进行相应的处置。
在本实施例中,所述体外肺部肿块定位装置中,伞状结构定位板构成本发明中的靶位点定位板,中心定位模块构成本发明中的定位角度辅助单元,在所述中心定位模块上设有与肺部肿块位置相对应的处置装置。
在本实施例中,所述步骤一中CT扫描包括标记并计算患者肺部的肺部肿块的部位、大小、深度和个数。所述步骤二中,所述体外辅助定位装置模型的设计方法为:
a、在所述体表形貌和骨性解剖结构的数字模型上设计定位路径,所述定位路径为经过所述靶位点且距离体表的最短距离;沿所述定位路径在体表上的点为穿刺点;并在所述体表形貌和骨性解剖结构的数字模型上以患者的体表标志为参考点,设计用于辅助所述体外靶位点定位装置正确放置和定位的解剖定位点,所述解剖定位点对应于患者的体表标志;
b、以解剖定位点、定位路径和穿刺点为参考,在所述体表形貌和骨性解剖结构的数字模型内的体表刻画出肺部靶病灶定位导板的轮廓;
c、在所述刻画的轮廓的基础上,利用计算机建模软件设计贴合在所述体表形貌和骨性解剖结构的数字模型表面的肺部靶病灶定位导板模型。
在所述步骤二中,所述定位角度辅助单元模型的辅助通道位于用于定位的解剖定位点与所述穿刺点之间的所述定位路径上,所述定位路径是在医生的指导下根据需要避开所述体表形貌和骨性解剖结构的数字模型的重要血管、神经、骨骼而设置的最短距离。
本实施例的体外肺部肿块定位装置在使用时,将体外辅助定位装置的支脚攀附于相对应的患者体表标志位置,使体外辅助定位装置与患者胸廓紧密贴合且无局部应力/形变,固定于患者体表;安放到位后,中心定位模块所在方位即为穿刺针的进针部位,经中心定位模块上预留的进针孔道插入穿刺针,并以定位模块上的标记点为参照,根据预先计算的数据循进针孔道轨迹插入相应深度,使针尖到达肿块位置附近;经CT扫描以确认穿刺针位置良好,患者无明显并发症迹象后,手动释放hook-wire或者弹簧圈,拔出穿刺针,消毒包扎后完成穿刺定位;在腔镜术中,通过寻找hook-wire或弹簧圈的位置,便可确定病灶方位,精确切除病变组织。
如图13所示,本实施例提供了一种3D打印的肺部肿块体外辅助定位装置,所述定位装置采用3D打印,其整体呈伞状结构或“蜘蛛”状或章鱼状,包括:中心定位模块401,中心定位模块401内开设有进针孔道403,用于穿刺针404对肺部肿块进行标记时限制和稳定穿刺针404的进针方向;和支脚402,支脚402为弯曲状,其前端与中心定位模块401固定连接、末端向下弯曲与人体接触,支脚402为多个且可将中心定位模块401向上撑起,形成以支脚402为伞架、以中心定位模块401为顶部和以穿刺针404为伞杆的伞状结构。
在本实施例中,以多个支脚402组成的伞状结构为本发明中的靶位点定位板,中心定位模块即为本发明中的定位角度辅助单元。所述步骤一中CT扫描包括标记并计算患者肺部的肺部肿块的部位、大小、深度和个数。
如图14所示,支脚402的个数大于等于403个,优选的是支脚402的个数为4个;支脚402的末端为扁平状;支脚402的末端位于人体的体表标志位置,体表标志为胸骨上窝、胸骨角、剑突、第七颈椎、患侧胸壁第十二肋中的多个;中心定位模块401为圆柱形或立方体;中心定位模块401上设有用于使穿刺针404固定在进针孔道403内的夹紧装置;中心定位模块401与支脚402一体注塑成型。
实施例肺部肿块体外辅助定位装置的制备方法,包括以下步骤:
步骤一,根据预处理得到的具有肺部肿块的定位片图像,利用建模软件对患者胸腔和具有肿块的肺部进行模型重建,在胸腔和肺部模型上确定肺部肿块在体表的投影位置;
步骤二,根据预先计算的进针角度和深度,再次利用建模软件在上述胸腔和肺部模型上重建贴合的包括支脚402和中心定位模块401的伞状结构模型;
步骤三,将伞状结构模型导入打印机并进行3D打印,制得体外辅助定位装置。
在使用本实施例的体外辅助定位装置对肺部肿块进行标记处置时,将该体外辅助定位装置的支脚402按预先设定攀附于患者体表,嘱患者深吸气并屏气。由于该定位装置是根据患者胸廓外形个体化打印的,故当装置与患者胸廓紧密贴合且无局部应力/形变的情况下,说明患者体位正确,装置安装到位。安放到位后,中心定位模块401所在方位即为穿刺针404的进针部位。经中心定位模块401上预留的进针孔道403插入穿刺针404,并以穿刺针404上的标记点为参照,根据预先计算的数据和进针孔道403轨迹插入相应深度,使针尖到达肿块位置附近。如图14所示,并使用中心定位模块401夹紧装置夹紧固定进针孔道403内的穿刺针。然后,经CT证实穿刺针404针尖所处的位置良好,患者无明显并发症迹象后,手动释放hook-wire或者弹簧圈,拔出穿刺针404,消毒包扎后完成穿刺定位。在进行腔镜术的过程中,通过寻找hook-wire或弹簧圈的位置,便可确定病灶方位,精确切除病变组织。
应用实施例4 实施例4的基于3D打印的肺部肿块体外辅助定位方法的临床应用
男性患者一名,年龄65岁,体检CT发现右肺中叶有磨玻璃结节影一个。利用患者术前CT重建胸部数字数字模型。根据数字模型进行测量和设计,结节的体表投影位于右侧腋前线第4、5肋之间;以与患者胸廓相切的平面作为基准水平面,以体表穿刺点为原点,规定三维坐标系:其中x轴正方向大致由患者尾端指向患者头端,y轴正方向大致由患者背侧指向患者腹侧,z周正方向大致由患者内侧指向患者外侧。进针角度与x、y、z轴正方向缩成角度分别为41°、49°、7°,进针深度相对穿刺点为5cm。
利用3DMax软件绘制装置草图,装置五个触手贴附患者胸壁表面走行,宽1.5cm,高1cm;末端分别对应胸骨上窝、胸骨角、剑突、第七颈椎棘突和右侧第十二肋与脊柱的交角;5条支脚402汇聚于体表穿刺点亦即中心定位模块。中心定位模块为圆柱形,高3cm直径3cm,和5只支脚402相连成一体。中心定位模块自上表面到下表面有一直径21G预留贯通孔道,其角度与前述进针角度相同,下端对应结节体表穿刺点,上端为进针孔。将生成的三维数字模型导入打印机驱动程序,经过分层解析和内部结构计算后,用刚性透明硬质材料作为原料,用热熔融分层堆积的方法打印出成品模型。经医院供应室环氧乙烷消毒后,包装于无菌袋内备用。
在使用本实施例的体外辅助定位装置对肺部肿块进行标记处置时,患者平躺在CT机检查床上,充分暴露胸廓,右侧胸廓常规术前消毒。操作医生带无菌手套,将体外辅助定位装置从无菌袋内取出,将外辅助定位装置安置固定于患者右胸壁,支脚402放置于对应的人体体表标志位置;嘱患者深吸气后,由医生检查各体表标志对准良好,支脚不收异常应力影响,整个体外辅助定位装置能够严密贴附患侧胸廓。取穿刺针一根,医生操作前再次检查体外辅助定位装置的位置,并用触诊法确定中心定位模块有没有位于肋骨上方或肋骨下缘靠近血管神经处。循预留孔道角度缓缓插入穿刺针,直至预定进针深度。取下定位装置后先行CT检查,经检查确定确定穿刺针位置理想,无需任何调整,故释放弹簧圈,拔出穿刺针,常规消毒包扎。观察半小时无并发症表现后,将患者送回病房等待择期手术。
实施例5 相比前述的实施例1-4的定位处置方法,本实施例提供一种操作更加方便、定位更为精准的肺部靶病灶体外定位处置方法,包括以下步骤:
步骤一,根据预处理得到的具有肺部肿块的CT影像序列,利用计算机建模软件重建体表形貌和骨性解剖结构的数字模型,并在体表形貌和骨性解剖结构的数字模型上确定肺部肿块在体表的投影位置;
步骤二,根据所述步骤一得到的体表形貌和骨性解剖结构的数字模型,再次利用计算机建模软件个性化设计紧密贴合在所述体表形貌和骨性解剖结构的数字模型的三角形结构或蝶形结构定位板模型;并根据所述步骤一确定的肺部肿块的三维位置,在所述三角形结构或蝶形结构定位板模型上设计定位角度辅助单元模型,所述定位角度辅助单元模型包括辅助通道,所述辅助通道的相对角度根据肺部肿块的位置、定位角度辅助单元模型的位置、涉及的重要脏器或组织的位置三者共同决定,依此来设计定位针的进针角度和深度;在该体表形貌和骨性解剖结构的数字模型上,以胸骨上凹、胸锁关节上缘连线、前正中线、胸骨角和剑突为体表标志,循体表形貌起伏刻画出肺部靶病灶定位导板模型;由肺部靶病灶定位导板模型和定位角度辅助单元模型构成定位/活检辅助装置的数字模型;
步骤三,将上述步骤二建成的定位/活检辅助装置的数字模型导入打印机并进行3D一体打印成型,制得定位/活检辅助装置,即为本发明的靶位点定位板;
步骤四,将所述步骤三制得的定位/活检辅助装置安置于患者体表相应位置上,在定位角度辅助单元的辅助下,利用处置装置对肺部肿块进行相应的处置。
在本实施例中,所述体定位/活检辅助装置中,三角形结构或蝶形结构定位板即为本发明中的靶位点定位板,在所述中心定位模块上设有与肺部肿块位置相对应的处置装置。
在本实施例中,所述步骤一中CT扫描包括标记并计算患者肺部的肺部肿块的部位、大小、深度和个数。所述步骤二中,所述三角形结构或蝶形结构定位板模型的设计方法为:
a、在所述体表形貌和骨性解剖结构的数字模型上设计定位路径,所述定位路径为经过所述靶位点且距离体表的最短距离;沿所述定位路径在体表上的点为穿刺点;并在所述体表形貌和骨性解剖结构的数字模型上以患者的体表标志为参考点,设计用于辅助所述体外靶位点定位装置正确放置和定位的解剖定位点,所述解剖定位点对应于患者的体表标志,所述体表标志为胸骨上凹、胸锁关节上缘连线、前正中线、胸骨角和剑突;
b、以解剖定位点、定位路径和穿刺点为参考,在所述体表形貌和骨性解剖结构的数字模型内的体表刻画出肺部靶病灶定位导板的轮廓;
c、在所述刻画的轮廓的基础上,利用计算机建模软件设计贴合在所述体表形貌和骨性解剖结构的数字模型表面的所述三角形结构或蝶形结构定位板模型。在所述步骤二中,所述定位角度辅助单元模型的辅助通道位于用于定位的解剖定位点与所述穿刺点之间的所述定位路径上,所述定位路径在手术医生的指导下根据需要避开所述体表形貌和骨性解剖结构的数字模型的重要血管、神经、骨骼设置。
如图15-16所示,本实施例得到定位/活检辅助装置采用3D打印一体成型,其包括:肺部靶病灶定位导板506,肺部靶病灶定位导板506为与躯体表面相贴合的三角形结构或蝶形结构,其上开设有若干对应于体表标志的凸起501和/或镂空通孔,从整体结构上来看,三角形结构或蝶形结构的肺部靶病灶定位导板506整体呈弧面弯曲,以更好的贴合在躯体表面;和设置于肺部靶病灶定位导板506上的定位角度辅助单元507,如图17所示,其由进针导轨508、导轨接柱509和消毒麻醉孔5010组成,导轨接柱509为设置于肺部靶病灶定位导板506上的圆柱形中空结构,消毒麻醉孔5010开设于导轨接柱509与肺部靶病灶定位导板506的连接部上,以及进针导轨508为中空结构并可拆卸装配于导轨接柱509上端,使得穿刺针可穿过进针导轨508和导轨接柱509形成的辅助通道,即如图18所示的针道结构,穿刺针通过由辅助通道形成的模拟进针针道5014穿至目标病灶5013。
在实际应用时,根据肺内病灶位置的不同,穿刺针进入胸腔的途径有三种,即:后背进针、前胸壁进针和侧胸壁进针。对于第一种情况,穿刺时患者取侧卧位,本发明3D打印的肺部靶病灶定位/活检体外辅助装置采取蝶形(双翼)结构设计,如图16所示;对于后两种情况,穿刺时患者取仰卧位,3D打印的肺部靶病灶定位/活检体外辅助装置采取三角型(单翼)结构设计,如图15所示。这样的设计可以在保证肺部靶病灶定位导板506安放稳定性的基础上,在患者取侧卧位时最大限度利用前胸壁的体表标志,而在患者取仰卧位时不会因躯体压迫肺部靶病灶定位导板506导致形变和错位。
在本实施例中,镂空通孔包括位于肺部靶病灶定位导板506的边框上且分别对应胸锁关节上缘连线的镂空线502、对应前正中线和胸骨角水平线的十字形镂空线503和对应前正中线的镂空线504,和位于肺部靶病灶定位导板506的一顶点位置对应于躯体剑突的圆形镂空505,或对应后正中线(棘突连线)的镂空线5012;以及对应于躯体胸骨上凹的凸起501设置于肺部靶病灶定位导板506的另一顶点位置上。对应前正中线的镂空线504与对应前正中线和胸骨角水平线的十字形镂空线503分开是为了提高支架的强度,避免镂空线太长导致前部结构脆弱,对应前正中线和胸骨角水平线的十字形镂空线503由对应前正中线的竖直镂空线和对应胸骨角水平的水平镂空线组成。
如图15-16所示,定位角度辅助单元507设置于肺部靶病灶定位导板506向内侧的延伸部上,这样的设计可以在保证穿刺针进行穿刺时安放的稳定性。
如图17所示,进针导轨508呈中空的螺栓状结构,进针导轨508采用不锈钢材质,方便高温高压灭菌。进针导轨508的下端可伸入导轨接柱509的中空腔体内;进针导轨508上端的帽状结构防止其滑入导轨接柱509的中空腔体内,方便安装和取出。导轨接柱509角度按前述方法设计,与装置体部506相连并一次打印成型。此外,方便装置安放稳妥后局麻药物注射,消毒麻醉孔5010开设于导轨接柱509侧面及底部周围并呈半月形开口状结构。
在本实施例中,肺部靶病灶定位导板506上近定位角度辅助单元507的位置刻设有铭文5011,铭文5011为进针角度、深度以及患者信息等。
本发明还提供一种上述3D打印的肺部靶病灶定位/活检体外辅助装置的制备方法,其主要是利用患者入院时的CT影像资料,使用计算机软件重建患者体表形貌的数字模型和骨性解剖结构的数字模型。以胸骨上凹、胸锁关节上缘连线、前正中线、胸骨角和剑突为体表标志,循患者体表形貌起伏刻画出定位装置的数字模型。在避开重要血管、神经、骨骼后,以病灶在躯体表面的穿刺点为进针点,以两者之间的连线为进针角度,以病灶中心到装置进针导轨上缘的距离为进针深度,设计进针针道和导轨接柱,再次利用计算机建模软件在上述肺部靶病灶定位导板模型上重建贴合的定位角度辅助单元模型,由肺部靶病灶定位导板模型和定位角度辅助单元模型构成定位/活检辅助装置的数字模型。然后利用3D打印技术,打印出个性化的定位/活检辅助装置。具体包括如下步骤:
步骤一,根据预处理得到的具有肺部肿块的CT影像序列,利用计算机建模软件重建体表形貌和骨性解剖结构的数字模型,并在体表形貌和骨性解剖结构的数字模型上确定肺部肿块在体表的投影位置;
步骤二,在该体表形貌和骨性解剖结构的数字模型上,以胸骨上凹、胸锁关节上缘连线、前正中线、胸骨角和剑突为体表标志,循体表形貌起伏刻画出肺部靶病灶定位导板6模型;
步骤三,根据预先设计的进针角度和深度,再次利用计算机建模软件在上述肺部靶病灶定位导板506模型上重建贴合的定位角度辅助单元507模型,由肺部靶病灶定位导板506模型和定位角度辅助单元507模型构成定位/活检辅助装置的数字模型;
步骤四,将上述步骤三建成的定位/活检辅助装置的数字模型导入打印机并进行3D一体打印成型,制得定位/活检辅助装置。
在定位/活检辅助装置的制备方法中,步骤一中计算机建模软件选自Mimics、Magics、Geomagic Studio、3Dmax、PROE、UG、AUTOCAD或SOLIDWORK。步骤三中进针角度和深度的计算方法为:在避开重要血管、神经、骨骼后,以病灶在躯体表面的穿刺点为进针点,以进针点和病灶之间的连线为进针角度,以病灶中心到进针导轨508上缘的距离为进针深度。步骤四中对定位/活检辅助装置的数字模型进行3D一体打印的材质选自金属、ABS树脂、聚乳酸、聚乙烯醇和尼龙中的一种或几种。
本实施例的肺部靶病灶定位/活检体外辅助装置在使用时,将该定位/活检辅助装置的肺部靶病灶定位导板506按预先设定安放于患者体表,使各体表标志点和装置相应镂空/凸起对齐后,用医用胶带固定装置于患者胸廓。嘱患者深吸气并屏气。由于该肺部靶病灶定位导板506是根据患者胸廓外形一体化打印的,故当装置与患者胸廓紧密贴合且无局部应力/形变的情况下,说明患者体位正确,装置安装到位。安放到位后,通过消毒麻醉孔5010对穿刺部位进行酒精消毒,然后将经消毒处理后的进针导轨508装入导轨接柱509的中空腔体内,进针导轨508和导轨接柱509形成的中空的通道即为穿刺针的进针针道。经进针导轨508上预留的进针孔道插入穿刺针,并以穿刺针上的刻度为参照,根据预先计算的数据和进针孔道轨迹插入相应深度,使针尖到达肿块位置附近。
然后,经CT证实穿刺针针尖所处的位置良好,患者无明显并发症迹象后,手动释放hook-wire或者弹簧圈,拔出穿刺针,消毒包扎后完成穿刺定位。在进行腔镜术的过程中,通过寻找hook-wire或弹簧圈的位置,便可确定病灶方位,精确切除病变组织。
应用实施例5 实施例5中所述肺部靶病灶体外定位处置方法的临床应用
女性患者一名,年龄65岁,体检CT发现左肺有磨玻璃结节影一个,拟行穿刺定位。利用患者术前CT重建胸部数字数字模型,如图19所示。根据数字模型进行测量和设计,结节的体表投影位于左侧锁骨中线第4、5肋之间,拟从前胸壁进针。
利用3DMax软件绘制装置草图,三角形结构(单翼)的定位/活检辅助装置三边沿患者胸壁表面走行,宽3cm,厚0.3cm;其沿胸骨走行的一边分别按照解剖结构刻画出对应胸骨上窝、胸骨角、前正中线和剑突的定位凹陷和镂空线,定位角度辅助单元亦附着于此边;其余两边沿患者胸廓体表形貌走行,提高装置安放的稳定性。以病灶在躯体表面的穿刺点为进针点,以两者之间的连线为进针角度,以病灶中心到装置进针导轨上缘的距离为进针深度,设计进针针道和导轨接柱。全部设计完成后,生成三维数字模型文件。将生成的三维数字模型导入打印机驱动程序,经过分层解析和内部结构计算后,以尼龙粉末为原料,用热熔融分层堆积的方法打印出成品定位/活检辅助装置模型。将打印好的定位/活检辅助装置整体经医院供应室环氧乙烷消毒后,包装于无菌袋内备用,进针导轨使用高温高压灭菌后,包装于无菌袋内备用。
患者平躺在CT机检查床上,充分暴露胸廓,助手以记号笔刻画出患者胸骨上窝、胸骨角、前正中线和剑突的位置;将装置从无菌袋内取出,并在按记号对线对位安放,以弹力带固定于患者躯体上。由胸外科医生检查各定位点对准良好,装置各边不受异常应力影响,整个装置能够严密贴合患侧胸廓;胸外科医生核对患者信息,确认进针深度;经CT检查确定装置位置理想,无需任何调整。助手对拟穿刺区域行常规术前消毒,胸外科医生带无菌手套,取穿刺定位针一根,嘱患者深吸气后,循穿刺导轨上的预留孔道插入穿刺针至预定进针深度。释放定位钩,拔出穿刺针,常规消毒包扎。复查CT证实命中病灶。观察半小时无并发症表现后,将患者送回病房等待手术,如图20所示,复查CT确认进针路径准确,穿刺操作成功。
应用实施例6 实施例5中所述肺部靶病灶体外定位处置方法的临床应用
女性患者一名,年龄61岁,体检CT发现右肺有结节影二个,拟行穿刺定位。利用患者术前CT重建胸部数字数字模型,如图21所示。根据数字模型进行测量和设计,结节的体表投影分别位于右侧近腋前线第1、2肋之间和5、6肋之间,拟从前侧胸壁进针。
利用3DMax软件绘制装置草图,三角形(单翼)装置三边沿患者胸壁表面走行,宽3cm,厚0.3cm;其沿胸骨走行的一边分别按照解剖结构刻画出对应胸骨上窝、胸骨角、前正中线和剑突的定位凹陷和镂空线。其余两边沿患者胸廓体表形貌走行,定位角度辅助单元亦分别附着于此二边。以病灶在躯体表面的穿刺点为进针点,以两者之间的连线为进针角度,以病灶中心到装置进针导轨上缘的距离为进针深度,设计进针针道和导轨接柱。全部设计完成后,生成三维数字模型文件。将生成的三维数字模型导入打印机驱动程序,经过分层解析和内部结构计算后,以尼龙粉末为原料,用热熔融分层堆积的方法打印出成品定位/活检辅助装置模型。将打印好的定位/活检辅助装置整体经医院供应室环氧乙烷消毒后,包装于无菌袋内备用。进针导轨使用高温高压灭菌后,包装于无菌袋内备用。
患者平躺在CT机检查床上,充分暴露胸廓,助手以记号笔刻画出患者胸骨上窝、胸骨角、前正中线和剑突的位置。将装置从无菌袋内取出,并在按记号对线对位安放,以弹力带固定于患者躯体上。由胸外科医生检查各定位点对准良好,装置各边不受异常应力影响,整个装置能够严密贴合患侧胸廓。胸外科医生核对患者信息,确认进针深度。胸外科医生带无菌手套,取穿刺定位针一根,嘱患者深吸气后,循穿刺导轨上的预留孔道插入穿刺针至预定进针深度。释放定位钩,拔出穿刺针,常规消毒包扎。复查CT证实命中病灶。观察半小时无并发症表现后,将患者送回病房等待手术,如图22所示,复查CT确认进针路径准确,穿刺操作成功。
应用实施例7 实施例5中所述肺部靶病灶体外定位处置方法的临床应用
男性患者一名,年龄59岁,体检CT发现右肺阴影一个,拟行穿刺活检。利用患者术前CT重建胸部数字数字模型,如图23所示。根据数字模型进行测量和设计,肿块的体表投影位于右侧近肩胛下角线6、7肋之间,拟从后背进针。
利用3DMax软件绘制装置草图,蝶形(双翼)装置各边沿患者胸壁表面走行,宽3cm,厚0.3cm;其沿胸骨走行的一边分别按照解剖结构刻画出对应胸骨上窝、胸骨角、前正中线和剑突的定位凹陷和镂空线。其余各边沿患者胸廓体表形貌走行,定位角度辅助单元附着于背后走行靠上的一边。以病灶在躯体表面的穿刺点为进针点,以两者之间的连线为进针角度,以病灶中心到装置进针导轨上缘的距离为进针深度,设计进针针道和导轨接柱。全部设计完成后,生成三维数字模型文件。将生成的三维数字模型导入打印机驱动程序,经过分层解析和内部结构计算后,以尼龙粉末为原料,用热熔融分层堆积的方法打印出成品定位/活检辅助装置模型。将打印好的定位/活检辅助装置整体经医院供应室环氧乙烷消毒后,包装于无菌袋内备用。进针导轨使用高温高压灭菌后,包装于无菌袋内备用。
患者侧卧在CT机检查床上,充分暴露胸廓,助手以记号笔刻画出患者胸骨上窝、胸骨角、前正中线和剑突的位置。将装置从无菌袋内取出,并在按记号对线对位安放,以弹力带固定于患者躯体上。由胸外科医生检查各定位点对准良好,装置各边不受异常应力影响,整个装置能够严密贴合患侧胸廓。胸外科医生核对患者信息,确认进针深度。经CT检查确定装置位置理想,无需任何调整。助手对拟穿刺区域行常规术前消毒。胸外科医生带无菌手套,取穿刺活检针一根,嘱患者深吸气后,循穿刺导轨上的预留孔道插入穿刺针至预定进针深度。反复抽吸,取出少量组织送病理科检查。拔出穿刺针,常规消毒包扎观察半小时无并发症表现后,将患者送回病房等待手术。穿刺活检病理提示肺腺癌,与术中冰冻病理检查结果一致。
以上对本发明的具体实施例进行了详细描述,但其只是作为范例,本发明并不限制于以上描述的具体实施例。对于本领域技术人员而言,任何对本发明进行的等同修改和替代也都在本发明的范畴之中。因此,在不脱离本发明的精神和范围下所作的均等变换和修改,都应涵盖在本发明的范围内。
- 还没有人留言评论。精彩留言会获得点赞!