包含替莫唑胺的稳定的抗肿瘤药物组合物,以及该组合物的制备方法与流程
本发明涉及包含抗肿瘤试剂替莫唑胺的稳定的药物组合物及其制备和应用。
背景技术:
式1中的替莫唑胺(tmz),4-甲基-5-氧代-2,3,4,6,8-五氮杂双环[4.3.0]壬-2,7,9-三烯-9-甲酰胺
是一种抗肿瘤的烷化剂,其用于治疗脑部恶性神经胶质瘤黑色素瘤以及其它肿瘤疾病。tmz通过血脑屏障并且在cns中自发水解成活性化合物。
达卡巴嗪(dtic)是一种相似的药物,它只在肝脏中代谢,而且毒性高于替莫唑胺(tmz)。tmz和dtic都是前药,并且都形成同样的药理学活性化合物5-(3-二甲基-1三氮烯基)咪唑-4-甲酰胺(mtic)。5-氨基咪唑-4-甲酰胺(5-aminoimidazole-4-carboxamide)(aic)是在tmz和dtic组合物中都会形成的不需要的代谢副产物。tmz不需要代谢产生药理学活性化合物mtic,而dtic需要。
tmz组合物包含tmz与右旋糖苷磷酸根的钠盐混合物,相较于tmz,在制造时,aic的杂质含量高达0.3%,并且该含量在2年的储存期间增加至约0.5%。
除了口服给药以外,tmz能经鞘内给药,例如wo2006/060464a1中公开所述。
tmz能良好地渗透通过血脑屏障,但是半衰期却很短。在口服给药之后,tmz被迅速吸收,其在0.7小时后达到峰值血浆浓度,其半衰期为1.8小时。例如,为了在脑中能提供有效浓度的tmz,需要重复给药,这与患者的不适相关并且造成出现毒性作用的风险。
by11838c1揭示了一种针对恶性脑部肿瘤的联合治疗方法。该方法包括外科切除肿瘤组织后施用tmz,tmz包含ph为7.2-7.4的高度取代的右旋糖苷磷酸根凝胶。在制备时,tmz/高度取代右旋糖苷磷酸根的干重比为0.03:1.0。冻干的凝胶通过添加无菌水重建,在使用之前调整ph,然后用于伤口表面。在操作室中调整ph无法提供足够的精度,并且浪费时间。除此之外,高度取代的右旋糖苷磷酸根的结构包含大量的双取代和三取代的磷酸基团,这提供额外的大分子交联,使得对水的吸收能力降低,并将高度取代的右旋糖苷磷酸根凝胶中的tmz的量限制到30mg/g。组合物中的低浓度tmz意味着必须增加体积来给予更高剂量的物质,即前药tmz,高度取代的右旋糖苷磷酸根的给药量也因此增加。高度取代的右旋糖苷磷酸根的量的2倍或3倍的提高会导致与生物降解过程的持续时间相关的不良反应。此外,正如作者所确立的,tmz在ph为7.2-7.4的情况下分解,部分水解并形成超出关于tmz的许可水平的量的5-氨基咪唑-4-甲酰胺(aic)。
发明目的
已知组合物的一个问题是,在药物储存之后,其5-氨基咪唑-4-甲酰胺(aic)的含量增加超过0.5重量%的限值。
本发明寻求解决这个问题,并提供了一种稳定的、可重复生产的包含替莫唑胺的药物组合物,以及所述组合物的制备方法。
技术实现要素:
为此,本发明提供了一种稳定的抗肿瘤药物组合物,它包含替莫唑胺(tmz)以及盐形式与酸形式的多糖磷酸根的混合物或者基本上由替莫唑胺(tmz)以及盐形式与酸形式的多糖磷酸根的混合物组成。本组合物将ph维持在所需区间内,即4.5-7.0,因此不像现有技术所述的其他组合物,在制造制剂时不需要调剂ph。另一个非常重要的优点是组合物非常稳定,并且5-氨基咪唑-4-甲酰胺(aic)这种不需要的代谢物的量相比如今使用的组合物而言要低得多,并且在储存之后的量不会增加。
优选的制剂形式包括5-20重量%的tmz以及95-80重量%的盐形式与酸形式的多糖磷酸根混合物。
本发明还提供了一种稳定的抗肿瘤药物制剂,用于以水性凝胶的形式经鞘内给药。该组合物包含tmz以及盐形式和酸形式的多糖磷酸根混合物或者基本上由tmz以及盐形式和酸形式的多糖磷酸根混合物构成。盐形式:酸形式的多糖磷酸根的重量比约为1:0.4到5:1。在另一个实施方式中,盐形式:酸形式的多糖磷酸根的重量比是1:1到1:3。
优选地,多糖选自右旋糖苷,淀粉,半纤维素,纤维素以及它们的混合物。
最优选择是右旋糖苷。具体来说,右旋糖苷的分子量约为40kda至100kda之间。更优选分子量是60kda至70kda的右旋糖苷。
盐形式的多糖磷酸根选自钠盐,钾盐,铵盐,镁盐和钙盐,或者它们的混合物。钠盐是最优选的。
根据本发明的一个优选方面,组合物中tmz与总多糖磷酸根的重量比是1:4至1:19。具体的说,组合物中tmz与总多糖磷酸根的重量比约为1:9。
本发明的另一个目的还提供一种制备本发明组合物的第一方法,这个方法包括以下步骤:
a)提供tmz的水性溶液;
b)在tmz溶液中引入盐形式的高度取代的多糖磷酸根和酸形式的高度取代的多糖磷酸根的干燥混合物;
c)冷冻干燥步骤b)中所得溶液以获得沉淀物;
c)对组合物进行灭菌。
tmz的量优选为5-20重量%。
盐形式的多糖磷酸根和酸形式的多糖磷酸根的干燥混合物的量,其中,盐形式优选在30-80重量%的范围内,剩下的加和至100%的是酸形式。
可以用冷沉淀或者冻干来进行冷冻干燥。
灭菌可以通过任意合适的方法进行。优选地,通过辐照来灭菌。
本发明还提供了制备本发明组合物的第二方法,所述方法包含以下步骤:
a)提供盐形式的高度取代的多糖磷酸根以及酸形式的高度取代的多糖磷酸根的混合物;
b)通过添加水性溶剂从混合物形成水凝胶;
c)冷冻干燥所述凝胶;
d)向步骤c)中所得沉淀物添加粉状的tmz;
e)混合tmz粉末和沉淀物;
f)任选地,研磨tmz与沉淀物的混合物来形成粉状组合物;
g)任选地,将粉状组合物灭菌。
tmz的量优选为5-20重量%。
盐形式的多糖磷酸根和酸形式的多糖磷酸根的干燥混合物的量,其中,盐形式优选是30-80重量%,剩下的加和至100%的是酸形式。
可以用冷沉淀或者冻干来进行冷冻干燥。
灭菌可以通过任意合适的方法进行。优选地,通过辐照来灭菌。
用于实例中的水性溶剂是水,但也可以是其它药理学可接受的液体,例如盐水或磷酸盐缓冲液。
本发明的另一个目的是提供一种用于鞘内给药的水凝胶形式的药物制剂。所述水凝胶是通过把本发明的组合物与水性溶剂接触来形成的。水性溶剂可以是水,但也可以是其它药理学可接受的溶剂,例如也能使用盐水或磷酸盐缓冲液。
水凝胶是通过混合1重量份的上述组合物和10-30重量份的水性溶剂获得的。
水凝胶的一个优选实施方式是通过混合1重量份的上述组合物和10-15重量份的无菌水获得的。最优选的是一份组合物和15份无菌水。
上述制剂中aic含量低于0.5重量%或更低,具体的说是0.3重量%或0.1重量%或更低。
根据本发明的另一个优选方面,所述水凝胶基本上由盐形式的高度取代的多糖磷酸根,酸形式的高度取代的多糖磷酸根,tmz和水构成。aic的含量约为小于或等于0.01重量%的tmz。最优地,制剂不含可通过hplc检测得出的aic量。
所述制剂可以通过向用第一种方法获得的组合物添加水性溶剂来制备,也可以通过向用第二种方法获得的组合物添加水性溶剂来制备,两种方法已在之前描述。
还揭示了药物组合物/制剂以及通过使组合物和水性溶剂接触形成的水凝胶(即制剂)用于癌症治疗的应用。具体的说,该癌症位于脑部,例如脑部肿瘤;ii–iv级的恶性肿瘤,例如少突星形细胞瘤(oligoastrocytoma),渐变型星形细胞瘤,和胶质细胞瘤。
本发明提供了一种包含tmz的水凝胶,其中tmz的含量是0.5-5mg/ml。
最后,本发明提供了一种治疗癌症的方法,其中包含权利要求1中所定义的组合物的制剂以任何合适的给药途径给予对象。
方法能用于一线治疗或二线治疗或和其它方法联合使用。制剂也可以植入因肿瘤切除而留下的空腔中。
参考大量的优选实施方式,现在将描述本发明的更多细节。
附图说明
图1附图1a和1b展示了tmx聚合物组合物(a)以及本发明tmx组合物(b)的aic含量的杂质水平分析的hplc色谱图。
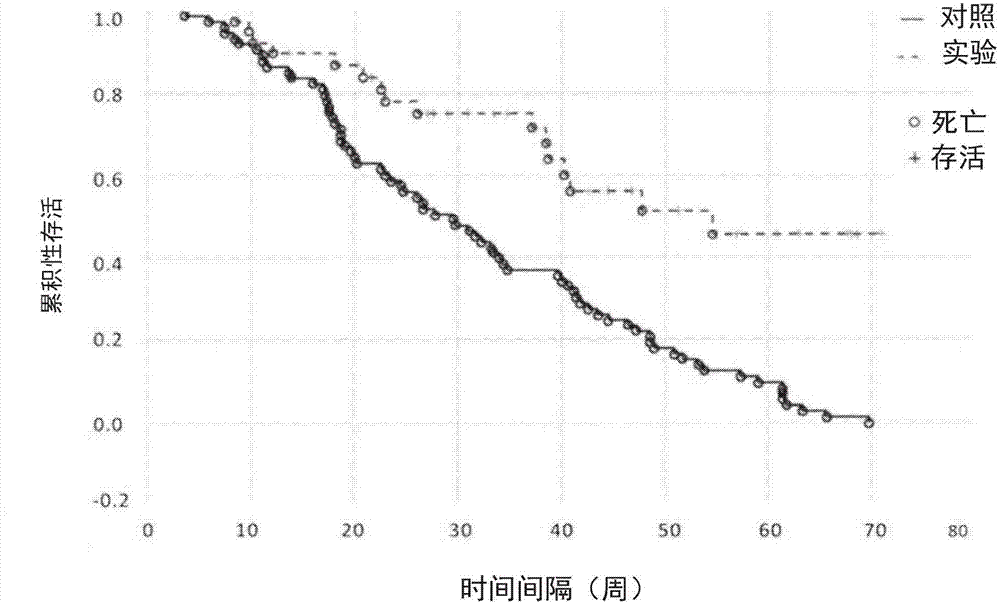
图2说明在ii-iv级脑部肿瘤完全切除后,使用本发明的组合物/制剂治疗的患者与对照组的术后存活情况。
图3说明使用本发明的组合物/制剂治疗的患者与对照组未复发脑部肿瘤的时间长短。
具体实施方式
应该理解本发明不局限于本文所揭示的特定构成,工艺步骤及材料,因为有时可对此类构成,工艺步骤及材料稍作改变。还应理解,本文所用术语的目的仅是描述具体实施方式,不用来构成限制,因为本发明的范围仅受所附权利要求书及其等价形式的限制。
本文引用的所有参考文献通过以不冲突的形式引用全文纳入本文以用于所有目的,就好像将各篇单独的出版物、专利或专利申请特定和单独地通过引用全文纳入本文用于所有目的一样。
最佳地,通过参考本文提供的下列定义、附图和示例性内容来理解本发明。
tmz在所述药物制剂中的最高含量(20质量%)是基于tmz在水中或其它药理学可接受溶剂中的溶解度来定义的,所述药理学可接受溶剂被添加用于制备凝胶形式的植入物。tmz的最低含量(5质量%)是由所述药物制剂的最低功效决定的。
所述药物制剂中所述盐形式的多糖磷酸根的含量(30-80质量%)和所述酸形式的多糖磷酸根的含量(加和至100质量%)是由5-氨基咪唑-4-甲酰胺氢氯化物(usp氨烯咪胺相关的化合物a)的含量增加所决定的,在经批准药物(tmz)质量的0.5%的限值内标准化。本药物制剂中氨烯咪胺相关的化合物a的含量低于0.5质量%,低至0.01重量%或者甚至无法用hplc检测出。
所述药物制剂的组分的质量比通过实验进行选择,主要根据抗肿瘤效果和储存稳定性,用以下指标来表示:“tmz的定量含量”,“氨烯咪胺相关的化合物a”,“吸水性”,“无菌性”。
实施例1-5包含替莫唑胺的高度取代的右旋糖苷磷酸根组合物的制造。
实施例1,100g通过任何已知方法获得的右旋糖苷磷酸根置于反应容器中,加入5l蒸馏水,搅拌混合物直到形成均匀的悬浮液。将10%的氢氧化钠溶液分批加入已获得的右旋糖苷磷酸根水悬浮液中,在每一批次加入后搅拌5分钟并测量ph。当反应介质的ph稳定在6.0-7.0时,不再添加10%氢氧化钠溶液。反应混合物然后在室温下放置30分钟并冻干。冻干产物中钠形式的右旋糖苷磷酸根的含量和酸形式的右旋糖苷磷酸根的含量分别为60重量%和40重量%。
添加10克替莫唑胺至90克的所得到的由盐形式和酸形式的右旋糖苷磷酸根混合物的冻干粉末中,充分搅拌干燥混合物,分成每份1克,装入任何合适的气密密封袋中,在0.5m拉德剂量的伽马射线下辐照灭菌。所得组合物包含10重量%的替莫唑胺,54重量%的盐形式的右旋糖苷磷酸根以及36重量%的酸形式的右旋糖苷磷酸根。
实施例2,80g通过任何已知方法获得的纤维素磷酸根置于反应容器中,加入5l蒸馏水,并搅拌混合物直到得到均匀的悬浮液。将10%的氢氧化钠溶液分批加入已获得的纤维素磷酸根的水悬浮液中,在每一批次加入后搅拌5分钟并测量ph。当反应介质的ph稳定在6.0-7.0时,不再添加10%氢氧化钠溶液。反应混合物然后在室温下放置30分钟并冻干。冻干产物中钠形式的纤维素磷酸根的含量和酸形式的纤维素磷酸根的含量分别为70重量%和30重量%。
添加20克替莫唑胺至80克所获得的由盐形式和酸形式的纤维素磷酸根混合物构成的冻干粉末中,充分搅拌干燥混合物,置于成型模具(formingmold)中,加压,所得片材置于塑料袋中,气密密封并在0.5m拉德剂量的伽马射线下辐照灭菌。所得制剂包含20重量%的替莫唑胺,56重量%的盐形式的纤维素磷酸根以及24重量%的酸形式的右旋糖苷磷酸根。
实施例3,100g通过任何已知方法获得的右旋糖苷磷酸根置于反应容器中,加入5l蒸馏水,以及搅拌混合物直到得到均匀悬浮液。将10%的氢氧化镁溶液分批加入已获得的右旋糖苷磷酸根水悬浮液中,在每一批次加入后搅拌5分钟并测量ph。当反应介质的ph稳定在6.0-7.0时,不再添加10%氢氧化镁溶液。反应混合物然后在室温下放置30分钟并冻干。冻干产物中镁形式右旋糖苷磷酸根的含量和酸形式的右旋糖苷磷酸根的含量分别为80重量%和20重量%。
添加5克替莫唑胺至95克所获得的由盐形式和酸形式的右旋糖苷磷酸根混合物构成的冻干粉末中,充分搅拌干燥混合物,分成每份1克,装入适当气密密封袋,在0.5m拉德剂量的伽马射线下辐照灭菌。所得制剂包含5重量%的替莫唑胺,76重量%的盐形式的右旋糖苷磷酸根以及19重量%的酸形式的右旋糖苷磷酸根。
实施例4,10g替莫唑胺溶解于3l无菌蒸馏水和90g包含60重量%盐形式的右旋糖苷磷酸根和40重量%酸形式的右旋糖苷磷酸根的混合物中。搅拌混合物,直到得到均匀混合物,然后冻干,充分搅拌干混合物,分成每份1克,装入任何适当气密密封袋,在0.5m拉德剂量的伽马射线下辐射灭菌。所得制剂包含10重量%的替莫唑胺,54重量%质量的盐形式的右旋糖苷磷酸根以及36重量%的酸形式的右旋糖苷磷酸根。
实施例5,药物制剂的制备
如实施例1中所述获得药物制剂,不同之处在于使用盐形式的淀粉磷酸根和酸形式的淀粉磷酸根。所述药物制剂的组成如表1所示。
用hplc确定替莫唑胺和aic的含量(分别参见图1a和1b)。通过以下方式制备溶液进行实验:0.2500g实验药物制剂加入到25ml容量瓶中,添加20ml二甲亚砜,混合物超声处理15分钟,用相同的溶剂调整体积至标线。
所得溶液过滤通过0.45μm孔径的滤膜。使用新鲜制得的溶液。
色谱条件:液相色谱的分光光度计检测器设为254nm,
填满粒度为5μm的十八烷基硅胶的250х4.6mm不锈钢柱用于色谱,例如,nucleodurc18gravity。
流动相速率为1ml/分钟。注入样品体积为10μl。
流动相:0.846g/l水性溶液,其中己烷磺酸钠:甲醇:冰醋酸的比例为895,5:100:4,5。
使用标准药物方法来确定所述药物制剂的无菌性。
为了检测吸收率,本发明的药物制剂的0.2g的样品放入50ml蒸馏水中,放置1小时。随后在玻璃过滤器上,从过量的液体分离水凝胶,并将水凝胶置于预先称重的重量瓶中,称重,并在323°k的真空烘箱中在磷的氧化物上干燥至恒定质量。基于溶胀和干燥样品间的质量差异来计算本发明的药物制剂的吸水能力。
通过上述任意方法获得的药物制剂可以用于鞘内注射,局部给药或者用于其它意图口服给药的药物制剂的生产。
实施例6-8口服剂型的生产
实施例6,将大约50mg通过实施例1-5中任一所述方法获得的药物制剂(计算为5mg替莫唑胺含量)与助剂混合,所述助剂是:乳糖-90mg,羧基甲基淀粉钠-7.5mg,胶态二氧化硅-0.2mg,酒酸(wineacid)-3.0mg。所得混合物经受湿法或干法制粒。所得颗粒填充于硬明胶胶囊中。药物意图以5mg的替莫唑胺的剂量用于口服。
example7.实施例7,将大约500mg通过实施例1-5中任一所述方法获得的药物制剂(计算为50mg替莫唑胺含量)与助剂混合,所述助剂是:55mg乳糖,15mg羧基甲基淀粉钠,10.0mg酒酸,14mg硬脂酸。所得混合物经受湿法或干法制粒,所得颗粒送去压制。该药丸用于口服剂量为50mg的替莫唑胺。
实施例8,将大约2,500mg(通过实施例1-5中任一所述方法获得的药物制剂(计算为250mg替莫唑胺含量)与助剂混合,所述助剂是:乳糖-180mg,羧基甲基淀粉钠-28mg,酒酸-20mg,并经受湿法制粒。该颗粒与硬脂酸钙(或镁)去灰(dust)并装入一次性包装中。该药物意图用于250mg替莫唑胺的一次性口服剂量。
所述抗肿瘤药物制剂的效力评估来自于41个患有恶性(ii-iv级)脑部肿瘤的患者(实验组)的临床情况。在操作室中,向所述包含10重量%替莫唑胺,54重量%钠形式的右旋糖苷磷酸根和36重量%酸形式的右旋糖苷磷酸根的1g药物制剂中加入15ml无菌水,静置20-30分钟,直到形成均匀的致密物。将所得物体植入切除肿瘤的空腔中。
图2和图3展示了研究成果。使用本文所揭示的抗肿瘤药物制剂导致患有恶性脑部肿瘤的患者的平均寿命的明显增加,并降低复发的风险。
表1展示了本发明的组合物在至少2.5年的储存中是稳定的,而且在储存过程中aic的量没有增加。测量了tmx和aic的含量,吸水量和无菌性,结果见下表1所示。
缩写:ps:多糖,ps盐:盐形式的多糖磷酸根,psp酸:酸形式的多糖磷酸,tmz:替莫唑胺,aic:5-氨基咪唑-4-甲酰胺,nd:无法测得。
- 还没有人留言评论。精彩留言会获得点赞!