一种经皮光动力药物5-氨基酮戊酸己酯盐酸盐醇质体及其制备方法和应用与流程
本发明属于经皮动力药物领域,特别涉及一种经皮光动力药物5-氨基酮戊酸己酯盐酸盐(hla)醇质体及其制备和应用。
背景技术:
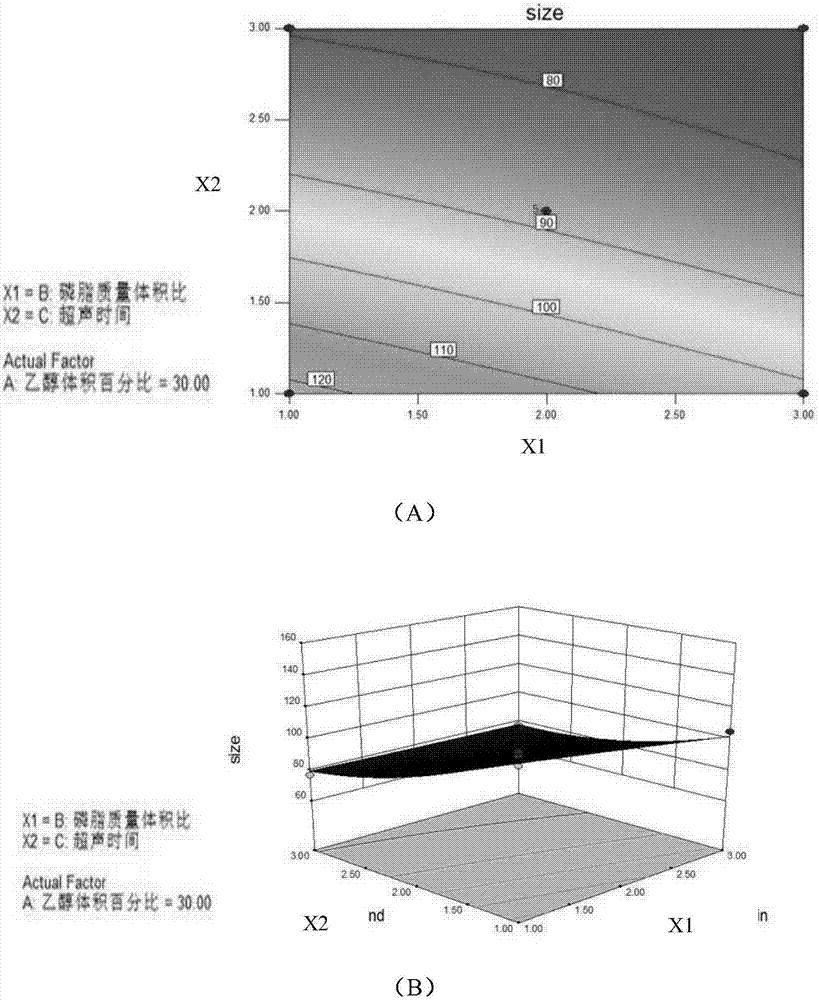
:5-氨基酮戊酸(5-ala)光动力治疗具有疗效好、选择性高、损伤小、副作用小、无明显刺激、耐受性好的优点,不易形成瘢痕,不影响重要组织器官的功能,易愈合,无耐药性,已成为一些皮肤病药物治疗的重要手段。5-氨基酮戊酸作用机制为药物经皮渗透进入皮肤后,经一系列酶促作用产生强光敏作用的原卟啉ix(ppⅸ)而发挥药效,但实际应用中,5-氨基酮戊酸存在以下问题:5-ala由于稳定性不佳而需现用现配;由于目前在临床上所用凝胶等剂型以及5-ala本身亲水性的性质,其经皮渗透性不够理想而需要长时间封包时间,也导致药物无法有效进入皮肤而严重影响临床治疗效果并造成大部分药物的浪费,以上问题已经严重到5-ala在皮肤光动力治疗上的临床应用。经皮药物传递系统,能避免肝脏首过效应、肝肾毒性、胃肠道反应,提高生物利用度。但经皮药物传递系统在实际应用中常遇到药物难以吸收或吸收缓慢的问题,对于大分子药物经皮吸收就更难,醇质体是具有脂质体双分子层结构的囊泡,首先由touitou提出,醇质体可包裹药物经皮渗透,制剂稳定、包封率高,更容易透过皮肤屏障,并且具有无毒、无刺激的优势,为经皮药物传递系统提供了新的研究方向,我们已成功建立新型皮肤药物载体-醇质体研发平台,通过前期研究已经掌握合成包括粒径、稳定性、包封率和载药量等均符合要求的多种载药醇质体制剂的制备和质量控制研究技术和方法,利多卡因醇质体、脂溶性罗丹明醇质体等也已充分证实醇质体可以有效促进药物渗透进入皮肤并具有较好的使用安全性。近年来,我们对新型速释型经皮给药载体做了研究和筛选,包括:纳米乳、聚乳酸(pla)等多聚物纳米粒和脂质固体纳米粒等。但是,在促进药物经皮渗透的同时,这些载体由于自身存有尚无法解决的不足和缺陷而难以获得实际应用,如:纳米乳制备所必须添加高浓度(≥30%)的表面活性剂可能会引发皮肤刺激性危害、某些多聚物成分就不同皮肤条件在安全性方面具有不确定性、固体脂质纳米粒稳定性差等。醇质体作为一种特殊类型的纳米级脂质体,我们对其制备工艺、质量控制、经皮机制和药物研发等方面进行了大量工作并确定一定研究成果,课题组前期研究中发现脂溶性罗丹明醇质体不仅能促进药物的快速经皮渗透,并且,在皮肤中的储留时间显著高于脂质体、酊剂等其它制剂,从而减少光敏性物质的系统性吸收,以实现皮肤给药的被动靶向和使用安全性。。醇质体的组分主要包括磷脂、短链醇和水等,相关研究显示它具有理想的理化特征,如:制备过程无需有机溶剂或去除醇,可简化常规脂质体制备所需的成膜和水化等工艺流程,也避免了有机溶剂挥发而造成的污染和危害;它对亲脂、亲水和两亲性药物均有很高的包封率,可以是常规脂质体的数倍,甚至高达88.2%;由于粒子的粒径小(﹤100nm),因此在包封率相同的条件下,载药量可为脂质体的6倍;可显著提高药物的生物利用度;动态光散射法结合电镜显示醇质体室温保存2年后的平均粒径、粒径分布及囊泡结构可维持不变,这也避免了一些其它类型脂质载体所存有的问题,如:固体脂质纳米粒在由不稳定脂质晶型向稳定晶型转变过程中,因晶体空间结构减少而导致其中包裹的药物被挤出载体,从而降低载药能力和稳定性等,因此,醇质体的理化特性非常符合理想速释型经皮载体的要求。因此,本发明5-氨基酮戊酸己酯盐酸盐的醇质体在医学应用上起着重要的作用。技术实现要素:本发明的首要目的在于提供一种5-氨基酮戊酸己酯盐酸盐醇质体。本发明另一目的在于提供上述醇质体的制备方法。本发明再一目的在于提供上述醇质体在制备诊断或/和治疗皮肤病、皮肤肿瘤的药剂中的应用。本发明所采取的技术方案是:一种5-氨基酮戊酸己酯盐酸盐醇质体,制备该醇质体的原料中含有0.4~0.6%w/v的5-氨基酮戊酸己酯盐酸盐、25~35%v/v的乙醇、1~3%w/v的大豆磷脂,余量为水。进一步的,5-氨基酮戊酸己酯盐酸盐醇质体,制备该醇质体的原料中含有0.5%w/v的5-氨基酮戊酸己酯盐酸盐、31.31%v/v的乙醇、3%w/v的大豆磷脂,余量为水。一种5-氨基酮戊酸己酯盐酸盐醇质体的制备方法,包括以下步骤:1)按上述任一所述的配方称取各原料;2)将大豆磷脂加入到乙醇中,搅拌制成醇相;3)将5-氨基酮戊酸己酯盐酸盐加入水中,搅拌制成水相;4)将醇相注入水相,搅拌得混合相;5)将混合相冰浴超声,过滤即得醇质体。进一步的,步骤2)、3)、4)中,反应在密封条件下进行。进一步的,步骤4)中,所述的搅拌的时间为4~6min,转速为600~800rpm。进一步的,步骤4)中,所述的注入速度为150~250μl/min。进一步的,步骤5)中,所述的超声功率为90~105w,超声4~6s,停2~3s;总超声时间为1~3min。进一步的,步骤5)中,所述过滤的孔径不超过0.22μm。进一步的,所制得的5-氨基酮戊酸己酯盐酸盐醇质体的粒径为70~90nm。进一步的,任一所述方法制备的5-氨基酮戊酸己酯盐酸盐醇质体在制备诊断或/和治疗皮肤病、皮肤肿瘤的药剂中的应用。进一步的,所述的皮肤病为银屑病、痤疮、尖锐湿疣、日光性角化;所述的皮肤相关肿瘤为基底细胞癌、基底细胞癌、鳞状细胞癌、bowen’s病、乳房外paget’s病。本发明的有益效果是:(1)制备过程不需要去除有机溶剂或醇,可简化常规脂质体制备所需的成膜和水化等工艺流程。(2)具有更好的稳定性、脂溶性和极性,尤其在皮肤中能以更低药量产生更充足的ppⅸ,从而大大减少药物使用量、减轻副作用的发生以及降低pdt治疗成本。附图说明图1:乙醇体积及大豆磷脂质量体积比对hla醇质体粒径的等高线(a)和响应面(b),注:size表示粒径;图2:大豆磷脂质量体积比及超声时间对hla醇质体粒径的等高线(a)和响应面(b),注:size表示粒径;图3:乙醇体积及超声时间对hla醇质体粒径的等高线(a)和响应面(b),注:size表示粒径;图4:本发明制备的0.5%hla醇质体外观图;图5:最优工艺条件的乙醇体积及磷脂质量体积比对hla醇质体粒径的等高线(a)和响应面(b);图6:本发明制备的0.5%hla醇质体的透射电镜图;图7:本发明制备的0.5%hla醇质体的粒径分布图;图8:不同时间的0.5%hla醇质体、0.5%ala水溶液、5%ala水溶液、空白醇质体对组织的影响;图9:0.5%hla醇质体、0.5%ala水溶液、5%ala水溶液经皮后平均荧光强度的柱状统计图。具体实施方式一种5-氨基酮戊酸己酯盐酸盐醇质体,制备该醇质体的原料中含有0.4~0.6%w/v的5-氨基酮戊酸己酯盐酸盐、25~35%v/v的乙醇、1~3%w/v的大豆磷脂,余量为水。优选的,5-氨基酮戊酸己酯盐酸盐醇质体,制备该醇质体的原料中含有0.5%w/v的5-氨基酮戊酸己酯盐酸盐、31.31%v/v的乙醇、3%w/v的大豆磷脂,余量为水。一种5-氨基酮戊酸己酯盐酸盐醇质体的制备方法,包括以下步骤:1)按上述任一所述的配方称取各原料;2)将大豆磷脂加入到乙醇中,搅拌制成醇相;3)将5-氨基酮戊酸己酯盐酸盐加入水中,搅拌制成水相;4)将醇相注入水相,搅拌得混合相;5)将混合相冰浴超声,过滤即得醇质体。优选的,步骤2)、3)、4)中,反应在密封条件下进行。优选的,步骤4)中,所述的搅拌的时间为4~6min,转速为600~800rpm。优选的,步骤4)中,所述的注入速度为150~250μl/min。优选的,步骤5)中,所述的超声功率为90~105w,超声4~6s,停2~3s;总超声时间为1~3min。优选的,步骤5)中,所述过滤的孔径不超过0.22μm。优选的,所制得的5-氨基酮戊酸己酯盐酸盐醇质体的粒径为70~90nm。优选的,任一所述方法制备的5-氨基酮戊酸己酯盐酸盐醇质体在制备诊断或/和治疗皮肤病、皮肤肿瘤的药剂中的应用。优选的,所述的皮肤病为银屑病、痤疮、尖锐湿疣、日光性角化;所述的皮肤相关肿瘤为基底细胞癌、基底细胞癌、鳞状细胞癌、bowen’s病、乳房外paget’s病。下面结合具体实施例对本发明作进一步的说明。实施例15-氨基酮戊酸己酯盐酸盐醇质体的制备表15-氨基酮戊酸己酯盐酸盐醇质体的配方制备方法:1)按以上表1配方称取各原料;2)将大豆磷脂加入到乙醇中,置于密封的玻璃瓶中,恒温磁力搅拌使其溶解,直至形成均匀的淡黄色透明液体,制成醇相。3)将5-氨基酮戊酸己酯盐酸盐加入到水中,置于密封的玻璃瓶,恒温磁力搅拌器,搅拌溶解,制成水相。4)密封条件下细流缓慢将醇相注入水相中(200μl/min),再搅拌5min,磁力搅拌器稳定维持700rpm的转速。5)冰浴条件下使用超声细胞粉碎仪超声,其中超声功率比为15%(大约97.5w),超声5s,停止3s,总超声时间为3min,之后用0.22μm微孔滤膜滤过,收集滤液即得醇质体,4℃密封保存。实施例25-氨基酮戊酸己酯盐酸盐醇质体制备工艺的优化1.最优工艺的设置与选择5-氨基酮戊酸己酯盐酸盐(hla)醇质体最优工艺的选择以hla醇质体粒径为筛选指标,采用designexpert8.0.6软件对各个因素(见表2,表2中未提到的参数条件与实施例1相同)的各个水平进行分析,确定最优工艺的条件。确定粒径为效应值,采用box-behnken设计(表3)优选hla醇质体的制备工艺。粒径分布的测定方法:将hla醇质体倒入测试杯中,直接采用动态光散射以90度散射角测量颗粒和分子粒度,采用zetasizernanos90测定hla醇质体的粒径及分散系数。1.1效应面实验因素水平设计表2box-behnken实验设计的因素和水平1.2box-benknken实验设计与结果表3box-behnken实验设计与结果a:乙醇体积分数(%)b:大豆磷脂质量分数(%)c:超声时间(min)y1:粒径(nm)结果:根据表2、表3的结果,由软件design-expert8.0.6分析,得到粒径的回归方程:y1=88.18-14.82a-5.65b-16.84c+1.11ab+13.26ac+4.68bc+10.77a2+0.25b2+7.14c2。1.3回归模型方差分析表4各因素对效应值影响的方差分析注:*表示有显著影响。结果:结合表4得出,a、b、c三个因素及其相互作用对于hla醇质体粒径的影响中,一次项中的a(乙醇体积分数)、b(大豆磷脂质量体积比)、c(超声时间),二次项ab、ac、bc、c2对粒径的影响有显著意义(见图1、图2和图3)。根据曲面图和上述的回归方程得出的最优处方条件分别是:乙醇体积分数为31.31%,大豆磷脂质量体积比为3%,超声时间为2.61min。0.5%醇质体的外观图如图4。最优处方用归一值(desirability)来进行评价,归一值是依据分配到每个效应值的重要程度来确定,因此归一值是评价最优处方的合理指标。同时,归一值的取值越接近1,表明预测值越接近目标值,取值为0时,表明预测值已经超出取值范围限制,取值为1时,预测值与目标值完全一致。本发明在筛选最优工艺的方案中归一值的取值为0.994,即预测值接近目标值。因此采用design-expert软件得到的拟合方程筛选发现:0.5%hla醇质体的最优制备工艺具有可靠性和有效性(图5)。实施例35-氨基酮戊酸己酯盐酸盐醇质体的制备表55-氨基酮戊酸己酯盐酸盐醇质体的配方制备方法:1)按以上表5配方称取各原料;2)将大豆磷脂加入到乙醇中,置于密封的玻璃瓶中,恒温磁力搅拌使其溶解,直至形成均匀的淡黄色透明液体,制成醇相。3)将5-氨基酮戊酸己酯盐酸盐加入到水中,置于密封的玻璃瓶,恒温磁力搅拌器,搅拌溶解,制成水相。4)密封条件下细流缓慢将醇相注入水相中(200μl/min),再搅拌5min,磁力搅拌器稳定维持700rpm的转速。5)冰浴条件下使用超声细胞粉碎仪超声,其中超声功率比为15%(大约97.5w),超声5s,停止3s,总超声时间为2.61min,之用0.22μm微孔滤膜滤过,收集滤液即得醇质体,4℃密封保存。下面对本实施例制备的5-氨基酮戊酸己酯盐酸盐醇质体作进一步的效果检测。一、透射电镜观察5-氨基酮戊酸己酯盐酸盐醇质体(hla)的微观形态方法:吸取一滴实施例3制备的0.5%w/vhla醇质体滴于碳膜铜网上,2min后从铜网边缘用滤纸吸去多余液体;再轻轻滴加一滴磷钨酸(3%,ph7.0)于铜网,2min后从铜网边缘用滤纸吸去多余染液,待自然晾干,在80kv加速电压下观察0.5%w/vhla醇质体的粒子形态,并进行统计。结果:图6为本发明0.5%hla醇质体投射电镜图,从中可以看出hla醇质体的粒径约70-90nm,粒径较均一。二、5-氨基酮戊酸己酯盐酸盐醇质体分粒径分布检测方法:将实施例3制备的2ml0.5%hla醇质体倒入测试杯中,直接采用动态光散射以90度散射角测量颗粒和分子粒度,采用zetasizernanos90测定hla醇质体的粒径及分散系数。结果:测定0.5%hla醇质体分粒径为80.87±1.82nm(结果见表6),分散系数0.31±0.032,与响应面预测的结果相符(图7)。表6hla醇质体粒径的实测值和预测值因变量预测值实测值(n=3)预测误差(%)粒径77.282580.87333±1.8366674.6predictederror(%)=|predictedvalue-actualvalue|/predictedvalue×100%预测误差=|预测值-实测者|/预测值×100%三、载药率的测定方法:1.标准曲线的建立对照品的制备:称取5-氨基酮戊酸己酯盐酸盐(hla)对照品10mg,置于10ml容量瓶中,加入蒸馏水稀释至刻度,超声震荡,即得1mg/ml的hla对照品储备液。分别量取适量的hla储备液于10ml量瓶中,加水定容,摇匀,配制成浓度为0.003,0.006,0.03,0.06,0.3,0.6mg/ml的系列对照品溶液,按上述色谱条件次进样20μl,记录峰面积。以峰面积(a)为纵坐标和对照品浓度(c)(mg/ml)为横坐标,得出在0.003--1mg/ml的hla浓度范围与峰面积的线性回归方程,并绘制标准曲线。2.载药率的测定将实施例3制备的0.2ml0.5%hla醇质体样品置于1ml容量瓶中,加入适量甲醇溶液定容,超声处理20min,进行hplc检测,根据标准曲线,测定样品的载药率。载药率(loadingefficacy,le)的计算方法为:公式中:ρ测为hplc测得的药物浓度,ρ总为总药物浓度。进行3次重复实验。3.包封率的测定采用超速离心法将实施例3制备的2ml0.5%hla醇质体置于超滤离心管中(millipore公司,截留分子量为3kda),使用离心机14000xg条件下离心45min,收集内管滤液,4℃保存,进行hplc检测,以测定样品的包封率包封率(entrapmentefficacy,ee)的计算方法为:公式中ρ总为总的药物浓度,ρ游为游离的药物浓度,进行3次实验。结果:本发明方法得到的0.5%hla醇质体包封率为38.63±0.003%,载药率为82.85±0.004%。四.药效学研究方法:sd大鼠每只的平均重量为250~300g,分为4组,每组12只。四组分别为本发明制备的0.5%的5-氨基酮戊酸己酯盐酸盐醇质体组(0.5%的hla醇质体)(a组)、0.5%的5-氨基酮戊酸水溶液组(0.5%的5-ala水溶液)(b组)、5%的5-氨基酮戊酸水溶液(5%的5-ala水溶液)(c组)、空白醇质体(d组)。用0.3g/kg水合氯醛麻醉大鼠的腹腔,用生理盐水清洁皮肤三次。将直径5cm的给药池用丙烯基粘合剂水平固定于腹部,每只大鼠加样0.6ml,封口膜密封,整个实验过程中室温条件下严格避光。每组取三只大鼠分别在给药后1,2,3和4h时清除药物,取给药部位的皮肤,剔除皮下组织及脂肪。利用leicacm1860冰冻切片机(德国徕卡仪器有限公司)制作切片厚度为10μm的冰冻切片,当天置于激光共聚焦显微镜下观察,设置的激发波长为488nm,发射波长为561nm。结果:结果见图8和图9,从中可以看出不同时间的不同醇质体在组织中的平均荧光强度。给药1h后,所有组别在表浅皮肤以及深层真皮层均有微弱红色荧光,考虑该荧光为内源性ppix,0.5%hla醇质体组在浅层毛囊以及角质层、表浅皮肤可见散在高亮红色荧光;0.5%5-ala水溶液组和5%5-ala水溶液组在毛囊周围可见微弱红色荧光,但是角质层及浅层皮肤未见明显高亮红色荧光;0.5%hla醇质体组平均荧光强度与5%5-ala水溶液组相比均有显著性差异。给药2h后,0.5%hla醇质体组的高亮红色荧光点密集分布在角质层、毛囊、皮脂腺、浅表皮肤、真皮层;0.5%5-ala水溶液组、5%5-ala水溶液组在毛囊、角质层及浅层皮肤可见散在高亮红色荧光点;0.5%hla醇质体平均荧光强度与0.5%5-ala水溶液组、5%5-ala水溶液组相比均有显著性差异。给药3h后,0.5%hla醇质体组的高亮红色荧光点密集分布在角质层、毛囊、皮脂腺、浅表皮肤、真皮层,较给药2h的高亮红色荧光点增多,0.5%5-ala水溶液组、5%5-ala水溶液组在毛囊、角质层及浅层皮肤可见散在高亮红色荧光点,同样较给药2h的高亮红色荧光有所增多。0.5%hla醇质体组与0.5%5-ala水溶液组、5%5-ala水溶液组相比均有显著性差异。给药4h后,0.5%hla醇质体组的高亮红色荧光在角质层、真皮处分布均匀,0.5%5-ala水溶液组、5%5-ala水溶液组在毛囊、角质层及浅层皮肤可见较多高亮红色荧光点。0.5%hla醇质体组与0.5%5-ala水溶液组、5%5-ala水溶液组相比均有显著统计学差异。综上所述,本发明制备的0.5%hla醇质体的粒径为70~90nm,具有高包封率、快速渗透、皮肤内产生高浓度ppix等特点。上述实施例为本发明较佳的实施方式,但本发明的实施方式并不受上述实施例的限制,其他的任何未背离本发明的精神实质与原理下所作的改变、修饰、替代、组合、简化,均应为等效的置换方式,都包含在本发明的保护范围之内。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1