柔性螺旋电极的制造方法及神经束检测治疗装置与流程
本公开涉及医疗器械技术领域,尤其涉及一种柔性螺旋电极的制造方法及神经束检测治疗装置。
背景技术
外周神经束电刺激作为神经调控的一种重要分支,在一些药物难治性疾病如癫痫、高血压、心衰等疾病治疗领域发挥着重要的作用。此外,近年来发展的用于治疗瘫痪病人的神经假体中,外周神经束电信号的监测和刺激也至关重要。用于外周神经束电刺激与电信号采集的神经电极主要有cuff电极和螺旋结构电极。其中,螺旋结构电极已被证明可降低对神经的卡压或摩擦力学损伤,因而逐渐成为临床首选。
但相关技术中,螺旋结构电极中的金属电极易脱粘,易对神经及周围组织造成机械损伤。同时脱粘后的金属电极产生漏电流,刺激非目标组织,造成极大的副作用,如恶心、呕吐、头痛等。且螺旋结构电极与神经束的匹配性差,在神经变形过程中,螺旋结构电极对神经依然有较大的束缚和卡压作用,造成不必要的副作用,不便医生手术操作。
技术实现要素:
有鉴于此,本公开提出了一种柔性螺旋电极的制造方法及神经束检测治疗装置。
根据本公开的第一方面,提供了一种柔性螺旋电极的制造方法,所述柔性螺旋电极用于植入到生物体的神经束处,获取所述神经束的电信号和/或对所述神经束进行电刺激,所述方法包括:
将衬底的温度加热至转变温度,将处于高弹态的所述衬底螺旋缠绕在第一成型棒上,形成待成型的衬底,所述衬底的材料为具备形状记忆功能的聚合物材料;
对所述待成型的衬底进行加热,保持所述待成型的衬底的温度在第一时间内大于或等于第一塑性变形温度,形成螺旋状的衬底;
将所述螺旋状的衬底的温度加热至转变温度,将处于高弹态的所述螺旋状的衬底展平,获得展平的衬底;
将金属电极转印到所述展平的衬底上;
将引线连接到所述金属电极的引线连接端,以通过所述引线向所述金属电极发送电刺激信号,和/或获取与所述金属电极接触的神经束的电信号;
将带有所述金属电极的展平的衬底的温度加热至转变温度,使展平的衬底的形状转变为螺旋状,获得柔性螺旋电极,
其中,所述转变温度小于所述第一塑性变形温度,所述衬底的转变温度小于或等于所述生物体的体温。
对于上述方法,在一种可能的实现方式中,所述方法还包括:
在基板上形成牺牲层;
在所述牺牲层上生成金属层;
对所述金属层进行刻蚀处理,生成具备预定形状的金属电极。
对于上述方法,在一种可能的实现方式中,所述方法还包括:
在基板上形成牺牲层;
在所述牺牲层上生成可塑化电介质层;
在所述可塑化电介质层上生成金属层;
对所述金属层和所述可塑化电介质层进行刻蚀处理,生成具备预定形状的金属电极;
将所述金属电极的温度加热至第二塑性变形温度,将所述金属电极螺旋缠绕在第二成型棒上,形成螺旋状的金属电极;
在外力的作用下将所述螺旋状的金属电极展平,获得展平的金属电极,
其中,所述第二成型棒的直径小于或等于所述第一成型棒。
对于上述方法,在一种可能的实现方式中,所述金属电极的预定形状为蛇形、s形和网状形的任一种。
对于上述方法,在一种可能的实现方式中,所述衬底的厚度小于200微米,所述衬底的宽度小于或等于所述生物体的神经束的直径,所述衬底的长度大于或等于所述神经束的周长,
所述第一成型棒的直径小于或等于所述生物体的神经束的直径,所述第一成型棒包括玻璃棒和/或金属棒。
对于上述方法,在一种可能的实现方式中,所述方法还包括:
制备具有形状记忆功能的聚合物材料的薄膜;
根据确定的尺寸对所述薄膜进行剪裁处理,获取所需的衬底。
对于上述方法,在一种可能的实现方式中,所述方法还包括:
在所述衬底上生成粘附层,以提高衬底与金属电极的粘附性。
对于上述方法,在一种可能的实现方式中,所述聚合物材料和所述金属电极在所述生物体内能够降解,
其中,所述金属层的材料包括铁、锌和镁中的任一种。
对于上述方法,在一种可能的实现方式中,所述聚合物材料在所述生物体内能够降解,所述金属电极在所述生物体中不能够降解,
其中,所述金属层的材料包括金、铂金和铂铱合金中的任一种。
根据本公开的第二方面,提供了一种神经束检测治疗装置,包括:柔性螺旋电极,
所述柔性螺旋电极包括引线、金属电极和螺旋状的衬底,所述金属电极固定在所述衬底上,所述引线与所述金属电极的引线连接端连接,
在所述柔性螺旋电极被植入到生物体,缠绕在对应的神经束上时,通过所述金属电极获取所述神经束的电信号,以及通过所述金属电极将接收到的电刺激信号作用于所述神经束,
其中,所述柔性螺旋电极是根据上述柔性螺旋电极的制造方法制造的。
对于上述装置,在一种可能的实现方式中,所述装置还包括:
控制模块,用于与所述引线连接,将所述电刺激信号通过所述引线发送至所述金属电极,以及通过所述引线获取所述金属电极检测到的所述神经束的电信号。
本公开实施例所提供的柔性螺旋电极的制造方法及神经束检测治疗装置,简单易行,所制造的柔性螺旋电极的延展性好,与神经束的贴合度、匹配度高,便于进行植入生物体的手术操作,且使用寿命长、稳定性高,对生物体的副作用小。
根据下面参考附图对示例性实施例的详细说明,本公开的其它特征及方面将变得清楚。
附图说明
包含在说明书中并且构成说明书的一部分的附图与说明书一起示出了本公开的示例性实施例、特征和方面,并且用于解释本公开的原理。
图1示出根据本公开一实施例的柔性螺旋电极的制造方法的流程图;
图2示出根据本公开一实施例的柔性螺旋电极的制造方法的流程图;
图3示出根据本公开一实施例的柔性螺旋电极的制造方法的流程图;
图4a、图4b示出根据本公开一实施例的柔性螺旋电极的制造方法中步骤s104的制造流程示意图;
图5示出根据本公开一实施例的柔性螺旋电极的结构的示意图;
图6示出根据本公开一实施例的柔性螺旋电极的制造方法的流程图;
图7示出根据本公开一实施例的柔性螺旋电极的制造方法中金属电极的示意图;
图8示出根据本公开一实施例的柔性螺旋电极的制造方法的流程图;
图9a、图9b示出根据本公开一实施例的柔性螺旋电极的制造方法中螺旋电极的示意图;
图10示出根据本公开一实施例的柔性螺旋电极的制造方法的应用场景的示意图;
图11示出根据本公开一实施例的外周神经检测治疗装置的结构示意图;
图12示出根据本公开一实施例的外周神经检测治疗装置的结构示意图。
具体实施方式
以下将参考附图详细说明本公开的各种示例性实施例、特征和方面。附图中相同的附图标记表示功能相同或相似的元件。尽管在附图中示出了实施例的各种方面,但是除非特别指出,不必按比例绘制附图。
在这里专用的词“示例性”意为“用作例子、实施例或说明性”。这里作为“示例性”所说明的任何实施例不必解释为优于或好于其它实施例。
另外,为了更好的说明本公开,在下文的具体实施方式中给出了众多的具体细节。本领域技术人员应当理解,没有某些具体细节,本公开同样可以实施。在一些实例中,对于本领域技术人员熟知的方法、手段、元件和电路未作详细描述,以便于凸显本公开的主旨。
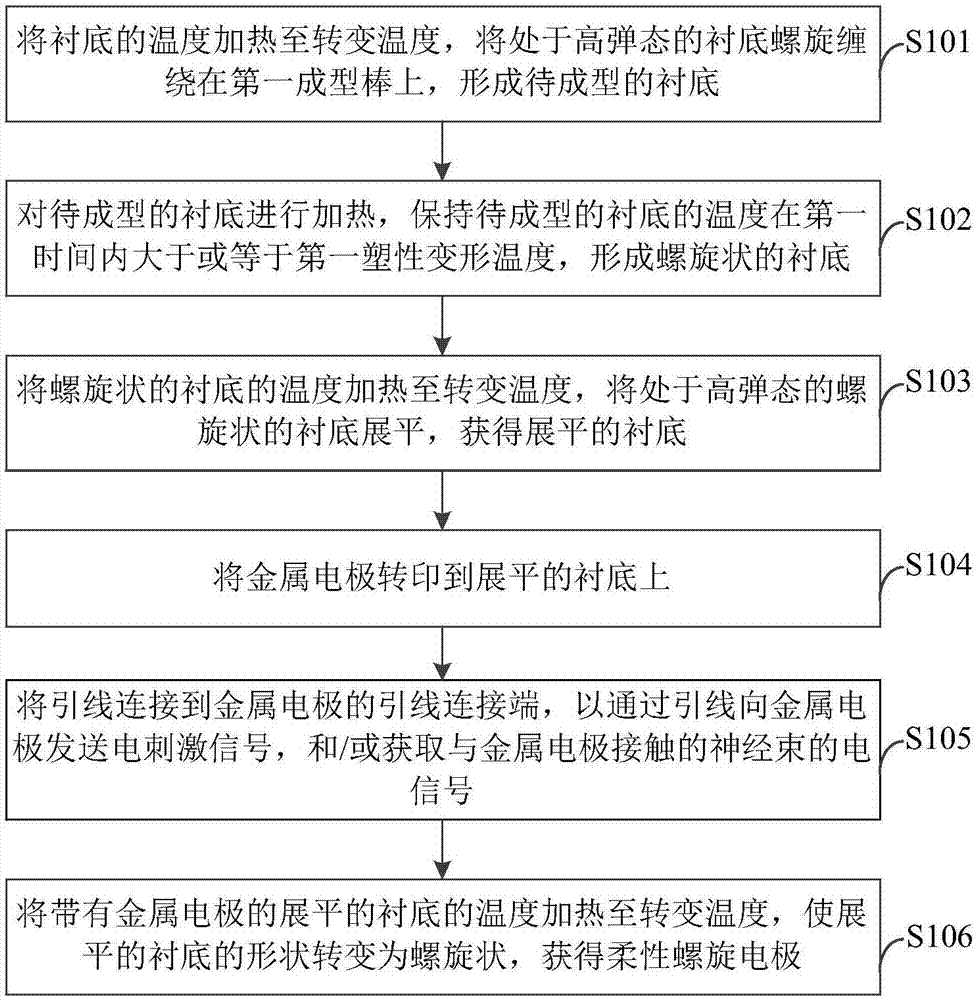
图1示出根据本公开一实施例的柔性螺旋电极的制造方法的流程图。如图1所示,柔性螺旋电极可植入到生物体的外周神经束等神经束处,获取神经束的电信号和/或对神经束进行电刺激。该方法包括步骤s101至步骤s106。
在步骤s101中,将衬底的温度加热至转变温度,将处于高弹态的衬底螺旋缠绕在第一成型棒上,形成待成型的衬底,衬底的材料为具备形状记忆功能的聚合物材料。其中,衬底的转变温度小于或等于生物体的体温。
在本实施例中,转变温度是衬底从玻璃态刚性塑料转变为高弹体态的温度。将衬底的温度加热至转变温度后,衬底处于高弹态,且在外力的作用下可以将其螺旋缠绕在第一成型棒上。
在本实施例中,具备形状记忆功能的聚合物材料可以是形状记忆聚合物(shapememorypolymer,简称smp)等聚合物,本公开对此不作限制。具备形状记忆功能的聚合物材料还可以具有生物兼容性,以满足植入生物体中的使用需求。具备形状记忆功能的聚合物材料可具有可塑性,以便对柔性螺旋电极的螺旋结构的内半径、螺旋角等参数进行设计和永久形状固定。其可具有较低的弹性模量和良好的弹性,同时具备良好的生物兼容性。其可塑性为其可在较高温度下固定成一定的形状,冷却至室温时形状保持不改变,获得其永久形状。永久形状为具备形状记忆功能的聚合物材料可以永久记忆、保持的形状,即在温度高于其形状记忆转变温度时可自由恢复至的永久形状。为保证柔性螺旋电极在植入生物体后可以以其永久形状(螺旋状)缠绕在神经束上,其转变温度可与生物体的体温相近,其弹性模量在其温度处于转变温度以上时应不高于1mpa。例如,在生物体为人类的情况下,转变温度需在35℃~40℃之间。
在一种可能的实现方式中,衬底的厚度小于200微米,衬底的宽度小于或等于生物体的神经束的直径,衬底的长度大于或等于神经束的周长。第一成型棒的直径小于或等于生物体的神经束的直径,第一成型棒可以包括玻璃棒和/或金属棒。
在该实现方式中,衬底的厚度、宽度和长度可以根据神经束的尺寸、形状等进行设置,以便于操作人员将柔性螺旋电极植入生物体中,也有利于柔性螺旋电极与神经束的紧密贴合。第一成型棒可以是圆柱状等与神经束的形状相似的形状,本公开对此不作限制。第一成型棒的直径小于或等于生物体的神经束的直径,可以使制成的柔性螺旋电极能与神经束紧密贴合,提供检测到的神经束的电信号的精度,可以对神经束进行精准的电刺激。第一成型棒在其温度大于或等于第一塑性变形温度的情况下,其形状不会发生变化。第一成型棒还可以是塑料棒等,本公开对此不作限制。
图2示出根据本公开一实施例的柔性螺旋电极的制造方法的流程图。如图2所示,在一种可能的实现方式中,该方法还可以包括步骤s107和步骤s108。
在步骤s107中,制备具有形状记忆功能的聚合物材料的薄膜。
在本实施例中,薄膜的厚度可小于200微米。这样,可以直接对薄膜进行剪裁,获得所需形状和尺寸的衬底。可以采用注塑模具成型、模压成型等方式制备薄膜,本公开对此不作限制。
在步骤s108中,根据确定的尺寸对薄膜进行剪裁处理,获取所需的衬底。
在本实施例中,可根据确定的衬底的尺寸,对薄膜进行剪裁,获得所需的衬底。
图3示出根据本公开一实施例的柔性螺旋电极的制造方法的流程图。如图3所示,在一种可能的实现方式中,该方法还可以包括步骤s109。
在步骤s109中,在衬底上生成粘附层,以提高衬底与金属电极的粘附性。
在本实施例中,可以在获取到所需的衬底之后,直接在衬底上生成粘附层。或者在制备出薄膜之后,直接在薄膜上生成粘附层。或者,可以在获得展平的衬底之后,在展平的衬底上生成粘附层。只要在将金属电极转印至展平的衬底之前,均可以在衬底上生成粘附层,本领域技术人员可以根据实际需要对生成粘附层的时间进行设置,本公开对此不作限制。
这样,在将金属电极转印至展平的衬底时,粘附层的存在可以提高金属电极与展平的衬底之间的粘附性。避免由于金属电极的脱粘对生物体的神经以及周围组织造成机械损伤。同时,避免由于脱粘的金属电极产生的漏电流刺激非目标作用位置,给生物体带来恶心、头痛等不良副作用。
在本实施例中,粘附层可以选用生物兼容性好、电学绝缘特性好、以及机械柔韧性好的材料,例如,液体绷带,双面胶敷料等,本公开对此不作限制。
在步骤s102中,对待成型的衬底进行加热,保持待成型的衬底的温度在第一时间内大于或等于第一塑性变形温度,形成螺旋状的衬底。其中,转变温度小于第一塑性变形温度。
在本实施例中,第一塑性变形温度是衬底发生塑性变形的温度。塑性变形是物质(包括流体及固体)在一定的条件下,在外力的作用下产生形变,当施加的外力撤除或消失后该物体不能恢复原状的一种物理现象。可以根据衬底发生塑性变形所需的时间等对第一时间进行设置,以保证待成型的衬底可以在第一时间内完成变形过程,形成螺旋状的衬底。
在步骤s103中,将螺旋状的衬底的温度加热至转变温度,将处于高弹态的螺旋状的衬底展平,获得展平的衬底。
在本实施例中,可在外力的作用下,将处于高弹态的、螺旋状的衬底展平为条带状的平面形状,以便于在其上固定金属电极。
在步骤s104中,将金属电极转印到展平的衬底上。
在本实施例中,转印到展平的衬底上的金属电极的数量可以是1、2、3等任意数量,可以根据植入不同神经束的使用需要对金属电极的数量进行设置,本公开对此不作限制。可以采用印章转印法、溶液转印法等转印方法将金属电极转印到展平的衬底上,本公开对此不作限制。图4a、图4b示出根据本公开一实施例的柔性螺旋电极的制造方法中步骤s104的制造流程示意图。如图4a、图4b所示,将带有引线连接端21的金属电极2转印到展平的衬底3上,将二者固定在一起。
在步骤s105中,将引线连接到金属电极的引线连接端,以通过引线向金属电极发送电刺激信号,和/或获取与金属电极接触的神经束的电信号。
在本实施例中,引线的材料可以是铜、银等能够导电、不受生物体内的组织液腐蚀、具有良好化学惰性的金属材料,本公开对此不作限制。还可以在制备金属电极的过程中,直接在金属电极的引线连接端连接引线,本公开对引线的连接时间不作限制。
在步骤s106中,将带有金属电极的展平的衬底的温度加热至转变温度,使展平的衬底的形状转变为螺旋状,获得柔性螺旋电极。
在本实施例中,图5示出根据本公开一实施例的柔性螺旋电极的结构的示意图。如图5所示,柔性螺旋电极可包括引线1、金属电极2和衬底3,柔性螺旋电极的形状可为螺旋状,可以缠绕在神经束上。为便于运输和储存,还可以将柔性螺旋电极加热至转变温度,并在外力的作用下将其加工需要的形状,本公开对此不作限制。
在本实施例中,在植入生物体之前,可以将柔性螺旋电极的温度加热至转变温度,在外力的作用下将其加工成易于植入生物体的植入形状。例如,将其植入形状加工成直径大于神经束直径的螺旋状。在确定植入形状的柔性螺旋电极已经被植入到目标的神经束上时,可以等待一定时间,生物体的体温会将植入形状的柔性螺旋电极的温度加热至其转变温度,植入形状的柔性螺旋电极的形状会转变为螺旋状,缠绕在目标的神经束上。
图6示出根据本公开一实施例的柔性螺旋电极的制造方法的流程图。如图6所示,在一种可能的实现方式中,该方法还可以包括步骤s110至步骤s112。
在步骤s110中,在基板上形成牺牲层。
在本实施例中,基板可以是由于玻璃、硅等硬质材料制成的薄片,牺牲层的材料可以是聚甲基丙烯酸酯、氧化硅、多晶硅、光刻胶等,本公开对此不作限制。
在步骤s111中,在牺牲层上生成金属层。
在本实施例中,可以利用物理气相沉积和化学气相沉积等薄膜生长方法在牺牲层上制备金属层。金属层的厚度不超过500nm,以保证金属层具有良好的柔性。
在步骤s112中,对金属层进行刻蚀处理,生成具备预定形状的金属电极。
在本实施例中,可以采用光刻技术、剥离技术(liftoff)、干法刻蚀等技术对金属层进行蚀刻处理,制备出具有预定形状的金属电极。例如,可以根据金属电极的预定形状和尺寸预先制备掩膜版,以掩膜版为掩膜对金属层进行刻蚀处理,生成具备预定形状的金属电极。本领域技术人员可以根据实际需要对制备金属电极的方式进行设置,本公开对此不作限制。
在本实施例中,所生成的金属电极上还可包括用于连接引线的引线连接端,引线连接端可以位于金属电极的两端,以便于将引线连接到金属电极上。图7示出根据本公开一实施例的柔性螺旋电极的制造方法中金属电极的示意图。如图7所示,生成的金属电极2包括在一端的引线连接端21。引线连接端的形状可以是的多变形(如图7所示)、圆形、椭圆形等形状,本公开对此不作限制。
图8示出根据本公开一实施例的柔性螺旋电极的制造方法的流程图。如图8所示,在一种可能的实现方式中,该方法还可以包括步骤s113至步骤s118。
在步骤s113中,在基板上形成牺牲层。其中,步骤s113可以参考步骤s110的相关描述,不再赘述。
在步骤s114中,在牺牲层上生成可塑化电介质层。
在本实施例中,可塑化电介质层的材料可以具有良好的电学绝缘性、化学稳定性、机械强韧性和一定的可延展性的材料。可塑化电介质层的材料可以在生物体内能够降解,也可以在生物体中不能降解,本公开对此不作限制。例如,可塑化电介质层的材料可以是聚酰亚胺(polyimide,简称pi)等。可塑化电介质层的厚度可以在1微米~20微米之间。本领域技术人员可以根据实际需要对可塑化电介质层的材料和厚度等进行设置,本公开对此不作限制。
在步骤s115中,在可塑化电介质层上生成金属层。其中,步骤s113可以参考步骤s111的相关描述,不再赘述。
在步骤s116中,对金属层和可塑化电介质层进行刻蚀处理,生成具备预定形状的金属电极。
在本实施例中,金属电极可以由金属层和可塑化电介质层构成。可以参考步骤s112的相关描述,对金属层和可塑化电介质层进行刻蚀处理,生成具备预定形状的金属电极。例如,可以根据金属电极的预定形状和尺寸,预先制备掩膜版,以掩膜版为掩膜对金属层进行刻蚀处理,掩膜版图形转移到金属层上,形成具有预定形状的金属层图形(具有预定形状)。而后以金属层图形为掩膜,采用反应离子刻蚀(干法刻蚀)对可塑化电介质层进行刻蚀,形成与金属层的图形一致的可塑化电介质层图形(具有预定形状),获得金属电极。本领域技术人员可以根据实际需要对制备金属电极的方式进行设置,本公开对此不作限制。
在步骤s117中,将金属电极的温度加热至第二塑性变形温度,将金属电极螺旋缠绕在第二成型棒上,形成螺旋状的金属电极。其中,第二成型棒的直径小于或等于第一成型棒。
在本实施例中,形成螺旋状的金属电极,以保证金属电极与衬底具有相同的螺旋状结构,便于与神经束紧密贴合。并且,可以使衬底与金属电极之间的结合更为紧密,防止金属电极脱粘。
在步骤s118中,在外力的作用下将螺旋状的金属电极展平,获得展平的金属电极。
在本实施例中,可以将展平的金属电极转印至展平的衬底上。并当去除外力、且将带有金属电极的展平的衬底的温度加热至第一转变温度时,使金属电极的形状恢复至螺旋状、展平的衬底形状转变为螺旋状,获得柔性螺旋电极。
在本实施例中,可先执行步骤s112至步骤s116,而后将金属电极转印至衬底上,形成平面结构的柔性电极。将柔性电极的温度加热至转变温度,将柔性电极螺旋缠绕在第一成型棒上,形成待成型的柔性电极。对待成型的柔性电极进行加热,保持待成型的柔性电极的温度在第一时间内大于或等于第一塑性变形温度,冷却形成柔性螺旋电极。金属电极中的可塑化电介质层的第二塑性变形温度小于或等于第一塑性变形温度,以保证可塑化电介质层可以以螺旋状为其固定形状。通过这种方式可以简化形成柔性螺旋电极的制造过程。
在本实施例中,所制造的柔性螺旋电极可以是在生物体内能够完全降解、部分降解和完全不降解的,可以根据实际的应用场景需要对柔性螺旋电极的衬底、金属电极的材料、结构等进行设置,以满足柔性螺旋电极的不同使用需求。
在一种可能的实现方式中,聚合物材料和金属电极在生物体内能够降解。其中,金属层的材料可以包括铁、锌和镁中的任一种。其中,金属电极包括金属层,还可以包括可塑化电介质层。
在该实现方式中,可以根据通过对柔性螺旋电极的材料和结构进行调整,以对柔性螺旋电极在生物体内的降解时间进行设置,使柔性螺旋电极在被使用之后,可以直接在生物体内降解。无须通过对生物体进行二次手术等形式取出或去除生物体内的柔性螺旋电极。减少二次手术对生物体所造成的伤害,也节省了进行二次手术的时间、资源等的耗费。
在一种可能的实现方式中,聚合物材料和金属电极在生物体内均不能够降解。其中,金属电极的材料可以是金、铂金和铂铱合金中的任一种。其中,金属电极包括金属层,还可以包括可塑化电介质层。这样,可以满足生物体中需长时间植入柔性螺旋电极,以达到通过柔性螺旋电极获取神经束的电信号和/或对神经束进行电刺激的目的。
在一种可能的实现方式中,聚合物材料在生物体内能够降解,金属电极在生物体内均不能够降解。其中,金属电极的材料可以是金、铂金和铂铱合金中的任一种。其中,金属电极包括金属层和可塑化电介质层。
在该实现方式中,可以根据衬底需要在生物体内存留的时间对聚合物材料进行选择,本公开对此不作限制。这样,衬底在生物体内存留一定时间后会降解,可降低柔性螺旋电极的弯曲刚度和拉伸刚度,以减少柔性螺旋电极对神经束的束缚。且由于可塑化电介质层和金属层并不降解,二者可以继续实现柔性螺旋电极的功能。
举例来说,生物体为发育尚未完全的青少年。柔性螺旋电极植入青少年体内的外周神经束上之后,由于青少年的外周神经束还会不断生长,直径还会增长1~2倍才会成熟稳定。因此,需要柔性螺旋电极在植入青少年体内之后,其弯曲刚度和拉伸刚度还能降低,以满足外周神经束的生长需求。图9a、图9b示出根据本公开一实施例的柔性螺旋电极的制造方法中螺旋电极的示意图。如图9a所示,柔性螺旋电极包括衬底3和金属电极2。其中,金属电极2包括具有预定形状的金属层22、可塑化电介质层23和引线连接端21。衬底3(聚合物材料)可降解。将该柔性螺旋电极植入青少年的外周神经束之后,在衬底3降解(如图9b所示)之后,可以通过可塑化电介质层23和金属层22继续获取外周神经束的电信号和/或对外周神经束进行电刺激。
在一种可能的实现方式中,金属电极的预定形状可以为蛇形、s形和网状形的任一种。
在该实现方式中,金属电极的预定形状可以是“之”字形等易于延展和拉伸的形状,以降低柔性螺旋电极的拉伸和弯曲刚度,以保证在柔性螺旋电极缠绕在神经束上时,可以随神经束由于生长等原因导致的变形而变形,不会对神经束造成束缚、卡压等损伤。金属电极的材料还可以是银、铜等延展性、导电性能较好、不受生物体内的组织液腐蚀、具有良好化学惰性的金属材料,本公开对此不作限制。
需要说明的是,尽管以上述实施例作为示例介绍了柔性螺旋电极的制造方法如上,但本领域技术人员能够理解,本公开应不限于此。事实上,用户完全可根据个人喜好和/或实际应用场景灵活设定各步骤,只要符合本公开的技术方案即可。
本公开实施例所提供的柔性螺旋电极的制造方法,简单易行,所制造的柔性螺旋电极的尺寸小、延展性好,与神经束的贴合度、匹配度高,便于进行植入生物体的手术操作,且使用寿命长、稳定性高,对生物体的副作用小。
应用示例
以下结合“制造某柔性螺旋电极”作为一个示例性应用场景,给出根据本公开实施例的应用示例,以便于理解柔性螺旋电极的制造方法的流程。本领域技术人员应理解,以下应用示例仅仅是出于便于理解本公开实施例的目的,不应视为对本公开实施例的限制。
图10示出根据本公开一实施例的柔性螺旋电极的制造方法的应用场景的示意图。如图10所示,制造某可以植入到生物体的外周神经束上的柔性螺旋电极的过程包括步骤s301至步骤s312。
在步骤s301中,采用注塑模具成型的方式,在预先制备的模具中制备具备形状记忆功能的聚合物材料的薄膜,薄膜的厚度不超过200微米。
在步骤s302中,按照确定尺寸对薄膜进行裁剪,获得所需的衬底。其中,衬底的宽度不大于外周神经束直径,衬底的长度大于或等于外周神经束的周长。
在步骤s303中,将衬底的温度加热至器对应的转变温度(衬底的温度大于转变温度)。在外力作用下,将处于高弹态的衬底螺旋缠绕到成型棒(如玻璃棒)上,形成待成型的衬底。其中,成型棒的直径小于或等于外周神经束的直径。
在步骤s304中,对待成型的衬底进行加热,使待成型的称帝的温度在第一时间内保持在大于或等于第一塑性变形温度的状态。
在步骤s305中,将待成型的衬底的温度保持第一时间之后,将其冷却至室温,形成螺旋状的衬底。
在步骤s306中,将螺旋状的衬底的温度加热至转变温度,在外力作用下将螺旋状的衬底展平,获得展平的衬底。例如,可以将螺旋状的衬底展平成条带状。
在步骤s307中,在基板上制备牺牲层。基板可以是硅片、玻璃片等。
在步骤s308中,利用薄膜生长技术制备好的牺牲层上进行纳米金属层材料的生长,形成金属层。
在步骤s309中,采用光刻、剥离等方法对金属层进行刻蚀处理,生成具备预定形状的金属电极。
在步骤s310中,将牺牲层刻蚀掉,利用转印法金属电极转印至展平的衬底。
在步骤s311,将引线连接到金属电极的引线连接端,以通过引线向金属电极发送电刺激信号,和/或获取与金属电极接触的外周神经束的电信号。
在步骤s312中,将带有金属电极的展平的衬底的温度加热至转变温度,是展平的衬底的形状转变为螺旋状,获得柔性螺旋衬底。
这样,所制造的柔性螺旋电极的延展性好,与外周神经束的贴合度、匹配度高,便于进行植入生物体的手术操作,且使用寿命长、稳定性高,对生物体的副作用小。
图11示出根据本公开一实施例的外周神经检测治疗装置的结构示意图。如图11所示,该装置可以包括柔性螺旋电极40。柔性螺旋电极40可以包括引线401、金属电极402和螺旋状衬底403。金属电极402固定在衬底403上,引线401与金属电极402的引线连接端(未示出)连接。在柔性螺旋电极40被植入到生物体,缠绕在对应的神经束上时,通过金属电极402获取神经束的电信号,以及通过金属电极402将接收到的电刺激信号作用于神经束。其中,柔性螺旋电极40是根据上述柔性螺旋电极的制造方法制造的。
图12示出根据本公开一实施例的外周神经检测治疗装置的结构示意图。如图12所示,该装置还可以包括控制模块50。
控制模块50用于与引线401连接,将电刺激信号通过引线401发送至金属电极402,以及通过引线401获取金属电极402检测到的神经束的电信号。
在本实施例中,电刺激信号可以是根据治疗、检测等需要生成的,本公开对此不作限制。获取到电信号之后,可以通过获取的电信号对神经束的生理状态进行分析,获得所需的神经束的相关数据,便于相关人员根据相关数据对神经束以及生物体的健康状况进行分析。
本公开实施例所提供的神经束检测治疗装置,其柔性螺旋电极的延展性好,与神经束的贴合度、匹配度高,便于进行植入生物体的手术操作,且使用寿命长、稳定性高,对生物体的副作用小。在柔性螺旋电极被植入到生物体,缠绕在对应的神经束上时,通过金属电极获取神经束的电信号,以及通过金属电极将接收到的电刺激信号作用于神经束。
以上已经描述了本公开的各实施例,上述说明是示例性的,并非穷尽性的,并且也不限于所披露的各实施例。在不偏离所说明的各实施例的范围和精神的情况下,对于本技术领域的普通技术人员来说许多修改和变更都是显而易见的。本文中所用术语的选择,旨在最好地解释各实施例的原理、实际应用或对市场中的技术的技术改进,或者使本技术领域的其它普通技术人员能理解本文披露的各实施例。
- 还没有人留言评论。精彩留言会获得点赞!