褐藻寡糖在制备抗炎症性肠病药物中的应用的制作方法
本发明属于医药领域,涉及褐藻寡糖在制备抗炎症性肠病药物中的应用。
背景技术:
ibd(inflammatoryboweldisease)为累及直肠、结肠和回肠的一种慢性非特异性肠道炎症性疾病。其病因和发病机制尚未完全阐明,目前认为主要是由包括遗传、环境、感染和免疫等多因素引起的。目前采用的治疗ibd的药物主要为氨基水杨酸、糖皮质激素等,但多数无法达到根治的疗效且具有副作用,因而急需探索能使ibd患者获得更好治疗的药物。
scfa(short-chainfattyacid)是肠道菌群以碳源为底物发酵的主要产物,被后肠迅速吸收从而进入体循环,继而对个体的器官和代谢产生影响。scfa对机体具有重要的生理活性,如调节肠道菌群、提供肠道上皮细胞营养以及机体能量等。有研究表明scfa中的丁酸、乙酸和丙酸具有抗炎特性,3种酸均能使炎症因子tnf-α表达量下降,并能抑制nf-kb活性(sofiatedelind,fredrikwestberg,martinkjerrulf,etal.anti-inflammatorypropertiesoftheshort-chainfattyacidsacetateandpropionate:astudywithrelevancetoinflammatoryboweldisease[j].世界胃肠病学杂志:英文版(电子版),2007,13(20):2826-2832)。scfa对人体健康有重要作用,深入研究scfa为治疗人体ibd疾病提供理论依据。
aos(alginateoligosaccharides)是褐藻胶的一种功能性寡聚物,具有多种生物活性,如抗肿瘤、免疫和抑菌等。有研究发现褐藻寡糖能够促进双歧杆菌和乳酸菌的生长(yewang,fenghan,binhu,etal.invivoprebioticpropertiesofalginateoligosaccharidespreparedthroughenzymatichydrolysisofalginate[j].nutritionresearch,2006,26(11):597-603.),而双歧杆菌和乳酸菌为人体肠道益生菌,可发酵低聚糖产生多种有机酸,抑制有害菌生长,维持肠道环境稳态。褐藻寡糖由肠道益生菌作为能源降解后,可产生具有生理活性的小分子如scfa,从而进入体循环影响人体健康。
技术实现要素:
本发明的目的是提供褐藻寡糖在制备抗炎症性肠病药物中的应用。同时,本发明公开了褐藻寡糖在制备抗炎症性肠病药物中的应用。
为了实现上述目的,本发明采取的关键技术方案为:
本发明中,褐藻寡糖是由β-d-甘露糖醛酸(m)和α-l-古罗糖醛酸(g)组成的线型低聚合物,具有聚甘露糖醛酸(pm)、聚古罗糖醛酸(pg)和杂合褐藻寡糖(pmg)三种结构式。3种低聚物分子式均为(c12h14na2o12)n,n范围为1~10,结构式分别如下:
pm结构式为:
;pg结构式为:
;pmg结构式为:
炎症性肠病包括溃疡性结肠炎和克罗恩病。
在本发明中,溃疡性结肠炎动物模型由葡聚糖硫酸钠(dss)诱导。
抗炎药物褐藻寡糖的给药方式为灌胃给药。
本发明中,褐藻寡糖用于治疗ibd。
进一步地,药物剂型为口服剂。
经本发明验证,褐藻寡糖在制备抗炎症性肠病的药物中,通过提高肠道乳酸、乙酸和丙酸水平,达到治疗炎症性肠病的效果。具体表现在缓解动物体重下降、降低结肠病理损伤等,且相比于氨基水杨酸类药物无明显毒副作用。
此外,我国是海洋大国,富产海带、马尾藻等褐藻类产品,褐藻寡糖是由褐藻植物中提取出的褐藻胶经过降解作用成为的产品,目前已被应用于工业化。因而褐藻寡糖具有来源广泛且成本较低的特点,利于大规模生产。
相对于现有抗炎药物,本发明至少具有以下优点:
本发明公开了一种新的治疗ibd的药物,即通过褐藻寡糖治疗ibd。通过动物实验验证褐藻寡糖能够抑制炎症性肠病,并且在发挥药效过程中无明显的毒副作用。对比于现有治疗ibd的药物,褐藻寡糖具有无毒副作用、来源广泛且成本较低的优势,具有潜在的开发价值和广阔的应用前景。
附图说明
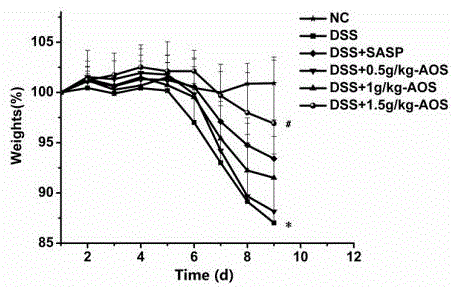
图1为小鼠体重变化;
图2为小鼠结肠长度比较;
图3为小鼠结肠形态观察;
图4为小鼠结肠组织病理切片;
图5a为小鼠结肠乳酸浓度测定结果图;
图5b为小鼠结肠乙酸浓度测定结果图;
图5c为小鼠结肠丙酸浓度测定结果图。
具体实施方式
为了更加详细阐述本发明的技术方法,以下列举实施方案并配图说明。
实施例1
本发明提供了褐藻寡糖在制备抗炎症性肠病药物中的应用。
在本发明中,为了体现褐藻寡糖的抗炎作用需要先对小鼠进行造模,优选的造模方法为以下步骤:
1)使用质量浓度为1.5%的dss溶液给小鼠自由饮用,饮用时间为5天。
2)第6天开始换除dss溶液,改用灭菌的纯净水为小鼠自由饮用水,饮用时间为4天即实验结束。
3)各组小鼠从第1天开始给药干预,给药至实验结束。
在本发明中,所述小鼠优选为spf级别的c57bl/6小鼠,均为雄性,且周龄为7~9周,体质量为20~22g。本发明对小鼠来源无特殊限制,使用符合上述优选条件的实验用鼠均可,本实施方案中采用的小鼠购置于上海斯莱克动物有限公司。
本发明中小鼠饲养的温度为22~24℃,湿度为50~60%,作息规律为白天12h光照,夜晚12h黑暗的模式交替进行。
本发明中,对于造模试剂dss来源无特殊要求,使用市售的实验室用造模试剂均可。本实施中采用的是美国mpbiomedicals公司的分子量为36000~50000的dss。
本发明中,所述的褐藻寡糖无特殊来源限制,使用市售的食品级的褐藻寡糖均可。本实施例中采用的褐藻寡糖购买于青岛博智汇力生物科技有限公司,为食品级别,且聚合度为2~20,纯度大于80%。
本发明中,实验分为正常对照小鼠(nc)、模型组小鼠(dss)、阳性药物治疗组(dss+sasp)和褐藻寡糖低、中、高浓度组(dss+aos)。各组随机分配6只小鼠。
优选的,正常对照小鼠实验过程中均饮用灭菌的纯净水,对于造模的小鼠前5天自由饮用dss溶液,第6天换为饮用纯净水。
优选的,各组小鼠从第1天开始灌胃给药。正常对照组和模型组小鼠灌胃ph=7.4,浓度为0.01mol/l的pbs溶液,阳性药物组灌胃0.5g/kg的柳氮磺吡啶(sasp)溶液,褐藻寡糖组分别灌胃浓度为0.5g/kg、1g/kg、1.5g/kg的褐藻寡糖溶液。每只小鼠给药剂量均为0.4ml。
实验过程中需要记录的数据为:
1)每日观察小鼠毛色、精神状态和摄食量的变化;
2)每日称量小鼠体重,计算小鼠体重下降百分比;
3)每日观察小鼠粪便的形态和出血情况;
4)整合以上数据对小鼠疾病程度进行dai评分。
dai评分标准根据文献制定,具体为表1所示:
表1
实验进行9天后二氧化碳窒息处死小鼠。
图1是小鼠每日体重变化的曲线图。由图可以看出各组中模型组小鼠体重下降程度最大,第9天时体重下降至87%。其次为0.5g/kgaos、1g/kgaos、sasp、1.5g/kgaos、nc组,体重百分比分别为88%、92%、93%、97%和101%。其中模型组与正常对照组相比具有显著性差异(*p<0.05),与1.5g/kgaos组相比也具有显著性差异(#p<0.05)。以上结果表明高浓度的aos可以显著缓解ibd小鼠体重下降的问题。
表2是小鼠第8天的炎症患病程度评分,即dai评分。由结果可知,正常对照组和模型组小鼠的dai分数分别为0和2.33±0.85,两组具有极显著性差异(**p<0.01),说明实验造模成功。1.5g/kgaos组dai分数为0.6±0.25,与模型组相比分值下降且具有极显著性差异(##p<0.01),说明高浓度的aos可以有效降低小鼠肠炎患病程度,即抑制ibd。
表2小鼠第8天dai评分
注:*p<0.05v.nc,#p<0.05v.dss.
实施例2
小鼠结肠长度测量和组织染色:
根据实施例1处死小鼠后,取其肛门至回盲部的结肠,测量整个肠段长度并拍照记录。沿肠系膜纵行剪开肠道,收集粪便于无菌的ep管,用中性pbs将肠道内残留粪便冲洗干净,铺平展开。取结肠远端0.5cm左右,中性甲醛溶液固定24~48h后进行he染色。整个he染色步骤大致分为乙醇梯度脱水、二甲苯透明、石蜡包埋、切片、脱蜡水化、染色和封片,最后拍照观察切片。
图2为各组小鼠结肠长度比较。其中,模型组小鼠的结肠最短,平均为6.77cm。aos组小鼠的结肠随aos浓度的增高而增加,且1.5g/kgaos小鼠结肠长度平均为7.87cm,与模型组小鼠相比具有极显著性差异(p<0.01)。由结果可知,aos可以减轻小鼠ibd带来的结肠缩短的问题。
图3为小鼠结肠形态观察。由图可发现,除正常对照组外,其余组结肠均有不同程度的水肿现象,其中模型组水肿更为明显,且结肠最短。sasp组和aos组结肠水肿均有所减轻,结肠缩短问题也有改善。
图4为小鼠组织切片观察。有图可发现,正常组小鼠结肠组织结构完整,未见溃疡、坏死;固有层肠腺完整且排列有序;黏膜肌层完整;黏膜下层未见淋巴细胞浸润与炎症反应;肌层完整、平滑。模型组固有层腺体变形、肿大且排列紊乱;黏膜下层有大量炎性细胞浸润,局部有糜烂,炎症侵及肌层。低剂量组aos结肠损伤程度与模型组相似。sasp和中、高剂量aos组的炎症损伤程度较模型组轻,虽仍然可见部分腺体变形或肿大,局部炎症因子浸润,但粘膜结构整体较为完整,腺体排列有序。
由以上结果分析可知,高浓度的褐藻寡糖能够改善ibd小鼠的结肠缩短和水肿问题,且减轻了结肠组织的病理损伤。
实施例3
小鼠结肠scfa含量测定:
根据实施例1处死小鼠并根据实施例2收集结肠粪便后,采用高效液相(hplc)对小鼠结肠粪便的scfa进行测定。样品处理方法和测定方案如下:
1)按照小鼠粪便10μl/mg加入ddh2o配制成粪便浑浊液;
2)使用超声清洗器对粪便浑浊液进行超声,设置条件为15℃、2h。随后涡旋混匀,静置5h;
3)使用高速冷冻离心机将浑浊液在15,000rmp/min、4℃条件下离心10min;
4)取150μl上清液加入50μl0.15mhcl溶液,涡旋混匀;
5)使用0.22μm滤膜过滤后上样;
6)hplc设定程序如下:
其中第一相为ph=2.2,浓度为20mm的nah2po4·2h2o溶液,第二相为乙腈。
使用syncronisc18(5um,250×4.6mm)色谱柱进行测定。
表3
图5a为乳酸浓度测定结果图。由图可发现,正常小鼠结肠内乳酸浓度较高,而模型组小鼠结肠内乳酸浓度显著降低(**p<0.01)。其余组的乳酸均比模型组增高,且1.5g/kg的aos组小鼠乳酸浓度比模型组显著增多(#p<0.05)。
图5b为乙酸浓度测定结果图。由图可知,ibd造模小鼠结肠内乙酸含量均比正常小鼠低,且模型组降低的更为明显,1.5g/kg的aos与模型组相比乙酸含量有显著提高(#p<0.05)。
图5c为丙酸浓度结果图。与乳酸和乙酸类似,模型组结肠丙酸水平显著低于正常组小鼠(*p<0.05)。其余各组的丙酸浓度均比模型组高,且sasp组和1.5g/kgaos组小鼠结肠丙酸均比模型组显著增多(#p<0.05)。
由以上结果分析可以得出,模型组小鼠结肠内的scfa包括乳酸、乙酸和丙酸浓度相比于正常小鼠显著降低,提示ibd可能导致小鼠结肠内环境紊乱,包括肠道菌群失衡、酸碱度失调和能量不足等,由此引发具有生理活性的小分子scfa表达量下降。而aos能够上调乳酸、乙酸和丙酸表达水平,预示着aos可能通过改善以上所述的内环境失衡问题,提高scfa含量,进而调控身体健康,缓解ibd疾病。
由上诉实例可验证褐藻寡糖对炎症性肠病的改善作用,由此说明本发明的褐藻寡糖在制备抗炎症性肠病药物中的应用。但应该指出,上诉实例为本发明的优选方式,不意味着仅有此方式才能实现本发明。对于本技术领域的普通技术人员来说,在不脱离本发明原理的前提下,还可以对该技术和实施方式进行变换或者改进,这些变换和改进也应属于本发明的保护范围。
-
 0访客 来自[中国] 2022年01月28日 11:33褐藻寡糖 褐藻寡糖M段(甘露糖醛酸寡糖) 褐藻寡糖G段(古罗糖醛酸寡糖)厂家 0532-88890589
0访客 来自[中国] 2022年01月28日 11:33褐藻寡糖 褐藻寡糖M段(甘露糖醛酸寡糖) 褐藻寡糖G段(古罗糖醛酸寡糖)厂家 0532-88890589