一种雷帕霉素局部注射制剂及其制备方法与流程
本发明属于药物领域,具体涉及一种雷帕霉素局部注射制剂及其制备方法。
背景技术:
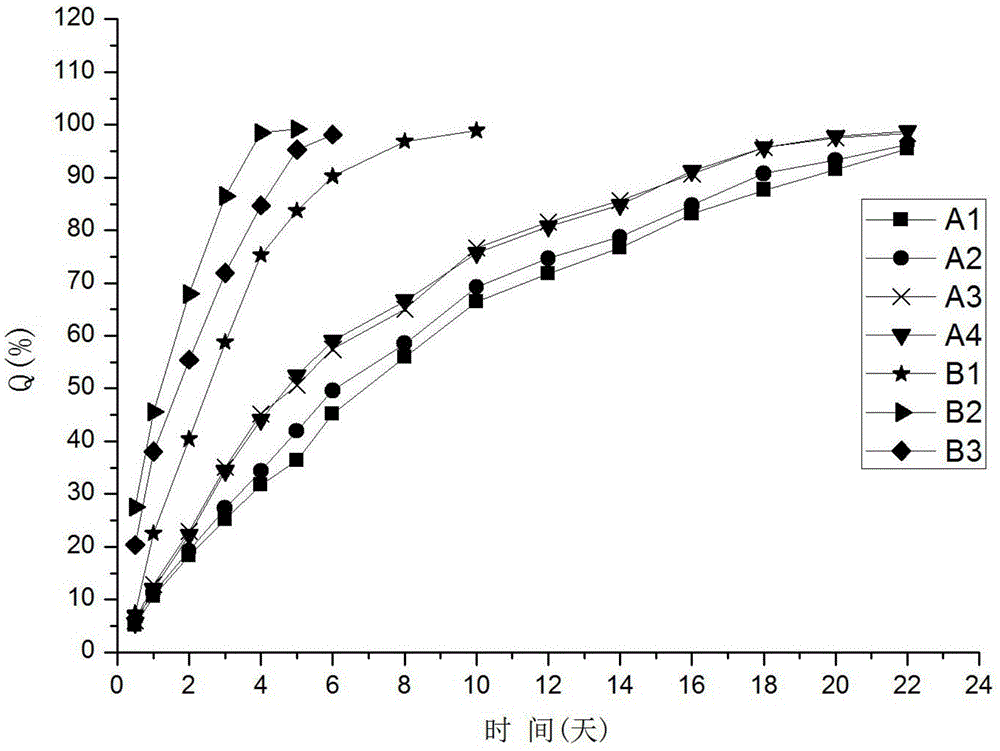
:血管畸形(vasculartumor)亦称管型瘤,根据病变部位及亚型或分别称血管瘤,淋巴管瘤。血管畸形并非真性肿瘤系来源于血管或淋巴管的异常增生。目前,对血管畸形治疗常用方法有口服及外用药物治疗、手术切除、激光治疗、硬化剂注射等,还没有一种方法可以治疗所有类型的血管畸形;应根据病变的类型、部位、深浅及病员的年龄等因素而定。手术治疗一般适用于病变部位较大,非暴露位置,对于独立病灶效果良好的患者。但由于病变位置血管丰富、血量大,手术过程中风险较大,切除病变组织后,有时会引起局部畸形,甚至是功能障碍。激光治疗对浅表性血管畸形治疗效果明显,副作用较小,但无法治疗深层血管畸形。硬化剂注射,可以使血管组织纤维化、闭锁产生瘢痕收缩,使瘤体缩小,但硬化剂注射后,病变位置血管组织纤维化,可能会影响甚至丧失机体局部的功能,不太适合治疗关键部位和大体积的血管畸形。药物治疗血管畸形是一种重要的手段。婴幼儿血管瘤的治疗常用普萘洛尔、噻吗洛尔、平阳霉素等,如专利cn107281094a、cn102836418a,成人的血管畸形常用局部注射硬化剂、口服雷帕霉素等。药物可以制成不同的剂型,根据不同的病变情况,可以选择更合适的剂型。如皮肤表层的血管畸形,可以采用乳膏制剂或贴剂等外用制剂;体内较小的血管畸形,可以采用口服制剂;而对于病变严重、位于皮下较深的血管畸形,外用制剂难以达到治疗的效果,口服因为局部药物的浓度不高也很难达到治疗效果,为了控制病情通常需要局部注射。局部注射用药是临床常用的一种治疗方法,具有局部药物浓度高、疗效好、用药方便等优点。但普通的注射剂局部注射后病灶部位的药物会因为血液循环而被带走导致病变部位药物浓度降低,同时因为药物不能持续地在病变部位释放也影响了治疗效果。因此雷帕霉素局部注射的长效制剂有望带来更好的治疗效果。目前局部注射的长效制剂通常采用微球、温敏凝胶等技术。长效局部注射制剂存在的技术问题在于:一是药物载体的选择,需要与人体具有良好的相容性以及可降解性,从而避免注射到人体后产生严重副作用,如过敏反应等;二是局部注射制剂需要具有良好的缓释作用,否则药物过快进入全身血液循环,引起过高的血药浓度,导致发热、低血压、心动过缓等不良反应,同时也不利于在病变部位持久地发挥药效。溶致液晶是一种包含溶剂化合物在内的两种或多种化合物形成的液晶,在水溶液中浓度处于一定范围内时就会出现液晶相,溶致液晶在药物载体方面得到了广泛的关注,尤其是作为长效注射剂载体应用方面。溶致液晶中的成分磷脂、甘油酯是人体相容性良好的材料,在人体内容易代谢,并且注射到人体后能够快速形成液晶,从而起到缓释的作用。如cn106924172a公开了一种石杉碱甲溶致液晶制剂,具有良好的中长效缓释性能。目前在血管畸形治疗领域,亟需一种用于治疗病变严重、位于皮下较深的血管畸形的局部缓释长效注射制剂。技术实现要素:本发明的目的是针对现有技术存在的问题,提供一种雷帕霉素局部注射制剂,用于治疗病变严重、位于皮下较深的血管畸形,具有长效缓释的效果,并且在体内相容性好、容易代谢。为实现上述目的,本发明采用的技术方案是:一种雷帕霉素局部注射制剂,包括0.02-0.05g的雷帕霉素、1-3g的有机溶剂、6-10g的磷脂、8-12g的甘油酯和0.6-1.2g稳定剂。优选的,雷帕霉素局部注射制剂,包括0.02-0.05g的雷帕霉素、1-2g的有机溶剂、7-9g的磷脂、8-10g的甘油脂和0.8-1g的稳定剂。进一步地,所述磷脂包括大豆卵磷脂、蛋黄卵磷脂中的一种或两种,优选蛋黄卵磷脂。进一步地,所述甘油酯包括二油酸甘油酯、三油酸甘油酯和硬脂酸甘油酯中的一种或多种,优选二油酸甘油酯。进一步地,所述有机溶剂为乙醇。进一步地,所述稳定剂为泊洛沙姆407或低分子聚乙二醇。本发明还提供了所述雷帕霉素局部注射制剂的制备方法:将雷帕霉素溶解在有机溶剂中,然后加入磷脂、甘油脂和稳定剂,混合均匀得到流动液体,最后经过滤除菌,得到雷帕霉素局部注射制剂。与现有技术相比,本发明的有益效果是:(1)雷帕霉素局部注射制剂是现有技术未有的,将雷帕霉素制成局部缓释注射制剂,有利于提高雷帕霉素治疗血管畸形的靶向性,特别适用于对病变较深的血管畸形治疗。(2)选择磷脂和甘油酯作为溶致液晶材料,与人体相容性好,容易代谢。(3)雷帕霉素局部注射制剂的粘度小,便于注射;注射到病变位置后遇水转变成液晶,起到良好的缓释作用,缓释时间可超过20天。(4)在制剂中加入稳定剂,有利于提高溶质液晶的稳定性,延长缓释时间。附图说明图1为雷帕霉素局部注射制剂体外缓释累计释放率曲线。具体实施方式下面将结合本发明中的附图,对本发明的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动条件下所获得的所有其它实施例,都属于本发明保护的范围。下面结合具体实施例,对本发明技术方案作进一步详细说明。实施例1雷帕霉素局部注射制剂的制备(1)一种雷帕霉素局部注射制剂,包括0.02g雷帕霉素、2g乙醇、7g大豆卵磷脂、10g二油酸甘油酯、0.6g泊洛沙姆407。制备方法如下:将0.02g雷帕霉素溶解在2g乙醇中,搅拌溶解完全后,加入7g大豆卵磷脂、10g二油酸甘油酯和0.6g泊洛沙姆407,继续搅拌1h得到流动液体,最后经60co照射的γ射线辐射灭菌,得到雷帕霉素局部注射制剂a1。(2)一种雷帕霉素局部注射制剂,包括0.03g的雷帕霉素、2g乙醇、8g蛋黄卵磷脂,8g二油酸甘油酯、1g聚乙二醇200。制备方法如下:将0.03g雷帕霉素溶解在2g乙醇中,搅拌溶解完全后,加入8g蛋黄卵磷脂、8g二油酸甘油酯和1g聚乙二醇200,继续搅拌0.5h得到流动液体,最后经60co照射的γ射线辐射灭菌,得到雷帕霉素局部注射制剂a2。(3)一种雷帕霉素局部注射制剂,包括0.04g的雷帕霉素、3g乙醇、7g蛋黄卵磷脂,8g三油酸甘油酯、1.2g泊洛沙姆407。制备方法如下:将0.04g雷帕霉素溶解在3g乙醇中,搅拌溶解完全后,加入7g蛋黄卵磷脂、8g三油酸甘油酯和1.2g泊洛沙姆407,继续搅拌2h得到流动液体,最后经60co照射的γ射线辐射灭菌,得到雷帕霉素局部注射制剂a3。(4)一种雷帕霉素局部注射制剂,包括0.05g的雷帕霉素、1g乙醇、6g蛋黄卵磷脂,12g硬脂酸甘油酯、0.8g聚乙二醇400。制备方法如下:将0.05g雷帕霉素溶解在5g乙醇中,搅拌溶解完全后,加入30g蛋黄卵磷脂、60g硬脂酸甘油酯和4g聚乙二醇400,继续搅拌2h得到流动液体,最后经60co照射的γ射线辐射灭菌,得到雷帕霉素局部注射制剂a4。(5)一种雷帕霉素局部注射制剂,包括0.02g雷帕霉素、2g乙醇、7g大豆卵磷脂、10g二油酸甘油酯。制备方法如下:将0.02g雷帕霉素溶解在2g乙醇中,搅拌溶解完全后,加入7g大豆卵磷脂和10g二油酸甘油酯,继续搅拌1h得到流动液体,最后经60co照射的γ射线辐射灭菌,得到雷帕霉素局部注射制剂b1。(6)一种雷帕霉素局部注射制剂,包括0.02g雷帕霉素、2g乙醇、4g大豆卵磷脂、13g二油酸甘油酯、0.6g泊洛沙姆407。制备方法如下:将0.02g雷帕霉素溶解在2g乙醇中,搅拌溶解完全后,加入4g蛋黄卵磷脂和13g二油酸甘油酯,继续搅拌0.5h得到流动液体,最后经60co照射的γ射线辐射灭菌,得到雷帕霉素局部注射制剂b2。(7)一种雷帕霉素局部注射制剂,包括0.03g的雷帕霉素、3g乙醇、11g蛋黄卵磷脂,4g三油酸甘油酯、1.2g泊洛沙姆407。制备方法如下:将0.03g雷帕霉素溶解在3g乙醇中,搅拌溶解完全后,加入11g蛋黄卵磷脂、4g三油酸甘油酯和1.2g泊洛沙姆407,继续搅拌2h得到流动液体,最后经60co照射的γ射线辐射灭菌,得到雷帕霉素局部注射制剂b3。实施例2雷帕霉素局部注射制剂抗稀散性及通针性实验分别取0.5ml实施例1中制备的雷帕霉素局部注射制剂a1-a4、b1-b3,置于5ml离心管中,加入4ml水,观察是否有扩散现象,无扩散现象,说明制剂抗稀散性能良好。扩散记为“-”,未扩散记为“+”。再分别取雷帕霉素局部注射制剂a1-a4、b1-b3,采用1ml灭菌注射器和5号针头进行通针性实验,制剂能顺利注射表明其通针性良好。顺利通过记录为“+”,不能顺利通过记为“-”。测试结果如表1所示。表1:抗稀散性及通针性实验样品号抗稀散性通针性a1++a2++a3++a4++b1-+b2-+b3--本发明的雷帕霉素局部注射制剂具有良好的抗稀散性和通针性,当未加入稳定剂或磷脂的用量偏低时,会导致抗稀散性较差,而磷脂的用量偏高会导致抗稀散性和通针性均达不到制剂的需求。实施例3雷帕霉素局部注射制剂体外缓释实验取实施例1中制备的雷帕霉素局部注射制剂a1-a4、b1-b3,采用透析袋法进行体外释放特性实验考察。释放介质为ph7.4的包含5%吐温20的pbs缓冲液。具体实验步骤为:分别取5g雷帕霉素局部注射制剂加入等量的水,静置0.5h形成液晶。然后加入透析袋中,两头用夹子夹住,将透析袋放入300ml的ph7.4的包含5%吐温20的pbs缓冲液,水浴保持温度为t=37℃,转速为30r/min,将整个体系密封,防止蒸发,分别于第0.5,1,2,3,4,5,6,8,10,12,14,16,18,20、24天取样1ml,每次再补入1ml释放介质。取出的样过0.22μm微孔滤膜,hplc测定雷帕霉素浓度。计算各时间点的累计释放率q,如图1所示。从图1中可以看出,实施例a1-a4具有优异的缓释技术效果,超过20天才会缓释结束,因而证明将雷帕霉素制成的局部注射制剂具有长效缓释的技术效果。而对比例b1-b3的缓释效果较差。其中b1未使用稳定剂,但由于磷脂和甘油酯的配比较好,也有一定的缓释效果,大概10天能够缓释完毕,但由于缺少稳定剂缓释效果劣于实施例。b2和b3磷脂和甘油酯的比例落在本发明用量比例的范围之外,虽然有稳定剂的加入,缓释效果也较差,并且劣于对比例b1。由此证明,磷脂和甘油酯的比例对缓释效果起决定作用,作用大于稳定剂的作用。从最终累计释放率可以看出,所有样品的累计释放率均接近100%,说明采用发明配方制备的雷帕霉素局部注射制剂最终都能够完全释放。实施例4雷帕霉素局部注射制剂稳定性实验温度影响:取同一批次a1的雷帕霉素局部注射制剂适量,分别装于密封洁净的棕色西林瓶中,于4℃、25℃、37℃和60℃温度条件下,分别于第0天、5天和第10天取样,与初始样品对照,比较其外观形状和药物含量的变化,采用hplc法测定含量,考察温度对雷帕霉素局部注射制剂,实验结果如表2所示。结果表明,温度高于25℃会对雷帕霉素局部注射制剂稳定性产生影响,因而雷帕霉素局部注射制剂需要在阴凉处保存。表2:温耋对雷帕霉素局部注射制剂的影响温度(℃)时间(天)外观性状含量(%)40淡黄色油状液体100.1345淡黄色油状液体100.13410淡黄色油状液体100.12250淡黄色油状液体100.13255淡黄色油状液体99.872510淡黄色油状液体99.86370淡黄色油状液体100.13375淡黄色油状液体99.593710黄色加深液体99.42600淡黄色油状液体100.13605黄色加深,沉积87.426010深黄色,凝固76.21长期稳定性:取a1-a4的雷帕霉素局部注射制剂适量,分别装于密封洁净的棕色西林瓶中,于4℃温度条件下,分别于第0天、5天和第10天取样,与初始样品对照,比较其外观形状和药物含量的变化,采用hplc法测定含量,考察温度对雷帕霉素局部注射制剂,实验结果如表3所示。结果表明,在4℃密封保存的条件下,雷帕霉素局部注射制剂的性能稳定。表3:长期稳定性实验结果温度(℃)时间(月)外观性状含量(%)a10淡黄色油状液体100.13a11淡黄色油状液体100.10a12淡黄色油状液体100.02a20淡黄色油状液体100.25a21淡黄色油状液体100.24a22淡黄色油状液体100.24a30淡黄色油状液体99.36a31淡黄色油状液体99.35a32淡黄色油状液体99.30a40淡黄色油状液体100.14a41淡黄色油状液体100.11a42淡黄色油状液体100.09尽管已经示出和描述了本发明的实施例,对于本领域的普通技术人员而言,可以理解在不脱离本发明的原理和精神的情况下可以对这些实施例进行多种变化、修改、替换和变型,本发明的范围由所附权利要求及其等同物限定。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1