白芍总苷在制备治疗甲状腺癌及提高肿瘤放疗增效药物的应用的制作方法
本发明涉及一种中药新用途,特别涉及一种白芍总苷在制备治疗甲状腺癌及提高肿瘤放疗增效药物的应用,属于中医药
技术领域:
。
背景技术:
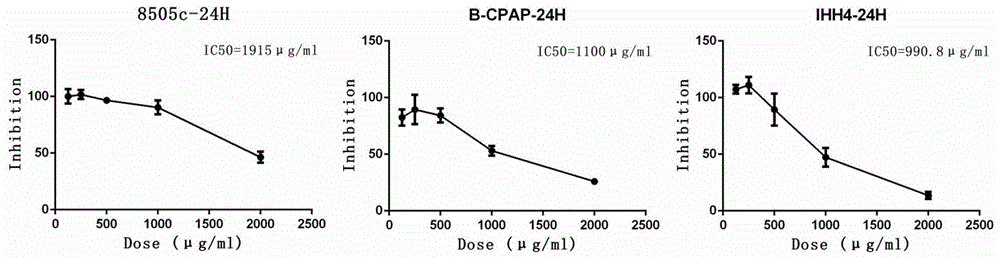
:甲状腺癌(thyroidcancertc)是最常见的内分泌恶性肿瘤,近年来由于发病率快速上升而成为研究热点。甲状腺乳头状癌(papillarythyroidcancer,ptc)及滤泡状癌(follicularthyroidcancer,ftc)占甲状腺癌的90%以上,由于它们在一定程度上保留了甲状腺滤泡细胞的功能,如钠碘转运体(sodiumiodidesymporter,nis)的表达及摄碘的能力、分泌甲状腺球蛋白(thyroglobulin,tg)的能力、依赖于促甲状腺激素(thyrotropin,tsh)生长的方式等,被称为分化型甲状腺癌(differentiatedthyroidcancer,dtc)。dtc通常临床进展缓慢预后好,尤其当dtc仅局限于甲状腺内或仅有累及颈部淋巴结。ptc和ftc的10年存活率分别为93%和85%。远处转移是dtc患者主要的致死原因。dtc远处转移发生率为10%-20%,发生远处转移的患者50%以上有肺转移。最近研究证明发生dtc远处转移者预后差,但远处肺转移的治疗效果要优于累及其他器官如骨骼和脑转移。有研究显示,远处转移病灶的摄碘特征与其预后密切相关,摄碘的患者10年生存率可达56%,而不摄碘患者10年生存率不足10%,这部分碘难治性dtc(radioiodine-refractorydtc,rair-dtc)的早期诊断及后续治疗已成为目前甲状腺癌领域的难点和热点。因此研究rair-dtc放射碘抵抗的机制具有重要科学意义。rair-dtc涵盖所有经过规范的131i治疗后仍出现复发及转移或已知病灶进展的dtc患者。nis是一种dtc细胞基底膜上表达的糖蛋白,可利用细胞跨膜的钠离子浓度梯度将碘逆浓度梯度转运至细胞内,这也是放射性碘治疗dtc的基础。rair-dtc主要是由于nis表达水平的下降或出现基底膜以外的异位表达,致使131i治疗无法奏效。目前研究表明,dtc细胞的碘代谢能力与放射碘抵抗密切相关。碘摄取和有机化是甲状腺细胞碘代谢的两个关键性步骤,其中钠碘转运体(nis)主要介导碘的摄取,甲状腺过氧化物酶(tpo)与碘的有机化密切相关,而促甲状腺激素(tsh)促进了碘代谢的所有步骤。技术实现要素:本发明提供一种白芍总苷在制备治疗甲状腺癌及提高肿瘤放疗增效药物的应用。本发明解决其技术问题所采用的技术方案是:一种白芍总苷在制备治疗甲状腺癌及提高肿瘤放疗增效药物的应用。作为优选,所制备的药物还含有制剂允许的药物赋形剂。本发明的白芍总苷可以作为活性成分,加入药剂学上接受的药物赋形剂或载体,按照药剂学上记载的方法制成制剂。本发明的白芍总苷还可以作为活性成分之一,还含有其他药物,加入药剂学上接受的药物赋形剂或载体,按照药剂学上记载的方法制成制剂。作为优选,所述药物的制剂形式包括液体制剂、固体制剂、胶囊剂、胶丸剂。作为优选,所述药物的给药方式包括注射液、滴注液、粉针剂、颗粒剂、片剂、冲剂、散剂、口服液、糖衣片剂、薄膜衣片剂、肠溶衣片剂、胶囊剂、硬胶囊剂、软胶囊剂、口含剂、颗粒剂、丸剂、膏剂、丹剂、喷雾剂、滴丸剂、崩解剂、口崩片、微丸等。作为优选,所述白芍总苷的制备方法是:取白芍适量,分别加70%乙醇,10倍量,提取2次,每次2h。将药液浓缩至1ml药液含1g生药,采用hpd300大孔树脂纯化麸炒白芍总苷的工艺通过考察确定为:药液加水稀释成每1ml药液含0.1g生药,以上样流速为4bv/h通过hpd300大孔吸附树脂柱(树脂柱径高比为1:11),先5倍柱体积水洗,继以7倍柱体积50%乙醇洗脱,洗脱流速为4bv/h,收集洗脱液,减压回收乙醇,滤过,滤液加3%明胶溶液至不产生沉淀,加乙醇使含醇量达80%,放置过夜,滤过,减压回收乙醇,经高效液相得到质量分数为80%的白芍总苷。作为优选,白芍总苷的使用剂量为每日6-10mg/kg,给药方式为口服。本发明的有益效果是:本发明人经研究发现白芍总苷具有显著的抗甲状腺癌和增强癌细胞的摄碘功能,可以提高放疗敏感性,从而可以制备治疗甲状腺癌方面的药物,以及制备提高肿瘤放疗增效药物。与现有技术比较,本发明涉及的白芍总苷具有如下优点和显著的进步:(1)现有白芍总苷临床用于抗炎与免疫方面如类风湿关节炎,甲状腺炎等;本发明首次发现本制品具有显著的抗甲状腺癌作用;cck-8检测不同浓度白芍总苷给药组对不同的甲状腺癌细胞增殖具有明显抑制作用;流式仪检测显示白芍总苷能够诱导细胞的凋亡,且呈现一定的量效关系;划痕愈合实验证实甲状腺腺癌细胞经白芍总苷干预后细胞迁移或转移能力明显下降;traswell实验证实药物干预后甲状腺细胞侵袭能力明显下降;本研究证明了白芍总苷具有介导tc细胞nis高表达,并具有抗甲状腺癌作用;(2)目前,在甲状腺癌伴有肺远处转患者中,摄碘的10年生存率可达56%,而不摄碘患者10年生存率不足10%,这部分患者的生存期预后极差,目前临床选择随访、观察和对症治疗,无有效治疗药物或其他治疗手段。本发明首次发现本制品具有显著的提高癌细胞中钠碘转运体(nis)表达及定向分布,提高甲状腺癌细胞的摄碘功能,从而改善放疗敏感性:在3种甲状腺癌细胞株中,白芍总苷均具有明显提高nis基因和蛋白的表达;共聚焦显微镜下观察到白芍总苷能介导nis高表达并主要在细胞膜上分布。这些都表明,白芍总苷在治疗甲状腺癌及提高放射敏感性方面具有很好的应用前景,可用于制备治疗甲状腺癌及提高肿瘤放疗增效药物。附图说明图1是白芍总苷给药24h后各细胞的ic50值曲线;图2是白芍总苷对8505c细胞nis蛋白表达的影响照片(40×);图3是白芍总苷对b-cpap细胞nis蛋白表达的影响照片(40×);图4是白芍总苷对ihh4细胞nis蛋白表达的影响照片(40×);图5是白芍总苷对3种甲状腺癌细胞凋亡的影响图;图6是白芍总苷生药对nis基因表达量的影响图;图7是白芍总苷促进各种类型tc细胞nis蛋白高表达图;图8是白芍总苷干预后对8505c细胞转移及侵袭能力的影响照片;图9是免疫荧光显微镜下观察白芍总苷对8505c细胞凋亡及nis表达的影响照片。具体实施方式下面通过具体实施例,对本发明的技术方案作进一步的具体说明。应当理解,本发明的实施并不局限于下面的实施例,对本发明所做的任何形式上的变通和/或改变都将落入本发明保护范围。在本发明中,若非特指,所有的份、百分比均为重量单位,所采用的设备和原料等均可从市场购得或是本领域常用的。下述实施例中的方法,如无特别说明,均为本领域的常规方法。材料与仪器样本:正常甲状腺细胞,b-cpap、8505c、ihh4甲状腺细胞,主要材料见表1,主要仪器见表2。表1主要材料表2主要仪器实施例1白芍总苷的制备方法,具体过程是:取白芍适量,分别加70%乙醇,10倍量,提取2次,每次2h。将药液浓缩至1ml药液含1g生药,采用hpd300大孔树脂纯化麸炒白芍总苷的工艺通过考察确定为:药液加水稀释成每1ml药液含0.1g生药,以上样流速为4bv/h通过hpd300大孔吸附树脂柱(树脂柱径高比为1:11),先5倍柱体积水洗,继以7倍柱体积50%乙醇洗脱,洗脱流速为4bv/h,收集洗脱液,减压回收乙醇,滤过,滤液加3%明胶溶液至不产生沉淀,加乙醇使含醇量达80%,放置过夜,滤过,减压回收乙醇,经高效液相得到质量分数为80%的白芍总苷。实施例2白芍总苷的药理实验1、实验分组细胞、分子生物实验:加上述方法制得的白芍总苷处理72h,白芍总苷浓度为:0.3mg/ml、0.6mg/ml、0.9mg/ml、1.2mg/ml(normal、ihh4、b-cpap);0.5mg/ml、1mg/ml、1.5mg/ml、2.0mg/ml(8505c)。2、ic50筛选药物浓度1)种板:在96孔板中接种细胞悬液(200μl/孔),实验每孔约5000个细胞。2)24h后,pbs洗涤3次。3)药物处理:按照实验需要,进行培养并给予200μl特定浓度的药物溶液刺激,处理一段适当的时间(例如:24h)。4)pbs洗涤3次。5)每孔加入200μlcck-8溶液。用加相应量细胞培养基和cck-8但不加细胞的孔作为空白对照。在细胞培养箱内继续共孵育0.5-2h。6)用酶标仪测定在450nm处的吸光值。3、wb&qrt-pcr蛋白及核酸提取逆转录:qrt-pcr和westernblot(蛋白提取)检测碘代谢相关基因(tshr、tpo和nis)及蛋白的表达,评估碘代谢相关基因表达恢复或抑制情况。sds-page电泳和转膜1)取干净的1.5mm玻璃板,按说明书在制胶架上装好。2)配制10%分离胶和5%浓缩胶10%分离胶加入各物质后充分混匀,灌分离胶,然后用水液封。5%浓缩胶加入各物质后混匀,灌浓缩胶。3)配制好5%浓度的sds-page浓缩胶并注入分离胶的上端,小心插入与玻璃板厚度相适应的样品梳子,避免产生气泡。4)成层胶聚合后,小心拔去样品梳子,然后加入1×tris-gly的电泳缓冲液。5)吸取适量样品上清加入样品孔中,在样品旁的孔中加入预染的蛋白marker,未添加样品上清的孔中,加入1×sds上样缓冲液保持胶面平衡。6)打开电源,电压开始设置为80v,当蛋白样品进入分离胶后,电压可提高到120v。参照预染marker的位置,待目的条带进入凝胶最佳分离区(大约凝胶的2/3)时,停止电泳。7)预先将转膜液4℃预冷。8)在托盘上打开转移盒,靠近阴极侧的内面铺上已经用转膜缓冲液浸湿的有孔维垫,其上放三层浸有转膜缓冲液的滤纸,注意排净气泡。9)小心撬开玻璃板,将胶放置含有转膜液的托盘内,将含有目的条带的分离胶切下,用转膜液浸泡后置于滤纸上。10)在凝胶上铺上经甲醇和转膜液浸湿的pvdf膜,胶和膜之间不能存有气泡,膜、滤纸和凝胶的大小,大致相同。11)在pvdf膜上再放三层浸过转膜液的滤纸,注意排净气泡。12)放上第二块海绵垫,使整个转印夹层依次形成“纤维垫—滤纸—凝胶—nc膜—滤纸—纤维垫”层次,关闭转印夹,放入转移槽中,槽中灌满转膜液。13)打开电源,稳流200ma,120min。14)转膜结束后,取出pvdf膜并作好标记,用tbst洗膜10min×3次。免疫印迹封闭及抗原抗体反应1)封闭:将pvdf膜放入孵育盒中,加入含5%脱脂奶粉的封闭液,摇床振荡1.5~2h;2)封闭结束后,用tbst洗膜10min×3次;3)将膜放入含一抗caspase-3(1:1000)稀释液的孵育盒中,4℃摇床振荡孵育过夜;4)第二天取出,室温振荡30min,吸弃一抗,tbst洗10min×3次;5)用5%脱脂奶粉封闭液稀释二抗,室温摇床振荡反应1~2h;6)二抗反应结束后,回收二抗。然后用tbst洗膜5~10min×3次。x胶片感光、显影、定影1)将试剂盒中a和b两种试剂在保鲜膜上等体积混合形成曝光液;1min后,将膜蛋白面朝下与此混合液充分接触;1min后,将膜移至另一保鲜膜上,去尽残液,包好,放入x-光片夹中。2)在暗室中,将1×显影液和定影液分别到入塑料盘中;在红灯下取出x-光片,用切纸刀剪裁适当大小(比膜的长和宽均需大1cm);3)打开x-光片夹,把x-光片放在膜上,一旦放上,便不能移动,关上x-光片夹,开始计时;根据信号的强弱适当调整曝光时间,一般为1min或5min,也可选择不同时间多次压片,以达最佳效果;4)曝光完成后,打开x-光片夹,取出x-光片,迅速浸入显影液中显影,待出现明显条带后,即刻终止显影。显影时间一般为1~2min(20~25℃),温度过低时(低于16℃)需适当延长显影时间;5)显影结束后,马上把x-光片浸入定影液中,定影时间一般为5~10min,以胶片透明为止;用自来水冲去残留的定影液后,室温下晾干。应注意的是:显影和定影需移动胶片时,尽量拿胶片一角,手指甲不要划伤胶片,否则会对结果产生影响。4、免疫荧光1)将3.5cm培养皿(或六孔板)中的旧培养液吸走,然后加入1-2ml预冷的4%多聚甲醛(pfa),固定10min;2)10min结束,吸出多聚甲醛(pfa),每孔加入1ml-2ml0.5%tritonx-100,处理约2min;3)然后吸出0.5%tritonx-100,每孔加入1-2mlpbs,漂洗,随即吸出pbs;4)每个盖玻片上滴加80μl一抗(一抗稀释比例根据说明书,用5%goatserum稀释),孵育1h(从四个角滴加,使其慢慢融合为一体),吸走一抗;5)然后再加入1-2ml0.5%tritonx-100,吸走,然后每孔加1-2mlpbs,漂洗;6)吸出pbs,每个盖玻片上加入80μl二抗(二抗稀释比例根据说明书,用5%goatserum稀释,一般1:500),室温下孵育0.5h,吸走二抗;7)每孔加入2mlpbs,漂洗;8)吸出pbs,每孔加入核染试剂(dapi或hoechst33342,一般1-2min即可,具体视情况而定)。9)吸出染核试剂,用pbs漂洗3次,再加1mlpbs,保持湿润;10)先在载玻片上加入适量封片剂(mountingmedia,抗荧光淬灭封片剂,一般放在-20℃),用细针头将盖玻片挑起,细胞的一面朝下压到载玻片上,从盖玻片的一边向另一边压过去,把多余的mountingmedia用吸水纸吸走。11)共聚焦荧光显微镜下观察拍照。12)监测nis定位于细胞膜情况:免疫荧光:应用共聚焦显微镜和细胞免疫荧光方法监测nis定位于细胞膜情况,直观评估nis膜定位情况。5、流式检测准备预热的无edta的胰酶、pbs、含血清的培养基1)吸取6孔板细胞上清,500μl-1mlpbs轻轻洗涤2次;(1ml移液枪对细胞冲击比较大,注意操作手劲)2)每孔加入无edta胰酶200μl,摇匀,放入培养箱,不同的细胞消化时间不同;3)待细胞消化,贴壁细胞形态变圆润,但不至于从培养板上脱落;(切勿消化过头)4)细胞消化结束,加入含血清培养基500μl中止消化;5)轻轻吹打细胞,细胞即可脱落;6)收集细胞到1mlep管中,1000rpm离心3min,用1ml移液枪移弃上清,可留50μl左右液体。pbs洗涤2次,重悬时尽量不要用枪头去重悬,可减少机械损伤和细胞损耗。7)用去离子水按1:3稀释bindingbuffer(4mlbindingbuffer+12ml去离子水)。8)用250μlbindingbuffer重新悬浮细胞。9)取100μl的细胞悬液于1ml离心管中,加入5μlannexinv/fitc和10μl20μg/ml的pi溶液。10)混匀后于室温避光孵育30分钟。11)重悬细胞,过300目滤膜,移至新离心管。流式细胞仪分析。6统计学处理采用excel统计、zen以及graphpad软件进行数据分析,所有数据以均值±标准差表示。①cck-8检测不同药物浓度处理24h后的细胞增殖不同浓度白芍总苷给药组作用于不同的甲状腺癌细胞24h后的ic50结果见图1。由图中可知,白芍总苷对8505c、b-cpap、ihh4细胞的ic50值分别为1915μg/ml、1100μg/ml、990.8μg/ml。②免疫荧光观察nis细胞膜定位激光共聚焦观察白芍总苷作用于8505c,b-cpap和ihh4三株细胞48h后,不同给药浓度对各细胞的nis蛋白的表达的影响见图2-4,高剂量的白芍总苷均能明显能提高各个类型tc细胞中的nis表达,并主要分布在细胞膜上。③白芍总苷促进tc细胞凋亡尤其是dtc细胞对细胞凋亡率的影响:白芍总苷作用3种甲状腺细胞48小时后,结果显示白芍总苷浓度为0.3mg/ml时,细胞凋亡率均升高,与对照组相比有统计学意义(p<0.01);随着给药浓度加大,各种细胞的凋亡率逐渐上升,且均存在统计学意义(p<0.01),尤其对dtc细胞株最为明显,结果见图5和表3。表3白芍总苷3种甲状腺癌细胞凋亡的影响(%,x±s,n=3)备注:与对照组相比,*p<0.05,**p<0.01④qrt-pcr检测白芍总苷生药对nis基因表达量的影响从图6可以看出,与对照组比较,8505-c、b-cpap和ihh4细胞的nis基因相对表达量随着给药浓度的上升而逐渐增加,呈现浓度依赖性,而超过0.9mg/ml到达1.2mg/ml给药浓度,nis基因相对表达量明显降低。⑤wb检测白芍总苷对nis蛋白表达量的影响从图7可以看出8505c、bcpap、ihh4在白芍总苷处理后nis蛋白表达均明显升高,但8505c细胞上升比较弱,而dtc细胞株中ihh4上升最为明显。⑥划痕愈合、transwell和免疫荧光实验研究划痕愈合实验证实8505c细胞株经白芍总苷干预后细胞迁移或转移能力明显下降;traswell实验证实白芍总苷干预后8505c细胞侵袭能力明显下降;免疫荧光显微镜下观察到白芍总苷促进8505c细胞凋亡和提高细胞膜上nis表达,数据见图8、图9。(1)本发明通过不同的甲状腺癌细胞研究首次发现本制品具有显著的抗甲状腺癌作用:cck-8检测不同浓度白芍总苷给药组对不同的甲状腺癌细胞增殖具有明显抑制作用;流式仪检测显示白芍总苷能够诱导细胞的凋亡,且呈现一定的量效关系;划痕愈合实验证实甲状腺腺癌细胞经白芍总苷干预后细胞迁移或转移能力明显下降;traswell实验证实药物干预后甲状腺细胞侵袭能力明显下降;(2)本发明首次发现本制品具有显著的提高癌细胞中钠碘转运体(nis)表达及定向分布,提高甲状腺癌细胞的摄碘功能,提高放疗敏感性:在3种甲状腺癌细胞株中,白芍总苷均具有明显提高nis基因和蛋白的表达;共聚焦显微镜下观察到白芍总苷能介导nis高表达并主要在细胞膜上分布。(3)白芍总苷的最佳推荐使用剂量为每日6-10mg/kg,给药方式为口服。综上所述,白芍总苷在治疗甲状腺癌及提高放射敏感性方面具有很好的应用前景;白芍总苷在治疗甲状腺癌及提高放射敏感性方面具有很好的应用前景,可用于制备治疗甲状腺癌及提高肿瘤放疗增效药物。实施例2白芍总苷提取物片剂或其他保健品类白芍总苷提取物片剂的成分是按处方量将白芍总苷提取物(按实施例1方法制得)加入微晶纤维素、微粉硅胶、硬脂酸、乳糖混匀,制成颗粒后加入硬脂酸镁,混匀,压片,即得(每片含白芍总苷大于80mg)。成人推荐口服用量2-4片/次,每日2-3次。实施例3白芍总苷提取物胶囊或其他保健品类白芍总苷提取物胶囊的成分是成分每片用量白芍总苷提取物100mg微晶纤维素35mg微粉硅胶15mg硬脂酸15mg乳糖12mg按处方量将白芍总苷(按实施例1方法制得)加入微晶纤维素、微粉硅胶、硬脂酸、乳糖混匀,制成颗粒后,填装入0号硬胶囊壳,打光即制得(每粒胶囊含白芍总苷大于80mg)。成人推荐口服用量2-4粒/次,每日2-3次。以上所述的实施例只是本发明的一种较佳的方案,并非对本发明作任何形式上的限制,在不超出权利要求所记载的技术方案的前提下还有其它的变体及改型。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1