一种万古霉素修饰的黑磷量子点抗菌剂、制备方法及应用与流程
本发明属于抗菌技术领域,具体涉及一种万古霉素修饰的黑磷量子点抗菌剂、所述抗菌剂的制备方法及在制备抗菌产品中的应用。
背景技术:
公开该背景技术部分的信息仅仅旨在增加对本发明的总体背景的理解,而不必然被视为承认或以任何形式暗示该信息构成已经成为本领域一般技术人员所公知的现有技术。
各种致病细菌在自然界里分布十分广泛,它们的传播和感染能够引发多种疾病,从而威胁人类的健康。杀灭细菌或者阻止细菌繁殖是当前抗菌的主要思路。在传统的多类抗菌药物中,抗生素是临床应用范围最广、品种最多的一大类药品,具有较好的杀菌效果。然而,过度使用抗生物会带来一系列严重问题:耐药性、毒副作用、菌群失调等。但是,近年来研发新的抗生素陷入十分艰难的困境。一方面过度开发的土壤资源导致无法从土壤微生物中筛选出新的抗生素,而合成化学只在某一类抗生素上做改进导致种类单一;另一方面开发抗菌需要的周期长(10年以上)、费用昂贵(10亿美元以上),而一代耐药细菌的产生却仅仅只需两年,抗菌药物的研制速度远低于耐药细菌的发展速度。因而,在寻找下一代抗生素的同时,转换思路找到新的抗菌机理,研究开发新一代、绿色、广谱、经济的抗菌药物和材料非常之急迫。
近年来,纳米材料抗菌功能研究已成为纳米医药研究领域内的一个新的交叉学科前沿热点。二维纳米材料除了拥有良好的生物相容性,还拥有非常良好的可修饰性。随着纳米材料制备和表征技术的发展日新月异,人们制备了越来越多的新型纳米材料,比如磷烯。新型二维纳米材料磷烯,除了具备石墨烯的二维结构外,其自身的特殊电学性质使它们还具备了氧化能力,能够显著增强其抗菌能力。同时,磷是生物体内必须元素,使其在生物医学领域的应用具有无可比拟的优势。
万古霉素属于三环糖肽类抗生素,目前,对万古糖近来研究表明万古霉素联合用药对某些细菌的耐药性有一定的抑制作用,因此,研究一种万古霉素修饰黑磷量子点抗菌剂具有良好的前景。
技术实现要素:
基于上述研究背景,本发明设计采用抗菌药物与二维纳米材料联合使用的方式获取抗菌效果提升的活性成分。依据本发明的研究,将万古霉素修饰于黑磷量子点表面,能够显著的提升药物体外抑菌活性,扩大药物的抑菌范围,有望降低药物使用剂量,减少耐药株的产生。
依据上述技术效果,本发明提供以下技术方案:
本发明第一方面,提供一种抗菌剂,所述抗菌剂为万古霉素修饰的黑磷量子点。
本领域公知,万古霉素是一种糖肽类抗生素,用于治疗其他抗生素治疗均无效的严重感染,肾毒性较高、抑菌谱窄,只用于革兰氏阳性菌。依据本发明的研究结果,黑磷量子点单用应用于细菌时的抑菌效果不明显,但采用万古霉素修饰黑磷量子点之后抑菌效果提升了四倍作用,并且采用万古霉素修饰后的黑磷量子点不仅对于革兰氏阳性菌具有抑制效果,对于革兰氏阴性菌也表现显著的抑制作用。修饰后黑磷量子点扩大了万古霉素的抑菌谱,并且可以降低万古霉素的用量,减少耐药情况的发生,作为抗菌活性成分开发成为抗菌药物、与其他抗菌活性成分联合制备抗菌药物,或将其与表面活性剂类成分联合用于制备具有抑菌效果的洗护产品。
本发明第二方面,提供第一方面所述抗菌剂的制备方法,所述制备方法包括将盐酸万古霉素、n-羟基琥珀酰亚胺混合溶解后加入1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐、n-boc-(亚乙二氧基)二乙胺及n,n-二异丙基乙胺,混合后离心,将离心所得沉淀部分干燥,采用二氯甲烷、三氟乙酸及乙醚处理所述沉淀部分,之后加入黑磷量子点得到所述抗菌剂。
本发明第三方面,提供第一方面所述抗菌剂在制备抗菌产品中的应用。
以上一个或多个技术方案的有益效果是:
本发明的万古霉素修饰的黑磷量子点抗菌剂及其制备方法,新型光电纳米材料黑磷量子点为主要抗菌组分,将其表面功能化,与抗生素万古霉素相结合。黑磷量子点仅有单原子层厚度,比表面积非常大,其原子厚度的“锋利”边界可以直接损伤细菌的细胞膜;而且,黑磷量子点具有优异的光学性能,能够诱导活性氧的产生,引起菌体生物系统的过氧化反应;修饰后的抗菌材料,当进入生物微环境中仍然会吸附蛋白质、核酸、磷脂等生物大分子,在其表面形成二维纳米材料-生物大分子复合物,能够阻碍材料与细菌的接触,从而提高抗菌材料的抗菌效果。本发明制备出的万古霉素修饰的黑磷量子点抗菌剂生物相容性好、抗菌效果强。
附图说明
构成本发明的一部分的说明书附图用来提供对本发明的进一步理解,本发明的示意性实施例及其说明用于解释本发明,并不构成对本发明的不当限定。
图1为实施例1中所述黑磷量子点的tem图。
图2为实施例2中所述黑磷量子点对细菌抑制实验照片图;
其中,图2a为培养2h的空白对照组,图2b为加入量子点黑磷10微升的实验组,图2c为加入量子点黑磷20微升的实验组。
图3为实施例2中所述盐酸万古霉素的质谱图。
图4为实施例2中所述中间产物的质谱图。
图5为实施例2中所述万古霉素修饰黑磷量子点的质谱图。
图6为实施例2中所述盐酸万古霉素、黑磷量子点及万古霉素修饰的黑磷量子点的紫外荧光光谱图。
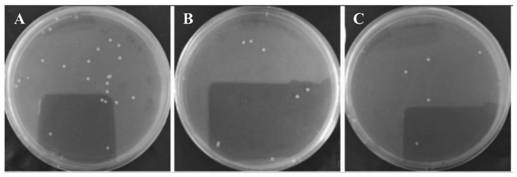
图7为实施例2中所述万古霉素修饰后的黑磷量子点杀菌效果照片图;
其中,图7a为培养1h的空白对照组,图7b为加入万古霉素修饰的黑磷量子点10微升,图7c为加入万古霉素修饰的黑磷量子点20微升。
图8为量子点黑磷与万古霉素修饰后量子点黑磷杀菌效果直方图。
具体实施方式
应该指出,以下详细说明都是例示性的,旨在对本发明提供进一步的说明。除非另有指明,本文使用的所有技术和科学术语具有与本发明所属技术领域的普通技术人员通常理解的相同含义。
需要注意的是,这里所使用的术语仅是为了描述具体实施方式,而非意图限制根据本发明的示例性实施方式。如在这里所使用的,除非上下文另外明确指出,否则单数形式也意图包括复数形式,此外,还应当理解的是,当在本说明书中使用术语“包含”和/或“包括”时,其指明存在特征、步骤、操作、器件、组件和/或它们的组合。
正如背景技术所介绍的,为了进一步开发抗菌活性成分,本发明提出了一种万古霉素修饰的黑磷量子点抗菌剂作为抗菌活性成分。
本发明第一方面,提供一种抗菌剂,所述抗菌剂为万古霉素修饰的黑磷量子点。
优选的,所述万古霉素通过共价键与黑磷量子点结合。
优选的,所述黑磷量子点尺寸为1.5-2nm。
优选的,所述黑磷量子点与万古霉素的质量比为1:18~22。
本发明第二方面,提供第一方面所述抗菌剂的制备方法,所述制备方法包括将盐酸万古霉素、n-羟基琥珀酰亚胺混合溶解后加入1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐、n-boc-(亚乙二氧基)二乙胺及n,n-二异丙基乙胺,混合后离心,将离心所得沉淀部分干燥,采用二氯甲烷、三氟乙酸及乙醚处理所述沉淀部分,hplc分离后加入黑磷量子点得到所述抗菌剂。
优选的,所述制备方法具体步骤如下:将盐酸万古霉素、n-羟基琥珀酰亚胺溶于dmso中,冷却所述溶剂后加入1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐(edc),混合后放入冰浴中,继续加入n-boc-(亚乙二氧基)二乙胺及n,n-二异丙基乙胺(dipea)搅拌一夜,加入丙酮离心得到沉淀部分;通过液相分离得到所述样品,将样品依次通过二氯甲烷、三氟乙酸的混合液及乙醚进行处理;加入黑磷量子点溶液,调节ph至7~8得到所述万古霉素修饰的黑磷量子点。
优选的,将沉淀部分依次通过二氯甲烷、三氟乙酸的混合液及乙醚进行处理的方式如下:将所述样品置于二氯甲烷、三氟乙酸的混合液中冰浴条件下搅拌0.8~1.2h,去除溶剂部分,再分次缓慢加入冷乙醚溶液,去掉乙醚并进行干燥。
优选的,所述通过液相分离得到所述样品,所述液相条件为甲醇/水(v:v=90:10);保留氨基脱保护产物,干燥后得到所述样品氨基-(亚乙二氧基)二乙胺-万古霉素。
进一步优选的,所述二氯甲烷与三氟乙酸混合液中,二氯甲烷与三氟乙酸的体积比为3:1.5~2.5。
进一步优选的,所述样品加入黑磷量子点溶液后,采用naoh溶液调节ph至7~8,离心得到上清部分,水洗后透析得到所述万古霉素修饰的黑磷量子点。
优选的,所述黑磷量子点的制备方法包括以下步骤:将黑磷置于n-甲基吡咯烷酮(nmp)试剂中分散均匀,在碱性条件下加热反应后获取上清部分中的黑磷量子点抗菌剂。
进一步优选的,黑磷量子点的制备方法具体步骤如下:在惰性气体保护下将黑磷晶体加入nmp中分散均匀,将黑磷的nmp溶液与碱在120~160℃、惰性气体保护条件下反应4~8h;反应结束后,离心得到上清黑磷,干燥后即为黑磷量子点。
更进一步的,所述黑磷晶体研磨成粉末状之后加入nmp中,通过超声分散均匀。
更进一步的,所述碱为氢氧化钠,所述黑磷与氢氧化钠的质量比为1:9~11。
更进一步的,所述惰性气体为氮气。
更进一步的,所述离心方式如下:将反应后的溶液在6000~8000r离心获取上清部分,继续在15000~16000r转速下离心所述上清部分得到上清黑磷,水洗干燥后得到黑磷量子点。
本发明第三方面,提供第一方面所述抗菌剂在制备抗菌产品中的应用。
优选的,所述抗菌产品包括抗菌药物或洗护产品。
进一步优选的,所述抗菌药物用于抑制革兰氏阳性菌及革兰氏阴性菌。
进一步优选的,所述抗菌药物包括第一方面所述抗菌剂,还包括药学上所述必须的辅料。
进一步优选的,所述抗菌药物包括第一方面所述抗菌剂,还包括其他抗菌活性成分。
为了使得本领域技术人员能够更加清楚地了解本发明的技术方案,以下将结合具体的实施例详细说明本发明的技术方案。
实施例1
(1)将100mg的黑磷晶体研磨成粉末状,在氮气的保护下存储于100ml的n-甲基吡咯烷酮(nmp)溶液中。取10ml黑磷的nmp溶液超声15min,待溶液混合均匀后,在250ml的三角烧瓶中加入10ml的黑磷的nmp溶液、90ml的nmp、100mg的naoh,在140℃氮气的保护下,搅拌反应6h。反应结束后,冷却至室温。将反应后的溶液在7000r的转速下离心20min,得到底部黑磷和上清液。再将上清液在15100r的转速下离心20min,得到上清黑磷,将上清黑磷水洗3次,自然晾干,既得黑磷量子点抗菌剂,其tem图如附图1所示。
(2)以氯化钠10g/l、酵母提取物5g/l、胰蛋白胨10g/l的比例配置细菌培养液,并进行高温高压灭菌,灭菌后取出得到lb培养液,在无菌工作台中冷却至室温。准备若干个10ml的试管,分别倒置8ml,在无菌工作台中用接种环向培养液中接种大肠杆菌。将接种细菌后的离心管置于恒温摇床中培养,12小时后取出。测菌液在600nm处的od值并将其用蒸馏水稀释到0.1(1.0*108cfu/ml),并再次稀释1000倍用于下一步实验。在上述lb培养液组成的基础上加入20g/l琼脂粉,再次灭菌。将灭过菌的盛有培养基的试剂瓶和培养皿放于无菌工作台中,左手打开培养皿盖,右手迅速将培养基倒入培养皿中,每皿约倒入10毫升,以铺满皿底为度,待培养基冷却至固体后,盖上培养皿盖,缝隙处用密封纸密封好用于下一步的实验。
(3)取一定量的黑磷量子点,稀释至0.1mg/ml备用。取稀释好的菌液各200μl,分别加入黑磷量子点10微升,20微升,恒温箱37℃培养0.5h、1h、2h,取出混合培养液,稀释1000倍后取10微升涂布到培养皿,恒温箱内放置过夜,计算菌斑个数。
实施例2
(1)同实施例1中的步骤(1)。
(2)称取盐酸万古霉素0.1040g(70μmol,1当量),n-经基琥珀酰亚胺(84μmol,1.2当量)0.0097g溶于2ml干燥的dmso中,将混合物溶液置于冰水混合物中冷却到0℃,加入edc(1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐,84μmol,1.2当量)0.161g,搅拌30min,放入冰水混合物中加入n-boc-(亚乙二氧基)二乙胺(77μmol,1.1当量)0.0191g及dipea(860μmol,2.4当量)0.15mol,搅拌一夜。将搅拌一夜的溶液置于离心管中,加入丙酮,离心10min,将上清液取出,封好置于冰箱,将沉淀也封好放入冰箱冷藏。将冷藏与冰箱的沉淀用色谱甲醇溶解,离心取出上清液,用液相色谱分离产物,将产物旋蒸,冷藏,冻干。取出冻干后的样品,得絮状沉淀物,用色谱甲醇溶解,旋蒸后真空干燥。将所得样品,加入1.5ml二氛甲烷和1ml三氟乙酸在冷浴下搅拌1h,37℃旋干,每次加入0.5ml的冷乙轻轻摇晃,把乙醚吸掉,真空干燥。将样品配成1.5mg/ml短链产物,取其2ml,加入3ml的50μg/ml量子点,用1mmol/lnaoh调节ph至7.4。将此溶液离心5min,收集上清液,用水清洗。用100ml的透析袋透析,每2h换一次水,共8-12h,既得万古霉素修饰的黑磷量子点抗菌剂。
(3)同实施例一的步骤(2)。
(4)准备已修饰的黑磷量子点0.1mg/ml,取稀释好的菌液各200微升,分别加入已修饰的量子点10微升,20微升,在恒温培养箱培养0.5h,1h,取出混合培养液再次稀释1000倍后取10微升涂布到培养皿,过夜培养后计算菌斑个数。
如图2所示,从图中可以看出黑磷量子点在培养2h后表现出了较为优异的杀菌效果,且杀菌能力随着黑磷量子点浓度的增加而增强,但在混合培养液培养0.5h,1h后,黑磷量子点并未表现出特别明显的杀菌效果;从图3、图4、图5的质谱图中可以看出,原料盐酸万古霉素的峰值在1450,合成的中间产物的峰值在1680,说明万古霉素酰胺中的羧基与n-boc-(亚乙二氧基)二乙胺的氨基成功缩合;脱boc后的最终产物的峰值在1579,说明脱boc成功,产物合成成功;从图6所示的紫外荧光光谱中可以看出,单独的黑磷量子点无紫外吸收,但经万古霉素修饰后的量子点明显有了吸收峰,说明万古霉素已经成功的负载在黑磷量子点上;图7为修饰的量子点黑磷在培养1h后表现出的杀菌效果。为了直观的表现出修饰前量子点黑磷与修饰后量子点黑磷的杀菌效果的不同,本实施例将同为培养一小时后材料加入量10微升、20微升后的杀菌率进行比较,如图8,可以看出经万古霉素修饰后的黑磷量子点杀菌率高于修饰前的黑磷量子点。
以上所述仅为本发明的优选实施例而已,并不用于限制本发明,对于本领域的技术人员来说,本发明可以有各种更改和变化。凡在本发明的精神和原则之内,所作的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!