一种柔性磁兼容的植入式脑电电极阵列及其制备方法与流程
1.本发明属于生物医学领域,具体涉及一种柔性磁兼容的植入式脑电电极阵列及其制备方法。
背景技术:
2.脑电信号是大脑神经元细胞体生理活动所产生的电位综合,具有丰富的大脑活动信息。脑电信号与脑区域、脑状态有着密切的关系,可以反映出其他物理信号无法或不方便测量和获取的信息,从而成为人类研究脑活动机制、诊断脑疾病的重要依据。
3.脑电电极可大致分为植入式与非植入式两种,其中非植入式电极一般指脑电图(英文:electroencephalograph,简称:eeg),能无创地对大脑活动进行观察和记录,一般为电极帽形式,通过从头皮的特定位置采集和记录信号,其优点为较为安全,缺点为信号微弱且噪声较强。植入式电极则多指皮层脑电图(英文:electrocorticography,简称:ecog)和穿刺型皮质内电极iris(intracortical recordinginterfaces,简称iris)。其中ecog属于非穿刺式脑电信号检测方式,通过将电极植入脑部贴附在硬脑膜上方或者下方,记录神经元的电生理活动;而iris则需要刺入脑组织,显然可以获得更强大质量更高的脑电信号。因此在脑电信号的检测和脑科学研究中,植入式电极有着广阔的应用前景。
4.但植入式电极也面临着一系列的问题,例如当电极长期植入脑组织之后,会引发炎性反应。影响植入电极炎性反应的因素很多,包括:第一是电极植入时引起的创伤:植入创伤与电极的大小,电极表面的物理性质以及植入手术操作有关。要想减小电极植入时所引起的创伤,首先电极表面应该光滑无棱角,尽可能柔软,这就是所谓的结构相容性;第二个影响炎性反应的因素是:电极的植入方法;第三,电极相对于脑组织的移动,会使进入脑组织的血清增加。
5.要解决这些问题,第一就是减小电极的尺寸,发展微型植入式神经电极;第二是降低神经电极与脑组织之间的机械不匹配,也就是弹性模量不匹配;第三是优化电极表面的物理性质和植入方法及操作,提升结构相容性。从而新电极植入方式、电极结构以及电极材料的研究与发展都十分有意义。
6.传统的植入式电极,例如ecog电极对于脑电信号的观测停留在脑皮层的阶段,虽然信号强度已经远远大于非植入式的eeg电极,但仍可以深入至皮质中获取信号。而对于穿刺型电极来说,传统的电极,例如已经获得广泛应用的犹他阵列电极,虽然拥有更深的刺入深度,但在硬度上无法与脑组织的弹性模量匹配,从而容易引起引起周围脑组织发炎。
7.考虑到这个理念,一个理想的植入式电极应当满足以下条件:(1)便于植入,且植入创伤小;(2)与脑组织弹性模量匹配,以减轻炎症反应;(3)实现结构相容,电极表面应该光滑无棱角;(4)电极阻抗应尽量小,以记录高质量的信号。
8.完全满足以上所有需求的电极是很稀少的,因此,设计一种易植入、柔性、记录信号质量高的植入式电极非常必要。
技术实现要素:
9.本发明的目的是提供一种柔性磁兼容植入式脑电电极阵列及其制备工艺。该电极通过头部圆环结构用以辅助植入脑组织,通过大面积的触点与脑组织接触以获取信号,经过金属电极层传输信号,由预留的电极接口连接至外部采集设备以完成对脑电信号的采集。
10.为实现上述发明目的,本发明提供以下技术方案:
11.一种柔性磁兼容植入式脑电电极阵列,该电极阵列为双面电极,以垂直于大脑皮层的方向被植入皮层内部;该电极包括六层,从下到上,依次为第一柔性封装层、第一金属电极层、第一柔性衬底层、第二柔性衬底层、第二金属电极层、第二柔性封装层;所有的柔性封装层和柔性衬底层选自生物相容性材料;所述第一金属电极层和第二金属电极层头部部分裸露,作为电极触点,尾部部分裸露,作为电极接口;位于所述头部和尾部的中间部分作为电极通道;
12.整个电极的头部设置引导孔,辅助电极的植入。
13.进一步地,所有的柔性封装层和柔性衬底层选自以下材料中的任意一种:聚酰亚胺、聚二甲基硅氧烷、聚对苯二甲酸乙二醇酯、聚对二甲苯和光刻胶;柔性封装层和柔性衬底层的厚度为1
‑
100μm。这些材料均拥有良好的化学稳定性、易加工性能、柔软和延展性。
14.进一步地,所有的衬底层和封装层采用同种材料,可以有效的防止衬底层和封装层结合不够紧密而产生渗漏。
15.进一步地,第一金属电极层和第二金属电极层选自银、金、铂、铜中的任意一种,金属电极层厚度0.1~100μm。这些金属有良好的生物兼容性、抗腐蚀性能和电导率,使得电极在拥有极小的截面的同时,拥有较大的电导率,从而记录到质量更高的信号。
16.进一步地,所述牺牲层材料为pmma或光刻胶。牺牲层在工艺步骤上起着连接基片和柔性衬底层的作用,使得脑电电极在制备时可以固定在用于支撑的基片上。
17.进一步地,第一金属电极层和第二金属电极层的电极触点为带有圆角的矩形,且电极触点与电极通道连接处通过圆弧过渡;电极触点面积为100~3000μm2,电极通道宽度为 1~50μm,电极通道数为2~100个。相比较于细长的电极通道,电极触点面积很大且过渡平滑,增加了与组织间的接触面积,减小接触电阻,提高采集到的信号质量。
18.进一步地,第一金属电极层和第二金属电极层的电极触点修饰有导电聚合物或碳纳米管,提高信号质量。修饰导电性能和生物相容性良好导电聚合物将有助于形成双电层的电荷分布。当金属置于电解液中后,金属和电解液的界面就会发生化学反应,并在该界面形成双电层的电荷分布,进而改进电极性能。同时,由于修饰使得电极触点被聚吡咯包覆,呈现疏松多孔结构,有效增加电极触点和组织的接触面积,提高了可获取的脑电信号的质量。
19.与现有技术相比,本发明具有的有益效果为:
20.(1)该柔性磁兼容植入式脑电电极阵列的衬底和封装层材料均为柔性材料,且电极通道宽度小,总体形状为细长形,在植入过程中及植入后对组织的创伤均比较小。
21.(2)该柔性磁兼容植入式脑电电极阵列头部具有引导孔的结构,可用于辅助植入,解决了本身电极材料较软植入困难的问题,同时可由外部植入设备进行精准定位,达到准确植入的效果。
22.(3)该柔性磁兼容植入式脑电电极阵列的电极触点面积设计较大,且过渡平滑,有效的增大了与组织间的接触面积,同时降低了信号传输的阻抗。
23.(4)该柔性磁兼容植入式脑电电极阵列的电极触点处可采用导电聚合物或碳纳米管等材料进行修饰,增加了触点与组织的接触面积,有效的增大了可获取的脑电信号的强度,改进电极性能。
24.(5)该柔性磁兼容植入式脑电电极阵列的电极触点封装层外可增加氧化铝保护层,可减轻组织反应,增强生物相容性。
25.(6)该柔性磁兼容植入式脑电电极阵列采用微纳加工工艺完成制作,工艺一致性较好,易于批量生产。
附图说明
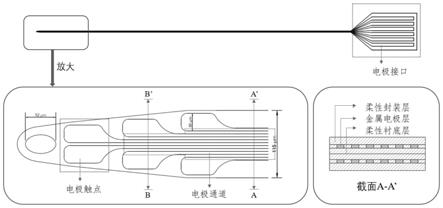
26.图1是实施例提供柔性磁兼容植入式脑电电极阵列的结构示意图;
27.图2以图1的截面bb’截面为例的柔性磁兼容植入式脑电电极阵列的工艺流程图;
28.图3是实施例提供的柔性磁兼容植入式脑电电极阵列的掩模版,其中(a)为金属电极层图形(负片),(b)为电极触点及电极接口部分图形(正片),(c)为电极触点及电极接口部分图形(负片),(d)为电极轮廓图形(负片);
29.图4是实施例提供的柔性磁兼容植入式脑电电极阵列的实物图;
30.图5是实施例提供的柔性磁兼容植入式脑电电极阵列的测试结果图。
具体实施方式
31.下面根据附图和优选实施例详细描述本发明,本发明的目的和效果将变得更加明白,应当理解,此处所描述的具体实施例仅仅用以解释本发明,并不用于限定本发明。
32.本发明的柔性磁兼容植入式脑电电极阵列以垂直于大脑皮层的方向被植入皮层内部。如图1所示,作为其中一种实施方式,该脑电电极包括六层,从下到上,依次为第一柔性封装层、第一金属电极层、第一柔性衬底层、第二柔性衬底层、第二金属电极层、第二柔性封装层;所有的柔性封装层和柔性衬底层选自生物相容性材料;第一金属电极层和第二金属电极层在功能上可分为电极触点区、电极通道区、电极接口区,其中,头部部分裸露,作为电极触点,尾部部分裸露,作为电极接口;位于所述头部和尾部的中间部分作为电极通道。
33.整个电极的头部设置引导孔,结合摄像头、显微镜和其他植入设备,可将电极准确植入至需要的部位。同时,头部宽度略小于电极整体宽度,可使电极平滑植入而造成较小的损伤。图1中给出的引导孔为椭圆形孔,其尺寸为54
×
32μm2,用于和植入设备结合,对电极进行辅助植入。电极触点为30
×
60μm2的圆角矩形,与脑组织接触获取信号;电极通道为宽度5μm、长度3mm的ag金属层,信号经过电极通道传输至电极接口及外部采集设备进行采集。
34.如图2所示,展示了柔性磁兼容植入式脑电电极阵列的工艺流程,选取图1中截面bb’来对该工艺流程进行解释说明。本实施例中重点介绍以pi(聚酰亚胺)为柔性材料、ag为金属电极层、pmma为牺牲层的工艺流程。
35.步骤(a):准备玻璃基板:由于电极无法在柔软的pi材料上直接制备,需要准备玻璃基板或硅片作为支撑。在此可准备4英寸玻璃基板。(由于光刻机适合4英寸及以下晶圆及不规则小片材的光刻)
36.实验先将坡璃片在丙酮、无水乙醇、去离子水分别超声清洗,用氮气吹干表面水膜,用热板完全烘干,得到干燥洁净的玻璃基板。
37.步骤(b):制作pmma牺牲层:匀胶机匀涂pmma溶液,前转500r/min,5s;后转 2000r/min,30s,热板180℃烘烤30min,作为牺牲层。pmma材料可溶解于丙酮,因此在需要去除牺牲层释放电极时,只需要将带有电极的基片浸泡在丙酮中即可。
38.步骤(c):制作pi柔性衬底层:匀胶机匀涂pi溶液,前转500r/min,5s;后转200r/min, 30s加热至pi固化(厚度约30μm)。制备柔性衬底层时,若衬底层厚度过薄,易使金属电极层发生断裂,因此建议厚度10μm以上,本实施例采用30μm厚度的pi柔性衬底层,在保证材料柔性的基础上,可以保证金属电极层完整、不发生断裂。
39.步骤(d)涂覆光刻胶:匀涂光刻胶,热板烘烤(5350正性剥离专用光刻胶,前转500r/min,5s;后转3000r/min,60s,热板105℃烘烤4min)。
40.步骤(e)光刻出电极通道及触点图形:光刻机相应位置放置掩模版(如图3a所示) 和样品,曝光3s,显影25s。
41.步骤(f)氧等离子清洗:140w,5min。镀金属膜之前,为保证金属层和衬底层的结合力,对样品进行一次氧等离子清洗,这一步操作使得样品表面悬挂键数量增加。
42.步骤(g)溅射电极层cr
‑
ag
‑
cr:采用磁控溅射镀膜系统,先溅射一层cr10nm,再溅射ag600nm,再溅射一层cr10nm。其中cr作为增加粘附性的金属材料,使得ag和pi的结合更牢固。
43.步骤(h)剥离光刻胶:丙酮清洗剥离。
44.步骤(i)制作封装层pi:匀胶机匀涂pi溶液,前转500r/min,5s;后转800r/min,60s,加热至pi固化(10μm)。
45.步骤(j)溅射铝膜,刻蚀;暴露出电极触点:光刻露出电极接口和电极触点位置,并溅射一层铝膜(400nm)作为阻挡层,随后将样品浸泡在丙酮中,去除剩余光刻胶,得到除电极接口和电极触点位置外表面被铝膜包裹的样品。其中,掩模版如图3(b)所示。样品放入感应耦合干法刻蚀机中刻蚀,样品被铝膜覆盖的部分不会被刻蚀,而裸露出pi的电极接口和电极触点位置将被刻蚀。在刻蚀中,铝膜厚度如果过薄,将会在可是过程中被打掉,若过厚,则不好去除。因此选择溅射400nm的铝膜作为阻挡层。最后采用弱碱性溶液,例如koh溶液洗去al层。
46.表1 icp参数设置
47.rf power/wicp power/wo2/sccmar/sccm时间/min100600501540
48.步骤(k)蒸发au层:进行第三次光刻,其中,掩模版如图3(c)所示。蒸镀200nm 的金膜,去除光刻胶。
49.柔性pi封装层刻蚀后电极接口和触点位置金属和封装层表面有一定距离,因此可以溅射au层以减小这一段距离使电极和皮层组织贴合更紧密。阻隔具有生物毒性的cr层,防止氧化和组织液渗透。
50.步骤(l)刻蚀出电极阵列轮廓,剥离电极:进行第四次光刻,光刻出电极轮廓,用铝膜作为阻挡层,刻蚀出电极轮廓。丙酮洗去pmma,剥离电极,得到单面电极。刻蚀所用参数同上,时间约为60min。
51.一个4英寸的玻璃基板上有18个相同的柔性磁兼容植入式脑电电极阵列,在完成前面的工艺后,需要将这18个电极剥离下来。因此对样品进行第四次光刻,此次光刻掩膜图形为18个柔性电极的轮廓,包括用于辅助植入的电极头部圆环。其中,掩模版如图3(d)所示。
52.步骤(m)将两层电极背向粘贴,形成双面电极,共六层结构。本实施例提供的柔性磁兼容植入式脑电电极阵列的实物图如图4所示。
53.由于单面电极的背面不具有触点结构,因此只有单面的触点结构可以与组织接触,通道数少,可以采集到的数据量少。因此,将两个单面电极背向粘贴,形成双面电极,使得双面均具有触点结构,均可以与组织接触,且通道数翻倍,采集数据量大。
54.为检测本实施例提供的柔性磁兼容植入式脑电电极阵列结构具有采集并记录信号的能力,利用skx
‑
8000微弱电生理信号模拟仪模拟脑电信号,对该柔性磁兼容植入式脑电电极阵列进行了测试。随后将电极输出端经过fpc接口,并通过自制的基于针对脑电采集的adc 芯片ads1299的采集设备来对信号进行采集,由上位机接收数据并进行处理。使用探针台来对电极施加用于测试的信号。使用探针轻轻戳在电极触点处,以免划伤电极,并在启动生理信号发生仪和上位机软件后观察输入及输出的信号波形。
55.为方便测试,在对步骤l得到的单面电极进行测试时未释放电极,在基片的支撑下完成测试。
56.测试信号频率为10hz,幅度为300μv,并对输出信号进行滤直流及1
‑
50hz的滤波处理。图5为经过滤直流后的信号波形图、带通滤波后的信号波形图和傅里叶变换后得到的频谱图。虽然有噪声成分的干扰,但是采集到的信号波形也可以分辨出与原始信号的频率相近,幅度略有衰减。
57.本领域普通技术人员可以理解,以上所述仅为发明的优选实例而已,并不用于限制发明,尽管参照前述实例对发明进行了详细的说明,对于本领域的技术人员来说,其依然可以对前述各实例记载的技术方案进行修改,或者对其中部分技术特征进行等同替换。凡在发明的精神和原则之内,所做的修改、等同替换等均应包含在发明的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1