铁素体合金的制作方法
本公开涉及根据权利要求1的前序部分的铁素体合金(fecral合金)。本公开还涉及根据权利要求16的铁素体合金的用途,其在300-800℃的温度范围内使用。
背景技术:
在所谓的铅冷快堆(lfr)系统中,使用液态铅作为冷却剂。液态铅和铅铋低共熔物(lbe)提供被动冷却的可能性,并因此有助于使核能安全。然而,液态铅具有高度腐蚀性,并对在lfr系统中使用的建造材料的耐腐蚀性提出高要求。
最近已提出将fecral合金作为候选材料用于铅冷快堆中,这是由于这些合金的良好的氧化性质,这是在合金表面上形成氧化铝(al2o3)层的结果。fecral合金基于铝、铬和铁,并且由于它们的抗氧化性和良好的抗蠕变性,这些合金常用于温度在1000℃左右和超过1000℃的加热元件和加热线中。然而,铅冷快堆在400-600℃的温度区间中运转,并且在这个温度范围内,通常含有15-20wt%左右的cr的商购fecral合金,由于所述fe-cr系统中存在的混溶间隙而遭受α-α’相分离困扰。所述α-α’相分离引起所述fecral合金脆化,这使所述商购fecral合金不适合在lfr系统中使用的温度范围内作为建造材料。
已在液态铅或液态铅-铋-低共熔溶液中测试了fecral组合物。在weisenburger等人的研究中显示,含有≥12.5wt%cr和≥6wt%al的模型fecral合金能够在400-600℃的温度区间内形成薄的保护性氧化铝垢[weisenburger,jianu,doyle,bruns,fetzer,heinzel,delgiacco,an,müller,“在暴露于含有氧的熔融铅的基于fe-cr-al的模型合金上形成的氧化物垢”(oxidescalesformedonfe-cr-al-basedmodelalloysexposedtooxygencontainingmoltenlead),journalofnuclearmaterials437(2013)282-292]。由lim等人进行的另一项工作显示,fe-13cr-4al合金能够从500℃起形成保护性氧化铝[lim,hwang,kim,“用于铅或铅-铋冷却的快速反应堆的形成氧化铝的fecral钢的设计”(designofaluminaformingfecralsteelsforleadorlead-bismuthcooledfastreactors),journalofnuclearmaterials441(2013)650-660]。
韩国专利kr10-1210531示出了一种旨在用于核能应用的fecral合金。
fecral合金也可以包含反应性元素(re),其是对氧和碳具有高亲和性的元素。在约1000℃的高温下,反应性元素例如y、zr和hf的添加通过平衡金属离子的向外扩散和氧的向内扩散来改进所述合金的氧化性质,这导致平衡的氧化物生长以及因此氧化物垢中机械应力和/或孔隙度的降低。关于zr和ti的添加对fe-10cr-6al合金在550℃的液态铅中的长期(10,000h)耐腐蚀性的影响,已进行了研究[ejenstam等,“在550℃下暴露于pb10,000h的fe10cral-re合金的氧化研究”(oxidationstudiesoffe10cral-realloysexposedtopbat550℃for10,000h),journalofnuclearmaterials443(2013)161-170]。
然而,尽管上面公开的研究有助于改进fecral合金的性能,但仍需要进一步提高这些合金的耐腐蚀性。
因此,本公开的一个方面是提供一种具有改进的耐腐蚀性的fecral合金。具体来说,本发明的一个方面是提供一种在300-800℃范围内的温度下,在高腐蚀性环境中具有非常好的耐腐蚀性的fecral合金。此外,本发明的另一个方面是提供一种在300-800℃范围内的温度下,对液态铅中的腐蚀具有抗性的fecral合金。本公开的另一方面是提供一种适合在诸如锅炉、熔炉和产热和产能设备和工艺的应用中作为建造材料的fecral合金。其他适合的应用包括用于堆焊、喷涂或复合管的材料。具体来说,本发明的一个方面是提供一种适合在300-800℃的温度范围下的铅冷快堆系统中作为建造材料的fecral合金。
发明详述
因此,本公开涉及一种铁素体(fecral)合金,其以重量%计包含:
c:0.01–0.1;
n:0.001-0.1;
o:≤0.2;
b:≤0.01;
cr:9–13;
al:2.5–8;
si:≤0.5;
mn:≤0.4;
y:≤2.2;
sc+ce+la:≤0.2;
mo+w:≤4.0;
ti:≤1.7;
zr:≤3.3;
nb:≤3.3;
v:≤1.8;
hf+ta+th:≤6.5;
余量为fe和不可避免的杂质,
其中,使ti+zr+nb+hf+v+ta+th以及c、n和o的量平衡,使得:
其中x是0.5,除非y的含量大于或等于0.01wt%,此时x是0.67。
本公开还涉及一种铁素体合金,其以重量%计包含:
c:0.01–0.1;
n:0.001-0.1;
o:≤0.2;
b:≤0.01;
cr:9–11.5;
al:2.5–8;
si:≤0.5;
mn:≤0.4;
y:≤2.2;
sc+ce+la:≤0.2;
mo+w:≤4.0;
ti:≤1.7;
zr:≤3.3;
nb:≤3.3;
v:≤1.8;
hf+ta+th:≤6.5;
余量为fe和不可避免的杂质,
其中,使ti+zr+nb+hf+v+ta+th以及c、n和o的量平衡,使得:
其中x是0.5,除非y的含量大于或等于0.01wt%,此时x是0.67。
本公开还涉及一种铁素体合金,其以重量%计包含:
c:0.01–0.1;
n:0.001-0.1;
o:≤0.2;
b:≤0.01;
cr:9–11;
al:2.5–8;
si:≤0.5;
mn:≤0.4;
y:≤2.2;
sc+ce+la:≤0.2;
mo+w:≤4.0;
ti:≤1.7;
zr:≤3.3;
nb:≤3.3;
v:≤1.8;
hf+ta+th:≤6.5;
余量为fe和不可避免的杂质,
其中,使ti+zr+nb+hf+v+ta+th以及c、n和o的量平衡,使得:
其中x是0.5,除非y的含量大于或等于0.01wt%,此时x是0.67。
本公开还涉及一种铁素体合金,其以重量%计包含:
c:0.01–0.1;
n:0.001-0.1;
o:≤0.2;
b:≤0.01;
cr:9–13;
al:2.5–8;
si:≤0.5;
mn:≤0.4;
y:≤2.2;
mo+w:≤4.0;
sc:≤0.2;
ti:≤1.7;
zr:≤3.3;
nb:≤3.3;
v:≤1.8;
hf+ta+th:≤6.5;
余量为fe和不可避免的杂质,
其中,使ti+zr+nb+hf+v+ta+th以及c、n和o的量平衡,使得:
其中x是0.5,除非y的含量大于或等于0.01wt%,此时x是0.67。
本公开还涉及一种铁素体合金,其以重量%计包含:
c:0.01–0.1;
n:0.001-0.1;
o:≤0.2;
b:≤0.01;
cr:9–13;
al:2.5–8;
si:≤0.5;
mn:≤0.4;
y:≤2.2;
mo+w:≤4.0;
ti:≤1.7;
zr:≤3.3;
nb:≤3.3;
v:≤1.8;
hf+ta+th:≤6.5;
余量为fe和不可避免的杂质,
其中,使ti+zr+nb+hf+v+ta+th以及c、n和o的量平衡,使得:
其中x是0.5,除非y的含量大于或等于0.01wt%,此时x是0.67。
本公开的合金还包含铬和反应性元素例如ti、zr、nb、hf、v、ta和th。所述反应性元素可以单独地或以任何组合存在于所述合金中。正如将在下面更详细解释的,将这些元素添加到所述合金以改善保护性al2o3层的形成或其性质。fecral合金通常含有碳。碳可能是故意添加的,以例如提高强度,或者可能作为例如由生产过程产生的偶然杂质存在于所述合金中。这些反应性元素例如ti、zr、nb、hf、v、ta和th,也是强的碳化物形成剂,即它们对碳的亲和性高,因此所述合金中存在的碳将被吸引到铬或所述反应性元素并形成碳化物。
通过实验,本发明人令人吃惊地发现,当所述反应性元素的以原子百分数计的量与所述合金中碳的以原子百分数计的量平衡,使得反应性元素与碳之间的商等于或大于1时,fecral合金的抗氧化性得到极大改进。
当在相对于碳来说缺乏反应性元素的合金中进行腐蚀研究时,更容易理解本公开背后的机制。
图1示意性示出了其中反应性元素与碳的商接近或小于1的fecral合金。
在所述合金铸造后的固化期间,反应性元素(re)首先在所述合金的本体中形成碳化物和氮化物。
根据本公开,所述反应性元素的以原子百分数计的量与所述合金中碳的以原子百分数计的量平衡,使得可用于形成碳化物的反应性元素与可用的碳之间的商等于或大于1。这导致在上文中或下文中所定义的合金中存在至少等量的可用反应性元素原子和可用碳原子。由于所述反应性元素是所述合金中最强的碳化物形成剂,比铬和其他合金组成成分更强,因此所有游离碳将被吸引到所述可用的反应性元素并与其形成碳化物。因此,只要可用的反应性元素的含量足够,合金中将没有游离的碳留下以形成富铬碳化物。
其他的积极效应是所述反应性元素的形成的碳化物均匀分布在上文中或下文中所定义的fecral合金的整个本体中,因此通过弥散硬化对所述合金的机械强度有贡献。
根据上文中或下文中所定义的fecral合金的一个实施方式,可用的反应性元素与碳之间的商大于或等于1,即在所述合金中存在过剩的反应性元素。因此,原因在于一些反应性元素将在保护性al2o3层的形成过程中消耗并有助于提高所述al2o3层与所述合金表面之间的粘附性。通过平衡反应性元素的量使得在它与碳和氮反应后存在过剩的反应性元素,避免了即使是少量的富铬碳化物的形成。
根据另一个实施方式,对于上文中或下文中所定义的fecral合金来说,最低的商为至少或等于1.1。这个商意味着在形成al2o3层以消耗掉所有游离的碳之后,所述合金中存在至少足够的反应性元素。
所述反应性元素与碳之间的可能的最高的商由所述反应性元素在所述合金中可能形成的金属间化合物的稳定性决定。根据本发明的fecral合金的实施方式,最高的商可能为2.3或更低。
反应性元素与碳之间的商也可以为1.1–2.2,例如1.2–2.0。
上文中或下文中所定义的铁素体合金可以通过常规的钢铁制造方法、即所谓的熔体冶金来制造,其包括:在感应炉中熔化,通过在模具中浇铸对所述熔体进行钢包精炼,随后进行热轧。上文中或下文中所定义的铁素体合金也可以通过粉末冶金来制造,在这种情况下包括通过粉化生产金属粉末,将所述粉末压实,并且随后进行烧结或热等静压的步骤。
下面将详细描述上文中或下文中所定义的合金的组成成分。
上文中或下文中所定义的fecral合金中的余量是fe和不可避免的杂质。不可避免的杂质的实例是没有故意添加,但由于通常作为杂质出现在例如用于制造所述fecral合金的材料中而不能完全避免的元素和化合物。
当在下面的背景、即“元素≤数字”中使用术语“≤”时,本领域技术人员知道所述范围的下限是0wt%,除非具体陈述了另一个数字。
碳(c)
碳被包含在上文中或下文中所定义的fecral合金中,以通过沉淀硬化提高强度。碳也可能作为由生产过程带来的不可避免的杂质而存在。为了在所述合金中实现足够的强度,碳应该以至少0.01wt%的量存在。在过高含量下,碳可能造成材料形成困难和对耐腐蚀性的不利影响。因此,在上文中或下文中所定义的合金中碳的最大量为0.1wt%。例如,碳为0.02–0.09wt%,例如0.02–0.08wt%,例如0.02–0.07wt%,例如0.02–0.06wt%,例如0.02–0.05wt%,例如0.01–0.04wt%。
氮(n)
氮可以被包含在上文中或下文中所定义的fecral合金中,以通过沉淀硬化提高强度。氮也可能作为由生产过程带来的不可避免的杂质而存在。在过高含量下,氮可能造成材料形成困难并可能对耐腐蚀性有不利影响。因此,在上文中或下文中所定义的fecral合金中氮的最大量为0.1wt%。为了在熔体冶金中实现充分的沉淀硬化,氮应该为至少0.001wt%,氮的适合范围的实例是例如0.001–0.08wt%,例如0.001–0.05wt%,例如0.001–0.04wt%,例如0.001–0.03wt%,例如0.001–0.02wt%,例如0.001–0.01wt%。在粉末冶金中,氮含量可以为至少0.01wt%。例如,在粉末冶金中,氮为0.01–0.1wt%,例如0.01–0.08wt%。
氧(o)
氧可能作为由生产过程带来的杂质,以最高0.02wt%、例如最高0.005wt%的量存在于上文中或下文中所定义的铁素体合金中。
在熔体冶金中,氧可以为0.001–0.08wt%,例如0.001–0.05wt%,例如0.001–0.02wt%。在粉末冶金中,可以故意添加氧以实现沉淀硬化效果。此时上文中或下文中所定义的合金包含最多0.2wt%的氧,例如0.01–0.2wt%的氧,例如0.01–0.1wt%,例如0.01–0.08wt%。
铬(cr)
铬通过所谓的第三元素效应,即通过在瞬态氧化阶段中氧化铬的形成,促进在上文中或下文中所定义的合金上形成al2o3层。铬应该以至少9wt%的量存在于上文中或下文中所定义的合金中。然而,由于上文中或下文中所定义的合金旨在用于300–800℃的温度范围内,铬应该不超过13wt%以便避免fe-cr系统中的混溶间隙,其中在混溶间隙中α-α’相分离引起所述fecral合金的脆化。例如,铬可以为9–13wt%,例如9–12wt%,例如9–11wt%,例如9-10wt%。根据一个特定实施方式,cr在9-11wt%、例如9至10wt%的范围内。根据又一个特定实施方式,cr在9至11.5wt%的范围内。
铝(al)
铝是上文中或下文中所定义的合金中的重要元素,因为铝在高温下暴露于氧时将形成致密且薄的氧化物al2o3,其将保护下方的合金表面免于进一步氧化。铝的量应该为至少2.5wt%,以确保形成所述al2o3层并且存在足够的铝以在损坏时使所述al2o3层恢复。然而,铝对合金的成形性具有不利影响,并且在上文中或下文中所定义的合金中铝的量应该不超过8wt%。例如,铝可以为3–7wt%,例如3–5wt%,例如3.5–6wt%,例如4至6wt%。
硅(si)
硅可能作为杂质以最多0.5wt%、例如0至0.4wt%的量存在于上文中或下文中所定义的合金中。
锰(mn)
锰可能作为杂质以最多0.4wt%、例如0至0.3wt%的量存在于上文中或下文中所定义的合金中。
钇(y)
钇可以以最高0.8wt%的量添加以提高al2o3层的粘附性,例如最高0.3wt%,例如最高0.1wt%。然而,如果以大于或等于0.01wt%的量向上文中或下文中所定义的铁素体合金添加钇,则钇氧化物的形成将影响商,且x将为0.67。此外,当使用粉末冶金时,如果添加钇,则钇含量以至少0.01wt%的量存在,以便通过氧化物和/或氮化物实现所需的弥散硬化效果。在弥散硬化的合金中钇的最大量可以高达2.2wt%,例如高达1.2wt%,例如高达1wt%。适合的范围的实例是:0.01至1.2wt%,0.01至1wt%和0.04至1wt%。
钪(sc)、铈(ce)和镧(la)
钪、铈和镧是可互换的元素,并且可以单独地或组合地以最多0.2wt%的总量添加,以改善氧化性质、al2o3层的自我恢复或合金与al2o3层之间的粘附性。根据一个特定实施方式,上文中或下文中所定义的铁素体合金不包含任何添加的sc、ce和la,即故意添加的sc、ce和/或la为0wt%。根据又一个特定实施方式,上文中或下文中所定义的铁素体合金不包含任何添加的ce和/或la。
钼(mo)和钨(w)
钼和钨两者对上文中或下文中所定义的合金的热强度具有积极效应,并且可以单独地或组合地以最高4.0wt%、例如0至2.0wt%的量添加。
反应性元素(re)
根据定义,反应性元素与碳、氮和氧具有高反应性。在对碳具有高亲和性的意义上,钛(ti)、锆(zr)、铌(nb)、钒(v)、铪(hf)、钽(ta)和钍(th)是反应性元素,因此是强的碳化物形成剂。添加这些元素是为了通过平衡金属离子和氧的扩散来改善上文中或下文中所定义的合金的氧化性质,所述扩散将控制氧化物生长过程的动力学。各反应性元素的最大量主要取决于所述元素形成不利的金属间相的倾向性。钇通常被认为是反应性元素,但是在单独的段落中讨论的本公开中不是反应性元素,并且也不是商的一部分(除了它将影响数字x应该具有的值之外),因为它不像上面提到的其他反应性元素那样形成为强的碳化物。
因此,在上文中或下文中所定义的合金中,钛的最大量为1.7wt%,例如0.02-1.7wt%。在熔体冶金中,钛的适合的量为0.02–1.3wt%,例如0.02–0.98wt%,例如0.02–0.85wt%,例如0.04–0.75wt%。在粉末冶金中,钛的适合的量为0.02–1.3wt%,例如0.04–0.75wt%,例如0.05–0.75wt%。
在上文中或下文中所定义的合金中,锆和铌的最大量分别为3.3wt%。锆和铌的量可以分别为0.04–3.3wt%。在熔体冶金中,锆可以为0.04–2.4wt%,例如0.04–1.9wt%,例如0.04–1.6wt%,例如0.08–1.4wt%,例如0.1至0.9wt%,例如0.1至0.6wt%。在粉末冶金中,锆可以为0.04–2.4wt%,例如0.08–1.4wt%,例如0.3–1.4wt%,例如0.1至0.9wt%,例如0.1至0.6。在熔体冶金中,铌可以为0.04–2.4wt%,例如0.04–1.9wt%,例如0.04–1.6wt%,例如0.08–1.4wt%。在粉末冶金中,铌可以为0.04-2.4wt%,例如0.08–1.4wt%,例如0.08–1.2wt%。
作为实例,合金可以包含量为0.04–3.1wt%的ti+zr。适合于熔体冶金的合金可以包含量为0.06–2.0wt%、例如0.12–1.7wt%的ti+zr。适用于粉末冶金的合金可以包含量为0.04–2.3wt%、例如0.06-2.0wt%的ti+zr。
其他实例是:
合金可以包含量为0.04–3.1wt%的ti+nb。适合于熔体冶金的合金可以包含量为0.06–2.0wt%、例如0.12–1.7wt%的ti+nb。适合于粉末冶金的合金可以包含量为0.04–2.3wt%、例如0.06–2.0wt%的ti+nb。
合金可以包含量为0.04–4.6wt%的zr+nb。适合于熔体冶金的合金可以包含量为0.08–2.8wt%、例如0.16–2.5wt%的zr+nb。适合于粉末冶金的合金可以包含量为0.04–3.3wt%、例如0.08–2.8wt%的zr+nb。
钒的最大量为1.8wt%。
铪、钽和钍是可互换的元素,并且可以单独地或组合地以最多6.5wt%的总量添加到上文中或下文中所定义的合金。
铁(fe)和不可避免的杂质构成上文中或下文中所定义的合金中的其余物质。
可用的反应性元素和氧、氮与碳之间的商:
在上文中或下文中所定义的合金中,考虑到在合金制造期间占优势的条件下热力学稳定的碳化物类型,将每种反应性元素的量调到与碳的量平衡。
在合金制造期间占优势的热力学条件下,所述反应性元素形成下述碳化物:
在某些情况下,反应性元素nb和v也可能形成较低价碳化物:
然而,在制造过程中合金中占优势的热力学条件下,这些碳化物具有低的稳定性,因此在所述商中可以被忽略。
此外,除了碳含量之外,所述fecral合金还可能含有氮和/或氧,因此在所述商中也必须考虑这两种元素。如上所述,氮和氧可能作为杂质存在于所述合金中,或者可能被故意添加以便改善所述fecral合金的性能。例如,当所述fecral合金被用于粉末冶金应用中时,fecral合金中氮和氧的含量可能是大量的。当氮和氧存在时,一些反应性元素以氮化物和氧化物的形式被消耗。这将导致留下更少的反应性元素与游离的碳反应以形成稳定的碳化物,这进而对保护性氧化物形成具有影响。
所述合金中反应性元素的热力学稳定的氮化物的实例是:tin,zrn,hfn,vn,tan和thn,并且所述合金中反应性元素的热力学稳定的氧化物的实例是:tio2,zro2,hfo2,y2o3和tho2。
因此,为了补偿由形成稳定的氮化物和氧化物所消耗的反应性元素,从所述商中反应性元素的量中扣除合金中氮和氧的量。
所述商中氧的量必须乘以权重因数“x”,其选自0.5或0.67。权重因数的值取决于形成的氧化物的类型,即它取决于合金中包含哪些元素并且也取决于在制造期间占优势的条件下哪种氧化物在热力学上最稳定。由于最通常形成的氧化物是二氧化物,因此可以将权重因数选择为约0.5。然而,如果在所述合金中存在元素钇(大于或等于0.01wt%),则形成的最稳定的氧化物是三氧化物例如y2o3或alyo3,此时x为0.67。
在所述商中,反应性元素、碳和如果适用的话氮和氧,在各元素的原子百分率的基础上平衡,因为重要的是确保对于每种反应性元素,添加足够的量以匹配合金中的游离碳的数量,以便形成所需碳化物。
在操作中,上文中或下文中所定义的铁素体合金将会形成,并因此构成表面氧化物层。所述表面氧化物层将包含(al2fe)o4-氧化物的外层、cr2o3氧化物的中间层和al2o3的内层。
上文中或下文中所定义的铁素体合金也可以包含zrc和/或nbc和/或nb2c和/或hfc和/或vc和/或thc和/或tac的分散胶体。所述分散胶体可以采取包含tic分散胶体核并被zrc和/或nbc和/或nb2c和/或hfc和/或vc和/或thc和/或tac的分散胶体包围的簇的形式。
附图简述
图1:示出了平衡re和碳的目的的示意图。
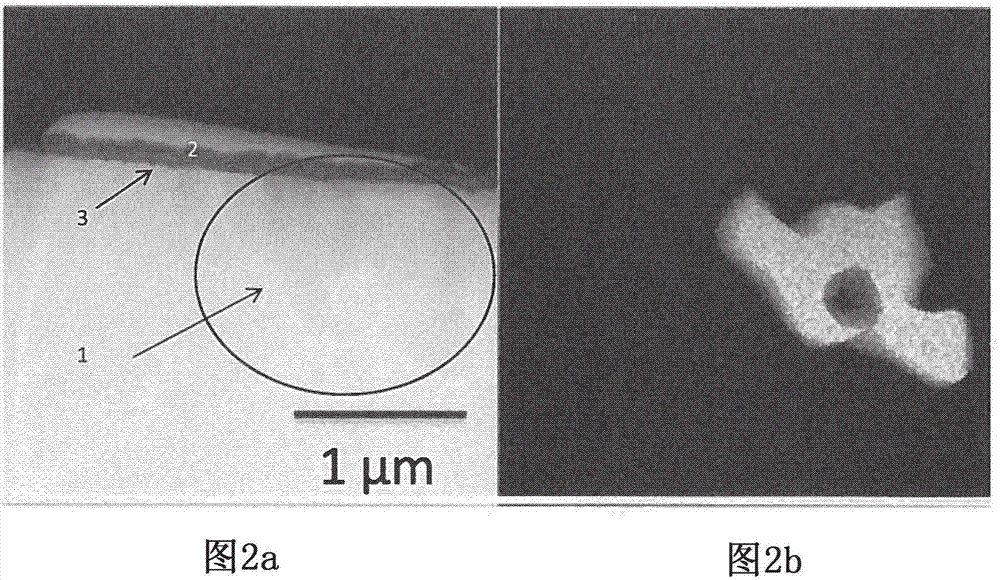
图2a和2b:示出了在比较性合金中形成的富铬碳化物的显微照片。
图3a和3b:示出了比较性合金中的氧化行为的显微照片。
图4a和4b:示出了根据本公开的第一可选方式的合金中的氧化行为的显微照片。
图5a和5b:示出了根据本公开的第二可选方式的合金中的氧化行为的显微照片。
实施例的详细描述
本公开将通过下面的非限制性实施例进行描述:
所述实施例旨在调查fe-10cr-4al合金,具体来说是调查不同反应性元素(re)对在550℃下的液态铅的长期(8,760h)耐腐蚀性的影响。此外,出于比较的原因,进行了450℃下的短期(1,000h)试验。
添加反应性元素(re)的影响:选择zr、nb和y用于本实施例。在真空感应炉中生产了具有不同re含量的9种实验性合金。将样品热轧成8×1mm带材,并在每一步后在1050℃下均化5分钟。所有研究的合金的分析的化学组成展示在表1中。
表1:研究的合金的化学组成(wt%)
*尽管根据本文中的定义的商不包含y,但对于最后三种合金来说将y
包含在商中用于比较。然而,正如将会显示的并且也在本公开中讨论的,与re相比钇的作用不同。
在所述9种样品中re和碳的含量不同,使得某些样品具有与碳的量相比缺乏的re(样品zr-0.1、y-0.02、y-0.1),某些样品中re和碳的量处于平衡(样品zr-0.2、nb-0.8c、y-0.2),并且某些样品中re与碳相比过量(样品zr-0.4、nb-0.4、nb-0.8)。
为了进行氧化研究,制备每合金的试片,尺寸为30×8×1mm。使用sic砂纸将表面抛光至#800磨砂光洁度,然后将试片在乙醇中超声处理,随后置于装有2mm99.9%(以金属计)铅粒的氧化铝坩埚中。在管式炉中进行氧化试验,其中将所述坩埚置于密封的石英管内。利用流动的ar-h2-h2o气体混合物控制液态铅中的溶解氧含量。使用1.3和0.2的h2/h2o比率分别在550℃和450℃的液态铅中实现10-7wt%的溶解氧浓度。在完成450℃下1000h和550℃下8760h的氧化试验后,将样品空气冷却,并在乙酸和过氧化氢的(1:1)溶液中清洁以除去残留的铅。使用feiquanta3d场发射扫描电子显微镜(feg-sem),通过标准的提升法(lift-out)制备透射电子显微术(tem)样品。使用jeoljem-2100ffegtem进行tem评估。使用oxfordinstruments80mm2x-maxn硅漂移探测器(sdd)进行能量色散谱(eds)元素分析。通过将氧化的样品模制在导电树脂中,然后精细抛光至最终0.25μm菱形阶梯(diamondstep),来制备sem样品。使用zeissleo1530feg-sem和oxford50mm2x-maxsddeds进行总体表征。热力学建模使用运行tcfe7和ssol4数据库的thermocalc来进行。
研究结果
来自于550℃下的8,760h氧化试验的结果显示出对于各种不同的re添加来说,氧化性质存在明显差异。
与碳相比缺乏re的三种合金(zr-0.1、y-0.02和y-0.1)形成显著量的富cr碳化物,图2a示出了cr-碳化物(1),其靠近形成在样品表面(3)上的富含al的氧化物垢(2)。在图2a中,所述富cr碳化物可能被检测为圆圈区域内的白色形状。图2b是图2a中圆圈围住的富铬区域(1)的temcreds图。在这里可以清楚地看到所述富铬区域的形状。
所述实施例显示,几乎所有形成的cr碳化物都与样品表面处的富含al的氧化物相接触。这可以被解释为是因为铝抑制碳化物形成,即使石墨稳定。因此,似乎可能在贫al的金属氧化物相边界处所述cr碳化物的成核受到促进。因此,保护性的al氧化物没有恰当形成。
此外,三种合金zr-0.1、y-0.02和y-0.1在氧化试验中都显示出不良的氧化性质。这种不良的结果在550℃和450℃下是一致的,这显示选择上文中或下文中所定义的正确的商是重要的。
图3a示出了在550℃的温度下氧化后从zr-0.1合金获取的样品的横截面的sem图像。在所述图像中可以清楚地看到形状不规则的混合氧化物,其已生长到合金本体中。zr-0.1样品的金属氧化物界面中大量的富铬表面碳化物,似乎引起点蚀类型的加速氧化,展现出尺寸高达约5μm的向内生长的混合金属氧化物。
在较低温度下,当需要低的cr含量以避免α-α’相分离时,富铬表面碳化物的存在导致形成非保护性氧化物垢。这通过在450℃下的较短(1000h)氧化试验得以验证。同样的三种合金含有接近表面的碳化物(zr-0.1、y-0.02、y-0.1)并且与碳相比缺乏re,它们完全被三层氧化物结构覆盖,所述结构由向外生长的fe3o4垢和向内生长的fecral混合氧化物构成,其下可以看到内部氧化区。图3b示出了具有上述氧化物层结构的y-0.02样品的sem显微照片。所述y-0.02样品上腐蚀侵蚀的总深度经测量为3-4μm。
平衡的合金
因此,通过平衡c和re的含量来改善fecral合金的腐蚀性能。这项研究中的三种合金zr-0.2、y-0.2和nb-0.8c含有相对于c含量接近平衡的re,在550℃下表现出显著不同的氧化行为。
zr-0.2
zr-0.2合金没有显示出氧化侵蚀的迹象。进行了tem评估以研究zr-0.2样品的表面,它显示出存在薄的约100nm厚的氧化物,其在液态铅中8,760h的暴露期间形成,参见图4b。所述氧化物分为三层,向内生长的al2o3层,向外生长的feal混合氧化物,以及隔开它们的薄的富cr氧化物层。图4b是temeds线性扫描,示出了图3a中的层的化学组成随所述层距表面的距离的变化。
在450℃下,zr-0.2合金表现出有利的氧化性质,即形成保护性氧化物层,参见图4a。利用tem来研究在其表面上形成的薄的氧化物,经测量约为40nm。与550℃下的tem结果相似,在450℃下形成的氧化物被分为三个区,只富含al的内层,富含fe的外部部分,以及富含cr的中间层(图4b)。图5b是temeds线性扫描,示出了图5a中的层的化学组成随所述层距表面的距离的变化。
nb-0.8c
nb-0.8c合金在550℃下没有显示出氧化侵蚀。
y-0.2
尽管y相对于c略微过量,但在550℃下处理后,在y-0.2合金上发现了局部氧化点蚀。这可以通过钇碳化物与zr和nb的碳化物相比相对弱的稳定性来解释。微观结构表征发现了富含y的沉淀物,其富含c、o、s,特别是fe。
大过量比率的合金
与c相比具有大过量re的样品(即样品zr-0.4、nb-0.4、nb-0.8)在550℃和450℃下都显示出不良的氧化性质。zr-0.4合金在550℃下显示出点蚀类型的氧化侵蚀,并且在整个基质中发现尺寸高达2μm的富含fe和zr的相。此外,同一合金上的氧化物点蚀富含zr。
合金zr-0.4和y-0.2在450℃下的表现相似。与550℃下的情况相同,在450℃下过量y和zr的影响不引起氧化性质的显著降低。然而,与550℃相比在450℃下较慢的反应动力学和较短的暴露时间可能掩盖了结果。
在550℃下处理后,nb-0.8合金几乎完全被尺寸高达5μm的氧化点蚀覆盖。优选地,发现这些沉淀物与莱夫斯相的行为类似,修饰合金晶界,但也存在于nb-0.8合金的晶粒内部。
结论
已显示,当re添加与合金的碳含量处于平衡,即re略微过量时,获得最佳的抗氧化性。相对于碳来说缺乏re将导致接近合金表面的富铬碳化物的形成,其进而引起不良的氧化性质并降低耐点蚀性。此外,re的过量掺入将导致金属间化合物或莱夫斯相的形成,其也降低合金的抗氧化性。
- 还没有人留言评论。精彩留言会获得点赞!