蛇纹石常压硫酸浸出液一锅提纯镁的方法
1.本发明涉及资源综合利用领域,具体涉及蛇纹石湿法纯镁方法。
背景技术:
2.蛇纹石是含水富镁硅酸盐矿物的总称,其化学组成为3mgo
·
2sio2·
2h2o,呈暗墨绿色、棕色或黄色,大都有斑点,因磨光面像蛇纹而得名,硬度2~3.5,密度2.2~3.69/cm3。其晶体结构,由一层硅氧四面体与一层氢氧镁石八面体以1:1结合形成双层结构。按矿物结构蛇纹石一般可分为三类:(1)具有圆柱结构的纤蛇纹石(chrysotile);(2)具有平整结构的利蛇纹石(lizardite);(3)具有一个交替波状结构的叶蛇纹石(antigorite)。所有蛇纹石矿物,无论是否具有纤维状特征,都属层状结构,与高岭石类似。矿石中六次配位的mg
2+
可以被a1
3+
、ni
2+
、fe
2+
、fe
3+
、mn
2+
等所置换,尤其在铝蛇纹石(zoblitzite)、镍蛇纹石(gamierite)和铁蛇纹石(greenallte)等中被置换。通常蛇纹石含有少量的铁、铝、铬、镍、钴、锰等金属。因此,蛇纹石是一种重要的镍、钴潜在资源。
3.蛇纹石的湿法冶炼是资源利用的主要手段,目前行业内涉及的湿法冶炼工艺主要为盐酸酸浸工艺、高压硫酸酸浸工艺,常压硫酸酸浸工艺。盐酸酸浸工艺浸出条件温和、设备投资小、所述的cl-能有效破坏胶体稳定性,降低溶液粘度,利于操作和分离,但是由于盐酸易挥发、成本高,因此对盐酸的回收有更高的要求,不利于工业的大规模应用。高压硫酸酸浸工艺常应用于镍品位高的蛇纹石矿的冶炼处理,其能够有效控制铁的浸出,常用来提取蛇纹石中的镍;然而,高温浸出工艺能耗高,成本大,对矿石品位要求高。与高压硫酸浸出工艺相比,常压硫酸酸浸工艺常用于低品位蛇纹石的冶炼,其浸出选择性不理想,浸出液金属离子种类多,并呈现高铁、高镁、低镍等特点,该工艺获得的浸出液的元素分离难度大,加上so
42-难于破坏胶体结构,在浸出和净化除杂阶段容易成胶,难于操作,且除杂时产生的渣量大、浸出液含so
42-多,镍、镁等有价元素的提纯难度大。
4.针对低品位硫酸常压浸出液的元素回收,行业内的主要手段在于分步分类回收,例如,公开号为cn103395796a公开了一种蛇纹石的综合利用方法,步骤为:蛇纹石经硫酸浸出后,过滤得第一滤液;向第一滤液中加入氧化剂;再加入ph值调节剂发生沉淀反应,再过滤得铁铝混合物和第二滤液;向铁铝混合物中加入水和氢氧化钠,后过滤得铁沉淀物和偏铝酸钠溶液;向第二滤液中加入硫化物反应,再过滤得镍钴混合物和第三滤液;向第三滤液中加入氧化剂反应;后加入碱性吸附剂,再过滤得硫酸镁溶液,加氨水制备出氢氧化镁。
5.对于低品位蛇纹石硫酸常压浸出液的冶炼而言,行业内大多都是经过多步分离的工艺分类冶炼,该工艺处理效率低、工艺操作性不强,且目标元素的回收率以及产物纯度有待提高。
技术实现要素:
6.针对蛇纹石常压硫酸浸出液湿法提取镁过程中容易成胶、粘性大、镁回收率和纯度不理想等问题,本发明目的在于,提供一种蛇纹石常压硫酸浸出液(本发明也简称为浸出
液)一锅提纯镁的方法,旨在提供一锅体系下实现浸出液中镁离子和其他离子选择性分离,改善镁的回收率和纯度的方法。
7.出于处理价值考量,低品位蛇纹石采用硫酸常压酸浸工艺进行回收,该工艺得到的浸出液为高铁、高镁、低镍、丰富的微量杂质元素的硫酸体系,该类型的浸出液难于实现镁的一锅分离回收,主要在于:(1)体系为高铁硫酸体系,溶液容易形成胶体,且硫酸根离子难于破坏胶体结构,如此将影响镁和其他成分的分离和回收,且工艺操作难度大,例如,难于过滤;(2)该体系下中,存在丰富的金属杂质成分,这些成分难于和镁实现一锅高选择性分离;(3)镁的回收率、纯度和白度不理想。针对蛇纹石硫酸常压酸浸出液难于实现一锅高选择性分离的问题,本发明提供以下改进工艺:
8.一种蛇纹石常压硫酸浸出液(本发明也简称为酸浸液)一锅提纯镁的方法,将蛇纹石硫酸常压酸浸的浸出液进行一锅三段反应处理,随后固液分离,得到纯化的镁溶液;
9.所述的浸出液中溶解有fe、cr、mn和mg;
10.所述的一锅三段反应过程包括:调控浸出液的pha为2.0~3.0,加入氧化剂进行第一段氧化处理;随后调控体系的phb至4.5~6,补加氧化剂进行第二段氧化处理;再调控体系的phc至7~8后进行第三段反应;
11.一锅三段反应过程中,第一段氧化反应、第二段氧化反应的温度为60~80℃,第三段反应的温度为80℃~90℃。
12.针对常压硫酸酸浸液成分特点难于实现一锅提纯镁、工艺操作难度大的问题,本发明创新地提出,在所述的一锅三段处理工艺下,配合各段的反应类型、ph和温度的联合控制,能够实现协同,能够解决常压酸浸体系、高铁、高杂质元素、硫酸体系所致的杂质元素与镁难于一锅高选择性分离的问题,能够有效使镁和各离子一锅高选择性分离,利于获得高纯度的镁溶液,不仅如此,本发明方法还能够有效改善浸出液一锅处理过程中工艺性差(如过滤性差)的问题,利用工业实际放大。
13.本发明研究发现,所述的一锅体系下的第一段氧化、第二段氧化以及第三段反应的三段反应工艺以及对各段反应的ph以及温度的联合控制是协同解决常压浸出液难于一锅处理问题、改善镁提取以及提纯效果的关键。
14.本发明中,所述的酸浸液由低品位的蛇纹石常压硫酸酸浸得到。
15.本发明中,所述的浸出液为蛇纹石常压下的硫酸酸浸液。所述的硫酸浓度例如为2~5mol
·
l-1
。所述的常压酸浸的温度例如为80~100℃,优选为80~95℃。
16.本发明中,所述的浸出液为高铁、低镍、高镁的硫酸体系。其浓度例如分别为:fe的浓度为5~18g/l;mn(ii)的浓度为0.2~0.5g/l、cr(ⅲ)的浓度为0.10~0.40g/l、mg的浓度为50~65g/l。进一步优选,fe的浓度为6~12g/l;mn(ii)的浓度为0.12~0.4g/l、cr(ⅲ)的浓度为0.20~0.4g/l、mg的浓度为50~65g/l。本发明技术方案,对于浸出液的一锅处理能够表现出更优的工业应用价值,但不排除本发明方法对其他浸出液的应用。
17.本发明中,酸浸液中,还允许含有镍、钴、铝中的至少一种;其中,所述的浸出液中,ni的浓度为0.20~0.6g/l;co的浓度为0.01~0.04g/l;al的浓度为0.2~2g/l;进一步优选,ni的浓度例如为0.30~0.6g/l;co的浓度例如为0.02~0.03g/l;al的浓度为0.3~1.8g/l。本发明技术方案能够实现镁和铁、锰、铬、镍、铝和钴在硫酸体系下一锅高选择性分离,具有优异的炼镁效果和效率。
18.本发明中,一锅三段处理过程中,采用碱性物质调控体系的ph,所述的碱性物质例如为氧化镁、碱金属氢氧化物、氧化钙、氨水中的至少一种。所述的碱性物质可通知固体或者溶液的形式添加使用。
19.本发明中,一锅三段处理过程中,氧化剂为氯酸盐、氧气或过氧化氢中的至少一种。
20.本发明中,预先向常压浸出液中添加碱性物质,调控体系的ph至需要的pha,并在所要求的60℃~80℃的温度下通入氧化剂,进行一锅反应中的第一段氧化处理。本发明研究发现,在所述的温度、ph下,如此,能够意外地调控铁的成核行为和形貌,如此能够意外地进一步协同改善一锅体系下的镁和铁以及其他元素的分离选择性,改善一锅处理的加工性能。
21.本发明中,第一段氧化反应阶段,氧化剂的用量为将体系中的fe氧化的理论摩尔量的1.2~1.5倍。作为优选,pha为2.0~3.0。第一段氧化处理的温度优选为60~70℃,进一步优选为60~65℃。
22.本发明中,第一段氧化处理的时间优选为0.5~1.0h。
23.本发明中,第一段氧化处理后,无需进行固液分离,直接调控体系的ph至phb,并在所要求的60℃~80℃的温度下通入氧化剂,进行一锅反应中的第二段氧化处理。本发明研究发现,在所述的第一段氧化处理的协同前提下,进一步配合第二段氧化处理的工艺和温度的联合控制,能够实现体系中的mn的选择性氧化,避免体系中的cr的伴随氧化,如此能够和第一氧化反应联合,协同改善镁和其他成分的一锅分离选择性,改善镁的一锅分离回收率和纯度。
24.优选地,第二段氧化反应阶段,氧化剂的用量为将体系中的mn氧化成mn(iv)氧化的理论摩尔量的1.2~1.5倍。
25.本发明中,第二段氧化反应过程的温度优选为60~70℃。
26.作为优选,phb为5.0~6.0。
27.优选地,第二段氧化反应的时间为0.5~1.0h。
28.本发明中,第二段氧化处理后,不进行固液分离,直接调控体系的ph至phc,并在所要求的80℃~90℃的温度下进行第三段反应,实现除镁以外的其他离子如cr等其他例如的选择性沉淀,并改善成核行为,如此能够意外地协同改善镁和其他离子的分离效果,改善镁的回收率和纯度,并改善其他元素在渣中的富集效果。
29.作为优选,phc为7.0~8.0。
30.优选地,第三段反应的时间为2.0~3.0h。
31.本发明中,通过所述的一锅三段反应下,配合各段的ph和温度的联合控制,能够实现协同,如此利于控制一锅体系下的元素的成核行为和形貌,且所述条件下构建的渣的形貌有能够和后续的条件协同诱导其他元素的成核选择性,如此利于控制mg和其他成分的分离选择性,利于改善镁的回收率和纯度,不仅如此,还能够降低过滤难度,改善工艺操作性。
32.本发明中,可采用已知的手段对镁溶液进行处理。例如,向镁溶液中添加沉淀剂,进行沉镁反应,制得氢氧化镁。
33.沉淀剂例如为氨水、碱金属氢氧化物中的至少一种。所述的沉淀剂以溶液的形式条件,所述的溶液的浓度例如为1mol
·
l-1
~13mol
·
l-1
。
34.优选地,沉镁反应过程及反应终点的ph为8.8~9.5;
35.优选地,沉镁反应过程的温度为70℃~80℃;
36.优选地,沉镁反应的时间为1~2h。
37.本发明中,将氢氧化镁置于碱液中进行陈化处理,随后固液分离、洗涤、制得提纯氢氧化镁;
38.优选地,所述的碱液为碱金属氢氧化物的水溶液,优选的溶质的浓度为0.2mol
·
l-1
~0.5mol
·
l-1
;
39.优选地,陈化的温度为70℃~80℃;
40.优选地,陈化的时间为60~120min。
41.本发明一种优选的利用浸出液制备高纯氢氧化镁的方法,所述方法包括以下步骤:
42.(1)将蛇纹石硫酸浸出液加入碱性物质,调控体系的ph为2.0~3.0;随后添加氧化剂,在60~70℃保温下进行第一段反应;随后无需过滤下,继续补加碱性物质至体系的ph至4.5~6.0,添加氧化剂并在50~60℃保温下进行第二段氧化处理;处理后无需进行过滤,补加碱性物质至体系的ph为7.0~8.0,在80~90℃下保温进行第三段反应;随后经一次过滤,可以得到纯净的硫酸镁溶液。
43.(2)在一定温度下,向过滤后得到的硫酸镁溶液中加入一定量的沉淀剂,进行沉镁反应。控制反应过程的ph为8.8~9.5,温度为70℃~80℃;时间为1~2h,随后经过滤,得到mg(oh)2。所述步骤(2)硫酸镁溶液和沉淀剂加入的方式为双向滴加。
44.(3)用热水洗涤氢氧化镁3~5次。
45.(4)将一定浓度的氢氧化钠溶液加入到氢氧化镁中进行反应,过滤、洗涤,控制反应温度为70℃~80℃,反应时间为60~120min,可制得符合质量标准的高纯氢氧化镁产品。
46.相对于现有技术,本发明具有以下优点和有益效果:
47.针对蛇纹石常压硫酸酸浸的浸出液成分特点难于实现一锅提纯镁、工艺操作难度大的问题,本发明创新地提出,在所述的一锅三段处理工艺下,配合各段的反应类型、ph和温度的联合控制,能够实现协同,能够解决常压酸浸体系高铁、丰富杂质元素所致的与镁难于一锅高选择性分离的问题,能够有效使镁和各离子一锅高选择性分离,利用获得高纯度的镁溶液,改善镁的回收率以及其他成分在渣中的富集回收率,不仅如此,本发明方法还能够有效改善浸出液一锅处理过程中工艺性差(如过滤性差)的问题,利用工业实际放大。
附图说明
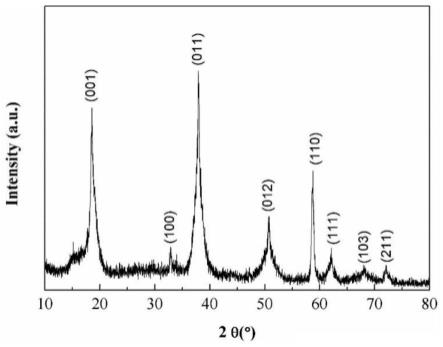
48.图1为实施例1产品的xrd图;
49.图2为实施例1产物的sem图;
具体实施方式:
50.下面结合实施例对本技术的技术方案进行详细说明:
51.根据工业氢氧化镁的化工行业标准hg/t 3607-2007可知,工业氢氧化镁可分为三类:
[0052]ⅰ类:主要用作阻燃剂的原料,[mg(oh)2]质量分数/%≥97.5;
[0053]ⅱ类:主要用作氧化镁和镁盐生产的原料;[mg(oh)2]质量分数/%≥93
[0054]ⅲ类:主要用于烟道脱硫,废水处理,农用肥料和土壤改良剂等;[mg(oh)2]质量分数/%≥92。
[0055]
所以本发明工艺所产的mg(oh)2的纯度要求符合行业ⅰ类标准。
[0056]
以下案例,所述的酸浸液为低品位的蛇纹石经硫酸常压酸浸得到,所述的蛇纹石常压硫酸浸出液中主要元素浓度(g
·
l-1
):mg 60,fe 12.89,al 1.54,cr(iii)0.33,co(ii)0.025,mn(ii)0.40,ni(ii)0.55。
[0057]
为使本发明的目的、技术方案和优点更加清楚明白,下面结合实施例,对本发明作进一步的详细说明,本发明的示意性实施方式及其说明仅用于解释本发明,并不作为对本发明的限定。
[0058]
实施例1:
[0059]
步骤(1):一锅处理:
[0060]
蛇纹石浸出液(酸浸液)为300ml,用10%mgo浆液将浸出液的pha调到2.0时,加入铁含量1.3倍的氯酸钠,60℃保温进行第一段氧化处理,氧化30分钟;无需过滤下,继续采用10%mgo浆液将浸出液的phb调到5.5时,通入氧气(为锰摩尔量的1.3倍),70℃保温进行第二段氧化处理30分钟;无需过滤下继续用10%mgo浆液调节phc至7.0,80℃保温进行第三段反应2h;
[0061]
一锅三段处理完成后,进行过滤,过滤的速率为12mg/min
·
cm2,过滤后滤液中镍的含量为0.13mg
·
l-1
,钴的含量为0.07mg
·
l-1
,锰的含量为0.43mg
·
l-1
,由于铬和铁的含量极低,icp没有测出;此方法渣中铁的回收率大于99.99%,镍的回收率为99.97%,锰的回收率为99.87%,铬的回收率大于99.99%,镁的损失率低于0.7%。
[0062]
步骤(2):沉镁以及陈化:
[0063]
将净化除杂后的溶液,滴加氨水进行沉淀反应,反应的温度为70℃,反应过程及反应终点的ph为8.9;反应时间1.0h,经过滤、洗涤得到mg(oh)2,洗涤得到的mg(oh)2用0.10mol
·
l-1
naoh陈化(温度为70℃)1.0h。氢氧化镁的硫含量为0.17%,镁的总回收率为80%,氢氧化镁中未检测到cr元素,氢氧化镁纯度为98.63%,白度为98.6%。氢氧化镁的xrd图和sem图如图1和2所示。
[0064]
实施例2:
[0065]
步骤(1):一锅处理:
[0066]
蛇纹石浸出液(酸浸液,同实施例1)为300ml,用10%mgo浆液将浸出液的ph调到3时,加入铁含量1.4倍的氯酸钠,60℃保温进行第一段氧化处理,氧化40分钟;10%mgo浆液将浸出液的ph调到6时,再通入锰含量1.4倍的双氧水,60℃保温进行第二段氧化处理40min;继续用10%mgo浆液调节ph,直至将ph调到8,90℃保温进行第三段反应2h;
[0067]
一锅三段处理完成后,进行过滤,过滤的速率为15mg/min
·
cm2,过滤后滤液中镍的含量为0.074mg
·
l-1
,钴的含量为0.019mg
·
l-1
,锰的含量为1.48mg
·
l-1
,铬的含量为0.041mg
·
l-1
,铁的含量为0.014mg
·
l-1
;此方法中铁的回收率大于99.9%,镍的回收率为99.92%,锰的回收率为99.57%,铬的回收率大于99.99%,镁的损失率低于0.8%
[0068]
步骤(2):沉镁以及陈化:
[0069]
将净化除杂后的溶液,加入氨水,控制加料温度为30℃,待体系的ph达到9后升温
至80℃,控制反应过程和终点的ph为9.2;保温反应时间1.5h,随后经过滤、洗涤得到mg(oh)2,洗涤得到的mg(oh)2用0.15mol
·
l-1
naoh陈化(温度为80℃)1.5h,镁的总回收率为82%,氢氧化镁的硫含量为0.18%,氢氧化镁中未检测到cr元素,氢氧化镁纯度为98.71%,白度为99.6%。
[0070]
实施例3:
[0071]
步骤(1):一锅处理(中试处理):
[0072]
蛇纹石浸出液(酸浸液,同实施例1)为300l,用10%mgo浆液将浸出液的ph调到2.5时,加入铁含量1.5倍的氯酸钠,65℃保温进行第一段氧化处理,氧化50分钟;10%mgo浆液将浸出液的ph调到5时,再通入锰含量1.5倍的氧气,65℃保温进行第二段氧化处理50分钟;继续用10%mgo浆液调节ph,直至将ph调到7.5,85℃保温进行第三段反应2h;
[0073]
一锅三段处理完成后,进行过滤,过滤的速率为73g/h
·
dm2,过滤后滤液中镍的含量为0.11mg
·
l-1
,钴的含量为0.09mg
·
l-1
,锰的含量为0.41mg
·
l-1
,铬的含量为0.85mg
·
l-1
,由于铁的含量极低,icp没有测出;此方法中铁的回收率大于99.9%,镍的回收率为99.98%,锰的回收率为99.89%,铬的回收率为99.7%,镁的损失率为1.2%。
[0074]
步骤(2):沉镁以及陈化:
[0075]
步骤(1)净化除杂后的溶液中加入氨水,控制加料温度为40℃,当体系的ph达到8.8后升温至75℃保温反应,控制反应过程及反应终点的ph为9.1,反应时间2.0h,随后经过滤、洗涤得到mg(oh)2,洗涤得到的mg(oh)2用0.20mol
·
l-1
naoh陈化(温度为75℃)2.0h,镁的总回收率为75%,氢氧化镁的硫含量为0.16%,氢氧化镁中未检测到cr元素,氢氧化镁纯度为98.5%,白度为99.3%。
[0076]
对比例1:
[0077]
和实施例1相比,区别仅在于,一锅处理过程中的第一段氧化过程的温度为50℃;其他操作和参数同实施例1。
[0078]
结果为:步骤(1)中,过滤效率为6mg/min
·
cm2;铁的回收率为80%,镍的回收率为95%,锰的回收率为96%;铬的回收率为94%;镁的损失率为10%;步骤(2)中,氢氧化镁的总回收收率为70%,纯度为98.5%,白度为98.6%;氢氧化镁中cr元素为0.0334%,硫含量为0.2%。工艺的过滤性能、产物质量如纯度、白度等性能均不及实施例1。
[0079]
对比例2:
[0080]
和实施例1相比,区别仅在于,一锅处理过程中的第二段氧化处理过程的温度为50℃;其他操作和参数同实施例1。
[0081]
结果为:步骤(1)中,铁的回收率为98.8%,镍的回收率为97.5%,锰的回收率为70%,铬的回收率为94%;镁的损失率低于0.8%;步骤(2)中,镁的总收率为79%,纯度为96.8%,白度为89%;硫含量为0.18%,cr元素为0.0771%。
[0082]
对比例3:
[0083]
和实施例1相比,区别仅在于,一锅处理过程中的第二段氧化处理的为90℃;其他操作和参数同实施例1。
[0084]
结果为:步骤(1)中,铁的回收率为97.7%,镍的回收率为98%,锰的回收率为96%;铬的回收率为80%,镁的损失率低于0.8%;步骤(2)中,镁的总收率为76%,纯度为95.4%,白度为87%;氢氧化镁中硫含量为0.21%、cr元素为0.0419%。
[0085]
对比例4:
[0086]
和实施例1相比,区别仅在于,一锅处理过程中的第三段处理的为60℃;其他操作和参数同实施例1。
[0087]
结果为:步骤(1)中,铁的回收率为97%,镍的回收率为96.4%,锰的回收率为94%;铬的回收率为95%;镁的损失率为3%;步骤(2)中,镁的总收率为77%,纯度为97.5%,白度为98%;氢氧化镁中硫含量为0.18%。
[0088]
对比例5:
[0089]
和实施例1相比,区别仅在于,步骤(1)的一锅第二段过程中,phb为4.0。其他参数同实施例1。
[0090]
结果为:步骤(1)中,铁的回收率为98%,镍的回收率为97%,锰的回收率为73%,铬的回收率为94%;镁的损失率为1%。
[0091]
步骤(2)中,镁的总回收率为80%,氢氧化镁的硫含量为0.2%,氢氧化镁纯度为96.4%,白度为87%。
[0092]
对比例6:
[0093]
和实施例1相比,区别仅在于,步骤(1)的一锅第二段过程中,phb为6.5。
[0094]
结果为:步骤(1)中,铁的回收率为96%,镍的回收率为97%,铬的回收率为82%,锰的回收率为96%;镁的损失率为0.9%。
[0095]
步骤(2)中,镁的总回收率为78%;氢氧化镁纯度为95.1%,硫含量为0.23%,白度为88%。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1