一种氮化锂废料的回收方法与流程
1.本发明属于电池材料回收技术领域,特别涉及一种氮化锂废料的回收方法。
背景技术:
2.氮化锂是一种快离子导体且其电导率比其他无机的锂盐都高,因此广泛运用于锂离子电池固体电极材枓。目前氮化锂的主要制备方法是利用锂在氮气中反应制备,但是制备高纯度的氮化锂(质量含量》99.5%)的产量比较低,且不合格品较多。不合格的氮化锂废料主要是含有较多未反应的金属锂,将不合格的氮化锂废料进行回收利用是一个难题。传统的处理方法是将氮化锂废料暴露在空气中,使得变成碳酸锂,而碳酸锂相比金属锂、硫化锂,其价值比较低,如何从氮化锂废料中回收未反应完全的金属锂,以及将氮化锂废料转化成价值较高的硫化锂是本领域亟待解决的问题。
技术实现要素:
3.本发明旨在至少解决上述现有技术中存在的技术问题之一。为此,本发明提出一种氮化锂废料的回收方法,能够从氮化锂废料中回收得到价值较高的金属锂和硫化锂。
4.本发明提供一种氮化锂废料的回收方法,包括以下步骤:
5.s1、将氮化锂废料和n-甲基吡咯烷酮混合,再通入硫化氢进行加热反应,过滤,得到金属锂粗料和含有硫氢化锂的n-甲基吡咯烷酮溶液;
6.s2、将所述含有硫氢化锂的n-甲基吡咯烷酮溶液进行加热,过滤,得到硫化锂粗料;
7.s3、将所述金属锂粗料和所述硫化锂粗料分别进行提纯,得到金属锂和硫化锂。
8.本发明通过氮化锂废料与硫化氢在n-甲基吡咯烷酮中进行反应,在一定温度下,氮化锂废料与硫化氢在n-甲基吡咯烷酮中反应生成可溶于n-甲基吡咯烷酮的硫氢化锂,硫氢化锂显酸性,当反应完全后整个浆料呈强酸性,金属锂不反应,通过过滤即得到金属锂粗料,对含有硫氢化锂的n-甲基吡咯烷酮溶液进行加热,过滤,得到硫化锂粗料,最终经提纯后得到金属锂和硫化锂。本发明的反应原理如下:
9.li3n+3h2s
→
3lihs+nh3;2lihs
→
2li2s+h2s。
10.由于反应全程不引进水分子,这就能避免硫化锂与水反应,同时避免nmp发生酰胺化反应。主要是在碱性环境或高温下,nmp中与n相邻的三个c都有可能被活化,其中c=o中的c活化后可直接造成nmp开环水解,生成n-甲基-4-氨基丁酸;若与n相邻的亚甲基和甲基的c被活化,先会发生氧化反应,生成过氧化物,由于该过氧化物不稳定,易生成羟基,即生成5-hnmp和nhmp;并且碱性环境下更容易造成5-hnmp和nhmp开环水解,生成n-甲基-4-羟基氨基丁酸和n-羟甲基-4-氨基丁酸,最后这三种nmp水解产物可发生聚合反应生成酰胺类聚合物。本反应不引进水分子,在高温条件下,nmp不发生水解反应,避免杂质引入硫化锂产品中,同时氮化锂废料中未反应的金属锂也得到回收,反应过程中产生的氨气会挥发掉。本发明回收方法得到的硫化锂、金属锂收率高,品质好、杂质低,纯度大于99%。
11.优选地,步骤s1中,所述氮化锂废料和n-甲基吡咯烷酮按照料液比为1kg:(6~8)l进行混合。
12.优选地,步骤s1中,所述反应的温度为70~130℃,所述反应的压强为50~150。
13.优选地,步骤s1中,所述氮化锂废料的颗粒d50小于3um。
14.优选地,步骤s2的具体过程为:在惰性气体,压强为-50~-150pa的条件下,对所述含有硫氢化锂的n-甲基吡咯烷酮溶液进行加热至170~190℃,搅拌6~8h,过滤,得到硫化锂粗料。
15.优选地,所述惰性气体包括氩气或氮气。
16.优选地,步骤s3中,所述提纯包括洗涤和干燥。
17.优选地,所述洗涤的具体过程为:采用烷烃类溶剂和醚类溶剂混合作为洗涤液进行洗涤。
18.优选地,所述烷烃类溶剂包括正己烷或环己烷;所述醚类溶剂包括1,3-二氧环戊烷或丙酮。
19.优选地,所述烷烃类溶剂和醚类溶剂的体积比为1:(1~5)。
20.优选地,步骤s3中,所述金属锂的纯度大于99%;所述硫化锂的纯度大于99%。
21.相对于现有技术,本发明的有益效果如下:
22.本发明通过氮化锂废料与硫化氢在n-甲基吡咯烷酮中进行反应,对含有硫氢化锂的n-甲基吡咯烷酮溶液进行加热,最终得到金属锂和硫化锂,由于反应全程不引进水分子,这就能避免硫化锂与水反应,另外也避免了n-甲基吡咯烷酮在强碱条件特别是有水分子条件下发生酰胺化的过程,避免杂质引入硫化锂产品中,同时氮化锂废料中未反应的金属锂也得到回收。本发明回收方法得到的硫化锂、金属锂收率高,以锂计回收率》95%,硫化锂和金属锂的品质好、杂质低,纯度大于99%。
具体实施方式
23.为了让本领域技术人员更加清楚明白本发明所述技术方案,现列举以下实施例进行说明。需要指出的是,以下实施例对本发明要求的保护范围不构成限制作用。
24.以下实施例中所用的原料、试剂或装置如无特殊说明,均可从常规商业途径得到,或者可以通过现有已知方法得到。
25.实施例1
26.一种氮化锂废料的回收方法,包括以下步骤:
27.s1、在200l密封反应釜内装入10kg氮化锂废料(含有金属锂31.6%)和80l n-甲基吡咯烷酮,搅拌均匀,并加热至70℃,将硫化氢气体通过潜管通入反应体系中进行反应,反应釜内的气压保持在50pa,反应温度维持在70℃,反应完全后,过滤,分别得到金属锂粗料和含有硫氢化锂的n-甲基吡咯烷酮溶液;反应过程中,可取少量反应浆液加入甲基橙溶液中,如变红色即可判定为反应完全;
28.s2、将含有硫氢化锂的n-甲基吡咯烷酮溶液加入密封反应釜内,通入氩气,使反应釜内的压强为-50pa,加热至170℃,保持在170℃下反应6h,反应过程中不断搅拌溶液,反应完全后,过滤,得到硫化锂粗料;
29.s3、将正己烷和1,3-二氧环戊烷按照体积比为1:1混合,得到洗涤液,将得到的硫
化锂粗料和金属锂粗料分别在密闭的环境中,用洗涤液洗涤三次并过滤,然后分别置于真空烘箱中,在450℃下真空干燥处理1h,得到13.18kg硫化锂和3.14kg金属锂。
30.实施例2
31.一种氮化锂废料的回收方法,包括以下步骤:
32.s1、在200l密封反应釜内装入15kg氮化锂废料(含有金属锂21.6%)和100l n-甲基吡咯烷酮,搅拌均匀,并加热至100℃,将硫化氢气体通过潜管通入反应体系中进行反应,反应釜内的气压保持在100pa,反应温度维持在100℃,反应完全后,过滤,分别得到金属锂粗料和含有硫氢化锂的n-甲基吡咯烷酮溶液;反应过程中,可取少量反应浆液加入甲基橙溶液中,如变红色即可判定为反应完全;
33.s2、将含有硫氢化锂的n-甲基吡咯烷酮溶液加入密封反应釜内,通入氮气,使反应釜内的压强为-100pa,加热至180℃,保持在180℃下反应7h,反应过程中不断搅拌溶液,反应完全后,过滤,得到硫化锂粗料;
34.s3、将环己烷和丙酮烷按照体积比为1:1混合,得到洗涤液,将得到的硫化锂粗料和金属锂粗料分别在密闭的环境中,用洗涤液洗涤三次并过滤,然后分别置于真空烘箱中,在450℃下真空干燥处理2h,得到22.08kg硫化锂和3.23kg金属锂。
35.实施例3
36.一种氮化锂废料的回收方法,包括以下步骤:
37.s1、在200l密封反应釜内装入20kg氮化锂废料(含有金属锂18.16%)和120l n-甲基吡咯烷酮,搅拌均匀,并加热至130℃,将硫化氢气体通过潜管通入反应体系中进行反应,反应釜内的气压保持在150pa,反应温度维持在130℃,反应完全后,过滤,分别得到金属锂粗料和含有硫氢化锂的n-甲基吡咯烷酮溶液;反应过程中,可取少量反应浆液加入甲基橙溶液中,如变红色即可判定为反应完全;
38.s2、将含有硫氢化锂的n-甲基吡咯烷酮溶液加入密封反应釜内,通入氩气,使反应釜内的压强为-150pa,加热至190℃,保持在190℃下反应8h,反应过程中不断搅拌溶液,反应完全后,过滤,得到硫化锂粗料;
39.s3、将环己烷和1,3-二氧环戊烷按照体积比为1:1混合,得到洗涤液,将得到的硫化锂粗料和金属锂粗料分别在密闭的环境中,用洗涤液洗涤三次并过滤,然后分别置于真空烘箱中,在450℃下真空干燥处理3h,得到31.35kg硫化锂和3.63kg金属锂。
40.对比例1
41.s1、在200l密封反应釜内装入10kg氮化锂废料(含有金属锂31.6%)、80l n-甲基吡咯烷酮和36.11kg硫氢化钠,搅拌均匀,于氮气条件下,加热至70℃,反应釜内的气压保持在50pa,反应温度维持在70℃,反应完全后,过滤,分别得到金属锂粗料、硫化钠和含有硫氢化锂的n-甲基吡咯烷酮溶液;反应过程中,可取少量反应浆液加入甲基橙溶液中,如变红色即可判定为反应完全;反应式为:2li3n+6nahs
→
3l2s+3na2s+2nh3;
42.s2、将含有硫氢化锂的n-甲基吡咯烷酮溶液加入密封反应釜内,通入氩气,使反应釜内的压强为-50pa,加热至170℃,保持在170℃下反应6h,反应过程中不断搅拌溶液,反应完全后,过滤,得到硫化锂粗料;
43.s3、将s1得到金属锂粗料、硫化钠装入80l n-甲基吡咯烷酮密封装置中,通入硫化氢气体,搅拌均匀,加热至70℃,反应釜内的气压保持在50pa,反应温度维持在70℃,反应完
全后,过滤,分别得到金属锂粗料和含有硫氢化钠的n-甲基吡咯烷酮溶液;
44.s4、将正己烷和1,3-二氧环戊烷按照体积比为1:1混合,得到洗涤液,将得到的硫化锂粗料和金属锂粗料分别在密闭的环境中,用洗涤液洗涤三次并过滤,然后分别置于真空烘箱中,在450℃下真空干燥处理1h,得到7.84kg硫化锂和3.01kg金属锂。
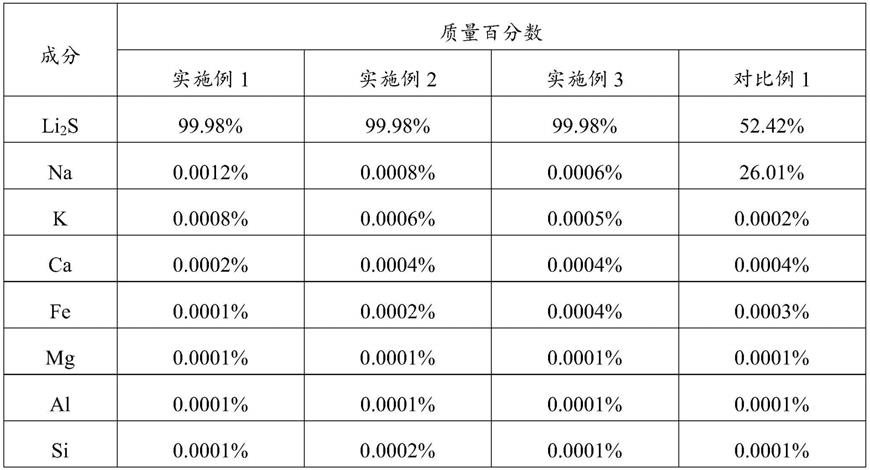
45.对实施例1-3回收得到的硫化锂和金属锂的品质进行检测,检测方式采用icp(电感耦合等离子体原子发射光谱仪)测定元素含量,结果见表1和表2所示。同时计算回收率,以锂计回收率结果见表3所示。
46.表1
[0047][0048]
其中表1中的li2s为折算值。
[0049]
表2
[0050][0051][0052]
表3
[0053] 硫化锂质量硫化锂纯度金属锂质量金属锂纯度回收率(以锂计)
实施例113.18kg99.98%3.14kg99.9%98.07%实施例222.8kg99.98%3.23kg99.9%95.07%实施例331.35kg99.98%3.63kg99.9%97.46%对比例117.84kg52.42%2.57kg98.04%65.45%
[0054]
从表1、表2和表3可以看出,采用本发明的回收方法,得到的硫化锂和金属锂的纯度非常高,达到99.9%,同时回收率(以锂计)也大于95%;而对比例1由于将硫化氢替换成硫氢化钠进行反应,导致硫化锂和金属锂的纯度以及回收率(以锂计)均明显降低。
[0055]
以上对本发明的较佳实施方式进行了具体说明,但本发明创造并不限于所述实施例,熟悉本领域的技术人员在不违背本发明精神的前提下还可作出种种的等同变型或替换,这些等同的变型或替换均包含在本技术权利要求所限定的范围内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1