一种甘氨酸锌络合物的制备方法与流程
本发明涉及一种化合物的制备方法,具体涉及一种甘氨酸锌络合物的制备方法。
背景技术:
锌是人和动物必需的微量元素。锌能够改善人味觉,还能加速生长发育;也可以调节机体免疫、防止感染和促进伤口愈合等。锌可协助葡萄糖在细胞上转运,一分子胰岛素中有2个锌原子。锌与胰岛素的活性有关。甘氨酸锌络合物是利用小肠对氨基酸的主动吸收。在体外将甘氨酸及锌结合成稳定的甘氨酸锌络合物.可不受食物因素的影响而整体吸收。甘氨酸锌络合物进入体内分解成甘氨酸和锌。其中,甘氨酸和锌的吸收快,安全性好,生物利用率不仅高于传统的补锌药物,且对降低血糖有效。
目前国内外合成甘氨酸锌络合物有很多的方法。主要有:复分解法、直接配位法、室温固相法等,但比例多为甘氨酸:七水合硫酸锌为2:1;关于合成比例为1:1的报导资料较少。而且在常温下结晶的甘氨酸锌络合物产率较高,但是合成的产品所含的结晶水数量较多,不利于生产和保存等。
技术实现要素:
本发明的目的在于克服现有技术存在的不足之处而提供了一种甘氨酸锌络合物的制备方法,本发明还提供了采用该方法制备的甘氨酸锌络合物。
为实现上述目的,所采取的技术方案:一种甘氨酸锌络合物的制备方法,所述制备方法包括以下步骤:
将甘氨酸和七水合硫酸锌溶解于水中,加入少量铁粉和数滴浓硫酸,在70-90℃下转动反应,然后冷却结晶后抽滤,得到结晶固体,用无水乙醇洗涤所述结晶固体数次,自然晾干,得到所述甘氨酸锌络合物。
本申请发明人为了生产出合成产率较高,而且为了得到的甘氨酸锌络合物产品所含的结晶水数量较低,方便甘氨酸锌络合物的保存和使用,研究了在不同温度下和不同的投料浓度下结晶,以产率和结晶水数量为依据,得出了最佳方案。
优选地,所述结晶温度为50~65℃。
优选地,所述结晶温度为50℃。
优选地,所述反应生成的甘氨酸锌络合物占所述反应体系总重量的67-85%。
优选地,所述反应生成的甘氨酸锌络合物占所述反应体系总重量的85%。
优选地,所述搅拌转动速度为50-70r/s,所述反应时间为30-60min。
优选地,所述铁粉的重量为所述七水合硫酸亚铁重量的0.5-1.5‰。
优选地,所述浓硫酸的重量为所述七水合硫酸亚铁重量的0.5-1‰。本发明提供了一种甘氨酸锌络合物,所述甘氨酸锌络合物采用上述所述方法制备而成。
本发明的有益效果在于:本发明提供了一种甘氨酸锌络合物的制备方法,。该方法结晶温度50-65℃,高于现存方法结晶温度25℃,减少了降温结晶过程所用时间和制冷降温能耗;同时通过该方法得到的甘氨酸锌络合物产率高,并且产品含结晶水少,产品后续烘干能耗低。
附图说明
图1为本发明所述甘氨酸铁的一种实施例的合成流程图;
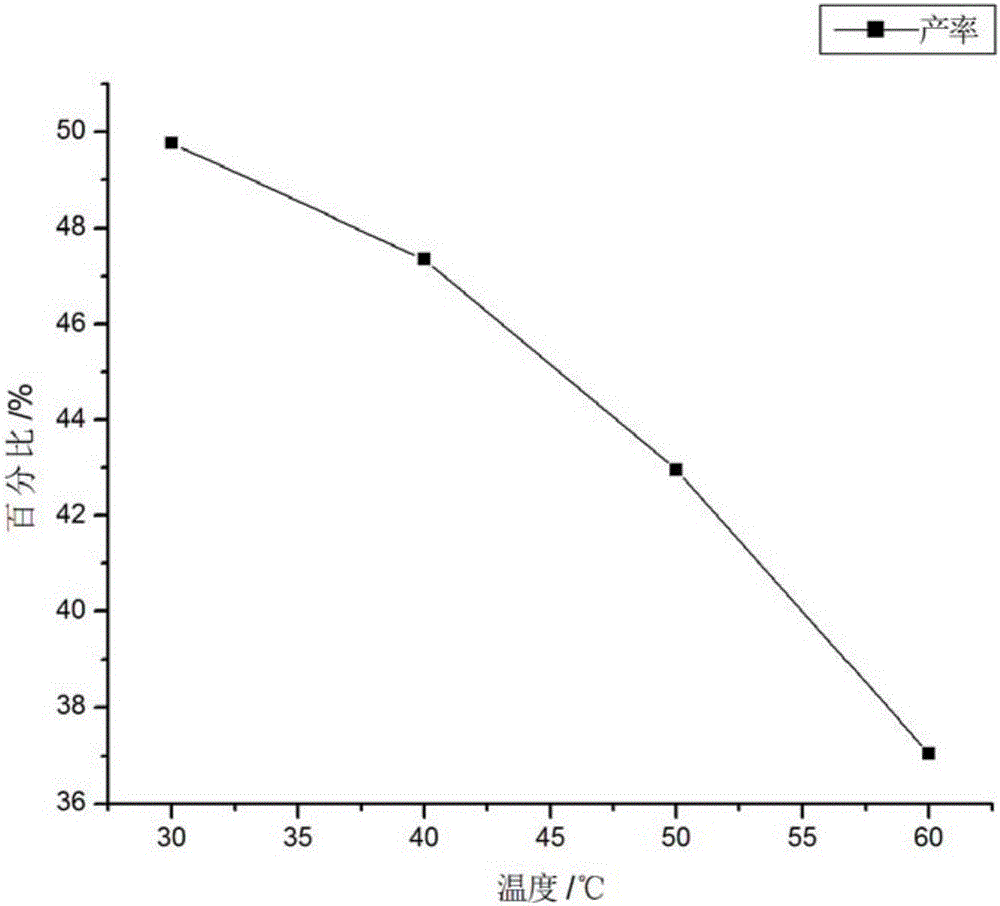
图2为本发明实施例1中甘氨酸锌络合物的温度与产率曲线图;
图3为本发明实施例1中甘氨酸锌络合物的溶解度曲线图;
图4为本发明实施例1中甘氨酸锌络合物的红外谱图。
具体实施方式
为更好的说明本发明的目的、技术方案和优点,下面将结合具体实施例对本发明作进一步说明。
实施例1
常温下结晶的甘氨酸锌络合物产率较高,但是合成的产品所含的结晶水数量较多,不利于生产和保存等,因此,为了生产出合成产率较高,而且甘氨酸锌络合物产品所含的结晶水数量较低,方便甘氨酸锌络合物的保存和使用,研究在不同温度下和不同的投料浓度下结晶,以产率和结晶水数量为依据,得出最佳的实验方案。
1 实验材料与方法
1.1 实验材料与仪器
原料:七水硫酸锌(ZnSO4·7H2O);水(H2O);甘氨酸(C2H5NO2);浓硫酸;铁粉;无水乙醇;所用试剂均为分析纯。
仪器:旋转烧瓶;定氮仪;水浴加热器;滤纸;漏斗;锥形瓶;消化管;烧杯;所用仪器均为广州天科生物科技有限公司提供。
1.2 实验配方
实验配方1:浓度67%,总量200g,如表1。
表1甘氨酸锌络合物实验配方1
实验配方2:浓度85%,总量200g,如表2。
表2甘氨酸锌络合物实验配方2
1.3 实验原理:
以原料1:1的甘氨酸和七水合硫酸锌在加温到一定温度,保持一定的时间和保持一定的转速,停止加热,待冷却到常温下可以直接合成。
1.4 产品合成步骤:
甘氨酸锌络合物的合成流程如图1所示。
具体实验方法:称取甘氨酸和七水合硫酸锌于烧杯中,加水溶解,加少量铁粉和数滴浓硫酸,保持70-90℃温度,转速50-70r/s,反应30-60min生成甘氨酸锌络合物,,冷却结晶后抽滤,然后用无水乙醇洗涤结晶固体数次,自然晾干,得产品,称重。
1.5 实验分析方法:
1.5.1 锌含量的测定
称取0.8g试样,先称准至0.0002g,置于250mL碘量瓶中。接着加5mL乙酸溶液使样品溶解,加30mL水以及5滴二甲酚橙指示剂;然后滴加六次甲基四胺溶液至稳定的紫红色后再过量5mL,用乙二胺四乙酸二钠标准溶液滴定至由紫红色变亮黄色即为终点,同时做空白校正。平行测3次,计算结果如下:
式中:c——乙二胺四乙酸二钠标准溶液的摩尔浓度,moL/L;
V——滴定试样时消耗乙二胺四乙酸二钠标准溶液体积,mL;
0.06539——每毫摩尔锌的质量克数;
m——试样质量,g。
1.5.2氮含量的测定:凯氏定氮法
(1)试样的消煮:称取0.2000g试样,放入消化管中,放入6.4g CuSO4·K2SO4混合催化剂,与试样混合均匀,再加入12mL硫酸,于420℃下消煮炉上消化至溶液呈透明的蓝绿色后,再消化2h。
(2)氨的蒸馏:采用全自动定氮仪并按仪器本身常量程序进行测定。
(3)滴定:用0.1moL/L的标准盐酸溶液滴定吸收液,如果溶液由蓝绿色变为灰红色为终点。
(4)空白测定:称取蔗糖0.2000g,代替试样按以上进行空白测定。消耗0.1moL/L盐酸标准溶液的体积不得超过0.2mL,消耗0.02moL/L盐酸标准溶液体积不得超过0.3mL。
(5)蒸馏步骤的检验:精确称取0.2g硫酸铵,代替试样进行操作。测得硫酸铵含氮量是否为21.19±0.2%,如果不是,应检查加碱、蒸馏和滴定步骤是否正确。
(6)计算:
式中:V2——滴定试样时所需标准盐酸溶液体积,mL
V1——滴定空白时所需标准盐酸溶液体积,mL
c——盐酸标准溶液浓度,moL/L;
m——试样质量,g;
0.0140——每毫克当量氮的克数。
2 结果与讨论
2.1 常温对其影响
常温下的甘氨酸锌络合物的结晶,主要是做对比和参考作用。通过在常温下结晶,研究其产品的产率和所含的结晶水的数量,作为一个参考体,方便甘氨酸锌络合物在高温下结晶和不同投料浓度下的产品进行对比。
当投料浓度为67%,投料量为200g时,所述投料浓度是指反应生成的甘氨酸锌络合物重量占反应体系总重量的百分比。先准确称取甘氨酸31.3g和七水合硫酸锌118.0g于烧杯中,加50.7g水溶解,之后加少量铁粉和数滴浓硫酸,所述铁粉的重量为所述七水合硫酸亚铁重量的1‰,所述浓硫酸的重量为所述七水合硫酸亚铁重量的0.5‰,放入恒温水浴锅的烧瓶中,保持85℃温度,转速50r/s,在反应30min之后,在常温下结晶,得到结晶固体,最后用无水乙醇洗涤结晶固体数次,自然晾干,得产品,称重得出产率。
将所得的产品通过凯氏定氮法和对锌离子的滴定之后,计算出氮含量和亚铁离子的含量,然后计算出结晶水的数量,结果如表3所示。
表3甘氨酸锌络合物常温结晶
由表3可以看出,甘氨酸锌络合物在常温下结晶,产率较高,但是得出的产品的结晶水数量较高,不利于生产。
2.2 温度对其影响
为了观察在不同的温度下,对合成甘氨酸锌络合物的影响,在温度的设置上,设置的温度间隔为10℃,但根据实际在高温结晶上的可能性,最后确定最高结晶温度为60℃。因此研究在不同的结晶温度下,以最终的产率和结晶水的数量为指标,观察其不同的影响。
当投料浓度为67%,投料量为200g时。先准确称取甘氨酸31.3g和七水合硫酸锌118.0g于烧杯中,加50.7g水溶解,之后加少量铁粉和数滴浓硫酸,所述铁粉的重量为所述七水合硫酸亚铁重量的1‰,所述浓硫酸的重量为所述七水合硫酸亚铁重量的0.5‰,放入恒温水浴锅的烧瓶中,保持85℃温度,转速50r/s,在反应30min之后,在常温下结晶,得到结晶固体,最后用无水乙醇洗涤结晶固体数次,自然晾干,得产品,称重得出产率。
由于该反应要达到过饱和浓度才能进行结晶,所以在试验之后,只有在投料浓度为70-82%时才能高温下结晶,因此,设置投料浓度在85%时,先准确称取甘氨酸39.1g和七水合硫酸锌149.6g于烧杯中,加11.3g水溶解,之后加少量铁粉和数滴浓硫酸,所述铁粉的重量为所述七水合硫酸亚铁重量的1‰,所述浓硫酸的重量为所述七水合硫酸亚铁重量的0.5‰,放入恒温水浴锅的烧瓶中,同样保持85℃温度,转速50r/s,在反应30min之后,分别在50℃、60℃下结晶,得到结晶固体,最后用无水乙醇洗涤结晶固体数次,自然晾干,得最终产品,称重得出产率。
将所得的产品通过凯氏定氮法和对锌离子的滴定之后,计算出氮含量和亚铁离子的含量,然后计算出结晶水的数量,结果如表4所示。
表4不同温度对甘氨酸锌络合物的影响
由表4和图2可以看出,在其他反应条件不变的情况下,随着结晶温度的升高,甘氨酸锌络合物产率逐渐降低,结晶水的数量也降低,然后维持一个稳定值。结晶的温度在50℃时,所得的产品产率与常温下结晶相差最小,而且结晶水数量降低了,考虑到实验效率的问题,最终确定当结晶温度为50℃时,为此反应的最佳温度。
2.3 原料配比对其影响
为了观察不同的原料配比对合成甘氨酸锌络合物的影响,在投料浓度的设置上,原本设置的浓度间隔为5%,但根据实际在高温结晶上的可能性,要达到过饱和浓度才能进行结晶,所以在试验之后,最后确定投料浓度只有在70-82%时,才能进行多个温度下的结晶,因此确定投料浓度为85%。研究在不同的投料浓度下,以最终的产率为指标,观察其不同的影响。
当投料浓度为67%,投料量为200g时。先准确称取甘氨酸31.3g和七水合硫酸锌118.0g于烧杯中,加50.7g水溶解,之后加少量铁粉和数滴浓硫酸,所述铁粉的重量为所述七水合硫酸亚铁重量的1‰,所述浓硫酸的重量为所述七水合硫酸亚铁重量的0.5‰,放入恒温水浴锅的烧瓶中,保持85℃温度,转速50r/s,在反应30min之后,在常温下结晶,得到结晶固体,最后用无水乙醇洗涤结晶固体数次,自然晾干,得产品,称重得出产率。
设置投料浓度在85%时,先准确称取甘氨酸39.1g和七水合硫酸锌149.6g于烧杯中,加11.3g水溶解,之后加少量铁粉和数滴浓硫酸,所述铁粉的重量为所述七水合硫酸亚铁重量的1‰,所述浓硫酸的重量为所述七水合硫酸亚铁重量的0.5‰,放入恒温水浴锅的烧瓶中,同样保持85℃温度,转速50r/s,在反应30min之后,分别在50℃、60℃下结晶,得到结晶固体,最后用无水乙醇洗涤结晶固体数次,自然晾干,得最终产品,称重得出产率。
将所得的产品通过凯氏定氮法和对锌离子的滴定之后,计算出氮含量和亚铁离子的含量,然后计算出结晶水的数量,结果如表5所示。
表5原料配比对甘氨酸锌络合物的影响
由表5可以看出,当投料浓度为67%,甘氨酸锌络合物在高温下不能结晶析出晶体,只能在常温下析出结晶,当投料浓度为82%时,甘氨酸锌络合物随着结晶温度的升高,甘氨酸锌络合物产率逐渐降低。因此当结晶的温度在50℃时,投料浓度为85%时,产率较高,反应最佳。
2.4 正交试验
为了更好的对合成甘氨酸锌络合物进行全面的了解和观察,本正交实验在温度的设置上,以温度间隔为10℃;在投料浓度的设置上,原本设置的浓度间隔为5%,但根据实际在高温结晶上的可能性,要达到过饱和浓度才能进行结晶,所以在试验之后,最后确定投料浓度在85%时,能进行多个温度下的结晶,因此确定最终的正交实验方案。研究在不同的结晶温度以及不同的投料浓度下,进行多方面的对比,对合成甘氨酸锌络合物产品得出一个最佳的实验方案。主要从最终的产率和结晶水数量等,观察其不同的影响。
当投料浓度为67%,投料量为200g时。先准确称取甘氨酸31.3g和七水合硫酸锌118.0g于烧杯中,加50.7g水溶解,之后加少量铁粉和数滴浓硫酸,所述铁粉的重量为所述七水合硫酸亚铁重量的1‰,所述浓硫酸的重量为所述七水合硫酸亚铁重量的0.5‰,放入恒温水浴锅的烧瓶中,保持85℃温度,转速50r/s,在反应30min之后,在常温下结晶,得到结晶固体,最后用无水乙醇洗涤结晶固体数次,自然晾干,得产品,称重得出产率。
设置投料浓度在85%时,先准确称取甘氨酸39.1g和七水合硫酸锌149.6g于烧杯中,加11.3g水溶解,之后加少量铁粉和数滴浓硫酸,所述铁粉的重量为所述七水合硫酸亚铁重量的1‰,所述浓硫酸的重量为所述七水合硫酸亚铁重量的0.5‰,放入恒温水浴锅的烧瓶中,同样保持85℃温度,转速50r/s,在反应30min之后,分别在50℃、60℃下结晶,得到结晶固体,最后用无水乙醇洗涤结晶固体数次,自然晾干,得最终产品,称重得出产率。
将所得的产品通过凯氏定氮法和对锌离子的滴定之后,计算出氮含量和亚铁离子的含量,然后计算出结晶水的数量,结果如表6。
表6不同温度、配料比对甘氨酸锌络合物的影响
由表6可以看出,在其他反应条件不变的情况下,只有在投料浓度为85%时,甘氨酸锌络合物才能高温结晶。而且随着结晶温度的升高,甘氨酸锌络合物产率逐渐降低,结晶水的数量也降低,然后维持一个稳定值。结晶的温度在50℃时,所得的产品产率与常温下结晶相差最小,而且结晶水数量降低了,考虑到实验效率的问题,最终确定当投料浓度为85%,结晶温度为50℃时,为最佳反应,所得产品含结晶水数量较少,且产率较高。
2.5 产品的感官和定性鉴定
合成的甘氨酸锌络合物是一种白色粉末状物品。基本无异味,但是易潮解和易溶于水;不溶于乙醇等有机溶剂,室温下能够稳定存在。
产品的溶解度曲线如图3所示。由图3可知,甘氨酸铁随着温度的上升,其溶解度逐渐增大,并且在温度大于50℃时,溶解度增加迅速。
2.6 红外谱图
用KBr压片法测定甘氨酸锌络合物在400~4 000cm-1的红外光谱,谱图如和图4所示。
甘氨酸与锌离子形成络合物后,它的一些主要吸收峰同配位体相比发生了明显位移。从而证实二价锌离子与甘氨酸发生了配位作用。甘氨酸的红外光谱在3101cm-1有较强宽谱带,这是NH的特征吸收峰,而甘氨酸锌络合物的红外光谱中无此吸收峰,同时在554cm-1处出现了Zn-N的伸缩振动峰,说明N原子参与了配位。同时,在3000cm-1处甘氨酸中羧酸的O-H的吸收峰在形成配合物后发生了明显位移,出现在3600cm-1,同时在480cm-1处出现了Zn-O伸缩振动峰,这进一步说明羧基参与了配位反应。
2.7 产品结构式分析
常温结晶甘氨酸锌络合物分子结构式如下:
由现有文献知,甘氨酸与锌离子以1:1的比例,在常温下结晶的甘氨酸锌络合物产品中,所含的结晶水数量为5个,如上式所示。而在高温结晶下,合成的甘氨酸锌络合物失去了大约两个结晶水,所剩的结晶水为三个。根据现有文献可知,锌离子为六配位,八面体结构,氢键结合六水合硫酸锌形成复合物的键长较锌离子与配体氢氧键和四个配位水中的氢键长,键能较弱。因此在高温状态下结晶,推测失去的2个结晶水可能为氢键结合六水合硫酸锌形成复合物的结晶水。
通过对甘氨酸锌络合物在不同的温度和不同的配料比下结晶的实验,得出在其他反应条件不变的情况下,只有在投料浓度为70-85%时,甘氨酸锌络合物才能高温结晶。而且随着结晶温度的升高,甘氨酸锌络合物产率逐渐降低,结晶水的数量也降低,然后维持一个稳定值。结晶的温度在50℃时,所得的产品产率与常温下结晶相差最小,而且结晶水数量降低了,考虑到实验效率的问题,因此最终确定当投料浓度为85%,结晶温度为50℃时,为合成甘氨酸锌络合物的最佳反应。
最后所应当说明的是,以上实施例仅用以说明本发明的技术方案而非对本发明保护范围的限制,尽管参照较佳实施例对本发明作了详细说明,本领域的普通技术人员应当理解,可以对本发明的技术方案进行修改或者等同替换,而不脱离本发明技术方案的实质和范围。
- 还没有人留言评论。精彩留言会获得点赞!