一种VC‑CAR分子及在清除HIV‑1感染细胞中的应用的制作方法
本发明涉及肿瘤免疫治疗技术领域,具体地,涉及一种VC-CAR分子及在清除HIV-1感染细胞中的应用。
背景技术:
人类免疫缺陷病毒1型(Human Immunodificiency Viruse 1,HIV-1)感染后,联合抗逆转录病毒疗法(combined antiretroviral therapy,cART)可以有效地抑制病毒复制。然而,由于病毒整合在被感染细胞中并形成一个稳定的潜伏感染储存库,被感染者一旦停止cART治疗,病毒血症即在短时间内再爆发,这构成了治愈HIV-1感染的主要障碍。
当前的研究热点是通过特异性的潜伏感染逆转药物(latency-reversing agents,LRAs)激活潜伏感染的病毒,进而药物治疗或诱导机体免疫系统杀灭被感染细胞。这种干预策略被称为“shock and kill”。然而,HIV-1可以迅速的发生突变以逃避免疫识别。研究显示在经过cART治疗的感染者当中,即使成功激活了其潜伏感染,体内的CD8+T淋巴细胞由于缺乏对HIV-1有效的免疫应答,所以不能完全清除被感染的细胞。因此,在“shock and kill”策略中,为了更好的清除潜伏感染储存库,需要在被感染者体内重建强有力的免疫监控机能。
近年来,由于具有高亲和力、TCR(T cell receptor)非依赖和MHC(major histocompatibility complex)非限制等特点,嵌合抗原受体(chimeric antigen receptor,CAR)的免疫细胞疗法成为了杀伤肿瘤细胞的全新途径。CAR是由抗体靶向区域与T细胞激活胞内信号区融合而成,从而赋予细胞特异性抗原识别能力。通过在患者自体免疫细胞中表达识别肿瘤天然抗原的CAR分子并对进行过继免疫回输,可以特异性的靶向杀伤患者体内的肿瘤细胞。CAR-T细胞疗法已在白血病和淋巴瘤的临床治疗中证明了有效性,并且获得了令人鼓舞的成功。该策略也可应用于抗病毒治疗,包括HIV-1、HBV(hepatitis B virus)和HCV(hepatitis C virus)等病毒感染的治疗。但是,传统构建的CAR分子还不能完全满足各种疾病的免疫治疗。
技术实现要素:
本发明为了克服现有技术的上述不足,提供一种新的CAR分子,称作VC-CAR分子,VC-CAR分子是将HIV-1广谱中和抗体VRC01来源的scFv序列和传统的CAR分子的胞内段序列连接在一起,分别作为胞外和胞内结构。
本发明的另一个目的是提供一种经VC-CAR分子改造的CD8+T细胞。
本发明的再一个目的是提供一种经VC-CAR分子改造的CD8+T细胞在清除HIV-1感染细胞的应用。
为了实现上述目的,本发明是通过以下技术方案予以实现的:
SEQ ID NO:1所示的HIV-1广谱中和抗体VRC01来源的scFv序列在作为CAR分子的胞外抗原结合域中的应用。
一种VC-CAR分子,由SEQ ID NO:1所示的HIV-1广谱中和抗体VRC01来源的scFv序列和CAR分子的胞内段序列连接而成,HIV-1广谱中和抗体VRC01来源的scFv序列在N端,CAR分子胞内段序列在C端。
优选地,一种VC-CAR分子,其核苷酸序列如SEQ ID NO:2或SEQ ID NO:3或SEQ ID NO:4所示。SEQ ID NO:2所示的VC-CAR分子的结构如图1中的VR C01-28BBZ-1所示;SEQ ID NO:3所示的VC-CAR分子的结构如图1中的VR C01-28BBZ-2所示;SEQ ID NO:4所示的VC-CAR分子的结构如图1中的VR C01-28BBZ-3所示。
更优选地,一种VC-CAR分子,其核苷酸序列如SEQ ID NO:4所示。
一种改造的CD8+T细胞,具体为使用本发明设计的VC-CAR分子转导CD8+T细胞制备得到。VC-CAR改造的CD8+细胞介导表达gp120细胞系的裂解效果更加明显。
本发明还要求保护以VC-CAR分子改造的CD8+T细胞在清除HIV-1感染细胞的应用。
一种改造的CD8+T细胞,由以下方法制备得到:(1)收集外周血单个核细胞并分离富集其中的CD8+T细胞,利用anti-CD3、anti-CD28和IL-2激活CD8+T细胞;(2)细胞激活48小时后,以1ml/1×106细胞的比例加入VC-CAR分子重组的病毒浓缩液进行感染,同时加入聚凝胺溶液,离心后继续培养;8~12小时后,进行第二轮病毒感染。
优选地,所述anti-CD3的浓度为1μg/mL,anti-CD28的浓度为1μg/mL,IL-2的浓度为10ng/mL。
优选地,所述聚凝胺溶液的浓度为8μg/mL。
一种扩增VC-CAR分子改造的CD8+T细胞的方法,包括如下步骤:(1)CD8+T细胞被VC-CAR分子重组的病毒感染改造后的12小时,离心换液,洗去培养基中的病毒,以新鲜培养基重悬细胞,并加入IL-2和IL-7保持细胞状态;(2)病毒感染改造后的第3天和第5天,根据细胞状态和增殖情况,对细胞添加完全RMPI1640培养基,细胞浓度维持在2×106/ml,并补充IL-2和IL-7,继续培养并及时传代,进一步扩增细胞。
优选地,所述IL-2的浓度为10ng/mL,IL-7的浓度为10ng/mL。
与现有技术相比,本发明具有如下有益效果:
本发明中全新改造的VC-CAR-T细胞与表达HIV-1包膜蛋白的细胞系或HIV-1感染的CD4+T细胞进行共培养,VC-CAR-T细胞可以被特异性激活并大量分泌细胞毒性相关的细胞因子(包括IFN-γ、和Granzyme B),进而强有力地介导靶细胞的裂解。
本发明中全新改造的VC-CAR-T细胞相比已报道的CD4-CAR-T细胞,VC-CAR-T细胞介导表达gp120细胞系的裂解效果更加明显。
本发明使用的IL-2+IL-7细胞因子组合,相比单独施加IL-2的传统扩增方法,可以进一步提高HIV-1感染患者CD8+T细胞扩增倍数。
附图说明
图1为构建的VC-CAR分子的结构示意图。
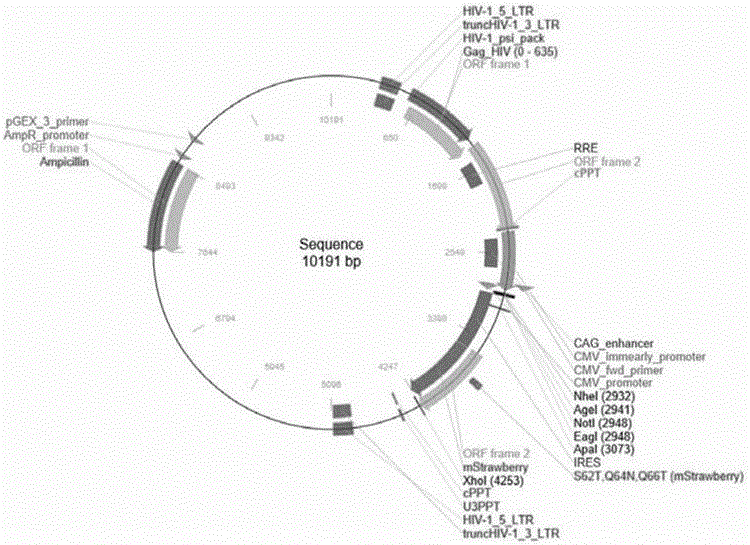
图2为pCPPT-IRES-mStrewbeery慢病毒载体结构示意图。
图3为VC-CAR在CD8+T细胞中的表达情况。
图4为VC-CAR和CD4-CAR改造的CD8+T细胞分别与靶细胞系混合后杀伤效果的比较。
图5为VC-CAR-T细胞与表达HIV-1包膜蛋白的靶细胞系混合培养后,IFN-γ和Granzyme-B的分泌情况。
图6为VC-CAR-T细胞与表达HIV-1包膜蛋白的靶细胞系混合培养后,通过检测LDH的释放,检测VC-CAR-T细胞的杀伤活性。
图7为VC-CAR-T细胞与野生型HIV-1NL4-3感染的CD4+T淋巴细胞进行混合培养,通过流式检测Gag+CD4+T淋巴细胞的比例。验证VC-CAR-T细胞的杀伤活性。
具体实施方式
下面结合说明书附图和具体实施例对本发明作出进一步地详细阐述,所述实施例只用于解释本发明,并非用于限定本发明的范围。下述实施例中所使用的试验方法如无特殊说明,均为常规方法;所使用的材料、试剂等,如无特殊说明,为可从商业途径得到的试剂和材料。
实施例1
一种以VRC01为胞外抗原结合域的VC-CAR分子,其核苷酸序列如SEQ ID NO:2或SEQ ID NO:3或SEQ ID NO:4所示。SEQ ID NO:2所示的VC-CAR分子的结构如图1中的VR C01-28BBZ-1所示;SEQ ID NO:3所示的VC-CAR分子的结构如图1中的VR C01-28BBZ-2所示;SEQ ID NO:4所示的VC-CAR分子的结构如图1中的VR C01-28BBZ-3所示。
HIV-1广谱中和抗体VRC01来源的scFv序列如SEQ ID NO:1所示。
下面以SEQ ID NO:4所示的VC-CAR分子详细介绍一下本发明的VC-CAR分子的结构设计。VC-CAR分子的序列N’端是HIV-1广谱中和抗体VRC01来源的scFv序列,可特异性结合病毒包膜蛋白的CD4结合域;VC-CAR分子序列C’端是以三代CAR结构为基础,包括CD28(nucleotides 460-660,GenBank NM_006139.3),CD137(nucleotides 640-765,GenBank NM_001561.5)和CD3ζ(nucleotides 160-492,Genbank NM_198053.2)胞内结构域串联组成,通过CD28分子的跨膜结构域将scFv和胞内信号分子相连。
实施例2
一、VC-CAR分子重组pCPPT-IRES-mStrewbeery慢病毒载体:按照SEQ ID NO:4所示序列合成VC-CAR,合成的VC-CAR通过NheI和NotI双酶切,插入pCPPT-IRES-mStrewbeery慢病毒载体中(见图2),酶切、连接的具体步骤参考本领域的常规方法;得到VC-CAR分子重组后的pCPPT-IRES-mStrewbeery慢病毒载体。
将一个生长状态的HEK293T细胞平均铺于用多聚赖氨酸处理的10cm培养皿中(细胞密度约为6.5×104/cm2),要求细胞呈单个均匀分布。培养约24小时后,细胞汇合度应接近80%,此时各皿均以12ml完全培养基换液,同时加入3.75ul氯喹(100mM,4000×)。换液后按表1配制磷酸钙-DNA混合液,颠倒数次混匀后静置1分钟,然后以3ml/皿迅速加入各皿细胞培养液中,边加边摇匀,逐滴快速加入。
表1为磷酸钙-DNA混合液体系配方
转染后12小时,细胞汇合度应接近100%,此时各皿均以12ml新鲜培养基换液,同时加入90μl丁酸钠(1M,100×)。转染后约48小时,收集全部34ml HEK293T细胞上清液,以0.45μm的过滤器过滤后装入50ml离心管,按下表2比例加入PEG-NaCl-PBS混合液,颠倒混匀后于4℃放置1.5小时,期间每20~30分钟混匀一次或颠倒混匀后于4℃放置过夜。
表2
将混合液于4℃,7000g离心10分钟,管壁上可见白色沉淀,小心去除全部上清液,加入适量体积(300ul~3ml)的新鲜培养基,轻轻摇晃使沉淀溶解,即得到VC-CAR分子重组的病毒浓缩液,立即使用或分装后于-80℃保存。
二、VC-CAR在CD8+T细胞中的表达情况:从外周血样本中分离外周血单个核细胞,然后通过偶联生物素的CD8抗体分离富集CD8+T淋巴细胞,计数,离心。用RPMI1640完全培养基重悬,然后按2×106/ml的细胞浓度,均匀铺至细胞培养板中。利用anti-CD3(终浓度为1μg/ml)、anti-CD28(终浓度为1μg/ml)抗体和IL2(终浓度为10ng/ml)对细胞进行刺激,作用48小时后,收集细胞,用于假病毒的感染。
取适量生长状态良好的目标细胞悬液,放入离心管中300g离心5分钟。弃去上清液,以1ml/1×106细胞的比例加入假病毒浓缩液,同时加入终浓度8μg/ml的Polybrene,轻轻吹打混匀。将细胞悬液移入培养皿,37℃、350×g离心90分钟,离心结束后,放回培养箱中继续培养。约8~12小时后,进行第二轮感染,步骤同上,约12小时后,离心换液,用PBS洗去培养基中的病毒,以新鲜培养基重悬细胞,并加入终浓度均为10ng/ml的IL-2和IL-7保持细胞状态。继续培养并及时传代,进一步扩增细胞。感染后的第3天,根据细胞状态和增殖情况,对细胞添加完全RMPI1640培养基,细胞浓度维持在2×106/ml。并补充IL-2和IL-7,终浓度均为10ng/ml。感染后的第5天,按照第3天的流程继续扩增细胞。并利用流式检测荧光蛋白mStrewbeery的表达,确定VC-CAR的感染效率,通常需确保感染率达到50%以上(图3)。感染后的第5天,细胞用于后续实验检测或继续培养以及冻存。此后,为了方便起见,以下实验均称其为VC-CAR-T细胞。
实施例3
一、VC-CAR和CD4-CAR改造的CD8+T细胞分别与靶细胞系混合后杀伤效果的比较:早前有研究利用CD4分子的胞外结构为基础,构建CAR-T细胞(CD4-CAR-T细胞)。由于CD4分子是HIV-1包膜糖蛋白gp120的天然受体,CD4-CAR-T细胞能够裂解表达gp120的靶细胞。为了对比VC-CAR-T细胞和CD4-CAR-T细胞效应,我们根据前人报道,将VC-CAR的scFv序列替换为CD4分子的胞外结构域构建了CD4-CAR。以同样的条件转导CD8+T淋巴细胞,然后与表达HIV-1包膜蛋白的靶细胞系(Jurkat-gp160NL4-3)混合,在U形底的96孔板中进行细胞杀伤实验。靶细胞数量为104/孔,RMPI1640完全培养基体积为200μl/孔。在给定的效靶比范围内(8:1至2:1),24小时后,通过检测乳酸脱氢酶的释放,以确定每个实验组经过改造CD8+T淋巴细胞的杀伤活性。结果显示:VC-CAR-T细胞比CD4-CAR-T细胞具有更强的靶细胞裂解能力。该结果可能的原因为HIV-1广谱中和抗体来源的scFv对HIV-1gp120亲和力强于天然的CD4分子(见图4)。
二、VC-CAR-T细胞与表达HIV-1包膜蛋白的靶细胞系混合培养后特异性细胞因子的分泌情况:为了进一步检测VC-CAR的功能,我们将VC-CAR-T细胞与表达HIV-1包膜蛋白的细胞系Jurkat-gp160NL4-3在预包被IFN-γ抗体的96孔PVDF板中进行混合培养,效应细胞数量为104/孔,在给定的效靶比范围内(4:1和2:1),24小时后,利用ELIspot实验检测VC-CAR-T细胞IFN-γ的分泌。结果显示:与两株靶细胞混合培养的VC-CAR-T细胞IFN-γ的分泌显著提高,而与HIV-1包膜蛋白阴性的对照细胞系Jurkat-GFP混合培养的VC-CAR-T细胞则不会分泌IFN-γ。另一方面,与表达HIV-1包膜蛋白的靶细胞系混合培养的对照效应细胞没有明显的IFN-γ分泌,从而进一步证明IFN-γ的分泌是VC-CAR-T细胞特异性的(图5)。
将VC-CAR-T细胞与Jurkat-gp160NL4-3分别混合培养24小时,在给定的效靶比范围内(4:1-2:1),granzyme B的ELISA实验也显示,随着靶细胞增加(Jurkat-gp160NL4-3),VC-CAR-T细胞的细胞因子分泌量会以剂量依赖的方式随之增加,而对照靶细胞(Jurkat-GFP)则不会刺激VC-CAR-T细胞分泌IL-2和granzyme B。结果说明,在特异性抗原刺激下,VC-CAR-T细胞具有高效分泌抗病毒细胞因子的能力(图5)。
三、VC-CAR-T细胞与表达HIV-1包膜蛋白的靶细胞系混合培养后杀伤活性的检测:为了进一步检测VC-CAR的功能,我们将VC-CAR-T细胞与两株表达HIV-1包膜蛋白的细胞系Jurkat-gp160NL4-3和Jurkat-gp160BaL分别进行混合培养,在U形底的96孔板中进行细胞杀伤实验。靶细胞数量为104/孔,RMPI1640完全培养基体积为200μl/孔。在给定的效靶比范围内(8:1-0.5:1),24小时后,通过LDH的释放,我们检测VC-CAR-T细胞对HIV-1包膜蛋白表达细胞的细胞毒性。结果显示:在从8:1到0.5:1的效靶比区间范围内,VC-CAR-T细胞以剂量依赖的方式显著杀伤两株表达HIV-1gp120的靶细胞(Jurkat-gp160NL4-3和Jurkat-gp160BaL),而对照靶细胞(Jurkat-GFP)没有显著的杀伤效果,说明VC-CAR-T细胞杀伤靶细胞作用是HIV-1gp120特异性的。无论Jurkat-gp160NL4-3和Jurkat-gp160BaL还是对照靶细胞Jurkat-GFP,对照效应细胞均没有显示明显杀伤作用,从而进一步说明了VC-CAR-T细胞作用的特异性(图6)。
四、VC-CAR-T细胞与野生型HIV-1NL4-3感染的CD4+T淋巴细胞进行混合培养后杀伤活性的检测:为了进一步证明在清除野生型HIV-1感染的细胞方面VC-CAR-T细胞的有效性,利用野生型HIV-1NL4-3,对健康人血液样本中分离的CD4+T淋巴细胞进行感染。进行感染时RMPI1640完全培养基的体积为1ml/孔(24孔板),包含2×106细胞,对应200ng(p24)的野生型病毒。感染后3小时换液。感染后的第8天,该细胞与VC-CAR改造的同源CD8+T淋巴细胞以1:2和1:4的比例混合,在24孔板中进行细胞杀伤实验。靶细胞数量为106/孔,RMPI1640完全培养基体积为500μl/孔。48小时后,通过流式细胞术检测Gag+CD4+T淋巴细胞的比例,验证VC-CAR-T细胞的杀伤作用。结果显示:VC-CAR-T细胞对HIV-1感染的细胞的清除率高达78%,表现了显著的杀伤效果,同时对照效应细胞的数值不足30%,两者差异具有统计学意义(图7)。
SEQUENCE LISTING
<110> 中山大学
<120> 一种VC-CAR分子及在清除 HIV-1感染细胞中的应用
<130>
<160> 4
<170> PatentIn version 3.3
<210> 1
<211> 735
<212> DNA
<213> VRC01
<400> 1
atggaaattg tgttgacaca gtctccaggc accctgtctt tgtctccagg ggaaacagcc 60
atcatctctt gtcggaccag tcagtatggt tccttagcct ggtatcaaca gaggcccggc 120
caggccccca ggctcgtcat ctattcgggc tctactcggg ccgctggcat cccagacagg 180
ttcagcggca gtcggtgggg gccagactac aatctcacca tcagcaacct ggagtcggga 240
gattttggtg tttattattg ccagcagtat gaattttttg gccaggggac caaggtccag 300
gtcgacatta agcgagaggg cagaggaagt ctgctaacat gcggtgacgt cgaggagaat 360
cctggccagg tgcagctggt gcagtctggg ggtcagatga agaagcctgg cgagtcgatg 420
agaatttctt gtcgggcttc tggatatgaa tttattgatt gtacgctaaa ttggattcgt 480
ctggcccccg gaaaaaggcc tgagtggatg ggatggctga agcctcgggg gggggccgtc 540
aactacgcac gtccacttca gggcagagtg accatgactc gagacgttta ttccgacaca 600
gcctttttgg agctgcgctc gttgacagta gacgacacgg ccgtctactt ttgtactagg 660
ggaaaaaact gtgattacaa ttgggacttc gaacactggg gccggggcac cccggtcatc 720
gtctcatcag aattc 735
<210> 2
<211> 1656
<212> DNA
<213> 人工序列
<400> 2
atggaaattg tgttgacaca gtctccaggc accctgtctt tgtctccagg ggaaacagcc 60
atcatctctt gtcggaccag tcagtatggt tccttagcct ggtatcaaca gaggcccggc 120
caggccccca ggctcgtcat ctattcgggc tctactcggg ccgctggcat cccagacagg 180
ttcagcggca gtcggtgggg gccagactac aatctcacca tcagcaacct ggagtcggga 240
gattttggtg tttattattg ccagcagtat gaattttttg gccaggggac caaggtccag 300
gtcgacatta agcgagaggg cagaggaagt ctgctaacat gcggtgacgt cgaggagaat 360
cctggccagg tgcagctggt gcagtctggg ggtcagatga agaagcctgg cgagtcgatg 420
agaatttctt gtcgggcttc tggatatgaa tttattgatt gtacgctaaa ttggattcgt 480
ctggcccccg gaaaaaggcc tgagtggatg ggatggctga agcctcgggg gggggccgtc 540
aactacgcac gtccacttca gggcagagtg accatgactc gagacgttta ttccgacaca 600
gcctttttgg agctgcgctc gttgacagta gacgacacgg ccgtctactt ttgtactagg 660
ggaaaaaact gtgattacaa ttgggacttc gaacactggg gccggggcac cccggtcatc 720
gtctcatcag aattcggtgg aggcggttca ggcggaggtg gctctggcgg tggcggatcg 780
ttcgtgccgg tcttcctgcc agcgaagccc accacgacgc cagcgccgcg accaccaaca 840
ccggcgccca ccatcgcgtc gcagcccctg tccctgcgcc cagaggcgtg ccggccagcg 900
gcggggggcg cagtgcacac gagggggctg gacttcgcct gtgatatcta catctgggcg 960
cccttggccg ggacttgtgg ggtccttctc ctgtcactgg ttatcaccct ttactgcaac 1020
cacaggaaca ggagtaagag gagcaggctc ctgcacagtg actacatgaa catgactccc 1080
cgccgccccg ggcccacccg caagcattac cagccctatg ccccaccacg cgacttcgca 1140
gcctatcgct cccgtttctc tgttgttaaa cggggcagaa agaagctcct gtatatattc 1200
aaacaaccat ttatgagacc agtacaaact actcaagagg aagatggctg tagctgccga 1260
tttccagaag aagaagaagg aggatgtgaa ctgagagtga agttcagcag gagcgcagac 1320
gcccccgcgt accagcaggg ccagaaccag ctctataacg agctcaatct aggacgaaga 1380
gaggagtacg atgttttgga caagagacgt ggccgggacc ctgagatggg gggaaagccg 1440
agaaggaaga accctcagga aggcctgtac aatgaactgc agaaagataa gatggcggag 1500
gcctacagtg agattgggat gaaaggcgag cgccggaggg gcaaggggca cgatggcctt 1560
taccagggtc tcagtacagc caccaaggac acctacgacg cccttcacat gcaggccctg 1620
ccccctcgcg attacaagga tgacgacgat aagtaa 1656
<210> 3
<211> 1491
<212> DNA
<213> 人工序列
<400> 3
atggaaattg tgttgacaca gtctccaggc accctgtctt tgtctccagg ggaaacagcc 60
atcatctctt gtcggaccag tcagtatggt tccttagcct ggtatcaaca gaggcccggc 120
caggccccca ggctcgtcat ctattcgggc tctactcggg ccgctggcat cccagacagg 180
ttcagcggca gtcggtgggg gccagactac aatctcacca tcagcaacct ggagtcggga 240
gattttggtg tttattattg ccagcagtat gaattttttg gccaggggac caaggtccag 300
gtcgacatta agcgagaggg cagaggaagt ctgctaacat gcggtgacgt cgaggagaat 360
cctggccagg tgcagctggt gcagtctggg ggtcagatga agaagcctgg cgagtcgatg 420
agaatttctt gtcgggcttc tggatatgaa tttattgatt gtacgctaaa ttggattcgt 480
ctggcccccg gaaaaaggcc tgagtggatg ggatggctga agcctcgggg gggggccgtc 540
aactacgcac gtccacttca gggcagagtg accatgactc gagacgttta ttccgacaca 600
gcctttttgg agctgcgctc gttgacagta gacgacacgg ccgtctactt ttgtactagg 660
ggaaaaaact gtgattacaa ttgggacttc gaacactggg gccggggcac cccggtcatc 720
gtctcatcag aattcggtgg aggcggttca ggcggaggtg gctctggcgg tggcggatcg 780
tttcccggac cttctaagcc cttttgggtg ctggtggtgg ttggtggagt cctggcttgc 840
tatagcttgc tagtaacagt ggcctttatt attttctggg tgaggagtaa gaggagcagg 900
ctcctgcaca gtgactacat gaacatgact ccccgccgcc ccgggcccac ccgcaagcat 960
taccagccct atgccccacc acgcgacttc gcagcctatc gctccaaacg gggcagaaag 1020
aaactcctgt atatattcaa acaaccattt atgagaccag tacaaactac tcaagaggaa 1080
gatggctgta gctgccgatt tccagaagaa gaagaaggag gatgtgaact gaagttcagc 1140
aggagcgcag acgcccccgc gtaccagcag ggccagaacc agctctataa cgagctcaat 1200
ctaggacgaa gagaggagta cgatgttttg gacaagagac gtggccggga ccctgagatg 1260
gggggaaagc cgcagagaag gaagaaccct caggaaggcc tgtacaatga actgcagaaa 1320
gataagatgg cggaggccta cagtgagatt gggatgaaag gcgagcgccg gaggggcaag 1380
gggcacgatg gcctttacca gggtctcagt acagccacca aggacaccta cgacgccctt 1440
cacatgcagg ccctgccccc tcgcgattac aaggatgacg acgataagta a 1491
<210> 4
<211> 1521
<212> DNA
<213> 人工序列
<400> 4
atggaaattg tgttgacaca gtctccaggc accctgtctt tgtctccagg ggaaacagcc 60
atcatctctt gtcggaccag tcagtatggt tccttagcct ggtatcaaca gaggcccggc 120
caggccccca ggctcgtcat ctattcgggc tctactcggg ccgctggcat cccagacagg 180
ttcagcggca gtcggtgggg gccagactac aatctcacca tcagcaacct ggagtcggga 240
gattttggtg tttattattg ccagcagtat gaattttttg gccaggggac caaggtccag 300
gtcgacatta agcgagaggg cagaggaagt ctgctaacat gcggtgacgt cgaggagaat 360
cctggccagg tgcagctggt gcagtctggg ggtcagatga agaagcctgg cgagtcgatg 420
agaatttctt gtcgggcttc tggatatgaa tttattgatt gtacgctaaa ttggattcgt 480
ctggcccccg gaaaaaggcc tgagtggatg ggatggctga agcctcgggg gggggccgtc 540
aactacgcac gtccacttca gggcagagtg accatgactc gagacgttta ttccgacaca 600
gcctttttgg agctgcgctc gttgacagta gacgacacgg ccgtctactt ttgtactagg 660
ggaaaaaact gtgattacaa ttgggacttc gaacactggg gccggggcac cccggtcatc 720
gtctcatcag aattcggtgg aggcggttca ggcggaggtg gctctggcgg tggcggatcg 780
tttcccggac cttctaagcc cttttgggtg ctggtggtgg ttggtggagt cctggcttgc 840
tatagcttgc tagtaacagt ggcctttatt attttctggg tgaggagtaa gaggagcagg 900
ctcctgcaca gtgactacat gaacatgact ccccgccgcc ccgggcccac ccgcaagcat 960
taccagccct atgccccacc acgcgacttc gcagcctatc gctccggtgg aggcggttca 1020
aaacggggca gaaagaaact cctgtatata ttcaaacaac catttatgag accagtacaa 1080
actactcaag aggaagatgg ctgtagctgc cgatttccag aagaagaaga aggaggatgt 1140
gaactgggcg gtggcggatc gaagttcagc aggagcgcag acgcccccgc gtaccagcag 1200
ggccagaacc agctctataa cgagctcaat ctaggacgaa gagaggagta cgatgttttg 1260
gacaagagac gtggccggga ccctgagatg gggggaaagc cgcagagaag gaagaaccct 1320
caggaaggcc tgtacaatga actgcagaaa gataagatgg cggaggccta cagtgagatt 1380
gggatgaaag gcgagcgccg gaggggcaag gggcacgatg gcctttacca gggtctcagt 1440
acagccacca aggacaccta cgacgccctt cacatgcagg ccctgccccc tcgcgattac 1500
aaggatgacg acgataagta a 1521
- 还没有人留言评论。精彩留言会获得点赞!