一种检测遗传性血管疾病致病基因的DNA文库及其应用的制作方法
本发明涉及一种通过靶向高通量半导体测序技术检测诊断遗传性血管疾病致病基因的DNA文库及其应用。具体说是根据遗传性血管疾病致病基因,设计能覆盖上述基因外显子及毗邻区域的超多重PCR引物,并对样本基因组DNA进行超多重PCR扩增,扩增产物利用高通量测序技术进行测序,寻找致病突变,明确遗传性血管疾病的遗传学病因,为临床诊断提供遗传学和分子生物学的理论依据,属于生物医学领域临床检测技术中的基因检测技术。
背景技术:
遗传性血管疾病是心脑血管系统中一类严重威胁患者生命安全疾病,受累患者死亡率高,医疗负担重,预后不佳。这类疾病包括:主动脉夹层、主动脉瘤、出血性脑卒中等疾病,病病人经常发生猝死,患病的病因复杂,遗传异质性高。由于具有很强的遗传性,这类疾病患者家族中可有多人患病,代代受累,因此对患者家族而言,危害性巨大。目前,针对这一类疾病尚无治疗效果满意的特异性药物,主要的治疗手段均属于对症治疗,甚至很多患者还未到医院就发生了猝死。因此,能否早期识别和诊断遗传性血管疾病的患者,对这类病的防治就显得至关重要。
传统的遗传性血管疾病的诊断主要依靠临床表现(突发的疼痛或晕厥)和传统生物标记物(C反应蛋白CRP、DD二聚体D-Dimer等)和影像学检查(头颅CT、大血管CTA、主动脉超声及核磁共振等)。然而,临床上不同种类的遗传性血管疾病患者出现临床症状的时间差异较大,症状发生的突然,甚至很多患者首发症状即为猝死。因此,传统检查诊断方法存在特异性差、确诊时间晚(症状出现后)等问题。相对传统检测方法,基因诊断具有高灵敏性、可以在症状发生前提前预报的重大优势,并且结合每个病人受累基因和突变类型的不同,指导临床进行相应的诊疗,将更符合精准医疗的新理念。但是,既往基因诊断基于Sanger测序方法,成本高、费时久、操作复杂,不适用于临床多基因致病的复杂疾病,因此对遗传性血管疾病无能为力。
近年来,DNA测序技术迅猛发展,多个平台纷纷推出了高通量的快速测序方法。基于此,利用高通量测序技术作为基因筛查的工具,可以实现低成本、短时间、高敏感性的重要优势。对比目前的已有各种高通量测序平台,新出现的基于半导体测序技术的扩增子测序技术以其快速的运行时间,灵活的通量选择,较低的运行成本和相对简单的操作方法脱颖而出。这种方法非常适用于医疗单位通量灵活性强,报告时间要求快速的特点。
基于以上原因,利用基于高通量半导体扩增子测序技术设计一种检测遗传性血管疾病致病基因突变的方法,将大大缩短临床基因诊断时间,降低成本和劳动强度,更有效地服务临床医疗。
技术实现要素:
为实现上述目的,本发明提供一种用于诊断遗传性血管疾病的DNA文库,所述DNA文库包括序号为1-103的至少一个基因。
表1:遗传性血管疾病的致病基因1
注:*标注的号码为pubmed数据库的基因ID,该基因尚未收录于OMIM数据库,暂无OMIM编号。
优选的,所述DNA文库包括下列任意一组或者多组基因:序号为1-16的基因,序号为17-33的基因,序号为34-39的基因,和/或序号为40-103的基因。
更优选的,所述DNA文库包括序号为1-103的基因。
表2:遗传性血管疾病的致病基因2
更优选的,所述DNA文库还包括序号为104-151的至少一个基因。
更优选的,所述DNA文库还包括下列任意一组或者多组基因:序号为104-105的基因,序号为106-109的基因,序号为110的基因,序号为111的基因,序号为112-114的基因,序号为115的基因,序号为116的基因,序号为117的基因,序号为118-123的基因,序号为124的基因,序号为125-133的基因,序号为134-147的基因,序号为148-150的基因和/或序号为151的基因。
更优选的,所述DNA文库包括下列任意一组或者多组基因:序号为1-16,112-114的基因,序号为17-33,125-133的基因,序号为34-39,134-147的基因,序号为40-103,148-150的基因,序号为104-105的基因,序号为106-109的基因,序号为110的基因,序号为111的基因,序号为115的基因,序号为116的基因,序号为117的基因,序号为118-123的基因,序号为124的基因,和/或序号为151的基因。
更优选的,所述任意多组基因包括上述任意2,3,4,5,6,7,8,9,10,11,12,13,14组基因的组合。
最优选的,所述DNA文库包括序号为1-151的基因。
本发明还提供一种上述任意DNA文库的检测试剂。
优选的,所述检测试剂是能扩增上述DNA文库的引物。
更优选的,所述引物为,根据上述DNA文库,设计能覆盖上述基因外显子及毗邻调控区域的适用于超多重PCR的引物池,从而能对样本基因组DNA进行超多重PCR扩增。
优选的,所述毗邻调控区域为每个外显子边缘至少5bp区域。
优选的,所述引物池通过软件进行超多重PCR扩增设计,使得每一个反应管中一次扩增即可同步平行扩增数千个扩增子,从而对目标区域进行操作简便的高效率扩增。
本发明还提供一种上述DNA文库或者DNA文库的检测试剂在制备诊断试剂盒中的应用,所述试剂盒用于诊断遗传性血管疾病。
本发明还提供一种上述DNA文库或者DNA文库的检测试剂在制备诊断装置中的应用,所述诊断装置用于诊断遗传性血管疾病。
优选的,所述诊断装置是基因芯片。
优选的,所述检测试剂是能扩增上述DNA文库的引物。
更优选的,所述引物为,根据上述DNA文库,设计能覆盖上述基因外显子及毗邻调控区域的适用于超多重PCR的引物池,从而能对样本基因组DNA进行超多重PCR扩增。
更优选的,所述应用包括下列步骤:
(1)提供受试者样本的基因组DNA;
(2)从Ion TorrentTM高通量测序平台自动合成覆盖上述致病基因的扩增引物池,对目标区域进行超多重PCR扩增;(请再次确认此处修改是否合适?)
(3)对步骤(2)得到的扩增产物进行酶切;
(4)对步骤(3)得到的酶切产物加Barcode接头;优选的,所述Barcode接头来自于高通量测序建库试剂盒;
(5)对步骤(4)得到的连接产物进行纯化;
(6)对步骤(5)得到的纯化产物用通用引物进行二次扩增;优选的,该通用引物来自于高通量测序建库试剂盒;
(7)对步骤(6)得到的二次扩增产物进行片段选择及浓度测定,即建成患者目标区域扩增文库;
(8)对步骤(7)所得到的文库经过油包水PCR扩增反应后,将待测序目的片段连接于ISP珠子,得到反应液;
(9)将步骤(8)得到的包含ISP珠子的反应液点入芯片,上Ion TorrentTM高通量测序仪进行测序;
(10)将步骤(9)得到的碱基序列信息进行生物信息学比对处理,得到与疾病相关的突变位点;
(11)对步骤(10)得到的突变位点进行Sanger测序法验证。
优选的,所述样本来自受试者的外周血、体液、组织器官样本。
更优选的,所述应用进一步用于指导治疗,例如:临床症状类似的主动脉瘤患者,通过基因检测确诊的TGFBR1基因突变患者比较FBN1基因突变的患者,发病将更早,严重程度更高,猝死发生可能性也更大,应更积极地考虑进行手术治疗,以改善预后。
本发明还提供一种诊断试剂盒,其中,所述试剂盒包括上述遗传性血管疾病的致病基因的DNA文库或者上述DNA文库的检测试剂。
本发明还提供一种诊断装置,其中,所述装置包括上述遗传性血管疾病的致病基因的DNA文库或者上述DNA文库的检测试剂。
优选的,所述装置为基因芯片。
优选的,所述检测试剂是能扩增上述DNA文库的引物。
更优选的,所述引物为,根据上述DNA文库,设计能覆盖上述基因外显子及毗邻调控区域的适用于超多重PCR的引物池,从而能对样本基因组DNA进行超多重PCR扩增。
优选的,所述毗邻调控区域为每个外显子边缘至少5bp区域。
优选的,所述引物池通过软件进行超多重PCR扩增设计,使得每一个反应管中一次扩增即可同步平行扩增数千个扩增子,从而对目标区域进行操作简便的高效率扩增。
本发明提供一种使用上述DNA文库、DNA文库的检测试剂、诊断试剂盒或诊断装置对患者进行检测的方法,所述方法包括下列步骤:
(1)提供受试者样本的基因组DNA;
(2)从Ion TorrentTM高通量测序平台自动合成覆盖上述致病基因的扩增引物池,对目标区域进行超多重PCR扩增;
(3)对步骤(2)得到的扩增产物进行酶切;
(4)对步骤(3)得到的酶切产物加Barcode接头,所述Barcode接头来自于高通量测序建库试剂盒;
(5)对步骤(4)得到的连接产物进行纯化;
(6)对步骤(5)得到的纯化产物用通用引物进行二次扩增,该通用引物来自于高通量测序建库试剂盒;
(7)对步骤(6)得到的二次扩增产物进行片段选择及浓度测定,即建成患者目标区域扩增文库;
(8)对步骤(7)所得到的文库经过油包水PCR扩增反应后,将待测序目的片段连接于ISP珠子,得到反应液;
(9)将步骤(8)得到的包含ISP珠子的反应液点入芯片,上Ion TorrentTM高通量测序仪进行测序;
(10)将步骤(9)得到的碱基序列信息进行生物信息学比对处理,得到与疾病相关的突变位点;
(11)对步骤(10)得到的突变位点进行Sanger测序法验证。
(12)受试者样本中若存在上述致病基因的突变体,则受试者可以诊断为遗传性血管疾病。
优选的,所述样本来自受试者的外周血、体液、组织器官样本。
更优选的,所述方法进一步用于指导治疗,例如:临床症状类似的主动脉瘤患者,通过基因检测确诊的TGFBR1基因突变患者比较FBN1基因突变的患者,发病将更早,严重程度更高,猝死发生可能性也更大,应更积极地考虑进行手术治疗,以改善预后。
采用本发明的DNA文库对遗传性血管疾病患者进行基因诊断有着以下重要意义和效果:
1.通过基因筛查可以及时发现尚未表现出临床症状的遗传性血管疾病患者:许多遗传性血管疾病患者起病突然,甚至首发症状即是猝死,之前毫无预兆。尤其是已经有猝死家族史的病人,猝死风险更高。对于已诊断遗传性血管疾(如出血性脑卒中)患者的直系血亲,有很大概率遗传了同样的致病突变,只不过因为年龄尚幼,疾病还未表现出来。对于这种早期“隐匿型”遗传性血管疾病患者,未发病时传统的检查方法无法对其进行确诊。因此而基因筛查成为了诊断这些潜在患者的唯一手段;
2.基因诊断有助于制定进一步个性化治疗方案:通过基因诊断筛选出已知的遗传性血管致病突变携带患者,可以根据致病基因的类型和致病突变的种类结合文献病例报道,对其病情和预后有一个较为全面的评估,进而选择对应的最佳治疗方式。如:同样是可能导致主动脉疾病的Ehlers-Danlos综合征,COL3A1基因受累的血管型Ehlers-Danlos综合征患者相较PLOD1基因受累的脊柱侧凸型Ehlers-Danlos综合征患者,更加容易发生主动脉夹层或动脉瘤,从而发生猝死。因而,发现COL3A1致病突变的有症状患者,应当选择更积极地手术治疗方式,发现COL3A1致病突变的却尚未表现出主动脉疾病症状的年轻患者应当更加频繁和积极地进行随访和影像学检查。
3.本申请的DNA文库是申请人从众多的遗传性血管疾病致病基因中选择的151个基因,这些基因尤其适合包括中国人在内的黄色人种患者的检测。国际上缺乏大规模的中国黄色人种,基于测序的遗传性血管疾病基因诊断相关信息,绝大多数已知遗传性血管疾病致病基因都主要来自欧美人群的报道,它们对中国人的致病性及特点目前没有详细报道。发明者进行了长期的临床观察和大规模中国黄色人种人群遗传性血管疾病的基因诊断研究。
4.本发明中采用基于Ion TorrentTM高通量测序技术对目标区域的扩增产物进行检测,能够在一次测序反应中同时检测本发明中涉及的151个相关致病基因的全部外显子及毗邻区域,并且能根据不同芯片数据量的大小,调整检测样本数量,在保证平均测序深度500×的前提下,检测1到20人不等的样本数量,整个测序反应和数据分析判读能在两天之内完成,大大降低了扩增反应的成本和劳动强度,提高了时效性,同时,该检测区域具有覆盖度广,整体覆盖度达到98.70%。通过对目标扩增区域的测序和数据判读,能够准确识别与疾病相关的突变,判断疾病种类和病因,为临床提供及时可靠的检测报告。本发明设计的检测方法经过Sanger测序法验证,对二代测序深度达到100×的点突变,本方法的准确度达到100%;
5.基因诊断有助于遗传咨询、产前诊断和新生儿筛查等。因很多遗传性血管疾病患者面临猝死的风险,家人非常关注患者的兄弟姐妹或将来下一胎的健康。患者致病基因突变的确诊,可以为孕育健康的下一代提供明确的遗传咨询服务。遗传性血管疾病多数为常染色显性遗传病,患者兄弟姐妹有50%的发病可能性。对尚无症状年幼兄弟姐妹或子女进行致病基因检测有助于早期发现疾病、早期治疗,改善预后。
6.优选的,本发明的DNA文库覆盖:主动脉夹层、主动脉瘤、出血性脑卒中等疾病。本发明是目前已知检测遗传性血管疾病最全面的靶向测序基因检测试剂盒,151个基因的选择基于国际已报道和公认的临床致病基因数据库(OMIM数据库、HGMD数据库、ClinVar数据库)以及发明者自己的课题研究内容。这151个基因上的致病突变既可以单独致病,也可以联合致病导致更加严重和复杂的临床表型,本发明首次做到可以一次性全面对其进行测序。
综合来看,本发明中涉及的DNA文库、其检测试剂及其应用具有准确、灵活、快速、低成本的特点;经过临床评估,该发明对遗传性血管疾病具有很好的辅助诊断价值。
附图说明
图1一次Ion TorrentTM高通量测序反应的数据采集概要图
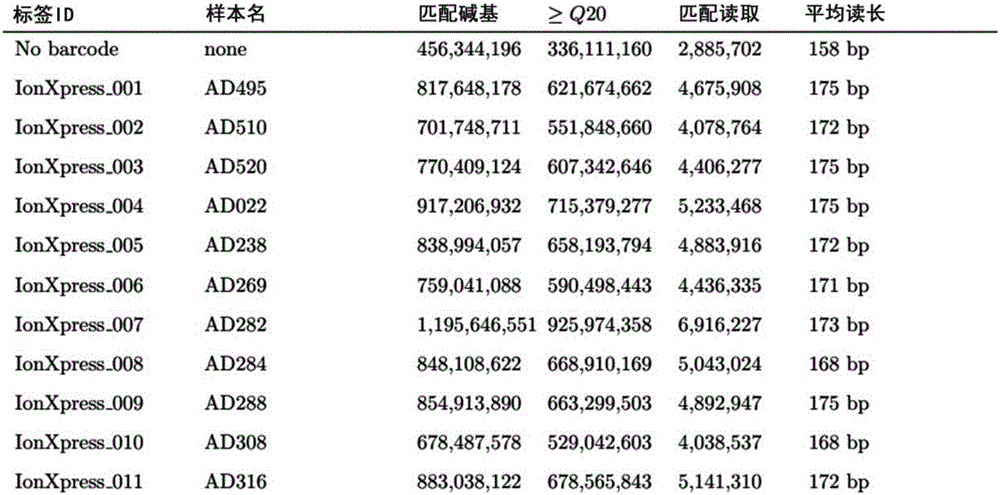
图2一次对151个基因的目标区域进行测序,不同标本得到的数据量信息
图3经过原始数据分析后,得到的不同标本的突变碱基数量
图4 Sanger测序法对本发明检测方法得到的突变位点进行验证
具体实施方式
下面结合具体实施方式对本发明作进一步说明,并非对发明的限定,依照本领域公知的现有技术,本发明的实施方式并不限于此,因此凡依照本公开内容所作出的本领域的等同替换,均属于本发明的保护范围。
实施例1
1.该方法中所用到的试剂:
Ion AmpliSeqTM Library Kit 2.0,Ion PITM Hi-QTM OT2 200Kit,Ion PITM Hi-QTM Sequencing 200Kit,Ion Xpress Barcode Adaptors 1-16Kit,Ion PITM Chip v3
2.标本采集和保存
(1)标本采集:标本为患者外周血。血液为常规取静脉血5ml,EDTA抗凝处理。
(2)保存:可立即检测,4℃保存一周,超过一周-80℃保存。
3.检测步骤和结果分析:
(1)标本基因组DNA的提取:标本DNA的提取按照天根生化科技(北京)有限公司的血液DNA提取试剂盒操作说明进行。
(2)目标检测区域的超多重PCR扩增及建库:以本发明中涉及的151个基因全外显子为检测区域,基于Ion AmpliSeqTM Designer自动合成超多重PCR引物,对标本DNA的目标区域进行扩增及建库,具体实施如下:
a.目标区域的扩增:
反应条件:
b.扩增产物二合一,酶切:
反应条件:
c.连接接头:
反应条件:
22℃ 30min
72℃ 10min
10℃ Up to 1h
d.纯化及纯化产物的二次扩增:纯化步骤按照Ion Ampliseq Library Preparation操作手册进行,最终产物溶解于52μl反应体系,该反应体系组成为:
反应条件:
e.片段选择:片段选择步骤按照Ion Ampliseq Library Preparation操作手册进行,得到的最终建库产物用Qubit 2.0Fluorometer定量后即建库完成。
(3)高通量测序:测序及前期准备步骤按照Ion PITM Hi-QTM OT2 200Kit及Ion PITM Hi-QTM Sequencing 200Kit操作手册进行:
a.油包水PCR反应:
将上述反应体系加入Ion OneTouch 2中进行油包水PCR反应。
b.油包水PCR反应完成后,连接有测序模板的Ion Sphere Particles经过Ion Onetouch ES纯化,加入测序引物及DNA聚合酶:
将得到的包含ISP珠子的反应液点入芯片,上Ion TorrentTM高通量测序仪进行测序。
(4)数据分析:测序数据经过coverage analysis和variant caller分析,得到碱基序列和突变位点,突变位点经过Ion Reporter在线注释后,得到对遗传性血管疾病诊断有意义的突变位点。
(5)Sange法验证:对于得到的突变位点,采用Sanger测序法进行验证。
结果说明及分析
通过本发明中涉及的高通量测序技术一次性对11个标本的目标区域进行检测(如图1),得到的总数据量为17.1G(Total Base),能够总共得到100,351,259的片段读长数据(Total Reads),每个片段的中位读长为166bp。11个标本平均能够被测到4886065(4038537-6916227)个片段读长Reads(如图2),以上测序结果为下一步的序列分析提供了充足的数据量。测序结果经过variant Caller分析,每个标本平均有398个变异(Variants)被读出(如图3)。检测区域的变异通过Ion Reporter在线注释后,与疾病相关的突变位点经过Sanger测序法验证(如图4),如图4例举的那样,图4箭头所指处显示TGFBR2基因c.1032G>A(p.Trp344Ter)杂合突变,最终明确患者的遗传缺陷类型,为临床提供诊断依据。也为患者家族中带有该突变尚未有临床症状的下一代提供诊断依据及治疗依据。
本发明的临床应用例证
利用本发明所提供的方法,对800名患有遗传性血管疾病但致病突变不明确的患者进行了基因检测。共诊断出451例患者带有致病基因突变。该方法对遗传性血管疾病检出的总阳性率达到56.38%,结合临床影像学检查,实验室检查及医生最终诊断结果,本方法的假阳性率为0,即所有经本方法确认的携带致病突变患者均符合相关遗传疾病的临床特征,并能够给予明确的临床诊断。本发明涉及的检测方法是利用高通量测序技术为突变快速筛选工具,以Sanger测序法为最终确定突变的金标准,因此具有快速,准确的特征。以高通量测序平均深度100×为例,所覆盖的90.21%的目标区域都能够被测序,且筛选得到的点突变能够被Sanger测序法验证,因此对以上区域检测的准确度为100%。根据800名受测患者的临床诊疗结果分析,受测患者未出现假阴性率。基于本发明涉及的检测方法给出的诊断报告得到临床医生的认可和采纳。本发明涉及的检测方法具有准确,快速,低成本的特点,对遗传性血管疾病的鉴别诊断有着重要意义和实用价值。
实施例2:
本发明中引物池里包含发明者新发现的遗传性血管疾病致病基因103个,如上文表1所示。新发现的103个遗传性血管疾病致病基因来自于发明者多年来的研究积累和家系调查。发明者首先在已知的遗传性血管疾病致病基因中通过KEGG信号通路检索,同源基因库,寻找已知致病基因的同源基因及相同致病通路上的关键基因。然后在多年积累的中国黄色人种病人大样本量病例样本库中对候选的致病基因进行靶向高通量测序,并进行生物信息学分析,筛选和寻找致病突变。对筛选到致病突变的病例进行随访和进一步的家系分析,对患者的整个家族进行致病位点测序验证,计算致病突变的共分离系数。当发现候选基因的致病突变在两个及以上无关联的家系中完全共分离时,即可初步判断该候选致病基因为新的致病基因。本发明发现,上述103个基因的致病突变在两个及以上无关联的家系中均出现完全共分离。
- 还没有人留言评论。精彩留言会获得点赞!