抵抗饮食诱导肥胖的猪R型载脂蛋白基因及猪R型载脂蛋白的制作方法
本发明属于生物技术领域,特别是一种抵抗饮食诱导肥胖的猪r型载脂蛋白基因及猪r型载脂蛋白。
背景技术:
猪r型载脂蛋白(apor)在ncbi核酸数据库中有确定的序列信息和相关的功能描述。现在还没有发现关于猪r型载脂蛋白(apor)与ncbi核酸数据库中不一样的的序列信息和用于抵抗饮食诱导肥胖的效果。
技术实现要素:
本发明针对上述问题,提出一种抵抗饮食诱导肥胖的猪r型载脂蛋白基因及猪r型载脂蛋白。
本发明的技术方案是:
本发明所述的抵抗饮食诱导肥胖的猪r型载脂蛋白基因,其特征在于所述的基因由seqidno1所示的核苷酸序列组成的多核苷酸。
所述的cdna全长696bp,编码202个氨基酸,从猪脂肪组织cdna克隆得到,在5’调控区与ncbi序列比较缺少三个碱基。
本发明所述的抵抗饮食诱导肥胖的猪r型载脂蛋白,特征在于所述的猪r型载脂蛋白seqidno2所示的氨基酸序列组成的蛋白。
所述的猪r型载脂蛋白基因抵抗饮食诱导肥胖的用途通过以下试验获得:
a.、利用体外培养细胞发现,猪r型载脂蛋白(apor)基因具有促进甘油三酯分解作用:将seqidno1所示的核苷酸序列(编码区序列)克隆至表达载体pcr3.1,向3t3-l1细胞转染并发现其在脂肪细胞内高表达,可以显著减少甘油三酯的积累,但不影响脂肪细胞分化。
b、转基因小鼠的构建与分析
1).转基因小鼠的制备:
构建脂肪组织特异性表达载体pcrii-fabp4-apor-beta-globin,包含脂肪组织特异性启动子fabp4,apor编码区和稳定序列beta-globin。两端使用kpni和xholi酶切,总长度9.6kb,选用c57bl/6小鼠,构建转基因小鼠,任务包括载体线性化、dna片段纯化和显微注射。
2)转基因小鼠鉴定:设计引物(p1&p2)用于pcr筛选阳性转基因小鼠(图1内p1和p2),提取鼠尾dna,以线性化载体作为阳性对照,野生型小鼠dna作为阴性对照,筛选获得转基因阳性小鼠3只,其中两只雄性(found3andfounder19),一只雌性。found3与野生型雌鼠交配获得分别获得f1小鼠19只(1-19),通过pcr进行阳性小鼠筛选得到5只阳性小鼠(1雄f113);found19与野生型雌鼠交配获得分别获得f1小鼠24只(1#-24#),通过pcr进行阳性小鼠筛选得到6只阳性小鼠(2雄,f16#和f18#)。
3)转基因小鼠基因组内apor的整合情况分析
选用xbali和puvii消化鼠尾基因组dna,p32标记探针,对founder和f1的雄性小鼠进行southern鉴定,选用同窝阴性雄鼠作为对照,结果表明,southern鉴定的结果,与pcr筛选结果完全吻合。并且所有转基因小鼠均为多拷贝整合,其中founder3及其后代阳性鼠的转基因拷贝数高于founder19及其后代。
4)转基因小鼠分析
1)转基因阳性(tg)小鼠的健康状况观察
对tg小鼠采食、饮水、排泄、交配及日常活动进行观察,与野生型小鼠相比未见差异。
(2)外源基因稳定遗传能力分析
利用两只雄性founder小鼠扩繁获得f1,f2和f3代小鼠。在f1和f2代中,阳性小鼠比例低于50%,但f3代中,阳性小鼠比例50%左右,推断可能由于f1和f2代小鼠数量少,导致阳性率受偶然性影响较大。基于现有数据,可以肯定apor具备稳定遗传能力,且与性别无关。
呈现表达,在骨髓有极微弱表达。该对引物在野生型小鼠任何组织中都无扩增产物,所以本研究结果不存在内源性干扰。
real-timepcr对各组织表达谱分析结果与rt-pcr一致,对比了apor在found3和founder19极其各自后代皮下脂肪中表达量,差异不显著。所以两个founder的后代都用于后继分析,每项分析均选用同一窝的阴性小鼠作为对照组。
由于未能拿到apor高质量抗体,所以未对蛋白水平进行检测。
本发明的的测定效果如下:
通过本发明的方法,发现通过转基因(tg)和野生型(wt)小鼠对比分析,apor对脂肪沉积的影响如下:
(1)低脂饲喂(脂肪含量10%左右),分析tg与wt小鼠脂肪沉积情况:4月龄小鼠(n=10),饲喂两个月,分析生长速度、胴体组成、体脂比例和血糖、血脂代谢情况,发现转基因(tg)与野生型(wt)小鼠无显著差异。
(2)高脂饲喂实验发现apor具有抵抗饮食诱导肥胖的作用:选用4月龄小鼠进行高脂饲喂(饲料脂肪含量45%左右),至6月龄宰杀小鼠,进行分析,转基因(tg)小鼠的体重显著低于野生型(wt),表现出明显的抗饮食诱导肥胖的能力。对体脂组成和糖脂代谢等指标分析,wt小鼠表现出高血脂症,而tg小鼠无异常。对上述tg和wt小鼠皮下脂肪进行切片分析,发现tg小鼠脂肪细胞显著小于wt小鼠,利用real-timepcr对与脂类代谢密切相关基因表达丰度分析发现,apor对c/ebpa、pparr、fabp4、adipoq、lgals12以及hsl的表达量都没有影响,推断apor在这些基因的下游。基于以上数据,初步判断apor具有抵抗饮食诱导型肥胖的功能。
(3)tg与wt原代培养脂肪细胞积累甘油三酯情况分析:建立tg与wt小鼠的脂肪细胞原代培养,首先对比在激素诱导下两种来源细胞的体外分化能力,未见差异。对比分化后的脂肪细胞内甘油三酯含量,油红o染色发现tg来源脂肪细胞内含量显著低于wt细胞;rt-pcr分析发现,tg小鼠脂肪原代细胞内apor呈现高表达,而wt来源脂肪原代细胞内apor未检测到表达;利用甘油三酯定量分析试剂盒(biovision)定量分析两种来源细胞内甘油三酯含量,结果印证了与油红o染色结果,tg胞内甘油三酯含量约为wt胞内1/3;最后,使用clb刺激两种来源的脂肪细胞(加入带有100um的clb刺激,24小时后收获细胞),定量分析表明,clb刺激对tg来源脂肪细胞积累甘油三酯情况影响不显著,而可以显著减少wt来源的脂肪细胞内甘油三酯的含量。
本发明通过构建脂肪组织特异性过表达猪源apor的转基因小鼠,外源基因仅在皮下和内脏脂肪中表达,通过对转基因小鼠分析发现:
1.apor可以稳定遗传,并且未见对转基因小鼠健康有任何影响;
2.在低脂饮食下,apor未见对转基因小鼠体重、体脂组成有任何影响;
3.在高脂饮食下,转基因小鼠体重、体脂显著低于野生型小鼠;
4.在高脂饮食下,转基因小鼠脂肪组织切片分析发现,脂肪细胞体积显著小于野生型,但与脂类代谢相关的基因c/ebpa、pparr、fabp4、adipoq、lgals12以及hsl表达量均为发生变化;
5.分离得到转基因小鼠的脂肪细胞原代培养,发现其积累甘油三酯能力显著小于从野生型小鼠分离得到的脂肪细胞;
6.对比分离得到的两种来源的脂肪细胞原代细胞培养物,发现转基因小鼠来源的脂肪细胞对盐酸克伦特罗刺激不敏感,而野生型小鼠来源的脂肪细胞对盐酸克伦特罗刺激敏感,甘油三酯积累量显著降低。
基于以上发现,推断猪apor在盐酸克伦特罗减少猪脂肪沉积过程中,位于通路下游,发挥关键性作用。在脂肪组织中过表达apor的转基因小鼠具有抵抗饮食诱导型肥胖的作用,并且安全、易进行转基因操作。
附图说明
图1为本发明过表达apor可减少3t3-l1胞内甘油三酯积累图。
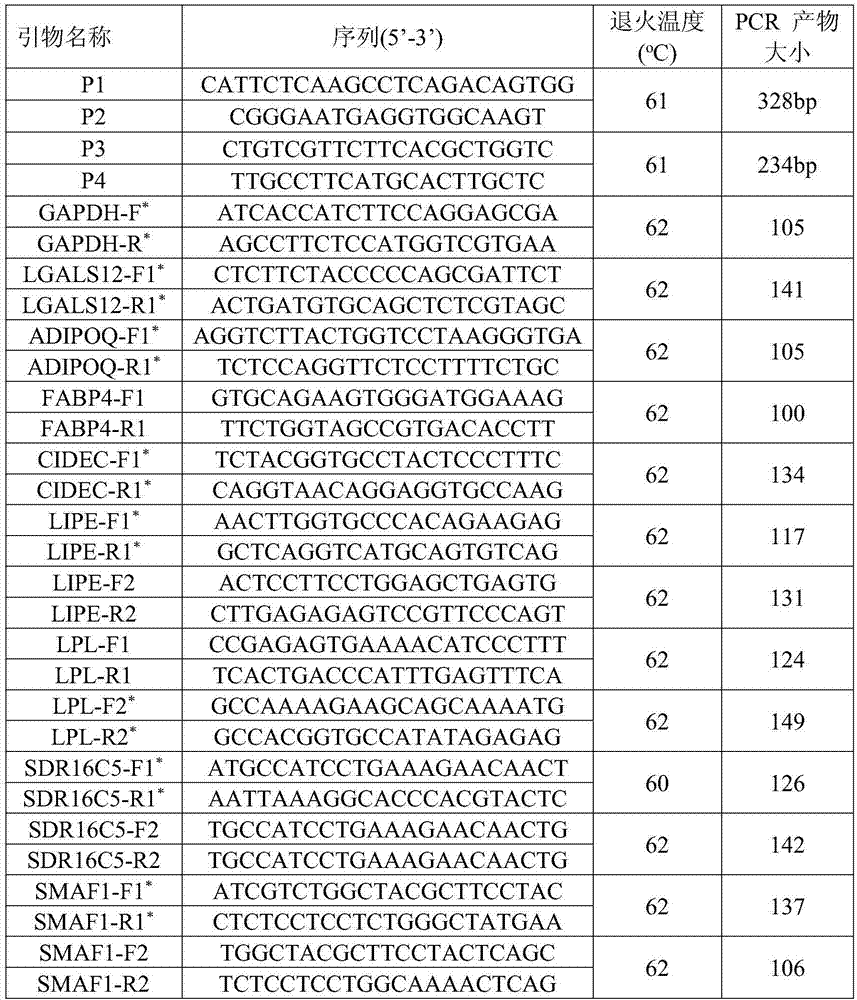
图2为设计引物(p1&p2)用于pcr筛选阳性转基因小鼠表。
图3为外源apor遗传情况分析表。
说明:fabp4promoter:脂肪酸结合蛋白4的启动子
aporcodingsequence:r型载脂蛋白编码区序列
betaglobinsequence:β球蛋白序列
具体实施方式
现结合附图和具体实施例对本发明作进一步的说明。
本发明所述的本发明所述的抵抗饮食诱导肥胖的猪r型载脂蛋白基因,其特征在于所述的基因由seqidno1所示的核苷酸序列组成的多核苷酸。
所述的cdna全长609bp,编码202个氨基酸,在5’调控区与ncbi序列比较缺少三个碱基。
本发明所述的抵抗饮食诱导肥胖的猪r型载脂蛋白,特征在于所述的猪r型载脂蛋白seqidno2所示的氨基酸序列组成的蛋白。
所述的猪r型载脂蛋白基因抵抗饮食诱导肥胖的用途通过以下试验获得:
a.、利用体外培养细胞发现,猪r型载脂蛋白(apor)基因具有促进甘油三酯分解作用:将seqidno1所示的核苷酸序列(编码区序列)克隆至表达载体pcr3.1,向3t3-l1细胞转染并发现其在脂肪细胞内高表达,可以显著减少甘油三酯的积累,但不影响脂肪细胞分化。
b、转基因小鼠的构建与分析
1).转基因小鼠的制备:
构建脂肪组织特异性表达载体pcrii-fabp4-apor-beta-globin,包含脂肪组织特异性启动子fabp4,apor编码区和稳定序列beta-globin。两端使用kpni和xholi酶切,总长度9.6kb,选用c57bl/6小鼠,构建转基因小鼠,任务包括载体线性化、dna片段纯化和显微注射。
2)转基因小鼠鉴定:设计引物(p1&p2)用于pcr筛选阳性转基因小鼠(图1内p1和p2),提取鼠尾dna,以线性化载体作为阳性对照,野生型小鼠dna作为阴性对照,筛选获得转基因阳性小鼠3只,其中两只雄性(found3andfounder19),一只雌性。found3与野生型雌鼠交配获得分别获得f1小鼠19只(1-19),通过pcr进行阳性小鼠筛选得到5只阳性小鼠(1雄f113);found19与野生型雌鼠交配获得分别获得f1小鼠24只(1#-24#),通过pcr进行阳性小鼠筛选得到6只阳性小鼠(2雄,f16#和f18#)。
3)转基因小鼠基因组内apor的整合情况分析
选用xbali和puvii消化鼠尾基因组dna,p32标记探针,对founder和f1的雄性小鼠进行southern鉴定,选用同窝阴性雄鼠作为对照,结果表明,southern鉴定的结果,与pcr筛选结果完全吻合。并且所有转基因小鼠均为多拷贝整合,其中founder3及其后代阳性鼠的转基因拷贝数高于founder19及其后代。
4)转基因小鼠分析
1)转基因阳性(tg)小鼠的健康状况观察
对tg小鼠采食、饮水、排泄、交配及日常活动进行观察,与野生型小鼠相比未见差异。
(2)外源基因稳定遗传能力分析
利用两只雄性founder小鼠扩繁获得f1,f2和f3代小鼠。在f1和f2代中,阳性小鼠比例低于50%,但f3代中,阳性小鼠比例50%左右,推断可能由于f1和f2代小鼠数量少,导致阳性率受偶然性影响较大。基于现有数据,可以肯定apor具备稳定遗传能力,且与性别无关。
呈现表达,在骨髓有极微弱表达。该对引物在野生型小鼠任何组织中都无扩增产物,所以本研究结果不存在内源性干扰。
real-timepcr对各组织表达谱分析结果与rt-pcr一致,对比了apor在found3和founder19极其各自后代皮下脂肪中表达量,差异不显著。所以两个founder的后代都用于后继分析,每项分析均选用同一窝的阴性小鼠作为对照组。
由于未能拿到apor高质量抗体,所以未对蛋白水平进行检测。
本发的测定发明的的测定效果如下:
通过本发明的方法,发现通过转基因(tg)和野生型(wt)小鼠对比分析,apor对脂肪沉积的影响如下:
(1)低脂饲喂(脂肪含量10%左右),分析tg与wt小鼠脂肪沉积情况:4月龄小鼠(n=10),饲喂两个月,分析生长速度、胴体组成、体脂比例和血糖、血脂代谢情况,发现转基因(tg)与野生型(wt)小鼠无显著差异。
(2)高脂饲喂实验发现apor具有抵抗饮食诱导肥胖的作用:选用4月龄小鼠进行高脂饲喂(饲料脂肪含量45%左右),至6月龄宰杀小鼠,进行分析,转基因(tg)小鼠的体重显著低于野生型(wt),表现出明显的抗饮食诱导肥胖的能力。对体脂组成和糖脂代谢等指标分析,wt小鼠表现出高血脂症,而tg小鼠无异常。对上述tg和wt小鼠皮下脂肪进行切片分析,发现tg小鼠脂肪细胞显著小于wt小鼠,利用real-timepcr对与脂类代谢密切相关基因表达丰度分析发现,apor对c/ebpa、pparr、fabp4、adipoq、lgals12以及hsl的表达量都没有影响,推断apor在这些基因的下游。基于以上数据,初步判断apor具有抵抗饮食诱导型肥胖的功能。
(3)tg与wt原代培养脂肪细胞积累甘油三酯情况分析:建立tg与wt小鼠的脂肪细胞原代培养,首先对比在激素诱导下两种来源细胞的体外分化能力,未见差异。对比分化后的脂肪细胞内甘油三酯含量,油红o染色发现tg来源脂肪细胞内含量显著低于wt细胞;rt-pcr分析发现,tg小鼠脂肪原代细胞内apor呈现高表达,而wt来源脂肪原代细胞内apor未检测到表达;利用甘油三酯定量分析试剂盒(biovision)定量分析两种来源细胞内甘油三酯含量,结果印证了与油红o染色结果,tg胞内甘油三酯含量约为wt胞内1/3;最后,使用clb刺激两种来源的脂肪细胞(加入带有100um的clb刺激,24小时后收获细胞),定量分析表明,clb刺激对tg来源脂肪细胞积累甘油三酯情况影响不显著,而可以显著减少wt来源的脂肪细胞内甘油三酯的含量。
本发明通过构建脂肪组织特异性过表达猪源apor的转基因小鼠,外源基因仅在皮下和内脏脂肪中表达,通过对转基因小鼠分析发现:
apor可以稳定遗传,并且未见对转基因小鼠健康有任何影响;
在低脂饮食下,apor未见对转基因小鼠体重、体脂组成有任何影响;
在高脂饮食下,转基因小鼠体重、体脂显著低于野生型小鼠;
在高脂饮食下,转基因小鼠脂肪组织切片分析发现,脂肪细胞体积显著小于野生型,但与脂类代谢相关的基因c/ebpa、pparr、fabp4、adipoq、lgals12以及hsl表达量均为发生变化;
分离得到转基因小鼠的脂肪细胞原代培养,发现其积累甘油三酯能力显著小于从野生型小鼠分离得到的脂肪细胞;
对比分离得到的两种来源的脂肪细胞原代细胞培养物,发现转基因小鼠来源的脂肪细胞对盐酸克伦特罗刺激不敏感,而野生型小鼠来源的脂肪细胞对盐酸克伦特罗刺激敏感,甘油三酯积累量显著降低。
基于以上发现,推断猪apor在盐酸克伦特罗减少猪脂肪沉积过程中,位于通路下游,发挥关键性作用。在脂肪组织中过表达apor的转基因小鼠具有抵抗饮食诱导型肥胖的作用,并且安全、易进行转基因操作。
sequencelisting
<110>嘉兴学院
<120>猪r型载脂蛋白基因及其蛋白质
<130>
<160>2
<170>patentinversion3.3
<210>1
<211>609
<212>dna
<213>unknown
<220>
<223>人工序列
<400>1
atgcctcccaatttacagagaattttcccagcactgtgcctccttggggtcctgtttctc60
ctgcactgcacacctgtcctgtgtggttgcgataatcctcctgtggttgcccatggacat120
catacacaaattattgggctatttggaatgaaaaaagatgaggttgtatataaatgtgat180
gaaggatacactctggttggagaggacagactctcctgtcgttcttcacgctggtcacct240
gcagcccctcaatgtaaagctttgtgtccgaaaccacagatagatcgtggaaagttatct300
gtggatcaggatgaatatattgagtctgaaaacgtcattgtccagtgtggctctggctat360
ggtttggttggtcccaaaattatcacttgcacagaagacggaacctggcacccacgggtg420
cccaagtgtgaatgggagtaccccgaagactgtgagcaagtgcatgaaggcaaaaaactc480
atgcagtgtctcccaaacctggaggagataaaattggccctggagctgtataagctgtcc540
ctggagactaaactactggagcttcagatagataaggaaaagaaagccaaagcgaagtac600
tcaatatag609
<210>2
<211>202
<212>prt
<213>unknown
<220>
<223>人工序列
<220>
<221>misc_feature
<222>(192)..(192)
<223>xaacanbeanynaturallyoccurringaminoacid
<400>2
metproproasnleuglnargilepheproalaleucysleuleugly
151015
valleupheleuleuhiscysthrprovalleucysglycysaspasn
202530
proprovalvalalahisglyhishisthrglnileileglyleuphe
354045
glymetlyslysaspgluvalvaltyrlyscysaspgluglytyrthr
505560
leuvalglygluaspargleusercysargserserargtrpserpro
65707580
alaalaproglncyslysalaleucysprolysproglnileasparg
859095
glylysleuservalaspglnaspglutyrileglusergluasnval
100105110
ilevalglncysglyserglytyrglyleuvalglyprolysileile
115120125
thrcysthrgluaspglythrtrphisproargvalprolyscysglu
130135140
trpglutyrprogluaspaspgluglnvalhisgluglylyslysleu
145150155160
metglncysleuproasnleuglugluilelysleualaleugluleu
165170175
tyrlysleuserleugluthrlysleuleugluleuglnileaspxaa
180185190
glulyslysalalysalalystyrserile
195200
- 还没有人留言评论。精彩留言会获得点赞!