一种提取洋葱多糖粗提物工艺的制作方法
本发明涉及食品加工领域,具体是一种提取洋葱多糖粗提物工艺。
背景技术:
洋葱多糖作为一种活性物质,具有很高的经济价值,多糖的提取是实现其利用的前提,洋葱多糖是一种水溶性的物质,不溶于乙醇、乙醚、石油醚等有机溶剂,因此本发明洋葱多糖的提取利用“水提醇沉”法。水提法是所有辅助提取方法的基础,通过对水提法提取洋葱多糖工艺进行研究,进一步优化基本提取方法的工艺条件,以前对水提法的影响因素多集中于水提温度、料液比、提取时间及PH,而忽略了洋葱粒径大小、乙醇含量对多糖提取率的影响,这两个因素对多糖的纯度也有很大的影响,洋葱中的多糖与其它大部分植物多糖类似,是由多个单糖通过α-糖苷键连接聚合而成的大分子多聚物,其生物活性与纯度也有一定的关系,对于纯度要求较高的粗多糖产品,这是两个必须考虑和优化的因素。
技术实现要素:
本发明针对现有技术的不足,提供一种提取洋葱多糖粗提物工艺。
本发明技术方案具体包括:
①将新鲜洋葱切片,在60~70℃条件下恒温鼓风干燥箱干燥后粉碎,过筛即制得洋葱干粉,低温密闭干燥保存,待用;
②将洋葱干粉与无水乙醇按照1:8~12的重量份之比混合均匀,在70~75℃水浴环境下回流脱脂1.5~2h,共脱脂两次,抽滤并收集滤渣;
③将按照重量份之比为滤渣:水=1:30~60的比例将滤渣和水混合均匀,置于70~85℃恒温水浴锅中加热回流提取3~6h后过滤,将滤渣反复提取3次,合并滤液后浓缩得到浓缩液,浓缩液用体积分数为85~90%的乙醇醇析,在4~5℃环境中静置,然后离心,再将离心得到的沉淀物干燥至恒重,即得洋葱多糖粗提物。
与现有技术相比较,本发明具备的有益效果:
洋葱多糖用作可食性膜的成分之一,主要是利用其抗氧化功能,能在防止鲜切果蔬褐变方面发挥至关重要的作用。在明胶可食性膜中添加洋葱多糖,复合之后的膜在机械性能、水溶性、阻隔性、抗氧化性上都将有明显的提升,其在食品保鲜包装膜方面的潜在应用价值明显,可用于果蔬表面的抗氧化防护、保水等。
附图说明
图1葡萄糖标准曲线。
图2粒径对洋葱多糖提取的影响。
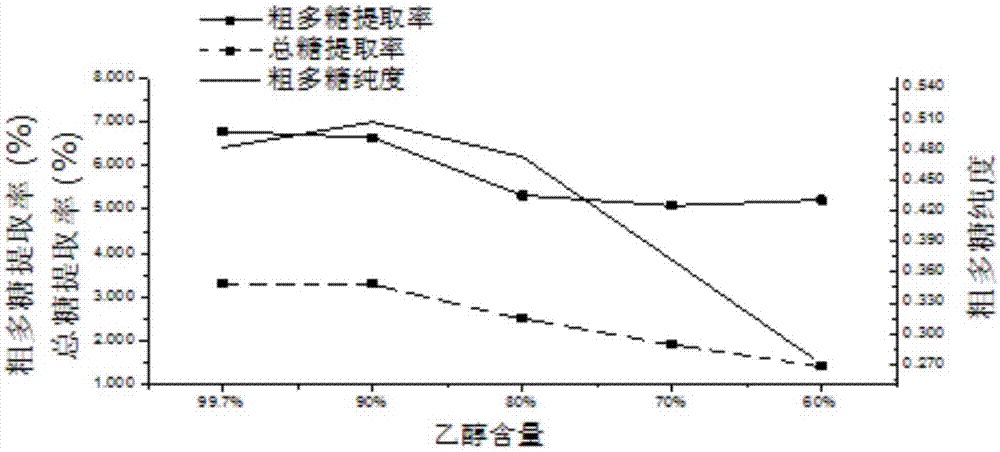
图3乙醇含量对洋葱多糖提取的影响。
图4料液比对洋葱多糖提取的影响。
具体实施方式
以下对本申请的优选实施例进行说明,应当理解,此处所描述的优选实施例仅用于说明和解释本申请,并不用于限定本申请。
实施例1:
2.3.1实验流程
洋葱切片→70℃干燥→粉碎过筛(低温干燥保藏)→醇析→抽滤残渣→加水溶解→热水浸提3次→合并滤液浓缩→无水乙醇密封、静置过夜→离心→干燥至恒重
2.3.2操作步骤
①将新鲜洋葱切片,在70℃条件下恒温鼓风干燥箱干燥后粉碎,过筛即制得洋葱干粉,低温密闭干燥保存,待用。
②将取洋葱干粉10g溶解,倒入500ml容量瓶中,加入10倍质量的分析纯乙醇,在75℃水浴环境下回流脱脂2h,共脱脂两次,抽滤、收集滤渣。
③将滤渣加入少量的蒸馏水溶解,溶液转移至烧瓶中,用蒸馏水多次清洗,使烧瓶中固液比为1:40,置于80℃恒温水浴锅中加热回流提取4h后,滤纸过滤,将滤渣反复提取3次,合并滤液,用旋转蒸发仪浓缩至约100ml,加入4倍体积无水乙醇醇析,静置于冰箱中(4~5摄氏度)过夜,离心,沉淀物干燥至恒重,即得洋葱多糖粗提物。
2.3.3多糖含量的测定
多糖得率是以总糖含量作为指标,多糖含量的分析测定以葡萄糖作为标准品,采用苯酚-硫酸法进行分析测定。
标准曲线制备:将标准葡萄糖105℃下干燥至恒重,称取50.0mg于500ml容量瓶中,加水定容至刻度,配得0.1000mg/ml的葡萄糖标准溶液。分别吸取0.4、0.6、0.8、1.0、1.2、1.4、1.6、1.8ml葡萄糖标准溶液于具塞试管中,各以去离子水补至2.0ml,加入5%苯酚溶液1.0ml,浓硫酸5.0ml,放置冷却至室温,放到40℃水浴环境中静置10min,取出摇匀后在室温环境下放置20min,摇匀后于490nm测定溶液吸光值。以2.0ml水代替溶液做空白对照,以吸光值A为纵坐标,葡萄糖浓度c(mg/ml)为横坐标做标准曲线。
洋葱多糖含量分析:先将洋葱粗多糖干燥至恒重,然后称取样品适量,按制备标准曲线方法测产品吸光度。根据标准曲线计算样品中粗多糖的含量,计算洋葱多糖得率。
洋葱粗多糖纯度:
粗多糖提取率:
总糖含量:
W=TE (公式2-3)
式中:E-洋葱粗多糖纯度;c-由标曲算出的样液的浓度(mg/ml);n-稀释倍数;v-样品测定溶液体积(ml);m-配制样液的粗多糖质量(mg);T-粗多糖提取率(%);m1-提取的洋葱粗多糖质量(g);m2-洋葱干粉的质量(g);W-总糖含量(%)。
2.3.4提取工艺条件对洋葱多糖提取率的影响
2.3.4.1洋葱粉颗粒
按2.3.2的方法,其他条件不变,洋葱粉分别过40、80、100、120、160目筛,测定不同颗粒大小的洋葱多糖提取率,分析洋葱粉颗粒大小对洋葱多糖提取率大小的影响。假定最佳粒度为U。
2.3.4.2醇沉阶段乙醇体积分数
按2.3.2的方法,其他条件不变,洋葱粉颗粒大小为U,乙醇含量分别为分析纯(99.7%)、95%、90%、85%、80%,测定不同条件下洋葱多糖提取率,分析醇沉阶段乙醇体积分数对洋葱多糖提取率大小的影响,假定最佳乙醇浓度为V。
2.3.4.3料液比
按2.3.2的方法,其他条件不变,洋葱粉颗粒大小为U,乙醇浓度为V,水提时的料液比分别为1:20、1:30、1:40、1:50、1:60,测定不同条件下洋葱多糖提取率,分析料液比对洋葱多糖提取率大小的影响,假定最佳料液比为W。
2.3.4.4提取温度
按2.3.2的方法,其他条件不变,洋葱粉颗粒大小为U,乙醇浓度为V,水提时的固液比为W,水提温度分别为50、60、70、80、90℃,测定不同条件下洋葱多糖提取率,分析提取温度对洋葱多糖提取率大小的影响,假定最佳提取温度为H。
2.3.5提取工艺条件的优化
依据单因素实验结果设计正交试验,以确定洋葱多糖提取的最佳条件,选择颗粒大小、乙醇含量、固液比、提取温度四个因素,各取三个较优水平,以总糖得率为衡量指标,采用L9(33)正交试验设计表布置试验,以确定洋葱多糖提取的最佳条件。
2.4.1标准曲线的建立
以溶液吸光度为纵坐标,葡萄糖浓度为横坐标,绘制标准曲线如图1,通过分析得到标准曲线的线性回归方程为A=44.031c+0.0105,R2=0.9928。
2.4.2洋葱粉颗粒大小对粗多糖提取的影响
粒径的大小会影响到速率,颗粒太大会影响洋葱组织的破裂,阻碍醇溶性物质和多糖的浸出,在相同的回流时间内,多糖浸出量降低,纯度降低;颗粒太小,也会由于毛细管作用不易使多糖从组织分离。本实验设计了不同的粒径梯度,考察粒径大小对粗多糖提取率、粗多糖纯度、总糖提取率的影响,实验结果如图2所示。
从图2可以看出,随着粒径的减小粗多糖提取率逐渐升高,这是由于颗粒越小在回流过程中水溶性物质更容易溶解出来;40目到100目粗多糖的纯度随粒径的减小而升高,这是由于粒径的减小使醇溶性物质更容易溶出,多糖也更容易在回流过程中溢出破裂细胞溶于水中,随着粒径的进一步减小,粗多糖纯度会有所降低,可能是由非糖的水溶性物质溶解以及多糖的毛细管作用造成的;总糖提取率的总体趋势是先随着粒径的减小,回流过程中组织更容易破碎,从而总糖提取率不断提高,粒径小到一定程度,组织基本破碎完全,总糖提取率趋于平稳,无显著差异(α=0.05)。
2.4.3醇沉阶段乙醇体积分数对粗多糖提取的影响
乙醇主要用于水提前的脱脂,乙醇含量越高对脱脂是越有利的,但相关文献也表明适当降低乙醇含量有利于非糖水溶性物质的溶出,对提高粗多糖的纯度有一定的作用。本实验设计了不同的乙醇用量梯度,考察乙醇用量对粗多糖提取率、粗多糖纯度、总糖提取率的影响,实验结果如图3所示。
从图3可以看出,当乙醇含量大于70%时,由于部分多糖溶于水中,粗多糖提取率随乙醇浓度的降低而减小,乙醇含量60%时,粗多糖提取率升高,可能由于大量醇溶性物质残留,导致粗多糖的纯度显著下降;图中可以看出,乙醇含量90%时,粗多糖纯度和总糖含量最高,分别为0.483和3.08%,可能的原因是少量的水有利于其他非糖水溶性物质的溶解,使糖的纯度略有升高,继续降低乙醇的含量,就会使多糖的溶解量增加、醇溶性物质的溶解度降低,从而纯度下降。
2.4.4料液比对粗多糖提取的影响
蒸馏水是多糖的溶剂,在回流提取过程中多糖不断的浸出组织溶于水中,若用水量过低浸出的多糖不能完全溶于水中,用水量太大则会给回流和后期的浓缩带来诸多不便,适量的料液比对充分提取多糖和实验的简洁性具有十分重要的意义,本实验设计了不同的料液比梯度,考察料液比对粗多糖提取率、粗多糖纯度、总糖提取率的影响,实验结果如图4所示。
从图4可以看出,当料液比>1/30时,粗多糖提取率、总糖提取率随料液比的减小而增大,而粗多糖纯度降低,当料液比在1/30-1/60之间时,总糖提取率没有显著变化,无明显差异(α=0.05)。这是因为当料液比>1/30时多糖达到饱和状态,增加水量有利于多糖的浸出,而料液比<1/30时,多糖已全部溶于水中,继续增加水量对总糖提取率影响不大。
2.4.5提取温度对粗多糖提取的影响
适当的提高回流温度有利于组织细胞的破碎,温度过高不仅经济型差,也会对多糖的稳定性产生影响,本实验通过对不同提取温度下粗多糖提取率、粗多糖纯度、总糖提取率的分析,确定提取的最适温度。
可以看出,粗多糖提取率随温度的升高而增大,这是因为高温有利于组织破碎,水溶性物质的浸出,相应的溶解度也会升高;粗多糖纯度和总糖提取率都是在70℃时达到极值,分别为0.5656和3.5135,温度低于70℃时,多糖纯度变化较小,无显著差异(α=0.05),温度大于70℃,多糖纯度显著降低,这是因为部分多糖由于热不稳定性发生分解以及非糖水溶性物质的溶出,从而也使总糖的提取率降低。
最后应说明的是:以上仅为本申请的优选实施例而已,并不用于限制本申请,尽管参照实施例对本申请进行了详细的说明,对于本领域的技术人员来说,其依然可以对前述各实施例所记载的技术方案进行修改,或者对其中部分技术特征进行等同替换,但是凡在本申请的精神和原则之内,所作的任何修改、等同替换、改进等,均应包含在本申请的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!