一种高价银抗菌剂及其制备方法与流程
本发明属于精细化工领域,具体涉及高价银抗菌剂的制备方法。
背景技术:
自然界中的有害细菌和真菌是人类社会的主要传染病病原体之一,曾经肆虐的黑死病,猩红热,炭疽等,到目前的食物中毒,细菌性皮肤病和肺炎等都是由鼠疫杆菌,链球菌,炭疽杆菌,大肠杆菌,葡萄球菌,肺炎球菌等致病菌引起的。
古时以来人们应用银器来来防止腐败。现代研究发现,银及银离子抗菌作用机理如下:一方面,银与蛋白质和酶的S-H作用,影响细胞的正常生理活动;再者,银离子通过库仑力吸附在细胞膜表面,释放细胞膜上的钾离子,破坏电子传输系统和物质输送,破坏细胞膜,使细胞破裂凋亡;银离子通过光催化作用产生过氧自由基(O2-),氢过氧自由基(HO2·)和过氧化氢(H2O2),抑制细菌生长,并且杀死细菌细胞。由于以上银抗菌剂的抗菌机理,使得银系抗菌剂成为应对烧伤、烫伤等大面积表皮损伤的引发的全身或部分微生物感染的优选药物之一。
由于银对细胞的杀灭没有靶向性,这就使得银抗菌剂存在一定毒性。为降低银抗菌剂的毒性,提高银系抗菌剂的光稳定性,同时减少银的用量,降低成本,载银抗菌剂的研发迅速发展。例如,A new concept for the treatment of atopic dermatitis: Silver–nanolipid complex (sNLC)合成Ag+ 与混合脂质的络合物,对过敏性皮炎有较好疗效,且副作用低。Ag/silk fibroin nanofibers: Effect of fibroin morphology on Ag+release and antibacterial activity中通过静电纺丝的方法,合成Ag/丝纤蛋白纳米纤维,实现Ag+ 的缓释。
研究发现,高价银的抗菌性能远高于低价银与纳米银粒子,Ag3+的抗菌性能是Ag+的200倍,Ag2+的抗菌性能是Ag+的60倍。但是高价银不稳定,尤其是Ag3+的稳定性更差。如美国专利No.20070042052公开了一种含Ag2+ 的抗菌剂,但这种含Ag2+的抗菌剂仅在浓酸环境下稳定存在,因此保存运输极为困难。能与Ag3+络合的配体极为有限,目前只有咔咯,卟啉,亚胺基肟,双胍可以与Ag3+配合,但是咔咯,卟啉,亚胺基肟与Ag3+所形成的络合物光稳定性较差,且在水中会分解。专利201080046629.X在水/AOT/ 庚烷中合成了银-氯己定配合物,但由于氯己定只能溶解在酸性环境中,在制备过程中需要消耗一定量的酸与中和剂。
聚六亚甲基双胍(PHMB)作为阳离子表面活性剂,可直接溶解在水中,其抗菌性能高于小分子量的胍,在人体创伤口依然保持高抗菌活性;能与抗生素协同抗菌;且细胞和组织毒性更低;自然条件下可以降解,对环境的危害更小。作为Ag3+的配体,在稳定Ag3+,降低其细胞毒性的同时,可与Ag3+起到协同抗菌的作用。
因此本发明以不同粘均分子量的PHMB作为配体,合成一系列光热稳定性好、抗菌性能良好并且低细胞与组织毒性的的Ag()-PHMB配合物,应用与人体表皮创伤的处理、医疗器械表面处理、水处理等方面。
技术实现要素:
本发明的目的在于提供一种高抗菌活性的纳米级或微米级的Ag()-PHMB配合物的合成方法,并用于人体表皮创伤的处理、医疗器械表面处理、水处理、纺织等方面。
为实现上述目的,本发明所采用的技术方案为:
一种数均粒径在1-10 nm的纳米级Ag()-PHMB配合物,包括Ag3+和PHMB,Ag以+3价态稳定存在,AgNO3,PHMB单体和氧化剂的摩尔比为1:2-4:2-4,反应环境为反相微乳液,合成步骤如下:
(1)制备反相微乳液:将表面活性剂溶于庚烷中,搅拌至透明;
(2)向步骤(1)中的反相微乳液中加入聚六亚甲基双胍(PHMB)水溶液并搅拌至澄清;
(3)向步骤(2)中的混合液中加入AgNO3溶液并搅拌至澄清;
(4)向步骤(3)中的混合液中加入氧化剂,并加入NaOH调节PH值在9-11,搅拌反应18-24 h,加入乙醇破坏微乳液体系并离心,用乙醇和去离子水洗涤,干燥后得到纳米级Ag()-PHMB配合物。
步骤(1)制备反相微乳液中采用的表面活性剂为双(2-乙基己基)琥珀酸酯磺酸钠,乙撑基双(十二烷基二甲基)氯化铵,5,5'-二壬基-2,2'-(α,ω-亚烷基二氧基)二苯磺酸钠中的一种;微乳液的连续相为庚烷;在常温下表面活性剂与庚烷按质量比1:12-15混合均匀。
一种数均粒径在1-10μm的微米级ζ电位大于0的 Ag()-PHMB配合物,Ag以+3价稳定存在,AgNO3,PHMB单体和氧化剂的摩尔比为1:2-4:2-4,在水溶液中合成,步骤如下:
(1)稀释PHMB;
(2)在快速搅拌下,向稀释后的PHMB溶液中慢慢滴加AgNO3;
(3)向步骤(2)所得溶液加入氧化剂,并加入NaOH溶液调节PH值在11-12之间,搅拌反应直至有橙棕色沉淀生成,离心,用去离子水洗涤,干燥后得到微米级Ag()-PHMB配合物。
所述氧化剂为过硫酸铵,过硫酸钠,过硫酸钾等过硫酸化合物。
所述的PHMB分子量在2000-7000之间。
与现有银系抗菌剂相比,本发明合成的Ag()-PHMB有以下优势:
1) 在反相微乳液环境下合成的纳米级Ag()-PHMB配合物,具有纳米材料的量子尺寸效应、表面效应、小尺寸效应等优势,Ag()-PHMB配合物抗菌性能更强;通过琼脂孔洞法可知,配体PHMB分子量越高,Ag(III)-PHMB配合物抗菌性能越好;
2) 合成环境温和,特别是在水中的合成方法,常温下即可反应,对设备要求低,适合于大规模工业化生产;
3) 在同等质量浓度下,Ag()-PHMB配合物的抗菌性能不仅远高于磺胺嘧啶银,AgNO3,PHMB,也高于AgO;Ag(III)-PHMB配合物光,热稳定性好,能够发挥长效抗菌机制;
4) 所用的双(2-乙基己基)琥珀酸酯磺酸钠和双子表面活性剂在油水界面都会形成楔形结构,不需要额外添加助表面活性剂,所得微乳液热力学稳定性更高。
5) 所得纳米级Ag(III)-PHMB配合物吸附在棉布上后耐洗度很好,在20次标准洗涤循环后依然可以杀灭99.8%以上细菌和99.7%以上真菌。
附图说明
图1为PHMB的红外吸收光谱。
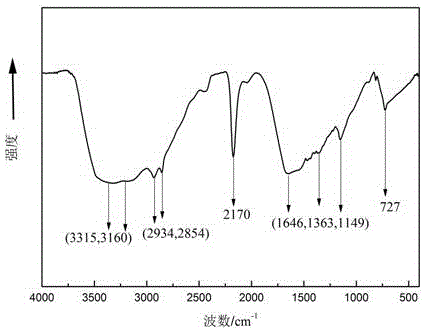
图2为Ag()-PHMB配合物的红外吸收光谱。
图3为实施例4的配合物中银元素的XPS能谱图。
具体实施方式
本发明进一步通过以下实施例进行详细说明,本发明并不限于这些实施方式。
实施例1 纳米级Ag()-PHMB配合物的合成
(1)反相微乳液的制备
取1.2 g双(2-乙基己基)琥珀酸酯磺酸钠(AOT),常温下溶解在18 g庚烷中并搅拌至透明状;
(2)向步骤(1)中加入255 μL水和256 μL 5 g/L的粘均分子量为2133的PHMB水溶液,在磁力搅拌下至澄清;
(3)向步骤(2)中加入0.04 mol/L的AgNO3 73 μL并搅拌至澄清无色;
(4)向步骤(3)中加入0.04 mol/L的Na2S2O8 146 μL,滴加PH=14的NaOH溶液调节PH在9-11之间并搅拌22 h至反相微乳液变为浅橙棕色。加入少量乙醇离心,用乙醇和去离子水洗涤,干燥后得到纳米级Ag()-PHMB配合物。
实施例2纳米级Ag()-PHMB配合物的合成
(1)反相微乳液的制备
取乙撑基双(十二烷基二甲基)氯化铵(阳离子型双子表面活性剂)1.4 g溶解于18 g庚烷中并搅拌至透明。
(2)向步骤(1)中加入380 μL 5 g/L 粘均分子量为3245的PHMB水溶液,在磁力搅拌下至澄清。
(3)向步骤(2)中加入0.04 mol/L的AgNO3 73 μL并搅拌至澄清无色。
(4)向步骤(3)中加入0.04 mol/L的K2S2O8 220 μL,滴加PH=14的NaOH溶液调节PH在9-11之间,搅拌18 h至反相微乳液变为浅橙棕色。加入少量乙醇离心,用乙醇和去离子水洗涤,干燥后得到纳米级Ag()-PHMB配合物。
实施例3 纳米级Ag()-PHMB配合物的合成
(1)反相微乳液的制备
取5,5’-二壬基-2,2’-(α,ω-亚烷基二氧基)二苯磺酸钠(阴离子型双子表面活性剂)1.5 g溶解于18 g庚烷中中并搅拌至透明。
(2)向步骤(1)中加入510μL 10 g/L 粘均分子量为5248的PHMB水溶液并搅拌至澄清。
(3)向步骤(2)中加入0.08 mol/L的AgNO3 73 μL并搅拌至澄清无色。
(4)向步骤(3)中加入0.08 mol/L的K 2S2O8 220 μL,滴加PH=14的NaOH
溶液调节PH在9-11之间,搅拌18h至反相微乳液变为浅橙棕色。加入少量乙醇离心,用乙醇和去离子水洗涤干燥后得到纳米级Ag()-PHMB配合物。
实施例4 微米级Ag()-PHMB配合物的合成
(1)稀释PHMB。取880 μL质量分数为20%的粘均分子量为3245的PHMB分散在80 mL水中。
(2)加入AgNO3。在避光条件下向步骤(1)中加入10 mL浓度0.04 mol/L的AgNO3,并中速搅拌。
(3)滴加0.16mol/L的(NH4)2S2O8 5 mL,滴加完毕后反应1 h,滴加PH=14的NaOH溶液调节PH在11-12,继续搅拌反应直至有橙棕色沉淀生成。离心,去离子水洗涤,干燥后得到微米级Ag()-PHMB配合物。
实施例5 微米级Ag()-PHMB配合物的合成
(1)稀释PHMB。取1760 μL质量分数为20%的粘均分子量为6607的PHMB分散在80 ml水中。
(2)在避光条件下向步骤(1)中加入10 mL浓度0.04 mol/L的AgNO3,并中速搅拌。
(3)加0.16 mol/L的Na2S2O8 7.5 mL,滴加完毕后反应1h,滴加PH=14的NaOH溶液调节PH在11-12,继续搅拌反应直至有橙棕色沉淀生成。离心,去离子水洗涤,干燥后得到微米级Ag()-PHMB配合物。
实验实施例1 Ag()-PHMB配合物的表征
为确认Ag()与PHMB为络合作用,而不是简单混合,现做如下测试进行表征。
对PHMB(2133)与实施例1的Ag()-PHMB(2133)配合物进行红外全波段扫描,所得红外吸收光谱如图1和图2所示。
从图1可以看出,Ag(III)-PHMB配合物在-N(H)-处的吸收峰只有3318 cm-1处有吸收峰,图2种PHMB在3315 cm-1和3160 cm-1有2处吸收峰,说明Ag3+与PHMB通过-N(H)-进行络合,说明有络合物的生成。
实验实施例2 银的氧化态测定
银的氧化态测定步骤如下:
通过X-射线光电子能谱测定实施例1样品的氧化态。当将具有恒定能量的X- 射线(光子) 辐射到样品上时,使原子或分子的内层电子或价电子受激发射出来,称为光电子。测量这些光电子的动能,可以示出从该样品发射光电子需要的结合能的量。因为此结合能为发射光电子的原子的固有性质之一,因此测量该能量值可以得到元素分析结果。因此,通过测量光电子的结合能量值进行样品的分析。通过多功能X射线光电子能谱 (AXIS ULTRA DLD,日本岛津)、使用短波长Mg Kα X-(1253.6 eV) 射线对实施例4所得Ag()-PHMB配合物进行表面分析。结果如图3所示。分别在377.42 eV 和371.40 eV 处的Ag 3d3/2 和Ag3d5/2峰确定Ag3+物质的存在。
实验实施例3 纳米级Ag()-PHMB配合物数均粒径分析
取含有Ag()-PHMB配合物的反相微乳液滴在碳支持膜上,待到液体完全挥发后送入场发射透射电子显微镜(Tecnai F30,Philips-FEI 公司,荷兰),测定当配体PHMB粘均分子量为2133,3245,4062,5428,6607时的粒径。
具体试验参数如表1所示
表1
由表1可知,在反相微乳液中合成的Ag()-PHMB配合物都是单分散的,且均为纳米级别。
实验实施例4 zeta电位测定
将Ag()-PHMB配合物超声分散在水中,用动态光散射粒度分析仪(Zetasizer Nano ZS,英国Malvern公司)对纳米级Ag()-PHMB配合物(配体是不同粘均分子量的PHMB)进行zeta电位分析,所得结果如表1所示,所有配合物的zeta电位均大于30 mV,则说明配合物是稳定存在的。
实验实施例5 抗菌性能评价
采用常量肉汤法比较实施例2合成的Ag()-PHMB配合物,AgNO3,PHMB的最低抑菌浓度比较抗菌性能作比较。应用的革兰氏阴性菌为大肠杆菌,格兰仕阳性菌为金黄色葡萄球菌。具体试验方法如下:
取13支高压灭菌后的试管,第一支试管中加入1.6 mL MH肉汤,其他试管加入1 mL MH肉汤,取配好的质量浓度为1280 mg/L的抗菌原液加入到第一支试管中,并在旋涡混合器上混合均匀后,取1 mL混合液到下一支试管,如此倍比稀释到第11支试管,从第11管中吸取1 mL弃去,第12管和13管为不含药物的生长对照。取稀释好的菌悬液1 mL,分别加到13支试管中,初始菌液浓度约为5×105 cfu/mL使得第1管至第11管药物浓度分别为128、64、32、16、8、4、2、1、0.5、0.25、0.125 mg/L。将试管转移到生化培养箱中37 ℃下培养16-20 h取出,用平板计数法测定细菌浓度。
实验结果如表2所示。可以看出是实施例4合成的微米级Ag()-PHMB配合物对革兰细菌的最低抑菌浓度要小于PHMB,AgNO3和AgO,由此可知Ag()-PHMB配合物的抗菌性能高于PHMB,AgNO3和AgO。由于纳米级颗粒与微米级颗粒相比,有高比表面积效应,量子尺寸效应,小尺寸效应等一些列优点,可推得纳米级Ag()-PHMB配合物的抗菌性能同样高于PHMB,AgNO3和AgO。
表2
实验实施例6 不同Ag(III)-PHMB配合物抗菌性能比较
测试菌包含革兰氏阴性菌(大肠杆菌),革兰氏阳性菌(金黄色葡萄球菌),接种在已经高压灭菌的MH肉汤中,在生化培养箱中37 ℃培养4 h,取出后离心分离,在PBS(磷酸盐缓冲液)中重悬浮。取500 μL PBS,与高压灭菌的液态营养琼脂(降温至40℃左右)充分混合。
取纳米级Ag(III)-PHMB配合物粉末加水配成0.4%的悬浊液,待超声分散均匀后,取5 μL悬浊液涂在先前挖好的直径5 mm的孔洞之中,并在生化培养箱中37 ℃培养24 h,通过抑菌环的大小来比较抗菌活性。所得结果如表3,从中可知,配体PHMB粘均分子量越高,Ag(III)-PHMB配合物抗菌性能越高。
表3
实验实施例7抗菌布样的制备及其抗菌性能表征
取实施例1的所得的Ag()-PHMB配合物0.2 g,超声分散于100 ml水中,取4 g符合纺织行业标准FZ/T 73023-2006的标准布样,剪成0.5×0.5 cm大小的碎片,放入悬浊液中常温下处理18 h后取出,并在120 ℃下烘干。
所得抗菌棉织物按照0.75 g为单位分开,按照FZ/T 73023-2006中提出的标准洗涤方法对抗菌棉织物分别洗涤1次,5次,10次,15次,20次,并120℃烘干。
按照纺织行业标准FZ/T 73023-2006中提到的震荡法测试抗菌棉织物的抗菌性能,方法如下所述:
取5-14代革兰氏阴性菌(大肠杆菌)和革兰氏阳性菌(金黄色葡萄球菌)接种于营养肉汤中,在生化培养箱中37 ℃培养4 h。取3-5代真菌(白色念珠菌)接种于沙保罗液体培养基上,于27 ℃下培养8 h。
取所得菌悬液1-2 mL,加入相应的液体培养基9 mL,并混合均匀后。再次取稀释后的菌悬液1 mL,加入相应的液体培养基9 mL,混合均匀后,再次取1ml加入到9 mL 0.03 mol/L的磷酸盐缓冲液(取0.02 mol磷酸二氢钠与0.01 mol磷酸二氢钾溶解于1000 mL水中)中并混合均匀。取5 mL含有菌液的连酸盐缓冲液于含有70 mL经过高温灭菌的0.03 mol/L的磷酸盐缓冲液的锥形瓶中,使得最终菌浓度在1-4×104 cfu/mL。
分别取0.75 g经过1次、5次、10次、15次、20次标准洗涤循环的抗菌棉织物和标准空白织物上述75 mL菌液中,将含有标准空白织物的锥形瓶震荡1 min后,取出菌液稀释后并通过平板记数法测定具体菌数。(注:革兰氏细菌的培养条件是生化培养箱中37 ℃下培养18 h,真菌的培养条件是生化培养箱中28 ℃下培养48 h)
把上述盛有菌液的锥形瓶放在恒温振荡器中在一定转速下震荡,16-20 h后取出并通过平板记数法测定菌液浓度,以此确定抗菌棉织物对细菌的杀灭能力。(注:革兰氏细菌的培养温度为37 ℃,真菌的培养温度为28 ℃,其中标准空白布样的菌落数达到初始菌数的10倍视为实验有效,否则重复实验)
不同洗涤次数的抗菌棉织物和标准空白布样的菌落计数及其抑菌率如表4所示。可以看出,实施例1所得Ag()-PHMB配合物抗菌性能良好,在震荡法试验中,抗菌棉织物初次洗涤后可以杀灭99.9%以上的革兰氏细菌和99.8%以上的真菌。而且纳米级Ag()-PHMB配合物与棉织物的结合作用较强经过20次洗涤后依然能杀灭99.8%以上的革兰氏细菌和99.7%以上的真菌。
表4
以上所述仅为本发明的较佳实施例,凡依本发明申请专利范围所做的均等变化与修饰,皆应属本发明的涵盖范围。
- 还没有人留言评论。精彩留言会获得点赞!