一种四价铂配合物氧化剂及其制备方法和应用与流程
本发明涉及配合物类氧化剂,具体的说是四价铂配合物氧化剂及其制备方法和应用。
背景技术:
含有分子内二硫键的多肽类药物已经用于各种疾病的治疗,在含分子内二硫键的多肽类药物的合成过程中,多肽分子内二硫键的合成是其关键步骤,同时,多肽类药物分子内二硫键的合成是精细有机化工及药物化学中的一个重要反应,目前一般采用氧化方法分为两类:(1)固液间多相氧化反应生成多肽分子内二硫键;(2)在溶液中均相氧化合成多肽分子内二硫键。其中,液相中均相氧化反应是目前常用的合成方法。
目前,用于多肽类药物分子内二硫键合成的氧化剂包括:碘、三氟乙酸铊(III)、氧气、DMSO、氧化型谷胱甘肽和Ellman’s试剂等。但是,这些氧化剂在合成多肽分子内二硫键时,有的会与多肽链中的蛋氨酸、酪氨酸、色氨酸残基发生副反应,有的会使多肽生成二聚体或多聚体的副产物,造成产率降低。有的氧化剂会产生毒性较大的副产物 (Eur. J. Org. Chem., 2014, 3519–3530; RSC Adv. 2014, 4, 13854–13881; Synthesis, 2008, 16, 2491–2509.) 。
除上述的常用氧化剂外,四价铂配合物氧化剂在合成药物分子内二硫键时得到了广泛的应用,例如四价铂配合物K2[Pt(CN)4Cl2]和[Pt(en)2Cl2]Cl2,这两种四价铂配合物都不能氧化多肽中的酪氨酸和色氨酸残基(J. Am. Chem. S℃. 2000, 122, 6809–6815; J. Org. Chem. 1999, 64, 4590–4595; Bioorg. Med. Chem. Lett. 2002, 12, 2237–2240.)。但是,K2[Pt(CN)4Cl2]会氧化多肽中的蛋氨酸残基,使多肽分子内二硫键的合成产率下降,增加多肽合成后的分离难度,因此,此氧化剂不适用于含有蛋氨酸多肽的分子内二硫键的合成。[Pt(en)2Cl2]Cl2虽然不能氧化蛋氨酸,但是,其最佳适用的反应介质的pH在4-5之间,在较强酸性介质中的反应速率非常慢。因此,如果能制备一种不氧化蛋氨酸残基且反应速率快,对反应介质条件要求低的四价铂配合物氧化剂,则能大大降低使用该类氧化剂来合成药物分子内二硫键的成本支出。
技术实现要素:
本发明的目的之一是提供一种四价铂配合物氧化剂及应用,以解决现有铂配合物氧化剂在合成多肽分子内二硫键时,反应速率慢,对反应体系要求高以及氧化蛋氨酸残基造成反应产率低的问题。
本发明的目的之二是提供一种四价铂配合物氧化剂的制备方法。
本发明的目的之一是这样实现的:
一种四价铂配合物氧化剂,其具有如式(Ⅰ)所示结构:
(Ⅰ)
式(Ⅰ)所示结构中,n=0或2,X为-1价卤离子。
本发明所述四价铂配合物氧化剂,其中,所述X为Cl-。
本发明还提供了所述四价铂配合物氧化剂在制备含分子内二硫键的多肽中的应用。
所述应用具体可通过如下技术方案实现:
将所述四价铂配合物氧化剂与还原型多肽溶液在室温条件下反应1~5 min。反应结束后,利用高效液相色谱分析反应产物。
所述还原型多肽溶液是以含有两个巯基的多肽为溶质,以≤0.1M的盐酸溶液、水或水和乙腈的混合液为溶剂制成。所述水和乙腈的混合液中水和乙腈的体积比为1∶1。
所述还原型多肽为还原型催产素、还原型精氨酸加压素、还原型多肽(1)、还原型多肽(2)、还原型多肽(3)、还原型多肽(4)、还原型多肽(5)或还原型多肽(6)中的一种。
反应体系中四价铂配合物氧化剂与还原型多肽的摩尔比为四价铂配合物氧化剂∶还原型多肽=1~2∶1。
所述还原型多肽为含有两个巯基的、可形成分子内二硫键的还原型多肽,具体的包括还原型催产素,还原型精氨酸加压素,还原型多肽(1),还原型多肽(2),还原型多肽(3),还原型多肽(4),还原型多肽(5),还原型多肽(6)。所述还原型催产素的氨基酸序列为:CYIQNCPLG-NH2;还原型精氨酸加压素的氨基酸序列为:CYFQNCPRG-NH2;还原型多肽(1)的氨基酸序列为:CGYCHKLHQMK-NH2;还原型多肽(2)的氨基酸序列为:CGYCHKLHQGK-NH2;还原型多肽(3)的氨基酸序列为:CLSSRLDAC-NH2;还原型多肽(4)的氨基酸序列为:CYFQNC-OH;还原型多肽(5)的氨基酸序列为:PFCNAFTGC-NH2;还原型多肽(6)的氨基酸序列为:CFFQNCPRG-NH2。
本发明的目的之二是这样实现的:
一类四价铂配合物氧化剂的制备方法,包括以下步骤:
a)以10mM~100mM的盐酸溶液为溶剂,将四氯铂酸钾与乙二胺按摩尔比1∶1~1.5,在80~100℃条件下加热反应12~20h,反应过程中持续滴加10mM~50mM的碱液,维持反应体系的pH小于6;
反应完毕,冷却至室温后过滤,所得固体用水洗涤后真空干燥,得到黄色固体物;
b)将所得黄色固体物于水中超声分散,然后加入含有两个氮原子的芳杂环试剂,100~120℃搅拌反应48~72h;
反应完毕,冷却至室温后过滤,所得液体浓缩后加入乙腈,将所得固体过滤洗涤后真空干燥,得到浅黄色的固体物;
c)将浅黄色固体物于H2O2/盐酸混合液中溶解后,60~80℃条件下充分反应;
反应完毕,浓缩,加入乙腈,析出固体物,所得到的浅黄色固体物为四价铂配合物氧化剂。
本发明所述四价铂配合物氧化剂的制备方法,步骤a)中,所述盐酸溶液为30 mM ~70 mM的盐酸溶液,所述碱液为10mM~30mM的KOH或NaOH溶液。
本发明所述四价铂配合物氧化剂的制备方法,步骤b)中,所述含有两个氮原子的芳杂环试剂为邻菲罗啉或2,2′-二联吡啶。芳杂环试剂的用量为芳杂环试剂与黄色固体物质的摩尔比为1∶1~1.5。
本发明所述四价铂配合物氧化剂的制备方法,步骤c)中,所述H2O2/盐酸混合液中H2O2和盐酸的体积比为10~50∶10~40,所述盐酸浓度为30 mM ~70 mM。
本发明所述四价铂配合物氧化剂的制备方法,步骤b)中,反应完毕后,所得液体浓缩至3~6mL。
本发明的氧化剂及其制备具有多方面的优点:
1、本四价铂配合物氧化剂制备简单,使用时对反应介质要求低,在强酸性介质中,本氧化剂相对于其他铂类氧化剂的反应速率快。
2、相对于传统氧化剂,本四价铂配合物氧化剂具有产率高,反应速率快的优点。
3、合成含有蛋氨酸多肽分子内二硫键后,蛋氨酸残基不被本四价铂配合物氧化为蛋氨酸亚砜。
4、由于反应溶剂简单,反应产物的提纯处理简便,通过液相色谱分离即可达到分离目标产物的目的。
附图说明
图1是本发明四价铂配合物氧化剂制备反应流程图。
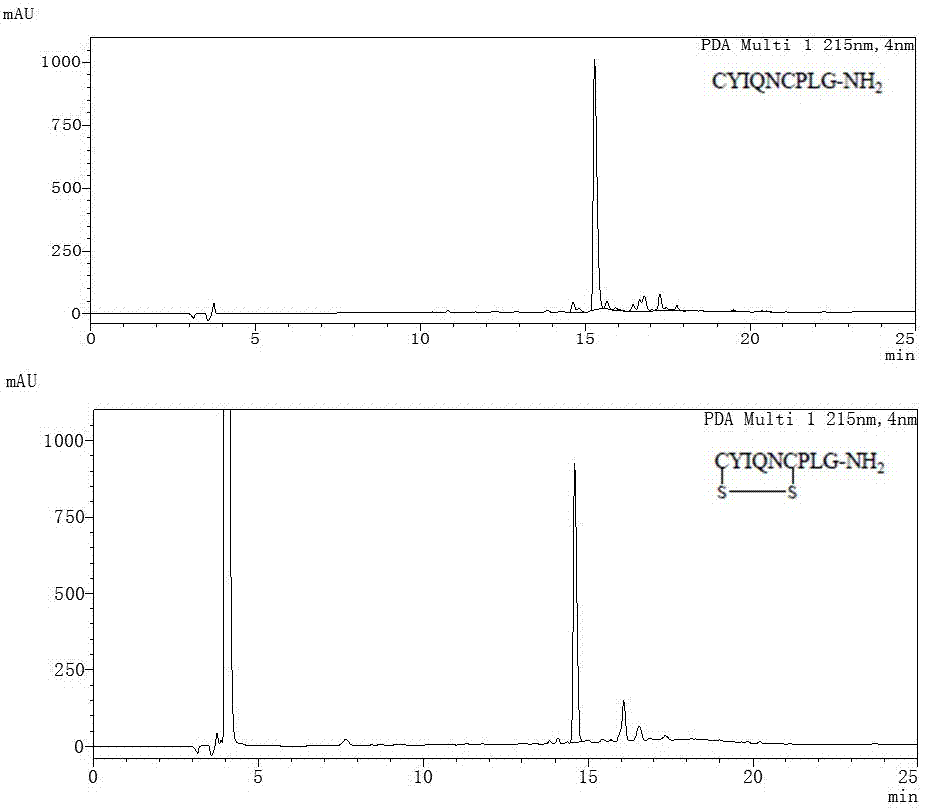
图2为还原型催产素与本发明氧化剂反应前后的色谱图对比。
图3为还原型催产素和氧化型催产素的氨基酸序列以及质谱图对比。
图4为还原型精氨酸加压素与本发明氧化剂反应前后的色谱图对比。
图5为还原型精氨酸加压素和氧化型精氨酸加压素的氨基酸序列以及质谱图对比。
图6为还原型多肽(1)与本发明氧化剂反应前后的色谱图对比。
图7为还原型多肽(1)和氧化型多肽(1)的氨基酸序列以及质谱图对比。
图8为还原型多肽(2)与本发明氧化剂反应前后的色谱图对比。
图9为还原型多肽(2)和氧化型多肽(2)的氨基酸序列以及质谱图对比。
图10为还原型多肽(3)与本发明氧化剂反应前后的色谱图对比。
图11为还原型多肽(3)和氧化型多肽(3)的氨基酸序列以及质谱图对比。
图12为还原型多肽(4)与本发明氧化剂反应前后的色谱图对比。
图13为还原型多肽(4)和氧化型多肽(4)的氨基酸序列以及质谱图对比。
图14为还原型多肽(5)与本发明氧化剂反应前后的色谱图对比。
图15为还原型多肽(5)和氧化型多肽(5)的氨基酸序列以及质谱图对比。
图16为还原型多肽(6)与本发明氧化剂反应前后的色谱图对比。
图17为还原型多肽(6)和氧化型多肽(6)的氨基酸序列以及质谱图对比。
图18为对比实施例2反应后的色谱图。
图19为对比实施例2所得产物多肽(7)的质谱图。
具体实施方式
图1给出了本发明四价铂配合物氧化剂制备反应流程图。如图1所示,本发明将四氯铂酸钾与乙二胺盐酸盐反应,得到二氯(乙二胺)合铂(为黄色固体物),如图1中式(Ⅲ)所示;二氯(乙二胺)合铂与含有两个氮原子的芳杂环反应,得到离子型的二价铂配合物(浅黄色固体物),如图1中式(Ⅱ)所示;离子型的二价铂配合物与含有双氧水的盐酸溶液发生氧化反应,得到四价铂配合物(浅黄色固体物),如图1中式(Ⅲ)所示,所得到的四价铂配合物即为本发明四价铂配合物氧化剂,其具体制备过程见实施例1~2:
实施例1
①在50 mL三颈烧瓶中,加入0.2 g 四氯铂酸钾和20 mL 浓度为50 mM的盐酸溶液,然后加入200μL乙二胺,磁力搅拌,100℃回流反应15 h;反应完毕后冷却至室温,过滤,所得固体用乙醇洗涤3次,然后50℃真空干燥12h,得到黄色的二氯(乙二胺)合铂配合物;
②将0.1 g 二氯(乙二胺)合铂加入到50mL的单颈瓶中,然后加入50 mL水,超声分散后加入0.3g 邻菲罗啉,搅拌,100℃反应50h;反应完毕后冷却至室温,过滤,浅黄色滤液浓缩至3-6 mL,然后加入100 mL乙腈,浅黄色固体析出,过滤,固体用乙腈洗涤3次,然后真空干燥,得到浅黄色离子型二价铂配合物;
③称取0.1g离子型二价铂配合物于50mL的单颈瓶中,加入10mL 双氧水和20 mL 浓度为50 mM的盐酸溶液,80℃反应5h;反应完毕后冷却至室温,过滤,浅黄色滤液浓缩至3-5 mL,加入100 mL乙腈,浅黄色固体析出,过滤,固体用乙腈洗3次,然后真空干燥过夜,得到浅黄色四价铂配合物。
所制得的四价铂配合物的元素分析结果为含有一分子结晶水的四价铂配合物(C14H18N4Cl4OPt): C% 28.5;H% 3.1;N% 9.3;理论计算值为:C% 28.2;H% 3.0;N% 9.4。
实施例2
①在50 mL三颈烧瓶中,加入0.2 g 四氯铂酸钾和20 mL 浓度为50 mM的盐酸溶液,然后加入200μL乙二胺,磁力搅拌,100℃ 回流反应12 h;反应完毕后冷却至室温,过滤,所得固体用乙醇洗涤3次,然后50 ℃真空干燥12h,得到黄色的二氯(乙二胺)合铂配合物;
②将0.2 g 二氯(乙二胺)合铂加入到50mL的单颈瓶中,然后加入100 mL水,超声分散后加入0.5 g 2,2′-二联吡啶,搅拌,100℃反应72 h;反应完毕后冷却至室温,过滤,浅黄色滤液浓缩至3-5 mL,然后加入80 mL乙腈,浅黄色固体析出,过滤,固体用乙腈洗涤3次,然后真空干燥,得到浅黄色离子型二价铂配合物;
③称取0.1 g 离子型二价铂配合物于50mL的单颈瓶中,加入10mL 双氧水和20 mL 浓度为50 mM的盐酸溶液,60 ℃反应6 h;反应完毕后冷却至室温,过滤,浅黄色滤液浓缩至3-5 mL,加入100 mL乙腈,浅黄色固体析出,过滤,固体用乙腈洗3次,然后真空干燥过夜,得到浅黄色四价铂配合物。
所制得的四价铂配合物的元素分析结果为含有一分子盐酸的四价铂配合物(C12H17N4Cl5Pt): C% 24.1;H% 3.1;N% 9.7;理论计算值为:C% 24.4;H% 2.9;N% 9.5。
实施例3
本发明所制备的氧化剂(即四价铂配合物)可与多种含有巯基的还原型多肽反应合成多肽分子内二硫键。
采用实施例1和实施例2所制备的四价铂配合物与含有巯基的还原型多肽通过以下方案合成多肽分子内二硫键:四价铂配合物与还原型多肽溶液在室温条件下反应1~5min;反应结束后,利用高效液相色谱分离反应产物,并通过质谱对反应产物进行鉴定。
本发明的氧化剂可氧化多种含有两个巯基的还原型多肽,这些多肽通过传统的固相多肽合成法合成,利用切割试剂切割后,通过乙醚沉淀出所需各种含有两个巯基的还原型多肽,得到的还原型多肽利用液相色谱和质谱进行鉴定并直接用于本发明。所用多肽的种类如下:还原型催产素,还原型精氨酸加压素,还原型多肽(1),还原型多肽(2),还原型多肽(3),还原型多肽(4),还原型多肽(5),还原型多肽(6)。这些多肽的还原型和氧化型氨基酸序列如下:
具体的,利用本发明所制备的四价铂配合物氧化剂氧化上述还原型多肽,具体反应过程如下:(四价铂配合物配制所用溶剂与对应多肽溶液溶剂相同)
一、实施例1制备的四价铂配合物与还原型催产素反应
在1.5 mL的反应瓶中,用10×10-3mol/L盐酸溶液配制0.5mL浓度为2.0×10-3mol/L的还原型催产素溶液,然后向反应瓶中加入0.5 mL浓度为2.0×10-3mol/L的四价铂配合物,室温震荡反应3 min。反应结束,溶液用液相色谱分离氧化型催产素,用质谱测定。其色谱和质谱的对比图分别如图2和图3所示,由图分析可知,还原型催产素全部被氧化为氧化型催产素,所得氧化型催产素的产率为95%,质谱图结果符合氧化型催产素的质谱信号峰。
二、实施例1制备的四价铂配合物与还原型精氨酸加压素反应
在1.5 mL的反应瓶中,用10×10-3mol/L盐酸溶液配制0.5mL浓度为2.0×10-3mol/L的还原型精氨酸加压素溶液,然后向反应瓶中加入0.5 mL浓度为2.0×10-3mol/L的四价铂配合物,室温震荡反应3 min。反应结束,溶液用液相色谱分离氧化型精氨酸加压素,用质谱测定。其色谱和质谱的对比图分别如图4和图5所示,由图分析可知,还原型精氨酸加压素全部被氧化为氧化型精氨酸加压素,所得氧化型精氨酸加压素的产率为96%,质谱图结果符合氧化型精氨酸加压素的质谱信号峰。
三、实施例1制备的四价铂配合物与还原型多肽(1)反应
在1.5 mL的反应瓶中,用10×10-3mol/L盐酸溶液配制0.5mL浓度为2.0×10-3mol/L的还原型多肽(1)溶液,然后向反应瓶中加入0.5 mL浓度为4.0×10-3mol/L的四价铂配合物,室温震荡反应3 min。反应结束,溶液用液相色谱分离氧化型多肽(1),用质谱测定。其色谱和质谱的对比图分别如图6和图7所示,由图分析可知,还原型多肽(1)全部被氧化为氧化型多肽(1),所得氧化型多肽(1)的产率为99%,质谱图结果符合氧化型多肽(1)的质谱信号峰。
四、实施例1制备的四价铂配合物与还原型多肽(2)反应
在1.5 mL的反应瓶中,用10×10-3mol/L盐酸溶液配制0.5mL浓度为2.0×10-3mol/L的还原型多肽(2)溶液,然后向反应瓶中加入0.5 mL浓度为2.0×10-3mol/L的四价铂配合物,室温震荡反应3 min。反应结束,溶液用液相色谱分离氧化型多肽(2),用质谱测定。其色谱和质谱的对比图分别如图8和图9所示,由图分析可知,还原型多肽(2)全部被氧化为氧化型多肽(2),所得氧化型多肽(2)的产率为99%,质谱图结果符合氧化型多肽(2)的质谱信号峰。
五、实施例2制备的四价铂配合物与还原型多肽(3)反应
在1.5 mL的反应瓶中,用10×10-3mol/L盐酸溶液配制0.5mL浓度为2.0×10-3mol/L的还原型多肽(3)溶液,然后向反应瓶中加入0.5 mL浓度为2.0×10-3mol/L的四价铂配合物,室温震荡反应3 min。反应结束,溶液用液相色谱分离氧化型多肽(3),用质谱测定。其色谱和质谱的对比图分别如图10和图11所示,还原型多肽(3)全部被氧化为氧化型多肽(3),所得氧化型多肽(3)的产率为96%,质谱图结果符合氧化型多肽(3)的质谱信号峰。
六、实施例2制备的四价铂配合物与还原型多肽(4)反应
在1.5 mL的反应瓶中,用10×10-3mol/L盐酸溶液配制0.5mL浓度为2.0×10-3mol/L的还原型多肽(4)溶液,然后向反应瓶中加入0.5 mL浓度为2.0×10-3mol/L的四价铂配合物,室温震荡反应3 min。反应结束,溶液用液相色谱分离氧化型多肽(4),用质谱测定。其色谱和质谱的对比图分别如图12和图13所示,还原型多肽(4)全部被氧化为氧化型多肽(4),所得氧化型多肽(4)的产率为98%,质谱图结果符合氧化型多肽(4)的质谱信号峰。
七、实施例2制备的四价铂配合物与还原型多肽(5)反应
在1.5 mL的反应瓶中,用10×10-3mol/L盐酸溶液配制0.5mL浓度为2.0×10-3mol/L的还原型多肽(5)溶液,然后向反应瓶中加入0.5 mL浓度为2.0×10-3mol/L的四价铂配合物,室温震荡反应3 min。反应结束,溶液用液相色谱分离氧化型多肽(5),用质谱测定。其色谱和质谱的对比图分别如图14和图15所示,还原型多肽(5)全部被氧化为氧化型多肽(5),所得氧化型多肽(5)的产率为99%,质谱图结果符合氧化型多肽(5)的质谱信号峰。
八、实施例2制备的四价铂配合物与还原型多肽(6)反应
在1.5 mL的反应瓶中,用10×10-3mol/L盐酸溶液配制0.5mL浓度为2.0×10-3mol/L的还原型多肽(6)溶液,然后向反应瓶中加入0.5 mL浓度为2.0×10-3mol/L的四价铂配合物,室温震荡反应3 min。反应结束,溶液用液相色谱分离氧化型多肽(6),用质谱测定。其色谱和质谱的对比图分别如图16和图17所示,还原型多肽(6)全部被氧化为氧化型多肽(6),所得氧化型多肽(6)的产率为98%,质谱图结果符合氧化型多肽(6)的质谱信号峰。
九、实施例1制备的四价铂配合物在不同溶剂中与还原型多肽(1)反应
1、在1.5 mL的反应瓶中,用0.1mol/L盐酸溶液配制0.5mL浓度为2.0×10-3mol/L的还原型多肽(1)溶液,然后向反应瓶中加入0.5 mL浓度为2.0×10-3mol/L的四价铂配合物,室温震荡反应5 min。反应结束,所得氧化型多肽(1)的产率为99%。
2、在1.5 mL的反应瓶中,用水配制0.5mL浓度为2.0×10-3mol/L的还原型多肽(1)溶液,然后向反应瓶中加入0.5 mL浓度为2.0×10-3mol/L的四价铂配合物,室温震荡反应1min。反应结束,所得氧化型多肽(1)的产率为98%。
3、在1.5 mL的反应瓶中,用水和乙腈的混合溶液(1:1 v/v)配制0.5mL浓度为2.0×10-3mol/L的还原型多肽(1)溶液,然后向反应瓶中加入0.5 mL浓度为2.0×10-3mol/L的四价铂配合物,室温震荡反应1min。反应结束,所得氧化型多肽(1)的产率为98%。
对比实施例1
在1.5 mL的反应瓶中,用10×10-3 mol/L盐酸溶液配制0.5 mL浓度为2.0×10-3mol/L的还原型催产素溶液,然后向反应瓶中加入0.5 mL浓度为2.0×10-3mol/L的[Pt(en)2Cl2]Cl2,室温震荡反应5 h时,反应不完全,氧化型催产素产率为58%,室温震荡反应10 h后,反应结束,溶液用液相色谱分离氧化型催产素。所得氧化型催产素的产率为98%。
对比实施例2
在1.5 mL的反应瓶中,用10×10-3mol/L盐酸溶液配制0.5mL浓度为2.0×10-3mol/L的还原型多肽(1)溶液,然后向反应瓶中加入0.5 mL浓度为4.0×10-3mol/L的K2[Pt(CN)4Cl2],室温震荡反应60 min。反应结束,溶液用液相色谱分离。得到多肽(7),即还原型多肽(1)被氧化得到分子内二硫键的同时,多肽中的蛋氨酸全部被氧化为蛋氨酸亚砜,所得色谱和质谱图如图18和图19所示。
对比实施例3
pH=4.65的醋酸-醋酸钠缓冲溶液按体积比1:1的比例加入乙腈得到混合溶液,混合溶液通氮气1h备用;在2 mL的反应瓶中,用配制的混合溶液配制1 mL浓度为1.0×10-3 mol/L的还原型多肽(1)溶液,此溶液与空气中的氧气反应,磁力搅拌反应36 h,反应结束。氧化型还原型多肽(1)的产率为70%。
对比实施例4
乙腈通氮气1 h备用;在5 mL的反应瓶中,配制1 mL浓度为1.0×10-3 mol/L的还原型多肽(1)溶液,加入50μL三乙胺,然后加入2 mL 含有10 mg碘的乙腈溶液,反应6 h,反应结束,去除过量的碘单质,分离氧化型多肽(1),产率为65%。
以上实施例及实验数据表明,本发明的四价铂配合物氧化剂能够用于不同结构的多肽分子内二硫键的合成,且适用于不同的反应介质。本发明的氧化剂与现有四价铂配合物试剂相比,本发明氧化剂反应速率快,尤其在酸性介质中,反应速率显著优于[Pt(en)2Cl2]Cl2,且不氧化多肽中的蛋氨酸残基;与传统的氧化剂如碘,氧气,DMSO相比,本发明四价铂配合物氧化剂具有产率高、反应速率快的优点,当合成氧化型多肽(1)时,利用氧气作为氧化剂,产率只有70%;而利用碘单质作为氧化剂时产率为65%。
合成多肽分子内二硫键后,多肽的提纯处理简单,而本领域技术人员公知当用DMSO作为氧化剂时,反应后多肽的提纯需要进行多次冷冻干燥处理,且DMSO被还原为毒性很大的二甲基硫醚,而四价铂配合物氧化剂以盐酸或水等为反应溶剂,反应后的溶液通过液相色谱法即能很好的将氧化型多肽产物与四价铂配合物氧化剂分离,即可到达分离目标产物的目的。
- 还没有人留言评论。精彩留言会获得点赞!