用于乳腺癌干细胞培养和药物分析的微流控芯片的制作方法
本发明涉及一种微流控芯片,特别是涉及一种用于乳腺癌干细胞培养和药物分析的微流控芯片。
背景技术:
关于肿瘤细胞的靶向药物分析已经成为肿瘤研究领域的热点,微流控芯片不但具有高通量,低成本,精度高,速度快等特点,而且具有结构设计灵活,规模集成的特点,可以将细胞培养和药物筛选的过程集成在同一个芯片上,大大提高工作效率,因此非常适合于肿瘤细胞的靶向药物分析。
文献“微流控芯片上的肿瘤组织微阵列构建.分析化学,2015,43(5):637-642.”构建了一种多层复合微流控芯片,在培养腔内利用海藻酸钠和cacl2反应形成水凝胶3d细胞支架,用于模拟肿瘤细胞生长的真实三维环境,通过连续灌流的方式实现乳腺癌细胞的培养,并通过浓度梯度发生器,进行了多种浓度靶向药物的分析,但构建细胞支架的方法一般只适用于贴壁细胞,而乳腺癌干细胞以其特殊的悬浮培养方式,对流体剪切力和生长空间有更高的要求,用于乳腺癌细胞培养和药物分析的微流控芯片,并不能适用于乳腺癌干细胞。
技术实现要素:
为了克服现有微流控芯片实用性差的不足,本发明提供一种用于乳腺癌干细胞培养和药物分析的微流控芯片。该微流控芯片包括四个相同的阵列单元,采用三层pdms结构,分别是顶层、中层和底层,在中层与底层之间是一层聚碳酸酯薄膜。每两个阵列单元共用一个细胞悬液入口,一个细胞悬液废液出口;顶层设置细胞悬液入口、细胞悬液废液出口和细胞悬液进液通道,中层设置细胞培养腔,细胞培养腔由多组通孔构成,底层设置培养基入口、药物入口、浓度梯度发生器、灌流通道、废液通道和废液出口。本发明通过构建高深宽比结构的细胞培养腔,为悬浮细胞提供更多的悬浮空间,并通过亲水聚碳酸酯薄膜的扩散传质进行溶质交换的方式进行灌流培养,降低了流体剪切力对悬浮细胞的伤害,达到培养乳腺癌干细胞及靶向药物分析的目的,实用性好。
本发明解决其技术问题所采用的技术方案是:一种用于乳腺癌干细胞培养和药物分析的微流控芯片,其特点是包括四个相同的阵列单元,采用三层pdms结构,分别是顶层、中层和底层,在中层与底层之间是一层聚碳酸酯薄膜5。每两个阵列单元共用一个细胞悬液入口1,一个细胞悬液废液出口2;顶层设置细胞悬液入口1、细胞悬液废液出口2和细胞悬液进液通道3,中层设置细胞培养腔4,细胞培养腔4由多组通孔构成,底层设置培养基入口6、药物入口7、浓度梯度发生器8、灌流通道9、废液通道10和废液出口11。所述细胞悬液进液通道3由宽50um、高50um的直通道构成,所述灌流通道9由直径200um、高50um的圆柱腔体构成;所述浓度梯度发生器8和废液通道10由宽50um、高50um的通道构成;所述细胞悬液入口1、细胞悬液废液出口2、培养基入口6、药物入口7及废液出口11的直径为1000um。
所述中层是厚度为150um的pdms薄膜。
所述细胞培养腔4上的通孔直径优选200um。
所述聚碳酸酯薄膜5是多孔结构。
所述聚碳酸酯薄膜5的孔径优选8um。
所述浓度梯度发生器8是圣诞树结构。
本发明的有益效果是:该微流控芯片包括四个相同的阵列单元,采用三层pdms结构,分别是顶层、中层和底层,在中层与底层之间是一层聚碳酸酯薄膜。每两个阵列单元共用一个细胞悬液入口,一个细胞悬液废液出口;顶层设置细胞悬液入口、细胞悬液废液出口和细胞悬液进液通道,中层设置细胞培养腔,细胞培养腔由多组通孔构成,底层设置培养基入口、药物入口、浓度梯度发生器、灌流通道、废液通道和废液出口。本发明通过构建高深宽比结构的细胞培养腔,为悬浮细胞提供更多的悬浮空间,并通过亲水聚碳酸酯薄膜的扩散传质进行溶质交换的方式进行灌流培养,降低了流体剪切力对悬浮细胞的伤害,达到培养乳腺癌干细胞及靶向药物分析的目的,实用性好。
下面结合附图和具体实施方式对本发明作详细说明。
附图说明
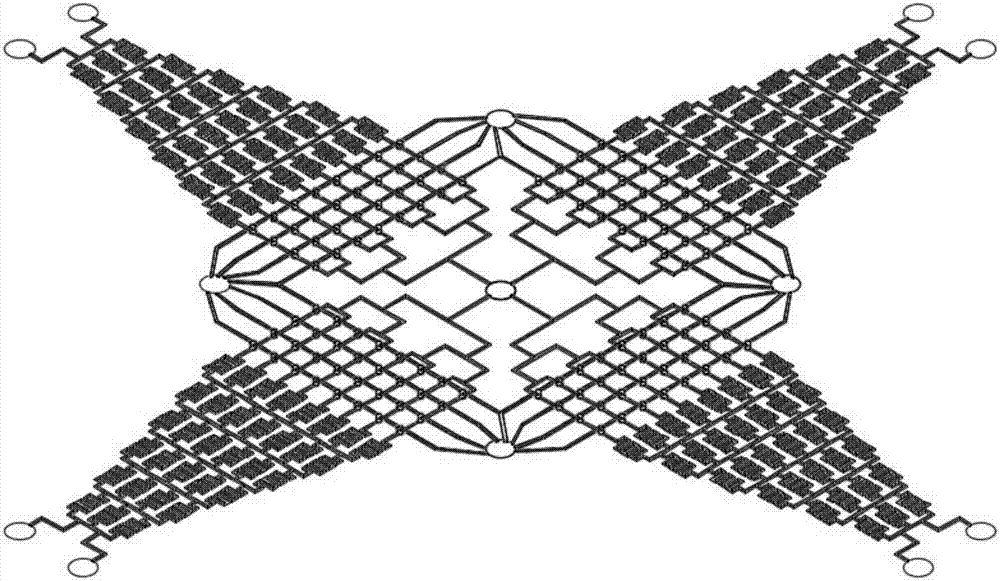
图1是本发明用于乳腺癌干细胞培养和药物分析的微流控芯片整体拼接示意图。
图2是本发明用于乳腺癌干细胞培养和药物分析的微流控芯片单个阵列单元局部示意图。
图3是本发明用于乳腺癌干细胞培养和药物分析的微流控芯片各层结构示意图,其中,图3(a)是芯片顶层,图3(b)是芯片中层,图3(c)是聚碳酸酯薄膜,图3(d)是芯片底层。
图中,1-细胞悬液入口;2-细胞悬液废液出口;3-细胞悬液进液通道;4-细胞培养腔;5-聚碳酸酯薄膜;6-培养基入口;7-药物入口;8-浓度梯度发生器;9-灌流通道;10-废液通道;11-废液出口。
具体实施方式
以下实施例参照图1~3。
本发明用于乳腺癌干细胞培养和药物分析的微流控芯片集成了4个相同的阵列单元,包含3层pdms结构。顶层含细胞悬液入口1、细胞悬液废液出口2和细胞悬液进液通道3;中层含一系列作为细胞培养腔4的通孔;底层含培养基入口6、药物入口7、“圣诞树”结构的浓度梯度发生器8、灌流通道9,废液通道10及废液出口11。细胞悬液进液通道3、灌流通道9由宽50um、高50um的直通道及直径200um、高50um的圆柱腔体构成;浓度梯度发生器8、废液通道10由宽50um、高50um的通道构成;细胞培养腔4为直径200um、高150um的圆柱腔体;细胞悬液入口1、细胞悬液废液出口2、培养基入口6、药物入口7及废液出口11的直径为1000um;聚碳酸酯薄膜5为孔径为8um的多孔亲水薄膜。
本发明微流控芯片的工作过程分为三个阶段:(1)从细胞悬液入口1注入细胞悬液,充满细胞悬液进液通道3,细胞自然沉降入细胞培养腔4,其余悬液通过细胞悬液废液出口2排出;从细胞进液口1通入无血清培养基,冲洗细胞悬液进液通道3内的残余细胞悬液,同时为细胞培养腔4内的细胞提供养分,多余培养基通过细胞悬液废液出口2排出。(2)从培养基入口6和药物入口7都注入无血清培养基,培养基经浓度梯度发生器8流经底层灌流通道9,通过聚碳酸酯薄膜5扩散至细胞培养腔4,实现细胞的灌流培养。(3)通过药物入口7注入药物,培养基入口6依旧注入培养基,在浓度梯度发生器8的出口依次形成不同的药物浓度,通过灌流通道9和聚碳酸酯薄膜5的扩散作用于细胞培养腔4内的细胞,并观察不同的药物和不同浓度的药物对细胞的影响。
技术特征:
技术总结
本发明公开了一种用于乳腺癌干细胞培养和药物分析的微流控芯片,用于解决现有微流控芯片实用性差的技术问题。技术方案是包括四个相同的阵列单元,采用三层PDMS结构,分别是顶层、中层和底层,在中层与底层之间是一层聚碳酸酯薄膜。每两个阵列单元共用一个细胞悬液入口,一个细胞悬液废液出口;顶层设置细胞悬液入口、细胞悬液废液出口和细胞悬液进液通道,中层设置细胞培养腔,底层设置培养基入口、药物入口、浓度梯度发生器、灌流通道、废液通道和废液出口。本发明通过构建高深宽比结构的细胞培养腔,为悬浮细胞提供更多的悬浮空间,降低了流体剪切力对悬浮细胞的伤害,达到培养乳腺癌干细胞及靶向药物分析的目的,实用性好。
技术研发人员:王少熙;敬冬阳;冯丹
受保护的技术使用者:西北工业大学;西北工业大学深圳研究院
技术研发日:2017.06.01
技术公布日:2017.10.10
- 还没有人留言评论。精彩留言会获得点赞!