18F标记的EGFR正电子示踪剂及其制备方法与应用与流程
本发明涉及一种18f标记的egfr正电子示踪剂及其制备方法和应用。
背景技术:
正电子发射断层扫描(positronemissiontomograghy,pet)是目前在活体监测肿瘤发生、发展过程的最佳影像学设备,可以实现对细胞代谢和功能的高分辨率显像,从分子水平对人体的生理、生化过程进行无创、三维、动态研究,pet可应用于肿瘤的诊断,良恶性鉴别、恶性肿瘤分期、分型及肿瘤复发、转移的早期诊断和鉴别,治疗方案的选择和化疗、放疗效果的检测以及肿瘤变化过程的观察和愈后情况的监测。pet检查依赖于广谱性或者特异性的靶向正电子显像剂在目标器官特异性代谢、吸收。18f-fdg是目前pet最常用显像剂,但18f-fdg存在特异性较差、有时出现假阳性、不能区分肿瘤和炎症等缺点,而且一些器官(脑、肝脏、心脏)的基础代谢原本就较高,在某些脑肿瘤、肺癌、前列腺癌等的诊断和鉴别中存在很多困难。因此18f-fdg是一种非特异的肿瘤显像剂,关于肿瘤的诊断和研究还需要研发新型的、特异性的显像剂。
随着分子生物学的发展,从分子水平对癌细胞的发生、发展、迁移有了新的认识,靶向药物蕴育而生。近年来基于表皮生长因子受体(egfr)的靶向小分子酪氨酸激酶抑制剂研究非常活跃,目前已经有多种tki类小分子药物用于癌症的治疗,其中埃罗替尼(erlotinib)是效果最好运用最广的生物靶向药物之一。egfr是一个很有吸引力的治疗靶点,它在诱导细胞增殖、侵袭、转移和抑制凋亡等复杂的信号通路中具有重要作用。egfr过度表达的肿瘤细胞接收细胞生长信号,激活细胞内的某些基因表达,加速细胞分化,释放血管生成因子和促转移因子,最终导致肿瘤的发生发展。egfr家族由四个跨膜受体组成,包括egfr(heri/erbb-1)、her2(erbb-2/neu)、(heri/erbb-3)以及(heri/erbb-4)。其蛋白质结构由胞外区、跨膜区、和胞内区组成。胞外区为配体结合区,跨膜区是单独一个α螺旋,胞内区包括一个酪氨酸激酶(tk)区和几个酪氨酸磷酸化位点的羧基末端。
近年来放射性标记的酪氨酸激酶抑制剂(tki)作为肿瘤示踪剂的研究成为热点,特别是作为pet/ct无创检查的正电子显像剂研究者众多。主要有两大类:18f标记和11c标记的正电子显像剂。继1998年peter详细报道11c-pd153035的几种标记方法后,众多正电子核素标记的tki类小分子示踪剂被国外研究者报道。11c标记的有:11c-erlotinib、11c-gefitinib、11c-m03、11c-azd8931、11c-vandetanib、11c-sorafenib等。18f标记的有:18f-gefitinib、18f-lapatinib、18f-ml04等。他们大多是具有4-氨基喹唑啉结构的erlotinib类衍生物。国外初步研究结果发现,此类小分子正电子显像剂能够与egfr-tk结合,可以达到受体显像的目的,egfr显像阳性的肿瘤患者肿瘤恶性程度高,容易发生转移,复发率高,预后差。同时在指导小分子酪氨酸激酶抑制剂生物靶向药物的临床靶向治疗有一定的价值。国内学者对此类表皮生长因子受体正电子显像剂也做了相关研究。山东省肿瘤医院于金明院士团队对11c-pd153035做了深入研究,发现其显像结果与egfr活性呈正相关,并且对临床指导用药有重要意义。近年来哈尔滨医科大学、北京师范大学、浙江大学等高校都对放射性标记的tki类正电子显像剂做了相关研究,发明了几种新的4-氨基喹唑啉类正电子显像剂并申请专利保护。可见,该类正电子显像剂具有较大应用前景及市场,并且有部分工作已经通过临床实践得到证实。
erlotinib在临床中广泛应用,其抗癌疗效得到广泛认可,同时由于其自身化学结构特点,具有较好的水溶性,在众多放射性标记的tki类正电子显像剂中,11c-erlotinib有其独特的优势,能快速经血液被脏器及目标靶区吸收,通过肝肠及泌尿系统代谢。memon09年首先在cancerresearch报道了11c-erlotinib作为正电子显像剂在小鼠肺癌移植肿瘤中的显像,研究运用egfr表达不同的三种肿瘤细胞hcc827,nci358,a549分别建模,结果表明其摄取与egfr表达成正相关。之后其团队将其应用于临床,进行了非小细胞肺癌患者显像研究,发现其病灶部分有较高的靶/非靶比,能显像某些18f-fdg不显像的病灶,对18f-fdg起到了很好的补充显像作用,对erlotinibb生物靶向药物的临床个性化治疗有很大指导意义。2013年耶鲁大学的petrulli等也报道了11c-erlotinibpet/ct显像在评价egfr表达水平和临床指导个性化治疗的突出表现。bahce等也研究了5例egfr19外显子缺失与5例未缺失的非小细胞肺癌患者的临床11c-erlotinib显像,发现缺失者能特异性摄取11c-erlotinib,这能指导埃罗替尼的临床靶向用药。
虽然近年学者们运用11c-erlotinib在基础研及临床究中取得不少成果,但是也存在一些不足限制了其进一步应用:(1)11c半衰期短,不易作大标本研究。(2)11c-erlotinib只能在有加速器的pet/ct中心应用,而且单次生产能满足的患者数量有限(每次生产的剂量最多仅能满足3名患者)。(3)从卫生经济学角度出发,在达到相同临床效果的情况下,长半衰期核素与短半衰期核素标记的显像剂相比,更节约成本。从临床实际情况考虑,迫切需要发展半衰期较长的正电子核素进行标记,18f标记的埃罗替尼是较佳的选择,其有希望成为未来临床中广泛用于指导临床个性化治疗的正电子显像剂,并有望在生物医药工业中做出一定贡献。我们前期研究中已通过“点击化学”法在erlotinib的4-氨基取代的苯环位置上进行了18f标记,并申请了专利保护。本研究中我们尝试在erlotinib4-氨基喹唑啉结构的6或者7位处进行18f标记,以期能有更好的靶向pet显像效果。
技术实现要素:
本发明的目的在于提供一种18f标记的egfr正电子示踪剂,结构如式a。
本发明的另一目的是提供此18f标记的egfr正电子示踪剂的制备方法,通过一下方法一或方法二实现:
方法一,两步法合成:用1ml淋洗液淋洗18f被捕获的qma柱,收集淋洗液到反应瓶中,加热110℃并不断吹入高纯氮气,共沸除去h2o。将1ml溶有10mg中间体前体的乙腈溶液加入到反应瓶,90℃反应15min;蒸干上述反应溶剂后,将溶有1-3mg去甲基前体及适量碱的0.3ml溶液加入反应瓶,115℃反应10min。冷却反应液后加入10ml水稀释,通过sep-parc-18柱,并用10ml水冲洗柱子,用2ml乙腈淋洗c-18柱,收集淋洗液,经半制备hplc分离得到目标产物,标记放化纯大于99%。
方法二,一步法合成:用1ml淋洗液淋洗18f被捕获的qma柱,收集淋洗液到反应瓶中,加热110℃并不断吹入高纯氮气,共沸除去h2o。将0.3ml溶有1mg一步法前体的溶液加入到反应瓶,120℃反应10min。冷却反应液后加入10ml水稀释,通过sep-parc-18柱,并用10ml水冲洗柱子,用2ml乙腈淋洗c-18柱,收集淋洗液,经半制备hplc分离得到目标产物,标记放化纯大于99%。
反应中淋洗18f用1ml溶液的组成为:12.0mg4,7,13,16,21,24-六氧-1,10-二氮双环[8.8.8]二十六烷溶于0.9ml乙腈加3.0mgk2co3,或者4.3mgkhco3溶于0.1ml水;溶解去甲基前体及一步法前体所用溶剂为无水乙腈、无水二甲基亚砜(dmso)或无水n,n-二甲基甲酰胺(dmf)中一种或几种混合。
方法一中中间体前体为1-甲基-4-[(4-甲基苯基)磺酰氧基甲氧基磺酰基]苯、1,2-双甲苯氧基乙烷、二乙二醇双(甲苯磺酸酯)、三乙二醇双(甲苯磺酸酯)中的一种;所用碱的种类为:氢氧化钠、氢氧化钾、氢化钾、氢化钠、氢氧化四丁基铵、氨基钾、氨基钠、丁基锂、二异丙基氨锂、苄基锂、甲醇钠、乙醇钠中的一种;其中去甲基前体结构式如式c所示。
方法二中前体结构式如式d所示。
本发明的第三个目的是提供18f标记的egfr正电子示踪剂作为肿瘤踪剂的应用,实验表明18f标记的egfr正电子示踪剂可用于肿瘤尤其是表皮生长因子(egfr)高表达的肿瘤pet显像,是一类新的肿瘤pet显像剂。
本发明的正电子示踪剂具有很好的特异性,能阳性识别表皮因子受体(egfr)高表达或变异肿瘤。其制备方法方便、简单、快速,可通过手动合成制备,也可通过放射性合成模块进行自动化合成,目前通过北京派特多功能模块及getracerlabfxfn模块经流程改造后可分别自动化合成,其他品牌合成器也可实现自动合成,可满足科学研究与临床试验需求。
附图说明
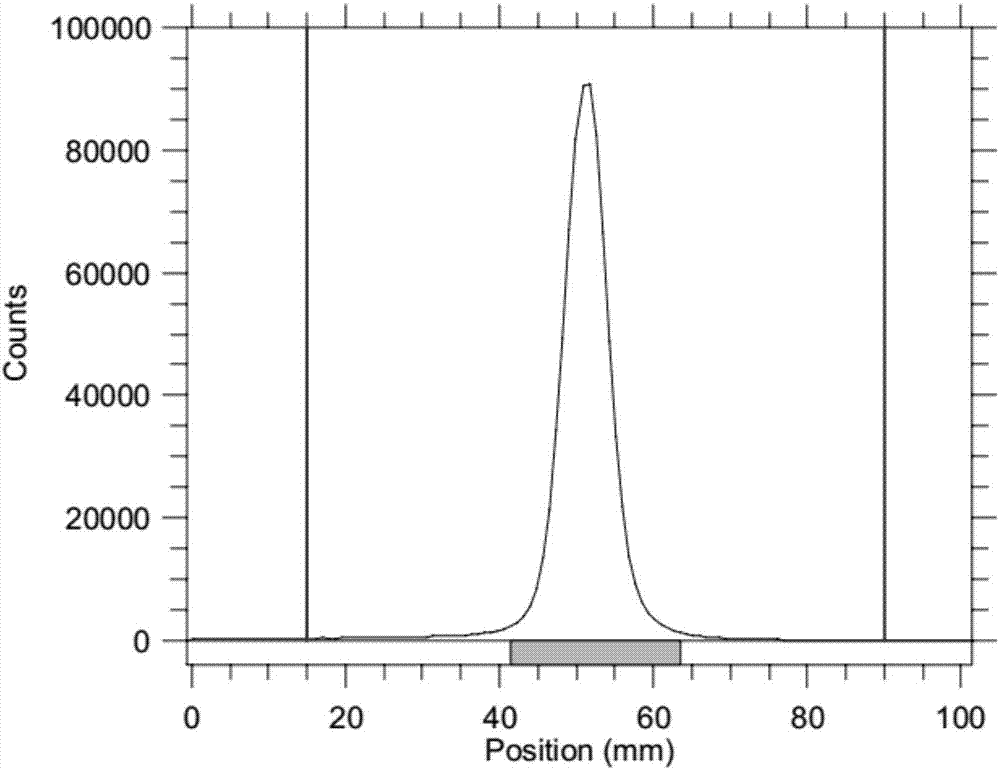
图1是中间体1-18f,2-对甲基苯磺酰氧基乙烷放射性薄层色谱(tlc)图(展开剂100%乙酸乙酯);
图2是[18f]-6-fluoromethylerlotinib放射性薄层色谱(tlc)图(展开剂100%乙酸乙酯);
图3是[18f]-6-fluoromethylerlotinib正常鼠体内生物分布图。
图4是hcc827荷瘤鼠[18f]-6-fluoromethylerlotinibmicropet/ct显像图。
具体实施方式
下面通过实验并结合实施例对本发明作进一步说明,这些实施例仅用于例证目的,但不限制本发明的保护范围。另外,实施例1-4均在getracerlabfxfn自动化合成模块中自动合成。
实施例1
1)应用医用回旋加速器轰击18o水,通过18o(pn)18f核反应生产得到500mci18f,并传导于阴离子交换柱中,测定活度并用1ml混合溶液(12.0mg4,7,13,16,21,24-六氧-1,10-二氮双环[8.8.8]二十六烷(k2.2.2.)加3.0mgk2co3溶于0.1ml水和0.9ml乙腈)将18f淋洗到反应瓶中;
2)向反应瓶中不断吹入高纯氦气,110℃下共沸除水,吹干;将15mg前体1(1,2-双甲苯氧基乙烷)溶于1ml乙腈,加入反应瓶中,90℃反应15min;反应结束后80℃除干溶剂;
3)将2mg去甲基erlotinib前体1溶于0.5mldmso、5mgnah加入反应瓶中,120℃密闭反应10min;
4)加入10ml水稀释,通过sep-parplusc-18柱,再用10ml水冲洗c-18柱,吹干后用2ml乙腈淋洗c-18柱,收集洗液并加水稀释至5ml,经半制备hplc分离得到目标产物。
经测算,放射化学产率20%以上,放射化学纯度大于99%。图1是实施例1制备得到的中间体1-18f,2-对甲基苯磺酰氧基乙烷放射性薄层色谱(tlc)(展开剂100%乙酸乙酯);图2是实施例1制备得到的[18f]-erlotinib放射性薄层色谱(tlc)图(展开剂100%乙酸乙酯)。
实施例2
1)应用医用回旋加速器轰击18o水,通过18o(pn)18f核反应生产得到500mci18f,并传导于阴离子交换柱中,测定活度并用1ml混合溶液(12.0mg4,7,13,16,21,24-六氧-1,10-二氮双环[8.8.8]二十六烷(k2.2.2.)加3.0mgk2co3溶于0.1ml水和0.9ml乙腈)将18f淋洗到反应瓶中;
2)向反应瓶中不断吹入高纯氦气,110℃下共沸除水,吹干;将方法二前体结构如式d(其中r1为ch3-,r2为tsoch2ch2-)1mg溶于0.3mldmso,加入反应瓶中,120℃密闭反应10min;
3)加入10ml水稀释,通过sep-parplusc-18柱,再用10ml水冲洗c-18柱,吹干后用2ml乙腈淋洗c-18柱,收集洗液并加水稀释至5ml,经半制备hplc分离得到目标产物。
经测算,放射化学产率20%以上,放射化学纯度大于99%。
实施例3
1)应用医用回旋加速器轰击18o水,通过18o(pn)18f核反应生产得到500mci18f,并传导于阴离子交换柱中,测定活度并用1ml混合溶液(12.0mg4,7,13,16,21,24-六氧-1,10-二氮双环[8.8.8]二十六烷(k2.2.2.)加3.0mgk2co3溶于0.1ml水和0.9ml乙腈)将18f淋洗到反应瓶中;
2)向反应瓶中不断吹入高纯氦气,110℃下共沸除水,吹干;将10mg中间体前体1-甲基-4-[(4-甲基苯基)磺酰氧基甲氧基磺酰基]苯溶于1ml乙腈,加入反应瓶中,90℃反应15min。反应结束后80℃除干溶剂;
3)将3mg去甲基前体2溶于0.4mldmf、5mgkoh加入反应瓶中,120℃密闭反应10min;
4)加入10ml水稀释,通过sep-parplusc-18柱,再用10ml水冲洗c-18柱,吹干后用2ml乙腈淋洗c-18柱,收集洗液并加水稀释至5ml,经半制备hplc分离得到目标产物。
经测算,放射化学产率20%以上,放射化学纯度大于99%。
实施例4
1)应用医用回旋加速器轰击18o水,通过18o(pn)18f核反应生产得到500mci18f,并传导于阴离子交换柱中,测定活度并用1ml混合溶液(12.0mg4,7,13,16,21,24-六氧-1,10-二氮双环[8.8.8]二十六烷(k2.2.2.)加3.0mgk2co3溶于0.1ml水和0.9ml乙腈)将18f淋洗到反应瓶中;
2)向反应瓶中不断吹入高纯氦气,110℃下共沸除水,吹干;将方法二前体(结构如式d中r1为ch3-,r2为tsoch2ch2och2ch2-)1mg溶于0.3mldmso,加入反应瓶中,120℃密闭反应10min;
3)加入10ml水稀释,通过sep-parplusc-18柱,再用10水冲洗c-18柱,吹干后用2ml乙腈淋洗c-18柱,收集洗液并加水稀释至5ml,经半制备hplc分离得到目标产物。经测算,放射化学产率20%以上,放射化学纯度大于99%。
实施例5[18f]-6-fluoromethylerlotinib的体内稳定性实验
实施例1制备得到的[18f]-6-fluoromethylerlotinib在含10%胎牛血清的培养基中37℃孵育4小时后,放射化学纯度仍达到97%以上,稳定性良好。
实施例6[18f]-6-fluoromethylerlotinib的体内分布试验
实施例2制备得到的[18f]-6-fluoromethylerlotinib,在正常昆明鼠体内生物分布图如图3,显示药物主要经肝肠代谢,肾脏也有部分代谢,血液清除速度快,骨中放射性不高,药物在体内不脱氟,稳定性好。
实施例7荷瘤鼠[18f]-6-fluoromethylerlotinibmicropet显像
选用egfr高表达非小细胞肺癌hcc827荷瘤鼠模型,利用实施例2制备得到的[18f]-6-fluoromethylerlotinib进行micropet显像(图4),图4显示肿瘤部位放射性摄取明显高于肌肉、骨骼、肺、脑等器脏(组织)。
以上所述仅为本发明优选实施例,对本发明而言仅具有说明性,但非限制性;相关领域普通技术人员可理解,在本发明权利要求所限定的精神和范围内可对其进行许多修改或者等效变更,但都将落入本发明的保护范围内。
- 还没有人留言评论。精彩留言会获得点赞!