一种检测氰根离子的荧光探针及其合成合应用方法与流程
本发明属于化学分析检测技术领域,具体涉及一种检测氰根离子的荧光探针及其制备和在检测氰根离子方面的应用。
背景技术:
众所周知,氰化物毒性极强,可经呼吸道或者皮肤吸收进入人体,极微量便可致人死亡,世界卫生组织规定饮用水中cn-的最大含量为1.9μmol·l-1。其中毒机理为氰根离子通过人体吸收进入血液循环后,与细胞色素氧化酶的三价铁离子络合,导致三价铁离子丧失传递电子的能力,使呼吸链中断,最终导致机体缺氧而死亡。氰化物的应用领域非常广泛,例如,冶金行业、黄金开采和电镀都会大量使用氰化物。此外在合成化肥、农药、杀虫剂树脂和医药等重要原料时氰化物也不可或缺。大量使用氰化物必然会导致氰根离子对环境的污染,因此发展快速、高效的检测cn-的方法在环境监测和食品分析中都非常重要。目前检测cn-的方法主要有离子色谱法、滴定分析法、流动注射分析法等。这些方法对样品的要求比较高,操作复杂,因此,发展易于操作,选择性好,灵敏度高,成本低廉的检测氰根离子的方法具有重大意义。
近年来,化学荧光探针检测阴离子由于其方法的简便性,高灵敏度,抗干扰能力强和仪器操作简单得到非常广泛的应用。荧光探针检测离子主要原理是以荧光光谱为手段,探针与待检测离子之间通过特异结合后,改变荧光基团的结构,从而导致其荧光性质发生改变,通过这种荧光信号的变化实现对待检测离子的定性以及定量分析。人们通过这个原理设计合成了许多氰根离子荧光探针。但是大部分探针合成方法复杂,成本高,检测时间长,不能做到实时检测,有些检测体系为有机溶剂,很难检测实际水样中的氰根离子,灵敏度也不够高,很少能达到纳摩尔级,此外有些报道探针选择性也不够好,醋酸根和氟离子容易造成干扰,因此,开发灵敏度高、选择性好,可在水相中检测氰根离子的荧光探针具有重要意义。
技术实现要素:
本发明的目的就是解决现有技术中存在的不足,提供一种易于制备、低成本、性能稳定的化学荧光探针,并提供该探针的合成方法,还在此基础上开发出对氰根离子进行高选择性和高灵敏度的快速检测方法。
为实现上述目的,本发明采用下述技术方案:
一种检测氰根离子的荧光探针hb,其化学名称为1,3,3-三甲基2-(1,3,5,6-四甲基8-(4(乙烯基苯基))氟化硼二吡咯)-3h-碘化吲哚盐,结构式如下:
一种检测氰根离子的荧光探针hb的合成方法,具体如下:
以2,4-二甲基吡咯和4-羟甲基苯甲醛为原料,通过缩合,氧化,再与1,2,3,3-四甲基-3h-碘化吲哚盐通过克脑文盖尔缩合反应所得:
具体工艺包括以下步骤:
(1)1,3,5,6-四甲基8-(4(羟甲基苯基))氟化硼二吡咯(2)的合成:
取干燥的500ml的两口瓶,瓶内置换成氮气,加入2,4-二甲基吡咯(2.2ml,20.0mmol),4-羟甲基苯甲醛(1.4g,10.0mmol),三氟乙酸(0.11ml,1mmol)和ch2cl2(150ml),室温搅拌12h,然后加入2,3-二氯-5,6-二氰对苯醌(2.3g,10.0mmol),室温搅拌1h,加入et3n(30ml),冰浴冷却至0摄氏度,加入bf3.et2o(30ml),室温搅拌3h,加入饱和nahco3洗涤,并用ch2cl2萃取,合并有机相,无水硫酸镁干燥,过滤,浓缩;硅胶柱层析分离提纯(石油醚:二氯甲烷=2:1)得黄色固体(0.9g,2.5mmol);
(2)1,3,5,6-四甲基8-(4(醛基苯基))氟化硼二吡咯(3)的合成:
250ml单口瓶中,加入1,3,5,6-四甲基8-(4(羟甲基苯基))氟化硼二吡咯(0.9g,2.5mmol),活化的mno2(5.4g,62.5mmol)和ch2cl2(150ml),回流12h,反应结束后,硅藻土过滤,收集滤液,浓缩,硅胶柱层析分离提纯(石油醚:二氯甲烷=2:1)得红色固体(0.7g,2.0mmol);
(3)1,3,3-四甲基2-(1,3,5,6-四甲基8-(4(乙烯基苯基))氟化硼二吡咯)-3h-碘化吲哚盐(1)的合成:
100ml两口瓶中加入1,3,5,6-四甲基8-(4(醛基苯基))氟化硼二吡咯(0.5g,1.4mmol))、1,2,3,3-四甲基-3h-碘化吲哚盐(0.4g,1.4mmol)和无水乙醇(60ml),置换成n2体系,加入2滴哌啶,回流12h,浓缩,硅胶柱层析分离提纯(石油醚:二氯甲烷=2:1)得红色固体(0.5g,0.78mmol)。
上述方法反应流程如下:
一种检测氰根离子的荧光探针hb的应用方法,利用hb对氰根离子进行定性和定量测定,所述的荧光探针由上述的方法合成。
所述的荧光探针hb用于水体、土壤中氰根离子的检测。
采用紫外吸收和荧光发射光谱法检测时,荧光探针hb溶解在水和乙醇1:1混合溶液中,对氰根离子进行测试。
所述的荧光探针hb另一种应用方式是在处理过的滤纸上滴加hb的乙醇与水(v/v=1/1)混合溶液,使hb分子均匀吸附在滤纸上,自然晾干,制备得到cn-监测试纸。
本发明的紫外吸收和荧光发射光谱法检测氰根离子的探针的具体特征如下:
hb是以氟化硼二吡咯为荧光信号基团,半花菁为识别位点,在乙醇和水(v/v=1:1)作为溶剂的条件下,在385nm,502nm和545nm处分别有吸收峰,加入cn─后,385nm处的吸收峰消失,在256nm处出现新的吸收峰。而加入其它阴离子,hb的紫外吸收光谱没有明显变化(图1)。在荧光光谱中,以385nm作为激发波长,hb的最大发射波长为515nm,荧光强度非常弱,加入cn─后,515nm处的发射波长明显增强,而加入其它阴离子,hb的发射波长没有明显变化(图2),在紫外灯365nm照射下,加入cn─后出现绿色荧光,而其它阴离子没有变化(图3)。
本发明的有益效果为:所述的探针分子合成方法简单,成本较低,灵敏度较高,对氰根离子识别能力强,响应速度较快,30s即可达到平衡,响应范围在0—10μmol·l-1,最低检测限可达59nm;在实际水样的检测中,相对标准偏差小于5%。因此该荧光探针hb在氰根离子的检测中具有很好的应用前景。
附图说明
图1为hb(10μmol·l-1)的乙醇和水(v/v=1/1)溶液中加入不同阴离子(8μmol·l-1)时的紫外吸收谱图;
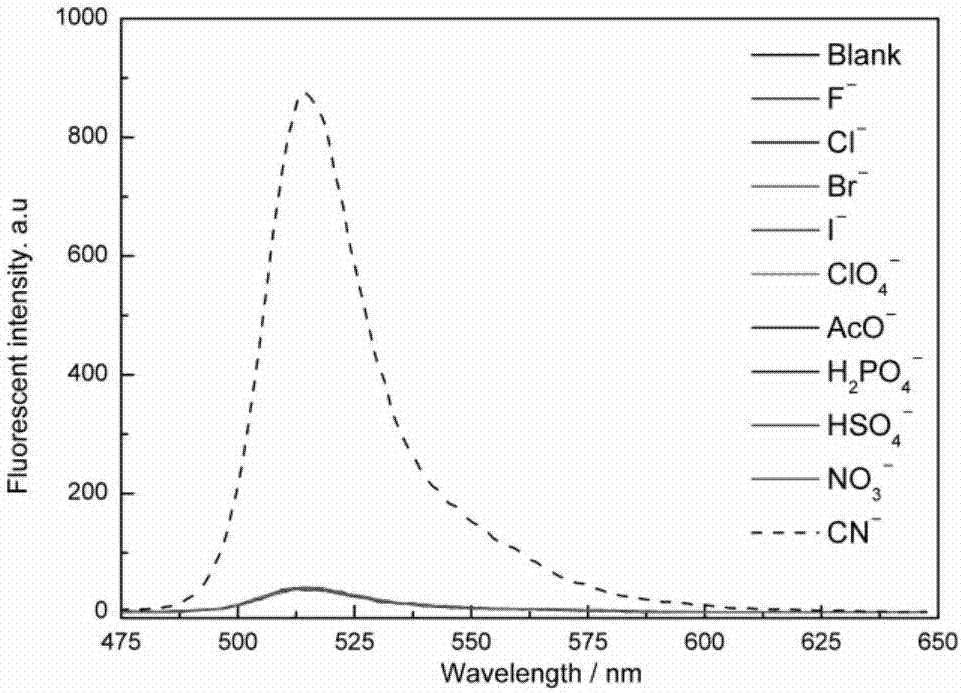
图2为hb(10μmol·l-1)的乙醇和水(v/v=1/1)溶液中加入不同阴离子(8μmol·l-1)时的荧光发射谱图(λex=385nm);
图3为hb(10μmol·l-1)的乙醇和水(v/v=1/1)溶液中加入不同阴离子(8μmol·l-1)时在手提紫外灯365nm照射下图片;
图4为hb(10μmol·l-1)的乙醇和水(v/v=1/1)溶液中在不同cn-浓度(0—60μmol·l-1)下紫外吸收光谱,插图:a385nm与cn-浓度关系曲线;
图5为hb(10μmol·l-1)的乙醇和水(v/v=1/1)溶液中在不同cn-浓度(0—60μmol·l-1)下荧光发射光谱,插图:i/i0与cn-浓度关系曲线;
图6为i/i0与cn-.浓度(1—10μmol·l-1)线性曲线图;
图7为hb(10μmol·l-1)在与其它阴离子(80μmol·l-1)共存时对cn-(40μmol·l-1)响应时i/i0的变化柱状图;
图8为hb与hb+cn-在ph值2—11体系中515nm处荧光强度。
图9为hb(10μmol·l-1)的乙醇和水(v/v=1/1)溶液中对cn-(20μmol·l-1)响应时间。
图10为hb试纸滴加入不同阴离子时在手提紫外灯365nm照射下图片
图11为hb试纸滴加不同浓度cn-时在手提紫外灯365nm照射下图片
具体实施方式
通过以下详细说明结合附图可以进一步理解本发明的特点和优点。所提供的实施例仅是对本发明方法的说明,而不以任何方式限制本发明揭示的其余内容。
【实施例1】检测氰根离子的荧光探针hb分子的合成
本发明检测氰根离子的荧光探针分子的合成,是以2,4-二甲基吡咯和4-羟甲基苯甲醛为原料,通过缩合,氧化,再与1,2,3,3-四甲基-3h-碘化吲哚盐通过克脑文盖尔缩合反应所得。
(1)1,3,5,6-四甲基8-(4(羟甲基苯基))氟化硼二吡咯(2)的合成:
取干燥的500ml的两口瓶,瓶内置换成氮气,加入2,4-二甲基吡咯(2.2ml,20.0mmol),苯甲醛(1.4g,10.0mmol),三氟乙酸(0.11ml,1mmol)和ch2cl2(150ml),室温搅拌12h,然后加入2,3-二氯-5,6-二氰对苯醌(2.3g,10.0mmol),室温搅拌1h,加入et3n(30ml),冰浴冷却至0摄氏度,加入bf3.et2o(30ml),室温搅拌3h,加入饱和nahco3洗涤,并用ch2cl2萃取,合并有机相,无水硫酸镁干燥,过滤,浓缩。硅胶柱层析分离提纯(石油醚:二氯甲烷=2:1)得黄色固体(0.9g,2.5mmol),收率为50%。1hnmr(400mhz,cdcl3)δ7.49(d,j=7.8hz,2h),7.27(d,j=7.8hz,2h),5.98(s,2h),4.80(s,2h),2.55(s,6h),1.38(s,6h).13cnmr(101mhz,cdcl3)δ155.49,143.10,141.89,141.56,134.20,131.48,128.18,127.39,121.22,64.66,14.48.
(2)1,3,5,6-四甲基8-(4(醛基苯基))氟化硼二吡咯(3)的合成:
250ml单口瓶中,加入1,3,5,6-四甲基8-(4(羟甲基苯基))氟化硼二吡咯(0.9g,2.5mmol),活化的mno2(5.4g,62.5mmol)和ch2cl2(150ml),回流12h,反应结束后,硅藻土过滤,收集滤液,浓缩,硅胶柱层析分离提纯(石油醚:二氯甲烷=2:1)得红色固体(0.7g,2.0mmol),收率为80%。1hnmr(400mhz,cdcl3)δ10.14(s,1h),8.03(d,j=7.8hz,2h),7.51(d,j=7.8hz,2h),6.00(s,2h),2.56(s,6h),1.36(s,6h).13cnmr(101mhz,cdcl3)δ191.46,156.26,142.76,141.41,139.69,136.68,130.83,130.34,129.16,121.64,14.63,14.52.
(3)1,3,3-四甲基2-(1,3,5,6-四甲基8-(4(乙烯基苯基))氟化硼二吡咯)-3h-碘化吲哚盐(1)的合成:
100ml两口瓶中加入1,3,5,6-四甲基8-(4(醛基苯基))氟化硼二吡咯(0.5g,1.4mmol))、1,2,3,3-四甲基-3h-碘化吲哚盐(0.4g,1.4mmol)和无水乙醇(60ml),置换成n2体系,加入2滴哌啶,回流12h,浓缩,硅胶柱层析分离提纯(石油醚:二氯甲烷=2:1)得红色固体(0.5g,0.78mmol),收率为56%。1hnmr(400mhz,cdcl3)δ8.36-8.23(m,2h),7.96(d,j=16.3hz,1h),7.62-7.59(m,3h),7.49-7.47(m,2h),5.99(s,2h),4.54(s,3h),2.56(s,6h),1.91(s,6h),1.42(s,6h).13cnmr(101mhz,cdcl3)δ182.66,174.25,156.14,152.78,143.08,142.89,141.53,140.51,139.82,134.37,131.70,130.84,130.43,129.86,129.48,128.94,125.39,122.65,122.01,121.57,115.35,114.66,110.90,105.02,52.92,48.86,37.66,32.77,28.11,26.70,14.88,14.66.
【实施例2】检测氰根离子的荧光探针hb对阴离子的识别性能
1、氰根离子的荧光探针的选择性研究
将hb溶于无水乙醇中配制10-3mol·l-1的储备液;分别配制f─、cl─、br─、i─、no3─、clo4─、hso4─、h2po4─、aco─、cn─的水溶液10-2mol·l-1。在比色皿中加入25μl的hb储备液,2475μl水和乙醇(v/v=1:1)混合溶液,检测紫外吸收光谱和荧光发射光谱,分别加入20μl的离子储备液,此时hb的浓度为10×10-6mol·l-1,阴离子的浓度为受体的8倍,检测紫外吸收光谱和荧光发射光谱(λex=383nm),观察荧光探针hb对各种阴离子的响应。
结果表明,hb在乙醇和水(v/v=1:1)作为溶剂的条件下,在385nm,502nm和545nm处分别有吸收峰,加入cn─后,385nm处的吸收峰消失,在256nm处出现新的吸收峰。而加入其它阴离子,hb的紫外吸收光谱没有明显变化(图1)。在荧光光谱中,以385nm作为激发波长,hb的最大发射波长为515nm,荧光强度非常弱,加入cn─后,515nm处的发射波长明显增强,而加入其它阴离子,hb的发射波长没有明显变化(图2),在紫外灯365nm照射下,加入cn─后出现绿色荧光,而其它阴离子没有变化(图3)。说明该荧光探针可以专一性的检测氰根离子。
2、氰根离子的荧光探针滴定实验
将hb溶于无水乙醇中配制10-3mol·l-1的储备液,在水溶液中配制cn─储备液,浓度为5×10-3mol·l-1.检测时在比色皿中加入25μl的hb储备液,2475μl水和乙醇(v/v=1:1)混合溶液(最终浓度10μmol·l-1),加入cn─储备液0.5μl,摇晃均匀后分别检测其紫外吸收光谱和荧光发射光谱,重复此操作,直至加入6.0当量的氰根离子溶液.
结果表明,hb的紫外吸收光谱受氰根离子浓度的影响(图4),随着氰根离子的逐渐加入,hb在385nm处的吸收峰逐渐降低,在256nm处的吸收波长逐渐增强,直至加入15μmol·l-1cn─时达到平衡。接着测其荧光发射光谱(图5),hb的荧光强度在515nm处很弱,随着氰根离子的加入,荧光强度逐渐增强,直至加入15μmol·l-1cn-时达到平衡。当cn─的浓度为0—10μmol·l-1时,i/i0与cn-的浓度表现出较好的线性关系,拟合得到的线性方程为y=1.8×106x+0.27(r2=0.9931),因此也可以通过荧光法定量检测cn─的浓度(图6)。
3、hb荧光探针对氰根离子最低限的测定
当cn─的浓度为0—10μmol·l-1时,i/i0与cn-的浓度表现出较好的线性关系,拟合得到的线性方程为y=1.8×106x+0.29(r2=0.9931)依据“检测限=3σ/k”可计算hb对cn-的检测限,其中σ为标准平均偏差,k为线性拟合直线的斜率.通过对hb(10μmol·l-1)分别进行15次荧光检测,将得到的测量结果计算标准偏差σ为0.03524,k为1.7×106.通过公式计算可以得出,hb对cn-的检测限为59nm,远低于世界卫生组织对饮用水中的氰根离子的最大规定值1.9μmol·l-1。因此,hb可用于实际水样中氰根离子的测定.
4、抗干扰能力检测
比色皿中分别加入配制好的hb储备液25μl,乙醇和水(v/v=9/1)混合溶液2475μl,使其最终浓度10μmol·l-1,检测紫外吸收光谱和荧光发射光谱,然后加入阴离子储备液(例如氟离子)20μl(cn-除外),充分摇匀,进行紫外吸收光谱和荧光发射光谱检测,最后加入10μl的cn-,摇匀,再次检测紫外吸收光谱和荧光发射光谱,其它每个阴离子重复上述操作。
实验表明,在与其他阴离子共存的情况下,cn-依然可以使hb在385nm处的紫外吸收峰降低,并且可以使hb在515nm处的荧光强度明显增强(图7),因此hb对cn-检测具有很好的抗干扰能力,其他阴离子不会对检测结果带来任何干扰。
5、hb在不同ph值的含水体系中对cn-的检测能力
分别配置柠檬酸-磷酸氢二钠ph=2.2、3.0、4.0、5.0、6.0、7.0、8.0和甘氨酸-氢氧化钠ph=9.0、10.0、10.6的缓冲溶液10mmol·l-1各20ml。在比色皿中加入hb储备液25μl,2475μlph=2.2的缓冲溶液和乙醇(v/v=1/1)混合溶液,20μlcn-储备液,振荡30s,检测荧光发射光谱(测三次,取其平均值)。每个不同的缓冲溶液重复此操作。
如图8所示的实验结果表明,在不同的ph体系中,hb在515nm处的荧光强度很低,基本保持稳定,加入cn-后在ph为5-9范围内,荧光强度明显增强,并保持稳定,从而可以看出hb在ph值5—9范围内可以有效地识别cn-。
6、hb对cn-响应时间
比色皿中分别加入配制好的hb储备液25μl,乙醇和水(v/v=9/1)混合溶液2475μl,使其最终浓度10μmol·l-1,检测荧光发射光谱,加入5μlcn-储备液(10-2mol·l-1),检测荧光发射光谱。振荡,每30s检测一次荧光发射光谱。
如图9所示的结果表明,hb对cn-响应时间非常快,30s后荧光强度不变,达到平衡,因此hb可作为快速检测cn-的荧光传感器。
【实施例3】hb用于实际水样的检测
分别取50ml自来水、湖水和矿泉水于烧杯中,装入样品管中用离心机进离心,离心后收集上层清液。在比色皿中加入hb储备液25μl,2475μl(自来水/乙醇=1/1)混合溶液。振荡,检测荧光发射光谱。向比色皿中加入5μmol·l-1的cn-,振荡,检测荧光发射光谱,重复此操作三次。每种水样重复上述操作。
结果表明,这三种水样中的氰根离子浓度均低于1.9μmol·l-1,加入5μmol·l-1的cn-后,在自来水,湖水和矿泉水中测得cn-的浓度为5.27±0.19μmol·l-1,5.23±0.11μmol·l-1,5.13±0.18μmol·l-1。加标回收率分别为105.46±3.67%,104.05±2.03%,102.56±3.73%。相对标准平均偏差均小于5%。因此hb可有效的用于实际水样中的cn-测定。
【实施例4】hb的cn-检测试纸及应用
在处理过的滤纸上滴加hb的乙醇与水(v/v=1/1)混合溶液(100μmol·l-1)(10μl),使hb分子均匀吸附在滤纸上,自然晾干。分别在滤纸上滴加cn─、f─、cl─、br─、i─、no3─、clo4─、hso4─、h2po4─、aco─的水溶液(200μmol·l-1)(10μl),自然晾干,在紫外灯365nm下观察其颜色变化。此外,取6份吸附hb分子的滤纸,分别滴加不同浓度的cn─(0μmol·l-1,10μmol·l-1,20μmol·l-1,50μmol·l-1,100μmol·l-1,200μmol·l-1)(10μl)。自然晾干,在紫外灯365nm下观察其颜色变化。
如图10所示,在紫外灯365nm照射下,hb没有明显荧光,为紫色,当加入cn─后,可看到黄绿色荧光,而加入其它阴离子则没有颜色变化。如图11所示,当加入不同浓度的cn─时,荧光强度逐渐增强,说明hb可通过试纸检测cn─。
- 还没有人留言评论。精彩留言会获得点赞!