一种复合溶磷菌剂及其制备方法和应用与流程
本发明属于微生物技术领域,具体涉及一种复合溶磷菌剂及其制备方法和应用。
背景技术:
磷是植物生长必需的营养物质之一,对于植物生长至关重要,但是土壤中的大部分有机磷和无机磷却不能直接被植物吸收利用。我国74%的耕地土壤缺磷,且土壤中95%以上的磷为无效磷,造成有效磷资源的极度匮乏。施用磷肥可给植物提供磷素养分,但植物对磷肥的当季利用率一般只有5%~25%,由于耕地长期施用磷肥,大部分磷肥作为无效态在耕地土壤中积累,对生态环境造成影响。
土壤溶磷微生物不但能够促进植物对各种营养元素的吸收,促进植株根系的生长,提高植物对磷的利用率,改善植物营养条件,提高作物产量,增加植株抗病能力,还可改善土壤结构,提高有机质含量,改良盐碱地,对培育和充分发挥土壤生态肥力、保持农业生态环境具有重要作用。因此,土壤溶磷微生物的研究具有良好的发展前景和应用意义。
技术实现要素:
为了解决上述问题,本发明的目的是提供一种复合溶磷菌剂,可以高效的将土壤中的无效磷转换为可供小麦直接吸收的优质磷。
本发明提供了如下的技术方案:
本发明的复合溶磷菌剂,由溶磷菌ws32与溶磷菌p1616混合发酵制成,所述溶磷菌ws32的分类命名为假单胞菌(pseudomonassp.),2017年6月9日保藏在中国典型培养物保藏中心,保藏编号为cctccno:m2017319,保藏单位地址为武汉大学,所述溶磷菌p1616的分类命名为芽孢杆菌(bacillussp.),2017年6月2日保藏在中国典型培养物保藏中心,保藏编号为cctccno:m2017298,保藏单位地址为武汉大学。
本发明菌株形态特征:溶磷菌ws32菌株为革兰氏阴性菌,菌落整齐,呈淡黄色,接触酶试验显示阴性,淀粉酶试验显示阳性;溶磷菌p1616为革兰氏阳性菌,菌落不整齐,呈白色,有芽孢,接触酶试验显示阳性,淀粉酶试验显示阳性。
本发明复合溶磷菌剂为液态复合溶磷菌剂或者固态复合溶磷菌剂。
本发明液态复合溶磷菌剂的制备方法如下,
将溶磷菌ws32和溶磷菌p1616的菌液按1:0.5~2的体积比混合,其中两种菌液中的菌数均在1×108~9×108cfu/ml范围内,然后将混合的菌液以2~5%的接种量接入80~120ml牛肉膏蛋白胨液体培养基中,在25~30℃、120~180r/min的条件下,震荡培养18~48h,即制得液态复合溶磷菌剂。
本发明固态复合溶磷菌剂的制备方法如下,
在上述液态复合溶磷菌剂中加入干燥的泥炭60~180g混匀,即制得固态复合溶磷菌剂。
本发明的液态复合溶磷菌剂中溶磷菌ws32和溶磷菌p1616的总菌数为1×108~9×108cfu/ml。
本发明复合溶磷菌剂在促进小麦的生长、促进小麦对磷素吸收以及降低化肥使用量的应用。
本发明复合溶磷菌剂用于小麦的拌种或包衣或浇根或蘸根。
本发明液态复合溶磷菌剂每亩小麦田施用量为1~4l,固态复合溶磷菌剂每亩小麦田施用量为1~4kg。
ws32的16srrna如seqidno.1所示,p1616的16srrna如seqidno.2所示。
本发明的有益效果是:
1、本发明的ws32和p1616与小麦具有亲和性,可与小麦凝集素发生凝集反应,可在小麦根部长期定居存活,发挥促进小麦生长的作用。
2、本发明的复合菌剂具有强的产有机酸和磷酸酶能力,保证高效溶磷、解磷效果。
3、采用本发明的ws32和p1616制备的液态复合溶磷菌剂或固态复合溶磷菌剂具有显著的溶磷效果,既能溶解难溶态无机磷,又能降解难溶态有机磷,利用ws32和p1616自身的代谢能力将不溶态的无机磷素和有机磷素释放出来,大幅度提高菌液中或土壤中速效性磷的含量。
4、本发明的复合溶磷菌剂使用方法简单,可采用拌种、包衣、浇根、蘸根等方法进行接种。
5、本发明的液态复合溶磷菌剂或固态复合溶磷菌剂的施用剂量低,液态复合溶磷菌剂每亩小麦田施用量仅为1~4l,固态复合溶磷菌剂每亩小麦田施用量仅为1~4kg,与其它每亩小麦田施用量为30~50kg的大剂量的生物肥料产品相比较,本发明可大幅度降低生产成本,节能环保。
附图说明
图1是难溶性无机磷磷酸三钙培养基发酵液中可溶性磷浓度;
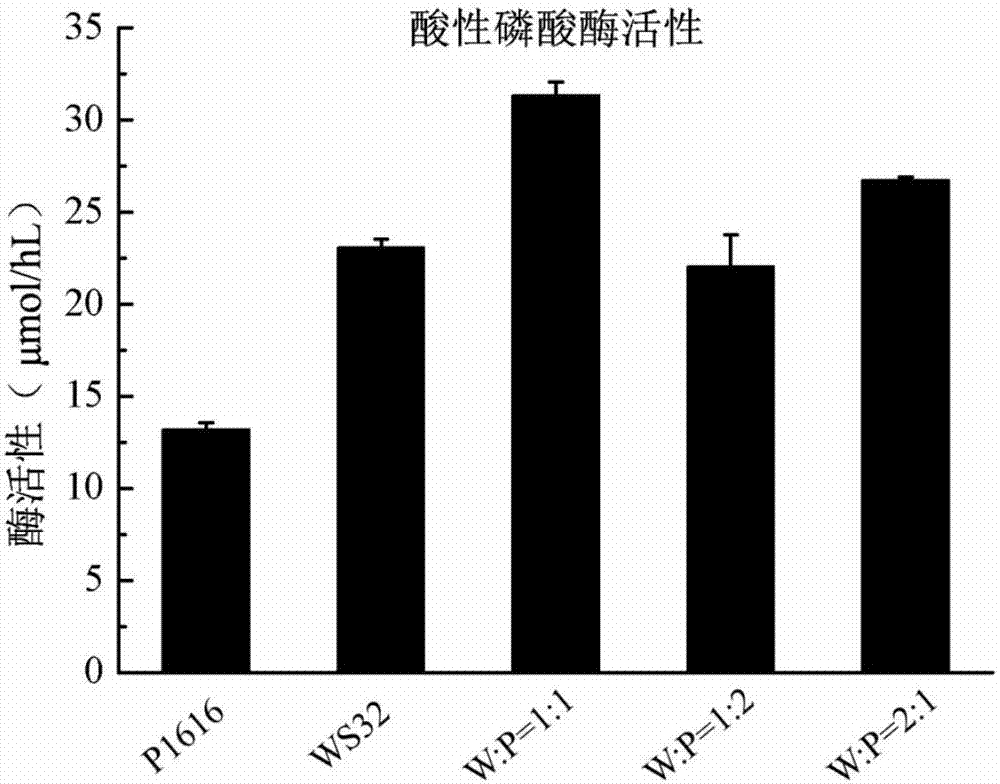
图2是难溶性有机磷植酸钙培养基发酵液中溶磷菌产酸性磷酸酶活性
图3是ws32的菌落图;
图4是p1616的菌落图;
图5是ws32与p1616菌液体积比为1:1的菌落图;
图6是ws32与p1616菌液体积比为1:2的菌落图;
图7是ws32与p1616菌液体积比为2:1的菌落图。
具体实施方式
下面结合具体实施例对本发明做具体说明。
实施例1ws32菌株与p1616菌株的筛选
采用选择培养基结合凝集素筛选法从小麦根际筛选出与小麦具有特异亲和作用的小麦根际溶磷菌29株;选用不同的溶磷培养基,分别添加ca3(po4)2、fepo4、alpo4、cahpo4·2h2o等难溶性无机磷,以及卵磷脂、植酸钙等难溶性有机磷;采用钼锑抗比色法测定各菌株发酵液中可溶性磷的浓度,测定29株菌株对不同形态难溶磷的溶解能力,确定其中5株菌溶磷效果较好。将这5株小麦高效溶磷菌分别以不同比例两两混合培养,测定其溶磷能力,发现其中ws32菌株与p1616菌株溶磷效果最佳,将两株菌经16srrna分子测序确定ws32为假单胞菌属,p1616为芽孢杆菌属。
实施例2复合溶磷菌剂的溶磷能力
将ws32和p1616菌液分别按体积比1:0、0:1、2:1、1:1、1:2混合,其中两种菌液中的菌数均在1×108~9×108cfu/ml范围内,以3%的接种量接入磷酸三钙培养基,三角瓶培养,培养条件为160r/min、28℃、培养9天;采用钼锑抗比色法每天定时测定发酵液中可溶性磷的浓度,结果如图1所示,图1中,w:p表示ws32:p1616,复合溶磷菌较单菌株的溶磷效果大大提高。
实施例3复合溶磷菌剂分泌有机酸和磷酸酶能力
(1)溶磷菌解无机磷原理为分泌有机酸,溶解土壤中难溶态无机磷为可溶态磷,供植物吸收利用。
采用磷酸三钙培养基,高效液相色谱法测有机酸种类和浓度。液体摇瓶培养7d,取菌液1ml,离心,再经0.22μm滤膜真空抽滤后上液相色谱。分离条件:色谱柱为hypersilc18(250nm×4.6mmid,5μm),流动相为0.02mol/l的kh2po4缓冲溶液-甲醇溶液(99%:1%),用1mol/l磷酸调节ph至2.60,紫外检测波长210nm,进样量10μl,流速0.5ml/min,柱温30℃,得到表1。
由表1可见,复合溶磷菌在磷酸三钙培养基中产生的有机酸种类更多,浓度更大,有利于对难溶态无机磷的溶解。
表1高效液相色谱法对菌株分泌有机酸种类和浓度的测定
(2)溶磷菌解有机磷原理为产生磷酸酶,通过磷酸酶的酶降解作用,将土壤中的难溶性有机磷降解为有效磷。
对菌液中磷酸酶活性的测定采用植酸钙培养基,磷酸苯二钠法测定。结果如图2所示。图2中,w:p表示ws32:p1616,复合溶磷菌酸性磷酸酶活性最高,这加速了植酸钙的分解,促进磷素释放,从而提高小麦磷素营养。
实施例4液态溶磷菌剂的制备以及用于小麦的盆栽实验
液态溶磷菌剂包括液态复合溶磷菌剂、液态ws32溶磷菌剂和液态p1616溶磷菌剂。
液态复合溶磷菌剂的制备
将ws32和p1616菌液分别按体积比2:1、1:1、1:2混合,其中两种菌液中的菌数均在1×108~9×108cfu/ml范围内,并以3%的接种量接入100ml牛肉膏蛋白胨液体培养基中,在28℃、160r/min条件下,震荡培养30h,即制得液态复合溶磷菌剂。
液态ws32溶磷菌剂的制备
将ws32(菌液中的菌数在1×108~9×108cfu/ml范围内)以3%的接种量接入100ml牛肉膏蛋白胨液体培养基中,在28℃、160r/min条件下,震荡培养30h,即制得液态ws32溶磷菌剂。
液态p1616溶磷菌剂的制备
将p1616(菌液中的菌数在1×108~9×108cfu/ml范围内)以3%的接种量接入100ml牛肉膏蛋白胨液体培养基中,在28℃、160r/min条件下,震荡培养30h,即制得液态p1616溶磷菌剂。
液态溶磷菌剂用于小麦的盆栽实验
小麦种子催芽,取适量小麦种子用水冲洗一次,然后用70%酒精浸泡3min消毒并去除干瘪种子,再用无菌水冲洗5次,最后用适量的水浸泡,放于25℃培养箱中催芽,待种子露白即可播种。小麦盆栽设3个处理组和1个对照组:即施液态复合溶磷菌剂处理组(ws32和p1616菌液体积比分别为2:1,1:1,1:2)、施液态ws32溶磷菌剂处理组、施液态p1616溶磷菌剂处理组和施空白培养基对照组。每个处理组三个重复样。处理组每盆接种液态溶磷菌剂5ml,对照组只接进5ml空白培养基,待苗出齐后每盆定苗5株,日常管理水肥,于125d采收,测定小麦株高、鲜重、干重、地上部分叶片磷含量及盆栽后土壤的磷含量。
试验结果如表2所示:
液态复合溶磷菌剂接种的小麦株高、鲜重、干重、土壤速效磷含量、叶片全磷含量分别较未接液态菌剂的对照增加6.1%~25.6%、6.9%~8.9%、15.1%~19.3%、8.3%~14.8%、37.8%~49.7%,各参数较单菌剂接种的小麦也有较大幅度提高。证明了施用液态复合溶磷菌剂能够提高小麦对磷的吸收,促进小麦生长。
表2液态溶磷菌剂用于小麦的盆栽实验
实施例5固态溶磷菌剂的制备以及用于小麦的盆栽实验
固态溶磷菌剂包括固态复合溶磷菌剂、固态ws32溶磷菌剂和固态p1616溶磷菌剂。
固态复合溶磷菌剂的制备
将ws32和p1616菌液分别按体积比2:1、1:1、1:2混合,其中两种菌液中的菌数均在1×108~9×108cfu/ml范围内,并以3%的接种量接入100ml牛肉膏蛋白胨液体培养基中,在28℃、160r/min条件下,震荡培养30h,加入干燥的泥炭150g混匀,即制得固态复合溶磷菌剂。
固态ws32溶磷菌剂的制备
将ws32(菌液中的菌数在1×108~9×108cfu/ml范围内)以3%的接种量接入100ml牛肉膏蛋白胨液体培养基中,在28℃、160r/min条件下,震荡培养30h,加入干燥的泥炭150g混匀,即制得固态ws32溶磷菌剂。
固态p1616溶磷菌剂的制备
将p1616(菌液中的菌数在1×108~9×108cfu/ml范围内)以3%的接种量接入100ml牛肉膏蛋白胨液体培养基中,在28℃、160r/min条件下,震荡培养30h,加入干燥的泥炭150g混匀,即制得固态p1616溶磷菌剂。
固态溶磷菌剂用于小麦的盆栽实验
本实施例的小麦的盆栽实验与实施例4的小麦的盆栽实验不同之处在于,实施例4的小麦的盆栽实验“处理组每盆接种液态溶磷菌剂5ml,对照组只接进5ml空白培养基”,本实施例的小麦的盆栽实验“每盆接种固态溶磷菌剂5g,对照组接入经121℃、20min灭活处理的固态溶磷菌剂5g”。
试验结果如表3所示
固态复合菌剂接种的小麦株高、鲜重、干重、叶片全磷含量分别较未接菌剂的对照增加6.3%~12.7%、7.6%~9.3%、13.1%~16.7%、42.5%~52.9%,各参数较单菌剂接种的小麦也有较大幅度提高。证明了施用固态复合溶磷菌剂能够提高小麦对磷的吸收,促进小麦生长。
表3固态溶磷菌剂用于小麦的盆栽实验
以上所述仅为本发明的优选实施例而已,并不用于限制本发明,尽管参照前述实施例对本发明进行了详细的说明,对于本领域的技术人员来说,其依然可以对前述各实施例所记载的技术方案进行修改,或者对其中部分技术特征进行等同替换。凡在本发明的精神和原则之内,所作的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
sequencelisting
<110>安徽农业大学
<120>一种复合溶磷菌剂及其制备方法和应用
<130>2
<160>2
<170>patentinversion3.3
<210>1
<211>1406
<212>dna
<213>假单胞菌(pseudomonassp.)
<400>1
cacatgcaagtcgagcggtagagagaagcttgcttctcttgagagcggcggacgggtgag60
taatgcctaggaatctgcctggtagtgggggataacgttcggaaacggacgctaataccg120
catacgtcctacgggagaaagcaggggaccttcgggccttgcgctatcagatgagcctag180
gtcggattagctagttggtgaggtaatggctcaccaaggcgacgatccgtaactggtctg240
agaggatgatcagtcacactggaactgagacacggtccagactcctacgggaggcagcag300
tggggaatattggacaatgggcgaaagcctgatccagccatgccgcgtgtgtgaagaagg360
tcttcggattgtaaagcactttaagttgggaggaagggttgtagattaatactctgcaat420
tttgacgttaccgacagaataagcaccggctaactctgtgccagcagccgcggtaataca480
gagggtgcaagcgttaatcggaattactgggcgtaaagcgcgcgtaggtggtttgttaag540
ttggatgtgaaatccccgggctcaacctgggaactgcattcaaaactgactgactagagt600
atggtagagggtggtggaatttcctgtgtagcggtgaaatgcgtagatataggaaggaac660
accagtggcgaaggcgaccacctggactaatactgacactgaggtgcgaaagcgtgggga720
gcaaacaggattagataccctggtagtccacgccgtaaacgatgtcaactagccgttgga780
agccttgagcttttagtggcgcagctaacgcattaagttgaccgcctggggagtacggcc840
gcaaggttaaaactcaaatgaattgacgggggcccgcacaagcggtggagcatgtggttt900
aattcgaagcaacgcgaagaaccttaccaggccttgacatccaatgaactttctagagat960
agattggtgccttcgggaacattgagacaggtgctgcatggctgtcgtcagctcgtgtcg1020
tgagatgttgggttaagtcccgtaacgagcgcaacccttgtccttagttaccagcacgtt1080
atggtgggcactctaaggagactgccggtgacaaaccggaggaaggtggggatgacgtca1140
agtcatcatggcccttacggcctgggctacacacgtgctacaatggtcggtacagagggt1200
tgccaagccgcgaggtggagctaatcccataaaaccgatcgtagtccggatcgcagtctg1260
caactcgactgcgtgaagtcggaatcgctagtaatcgcgaatcagaatgtcgcggtgaat1320
acgttcccgggccttgtacacaccgcccgtcacaccatgggagtgggttgcaccagaagt1380
agctagtctaaccttcgggaggacgg1406
<210>2
<211>1453
<212>dna
<213>芽孢杆菌(bacillussp.)
<400>2
gccgtgcggggtgctataatgcagtcgagcgaactgattagaagcttgcttctatgacgt60
tagcggcggacgggtgagtaacacgtgggcaacctgcctgtaagactgggataacttcgg120
gaaaccgaagctaataccggataggatcttctccttcatgggagatgattgaaagatggt180
ttcggctatcacttacagatgggcccgcggtgcattagctagttggtgaggtaacggctc240
accaaggcaacgatgcatagccgacctgagagggtgatcggccacactgggactgagaca300
cggcccagactcctacgggaggcagcagtagggaatcttccgcaatggacgaaagtctga360
cggagcaacgccgcgtgagtgatgaaggctttcgggtcgtaaaactctgttgttagggaa420
gaacaagtacgagagtaactgctcgtaccttgacggtacctaaccagaaagccacggcta480
actacgtgccagcagccgcggtaatacgtaggtggcaagcgttatccggaattattgggc540
gtaaagcgcgcgcaggcggtttcttaagtctgatgtgaaagcccacggctcaaccgtgga600
gggtcattggaaactggggaacttgagtgcagaagagaaaagcggaattccacgtgtagc660
ggtgaaatgcgtagagatgtggaggaacaccagtggcgaaggcggctttttggtctgtaa720
ctgacgctgaggcgcgaaagcgtggggagcaaacaggattagataccctggtagtccacg780
ccgtaaacgatgagtgctaagtgttagagggtttccgccctttagtgctgcagctaacgc840
attaagcactccgcctggggagtacggtcgcaagactgaaactcaaaggaattgacgggg900
gcccgcacaagcggtggagcatgtggtttaattcgaagcaacgcgaagaaccttaccagg960
tcttgacatcctctgacaactctagagatagagcgttccccttcgggggacagagtgaca1020
ggtggtgcatggttgtcgtcagctcgtgtcgtgagatgttgggttaagtcccgcaacgag1080
cgcaacccttgatcttagttgccagcatttagttgggcactctaaggtgactgccggtga1140
caaaccggaggaaggtggggatgacgtcaaatcatcatgccccttatgacctgggctaca1200
cacgtgctacaatggatggtacaaagggctgcaagaccgcgaggtcaagccaatcccata1260
aaaccattctcagttcggattgtaggctgcaactcgcctacatgaagctggaatcgctag1320
taatcgcggatcagcatgccgcggtgaatacgttcccgggccttgtacacaccgcccgtc1380
acaccacgagagtttgtaacacccgaagtcggtggagtaaccgtaaggagctagccgcct1440
aagggacagagtg1453
- 还没有人留言评论。精彩留言会获得点赞!