一种二元羧酸咪唑鎓盐的合成方法与流程
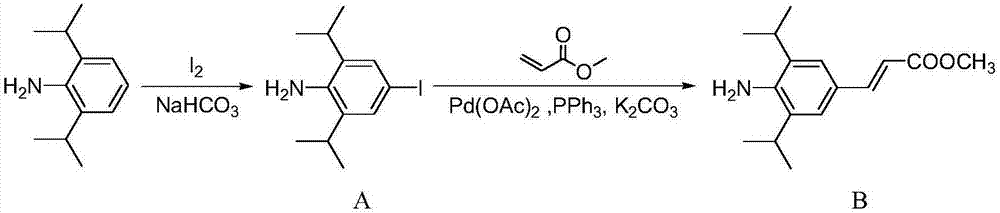
本发明涉及一种二元羧酸咪唑鎓盐的合成方法。
背景技术:
金属-有机框架(metal-organic frameworks,MOFs)是指金属离子(或金属离子簇)和有机配体在给定条件下,多组分体系中不同组分(构筑模块)之间,通过配位键、超分子作用等的导向,进行自组装而形成的三维结构的周期性网络结构的聚合物,又被称为配位聚合物。含羧基类配体之所以一直兴盛不衰是由其自身的特点和优势所决定的:(1)羧基配位能力很强,能与各种金属配位形成配位聚合物。(2)羧基具有丰富的配位方式,大致可分为三类,即单齿配位、螯合配位和桥联配位。(3)羧基去质子化的不同可形成不同的结构。芳香二元羧酸(如苯二酸类、联苯二酸类和萘二酸等)由于具有两个处于邻位、间位或对位的羧基,在空间上具有较好的拓展性,而具有刚性结构的二元羧酸可做为桥联配体支撑网络结构,因而常常被用来设计、合成金属有机拓扑的结构。如Yaghi Yaghi研究组以对苯二甲酸(1,4-BDC)为配体合成出了孔径为的MOF-5,(Zn O4(BDC)3·(DMF)8·C6H5Cl),实现了晶态微孔材料向晶态介孔材料的重要进展。MOF-5具有CaB6拓扑结构,是以八面体次级结构单元(ZnO4(CO2)6簇)作为6-连接的节点(node),1,4-BDC配体作为链接(linker)将节点桥连在一起形成的三维立方网络结构。MOF-5在空气中可稳定存在到300℃,在客体分子完全除去后,晶体仍能够保持完好。法国科学家Férey报道用对苯二甲酸和硝酸镉及氢氟酸为原料水热合成了MIL-101,Cr3F(H2O)2O[(O2C)-C6H4-(CO2)]3·nH2O(n-25)。MIL-101为具有MTN拓扑类型的超大孔穴的类分子筛,其单胞体积分别化合物的结构都是建立在三核Cr簇(Cr-SBU)的八面体建筑单元和对苯二甲酸相连接,MIL-101中四个Cr-SBU与六个对苯二甲酸连接成一个超四面体,再通过共顶点同时形成五边形与六边的笼。值得一提的是MIL-101结构可以空气中稳定到275℃,在失去客体后其骨架仍保持原来的完全性。同时MIL-101的比表面积高达5900m2g-1,具有较强的吸附能力。
延长的刚性二元羧酸配体通常能得到结构新颖、比表面积大的多微孔MOFs材料,并能改变微孔结构,使其微孔内电子环境得到优化从而提高上述应用性能,因此,设计合成结构新颖的延长二元羧酸配体并应用于MOFs材料的合成已成为当今研究的热点之一。然而,大尺寸的刚性二元羧酸化合物合成比较困难,特别是可作为N-杂卡宾前体的二元羧酸咪唑鎓盐化合物,因此本发明中所涉及的结构新颖的1,3-双[(4-羧基乙烯基-2,6-二异丙基)苯基]氯化咪唑鎓盐是一种具有巨大潜在应用价值的有机配体。目前尚无文献报道该化合物。
技术实现要素:
本发明的目的是提供一种合成成本低、产率高、产品纯度高的新型1,3-双[(4-羧基乙烯基-2,6-二异丙基)苯基]氯化咪唑鎓盐的合成方法。
本发明的一种二元羧酸咪唑鎓盐的合成方法,合成步骤为:
(i)以2,6-二异丙基苯胺为原料,加入一定量碳酸氢钠,加入甲醇作为溶剂,加入碘的二氯甲烷溶液,摩尔比2,6-二异丙基苯胺:碘:碳酸氢钠为1:1.1~1.5:2.5~3.5,2,6-二异丙基苯胺与甲醇的用量比是1毫摩:3~6毫升,2,6-二异丙基苯胺与二氯甲烷的用量比是1毫摩:1.5~2.5毫升。加完后在20~30℃反应10~15小时,反应结束将固体过滤,加二氯甲烷洗固体,真空浓缩滤液,加50~80mL饱和硫代硫酸钠溶液继续搅拌2小时,加二氯甲烷萃取(30~60mL×3),合并有机相,无水硫酸镁干燥,过滤,真空减压滤液得到化合物A:4-碘-2,6-二异丙基苯胺;
(ⅱ)在氩气或氮气保护下,在250mL三口瓶中分别加入4-碘-2,6-二异丙基苯胺、丙烯酸甲酯、碳酸钾、三苯基膦、四丁基溴化铵和一定量的溶剂DMF,摩尔比4-碘-2,6-二异丙基苯胺:丙烯酸甲酯:碳酸钾:三苯基膦:四丁基溴化铵为1:5.0~7.0:2.0~4.0:0.1~0.3:4~6,4-碘-2,6-二异丙基苯胺与溶剂的比为1毫摩:5.0~15.0毫升。加入一定量的钯盐作为催化剂,90℃反应30~50小时,反应结束后倒入50mL冰水中析出沉淀,加少量的盐酸淬灭催化剂,抽滤得到大量白色固体,加20~40mL水稀释,二氯甲烷萃取(40~70mL×3),收集有机相并用无水亚硫酸钠对其进行除水处理,过滤,蒸出二氯甲烷溶剂得粗产物,最后以二氯甲烷和石油醚按体积比为10:0.8~1.2的混合溶剂为洗脱剂用柱色谱法分离提纯得到化合物B:3,5-二异丙基-4-氨基-苯丙烯酸甲酯;
(ⅲ)3,5-二异丙基-4-氨基-苯丙烯酸甲酯、乙二醛和乙酸按摩尔比1:0.48~0.52:0.08~0.12混合后溶于一定溶剂中,3,5-二异丙基-4-氨基-苯丙烯酸甲酯与溶剂的用量比是1毫摩:8.0~15.0毫升,在20~30℃反应20~30小时,反应结束后过滤,粗产物用10~30mL无水甲醇重结晶纯化3次,过滤、干燥得化合物C:1,4-双[(4-甲氧羰基乙烯基-2,6-二异丙基)苯基]-1,4-二氮杂-1,3-丁二烯;
(ⅳ)在250mL三口瓶中分别加入1,4-双[(4-甲氧羰基乙烯基-2,6-二异丙基)苯基]-1,4-二氮杂-1,3-丁二烯、无水氯化锌、多聚甲醛和一定量的盐酸,摩尔比1,4-双[(4-甲氧羰基乙烯基-2,6-二异丙基)苯基]-1,4-二氮杂-1,3-丁二烯:无水氯化锌:多聚甲醛:盐酸为1:0.8~1.2:2.5~4.0:1~2,1,4-双[(4-甲氧羰基乙烯基-2,6-二异丙基)苯基]-1,4-二氮杂-1,3-丁二烯与溶剂四氢呋喃的比为1毫摩:20.0~40.0毫升。70℃反应4~8小时,反应结束蒸出四氢呋喃,加20~40mL乙酸乙酯和水的混合溶剂(体积比为1:1),直至产生大量固体,过滤,用冷乙酸乙酯洗涤粗产物,得到纯的化合物D:1,3-双[(4-甲氧羰基乙烯基-2,6-二异丙基)苯基]氯化咪唑鎓盐;
(V)将1,3-双[(4-甲氧羰基乙烯基-2,6-二异丙基)苯基]氯化咪唑鎓盐和LiOH按摩尔比1:10~30加入1,4-二氧六环和水的混合溶剂中,1,4-二氧六环与水的体积比为3~5:1,95℃回流8~12小时,蒸除过量1,4-二氧六环,加水稀释,加入过量的稀HCl酸化至pH=1,析出白色固体,真空干燥得最终化合物E:1,3-双[(4-羧基乙烯基-2,6-二异丙基)苯基]氯化咪唑鎓盐。
所述的一种二元羧酸咪唑鎓盐的合成方法,其特征在于:制备A时,摩尔比2,6-二异丙基苯胺:碘:碳酸氢钠为1:1.1~1.5:2.5~3.5。
所述的一种二元羧酸咪唑鎓盐的合成方法,其特征在于:制备A以甲醇和二氯甲烷为混合溶剂,2,6-二异丙基苯胺与甲醇的用量比是1毫摩:3~6毫升,2,6-二异丙基苯胺与二氯甲烷的用量比是1毫摩:1.5~2.5毫升。在20~30℃反应10~15小时。
所述的一种二元羧酸咪唑鎓盐的合成方法,其特征在于:制备化合物A时,粗产物中加入50~80mL饱和硫代硫酸钠溶液继续搅拌2小时,加二氯甲烷萃取(30~60mL×3),合并有机相,无水硫酸镁干燥。
所述的一种二元羧酸咪唑鎓盐的合成方法,其特征在于:制备化合物B时,摩尔比A:丙烯酸甲酯:碳酸钾:三苯基膦:四丁基溴化铵为1:5.0~7.0:2.0~4.0:0.1~0.3:4~6。需加150mL DMF作溶剂。纯化B用二氯甲烷和石油醚按体积比为10:0.8~1.2的混合溶剂为洗脱剂。
所述的一种二元羧酸咪唑鎓盐的合成方法,其特征在于:制备化合物B使用的催化剂为醋酸钯,用量为B的物质的量的3~7%,反应需在无氧条件下进行。
所述的一种二元羧酸咪唑鎓盐的合成方法,其特征在于:制备化合物C时,摩尔比B:乙二醛:乙酸为1:0.48~0.52:0.08~0.12,B与溶剂的用量比是1毫摩:5.0~15.0毫升。
所述的一种二元羧酸咪唑鎓盐的合成方法,其特征在于:制备化合物C时,纯化C用10~30mL无水甲醇重结晶3次。
所述的一种二元羧酸咪唑鎓盐的合成方法,其特征在于:制备化合物D时,摩尔比C:无水氯化锌:多聚甲醛:盐酸为1:0.8~1.2:2.5~4.0:1~2。C与溶剂的比为1毫摩:20.0~40.0毫升。70℃反应4~8小时。
所述的一种二元羧酸咪唑鎓盐的合成方法,其特征在于:制备化合物D时,加20~40mL乙酸乙酯和水的混合溶剂(体积比为1:1)纯化D。
所述的一种二元羧酸咪唑鎓盐的合成方法,其特征在于:制备化合物E时,D和LiOH按摩尔比1:50~70,溶剂1,4-二氧六环和水的混合溶剂中,体积比为2~4:1,酸化至pH=1。
用本方法合成结构新颖的1,3-双[(4-羧基乙烯基-2,6-二异丙基)苯基]氯化咪唑鎓盐的有益效果是:延长的刚性二元羧酸类配体广泛应用于MOFs材料的合成中,这类材料通常具有有序的孔道结构、大的比表面积,使这类材料在气体储藏与分离、化学传感、催化及药物缓释等不同领域具有潜在应用。延长的刚性二元羧酸咪唑鎓盐配体通常能得到结构新颖、比表面积大的多微孔MOFs材料,并能改变微孔结构,使其气孔内电子环境得到优化从而提高上述应用性能。由于1,3-双[(4-羧基乙烯基-2,6-二异丙基)苯基]氯化咪唑鎓盐可作为N-杂卡宾的前体,使用该配体合成的MOFs材料可通过后合成修饰的方法制备含N-杂卡宾及N-杂卡宾金属配合物的MOFs材料,这类材料将会产生更加广泛的应用,特别是在非均相催化领域。因此,设计合成结构新颖的延长二元羧酸咪唑鎓盐配体并应用于MOFs材料的合成已成为当今研究的热点之一。然而,大尺寸的刚性二元羧酸咪唑鎓盐合成比较困难。因此,用本方法合成结构新颖的1,3-双[(4-羧基乙烯基-2,6-二异丙基)苯基]氯化咪唑鎓盐是一种具有巨大潜在应用价值的二元羧酸咪唑鎓盐配体。
附图说明
图1本发明中目标化合物E的结构式示意图。
图2本发明中化合物A和B的合成示意图。
图3本发明中化合物C的合成示意图。
图4本发明中化合物D的合成示意图。
图5本发明中化合物E的合成示意图。
具体实施方式
本发明的1,3-双[(4-羧基乙烯基-2,6-二异丙基)苯基]氯化咪唑鎓盐的合成方法,合成步骤为:
以2,6-二异丙基苯胺,单质碘为原料经碘代反应生成4-碘-2,6-二异丙基苯胺(A),A与与丙烯酸甲酯经Heck偶联反应生成3,5-二异丙基-4-氨基-苯丙烯酸甲酯(B),合成路线如图2所示。B与乙二醛在乙酸催化下生成1,4-双[(4-甲氧羰基乙烯基-2,6-二异丙基)苯基]-1,4-二氮杂-1,3-丁二烯(C),合成路线如图3所示。C与多聚甲醛在无水氯化锌和盐酸催化下环化生成1,3-双[(4-甲氧羰基乙烯基-2,6-二异丙基)苯基]氯化咪唑鎓盐(D),合成路线如图4所示。D最后水解得到目标化合物1,3-双[(4-羧基乙烯基-2,6-二异丙基)苯基]氯化咪唑鎓盐(E),合成路线如图5所示。
具体实施例如下:
(i)如图2所示:在500mL圆底烧瓶依次加入2,6-二异丙基苯胺(10mL,53mmol)、碳酸氢钠(13.4g,110mmol)和甲醇(200mL)。随后加入碘(14.8g,58mmol)的二氯甲烷溶液(150mL),室温搅拌12小时。然后将固体过滤,二氯甲烷洗涤滤饼,真空浓缩滤液得深橙色油状粗产物,加入60mL硫代硫酸钠饱和溶液,室温搅拌2h。二氯甲烷萃取3次(40mL×3),合并有机层,无水MgSO4干燥,减压浓缩得棕色油状物A(14g),产率88%。
化合物A核磁1H NMR、13C NMR和高分辨质谱数据:1H NMR(400MHz,CDCl3)δ7.31(s,2H),3.79(s,2H),2.86(sept,J=6.8Hz,2H),1.27(d,J=6.8Hz,12H).13C NMR(101MHz,CDCl3)δ140.10,135.02,131.72,81.18,27.92,22.31。HRMS(ESI),C12H18IN,实测值(计算值),m/z:304.1829[M+H]+(304.1825)。
(ⅱ)如图2所示:在250mL三口瓶中分别加入化合物A(7.2g,24mmol)、丙烯酸甲酯(12g,36eq)、K2CO3(9g,66mmol)、PPh3(0.8g,3mmol)和四丁基溴化铵(36g,120mmol),加入150mL的DMF作为溶剂,通入Ar 10min后,加Pd(OAc)2(0.12g,5.0mmol%),120℃反应48h,反应结束后倒入150mL冰水中析出沉淀,加少量的盐酸淬灭催化剂,抽滤得到大量黄色固体,加30mL水稀释,二氯甲烷萃取(60mL×3)收集有机层,无水Na2SO3干燥、过滤,蒸出二氯甲烷溶剂得粗产物,干燥后经硅胶柱层析(洗脱剂:二氯甲烷/石油醚=10:1)纯化,得淡白色粉末B(5.6g),产率90%。熔点:115-116℃。
化合物B核磁1H NMR、13C NMR和高分辨质谱数据:1H NMR(400MHz,CDCl3)δ7.66(d,J=15.8Hz,1H),7.24(s,2H),6.29(dd,J=15.9,1.0Hz,1H),3.79(d,J=1.0Hz,3H),2.89(dt,J=13.5,6.7Hz,2H),1.29(dd,J=6.8,0.9Hz,12H).13C NMR(101MHz,CDCl3)δ168.22,146.25,142.97,132.21,124.32,123.52,112.62,51.38,27.87,22.24。HRMS(ESI),C16H23NO2,实测值(计算值),m/z:262.3587[M+H]+(262.3593)。
(ⅲ)如图3所示:在250mL圆底烧瓶依次加入化合物B(3.6g,14mmol)、乙二醛(40%,0.8mL,7mmol)、乙酸(0.08mL)和150mL甲醇,室温下搅拌24h,过滤分离固体,20毫升冷甲醇洗涤滤饼,粗产物用20无水甲醇重结晶3次得黄色晶体C(3.2g),产率85%。熔点:187-189℃。
化合物C核磁1H NMR、13C NMR和高分辨质谱数据:1H NMR(400MHz,CDCl3)δ8.08(s,2H),7.71(d,J=16.0Hz,2H),7.35(s,4H),6.44(d,J=16.0Hz,2H),3.82(s,6H),2.92(dt,J=13.5,6.7Hz,4H),1.22(d,J=6.8Hz,24H).13C NMR(101MHz,CDCl3)δ167.58,162.74,149.85,145.12,137.38,131.28,123.38,116.38,51.61,28.08,23.20。HRMS(ESI),C34H44N2O4,实测值(计算值),m/z:545.7248[M+H]+(545.7242)。
(ⅳ)如图4所示:在250mL圆底烧瓶依次加入化合物C(2.7g,4mmol)、无水氯化锌(593mg,4mmol)和100mL四氢呋喃,在70℃搅拌5min,逐滴加入多聚甲醛(393mg,13mmol)的盐酸溶液(4M在二氧六环中,1.65mL,6.5mmol),继续在70℃反应5h,浓缩滤液,加30mL乙酸乙酯和水(v/v=1:1)的混合液直至有固体析出,过滤、干燥得白色粉末D(2g),产率88%。熔点:264-265℃。
化合物D核磁1H NMR、13C NMR和高分辨质谱数据:1H NMR(400MHz,DMSO-d6)δ10.30(s,1H),8.58(s,2H),7.89(s,4H),7.78(d,J=16.1Hz,2H),6.97(d,J=16.1Hz,2H),3.75(s,6H),2.32(dt,J=13.5,6.7Hz,4H),1.28(d,J=6.7Hz,12H),1.17(d,J=6.8Hz,12H).13C NMR(101MHz,DMSO-d6)δ166.94,146.02,143.59,139.68,137.86,131.51,126.64,125.05,120.98,52.09,29.20,24.38,23.36。HRMS(ESI),C35H45ClN2O4[M+H]+,实测值(计算值),m/z:594.1951(594.1958)。
(V)如图5所示:在250mL的圆底烧瓶里依次加入化合物D(1.0g,1.7mmol)、LiOH(5.0g,208mmol),加入60mL 1,4-二氧六环和20mL水,95℃反应12h,蒸出1,4-二氧六环,加入适量的水溶解羧酸钠盐,过滤,滤液中加稀HCl酸化至pH=1,析出沉淀,静置,倾倒上层清液,抽滤、水洗干燥得白色粉末E(0.9g),产率98%。熔点:>300℃。
化合物E核磁1H NMR、13C NMR和高分辨质谱数据::1H NMR(400MHz,DMSO-d6)δ12.20(s,2H),10.31(s,1H),8.56(s,2H),7.88(s,4H),7.76(d,J=16.1Hz,2H),6.98(d,J=16.1Hz,2H),2.34(dt,J=13.5,6.7Hz,4H),1.26(d,J=6.7Hz,12H),1.18(d,J=6.8Hz,12H).13C NMR(101MHz,DMSO-d6)δ166.95,146.04,143.57,139.66,137.88,131.54,126.62,125.07,120.96,29.20,24.38,23.36。HRMS(ESI),C33H41ClN2O4[M-H]+,实测值(计算值),m/z:564.1429(564.1426)。
以上所述,仅是本发明的较佳实施例而已,并非对本发明作任何形式上的限制,任何未脱离本发明技术方案内容,依据本发明的技术实质对以上实施例所作的任何简单修改、等同变化与修饰,均仍属于本发明技术方案的范围内。
- 还没有人留言评论。精彩留言会获得点赞!