一种吡啶类双季铵盐表面活性剂及其制备方法和应用与流程
本发明涉及一种吡啶类双季铵盐表面活性剂及其制备方法和应用,属于表面活性剂
技术领域:
。
背景技术:
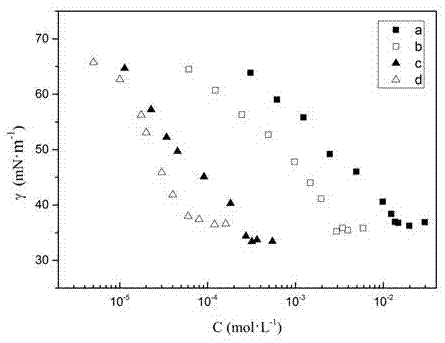
表面活性剂被喻为“工业味精”,由于其具有洗涤、润湿或抗黏、乳化或破乳、起泡或消泡、增溶、分散、防腐、抗静电等功能,被广泛应用于国民经济发展的各个领域。随着科技和经济的快速发展,传统的表面活性剂已经不能满足人们生产与生活的需要,对表面活性剂行业的要求越来越高。双子表面活性剂由于其具有较低的临界胶束浓度、良好的水溶性、较好的起泡性和乳化性等优点,备受相关领域科研人员的关注。尤其是含杂环的阳离子双子表面活性剂由于杂环头基的存在,使其具有许多新性能,在化学催化、医药学研究、化学分离和表面改性等方面都有潜在的应用。目前,许多含咪唑、吡啶、噻唑、喹啉、四氢吡咯和六氢吡啶等杂环的阳离子双子表面活性剂已经被报道,但大多数合成工艺比较复杂,仍处在小试规模,因此,开发具有新颖结构的双子表面活性剂及其性能研究一直是该研究领域的热点。技术实现要素:本发明旨在提供一种吡啶类双季铵盐表面活性剂及其制备方法和应用,该方法制备简单、绿色环保。该表面活性剂对大肠杆菌有很好的抑菌性能。本发明提供了一种吡啶类双季铵盐表面活性剂,具有如下结构式:其中r代表碳数为8、10、12或14的长链烷基。上述的吡啶类双季铵盐表面活性剂,以3-氨基吡啶为起始原料,与丙二酸二乙酯反应得到n,n'-二(3-吡啶基)丙二酰胺,再与溴代烷烃在无溶剂条件下反应制得吡啶类双季铵盐表面活性剂。其制备过程的反应式如下:本发明提供了上述吡啶类双季铵盐表面活性剂的制备方法,包括如下步骤:(1)制备n,n'-二(3-吡啶基)丙二酰胺:将丙二酸二乙酯和3-氨基吡啶加到n,n-二甲基甲酰胺中,加热到140~150℃反应6~7小时,冷却,过滤,用乙酸乙酯洗涤得n,n'-二(3-吡啶基)丙二酰胺,其中丙二酸二乙酯、3-氨基吡啶与n,n-二甲基甲酰胺的用量比例为:1mmol:3~5mmol:0.4~0.5ml;(2)将n,n'-二(3-吡啶基)丙二酰胺和8~10倍摩尔量的溴代烷烃加入反应瓶中,加热到110~120℃反应5~7小时,冷却,过滤,用丙酮重结晶得吡啶类双季铵盐表面活性剂。进一步地,步骤(1)中所述的加热到140~150℃的方法是:给反应装置安装分水器,在反应过程中用分水器分离出反应生成的低沸点的乙醇,反应温度才能达到140~150℃。本发明所得的吡啶类双季铵盐表面活性剂具有良好的表面活性。采用悬滴法测定表面活性剂的表面张力的方法,评价了该吡啶类双季铵盐表面活性剂的表面活性性能。实验结果显示:该吡啶类双季铵盐表面活性剂的cmc低于传统表面活性剂正辛基三甲基溴化铵1~3个数量级,γcmc为30~39mn·m-1。本发明提供了上述吡啶类双季铵盐表面活性剂作为抑菌剂的应用。上述表面活性剂用作抑菌剂时,对大肠杆菌的最小半抑菌浓度为2.699~6.538μg/ml。本发明的吡啶类双季铵盐表面活性剂的应用,是用作抑菌剂。采用微量液体稀释法测定最小半抑菌浓度的方法,评价了该吡啶类双季铵盐表面活性剂对大肠杆菌的抑菌效果,实验结果显示:该吡啶类双季铵盐表面活性剂对大肠杆菌有良好的抑制作用,尤其是表面活性剂b对大肠杆菌的抑菌效果最好,浓度为5μg/ml时,即可达到50μg/ml氨苄青霉素的抑菌效果,最小半抑菌浓度为2.699μg/ml。本发明的有益效果:(1)本发明提供的吡啶类双季铵盐表面活性剂,原料易得,制备简单,而且采用无溶剂合成法,绿色环保。(2)本发明提供的吡啶类双季铵盐表面活性剂具有良好的表面活性性能,且结构中含有酰胺键,易降解;该吡啶类双季铵盐表面活性剂的cmc低于传统表面活性剂正辛基三甲基溴化铵1~3个数量级。(3)本发明提供的吡啶类双季铵盐表面活性剂具有良好的抑菌效果,对大肠杆菌的抑菌效果优于氨苄青霉素。附图说明图1为本发明实施例1-4的吡啶类双季铵盐表面活性剂a-d的γ-c曲线图。具体实施方式下面通过实施例来进一步说明本发明,但不局限于以下实施例。实施例1:溴化n,n'-二(1-正辛烷基-3-吡啶基)丙二酰胺双季铵盐(表面活性剂a)的制备(1)制备n,n'-二(3-吡啶基)丙二酰胺:在反应瓶中,加入3-氨基吡啶(7.05g,75mmol)、丙二酸二乙酯(4.00g,25mmol)和10mln,n-二甲基甲酰胺,安装分水器,开动搅拌,加热反应。在反应过程中用分水器分离出反应生成的低沸点的乙醇,最终使反应温度达到140℃反应7小时,冷却,过滤,用乙酸乙酯洗涤,干燥得4.16gn,n'-二(3-吡啶基)丙二酰胺,产率65%,熔点:215-218℃。1hnmr(600mhz,dmso-d6,ppm)δ:10.43(s,2h),8.75(d,j=2.3hz,2h),8.29(m,2h),8.06(m,2h),7.37(m,2h),3.56(s,2h)。(2)在反应瓶中,加入n,n'-二(3-吡啶基)丙二酰胺(2.05g,8mmol)和溴代正辛烷(15.45g,80mmol),加热到110℃反应7小时,冷却,过滤,用丙酮重结晶,干燥得3.68g溴化n,n'-二(1-正辛烷基-3-吡啶基)丙二酰胺双季铵盐,产率71.6%,熔点:168-170℃。1hnmr(600mhz,cdcl3,ppm)δ:11.86(s,2h),9.68(s,2h),8.92(dd,j=13.6,7.0hz,4h),8.19(m,2h),4.77(t,j=7.2hz,4h),4.02(s,2h),2.03(m,4h),1.32(m,20h),0.87(t,j=6.9hz,6h)。实施例2:溴化n,n'-二(1-正癸烷基-3-吡啶基)丙二酰胺双季铵盐(表面活性剂b)的制备(1)制备n,n'-二(3-吡啶基)丙二酰胺:在反应瓶中,加入3-氨基吡啶(9.41g,100mmol)、丙二酸二乙酯(4.00g,25mmol)和10mln,n-二甲基甲酰胺,安装分水器,开动搅拌,加热反应。在反应过程中用分水器分离出反应生成的低沸点的乙醇,最终使反应温度达到150℃反应6小时,冷却,过滤,用乙酸乙酯洗涤,干燥得4.29gn,n'-二(3-吡啶基)丙二酰胺,产率67%,熔点:215-218℃。1hnmr(600mhz,dmso-d6,ppm)δ:10.43(s,2h),8.75(d,j=2.3hz,2h),8.29(m,2h),8.06(m,2h),7.37(m,2h),3.56(s,2h)。(2)在反应瓶中,加入n,n'-二(3-吡啶基)丙二酰胺(2.05g,8mmol)和溴代正癸烷(17.69g,80mmol),加热到120℃反应7小时,冷却,过滤,用丙酮重结晶,干燥得3.70g溴化n,n'-二(1-正癸烷基-3-吡啶基)丙二酰胺双季铵盐,产率66.2%,熔点:160-162℃。1hnmr(600mhz,cdcl3,ppm)δ:11.82(s,2h),9.66(s,2h),8.91(dd,j=24.2,7.0hz,4h),8.15(m,2h),4.76(t,j=7.2hz,4h),4.02(s,2h),2.03(m,4h),1.31(m,28h),0.87(t,j=7.0hz,6h)。实施例3:溴化n,n'-二(1-正十二烷基-3-吡啶基)丙二酰胺双季铵盐(表面活性剂c)的制备(1)制备n,n'-二(3-吡啶基)丙二酰胺:在反应瓶中,加入3-氨基吡啶(9.41g,100mmol)、丙二酸二乙酯(4.00g,25mmol)和11.25mln,n-二甲基甲酰胺,安装分水器,开动搅拌,加热反应。在反应过程中用分水器分离出反应生成的低沸点的乙醇,最终使反应温度达到140℃反应7小时,冷却,过滤,用乙酸乙酯洗涤,干燥得4.06gn,n'-二(3-吡啶基)丙二酰胺,产率63.5%,熔点:215-218℃。1hnmr(600mhz,dmso-d6,ppm)δ:10.43(s,2h),8.75(d,j=2.3hz,2h),8.29(m,2h),8.06(m,2h),7.37(m,2h),3.56(s,2h)。(2)在反应瓶中,加入n,n'-二(3-吡啶基)丙二酰胺(2.05g,8mmol)和溴代正十二烷(15.95g,64mmol),加热到120℃反应6小时,冷却,过滤,用丙酮重结晶,干燥得5.26g溴化n,n'-二(1-正十二烷基-3-吡啶基)丙二酰胺双季铵盐,产率87.1%,熔点:180-182℃。1hnmr(600mhz,cdcl3,ppm)δ:11.81(s,2h),9.66(s,2h),8.91(dd,j=26.4,6.9hz,4h),8.06(t,j=6.8hz,2h),4.76ppm(t,j=7.1hz,4h),4.02(s,2h),2.09(m,4h),1.39(m,36h),0.88(t,j=7.0hz,6h)。实施例4:溴化n,n'-二(1-正十四烷基-3-吡啶基)丙二酰胺双季铵盐(表面活性剂d)的制备(1)制备n,n'-二(3-吡啶基)丙二酰胺:在反应瓶中,加入3-氨基吡啶(11.76g,125mmol)、丙二酸二乙酯(4.00g,25mmol)和12.5mln,n-二甲基甲酰胺,安装分水器,开动搅拌,加热反应。在反应过程中用分水器分离出反应生成的低沸点的乙醇,最终使反应温度达到150℃反应6小时,冷却,过滤,用乙酸乙酯洗涤,干燥得4.03gn,n'-二(3-吡啶基)丙二酰胺,产率63%,熔点:215-218℃。1hnmr(600mhz,dmso-d6,ppm)δ:10.43(s,2h),8.75(d,j=2.3hz,2h),8.29(m,2h),8.06(m,2h),7.37(m,2h),3.56(s,2h)。(2)在反应瓶中,加入n,n'-二(3-吡啶基)丙二酰胺(2.05g,8mmol)和溴代正十四烷(19.96g,72mmol),加热到120℃反应5小时,冷却,过滤,用丙酮重结晶,干燥得5.64g溴化n,n'-二(1-正十四烷基-3-吡啶基)丙二酰胺双季铵盐,产率86.9%,熔点:189-191℃。1hnmr(600mhz,cdcl3,ppm)δ:11.87(s,2h),9.68(s,2h),8.91(m,4h),8.03(t,j=6.8hz,2h),4.76(t,j=6.7hz,4h),4.02(s,2h),2.04(m,4h),1.39(m,44h),0.89(t,j=6.4hz,6h)。实施例5:本发明的吡啶类双季铵盐表面活性剂的表面活性测定实验采用悬滴法测定表面活性剂的表面张力。根据所测表面活性剂的溶解度,用二次蒸馏水先配制表面活性剂的饱和溶液,然后按浓度梯度逐步稀释得到一系列不同浓度的表面活性剂溶液,依次用界面流变仪测定不同浓度表面活性剂溶液的表面张力,每次测定1~2小时,当动态表面张力数值在5分钟内间隔变化小于±0.25mn·m-1时,认为达到平衡表面张力。每个样品平行测定三次取平均值,作表面张力-浓度曲线(图1),并求得临界胶束浓度cmc和γcmc,见表1。实验结果显示:该吡啶类双季铵盐表面活性剂a-d的cmc低于传统表面活性剂正辛基三甲基溴化铵1~3个数量级,说明该吡啶类双季铵盐表面活性剂具有良好的表面活性性能。表1本发明的吡啶类双季铵盐表面活性剂a-d与传统表面活性剂正辛基三甲基溴化铵的临界胶束浓度比较表面活性剂cmc/mol·l-1γcmc/mn·m-1表面活性剂a1.3×10-239表面活性剂b1.5×10-333表面活性剂c1.68×10-430表面活性剂d1.69×10-535正辛基三甲基溴化铵2.6×10-141实施例6:本发明的吡啶类双季铵盐表面活性剂作为抑菌剂的应用实施例选取大肠杆菌dh5α为实验菌种,采用微量液体稀释法测定最小半抑菌浓度(mic50)。将培养至指数生长期的细菌菌液加入96孔细菌培养板,每孔90微升,再向各孔中加入10微升经倍比稀释的抗菌肽,即表面活性剂a-c(由于表面活性剂d的水溶性不太好,没有进行抑菌试验),各孔中抗菌肽的最终浓度分别为1.25μg/ml,2.5μg/ml,5μg/ml,10μg/ml,20μg/ml。阳性对照为50μg/ml的医用抗菌素氨苄青霉素(amp),阴性对照为无菌去离子水。将细菌培养板置于37℃黑暗培养箱中培养10小时,用酶标仪测定菌液的od值,见表2。实验结果显示:表面活性剂a--c对大肠杆菌dh5α有良好的抑制作用,尤其是表面活性剂b对大肠杆菌dh5α的抑菌效果最好,浓度为5μg/ml时,即可达到50μg/ml氨苄青霉素的抑菌效果。通过计算得到表面活性剂a,b和c的mic50值分别为4.130μg/ml、2.699μg/ml、6.538μg/ml。表2不同浓度的表面活性剂a,b和c与阳性、阴性的od值比较。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1