一种5-三氟甲基-4H-咪唑啉-4-酮衍生物及合成方法与流程
本发明属于材料、医药化工合成技术领域,具体涉及一种5-三氟甲基-4h-咪唑啉-4-酮衍生物及合成方法。
背景技术
鉴于氟原子的原子半径很小而且又具有高的电负性,很难被极化。因此,向有机化合物分子中引入氟原子或者含氟基团通常会显著改善化合物的化学性质、物理性质以及生物活性。据统计,市面上销售的农药或药物分子中,30%以上的农药或药物分子至少含有一个氟原子或含氟基团。然而,存在于自然界的含氟天然产物种类却十分有限。为了满足人们生产与研究对有机含氟化合物数量和种类增长的迫切需要,发展高效合成有机含氟化合物的方法,一直是化学家们亟待解决的核心任务之一。
鉴于4h-咪唑啉-4-酮化合物的在材料、医药领域的重要应用价值,其高效合成方法研究一直受到人们广泛的关注。但是,5-三氟甲基-4h-咪唑啉-4-酮衍生物及其合成方法却一直未被报道,该类化合物及其合成技术研究仍是空白。因此,发展高效合成5-三氟甲基-4h-咪唑啉-4-酮化合物的方法目前仍是一个挑战性的研究课题。
技术实现要素:
为了解决以上现有技术的空白,本发明的首要目的在于提供一种能够高效合成5-三氟甲基-4h-咪唑啉-4-酮衍生物。
本发明的另一目的在于提供5-三氟甲基-4h-咪唑啉-4-酮衍生物的合成方法。
本发明目的通过以下技术方案实现:
5-三氟甲基-4h-咪唑啉-4-酮衍生物,其结构为式i:
其中r1为苯基、对溴苯基、间溴苯基、对氯苯基、间氯苯基、对氟苯基、间氟苯基、邻氟苯基、对碘苯基、对甲苯基(对甲基苯基)、对甲氧基苯基、对甲硫基苯基、对二甲氨基苯基、对氰基苯基、对三氟甲基苯基、对甲砜基苯基、对甲酸甲酯基苯基、对硝基苯基、对羟基苯基、3,4-二甲氧基苯基、3,4-二氯苯基、2-萘基、2-噻吩基、3-吡啶基、2-苯基乙基、甲基、乙基、丙基、异丙基、环丙基、环丁基或叔丁基;
r为苯基、对碘苯基、间碘苯基、对溴苯基、间溴苯基、对氯苯基、间氯苯基、对氟苯基、间氟苯基、邻氟苯基、对甲苯基、对甲氧基苯基、对甲酸甲酯基苯基、氢、甲基、乙基、异丙基、环己基或叔丁基。
所述5-三氟甲基-4h-咪唑啉-4-酮衍生物的合成方法,包括以下步骤:
在碱和有机溶剂中,将脒盐与三氟甲基酮类化合物反应,后续处理,获得5-三氟甲基-4h-咪唑啉-4-酮衍生物;
所述脒盐为
所述的三氟甲基酮类化合物为
所述脒盐与三氟甲基酮类化合物的摩尔比为1:(1~3)。
碱的加入量与脒盐的摩尔比为(1~4):1。
所述碱为碳酸钠、碳酸钾、碳酸铯、氢氧化钠、氢氧化钾、甲醇钠、乙酸钠、叔丁醇钾和叔丁醇钠中的一种以上。
所述有机溶剂为n,n-二甲基甲酰胺、二甲基亚砜、1,4-二氧六环、甲苯、苯、二甲苯、1,2-二氯乙烷、四氢呋喃和乙腈中的一种以上。
所述反应的温度为50~90℃,反应的时间为12~24h;所述反应在空气或氧气氛围下进行。
所述后续处理是指反应结束后冷却至室温,加入水和有机溶剂,萃取反应液,将有机层进行减压旋蒸去除溶剂,得粗产物,经柱层析提纯得到5-三氟甲基-4h-咪唑啉-4-酮衍生物。所述有机溶剂为乙酸乙酯、二氯甲烷或乙醚。
所述柱层析提纯是指以石油醚:乙酸乙酯的混合溶剂为洗脱液的柱层析提纯。石油醚:乙酸乙酯的体积比为(2~100):1。
本发明的方法所涉及的反应方程式:
本发明的制备方法及所得到的产物具有如下优点及有益效果:
(1)本发明的合成方法不使用催化剂,不需要配体,所用原料无毒、廉价易得;反应对官能团适应性好,对底物适应性广,产物收率高;
(2)本发明的合成方法可以放大至克级规模生产,且操作简单、安全,反应条件温和,具有良好的工业应用前景;
(3)本发明所得产物在农药、医药及材料领域中具有广泛用途。
附图说明
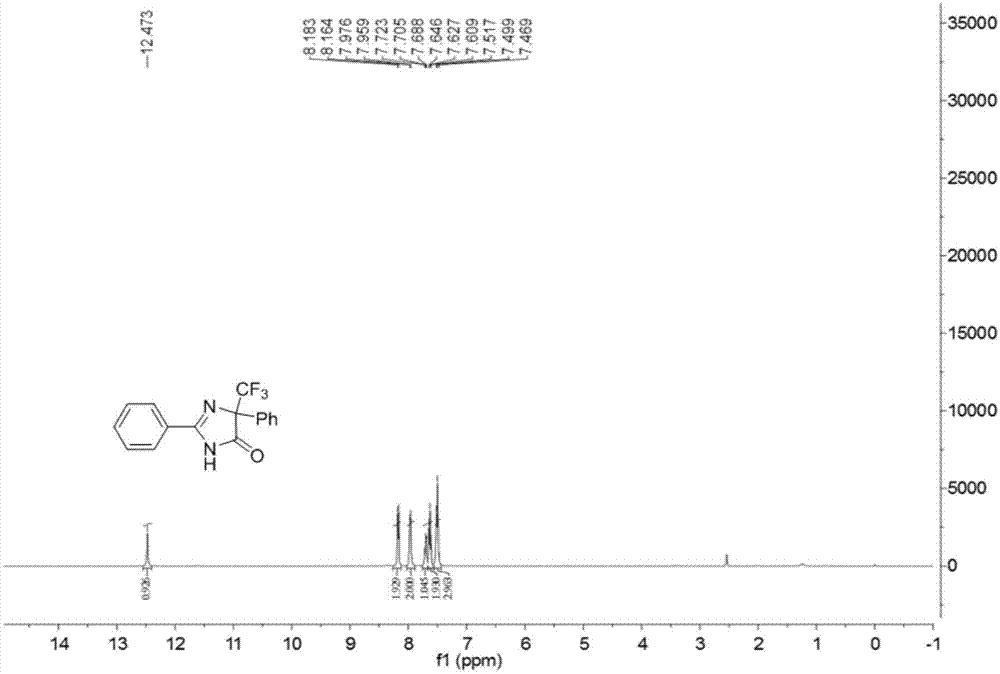
图1是实施例1-8所得产物的氢谱图;
图2是实施例1-8所得产物的碳谱图;
图3是实施例1-8所得产物的氟谱图。
具体实施方式
下面结合实施例及附图对本发明作进一步详细的描述,但本发明的实施方式不限于此。
实施例1
一种5-三氟甲基-4h-咪唑啉-4-酮衍生物的合成方法,包括以下步骤:
在空气氛围下,在装有回流冷凝管的25毫升反应瓶中,加入0.2毫摩尔苯甲脒盐酸盐、0.5毫摩尔叔丁醇钾、0.4毫摩尔3-苯基-1,1,1,-三氟丙酮,2毫升n,n-二甲基甲酰胺,反应体系在70℃搅拌反应12小时,停止加热及搅拌,冷却至室温,加入水,乙酸乙酯萃取反应液,将乙酸乙酯层进行减压旋蒸,去除溶剂,再通过柱层析分离纯化,得到目标产物,所用的柱层析洗脱液为体积比为10:1的石油醚:乙酸乙酯混合溶剂;产物的产率为96%。
实施例2
一种5-三氟甲基-4h-咪唑啉-4-酮衍生物的合成方法,包括以下步骤:
在空气氛围下,在装有回流冷凝管的25毫升反应瓶中,加入0.2毫摩尔苯甲脒盐酸盐、0.8毫摩尔碳酸钾、0.4毫摩尔3-苯基-1,1,1,-三氟丙酮,2毫升n,n-二甲基甲酰胺,反应体系在70℃搅拌反应12小时,停止加热及搅拌,冷却至室温,加入水,乙酸乙酯萃取反应液,将乙酸乙酯层进行减压旋蒸去除溶剂,再通过柱层析分离纯化,得到目标产物,所用的柱层析洗脱液为体积比为10:1的石油醚:乙酸乙酯混合溶剂;产物的产率为65%。
实施例3
一种5-三氟甲基-4h-咪唑啉-4-酮衍生物的合成方法,包括以下步骤:
在空气氛围下,在装有回流冷凝管的25毫升反应瓶中,加入0.2毫摩尔苯甲脒盐酸盐、0.2毫摩尔叔丁醇钾、0.4毫摩尔3-苯基-1,1,1,-三氟丙酮,2毫升1,4-二氧六环,反应体系在70℃搅拌反应12小时,停止加热及搅拌,冷却至室温,加入水,乙酸乙酯萃取反应液,将乙酸乙酯层进行减压旋蒸去除溶剂,再通过柱层析分离纯化,得到目标产物,所用的柱层析洗脱液为体积比为10:1的石油醚:乙酸乙酯混合溶剂;产物的产率为10%。
实施例4
一种5-三氟甲基-4h-咪唑啉-4-酮衍生物的合成方法,包括以下步骤:
在空气氛围下,在装有回流冷凝管的25毫升反应瓶中,加入0.2毫摩尔苯甲脒盐酸盐、0.5毫摩尔叔丁醇钾、0.2毫摩尔3-苯基-1,1,1,-三氟丙酮,2毫升n,n-二甲基甲酰胺,反应体系在50℃搅拌反应12小时,停止加热及搅拌,冷却至室温,加入水,乙酸乙酯萃取反应液,将乙酸乙酯层进行减压旋蒸去除溶剂,再通过柱层析分离纯化,得到目标产物,所用的柱层析洗脱液为体积比为10:1的石油醚:乙酸乙酯混合溶剂;产物的产率为21%。
实施例5
一种5-三氟甲基-4h-咪唑啉-4-酮衍生物的合成方法,包括以下步骤:
在空气氛围下,在装有回流冷凝管的25毫升反应瓶中,加入0.2毫摩尔苯甲脒盐酸盐、0.5毫摩尔叔丁醇钾、0.6毫摩尔3-苯基-1,1,1,-三氟丙酮,2毫升n,n-二甲基甲酰胺,反应体系在90℃搅拌反应12小时,停止加热及搅拌,冷却至室温,加入水,乙酸乙酯萃取反应液,将乙酸乙酯层进行减压旋蒸去除溶剂,再通过柱层析分离纯化,得到目标产物,所用的柱层析洗脱液为体积比为10:1的石油醚:乙酸乙酯混合溶剂;产物的产率为91%。
实施例6
一种5-三氟甲基-4h-咪唑啉-4-酮衍生物的合成方法,包括以下步骤:
在空气氛围下,在装有回流冷凝管的25毫升反应瓶中,加入0.2毫摩尔苯甲脒氢碘酸盐、0.5毫摩尔叔丁醇钾、0.4毫摩尔3-苯基-1,1,1,-三氟丙酮,2毫升n,n-二甲基甲酰胺,反应体系在70℃搅拌反应12小时,停止加热及搅拌,冷却至室温,加入水,乙酸乙酯萃取反应液,将乙酸乙酯层进行减压旋蒸去除溶剂,再通过柱层析分离纯化,得到目标产物,所用的柱层析洗脱液为体积比为10:1的石油醚:乙酸乙酯混合溶剂;产物的产率为94%。
实施例7
一种5-三氟甲基-4h-咪唑啉-4-酮衍生物的合成方法,包括以下步骤:
在氧气氛围下,在装有回流冷凝管的25毫升反应瓶中,加入0.2毫摩尔苯甲脒盐酸盐、0.5毫摩尔叔丁醇钾、0.4毫摩尔3-苯基-1,1,1,-三氟丙酮,2毫升n,n-二甲基甲酰胺,反应体系在70℃搅拌反应12小时,停止加热及搅拌,冷却至室温,加入水,乙酸乙酯萃取反应液,将乙酸乙酯层进行减压旋蒸去除溶剂,再通过柱层析分离纯化,得到目标产物,所用的柱层析洗脱液为体积比为10:1的石油醚:乙酸乙酯混合溶剂;产物的产率为96%。
实施例8
一种5-三氟甲基-4h-咪唑啉-4-酮衍生物的合成方法,包括以下步骤:
在空气氛围下,在装有回流冷凝管的250毫升反应瓶中,加入5毫摩尔苯甲脒盐酸盐、12.5毫摩尔叔丁醇钾、10毫摩尔3-苯基-1,1,1,-三氟丙酮,50毫升n,n-二甲基甲酰胺,反应体系在70℃搅拌反应12小时,停止加热及搅拌,冷却至室温,加入水,乙酸乙酯萃取反应液,将乙酸乙酯层进行减压旋蒸去除溶剂,再通过柱层析分离纯化,得到目标产物,所用的柱层析洗脱液为体积比为10:1的石油醚:乙酸乙酯混合溶剂;产物的产率为96%。
实施例1~8所得产物主要非对映异构体的氢谱图、碳谱图和氟谱图分别如图1、图2和图3所示;其结构表征数据如下所示:
1hnmr(400mhz,d6-dmso)δ12.47(s,1h),8.17(d,j=7.6hz,2h),7.97(d,j=6.8hz,2h),7.71(t,j=7.2hz,1h),7.63(t,j=7.6hz,2h),7.47-7.52(m,3h);
13cnmr(100mhz,d6-dmso)δ178.4,164.7,133.5,132.0,130.0,129.5,129.1,128.0,127.9,127.8,123.3(q,1jc-f=281.3hz),75.4(q,2jc-f=27.4hz);
19fnmr(376mhz,d6-dmso)δ=-73.5(s,3f);
ir(kbr):3187,1735,1629,1443,1257,1172cm-1;
hrms(esi,m/z):[m+h]+c16h11f3n2o+h,理论值305.0896;实际值,305.0898。
根据以上数据推断实施例1~8所得产物的结构如下式所示:
实施例9
一种5-三氟甲基-4h-咪唑啉-4-酮衍生物的合成方法,包括以下步骤:
在空气氛围下,在装有回流冷凝管的25毫升反应瓶中,加入0.2毫摩尔4-甲氧基苯甲脒盐酸盐、0.5毫摩尔叔丁醇钾、0.4毫摩尔3-苯基-1,1,1,-三氟丙酮,2毫升n,n-二甲基甲酰胺,反应体系在70℃搅拌反应12小时,停止加热及搅拌,冷却至室温,加入水,乙酸乙酯萃取反应液,将乙酸乙酯层进行减压旋蒸去除溶剂,再通过柱层析分离纯化,得到目标产物,所用的柱层析洗脱液为体积比为10:1的石油醚:乙酸乙酯混合溶剂;产物的产率为97%。
本实施例所得产物的结构表征数据如下所示:
1hnmr(400mhz,d6-dmso)δ12.29(s,1h),8.12(d,j=5.2hz,2h),7.93(s,2h),7.47(s,3h),7.15(d,j=6.8hz,2h),3.87(s,3h);
13cnmr(100mhz,d6-dmso)δ178.6,164.1,163.6,132.2,130.0,129.9,129.0,127.8,123.3(q,1jc-f=281.4hz),119.9,114.9,75.0,56.0;
19fnmr(376mhz,d6-dmso)δ=-73.5(s,3f);
ir(kbr):3062,2851,2743,1757,1609,1441,1262,1175cm-1;
hrms(esi,m/z):[m+h]+c17h13f3n2o2+h,理论值335.1002;实际值,335.1005。
根据以上数据推断本实施例所得产物的结构如下式所示:
实施例10
一种5-三氟甲基-4h-咪唑啉-4-酮衍生物的合成方法,包括以下步骤:
在空气氛围下,在装有回流冷凝管的25毫升反应瓶中,加入0.2毫摩尔4-羟基苯甲脒盐酸盐、0.5毫摩尔叔丁醇钾、0.4毫摩尔3-苯基-1,1,1,-三氟丙酮,2毫升n,n-二甲基甲酰胺,反应体系在70℃搅拌反应12小时,停止加热及搅拌,冷却至室温,加入水,乙酸乙酯萃取反应液,将乙酸乙酯层进行减压旋蒸去除溶剂,再通过柱层析分离纯化,得到目标产物,所用的柱层析洗脱液为体积比为10:1的石油醚:乙酸乙酯混合溶剂;产物的产率为60%。
本实施例所得产物的结构表征数据如下所示:
1hnmr(400mhz,d6-dmso)δ12.23(s,1h),10.43(s,1h),7.91-8.01(m,4h),7.47-7.47(m,3h),6.97(d,j=7.6hz,2h);
13cnmr(100mhz,d6-dmso)δ178.5,164.0,162.3,132.4,130.1,129.9,129.0,127.9,123.4(q,1jc-f=281.5hz),118.4,116.2,75.2(q,2jc-f=27.1hz);
19fnmr(376mhz,d6-dmso)δ=-73.5(s,3f);
ir(kbr):3459,3131,2843,1745,1608,1458,1263,1177cm-1;
hrms(esi,m/z):[m+h]+c16h11f3n2o2+h,理论值在321.0845;实际值,321.0850。
根据以上数据推断本实施例所得产物的结构如下式所示:
实施例11
一种5-三氟甲基-4h-咪唑啉-4-酮衍生物的合成方法,包括以下步骤:
在空气氛围下,在装有回流冷凝管的25毫升反应瓶中,加入0.2毫摩尔4-溴苯甲脒盐酸盐、0.5毫摩尔叔丁醇钾、0.4毫摩尔3-苯基-1,1,1,-三氟丙酮,2毫升n,n-二甲基甲酰胺,反应体系在70℃搅拌反应12小时,停止加热及搅拌,冷却至室温,加入水,乙酸乙酯萃取反应液,将乙酸乙酯层进行减压旋蒸去除溶剂,再通过柱层析分离纯化,得到目标产物,所用的柱层析洗脱液为体积比为10:1的石油醚:乙酸乙酯混合溶剂;产物的产率为94%。
本实施例所得产物的结构表征数据如下所示:
1hnmr(400mhz,d6-dmso)δ12.53(s,1h),8.11(d,j=7.6hz,2h),7.97(d,j=6.0hz,2h),7.85(d,j=7.6hz,2h),7.51-7.52(m,3h);
13cnmr(100mhz,d6-dmso)δ178.4,164.2,132.6,131.8,130.0,130.0,129.1,127.9,127.5,126.9,123.1(q,1jc-f=281.5hz),75.4(q,2jc-f=27.9hz);
19fnmr(376mhz,d6-dmso)δ=-73.5(s,3f);
ir(kbr):3178,1733,1626,1436,1251,1176cm-1;
hrms(esi,m/z):[m+h]+c16h10brf3n2o+h,理论值383.0001;实际值,383.0002
根据以上数据推断本实施例所得产物主要非对映异构体的结构如下式所示:
实施例12
一种5-三氟甲基-4h-咪唑啉-4-酮衍生物的合成方法,包括以下步骤:
在空气氛围下,在装有回流冷凝管的25毫升反应瓶中,加入0.2毫摩尔4-硝基苯甲脒盐酸盐、0.5毫摩尔叔丁醇钾、0.4毫摩尔3-苯基-1,1,1,-三氟丙酮,2毫升n,n-二甲基甲酰胺,反应体系在70℃搅拌反应12小时,停止加热及搅拌,冷却至室温,加入水,乙酸乙酯萃取反应液,将乙酸乙酯层进行减压旋蒸去除溶剂,再通过柱层析分离纯化,得到目标产物,所用的柱层析洗脱液为体积比为10:1的石油醚:乙酸乙酯混合溶剂;产物的产率为85%。
本实施例所得产物的结构表征数据如下所示:
1hnmr(400mhz,d6-dmso)δ12.73(s,1h),8.39-8.47(m,4h),7.94(d,j=6.8hz,2h),7.51-7.52(m,3h);
13cnmr(100mhz,d6-dmso)δ178.2,163.8,150.5,133.3,131.5,130.2,129.6,129.2,127.8,124.6,123.1(q,1jc-f=281.5hz),75.7(q,2jc-f=26.7hz);
19fnmr(376mhz,d6-dmso)δ=-73.5(s,3f);
ir(kbr):3173,3106,2883,1737,1610,1531,1442,1349,1255,1175cm-1;
hrms(esi,m/z):[m+h]+c16h10f3n3o3+h,理论值350.0747;实际值,350.0750。
根据以上数据推断本实施例所得产物的结构如下式所示:
实施例13
一种5-三氟甲基-4h-咪唑啉-4-酮衍生物的合成方法,包括以下步骤:
在空气氛围下,在装有回流冷凝管的25毫升反应瓶中,加入0.2毫摩尔3-吡啶甲脒盐酸盐、0.5毫摩尔叔丁醇钾、0.4毫摩尔3-苯基-1,1,1,-三氟丙酮,2毫升n,n-二甲基甲酰胺,反应体系在70℃搅拌反应12小时,停止加热及搅拌,冷却至室温,加入水,乙酸乙酯萃取反应液,将乙酸乙酯层进行减压旋蒸去除溶剂,再通过柱层析分离纯化,得到目标产物,所用的柱层析洗脱液为体积比为2:1的石油醚:乙酸乙酯混合溶剂;产物的产率为86%。
本实施例所得产物的结构表征数据如下所示:
1hnmr(400mhz,d6-dmso)δ12.60(s,1h),9.29(s,1h),8.87(d,j=2.8hz,1h),8.51(d,j=7.6hz,1h),7.94(d,j=5.2hz,2h),7.67(s,1h),7.50(s,3h);
13cnmr(100mhz,d6-dmso)δ178.3,163.7,154.0,148.9,135.6,131.7,130.1,129.1,127.9,124.5,124.0,123.1(q,1jc-f=278.1hz),75.3(q,2jc-f=27.9hz);
19fnmr(376mhz,d6-dmso)δ=-73.4(s,3f);
ir(kbr):3443,3064,1756,1615,1476,1267,1173cm-1;
hrms(esi,m/z):[m+h]+c15h10f3n3o+h,理论值306.0849;实际值,306.0853。
根据以上数据推断本实施例所得产物的结构如下式所示:
实施例14
一种5-三氟甲基-4h-咪唑啉-4-酮衍生物的合成方法,包括以下步骤:
在空气氛围下,在装有回流冷凝管的25毫升反应瓶中,加入0.2毫摩尔乙脒盐酸盐、0.5毫摩尔叔丁醇钾、0.4毫摩尔3-苯基-1,1,1,-三氟丙酮,2毫升n,n-二甲基甲酰胺,反应体系在70℃搅拌反应12小时,停止加热及搅拌,冷却至室温,加入水,乙酸乙酯萃取反应液,将乙酸乙酯层进行减压旋蒸去除溶剂,再通过柱层析分离纯化,得到目标产物,所用的柱层析洗脱液为体积比为10:1的石油醚:乙酸乙酯混合溶剂;产物的产率为39%。
本实施例所得产物的结构表征数据如下所示:
1hnmr(400mhz,d6-dmso)δ11.63(s,1h),7.81(d,j=4.4hz,1h),7.44-7.48(m,3h),2.22(s,3h);
13cnmr(100mhz,d6-dmso)δ177.8,166.5,131.8,129.9,129.0,127.9,123.2(q,1jc-f=280.9hz),75.2(q,2jc-f=27.7hz),16.6;
19fnmr(376mhz,d6-dmso)δ=-73.8(s,3f);
ir(kbr):3274,3058,2924,2848,1752,1643,1441,1260,1178cm-1;
hrms(esi,m/z):[m+h]+c11h9f3n2o+h,理论值243.0740;实际值,243.0745。
根据以上数据推断本实施例所得产物的结构如下式所示:
实施例15
一种5-三氟甲基-4h-咪唑啉-4-酮衍生物的合成方法,包括以下步骤:
在空气氛围下,在装有回流冷凝管的25毫升反应瓶中,加入0.2毫摩尔2-氯苯甲脒盐酸盐、0.5毫摩尔叔丁醇钾、0.4毫摩尔3-苯基-1,1,1,-三氟丙酮,2毫升n,n-二甲基甲酰胺,反应体系在70℃搅拌反应12小时,停止加热及搅拌,冷却至室温,加入水,乙酸乙酯萃取反应液,将乙酸乙酯层进行减压旋蒸去除溶剂,再通过柱层析分离纯化,得到目标产物,所用的柱层析洗脱液为体积比为10:1的石油醚:乙酸乙酯混合溶剂;产物的产率为86%。
本实施例所得产物的结构表征数据如下所示:
1hnmr(400mhz,d6-dmso)δ12.27(s,1h),7.94(d,j=8.0hz,2h),7.76(d,j=7.6hz,1h),7.63-7.70(m,2h),7.49-7.57(m,4h);
13cnmr(100mhz,d6-dmso)δ177.7,164.7,133.6,132.2,131.5,131.3,130.9,130.1,129.2,128.5,128.1,127.9,123.0(q,1jc-f=281.3hz),75.6(q,2jc-f=27.1hz);
19fnmr(376mhz,d6-dmso)δ=-73.5(s,3f);
ir(kbr):3265,3070,1756,1624,1437,1257,1179cm-1;
hrms(esi,m/z):[m+h]+c16h10clf3n2o+h,理论值339.0507;实际值,339.0510。
根据以上数据推断本实施例所得产物的结构如下式所示:
实施例16
一种5-三氟甲基-4h-咪唑啉-4-酮衍生物的合成方法,包括以下步骤:
在空气氛围下,在装有回流冷凝管的25毫升反应瓶中,加入0.2毫摩尔3-溴苯甲脒盐酸盐、0.5毫摩尔叔丁醇钾、0.4毫摩尔3-苯基-1,1,1,-三氟丙酮,2毫升n,n-二甲基甲酰胺,反应体系在70℃搅拌反应12小时,停止加热及搅拌,冷却至室温,加入水,乙酸乙酯萃取反应液,将乙酸乙酯层进行减压旋蒸去除溶剂,再通过柱层析分离纯化,得到目标产物,所用的柱层析洗脱液为体积比为10:1的石油醚:乙酸乙酯混合溶剂;产物的产率为85%。
本实施例所得产物主要非对映异构体的结构表征数据如下所示:
1hnmr(400mhz,d6-dmso)δ12.50(s,1h),8.32(s,1h),8.15(d,j=7.6hz,1h),7.90-7.93(m,3h),7.59(t,j=8.0hz,1h),7.49-7.52(m,3h);
13cnmr(100mhz,d6-dmso)δ178.2,163.7,136.3,132.7,131.7,131.7,130.5,130.1,129.9,129.2,127.9,127.1,123.1(q,1jc-f=281.4hz),122.7,75.5(q,2jc-f=24.1hz);
19fnmr(376mhz,d6-dmso)δ=-73.5(s,3f);
ir(kbr):3442,3201,1738,1627,1448,1257,1174cm-1;
hrms(esi,m/z):[m+h]+c16h10brf3n2o+h,理论值383.0001;实际值,383.0005。
根据以上数据推断本实施例所得产物的结构如下式所示:
实施例17
一种5-三氟甲基-4h-咪唑啉-4-酮衍生物的合成方法,包括以下步骤:
在空气氛围下,在装有回流冷凝管的25毫升反应瓶中,加入0.2毫摩尔苯甲脒盐酸盐、0.5毫摩尔叔丁醇钾、0.4毫摩尔3-(4-甲氧基苯基)-1,1,1,-三氟丙酮,2毫升n,n-二甲基甲酰胺,反应体系在70℃搅拌反应12小时,停止加热及搅拌,冷却至室温,加入水,乙酸乙酯萃取反应液,将乙酸乙酯层进行减压旋蒸去除溶剂,再通过柱层析分离纯化,得到目标产物,所用的柱层析洗脱液为体积比为10:1的石油醚:乙酸乙酯混合溶剂;产物的产率为91%。
本实施例所得产物主要的结构表征数据如下所示:
1hnmr(400mhz,d6-dmso)δ12.41(s,1h),8.14(d,j=7.6hz,2h),7.84(d,j=8.8hz,2h),7.70(t,j=7.6hz,1h),7.62(t,j=7.2hz,2h),7.05(d,j=8.8hz,2h),3.79(s,3h);
13cnmr(100mhz,d6-dmso)δ178.7,164.4,160.6,133.5,129.5,129.2,128.0,127.8,123.7,123.3(q,1jc-f=281.2hz),114.5,75.1(q,2jc-f=27.4hz),55.7;
19fnmr(376mhz,d6-dmso)δ=-73.8(s,3f);
ir(kbr):3175,2933,1738,1622,1509,1453,1252,1171cm-1;
hrms(esi,m/z):[m+h]+c17h13f3n2o2+h,理论值335.1002;实际值,335.1006。
根据以上数据推断本实施例所得产物的结构如下式所示:
实施例18
一种5-三氟甲基-4h-咪唑啉-4-酮衍生物的合成方法,包括以下步骤:
在空气氛围下,在装有回流冷凝管的25毫升反应瓶中,加入0.2毫摩尔苯甲脒盐酸盐、0.5毫摩尔叔丁醇钾、0.4毫摩尔3-(4-碘苯基)-1,1,1,-三氟丙酮,2毫升n,n-二甲基甲酰胺,反应体系在70℃搅拌反应12小时,停止加热及搅拌,冷却至室温,加入水,乙酸乙酯萃取反应液,将乙酸乙酯层进行减压旋蒸去除溶剂,再通过柱层析分离纯化,得到目标产物,所用的柱层析洗脱液为体积比为10:1的石油醚:乙酸乙酯混合溶剂;产物的产率为91%。
本实施例所得产物主要的结构表征数据如下所示:
1hnmr(400mhz,d6-dmso)δ12.50(s,1h),8.13(d,j=7.2hz,2h),7.87(d,j=8.0hz,2h),7.67-7.71(m,3h),7.60(t,j=7.2hz,2h);
13cnmr(100mhz,d6-dmso)δ178.1,165.1,138.0,133.6,131.7,130.0,129.5,128.1,127.6,122.9(q,1jc-f=281.5hz),97.2,75.1(q,2jc-f=27.8hz);
19fnmr(376mhz,d6-dmso)δ=-73.6(s,3f);
ir(kbr):3194,2921,1737,1628,1458,1251,1175cm-1;
hrms(esi,m/z):[m+h]+c16h10f3in2o+h,理论值430.9863;实际值430.9864。
根据以上数据推断本实施例所得产物的结构如下式所示:
实施例19
一种5-三氟甲基-4h-咪唑啉-4-酮衍生物的合成方法,包括以下步骤:
在空气氛围下,在装有回流冷凝管的25毫升反应瓶中,加入0.2毫摩尔苯甲脒盐酸盐、0.5毫摩尔叔丁醇钾、0.4毫摩尔3-(3-氯苯基)-1,1,1,-三氟丙酮,2毫升n,n-二甲基甲酰胺,反应体系在70℃搅拌反应12小时,停止加热及搅拌,冷却至室温,加入水,乙酸乙酯萃取反应液,将乙酸乙酯层进行减压旋蒸去除溶剂,再通过柱层析分离纯化,得到目标产物,所用的柱层析洗脱液为体积比为10:1的石油醚:乙酸乙酯混合溶剂;产物的产率为80%。
本实施例所得产物主要的结构表征数据如下所示:
1hnmr(400mhz,d6-dmso)δ12.58(s,1h),8.18(d,j=7.2hz,2h),7.94(s,2h),7.58-7.72(m,5h);
13cnmr(100mhz,d6-dmso)δ177.9,165.3,134.0,133.8,133.7,131.1,130.2,129.5,128.1,127.6,126.7,123.0(q,1jc-f=281.5hz),74.8(q,2jc-f=27.6hz);
19fnmr(376mhz,d6-dmso)δ=-73.7(s,3f);
ir(kbr):3187,2924,1736,1631,1457,1255,1177cm-1;
hrms(esi,m/z):[m+h]+c16h10clf3n2o+h,理论值339.0507;实际值,339.0508。
根据以上数据推断本实施例所得产物的结构如下式所示:
上述实施例为本发明较佳的实施方式,但本发明的实施方式并不受上述实施例的限制,其它的任何未背离本发明的精神实质与原理下所作的改变、修饰、替代、组合、简化,均应为等效的置换方式,都包含在本发明的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!