马流感病毒H3N8亚型的融合蛋白及其制备方法、应用和疫苗与流程
本发明涉及生物
技术领域:
,尤其是涉及一种马流感病毒h3n8亚型的融合蛋白及其制备方法、应用和疫苗。
背景技术:
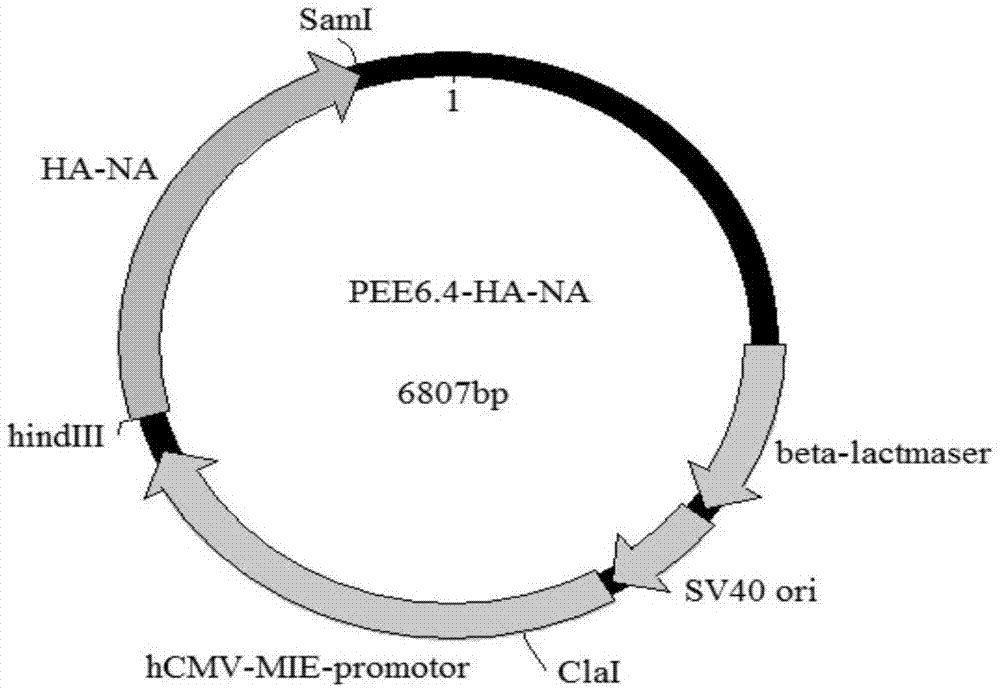
:马流行性感冒(equineinfluenza,ei)是由马流感病毒(equineinfluenzavirus,eiv)引起的一种急性传染病,它具有急性、高度接触传染性的特点。h3n8亚型是主要流行株,是马呼吸道传染病之一。马流感病毒属于正粘病毒科(orthomyxoviridae)、a型流感病毒属。是一种分节段的大小不等的单股负链rna有囊膜的病毒,基因组长约13.6kb。病毒粒子形态很多,大多数呈球形状,其直径约为80-120nm,丝状体能长达数微米。病毒粒子结构主要分为三层,最外层的囊膜是由双层类脂质所构成,两种形态不同的重要蛋白突起在囊膜里镶嵌着,一种像蘑菇样的是神经氨酸酶(neuraminidase,na),另一种像棒状的结构是血凝素(hemagglutinin,ha),囊膜上na与ha的比例大约为5:1-4:1。中间层是基质蛋白(m1)形成的球形蛋白壳,还有少量的离子通道蛋白(ionchannelprotein)在双层类脂膜上,称为m2蛋白。马流行性感冒一年四季均可发生,传播极为迅速,多呈暴发流行。染马流感病毒后,传播速度非常快,伴有发热、精神抑郁,结膜潮红,咳嗽和流浆性鼻液、呼吸困难,食欲大减,并且多因继发感染而引起病情加重或死亡、怀孕母马可能发生流产、赛马丧失竞技能力。流感的主要传染源是病马与带毒马,各个年龄和各个品种的马都有发生的可能性,春夏秋冬都会发生,患病率可以达到100%,给养马业造成较大经济损失。目前国内尚无预防马流感的亚单位疫苗。有鉴于此,特提出本发明。技术实现要素:本发明的第一目的在于提供一种马流感病毒h3n8亚型的融合蛋白,该融合蛋白将马流感病毒h3n8亚型的ha蛋白和na蛋白进行串联表达。本发明的第二目的在于提供一种上述融合蛋白的制备方法,该制备方可以表达出上述融合蛋白。本发明的第三目的在于提供一种上述融合蛋白或上述制备方法制备得到的蛋白的应用,可应用于制备疫苗、抗体和病毒检测等多个方面。本发明的第四目的在于提供一种包含上述融合蛋白的疫苗,该疫苗免疫原性好,保护效力高。为解决上述技术问题,本发明特采用如下技术方案:一种马流感病毒h3n8亚型的融合蛋白,包括ha区段和na区段;所述ha区段主要由seqidno.1所示的核苷酸序列表达,所述na区段主要由seqidno.2所示的核苷酸序列表达。优选地,ha区段和na区段的排列顺序为ha-na,通过linker连接;优选地,所述linker具有如seqidno.3所示的核苷酸序列。优选地,所述融合蛋白具有如seqidno.4所示的氨基酸序列。本发明还提供了一种上述融合蛋白的制备方法,该制备方法通过将所述融合蛋白的基因在宿主中表达;优选地,使用哺乳动物表达系统表达所述融合蛋白的基因;优选地,使用cho细胞表达系统表达所述融合蛋白的基因。优选地,提供包含表达所述融合蛋白的基因的表达载体,将所述表达载体导入cho细胞中,然后对cho细胞进行加压筛选,再将加压筛选出的cho细胞驯化成悬浮培养的细胞株,使所述悬浮培养的细胞株表达所述融合蛋白。优选地,使用谷氨酰胺合成酶筛选扩增系统筛选表达所述融合蛋白的cho细胞株;优选地,所述谷氨酰胺合成酶筛选扩增系统中使用的表达载体为pcdna3、pee6.4或pee12.4。优选地,采用逐渐驯化的方法传代至少6代获得悬浮培养的表达所述融合蛋白的cho细胞株。本发明还提供了一种上述融合蛋白或上述制备方法制备得到的蛋白的应用,包括如下(a)-(d)中的至少一种:(a)制备马流感病毒疫苗;(b)制备马流感病毒的抗体;(c)制备检测马流感病毒抗体的试剂盒;(d)制备马流感病毒诊断抗原。本发明还提供了一种包含上述融合蛋白的马禽流感h3n8亚型的疫苗。优选地,所述疫苗中所述融合蛋白的浓度为20-100μg/ml,优选30-80μg/ml,更优选50μg/ml;优选地,所述疫苗还包括辅料,所述辅料包括疫苗佐剂、稳定剂和抗生素中的一种或多种;优选地,所述疫苗佐剂包括氢氧化铝胶、弗氏完全佐剂、弗氏不完全佐剂、白油佐剂、mf59佐剂或isa201vg,优选使用isa201vg。与现有技术相比,本发明具有如下有益效果:本发明提供的马流感病毒h3n8亚型的融合蛋白,将马流感病毒h3n8亚型ha基因和na基因序列进行串联,本发明通过对ha基因和na基因进行分析,选取了抗原性好,易高表达的区域进行串联,得到的融合蛋白具有抗原性好,表达量高的优点。本发明提供的上述融合蛋白的制备方法,通过将上述融合蛋白的基因在宿主中表达即可。本发明提供的上述融合蛋白和上述制备方法制备得到的蛋白的应用范围十分广泛,可以用以制备马流感病毒疫苗和马流感病毒的抗体。马流感病毒的抗体和上述融合蛋白可以应用于制备多种检测试剂和试剂盒,以用于检测马流感病毒抗体,例如使用含有马流感病毒的抗体的elisa试剂盒以检测马流感病毒,或者使用含有该融合蛋白的胶体金免疫层析试纸检测待测血清样品中的马流感病毒抗体含量。本发明提供的包含上述融合蛋白的疫苗,具有较好的免疫原性,免疫动物后可以产生较高滴度的抗体滴度,使动物获得较好的保护效果。附图说明为了更清楚地说明本发明具体实施方式或现有技术中的技术方案,下面将对具体实施方式或现有技术描述中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图是本发明的一些实施方式,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他的附图。图1为本发明实施例2提供的pee6.4-ha-na质粒图谱;图2为本发明实施例2提供的酶切鉴定结果;图3为本发明实施例6提供的细胞表达蛋白的werstern-blotting检测;图4为本发明实施例8提供的免疫马流感病毒ha-na亚单位疫苗后balb/c小鼠抗体水平变化。具体实施方式下面将结合附图对本发明的技术方案进行清楚、完整地描述,显然,所描述的实施例是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。实施例中未注明具体条件者,按照常规条件或制造商建议的条件进行。所用试剂或仪器未注明生产厂商者,均为可以通过市售购买获得的常规产品。本发明提供了一种马流感病毒h3n8亚型的融合蛋白,该融合蛋白是马流感病毒融合蛋白,该融合蛋白包括ha区段和na区段;所述ha区段主要由seqidno.1所示的核苷酸序列表达,所述na区段主要由seqidno.2所示的核苷酸序列表达。血凝素(hemagglutinin,ha)是马流感病毒的主要表面抗原,负责病毒粒子、宿主细胞的连接,ha基因核苷酸长度为1742-1778个碱基,只有一个编码框,编码含562-566个氨基酸的蛋白肽,大小为70kd,其羧基在囊膜内,氨基端在囊膜外,为典型的ⅰ型糖蛋白。神经氨酸酶(neuraminidase,na)是马流感病毒另一个主要表面抗原,其成分为整体膜糖蛋白,含一个开放阅读框,有1443-1492个核苷酸,编码约459个氨基酸,有3-5个糖基化位点。na酶活性的催化中心位于头部顶端,每个na纤突有四个抗原位点,每个位点又含有多个抗原决定簇。本发明提供的融合蛋白,将马流感病毒h3n8亚型ha基因和na基因序列进行串联,本发明通过对ha基因和na基因进行分析,选取了抗原性高,并且较易高表达的区域进行串联,得到的融合蛋白具有抗原性好,表达量高的优点。在一些可选地实施方式中,ha区段和na区段的排列顺序为ha-na,通过linker连接,linker可以将融合蛋白彼此分开,不影响ha和na蛋白各自高级结构的形成,本发明优选使用具有如seqidno.3所示的核苷酸序列的linker。在一个优选的实施方式中,所述融合蛋白,具有如seqidno.4所示的氨基酸序列和具有如seqidno.5所示的核苷酸序列。本发明还提供了一种上述融合蛋白的制备方法,该制备方法通过将上述融合蛋白的基因在宿主中表达即可,例如可以为但不限于为在大肠杆菌表达系统、酵母表达系统、昆虫表达系统、植物表达系统或者哺乳动物表达系统均可,由于哺乳动物细胞表达的蛋白经翻译加工后,其结构与生物学特性更接近于天然蛋白,因此本发明优选使用哺乳动物表达系统表达所述融合蛋白的基因,更优选使用cho细胞表达系统表达所述融合蛋白的基因。cho细胞即中国仓鼠卵巢细胞(chinesehamsterovary),cho细胞表达系统具有如下优点:(1)具有准确的翻译后折叠及修饰功能,表达的蛋白在分子结构,理化特性和生物学功能方面最接近于天然蛋白分子。(2)具有产物胞外分泌功能,便于下游产物分离纯化。(3)具有重组基因的高效扩增和表达能力。(4)具有贴壁生长特性,具有较高的耐受剪切力和渗透压能力。也可以进行悬浮培养,表达水平较高。(5)cho属于成纤维细胞,很少分泌自身的内源蛋白质,利于外源蛋白的分离。在一些优选的实施方式中,本发明对cho表达系统进行加压筛选,以获得高表达融合蛋白的cho细胞株。可选地,可以选择谷氨酰胺合成酶基因筛选扩增系统或者二氢叶酸还原酶基因筛选系统进行加压筛选,这两种系统可以单独使用,也可以结合使用,本发明对此不做限制。选择标记和基因扩增cho细胞表达载体主要有两类选择标记。一类是非扩增基因,它对目的基因的拷贝数没有影响,用于构建瞬时表达载体。另一类具有基因扩增的功能,也称共扩增基因,如二氢叶酸还原酶基因(dihydrofolatereductase,dhfr),谷氨酰胺合成酶基因(glutaminesynthetase,gs)。当携带gs基因的表达质粒转染cho细胞后,可以得到在选择培养基生长的细胞克隆,gs可被甲硫氨酸亚枫(msx)所抑制,在极少数幸存下来的抗性细胞中,gs基因均得以扩增,结果会导致与gs基因串联在一起的外源基因的共扩增,拷贝数可增加几百到几千倍,从而使目的基因高水平表达,从而抵消msx的抑制效应。使用谷氨酰胺合成酶基因筛选扩增系统时,先将表达所述融合蛋白的基因克隆到具有gs筛选标记的表达载体上得到重组载体,然后将重组载体导入cho细胞中,然后通过使用含有msx的培养基培养cho细胞对cho细胞进行加压,以筛选出高表达目的基因。在一些优选的实施方式中,具有gs筛选标记的表达载体使用pcdna3、pee6.4或pee12.4。悬浮生长的细胞其培养和传代都十分简便。传代时不需要再分散,只需按比例稀释后即可继续培养。此法细胞增殖快、产量高、培养过程简单,是大规模培养动物细胞的理想模式。由于cho细胞具有既可以贴壁生长,也可以进行悬浮培养的特性,因此本发明优选将表达所述融合蛋白的cho细胞进行驯化,使其能够悬浮培养。并且优选采用逐渐驯化的方法传代至少6代获得悬浮培养的表达所述融合蛋白的细胞株,以使悬浮细胞株细胞表达量高,且传代稳定。在一个优选的实施方式中,所述制备方法参考如下方案:先将优化的马流感ha-na基因扩增后通过酶切连接到真核表达载体pcdna3、pee6.4或pee12.4,通过鉴定获得含有ha-na基因的阳性质粒。然后通过扩大培养,提取阳性质粒,转染至cho细胞内。加压筛选,转染至少24h后开始加压,加压7天;加压至阴性对照细胞死亡90%以上,开始单克隆筛选。细胞株驯化成悬浮培养,每隔24h计数细胞及活力,当第一代细胞活率达到94%左右时,进行第二代培养;第二代、第三代至第六代培养后得到的细胞活率达到95%,7周后细胞接种3天后繁殖3代,密度达到细胞活率达到1×106个/ml,认为适应悬浮培养。收集细胞培养液,离心取上清,过滤膜,然后纯化,采用bca法测定蛋白浓度,浓度约可以达到0.7-1.0g/l之间,采用hplc法检测纯度,纯度可以达到95%以上。本发明还提供了一种上述融合蛋白和上述制备方法制备得到的蛋白的应用,包括如下(a)-(d)中的至少一种:(a)制备马流感病毒疫苗;(b)制备马流感病毒的抗体;(c)制备检测马流感病毒抗体的试剂盒;(d)制备马流感病毒诊断抗原。由于本发明提供的马流感病毒h3n8亚型融合蛋白具有较好的免疫原性,因此可以用以制备马流感病毒疫苗,优选制备ha-na亚单位疫苗,免疫动物后可产生较高的抗体的滴度。使用该融合蛋白制备的马流感病毒的抗体以及该融合蛋白可以应用于制备多种检测试剂和试剂盒,以用于检测马流感病毒抗体,例如使用含有马流感病毒的抗体的elisa试剂盒以检测马流感病毒,或者使用含有该融合蛋白的胶体金免疫层析试纸检测待测血清样品中的马流感病毒抗体含量。本发明还提供了一种包含上述融合蛋白的马禽流感h3n8亚型的疫苗,该疫苗具有较好的免疫原性,免疫动物后可以产生较高滴度的抗体滴度,使动物获得较好的保护效果。在一些优选的实施方式中,疫苗中所述融合蛋白的浓度为20-100μg/ml,优选30-80μg/ml,更优选50μg/ml。优选地,所述疫苗还包括辅料,例如可以为但不限于为疫苗佐剂、稳定剂或抗生素。优选包括疫苗佐剂,所述疫苗佐剂例如可以为但不限于为氢氧化铝胶、弗氏完全佐剂、弗氏不完全佐剂、白油佐剂、mf59佐剂或isa201vg,优选使用isa201vg。下面结合优选实施例进一步说明本发明的有益效果,其中本发明试剂及药品来源如下:中华仓鼠卵巢细胞(cho)购自美国atcc公司;细胞培养基和血清均购自美国gibcom公司;真核表达载体pee6.4购自美国thermofisher公司;lipofectamineltx购自北京索莱宝科技有限公司;氨甲基喋呤(mnethotrexatemtx)购自sigma公司;甲硫氨酸亚砜亚铵(l-methioninesulfoximinemsx)购于sigma公司;bca蛋白质定量试剂盒购自美国thermofisher公司;isa201vg购自法国赛比克公司,其他试剂、试剂盒及耗材均为常规市售产品。需要说明的是,实施例中的反应体系和反应条件仅是一种举例。实施例中各步骤中的反应体系和反应条件均可以在可接受的范围内进行调整,以优化反应条件,本发明对此不做限制。实施例1:ha-na基因设计及合成ha-na基因设计及合成:ha基因(genbank登录号kx815377.1)经优化后,设计长度810bp,具有如seqidno.1所示序列;na基因(genbank登录号mg132049.1)经优化后设计长度900bp,具有如seqidno.2所示序列。ha基因与na基因间使用linker序列连接,linker序列具有如seqidno.3所示序列。ha-na基因全长1740bp,具有如seqidno.4所示氨基酸序列和如seqidno.5所示核苷酸序列。ha-na基因合成由上海生工生物公司完成。实施例2:pee6.4-ha-na重组质粒构建2.1添加酶切位点:通过pcr扩增在ha-na基因序列的上游和下游分别添加酶切位点:hindⅲ、smai,pcr扩增上游引物如seqidno.6所示,pcr扩增下游引物如seqidno.7所示。pee6.4-ha-na质粒图谱如图1所示。2.2ha-na基因及载体双酶切反应2.2.1构建50μl反应体系,按照下表将各组分混合均匀后37℃水浴2h。2.2.2目的dna片段回收:采用dna凝胶回收试剂盒(购自北京莱宝科技有限公司),回收酶切目的片段,步骤如下:(1)琼脂糖凝胶电泳后,将目的dna条带从琼脂糖凝胶中用刀片小心切下,放入1.5mlep管中,称取重量。(2)向ep管中加入3倍体积溶胶液,50-55℃水浴10min,期间小心翻转离心管,确保胶块充分溶解。(3)将上一步所得溶液加入吸附柱中(吸附柱放入收集管中),12000rpm离心30-60s,倒掉收集管中的废液,将吸附柱重新放入收集管中。(4)向吸附柱中加入600μl漂洗液,12000rpm离心1min,弃废液,将吸附柱放入收集管中。(5)向吸附柱中加入600μl漂洗液,12000rpm离心1min,弃废液,将吸附柱放入收集管中。(6)12000rpm离心2min,尽量除去漂洗液。将吸附柱敞口置于室温或50℃温箱放置2min。(7)将吸附柱放入1.5mlep管中,向吸附膜中央悬空滴加适量经65℃水浴预热的洗脱液,室温放置2min,12000rpm离心1min。2.3ha-na基因及载体连接反应,构建10μl反应体系,然后将连接反应体系混合均匀后置于16℃冷水浴中10-16h,后放入65℃水浴15min,最后4℃保存。10×t4buffer1μldna片段6μl载体2μlt4连接酶1μl2.4转化反应将10μl连接反应液加入到100μldh5α感受态细胞中,混匀后冰浴30min,42℃水浴100s,再冰浴2min。然后取出ep管,加入600μllb培养液,置于37℃恒温摇床,240rpm培养1h后取出ep管,室温离心8000rpm,2min,吸除500μl上清液,重悬吹匀菌体,将重悬的菌液滴到转化平板上,用涂菌棒将菌液均匀铺开。然后将转化平板置于恒温培养箱中,37℃培养1h后,将转化平板倒置进行培养15h,培养完毕后观察转化结果。2.5质粒抽提与双酶切鉴定2.5.1质粒提取,使用美国omega质粒提取试剂盒,提取方法按照试剂盒使用说明书进行提取。(1)挑取转化板中单个菌落至5ml含氨苄抗性的lb液体培养基中,37℃,220rpm培养8h。(2)取菌液1.5ml至ep管中,室温条件下离心10000rpm1min,弃上清,然后加入250μl溶液i,振荡混匀;再加入250μl溶液ii,小心颠倒ep管4-6次,室温静置2min,至澄清,然后加入350μl溶液iii,小心颠倒离心管4-6次,直至出现白色絮状沉淀,10000rpm室温离心10min。(3)小心吸取上清溶液,并移至吸附柱中心,10000rpm室温离心1min,倒掉收集管中液体后加入500μlbufferhb,10000rpm离心1min,弃滤液,然后加如700μlwashbuffer,10000rpm离心1min,弃滤液;重复1次。(4)室温离心空吸附柱,10000rpm,2min,将吸附柱放入干净的1.5mlep管中,加30μl去离子水在滤膜上,室温静置5min,10000rpm,2min。保存管中dna溶液。2.5.2双酶切鉴定,构建20μl反应体系:10×buffer2μldna样品1μghindⅲ1μlsmai1μl补ddh20至20μl后混合均匀,37℃水浴2h后进行凝胶电泳检测,并将插入dna片段送公司测序,双酶切鉴定结果如图2所示。2.6去内毒素质粒大提,采用去内毒素质粒大量提取试剂盒(北京索莱宝科技有限公司)(1)将测序正确的克隆接种至100ml含氨苄抗性的培养基中,240rpm,37℃恒温培养15h后,取50ml细菌培养物至50ml离心管中,11000rpm离心1min,吸除上清。(2)加4ml溶液p1,振荡器悬浮细菌细胞沉淀,然后加4ml溶液p2,温和颠倒6-8次使菌体充分裂解,最后再加4ml溶液p3,立即温颠倒6-8次,充分混匀,至出现白色絮状沉淀,11000rpm离心10min后,将上清移到另一个干净的离心管中。(3)加上清1/5体积的冰上预冷的内毒素清除剂,振荡混匀,冰浴2min至溶液变清亮,然后37℃水浴5min,不时振荡。(4)11000rpm室温离心5min,溶液分为两相,上层水相含质粒dna,下层油相含内毒素,将含质粒dna的上层水相转移至新管,弃下层油相;重复三次。(5)加入12ml的结合液,充分混匀后加入吸附柱中,室温放置2min,11000rpm离心1min,倒掉收集管中的废液,将吸附柱重新放回收集管中。(6)然后加入8ml漂洗液,11000rpm离心1min,弃废液,将吸附柱放入收集管中,再加入6ml漂洗液,11000rpm离心1min,弃废液,将吸附柱放入收集管中。然后11000rpm离心3min,将吸附柱敞口置于室温或50℃温箱放置4-5min。(7)最后将吸附柱放入一个干净的离心管中,向吸附膜滴2ml经65℃水浴预热的洗脱液,室温放置5min,11000rpm离心2min,-20℃保存。实施例3:pee6.4-ha-na重组质粒转染cho-k1细胞(1)取出细胞,弃去上清培养基,用预温的8mlpbs洗一次,弃去pbs,然后每个培养皿加入2ml0.25%trypsin-edta,室温消化2min,镜下观察细胞变圆,呈单个细胞。加入4mldmem/f12(含10%血清,1%氨苄-链霉素双抗)终止消化反应,用移液器将细胞吹散后转移至15ml离心管中,200rpm离心5min。(2)dmem/f12(含10%血清,1%氨苄-链霉素双抗)重新悬浮细胞,计数后,稀释细胞至2×105个/ml,取2ml混匀的细胞加入到六孔培养皿,置37℃、5%co2细胞培养箱中孵育过夜。(3)观察细胞状态:当细胞交汇度达到80%-90%时开始转染,转染前将培养基换dmem/f12(无血清无双抗),2ml/孔。(4)用opti-mem稀释质粒,125μlopti-mem中加入2.5μg质粒,然后加入2.5μlplus,混合均匀后室温静置5min。(5)稀释lipofectamineltx:125μlopti-mem中加入9μllipofectamineltx,然后加入2.5μlplus,轻轻混匀,室温静置5min。(6)将稀释质粒和稀释lipofectamineltx混合混匀,室温放置5min,然后逐滴加入六孔培养皿中均匀分布。(7)将六孔培养皿置于37℃,5%co2细胞培养箱中培养4-6h后换液:弃掉上清培养基,加入2mldmem/f12(含10%血清1%氨苄-链霉素双抗),将六孔板置于37℃,5%co2细胞培养箱中培养。实施例4:单克隆细胞株筛选(1)转染后24h开始加压:从37℃培养箱中取出六孔培养皿,弃去上清,加入2mldmem/f12(含10%血清+25μmmsx),加压7d,期间镜下观察,死细胞多换液。(2)加压筛选至阴性对照细胞死亡至少90%以上时,开始单克隆筛选;(3)取出六孔培养皿,弃培养基,用pbs洗一次,加入300μl0.25%trypsin-edta,室温消化2min,加2mldmem/f12(含10%血清+25μmmsx)终止消化反应,用移液器将细胞吹散,然后将细胞转移至15ml离心管中,200rpm离心5min。(4)dmem/f12(含10%血清+25μmmsx)重新悬浮细胞,计数,然后将细胞稀释至5个/ml,取200μl加入到96孔板中,放置到37℃,5%co2细胞培养箱中孵育4-6h后标记出单个细胞的孔。(5)96孔板中单个细胞的孔长满时,弃培养基,pbs洗一次,加入100μl0.25%trypsin-edta,室温消化2min,加入2mldmem/f12(含10%血清+25μmmsx)终止反应,用移液器将细胞吹散,然后将细胞液转移至12孔板,细胞长满时,取上清,elisa检测,高效表达的继续培养、冻存。(6)经过筛选,共收获2株细胞株,编号为11株、36株。实施例5:cho-k1细胞株驯化成悬浮培养细胞株(1)从37℃培养箱中取出细胞培养皿,弃去上清,用8mlpbs洗细胞一次,并弃去pbs,然后向培养皿加入2ml0.25%trypsin-edta,室温消化2min,镜下观察细胞由皱变圆,呈单个细胞。然后加入4mldmem/f12(含10%血清,25μmmsx)终止消化反应,用移液器将细胞吹散。然后将细胞液转移至15ml离心管中,200rpm离心5min。(2)使用100%dmem/f12(含10%血清,25μmmsx)悬浮细胞,计数后稀释细胞至5×105个/ml,接种30ml培养基于125ml摇瓶中,置37℃、5%co2细胞培养箱中的轨道式振荡器上130rpm孵育过夜,并且每隔24h计数1次,观察细胞密度及活力。(3)当第一代细胞培养一次后细胞活率达到94%-97%时,进行第二代培养,将第一代细胞转移至50ml离心管中,200rpm离心5min,然后将dmem/f12(含10%血清,25μmmsx)和ex-cell302按1:1混合同时加入对应浓度嘌呤霉素后混匀,重新悬浮细胞,计数后稀释细胞至5×105个/ml,接种30ml培养基于一个125ml摇瓶中,置37℃,5%co2细胞培养箱中的轨道式振荡器上120rpm孵育过夜,并且每隔24h计数1次,观察细胞密度及活力。(4)当第二代培养两次后得到的细胞存活率大于95%,第三至六代培养三次后得到的细胞存活率大于95%。7周后,细胞接种3天后繁殖三代,密度达到1×106个/ml,同时细胞存活率达到95%,该细胞被认为已经适应悬浮培养,接种密度降低到3×105个/ml。经过驯化,编号11株的细胞系满足要求,表明驯化成功。实施例6:细胞发酵(1)配制培养基:60%的cd-cho+40%的ex-cell302置于37℃水浴锅中预热;(2)从co2恒温摇床取出摇瓶细胞,计数后稀释细胞至3.0×105个/ml,接种30ml培养基于125ml摇瓶中,置37℃、5%co2恒温摇床中,100rpm过夜培养。(3)每隔24h细胞计数,观察密度及活力,监测葡萄糖浓度,当葡萄糖浓度低于2g/l的时候,添加葡萄糖到4g/l;每天取1ml样品上清,检测蛋白表达情况。(4)补料:约第4天,70g/lcb5,添加基础培养基的10%;第5天,将co2培养箱温度调整至32℃;第9天,补充70g/lcb5,添加基础培养基的10%;第12天,收获细胞。(5)werstern-blotting检测,结果如图3所示。实施例7:蛋白纯化(1)收集细胞培养液,4℃,10000rpm离心30min,取上清后过滤膜(0.45μm),准备上样。(2)柱平衡:用超纯水平衡3个柱体积,排出乙醇保存液;加入buffera(20mmnah2po4,500mmnacl)4-8ml/min,平衡3个柱体积。(3)上样:用5ml预装柱,1ml/min进行上样(根据预装柱体积调节上样流速,保留时间5min),收集flowthrough(ft)。(4)洗涤:4%bufferb(20mmnah2po4、500mmnacl、100mmimidazole)洗柱,流速为4ml/min,至od280nm基线平稳为止。(5)洗脱:50%bufferb(20mmnah2po4、500mmnacl、100mmimidazole)洗脱目的蛋白,至基线洗平,2ml/min,收集5ml/管。(6)洗涤:100%bufferb(20mmnah2po4、500mmnacl、500mmimidazole)4ml/min,冲洗2-3个柱体积,至uv基线洗平,超纯水平衡3柱体积。(7)透析:millipore10kdpbs(ph7.4)4℃透析,次换液咪唑稀释倍数为2,换液次数为10次。(8)除菌过滤:用0.22μm滤器过滤,蛋白样品溶液-80℃冰箱保存。(9)蛋白浓度和纯度测定:采用bca法测定蛋白浓度,其中112株蛋白得率为800mg/l,其他在500mg/l左右;采用hplc方法检测纯度,纯度都能达到95%以上。实施例8:疫苗制备与免疫接种8.1马流感病毒ha-na亚单位疫苗制备:将表达的重组蛋白ha-na与isa201vg佐剂按体积比45:55混合,乳化,蛋白终浓度为100μg/ml。8.2疫苗免疫及抗体检测:选取6周龄balb/c小鼠进行免疫接种,每次免疫cho表达的ha-na重组蛋白50μg(注:注射0.5ml),首免2周后,进行第二次免疫;首免前、二免前、二免后14天取血检测抗体水平,结果如图4所示。最后应说明的是:以上各实施例仅用以说明本发明的技术方案,而非对其限制;尽管参照前述各实施例对本发明进行了详细的说明,本领域的普通技术人员应当理解:其依然可以对前述各实施例所记载的技术方案进行修改,或者对其中部分或者全部技术特征进行等同替换;而这些修改或者替换,并不使相应技术方案的本质脱离本发明各实施例技术方案的范围。序列表<110>天康生物股份有限公司<120>马流感病毒h3n8亚型的融合蛋白及其制备方法、应用和疫苗<160>7<170>siposequencelisting1.0<210>1<211>810<212>dna<213>马流感病毒(equineinfluenzavirus)<400>1agtttctttagccgactgaattggctaacaaaatccggaagctcttaccccacattgaat60gtgacaatgcctaacaataaaaatttcgacaagctatacatctgggggatccatcacccg120agctcaaatcaagagcagacaaaattgtacatccaagaatcagggcgagtaacagtctca180acaaaaagaagtcaacaaacaataatccctaacatcgggtctagaccatggatcagaggt240caatcaggtaggataagcatatactggaccattgtaaaacctggagatatcctaatgata300aacagtaatggcaacttagttgcaccgcggggatattttaaattgaaaacagggaaaagc360tctgtaatgagatcagatgtacccatagacatttgtgtgtctgagtgtattacaccaaat420ggaagcatctccaacgacaagccattccaaaatgtgaacaaagttacatatggaaaatgc480cccaagtatatcaggcaaaacactttaaagctggccactgggatgaggaatgtaccagaa540aagcaaatcagaggaatctttggggcaatagcgggattcatcgaaaacggctgggaagga600atggttgatggatggtatgggttccgataccaaaactctgaaggaacagggcaagctgca660gatctaaagagcactcaagcagccatcgaccagatcaatggaaagttaaacagagtgatt720gaaagaaccaatgagaaattccatcaaatagagaaggaattctcagaagtagaaggaaga780attcaggacttggagaaatatgtagaagac810<210>2<211>900<212>dna<213>马流感病毒(equineinfluenzavirus)<400>2tactacatgaacaacaccgaaccactttgtgatgcccaaggctttgcaccattttccaaa60gataatggaatacgaattgggtcgagaggccatgtttttgtgataagagaaccttttgta120tcatgttcgccctcagaatgtagaacctttttcctcacacagggctcattactcaatgac180aaacattctaacggcacagtaaaggatcgaagtccatataggactttgatgagtgtcaaa240atagggcaatcacctaatgtgtatcaagctaggtttgaatcagtggcatggtcagcaaca300gcatgccacgatggaaaaaaatggatgacaattggagtcacagggcccgacaatcaagca360accgcaatagtgaactatgggggcattccagttgatattattaattcatgggaaggggac420atattaagaacccaagaatcatcatgcacctgcattaaaggaaactgttattgggtaatg480actgatggaccagcaaataggcaagccaaatacaggatattcaaagcaaaagatggaaga540gtaattggacagaccgatataagtttcaatgggggacacatagaggagtgttcttgttac600cccaatgaagggaaggtggaatgcatatgcagggacaattggactggaacaaatagacca660attctggtaatatcttctgatttatcgtacagagttggatatttgtgtgctggcattccc720actgacactcctaggggagaggatagtcaattcacaggctcatgtacaagtcctttggga780aataaagggtacggtgtaaaaggttttgggtttcgacaaggaactgacgtatgggccgga840aggacaattagtaggacttcgagatcaggattcgaaataataaaaatcaggaatggttgg900<210>3<211>30<212>dna<213>人工序列()<400>3ggaggaggaggatctggaggaggaggatct30<210>4<211>580<212>prt<213>人工序列()<400>4serphepheserargleuasntrpleuthrlysserglysersertyr151015prothrleuasnvalthrmetproasnasnlysasnpheasplysleu202530tyriletrpglyilehishisproserserasnglngluglnthrlys354045leutyrileglngluserglyargvalthrvalserthrlysargser505560glnglnthrileileproasnileglyserargprotrpilearggly65707580glnserglyargileseriletyrtrpthrilevallysproglyasp859095ileleumetileasnserasnglyasnleuvalalaproargglytyr100105110phelysleulysthrglylysserservalmetargseraspvalpro115120125ileaspilecysvalserglucysilethrproasnglyserileser130135140asnasplyspropheglnasnvalasnlysvalthrtyrglylyscys145150155160prolystyrileargglnasnthrleulysleualathrglymetarg165170175asnvalproglulysglnileargglyilepheglyalailealagly180185190pheilegluasnglytrpgluglymetvalaspglytrptyrglyphe195200205argtyrglnasnsergluglythrglyglnalaalaaspleulysser210215220thrglnalaalaileaspglnileasnglylysleuasnargvalile225230235240gluargthrasnglulysphehisglnileglulysglupheserglu245250255valgluglyargileglnaspleuglulystyrvalgluaspglygly260265270glyglyserglyglyglyglysertyrtyrmetasnasnthrglupro275280285leucysaspalaglnglyphealapropheserlysaspasnglyile290295300argileglyserargglyhisvalphevalileargglupropheval305310315320sercysserproserglucysargthrphepheleuthrglnglyser325330335leuleuasnasplyshisserasnglythrvallysaspargserpro340345350tyrargthrleumetservallysileglyglnserproasnvaltyr355360365glnalaargphegluservalalatrpseralathralacyshisasp370375380glylyslystrpmetthrileglyvalthrglyproaspasnglnala385390395400thralailevalasntyrglyglyileprovalaspileileasnser405410415trpgluglyaspileleuargthrglnglusersercysthrcysile420425430lysglyasncystyrtrpvalmetthraspglyproalaasnarggln435440445alalystyrargilephelysalalysaspglyargvalileglygln450455460thraspileserpheasnglyglyhisilegluglucyssercystyr465470475480proasngluglylysvalglucysilecysargaspasntrpthrgly485490495thrasnargproileleuvalileserseraspleusertyrargval500505510glytyrleucysalaglyileprothraspthrproargglygluasp515520525serglnphethrglysercysthrserproleuglyasnlysglytyr530535540glyvallysglypheglypheargglnglythraspvaltrpalagly545550555560argthrileserargthrserargserglyphegluileilelysile565570575argasnglytrp580<210>5<211>1740<212>dna<213>人工序列()<400>5agtttctttagccgactgaattggctaacaaaatccggaagctcttaccccacattgaat60gtgacaatgcctaacaataaaaatttcgacaagctatacatctgggggatccatcacccg120agctcaaatcaagagcagacaaaattgtacatccaagaatcagggcgagtaacagtctca180acaaaaagaagtcaacaaacaataatccctaacatcgggtctagaccatggatcagaggt240caatcaggtaggataagcatatactggaccattgtaaaacctggagatatcctaatgata300aacagtaatggcaacttagttgcaccgcggggatattttaaattgaaaacagggaaaagc360tctgtaatgagatcagatgtacccatagacatttgtgtgtctgagtgtattacaccaaat420ggaagcatctccaacgacaagccattccaaaatgtgaacaaagttacatatggaaaatgc480cccaagtatatcaggcaaaacactttaaagctggccactgggatgaggaatgtaccagaa540aagcaaatcagaggaatctttggggcaatagcgggattcatcgaaaacggctgggaagga600atggttgatggatggtatgggttccgataccaaaactctgaaggaacagggcaagctgca660gatctaaagagcactcaagcagccatcgaccagatcaatggaaagttaaacagagtgatt720gaaagaaccaatgagaaattccatcaaatagagaaggaattctcagaagtagaaggaaga780attcaggacttggagaaatatgtagaagacggaggaggaggatctggaggaggaggatct840tactacatgaacaacaccgaaccactttgtgatgcccaaggctttgcaccattttccaaa900gataatggaatacgaattgggtcgagaggccatgtttttgtgataagagaaccttttgta960tcatgttcgccctcagaatgtagaacctttttcctcacacagggctcattactcaatgac1020aaacattctaacggcacagtaaaggatcgaagtccatataggactttgatgagtgtcaaa1080atagggcaatcacctaatgtgtatcaagctaggtttgaatcagtggcatggtcagcaaca1140gcatgccacgatggaaaaaaatggatgacaattggagtcacagggcccgacaatcaagca1200accgcaatagtgaactatgggggcattccagttgatattattaattcatgggaaggggac1260atattaagaacccaagaatcatcatgcacctgcattaaaggaaactgttattgggtaatg1320actgatggaccagcaaataggcaagccaaatacaggatattcaaagcaaaagatggaaga1380gtaattggacagaccgatataagtttcaatgggggacacatagaggagtgttcttgttac1440cccaatgaagggaaggtggaatgcatatgcagggacaattggactggaacaaatagacca1500attctggtaatatcttctgatttatcgtacagagttggatatttgtgtgctggcattccc1560actgacactcctaggggagaggatagtcaattcacaggctcatgtacaagtcctttggga1620aataaagggtacggtgtaaaaggttttgggtttcgacaaggaactgacgtatgggccgga1680aggacaattagtaggacttcgagatcaggattcgaaataataaaaatcaggaatggttgg1740<210>6<211>24<212>dna<213>人工序列()<400>6ccaagcttagtttctttagccgac24<210>7<211>24<212>dna<213>人工序列()<400>7cccccgggccaaccattcctgatt24当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1