一种靶向治疗心肌损伤的纳米载体及应用的制作方法
本发明属于生物医药技术领域,尤其涉及一种靶向治疗心肌损伤的纳米载体及应用。
背景技术:
心肌梗死是世界范围内死亡率和发病率的主要原因,心肌梗死可导致多达10亿个心肌细胞的损失。由于心肌受伤后的再生能力非常有限,丢失的细胞被纤维化瘢痕组织所取代,导致心脏衰竭。虽然手术治疗降低了与心肌梗死相关的死亡率,但由于梗塞心肌细胞不能再生,从而损害了心脏功能。尽管已经做了大量的努力来预防、限制或治疗心力衰竭,但迄今为止,仍然没有能够成功恢复受伤心脏功能的治疗方法。
据报道,小药物分子有可能用于心肌的生成。在过去的几年中,发现了它们在缓解心肌梗塞、心绞痛、心律不齐、高血压和其他心血管疾病的症状方面具有特殊的有效性,如从丹参中提取的丹参酮iia得到了极大的关注,丹参酮iia含有雌性激素环(植物雌激素),其被中国医学从业者广泛应用于抗氧化、抗炎和抗增生。
在急性心肌缺血中,缺血心肌会产生心房肽,以减少左心室壁的应力,从而诱导心肌梗死的修复和愈合。心房肽可以通过与特定的受体结合,心肌细胞和非肌细胞均表达心房肽,如心脏成纤维细胞。
微纳米载体材料和纳米技术在心血管疾病治疗中应用是一个相对较新的领域,它是一种很有前途的治疗和诊断方法。这些载体可用作为短寿命的细胞因子、生长因子或水溶性分子药物的输送载体,由于材料特性和可调特性,输送载体系统的主要优点有:有效载荷保护、延长和增强药物治疗效果,降低药物管理频率,从而提高患者的依从性。由于纳米胶束可为治疗药物提供稳定的外壳保护而不被降解,生物相容性好,具有靶向性,常被用作药物载体。
传统的药物治疗和手术治疗肃然降低了心肌梗死的死亡率,但梗塞的心肌细胞不能再生,从而损害了心脏的功能。此外,在缺血性心脏组织中移植的干细胞由于梗死区的氧化性和炎症性微环境而受到细胞凋亡和坏死的影响,严重限制了干细胞移植的治疗效率。传统的纳米材料因其在运载药物时没有特异性,这导致对正常细胞产生了一定的毒副作用。
因此,有必要制备出一种能负载丹参酮iia且靶向治疗心肌损伤的纳米载体,以减轻丹参酮iia的毒副作用和控制丹参酮iia的释放率。
技术实现要素:
本发明目的在于克服现有技术存在的不足,而提供一种靶向治疗心肌损伤的纳米载体及应用,该纳米载体结合丹参酮iia后形成纳米复合物,纳米复合物能靶向治疗心肌损伤和有效控制释放率,提高了心肌修复的特异性以及增强了心肌修复的治疗效果。
为实现上述目的,本发明采取的技术方案为:一种负载丹参酮iia的纳米载体的制备方法,其依次包括以下步骤:
s1)将羧基盐化的聚乳酸-乙醇酸溶解至二氯甲烷中,再加入n-羟基琥珀酰亚胺和1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐,活化生成聚乳酸-乙醇酸-n-羟基琥珀酰亚胺;活化反应后,再依次进行冰乙醚沉淀、透析(透析除去多余的n-羟基琥珀酰亚胺)和真空干燥;聚乳酸-乙醇酸-n-羟基琥珀酰亚胺的缩写为plg-nhs,plg-nhs为式(ⅰ)所示结构的聚合物;
其中,n≥2;
s2)将plg-nhs溶解至三氯甲烷中,并加入氨基聚乙二醇羧基和n,n-二异丙基乙胺,活化生成聚乳酸-乙醇酸-聚乙二醇;活化反应后,再依次进行冰甲醇沉淀、冰甲醇清洗(除去多余的nh2-peg-cooh)和真空干燥;聚乳酸-乙醇酸-聚乙二醇的缩写为plg-peg,plg-peg为式(ⅱ)所示结构的聚合物,氨基聚乙二醇羧基的缩写为nh2-peg-cooh;
其中,n≥2,m≥1;
s3)将心房肽溶解至磷酸盐缓冲液中,配制成心房肽溶液;再将心房肽溶液加入到已调好ph值的plga-peg溶液中(溶剂可为去离子水),常温反应生成聚乳酸-乙醇酸-聚乙二醇-心房肽;反应结束后,转移到超滤离心管中进行超滤(去除未反应的聚合物和多肽),再冷冻干燥即可;聚乳酸-乙醇酸-聚乙二醇-心房肽的缩写为plga-peg-anp,plga-peg-anp为式(ш)所示结构的聚合物,在plga-peg-anp中,心房肽末端的氨基与plga-peg中羟基进行脱水缩合反应;
其中,n≥2,m≥1,anp表示心房肽。
作为上述技术方案的改进,在步骤s1中,聚乳酸-乙醇酸、n-羟基琥珀酰亚胺和1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐的物质的量比为(0.1~1):(1~10):1,二氯甲烷、聚乳酸-乙醇酸、n-羟基琥珀酰亚胺和1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐总体积与二氯甲烷体积的比为5~20:1,活化反应的时间为4~12h,二氯甲烷、聚乳酸-乙醇酸、n-羟基琥珀酰亚胺和1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐总体积与冰乙醚体积的比为1:(10~20),透析采用截留分子量为500~3500的透析袋,真空干燥的温度为40~60℃,真空干燥的时间为12~24h。
优选地,聚乳酸-乙醇酸、n-羟基琥珀酰亚胺和1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐的物质的量比为0.25:2:1,二氯甲烷、聚乳酸-乙醇酸、n-羟基琥珀酰亚胺和1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐总体积与二氯甲烷体积的比为10:1,活化反应的时间为8h,透析采用截留分子量为1000的透析袋,真空干燥的温度为40℃。
作为上述技术方案的改进,在步骤s2中,plga-nhs与n,n-二异丙基乙胺的物质的量比为1:(1~10),活化反应时间为4~12h,plga-nhs、n,n-二异丙基乙胺、三氯甲烷和氨基聚乙二醇羧基总体积与三氯甲烷体积的比为(5~20):1,plga-nhs、n,n-二异丙基乙胺、三氯甲烷和氨基聚乙二醇羧基总体积与冰甲醇体积的比为1:(10~20),真空干燥的温度为40~60℃,真空干燥的时间为12~24h。
优选地,在步骤s2中,plga-nhs与n,n-二异丙基乙胺的物质的量比为1:1,活化反应时间为6h,plga-nhs、n,n-二异丙基乙胺、三氯甲烷和氨基聚乙二醇羧基总体积与三氯甲烷体积的比为10:1,真空干燥的温度为40℃。
作为上述技术方案的改进,在步骤s3中,心房肽与plga-peg的物质的量比为1:(1~10),plga-peg溶液的ph值为6~7,磷酸盐缓冲液ph值为<7.2,常温反应的时间为2~6h,超滤的转速为12000rpm超滤的时间为30min,冷冻干燥的时间为24~48h。
优选地,在步骤s3中,心房肽与plga-peg的物质的量比为1:5,超滤离心管的型号为mwco10000。
另外,本发明还提供一种靶向治疗心肌损伤的纳米载体,所述纳米载体为所述制备方法制备的的聚乳酸-乙醇酸-聚乙二醇-心房肽或其药用酸加成盐,所述纳米载体为纳米胶束,纳米载体的直径为20~80nm。
另外,本发明还提供一种负载丹参酮iia的纳米复合物的制备方法,其包括以下步骤:以丹参酮iia和所述的纳米载体为原料,采用薄膜水化法制备出负载丹参酮iia的纳米复合物,所述纳米复合物的直径为20~80nm。
作为上述技术方案的改进,将纳米载体和丹参酮iia溶解在丙酮中,混合后旋转蒸发直至形成薄膜;薄膜烘干后,依次进行磷酸盐缓冲液复溶、水浴加热和透析(透析除掉未封装的丹参酮iia),即得负载丹参酮iia的纳米复合物,纳米复合物的缩写为plga-peg-anp/tan;
纳米载体与丹参酮iia的质量比是(1~10):1,丹参酮iia与丙酮的料液比为8:(1~10)mg/ml,旋转蒸发的温度为40~60℃,水浴加热的温度为40~80℃,水浴加热的时间为4~12h,透析采用截留分子量为500~3500的透析袋,冷冻干燥的时间为24~48h;优选地,纳米载体与丹参酮iia的质量比是5:1,丹参酮iia与丙酮的料液比为8:5mg/ml,旋转蒸发的温度为40~60℃,透析采用截留分子量为3500的透析袋。
另外,本发明还提供一种采用所述的纳米复合物的制备方法制备出的纳米复合物。
另外,本发明还提供所述的纳米复合物在制备用于靶向治疗心肌缺血损伤药物中的应用。
另外,本发明还提供一种包括所述的纳米复合物的药物,其还包括药学上可接受的辅料。
本发明的有益效果在于:本发明提供一种靶向治疗心肌损伤的纳米载体及应用,本发明纳米载体以聚乙二醇和聚乳酸-乙醇酸为原料,反应生成plga-peg,再接枝具有心肌靶向功能的心房肽anp,纳米载体负载丹参酮iia(tan)成为直径为20~80nm的纳米复合物,纳米复合物对心肌梗塞后的心脏损伤进行靶向性修复:既可以降低丹参酮iia对其他组织细胞的副作用,又可以使丹参酮iia得到合适的释放;将负载丹参酮iia药物的纳米载体静脉注射入体内,可对损伤的心肌组织进行修复与再生。
附图说明
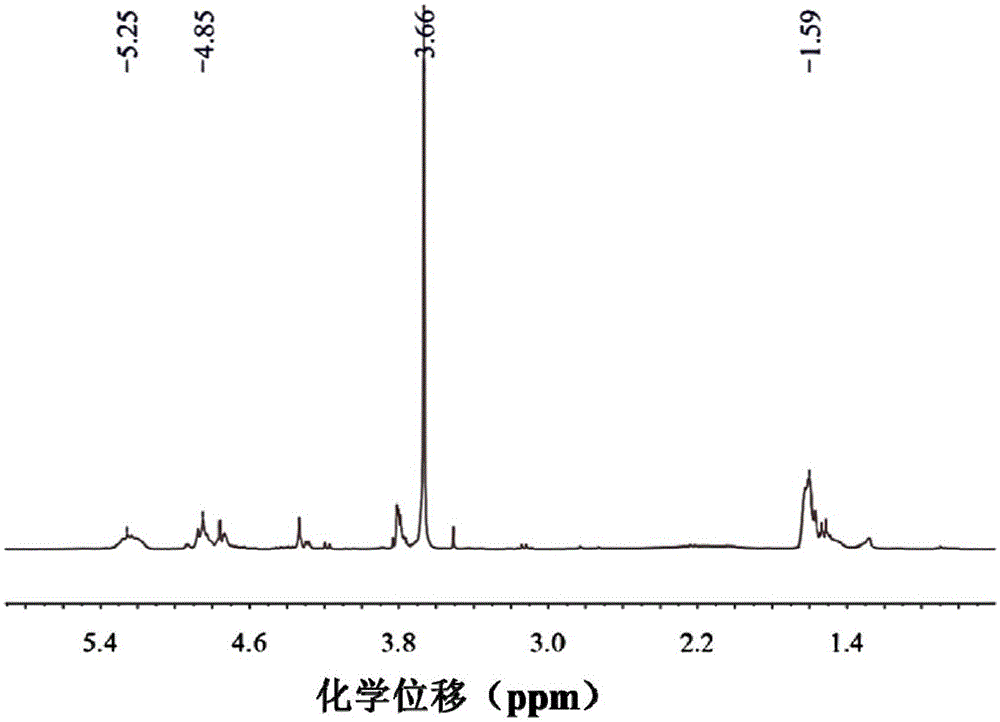
图1为本发明实施例制备的plga-peg的1h·nmr图;
图2为本发明实施例制备的plga-peg-anp的临界胶束图;
图3为本发明实施例制备的纳米载体和纳米复合物的透射电镜图,其中,3a为纳米载体的透射电镜图,3b为纳米复合物的透射电镜图;
图4为丹参酮iia释放曲线图;
图5显示纳米载体和纳米复合物对细胞存活率的影响。
具体实施方式
为更好地说明本发明的目的、技术方案和优点,下面将结合具体实施例、和附图对本发明作进一步说明。
实施例1
本实施例提供一种负载丹参酮iia的纳米载体的制备方法,其依次包括以下步骤:
s1)将羧基盐化的聚乳酸-乙醇酸溶解至二氯甲烷中,再加入n-羟基琥珀酰亚胺和1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐,活化生成聚乳酸-乙醇酸-n-羟基琥珀酰亚胺;活化反应后,再依次进行冰乙醚沉淀、透析和真空干燥;聚乳酸-乙醇酸-n-羟基琥珀酰亚胺的缩写为plg-nhs,plg-nhs为式(ⅰ)所示结构的聚合物;
其中,n≥2;
s2)将plg-nhs溶解至三氯甲烷中,并加入氨基聚乙二醇羧基和n,n-二异丙基乙胺,活化生成聚乳酸-乙醇酸-聚乙二醇;活化反应后,再依次进行冰甲醇沉淀、冰甲醇清洗和真空干燥;聚乳酸-乙醇酸-聚乙二醇的缩写为plg-peg,plg-peg为式(ⅱ)所示结构的聚合物,氨基聚乙二醇羧基的缩写为nh2-peg-cooh;
其中,n≥2,m≥1;
s3)将心房肽溶解至磷酸盐缓冲液中,配制成心房肽溶液;再将心房肽溶液加入到已调好ph值的plga-peg溶液中,常温反应生成聚乳酸-乙醇酸-聚乙二醇-心房肽;反应结束后,转移到超滤离心管中进行超滤,再冷冻干燥即可;聚乳酸-乙醇酸-聚乙二醇-心房肽的缩写为plga-peg-anp,plga-peg-anp为式(ш)所示结构的聚合物,在plga-peg-anp中,心房肽末端的氨基与plga-peg中羟基进行脱水缩合反应;
其中,n≥2,m≥1,anp表示心房肽;
在步骤s1中,聚乳酸-乙醇酸、n-羟基琥珀酰亚胺和1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐的物质的量比为0.25:2:1,二氯甲烷、聚乳酸-乙醇酸、n-羟基琥珀酰亚胺和1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐总体积与二氯甲烷体积的比为10:1,活化反应的时间为8h,二氯甲烷、聚乳酸-乙醇酸、n-羟基琥珀酰亚胺和1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐总体积与冰乙醚体积的比为1:15,透析采用截留分子量为1000的透析袋,真空干燥的温度为40℃,真空干燥的时间为24h;
在步骤s2中,plga-nhs与n,n-二异丙基乙胺的物质的量比为1:1,活化反应时间为6h,plga-nhs、n,n-二异丙基乙胺、三氯甲烷和氨基聚乙二醇羧基总体积与三氯甲烷体积的比为10:1,plga-nhs、n,n-二异丙基乙胺、三氯甲烷和氨基聚乙二醇羧基总体积与冰甲醇体积的比为1:15,真空干燥的温度为40℃,真空干燥的时间为24h;
在步骤s3中,心房肽与plga-peg的物质的量比为1:5,plga-peg溶液的ph值为6~7,磷酸盐缓冲液ph值为<7.2,常温反应的时间为2h,超滤的转速为12000rpm超滤的时间为30min,超滤离心管的型号为mwco10000,冷冻干燥的时间为24h。
另外,本实施例还提供负载丹参酮iia的纳米复合物的制备方法,其包括以下步骤:将上述纳米载体和丹参酮iia溶解在丙酮中,混合后旋转蒸发直至形成薄膜;薄膜烘干后,依次进行磷酸盐缓冲液复溶、水浴加热和透析,即得负载丹参酮iia的纳米复合物,纳米复合物的缩写为plga-peg-anp/tan;
纳米载体与丹参酮iia的质量比是5:1,丹参酮iia与丙酮的料液比为8:5mg/ml,旋转蒸发的温度为40℃,水浴加热的温度为40℃,水浴加热的时间为12h,透析采用截留分子量为3500的透析袋,冷冻干燥的时间为36h。
实施例2
本实施例提供一种负载丹参酮iia的纳米载体的制备方法,其与实施例1的区别点在于:
1)在步骤s1中,聚乳酸-乙醇酸、n-羟基琥珀酰亚胺和1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐的物质的量比为0.1:10:1,二氯甲烷、聚乳酸-乙醇酸、n-羟基琥珀酰亚胺和1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐总体积与二氯甲烷体积的比为5:1,活化反应的时间为4h,二氯甲烷、聚乳酸-乙醇酸、n-羟基琥珀酰亚胺和1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐总体积与冰乙醚体积的比为1:10,透析采用截留分子量为500的透析袋,真空干燥的温度为50℃,真空干燥的时间为19h;
2)在步骤s2中,plga-nhs与n,n-二异丙基乙胺的物质的量比为1:5,活化反应时间为4h,plga-nhs、n,n-二异丙基乙胺、三氯甲烷和氨基聚乙二醇羧基总体积与三氯甲烷体积的比为5:1,plga-nhs、n,n-二异丙基乙胺、三氯甲烷和氨基聚乙二醇羧基总体积与冰甲醇体积的比为1:10,真空干燥的温度为50℃,真空干燥的时间为17h;
3)在步骤s3中,心房肽与plga-peg的物质的量比为1:1,plga-peg溶液的ph值为6~7,磷酸盐缓冲液ph值为<7.2,常温反应的时间为4h,超滤的转速为12000rpm超滤的时间为30min,超滤离心管的型号为mwco10000,冷冻干燥的时间为35h。
另外,本实施例还提供负载丹参酮iia的纳米复合物的制备方法,其与实施例1的区别点在于:纳米载体与丹参酮iia的质量比是1:1,丹参酮iia与丙酮的料液比为8:1mg/ml,旋转蒸发的温度为50℃,水浴加热的温度为60℃,水浴加热的时间为8h,透析采用截留分子量为2500的透析袋,冷冻干燥的时间为24h。
实施例3
本实施例提供一种负载丹参酮iia的纳米载体的制备方法,其与实施例1的区别点在于:
1)在步骤s1中,聚乳酸-乙醇酸、n-羟基琥珀酰亚胺和1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐的物质的量比为1:1:1,二氯甲烷、聚乳酸-乙醇酸、n-羟基琥珀酰亚胺和1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐总体积与二氯甲烷体积的比为20:1,活化反应的时间为12h,二氯甲烷、聚乳酸-乙醇酸、n-羟基琥珀酰亚胺和1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐总体积与冰乙醚体积的比为1:20,透析采用截留分子量为3500的透析袋,真空干燥的温度为60℃,真空干燥的时间为12h;
2)在步骤s2中,plga-nhs与n,n-二异丙基乙胺的物质的量比为1:10,活化反应时间为12h,plga-nhs、n,n-二异丙基乙胺、三氯甲烷和氨基聚乙二醇羧基总体积与三氯甲烷体积的比为20:1,plga-nhs、n,n-二异丙基乙胺、三氯甲烷和氨基聚乙二醇羧基总体积与冰甲醇体积的比为1:20,真空干燥的温度为60℃,真空干燥的时间为12h;
3)在步骤s3中,心房肽与plga-peg的物质的量比为1:10,plga-peg溶液的ph值为6~7,磷酸盐缓冲液ph值为<7.2,常温反应的时间为6h,超滤的转速为12000rpm超滤的时间为30min,超滤离心管的型号为mwco10000,冷冻干燥的时间为48h。
另外,本实施例还提供负载丹参酮iia的纳米复合物的制备方法,其与实施例1的区别点在于:纳米载体与丹参酮iia的质量比是10:1,丹参酮iia与丙酮的料液比为8:10mg/ml,旋转蒸发的温度为60℃,水浴加热的温度为80℃,水浴加热的时间为4h,透析采用截留分子量为500的透析袋,冷冻干燥的时间为48h。
实施例4
本实施例提供一种负载丹参酮iia的纳米载体的制备方法,其与实施例1的区别点在于:
1)在步骤s1中,聚乳酸-乙醇酸、n-羟基琥珀酰亚胺和1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐的物质的量比为1:10:1,二氯甲烷、聚乳酸-乙醇酸、n-羟基琥珀酰亚胺和1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐总体积与二氯甲烷体积的比为13:1,活化反应的时间为8h,二氯甲烷、聚乳酸-乙醇酸、n-羟基琥珀酰亚胺和1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐总体积与冰乙醚体积的比为1:16,透析采用截留分子量为1000的透析袋,真空干燥的温度为40℃,真空干燥的时间为24h;
2)在步骤s2中,plga-nhs与n,n-二异丙基乙胺的物质的量比为1:6,活化反应时间为6h,plga-nhs、n,n-二异丙基乙胺、三氯甲烷和氨基聚乙二醇羧基总体积与三氯甲烷体积的比为14:1,plga-nhs、n,n-二异丙基乙胺、三氯甲烷和氨基聚乙二醇羧基总体积与冰甲醇体积的比为1:13,真空干燥的温度为40℃,真空干燥的时间为24h;
3)在步骤s3中,心房肽与plga-peg的物质的量比为1:7,plga-peg溶液的ph值为6~7,磷酸盐缓冲液ph值为<7.2,常温反应的时间为6h,超滤的转速为12000rpm超滤的时间为30min,超滤离心管的型号为mwco10000,冷冻干燥的时间为48h。
另外,本实施例还提供负载丹参酮iia的纳米复合物的制备方法,其与实施例1的区别点在于:纳米载体与丹参酮iia的质量比是8:1,丹参酮iia与丙酮的料液比为8:7mg/ml,旋转蒸发的温度为60℃,水浴加热的温度为80℃,水浴加热的时间为4h,透析采用截留分子量为3500的透析袋,冷冻干燥的时间为48h。
实施例5
本实施例提供一种负载丹参酮iia的纳米载体的制备方法,其与实施例1的区别点在于:
在步骤s1中,聚乳酸-乙醇酸、n-羟基琥珀酰亚胺和1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐的物质的量比为0.1:1:1;
另外,本实施例还提供负载丹参酮iia的纳米复合物的制备方法,其与实施例1的区别点在于:纳米载体与丹参酮iia的质量比是9:1。
纳米载体及纳米复合物的特性测定
1)本发明实施例制备的聚乳酸-乙醇酸-聚乙二醇(plga-peg)溶解于氘代氯仿中进行核磁氢谱表征。如图1所示,5.25ppm处的特征峰归因于(-o-ch-(ch3)-)中的次甲基氢;4.85ppm处的特征峰归因于(-o-ch2-o-)中的亚甲基氢;3.7ppm处的特征峰归因于(-ch2-ch2-o-)中的亚甲基氢;1.6ppm处的特征峰归因于(-o-ch-(ch3)-)的甲基氢。由此可见,本发明实施例成功合成了plga-peg。
2)将芘用丙酮配置成浓度为6×10-7mol/l的芘溶液,再用去离子水为溶剂将本发明实施例制备的的聚乳酸-乙醇酸-聚乙二醇-心房肽(plga-peg-anp)配置成连续的不同浓度的溶液;取20个ep管,每个ep管中加入等量的芘溶液,置于通风厨中过夜将丙酮自然挥发干净;然后依次向每个ep加入1ml不同浓度的plga-peg-anp溶液,超声处理30min,再置于60℃恒温水浴30min,待温度降至40℃后,恒温过夜,再使用荧光分光光度计分别测定不同浓度的plga-peg-anp溶液的荧光谱图;设置荧光扫描的激发波长为337nm,扫描范围为360~450nm,扫描速度设置为1200nm/min,激发狭缝设置为2.5nm,发射狭缝设置为10nm。
如图2所示,交叉点出得到plga-peg-anp的cmc值为0.0836mg/ml,可见在水溶液中plga-peg-anp可以形成胶束,且形成胶束的最低浓度为0.0836mg/ml。
3)将本发明实施例制备的聚乳酸-乙醇酸-聚乙二醇-心房肽/丹参酮iia(plga-peg-anp/tan,纳米复合物)与载药前的聚乳酸-乙醇酸-聚乙二醇-心房肽(plga-peg-anp,纳米载体)进行透射电镜表征。
如图3所示,plga-peg-anp和plga-peg-anp/tan胶束都呈现出一个球形或椭圆的几何形状,直径为20~80nm。此外,纳米复合物的胶束颗粒大小明显增加;可见plga-peg-anp可形成球形胶束并且可以成功的包载药物丹参酮iia。
4)准确称取10mg本发明实施例制备的纳米复合物置于截留分子3500的透析袋中,透析袋两头用绳子扎紧,再将透析袋放置到10ml含有不同浓度的pbs释放液中,室温(25~30℃)摇床振荡24h,缓释液为含有0.1%的吐温-80。开始计时,分别在预先设定时间点即0.5、1、2、4、8、12、24h取5ml释放液于ep管(取5ml的目的在于使后面的时间药物更好释放),然后补加入等量的含等体积的含有吐温-80的pbs溶液于相同条件下进行后续释放实验(可积累几个时间段的样品一起测)用uv-vis检测取出的上清液中丹参酮iia浓度,计算丹参酮iia的累积释放百分数;每个样品平行做三次,结果以平均值和标准偏差表示。
如图4所示,药物参酮iia的释放速率在最初12小时内是快速的,高达85%,12小时之后,随着时间的延长,参酮iia的释放速率开始变慢,趋于平缓。由此可见,plga-peg-anp纳米载体的缓释效果良好。
5)通过cck-8法对本发明实施例制备的纳米载体plga-peg-anp和纳米复合物plga-peg-anp/tan进行细胞活性检测。本实验所用的细胞是成纤维细胞(3t3细胞),而培养该细胞所用的培养液是含有10%的胎牛血清和1%的双抗(青霉素和链霉素的混合液)的dmem培养液,并且培养条件是在温度为37℃和co2浓度为5%的培养箱中;在培养的过程中,每两天要给细胞换一次培养液,换细胞培养液的目的是为细胞增加新的营养物质、去除不贴壁的细胞以及细胞的代谢物;将不同浓度的plga-peg-anp和plga-peg-anp/tan培养基溶液加入96孔板中,然后放在培养箱中,培养到1天后加入cck-8试剂,按照1:10的比例加入,也就是说100μl的培养液加入10μl的cck-8试剂,继续培养2~4h;在450nm波长的条件下,使用酶标仪读取每个孔的吸光光度值。
如图5所示,各实验组对3t3细胞的一直呈现出浓度依赖性,而且当浓度低于0.5mg/ml时,plga-peg-anp表现出的微乎其微的细胞毒性,细胞存活率都在80%以上;当浓度在0.5mg/ml浓度以上时,plga-peg-anp和plga-peg-anp/tan纳米胶束的细胞存活率都有所下降,而且plga-peg-anp/tan纳米胶束下降的更厉害。当浓度低于0.5mg/ml时,plga-peg-anp表现出的微乎其微的细胞毒性,而通常静脉注射的浓度都低于0.5mg/ml;由此可见,纳米载体plga-peg-anp具有较好的生物相容性。
最后所应当说明的是,以上实施例用以说明本发明的技术方案而非对本发明保护范围的限制,尽管参照较佳实施例对本发明作了详细说明,本领域的普通技术人员应当理解,可以对本发明的技术方案进行修改或者同等替换,而不脱离本发明技术方案的实质和范围。
- 还没有人留言评论。精彩留言会获得点赞!