一种利用毛细管电泳荧光SSR指纹图谱鉴别白蜡新品种金箭的方法与流程
本发明属于植物品种分子鉴定技术领域,具体而言,涉及一种利用毛细管电泳荧光ssr指纹图谱鉴别白蜡新品种‘金箭’的方法。
背景技术:
白蜡属植物为风媒花,混栽时很容易发生天然授粉杂交,尤其是绒毛白蜡(f.velutina)、红枔(f.pennsylvanica)、白枔(f.americana)等同为枔亚属样组,其形态特征非常相似,亲缘关系极为亲近,杂交后代传统的方法往往无法区分。以往在区分种苗时都是采用宏观遗传分析生物学特性和形态特征指标,但难以区分形态极为相似或亲缘关系极近的种苗,尤其是种内不同水平的良种更是无法识别,以致生产中出现混种、混系、混株,以假乱真的情况,其结果给生产带来了极大损失。在分子水平上对种质进行鉴定不受环境和生长阶段的影响,结果稳定,可靠性强。因此,寻求从分子水平真正准确识别白蜡良种极具现实意义。
简单重复序列(simple5equencerepeat,ssr)分子标记具有信息含量高、共显性遗传、数量丰富、分析方法简单、结果重复性好、省时省力省钱等优点,目前ssr标记是种质鉴定方面最灵敏、最可靠的一种分子标记。而利用毛细管电泳荧光ssr分子标记技术,开发基于毛细管电泳荧光ssr指纹图谱鉴别某些形态特征相似,亲缘关系亲近植物品种的方法的虽有应用于玉米、水稻、大豆、小麦、棉花等作物中的报道,但应用于林木尤其是白蜡的相关报道并不多见。
白蜡新品种‘金箭’为绒毛白蜡(fraxinusvelutina‘jinjian’)雄株,是由山东省林业科学研究院课题组培育的,2016年通过国家审定。该品种干形较直,耐盐碱,多年生,枝干黄色,当年生枝黄绿色,叶片革质且有光泽,适应范围广。但是在苗期的‘金箭’很难通过表型特征来进行鉴定,给操作者带来麻烦或对生产造成损失。因此,为了快速鉴定白蜡新品种‘金箭’,开发一种利用毛细管电泳荧光ssr指纹图谱鉴别白蜡新品种‘金箭’的方法具有重要意义。
技术实现要素:
针对现有技术的不足,本发明要解决的问题是供用一种利用毛细管电泳荧光ssr指纹图谱鉴别白蜡新品种‘金箭’的方法。
本发明所述利用毛细管电泳荧光ssr指纹图谱鉴别白蜡新品种‘金箭’的方法,步骤是:
(1)由白蜡幼嫩叶片提取白蜡基因组dna;
(2)以提取的dna为模板,利用筛选出的ssr引物对进行pcr扩增;
(3)将pcr扩增产物进行毛细管电泳;
(4)根据电泳结果中每对ssr引物的峰值,组合形成白蜡新品种‘金箭’的ssr指纹图谱,实现对白蜡新品种‘金箭’的鉴别;
其特征是:
步骤(1)中dna的提取采用ctab法,提取缓冲液中加入2%β-巯基乙醇和2%pvp;紫外分光光度法测定dna的浓度和纯度,稀释至30ng·μl-1,-20℃保存,备用;
步骤(2)筛选出的ssr引物对为6对,分别是f186和r186,f187和r187,f202和r202,f203和r203,f208和r208,f213和213其中在每对引物5′端加有选自fam、tamra、hex和rox中的任意一种荧光标记,正向引物为与携带荧光标记的tp-m13引物组成;所述f186和r186引物对中f186的核苷酸序列是如seqidno.1所示的正向引物序列,r186的核苷酸序列是如seqidno.2所示的正向引物序列,所述f187和r187引物对中f187的核苷酸序列是如seqidno.3所示的正向引物序列,r187的核苷酸序列是如seqidno.4所示的正向引物序列,所述f202和r202引物对中f202的核苷酸序列是如seqidno.5所示的正向引物序列,r202的核苷酸序列是如seqidno.6所示的正向引物序列,所述f203和r203引物对中f203的核苷酸序列是如seqidno.7所示的正向引物序列,r203的核苷酸序列是如seqidno.8所示的正向引物序列,所述f208和r208引物对中f202的核苷酸序列是如seqidno.9所示的正向引物序列,r208的核苷酸序列是如seqidno.10所示的正向引物序列,所述f213和r213引物对中f213的核苷酸序列是如seqidno.11所示的正向引物序列,r213的核苷酸序列是如seqidno.12所示的正向引物序列;
pcr反应体系为10μl:10ng.μl-1的dna模板1μl、2xtaqpluspcrmastermix5μl、10μmol·l-1的正反向引物各0.1μl以及ddh2o共10μl;
pcr扩增程序采用touchdown模式:95℃预变性5min;95℃变性30s,56℃退火30s;每个循环降低0.5℃;72℃延伸30s,15个循环;95℃变性30s,54℃退火30s,72℃延伸30s,20个循环;72℃延伸10min,4℃保存;
步骤(3)所述将pcr扩增产物进行毛细管电泳的方法是:取pcr产物0.3μl、gs-500liz分子量内标0.5μl和去离子甲酰胺9.5μl混合加入pcr板,95℃变性5min,4℃冷却后离心,1×buffer缓冲液上机检测;采用3730xldna测序仪进行毛细管电泳:预电泳15kv下3min;1.6kv下进样15s;电泳15kv下20min;
步骤(4)所述的鉴别方法是:采用genemarkerz.2.0软件进行数据整理和图像分析,根据每对ssr引物的峰值,组合形成白蜡新品种‘金箭’的ssr指纹图谱;其中,f186和r186引物对的峰值为93/99,f187和r187引物对的峰值为134/140,f202和r202引物对的峰值为109/112,f203和r203引物对的峰值为157,f208和r208引物对的峰值为139/145,f213和r213引物对的峰值为81/90/96。
本发明还公开了用于上述方法的ssr引物对,其特征是:所述ssr引物对为6对,分别是f186和r186,f187和r187,f202和r202,f203和r203,f208和r208,f213和213其中在每对引物5′端加有fam荧光标记,正向引物为与携带荧光标记的tp-m13引物组成;所述f186和r186引物对中f186的核苷酸序列是如seqidno.1所示的正向引物序列,r186的核苷酸序列是如seqidno.2所示的正向引物序列,所述f187和r187引物对中f187的核苷酸序列是如seqidno.3所示的正向引物序列,r187的核苷酸序列是如seqidno.4所示的正向引物序列,所述f202和r202引物对中f202的核苷酸序列是如seqidno.5所示的正向引物序列,r202的核苷酸序列是如seqidno.6所示的正向引物序列,所述f203和r203引物对中f203的核苷酸序列是如seqidno.7所示的正向引物序列,r203的核苷酸序列是如seqidno.8所示的正向引物序列,所述f208和r208引物对中f202的核苷酸序列是如seqidno.9所示的正向引物序列,r208的核苷酸序列是如seqidno.10所示的正向引物序列,所述f213和r213引物对中f213的核苷酸序列是如seqidno.11所示的正向引物序列,r213的核苷酸序列是如seqidno.12所示的正向引物序列。具体的,所述6对ssr引物对信息见表1。
表1:6对ssr引物对信息
本发明所述的ssr引物对在构建白蜡新品种‘金箭’的ssr指纹图谱中的应用。
本发明根据转录组测序获得的序列数据设计并通过大量的筛选,选出特异性稳定、多态性好的6对ssr特异引物,用于构建白蜡新品种‘金箭’的ssr指纹图谱;具有分辨率高、操作简便、快速、结果准确等特点,能够快速实现白蜡新品种‘金箭’样品的鉴定。
本发明提供了一种白蜡新品种‘金箭’的ssr指纹图谱,其特征是:所述图谱由上述利用毛细管电泳荧光ssr指纹图谱鉴别白蜡新品种‘金箭’方法中的相关步骤构建获得。
上述白蜡新品种‘金箭’的ssr指纹图谱中,ssr引物f186和r186引物对的峰值为93/99,f187和r187引物对的峰值为134/140,f202和r202引物对的峰值为109/112,f203和r203引物对的峰值为157,f208和r208引物对的峰值为139/145,f213和r213引物对的峰值为81/90/96。
与现有技术相比,本发明的优益效果体现在:
1)本发明提供的方法是一种从分子水平上快速、高效鉴定白蜡新品种方法,具有快速、准确、操作方便等优势,并且鉴定结果不易受环境影响。
2)本发明利用毛细管电泳荧光标记电泳技术,克服了聚丙烯酞胺凝胶电泳的不足,能准确读出产物片段的大小,精确度达到lbp之内,能对品种进行精确鉴定,而且成本较低,应用价值大。
3)本发明提供的ssr引物对以及白蜡新品种‘金箭’的ssr指纹图谱为dna指纹图谱的在白蜡上的进一步应用研究提供了坚实的理论支持。
附图说明
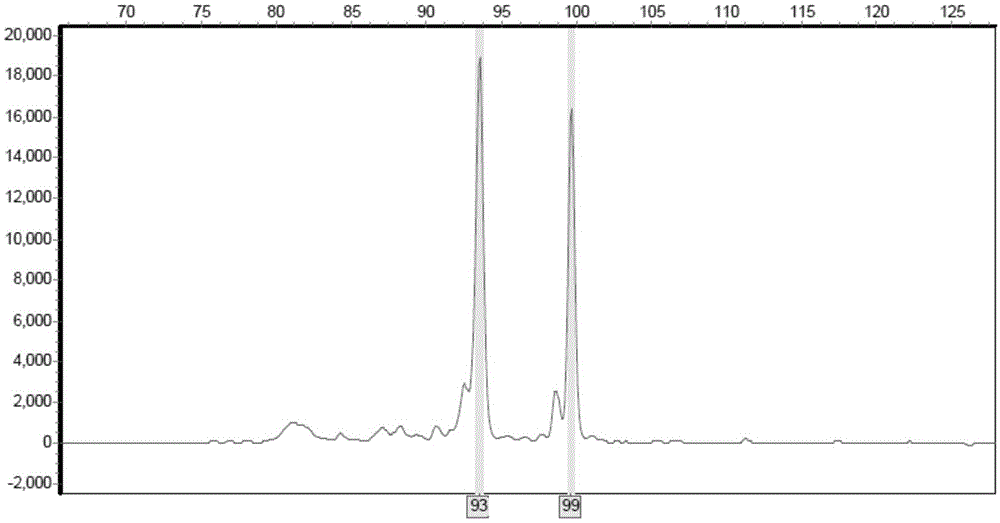
图1:ssr引物对186在‘金箭’中的pcr扩增产物毛细管电泳图。
图2:ssr引物对187在‘金箭’中的pcr扩增产物毛细管电泳图。
图3:ssr引物对202在‘金箭’中的pcr扩增产物毛细管电泳图。
图4:ssr引物对203在‘金箭’中的pcr扩增产物毛细管电泳图。
图5:ssr引物对208在‘金箭’中的pcr扩增产物毛细管电泳图。
图6:ssr引物对213在‘金箭’中的pcr扩增产物毛细管电泳图。
具体实施方式
实施例1
1.鉴定材料
选用‘金箭’幼嫩叶片提取基因组dna。
2.dna的提取
2.1将配制好的ctab提取缓冲液置于65℃的水浴锅中预热30min,氯仿一异戊醇(24:1)、无水乙醇、70%乙醇置于-20℃冰箱预冷备用,研钵需提前预冷,使用前再用少量液氮预冷;
2.2取0.4-0.5g白蜡幼叶,加充足液氮研磨至粉末状,迅速转入2ml离心管中,加入600μl2%的ctab提取液(含2%β-巯基乙醇),充分混匀。在65℃的水浴锅中水浴30min,其间轻轻颠倒3-4次;
2.3冷至室温后加入600μl的氯仿:异戊醇(24:1)抽提10min,其间不停地轻轻地摇动,冷却至室温,在12000r/min离心10min;
2.4将上清液(约500μl)转入另一离心管中,加等体积氯仿:异戊醇(24:l)重复步骤2.3;
2.5取出上清液并移到另一个干净的1.5ml的离心管中,再加1ml的预冷无水乙醇沉淀dna(-20℃放置30min),轻轻旋转离心管,出现絮状dna,-20℃放置1h,观察沉淀生成;
2.68000rmp室温离心5min,倒掉上清液,沉淀用1ml75%的酒精洗涤两次,超净工作台静置乙醇挥发干净。
2.7待dna风干后(dna不宜过分干燥,否则极难溶解),用适量的te(ph8.0、50μl)或超纯水溶解,4℃放置6-12h使其充分溶解;
2.8加入2μlrna酶10mg/ml,37℃水浴1h,-80℃保存备用;
3.dna定量和质量检测
3.1取2μldna用微量核酸蛋白检测仪检测,可以直接读出dna浓度和a260/a280的比值,比值在1.8~2.0之间符合要求。
3.2另取3μldna加1μl的溴酚蓝,在0.8%琼脂糖凝胶上电泳15min~20min,稳压100v,电泳缓冲液为1×tbe,325nm紫外灯下观察,照相,通过与标准溶液的荧光进行比较估测未知dna的浓度。
3.3植物总dna样品呈现一条相对分子量较大而迁移速率很小的清晰条带。
3.4将样品稀释成浓度为20ng/μl,在-80℃保存备用。
4.毛细管电泳系统检测
4.1在公知的196份资源中逐一筛选,选出多态性好的6对ssr引物(详细信息见表1),在每对引物5′端添加荧光标记fam(6-carboxy-fluorescein)。正向引物为与携带荧光标记的tp-m13引物组成,由山东华博基因工程有限公司合成。
表1:6对ssr引物对信息
4.2荧光标记毛细管电泳的pcr扩增采用10μl的反应体系:10ng.μl-1的dna模板1μl、2xtaqpluspcrmastermix5μl、正反向引物各0.1μl(10μmol·l-1)以及ddh2o共10μl。
4.3pcr扩增程序采用touchdown模式:95℃预变性5min;95℃变性30s,56℃退火30s(每个循环降低0.5℃),72℃延伸30s,15个循环;95℃变性30s,54℃退火30s,72℃延伸30s,20个循环;72℃延伸10min,4℃保存。
4.4pcr产物变性:pcr产物用双蒸水稀释10-20倍,取pcr产物0.3μl、分子量内标0.5μl和去离子甲酰胺9.5μl混匀加入pcr板;在pcr仪上运行变性程序:95℃变性5min,4℃冷却后离心,1×buffer缓冲液上机检测。
4.5pcr产物扩增检测:pcr产物检测采用美国abi公司生产的3730xldnaanalyzer基因分析仪,采用美国abi公司生产的50cm,96道毛细管电泳,预电泳15kv下3min;1.6kv下进样15s;电泳15kv下20min。
将上机结果原始文件导入genemarker2.2.0软件,进行数据收集和图像分析。
5.数据分析
根据筛选引物时确定的分子量大小及引物颜色进行分子量的确定,将收集的原始数据采用datacollection软件导入genemarker2.2.0系统进行分析。根据目标峰值大小系统软件与其泳道中的gs-500liz分子量内标进行比较,准确计算出目标dna片段大小,将电泳结果转化成pdf图片格式导出。
各荧光标记毛细管电泳检测3次重复,3次重复的平均值作为实验材料在该座位上的数据。
6.ssr指纹图谱构建及分子鉴定:
根据6对ssr引物的峰值大小,构建白蜡新品种‘金箭’的ssr指纹图谱,见表2。
表26对ssr荧光引物组合构建的白蜡新品种‘金箭’的ssr指纹图谱
上述白蜡新品种‘金箭’的ssr指纹图谱中,ssr引物f186和r186引物对的峰值为93/99,f187和r187引物对的峰值为134/140,f202和r202引物对的峰值为109/112,f203和r203引物对的峰值为157,f208和r208引物对的峰值为139/145,f213和r213引物对的峰值为81/90/96。
序列表
<110>山东省林业科学研究院山东华博基因工程科技有限公司
<120>一种利用毛细管电泳荧光ssr指纹图谱鉴别白蜡新品种金箭的方法
<141>2018-12-20
<160>12
<170>siposequencelisting1.0
<210>1
<211>23
<212>dna
<213>人工序列
<221>引物f186核苷酸序列
<400>1
tcttcacgtcttctgtttgttca23
<210>2
<211>23
<212>dna
<213>人工序列
<221>引物r186核苷酸序列
<400>2
gaaaacgtgtgaatgagtttggt23
<210>3
<211>23
<212>dna
<213>人工序列
<221>引物f187核苷酸序列
<400>3
tcgatctttccatctaaacaagc23
<210>4
<211>23
<212>dna
<213>人工序列
<221>引物r187核苷酸序列
<400>4
aacgtgtgaatgagtttggtttt23
<210>5
<211>23
<212>dna
<213>人工序列
<221>引物f202核苷酸序列
<400>5
agttttcaccgctttcagtgtta23
<210>6
<211>23
<212>dna
<213>人工序列
<221>引物r202核苷酸序列
<400>6
gggaatgaacatgagtttcagta23
<210>7
<211>23
<212>dna
<213>人工序列
<221>引物f203核苷酸序列
<400>7
gttatcagtagatgcaaccgcac23
<210>8
<211>22
<212>dna
<213>人工序列
<221>引物r203核苷酸序列
<400>8
aacaccggttttcaacatttct22
<210>9
<211>23
<212>dna
<213>人工序列
<221>引物f208核苷酸序列
<400>9
cctcctattgaatcattcgctta23
<210>10
<211>23
<212>dna
<213>人工序列
<221>引物r208核苷酸序列
<400>10
attttgatttccctcctctgaag23
<210>11
<211>23
<212>dna
<213>人工序列
<221>引物f213核苷酸序列
<400>11
gacaacatgcctaaattggactc23
<210>12
<211>23
<212>dna
<213>人工序列
<221>引物r213核苷酸序列
<400>12
aattctgaacttcaaggtgggat23
- 还没有人留言评论。精彩留言会获得点赞!