一种巴弗洛霉素高产工程菌及其构建和应用的制作方法
本发明属于生物技术和基因工程领域,具体的讲,是一种巴弗洛霉素高产工程菌及其构建和应用。
背景技术:
巴弗洛霉素(bafilomycins)属于十六元大环内酯类抗生素,具有广泛的生物活性,如抗细菌[1],抗真菌[2],抗寄生虫[3],抗骨质疏松[4],抗肿瘤[5],免疫抑制[3]等。其中最具代表性的化合物当属巴弗洛霉素a1,对酵母菌等真菌具有显著抑制活性[1]。巴弗洛霉素a1是第一个被鉴定的强力且专一的钾离子载体功能的大环内酯抗生素,其可促进线粒体对钾离子的吸收,并在纳摩尔水平发挥作用,引起线粒体膜电势的消失,氧化磷酸化解耦联以及呼吸作用抑制从而造成线粒体的功能损伤[6]。并且,巴弗洛霉素a1是强力的囊泡型质子泵(v-atpase)抑制剂,对来自大肠杆菌的k+依赖型质子泵,牛脑的钠钾质子泵和肌浆网钙泵(sarco/endoplasmicreticulumca2+-atpase,serca)等p型质子泵具有中等强度的抑制活性,对f型质子泵(f-atpase)无抑制活性[4]。因此,巴弗洛霉素a1在细胞生物学领域已发展为一种用于区分上述三种质子泵以及研究v-atpase生物学功能的重要工具。除此之外,v-atpase参与到人类及哺乳动物体内的一系列生理学过程,是一种重要的药物作用靶点[7,8]。例如,巴弗洛霉素a1通过阻止破骨细胞中的v-atpase质子通道的形成并抑制骨吸收,可在纳摩尔水平发挥作用,有望开发为骨质疏松症的治疗药物[9]。体外药理学研究表明,巴弗洛霉素a1有望应用于癌症治疗,巴弗洛霉素a1可通过抑制v-atpase可以遏制癌细胞内h+的泵出,降低癌细胞外微环境的酸性,抑制癌细胞的生长繁殖、转移以及化疗抵抗作用,进而引起肿瘤细胞的凋亡[10];或者通过作用于内质网腔上的肌浆网钙泵从而阻断内质网从胞浆摄取ca2+,进而抑制自噬体与溶酶体融合形成自噬溶酶体来抑制癌症细胞的自噬,提高其对化疗药物的敏感性[11]。
值得一提的是,巴弗洛霉素a1在药物联合治疗方面展现了巨大的潜力。巴弗洛霉素a1具有抗真菌作用,当与钙调磷酸酶抑制剂fk506联用,fk506和巴弗洛霉素a1对条件性致病真菌新型隐球菌的小抑菌浓度分别降低至0.39和0.06μg/ml,比分别单独用药的剂量降低33倍和1000倍以上[12];当巴弗洛霉素a1和化疗药物5-氟尿嘧啶联用时可以降低胃癌细胞对5-氟尿嘧啶的耐受[13]。正是因为v-atpase广泛参与到人体的生命活动,巴弗洛霉素在用于骨质疏松症、癌症等疾病治疗时也会靶向正常细胞造成伤害,从而限制了其临床应用。因此,巴弗洛霉素类化合物构效关系的研究将能够极大的催动该类药物在临床领域进一步发挥作用,巴弗洛霉素的结构复杂性造成其化学全合成存在步骤多、产率低的缺点。如何利用基因工程和发酵工程的方法获得巴弗洛霉素高产菌株,并对该类化合物产生途径进行理性设计获得高效低毒临床药物是极为重要的研究方向。
分离自巴布新几内亚(papuanewguinea)的皇冠岛(crownisland)海滩泥沙的海洋链霉菌streptomyceslohiiatccbaa-1276在常规发酵条件下可产生巴弗洛霉素a1,c1,b1。我们前期对s.lohii巴弗洛霉素生物合成基因簇(genbank:gu390405.1)、生物合成途径[14]和其后修饰过程进行了完整阐明[15],为巴弗洛霉素的高产工程菌株构建和抗生素发酵提供了关键的平台菌株。
技术实现要素:
本发明的目的是提供一种高效生产巴弗洛霉素工程菌的构建及发酵方法。
为实现上述目的,本发明采用技术方案为:
一种巴弗洛霉素高产工程菌,在streptomyceslohii野生株或突变株中过表达调控基因、其同源基因或与其功能等同体;其中,调控基因为bafg和/或orf1;所述调控基因bafg和orf1的序列,分别为seqidno.1和seqidno.2。
所述突变株为s.lohiiδorf2&orf3。
所述过表达调控基因、其同源基因或与其功能等同体的启动子来源于红霉素抗性基因启动子erme*或其功能等同体。
所述过表达调控基因、其同源基因或与其功能等同体的载体为链霉菌整合型载体pset152或其功能等同体。
一种所述巴弗洛霉素高产工程菌的构建方法,
将调控基因为bafg和/或orf1基因与载体连接,分别克隆得到含有目的基因的表达载体,再分别将该表达载体转化进大肠杆菌,而后分别将转入表达载体的大肠杆菌与s.lohii野生株或突变株整合即获得巴弗洛霉素高产的s.lohii野生株工程菌或巴弗洛霉素高产的s.lohii突变株工程菌。
所述载体为链霉菌整合型载体pset152或其功能等同体。
进一步的说,1)根据登陆到ncbi的s.lohii巴弗洛霉素生物合成基因簇(genbank:gu390405.1)获取调控基因bafg和orf1的序列,分别为seqidno.1和seqidno.2。
2)结合序列,设计pcr引物,以pset152-erme*为骨架,构建afsr家族调控基因bafg和luxr家族调控基因orf1的的过表达载体。
3)在s.lohii野生型菌株中过表达afsr家族调控基因bafg和luxr家族调控基因orf1。经hplc分析检测发酵产物,对其巴弗洛霉素的产量进行定量,评测两个调控因子对巴弗洛霉素产量的上调效果;
4)进一步的是,在仅产生的巴弗洛霉素a1的s.lohiiδorf2&orf3,过表达上调倍数更高的luxr家族调控基因orf1得到高产工程菌。
一种巴弗洛霉素高产工程菌的应用,所述工程菌在生产制备巴弗洛霉素中的应用。
所述野生菌的工程菌在生产制备巴弗洛霉素中的应用。
所述突变菌株的工程菌在生产制备巴弗洛霉素a1中的应用。
进一步的说,将工程菌的孢子体于2×yt液体培养基中,30℃,220rpm培养2天,再按照1:10的体积比例转接种子液到发酵培养基中,30℃,250rpm培养7天,收集发酵液经hplc定量/定性的检测巴弗洛霉素。
所述发酵培养基为大豆油60g/l,葡萄糖20g/l,豆粉20g/l,玉米浆1.5g/l,nz-amine2g/l,酵母提取物1g/l,nano38g/l,nacl5g/l,(nh4)2so46g/l,k2hpo40.3g/l,caco38g/l,ph=7.1;2×yt培养基为胰蛋白胨16g/l,酵母提取物10g/l,nacl5g/l。
本发明的有益效果:
利用有机化学合成化学结构复杂的巴弗洛霉素存在反应步骤多,得率低的缺点。本发明构建的工程菌能够稳定生产巴弗洛霉素,构建步骤简单,原料成本低廉,发酵周期短,发酵过程绿色环保;s.lohiiδorf2&orf3工程菌巴弗洛霉素a1的在250ml摇瓶中发酵7天后的产量可观(535.1±25.0mg/l),可为巴弗洛霉素a1的药理学、合成化学研究提供充足的原料来源,具有广阔的应用前景。
附图说明
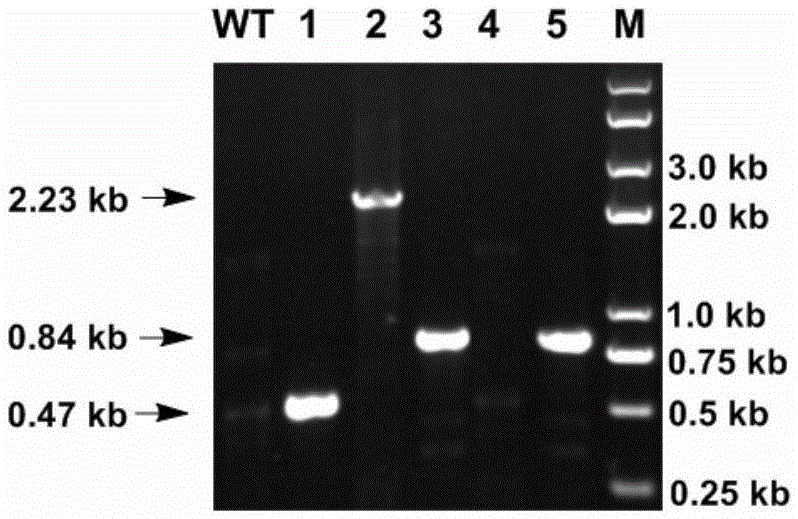
图1为本发明实施例提供的突变株pcr验证。注:wt:s.lohii野生型;1:s.lohii/pset152-erme*;2:s.lohii/pset152-erme*-bafg;3:s.lohii/pset152-erme*-orf1;4:s.lohiiδorf2&orf3;5:s.lohiiδorf2&orf3/pset152s-erme*-orf1;m:dnamarker。
图2为本发明发明实施例提供的hplc检测图。注:i:巴弗洛霉素a1,c1,b1标准品;ii:s.lohii野生型;iii:s.lohii/pset152-erme*;iv:s.lohii/pset152-erme*-bafg;v:s.lohii/pset152-erme*-orf1;vi:s.lohiiδorf2&orf3;vii,s.lohiiδorf2&orf3/pset152s-erme*-orf1。
图3为本发明发明实施例提供的巴弗洛霉素a1产量图。注:1:s.lohii野生型;2:s.lohii/pset152-erme*;3:s.lohii/pset152-erme*-bafg;4:s.lohii/pset152-erme*-orf1;5:s.lohiiδorf2&orf3;6:s.lohiiδorf2&orf3/pset152s-erme*-orf1。
具体实施方式
下面将结合实施例,对本发明作进一步的阐述。但本发明并不局限于此,凡依照本发明公开内容所做出的本领域等同替换,均属于本发明的保护范围。
下面将结合附图和实施例对本发明的实施方案进行详细描述,实施例中所采用的pcr扩增,质粒提取、转化等基础分子生物学实验技术,如无特殊说明,通常按照常规方法操作,具体可参见《分子克隆实验指南》(第三版)(sambrookj,russelldw,janssenk,argentinej.黄培堂等译,2002,北京:科学出版社),或按照相关产商提供的说明书执行。
实施例1
1.基因过表达载体构建
构建用于s.lohii野生型调控基因过表达的携带安普霉素抗性基因(aac(iv))的整合型质粒:以s.lohii野生型的基因组为模板,分别以引物bafg-bamhi-fp/bafg-kpni-rp和orf1-bamhi-fp/orf1-kpni-rp(表1)进行pcr,反应体系如下:5×primestargxlbuffer10μl,200μmdntps,4μldmso,上下游引物各0.3μm,dna模板适量(10-100ng),高保真聚合酶(primestargxldna聚合酶)2.5u,ddh2o补足至50μl;反应条件为:98℃预变性5min,98℃变性30s,55-65℃退火15s,68℃延伸(1kb/min,根据目的片段长度设定时间),反应35个循环,最后68℃延伸10min;分别扩增获得调控基因bafg和orf1的pcr产物;将上述获得调控基因bafg和orf1的pcr产物分别经核酸纯化试剂盒纯化后,利用一步克隆试剂盒将bafg和orf1分别整合到pset152-erme*的bamhi位点分别得到调控基因过表达质粒pset152-erme*-bafg和pset152-erme*-orf1。
构建用于携带安普霉素抗性基因(aac(iv))s.lohiiδorf2&orf3的调控基因过表达的携带壮观霉素抗性基因(aada)整合型质粒:以商品化质粒pij778作为模板,用spec-ndei-fp/spec-saci-rp引物对(表1)进行pcr扩增得到壮观霉素抗性基因(aada);安普霉素抗性质粒pset152-erme*经限制性内切酶saci酶切后回收质粒骨架,通过一步克隆连接aada得到壮观霉素抗性的质粒pset152s-erme*,并将orf1克隆到红霉素启动子的下游得到壮观霉素抗性的基因过表达载体pset152s-erme*-orf1。同样的策略,将bafg克隆到红霉素启动子的下游得到壮观霉素抗性的基因过表达载体pset152s-erme*-bafg。
以上构建完成的载体经dna测序完成序列确证。
表1.实例中用到的引物序列
2.调控基因过表达菌株构建
(1)将pset152-erme*-bafg和pset152-erme*-orf1转化到大肠杆菌et12567/puz8002中,37℃培养16h。挑取分别携带pset152-erme*-bafg或pset152-erme*-orf1的大肠杆菌et12567/puz8002到2mllb培养基(含50μg/ml安普霉素、50μg/ml卡那霉素和12.5μg/ml氯霉素)中,37℃,220rpm培养16h。第二天,将上述两个菌株的种子液分别按照1:100的体积比,转接到20ml含50μg/ml安普霉素、50μg/ml卡那霉素和12.5μg/ml氯霉素的lb培养基,37℃,220rpm,培养至od600到0.6与1.0之间。4℃,4000rpm离心10min收集菌体,弃上清,分别用20mllb培养液洗涤两次后,菌液经离心浓缩至500μl,即分别获得et12567/puz8002&pset152-erme*-bafg或et12567/puz8002&pset152-erme*-orf1的浓缩菌液。
(2)收集于ms培养基(豆粉20g/l,甘露醇20g/l,琼脂粉20g/l)上培养的野生株s.lohii的孢子或突变株(s.lohiiδorf2&orf3)的孢子,分别将其重悬于5ml2×yt(胰蛋白胨16g/l,酵母提取物10g/l,nacl5g/l)培养液中,6000rpm离心2min后弃去上清用等体积2×yt溶液洗涤3-5次后,6000rpm离心2min后,将孢子悬液浓缩至500μl。野生株或突变株孢子悬液于50℃热激10min后,冷却至常温。
(3)s.lohii工程菌的构建
分别取100μls.lohii野生型的孢子悬液与100μl提前准备好的et12567/puz8002&pset152-erme*-bafg或et12567/puz8002&pset152-erme*-orf1的浓缩菌液混合,分别均匀涂布于含50mmmgcl2和50mmcacl2的ms平板上。于30℃培养12h后,每个ms平板用溶有12.5mg安普霉素和0.5mg萘啶酮酸的1ml无菌水覆盖,待干后,重新放置于30℃条件下培养。待3-5天后,有白色的菌落长出,即为bafg过表达菌株s.lohii/pset152-erme*-bafg或orf1过表达菌s.lohii/pset152-erme*-orf1菌株。利用同样的策略,转化空载体pset152-erme*到s.lohii野生型得到对照突变株s.lohii/pset152-erme*。挑取单菌落到含25μg/ml萘啶酮酸和50μg/ml安普霉素的ms培养基。约3天产孢后,接种到4ml2×yt培养液中,28℃,220rpm培养2天后提取基因组供pcr验证基因型。
(4)s.lohiiδorf2&orf3工程菌构建
分别取100μls.lohii突变株s.lohiiδorf2&orf3的孢子悬液与100μl提前准备好的et12567/puz8002&pset152s-erme*-orf1的浓缩菌液混合,分别均匀涂布于含50mmmgcl2和50mmcacl2的ms平板上。于30℃培养12h后,每个ms平板用溶有经壮观霉素(100μg/ml)和萘啶酮酸(25μg/ml)双抗性筛选后得到转化子,置于30℃条件下培养。待3-5天后,有白色的菌落长出,即为s.lohiiδorf2&orf3/pset152s-erme*-orf1。挑取单菌落接种到4ml2×yt培养液中,28℃,220rpm培养2天后提取基因组供pcr验证基因型。
同样的策略,利用et12567/puz8002&pset152s-erme*-bafg与s.lohii突变株s.lohiiδorf2&orf3的接合转移,可得到s.lohiiδorf2&orf3工程菌s.lohiiδorf2&orf3/pset152s-erme*-bafg。
3.pcr验证突变株基因型
以突变株s.lohii/pset152-erme*,s.lohii/pset152-erme*-bafg,s.lohii/pset152-erme*-orf1,s.lohiiδorf2&orf3/pset152s-erme*-orf1的基因组为模板,采用通用引物m13f47/m13f-48(表1),进行pcr初步验证突变株的基因型(参见图1)。bafg过表达菌株s.lohii/pset152-erme*-bafg的pcr产物预期大小为2266bp;orf1过表达菌s.lohii/pset152-erme*-orf1的pcr产物预期大小为844bp;s.lohiiδorf2&orf3/pset152s-erme*-orf1的pcr产物预期大小为844bp;s.lohiiδorf2&orf3/pset152s-erme*-bafg的pcr产物预期大小为2266bp;空载体pset152-erme*转化s.lohii得到对照菌株s.lohii/pset152-erme*的pcr产物预期大小为471bp。pcr片段经纯化后进一步送往dna测序确证。
4.s.lohii野生株和突变株的发酵及hplc分析
从ms平板,挑取s.lohii野生株、突变株(s.lohiiδorf2&orf3)、上述获得野生株工程菌(s.lohii/pset152-erme*-bafg或s.lohii/pset152-erme*-orf1;)或突变株工程菌(s.lohiiδorf2&orf3/pset152s-erme*-orf1)孢子到装有30ml2×yt液体培养基的250ml锥形瓶中,30℃,220rpm培养2天。按照1:10的体积比例转接种子液到含有30ml发酵培养基(大豆油60g/l,葡萄糖20g/l,豆粉20g/l,玉米浆1.5g/l,nz-amine2g/l,酵母提取物1g/l,nano38g/l,nacl5g/l,(nh4)2so46g/l,k2hpo40.3g/l,caco38g/l,ph=7.1)的250ml锥形瓶中,30℃,250rpm培养7天。取200μl发酵液,加入3倍体积的甲醇后于涡旋振荡仪上振荡10min,14000rpm离心10min,取上清供hplc检测。选用的色谱柱为赛默飞(thermo)c18色谱柱(4.6×150mm),有机相为乙腈,水相为加入0.1%三氟乙酸的超纯水,hplc检测程序为:60-100%乙腈梯度洗脱15min,100%乙腈等度洗脱8min,100-60%乙腈梯度洗脱2min。以巴弗洛霉素a1,b1,c1的标准品对s.lohii野生株和突变株的巴弗洛霉素发酵产量进行定量,每组进行三个平行实验。经7天发酵后,与野生型菌株相比,携带空载体pset152-erme*的突变株(s.lohii/pset152-erme*)的巴弗洛霉素总产量无明显变化,过表达bafg的突变株(s.lohii/pset152-erme*-bafg)提高了0.5倍,过表达orf1的突变株(s.lohii/pset152-erme*-orf1)巴弗洛霉素总产量提高了1.3倍,对巴弗洛霉素产量提高的效果优于bafg;过表达orf1的突变株(s.lohiiδorf2&orf3/pset152s-erme*-orf1),巴弗洛霉素a1产量可达535.1±25.0mg/l(附图2,3)。由于过表达bafg可上调s.lohii野生株中的巴弗洛霉素的产量(附图2,3)。因此,类似地,将pset152s-erme*-bafg转化到阻断巴弗洛霉素a1的后修饰途径从而只积累巴弗洛霉素a1的s.lohiiδorf2&orf3得到的过表达bafg的突变株(s.lohiiδorf2&orf3/pset152s-erme*-bafg)也达到提高s.lohiiδorf2&orf3的巴弗洛霉素a1的产量的目的。
seqidno:1
gtgcacgtgtcggcgccgaggcagcgcgtggtcatggcagcgctcctcctcaacgccaaccgggtgatctcggtcgaccgcatcaccgagtacgtctgggacggcgccccgccgccgagtgccgccgcgaccgtccgcacctacgtgatgcgcctgcggcagtcgctgggcgagcacgcctccgcccgcatcctcacccgggcgcccggctacctcctcgaactcggggagcacgagagcgatctcggccagttcgccgcccaccgcaggcgcgcggcggagctggccgagcgcggagacctggagggctcctccgccgcgctggccgaggcactcgccctgtggcgcgaggagccgctggcggacatcccgtcgcggacgctgcgcgatgtggagggacgttacctccaggagctccggctgcagaccatggagctgcggttcgacgcggagctggcgctgctgcggcacgccgagatcgtgccggagctggtgcggctggtgcgggagcatcccttacgggaggccctggtgggcaagttgatgctggcgctcttccgctcgggacggcagtcggaggccctggacctctaccggcgcacccgggtactgctcgtcgaacagctcggggccgagcccggcgcggatctgcgcgaggtccaccggcacatcctctcggcccacgaccggccccgtacgcccgacccgcaggagcggcccgccccggccccggagacagccgccgcaccggccgctgccacggtccgggaaagatcctggcccgatcctgcgcagcttccctcggtcccgctgcccctgtcggcccgctccgacgcactggcgcgggtgcggcacttcctcacgaccggcacgatgcccgcgggcatggtggcgacggcggtggtgaccggccggggcggtgtcggcaagagcgccctggccctgcacgcggcgcacaccatgcgcggctcctccgtacacggccagctctacgcggatctcggcggggcggagcggccgctgaccgcccgggaggtgctgccgcggttcctggcggacctcggtgtgccccgggacgagatccccggggaggagtcggagcgggagagcctctaccgctcgctcaccgcgggccgccgtctgctggtggtgctcgacaacgcctccggcgccgcgcaggtgcggccgctgatcccgggcagcgggggcagcaggctgctggtgaccagccggcggcggctggccgatctggagggggcgcgcacccttctgctcggcccgctggacgaggccgggtcgctggagctgctgggcagcatcgtcggcacggccagggtcggcggcgaaccacgggcggcccgtacggtggtgacggtctgcgcgggcctgccgctggcgatccggatcgcggggacccggctgctggaacgcccgcactggagcatcgggcacctggcccggcggctcacggaggccccccggctgctggacgaactgtgcgcgggcgataccggtgtccggccctgcctggacgccgaggtggccgggctccggcggtcggcaccgggcggaatcgaccccgctgaggtgctggccgcgctgggcgccgccggggcgtcctcggtctccggcggcgaggtcgcggtgatggtcggctgcccggaggcgcaggccgaggaggccctggactccctggtcgtggcgaatctgctgggtgcgcccgcggggggccgctaccggctggacgcgctgcttcgggcgtacgcccgcgagcgtgcgcaggcggtcgcggtacggcggcacggccgctcctacatgcgcgccgggtga
(a)序列特征:
·长度:1830bp
·类型:核酸序列
(b)分子类型:脱氧核糖核酸
(c)假设:否
(d)反义:否
(e)最初来源:streptomyceslohii
(f)特异性名称:bafg
seqidno:2
gtgacaccgtcagcgacctctgaagagaccaagcccgcaccgcggccgccgaggtccgagcccgtcggcgacgcccgtccggcgggcggggacccgtccgccggcacgggtgtccggcggctgaccgccgtggacgtccgcatcctggaaggtgtcgcggtcggcaccccgaccgtccggctggcggcatcgctctatctgagccgacagggcgtcgagtaccgcatcgggctgatgatgcgccatttccaggccgcgaaccgggccgcactgatttcccgggcgcactcactcggtgtgctgagcgtcggggcatggccgccccgtgtcctcccggaattccttgaaccctag
(a)序列特征:
·长度:354bp
·类型:核酸
(b)分子类型:脱氧核糖核酸
(c)假设:否
(d)反义:否
(e)最初来源:streptomyceslohii
(f)特异性名称:orf1
参考文献
1.werner,g.,etal.,metabolicproductsofmicroorganisms.224.bafilomycins,anewgroupofmacrolideantibiotics.production,isolation,chemicalstructureandbiologicalactivity.jantibiot1984.37(2):p.110-117.
2.kinashi,h.,k.someno,andk.sakaguchi,isolationandcharacterizationofconcanamycinsa,bandc.jantibiot1984.37(11):p.1333-1343.
3.goetz,m.a.,etal.,l-155,175:anewantiparasiticmacrolidefermentation,isolationandstructure.thejournalofantibiotics,1985.38(2):p.161-168.
4.bowman,e.j.,a.siebers,andk.altendorf,bafilomycins:aclassofinhibitorsofmembraneatpasesfrommicroorganisms,animalcells,andplantcells.procnatlacadsci,1988.85(21):p.7972-7976.
5.wilton,j.,g.hokanson,andj.c.french,pd118,576:anewantitumormacrolideantibiotic.jantibiot1985.38(11):p.1449-1452.
6.teplova,v.v.,etal.,bafilomycina1isapotassiumionophorethatimpairsmitochondrialfunctions.journalofbioenergetics&biomembranes,2007.39(4):p.321-329.
7.sthudium,c.,etal.,disruptionofthev-atpasefunctionalityasawaytouncoupleboneformationandresorption-anoveltargetfortreatmentofosteoporosis.currentproteinandpeptidescience,2012.13(2):p.141-151.
8.hinton,a.,s.bond,andm.forgac,v-atpasefunctionsinnormalanddiseaseprocesses.pflügersarchiv-europeanjournalofphysiology,2009.457(3):p.589-598.
9.farina,c.,etal.,novelboneantiresorptiveagentsthatselectivelyinhibittheosteoclastv-h+-atpase.cheminform,2001.56(1):p.113-116.
10.pérez-sayáns,m.,etal.,v-atpaseinhibitorsandimplicationincancertreatment.cancertreatmentreviews,2009.35(8):p.707-713.
11.mauvezin,c.,etal.,autophagosome–lysosomefusionisindependentofv-atpase-mediatedacidification.natcommun,2015.6:p.7007.
12.delpoeta,m.,etal.,synergisticantifungalactivitiesofbafilomycina1,fluconazole,andthepneumocandinmk-0991/caspofunginacetate(l-743,873)withcalcineurininhibitorsfk506andl-685,818againstcryptococcusneoformans.antimicrobialagentsandchemotherapy,2000.44(3):p.739-746.
13.li,l.-q.,etal.,inhibitionofautophagybybafilomycina1promoteschemosensitivityofgastriccancercells.tumorbiology,2016.37(1):p.653-659.
14.zhang,w.,etal.,characterizationofthebafilomycinbiosyntheticgeneclusterfromstreptomyceslohii.chembiochem,2013.14(3):p.301-6.
15.li,z.,etal.,completeelucidationofthelatestepsofbafilomycinbiosynthesisinstreptomyceslohii.journalofbiologicalchemistry,2017.292(17):p.7095-7104.
序列表
<110>中国科学院青岛生物能源与过程研究所
<120>一种巴弗洛霉素高产工程菌及其构建和应用
<160>2
<170>siposequencelisting1.0
<210>1
<211>1830
<212>dna
<213>海洋链霉菌(streptomyceslohiibafg)
<400>1
gtgcacgtgtcggcgccgaggcagcgcgtggtcatggcagcgctcctcctcaacgccaac60
cgggtgatctcggtcgaccgcatcaccgagtacgtctgggacggcgccccgccgccgagt120
gccgccgcgaccgtccgcacctacgtgatgcgcctgcggcagtcgctgggcgagcacgcc180
tccgcccgcatcctcacccgggcgcccggctacctcctcgaactcggggagcacgagagc240
gatctcggccagttcgccgcccaccgcaggcgcgcggcggagctggccgagcgcggagac300
ctggagggctcctccgccgcgctggccgaggcactcgccctgtggcgcgaggagccgctg360
gcggacatcccgtcgcggacgctgcgcgatgtggagggacgttacctccaggagctccgg420
ctgcagaccatggagctgcggttcgacgcggagctggcgctgctgcggcacgccgagatc480
gtgccggagctggtgcggctggtgcgggagcatcccttacgggaggccctggtgggcaag540
ttgatgctggcgctcttccgctcgggacggcagtcggaggccctggacctctaccggcgc600
acccgggtactgctcgtcgaacagctcggggccgagcccggcgcggatctgcgcgaggtc660
caccggcacatcctctcggcccacgaccggccccgtacgcccgacccgcaggagcggccc720
gccccggccccggagacagccgccgcaccggccgctgccacggtccgggaaagatcctgg780
cccgatcctgcgcagcttccctcggtcccgctgcccctgtcggcccgctccgacgcactg840
gcgcgggtgcggcacttcctcacgaccggcacgatgcccgcgggcatggtggcgacggcg900
gtggtgaccggccggggcggtgtcggcaagagcgccctggccctgcacgcggcgcacacc960
atgcgcggctcctccgtacacggccagctctacgcggatctcggcggggcggagcggccg1020
ctgaccgcccgggaggtgctgccgcggttcctggcggacctcggtgtgccccgggacgag1080
atccccggggaggagtcggagcgggagagcctctaccgctcgctcaccgcgggccgccgt1140
ctgctggtggtgctcgacaacgcctccggcgccgcgcaggtgcggccgctgatcccgggc1200
agcgggggcagcaggctgctggtgaccagccggcggcggctggccgatctggagggggcg1260
cgcacccttctgctcggcccgctggacgaggccgggtcgctggagctgctgggcagcatc1320
gtcggcacggccagggtcggcggcgaaccacgggcggcccgtacggtggtgacggtctgc1380
gcgggcctgccgctggcgatccggatcgcggggacccggctgctggaacgcccgcactgg1440
agcatcgggcacctggcccggcggctcacggaggccccccggctgctggacgaactgtgc1500
gcgggcgataccggtgtccggccctgcctggacgccgaggtggccgggctccggcggtcg1560
gcaccgggcggaatcgaccccgctgaggtgctggccgcgctgggcgccgccggggcgtcc1620
tcggtctccggcggcgaggtcgcggtgatggtcggctgcccggaggcgcaggccgaggag1680
gccctggactccctggtcgtggcgaatctgctgggtgcgcccgcggggggccgctaccgg1740
ctggacgcgctgcttcgggcgtacgcccgcgagcgtgcgcaggcggtcgcggtacggcgg1800
cacggccgctcctacatgcgcgccgggtga1830
<210>2
<211>354
<212>dna
<213>海洋链霉菌(streptomyceslohiiorf1)
<400>2
gtgacaccgtcagcgacctctgaagagaccaagcccgcaccgcggccgccgaggtccgag60
cccgtcggcgacgcccgtccggcgggcggggacccgtccgccggcacgggtgtccggcgg120
ctgaccgccgtggacgtccgcatcctggaaggtgtcgcggtcggcaccccgaccgtccgg180
ctggcggcatcgctctatctgagccgacagggcgtcgagtaccgcatcgggctgatgatg240
cgccatttccaggccgcgaaccgggccgcactgatttcccgggcgcactcactcggtgtg300
ctgagcgtcggggcatggccgccccgtgtcctcccggaattccttgaaccctag354
- 还没有人留言评论。精彩留言会获得点赞!