重组人蛋白激酶Nek2蛋白表达和纯化方法与流程
本发明涉及基因工程领域,具体是重组人蛋白激酶nek2蛋白表达和纯化方法。
背景技术:
nima(neverinmitosisa)相关蛋白激酶2(nima-relatedexpressedkinase-2,nek2)与细胞有丝分裂密切相关,主要作用是调节中心体分离。nek2异常表达可导致中心体异常,会影响细胞有丝分裂的正常进行,导致细胞周期调控异常,造成细胞异常增殖,进而导致肿瘤的发生、发展。nek2在人类多种肿瘤,包括非小细胞型肺癌、骨髓瘤、卵巢癌、乳腺癌、前列腺癌、结肠直肠癌、恶性外周神经鞘瘤、肾细胞癌、胰腺导管腺癌等中的表达量异常升高,提示nek2可能是一个重要的肿瘤标志物,其表达量可以预示肿瘤增殖和预后情况。
技术实现要素:
本发明的目的是提供一种原核表达的高纯度、高产率、低成本、操作简便的重组人蛋白激酶nek2蛋白表达和纯化方法,有助于进一步自主研发和制备该蛋白的单克隆抗体。
本发明通过以下技术方案实现上述目的:提供一种重组人蛋白激酶nek2蛋白的基因,其核苷酸序列如序列表seqidno.1所示。
重组人蛋白激酶nek2蛋白,其氨基酸序列如序列表seqidno.2所示。
所述的重组人蛋白激酶nek2蛋白的表达方法,包括:
将人nek2基因构建到原核表达载体pet30a(+)上,构建重组表达载体pet30a(+)-nek2,并将所述的重组表达载体转化到大肠杆菌bl21(de3)中,获得重组工程菌株,将所述的重组工程菌株进行培养并加入诱导剂iptg进行诱导表达重组人蛋白激酶nek2蛋白,
所述的表达载体pet30a(+)上含有t7启动子和由6个组氨基酸组成的标签序列。
所述的重组人蛋白激酶nek2蛋白的目的基因序列为nek2全长序列,利用pcr技术从人hl7702细胞中克隆nek2全长cdna,以此cdna为模板进行pcr扩增,其上游引物f(b)如序列表seqidno.3所示:aaaggatccatgccttcccgggctgaggactat(划线部分为bamhⅰ酶切位点),下游引物r(sa1ⅰ)如序列表seqidno.4所示:aaagtcgacctagcgcatgcccaggatctgt(划线部分为sa1ⅰ酶切位点)。
所述的构建原核表达载体的方法为:利用pcr技术从人hl7702细胞中克隆nek2全长cdna,以此cdna为模板进行pcr扩增得到的pcr扩增产物与表达载体pet30a(+)分别用bamhⅰ和sa1ⅰ酶进行双酶切,酶切产物经dna纯化试剂盒纯化,然后将纯化产物用t4ligase连接,构建重组表达载体pet30a(+)-nek2。
所述的重组基因工程菌株为bl21-pet30a(+)-nek2。
诱导nek2蛋白表达的条件为:37℃,200rpm条件下培养约2.5-3h至对数生长期,加入终浓度为0.2mm的iptg诱导8h,诱导表达的重组人蛋白激酶nek2蛋白为包涵体蛋白。
诱导表达的重组人nek2蛋白的纯化方法为:超声破碎菌体,离心后沉淀重悬于bindingbuffer中;再次离心,将上清液负载到ni琼脂糖凝胶层析柱中4℃摇床过夜,先用bindingbuffer冲洗柱子,再用含150mm咪唑浓度的elutionbuffer洗脱,收集洗脱液;将洗脱液过10kda超滤管浓缩后跑sds-page电泳进行250mmkcl染色切胶回收。
诱导表达的重组人蛋白激酶nek2蛋白的纯化方法,所述的bindingbuffer组成为:20mmtris-hci,ph7.9,500mmnacl,5mm咪唑,8m尿素;elutionbuffer组成为:20mmtris-hci,ph7.9,500mmnacl,150mm咪唑,8m尿素。
所述诱导表达的重组人nek2蛋白纯化得到的重组人蛋白激酶nek2纯化蛋白在制备单克隆抗体中的应用。
本发明突出的优点是:
利用基因工程的方法构建了能够稳定表达人蛋白激酶nek2重组蛋白的大肠杆菌工程菌,表达产物可以通过ni琼脂糖凝胶层析柱纯化和kcl染色切胶二次纯化,纯化nek2蛋白操作简便,成本低,重复性好,最终可以得到高纯度、高产率的重组人蛋白激酶nek2蛋白,可作为抗原用于nek2抗体的制备。
附图说明
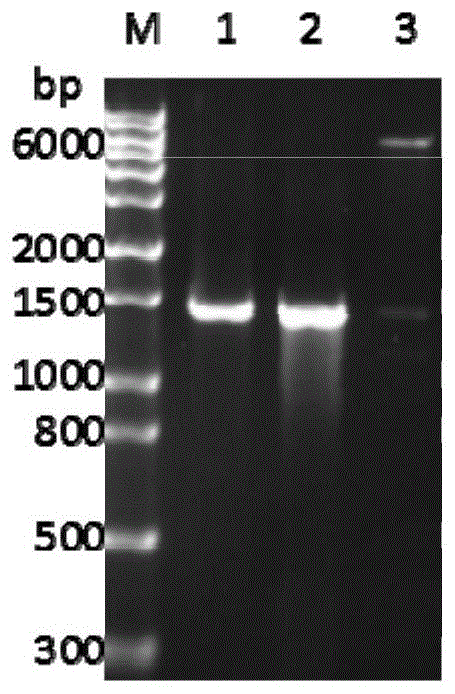
图1是nek2基因pcr扩增、菌液pcr检测以及pet30a(+)-nek2双酶切鉴定图。
其中m:dnamarker,1:nek2基因pcr扩增产物,2:菌液pcr验证产物,3:bamhⅰ和sa1ⅰ酶双酶切后的pet30a(+)-nek2。
图2是重组人蛋白激酶nek2蛋白诱导表达电泳图。
其中m:蛋白marker,kda:蛋白分子质量,1:pet30a(+)沉淀组分不诱导,2:pet30a(+)沉淀组分0.2mmiptg诱导,3:重组nek2蛋白沉淀组分不诱导,4:重组nek2蛋白沉淀组分0.2mmiptg诱导,5:pet30a(+)上清组分不诱导,6:pet30a(+)上清组分0.2mmiptg诱导,7:重组nek2蛋白上清组分不诱导,8:重组nek2蛋白上清组分0.2mmiptg诱导。
图3是重组人蛋白激酶nek2蛋白纯化电泳图。
其中m:蛋白marker,kda:蛋白分子质量,1:纯化后重组人蛋白激酶nek2蛋白。
具体实施方式
实施例1
重组表达载体pet30a(+)-nek2的构建
1.1pcr获取nek2目的基因
运用takara公司rna提取试剂盒提取人hl7702细胞totalrna,利用pcr技术,首先反转录得到的nek2全长序列cdna,以此为模板扩增得到1340bpnek2目的基因。引物序列如下:上游引物:aaaggatccatgccttcccgggctgaggactat(划线部分为bamhⅰ酶切位点),下游引物:aaagtcgacctagcgcatgcccaggatctgt(划线部分为sa1ⅰ酶切位点)。pcr反应体系:上游、下游引物各0.4ul,cdna模板2.0ul,pcrpfusupermix10ul,ddh2o7.2ul;95℃预变性1min,95℃变性20s、60℃退火20s、72℃延伸45s、38个循环,72℃延伸5min。pcr产物经1.0%琼脂糖凝胶电泳鉴定,由图1可见,在约1340bp处有一清晰的亮带,与预期大小吻合,即为nek2目的基因(1泳道)。
1.2pet30a(+)-nek2表达载体的构建
(1)上述pcr产物经纯化试剂盒纯化后,将pet30a(+)与纯化pcr产物同时进行bamhi和sa1ⅰ酶双酶切,37℃反应3.5h,应用omega公司的dna纯化试剂盒进行纯化并回收纯化后酶切产物,室温连接4h。连接体系为:nek2目的片段6ul,质粒2ul,t4ligasebuffer1ul,t4ligase1ul。
(2)将连接产物转化到stbl3感受态细胞中,获得转化菌。转化条件为:连接产物10ul加入50ulstbl3感受态细胞中,冰浴30min,42℃热激45s,冰浴2min,加入600ul无菌的lb培养基(不含抗生素),混匀后置于37℃、200rpm培养箱中培养1h,然后涂布于kan抗性的lb平板,37℃倒置培养过夜。
(3)挑取单菌落做进一步的pcr验证和双酶切验证,经1.0%琼脂糖凝胶电泳,筛选阳性克隆菌进行测序,测序结果正确,获得重组质粒pet30a(+)-nek2。pcr验证结果见于图1,在约1340bp处有一特异性条带(2泳道),其酶切鉴定图谱如图1所示,在约1340bp和6000bp处有特异性条带(3泳道)。
实施例2
重组人蛋白激酶nek2蛋白表达与鉴定
2.1将pet30a(+)-nek2重组质粒转化至表达宿主大肠杆菌bl21(de3)中,得到重组基因工程菌株,即bl21-pet30a(+)-nek2。挑取重组基因工程菌株bl21-pet30a(+)-nek2接种于10mllb培养基中(含kan25ug/ml),37℃,200rpm培养过夜。
2.2按1:9的比例转接种至10ml新鲜lb培养基中(含kan25ug/ml),37℃,200rpm条件下振荡培养约2.5-3h,并加入终浓度为0.2mm的iptg诱导表达蛋白,同时设立重组基因工程菌株bl21-pet30a(+)-nek2未进行iptg诱导组、表达质粒pet30a(+)iptg诱导组和未诱导组进行对照,37℃,200rpm诱导8h。
2.3菌体于4℃,12000g离心1min,弃上清,收集下层沉淀菌体。用1mlpbs缓冲液重悬菌体,超声破碎2min(384w,开5s,关5s)。4℃,12000g离心5min,吸取上清到新的离心管中,即为上清组分;沉淀用100ulpbs重悬,即为沉淀组分。进行12%sds-page电泳及考马斯亮蓝方法鉴定,结果如图2所示,在约58kda处有一特异性蛋白条带(4泳道),与预期的重组人蛋白激酶nek2蛋白分子量相符,诱导表达的重组人蛋白激酶nek2蛋白为包涵体蛋白。
实施例3
重组人蛋白激酶nek2蛋白纯化
3.1根据实施例2,诱导表达150ml重组基因工程菌株bl21-pet30a(+)-nek2,用适量预冷的pbs缓冲液重悬菌体,冰浴超声破碎60min(384w,开5s,关5s)后于4℃,12000rpm离心5min,收集沉淀。将沉淀重悬于bindingbuffer(20mmtris-hci,ph7.9,500mmnacl,5mm咪唑,8m尿素)中,冰浴1h,使包涵体溶解。4℃,10000g离心20min,收集上清液。
3.2将上清液负载到ni琼脂糖凝胶层析柱中,置于4℃摇床过夜。使用15倍柱体积的bindingbuffer(20mmtris-hci,ph7.9,500mmnacl,5mm咪唑,8m尿素)冲洗柱子,再使用5倍柱体积的含150mm咪唑浓度的elutionbuffer(20mmtris-hci,ph7.9,500mmnacl,150mm咪唑,8m尿素)洗脱目的蛋白,收集洗脱液。
3.3将洗脱液过10kda超滤管4℃,3500g离心30min,进行浓缩、脱盐后跑12%sds-page电泳(制备浓缩胶时不插入梳子),用预冷的250mmkcl染色3-5min,直至出现乳白色条带,切下目的条带位置所在的乳白色条带胶条,放在pbs缓冲液中浸泡,直到无色透明,将无色透明的胶条装入1.5ml离心管,切碎,加入适量pbs缓冲液,4℃摇床过夜。次日吸取上层液体到新的离心管中,即为纯化的蛋白液体,经12%sds-page电泳及考马斯亮蓝方法鉴定,结果如图3所示,在约58kda处有一特异性蛋白条带,与预期的重组人蛋白激酶nek2蛋白分子量相符,。通过进一步的质谱检测,验证该重组蛋白为人蛋白激酶nek2蛋白。经bca试剂盒定量,可获得纯化的重组人蛋白激酶nek2蛋白约1.20mg。最后将纯化蛋白进行冻干保存。
所述诱导表达的重组人nek2蛋白纯化得到的重组人蛋白激酶nek2纯化蛋白在制备单克隆抗体中的应用。
序列表
<110>广西医科大学
<120>重组人蛋白激酶nek2蛋白表达、纯化和制备方法
<160>4
<170>siposequencelisting1.0
<210>1
<211>1338
<212>dna
<213>人工序列(artificialsequence)
<400>1
atgccttcccgggctgaggactatgaagtgttgtacaccattggcacaggctcctacggc60
cgctgccagaagatccggaggaagagtgatggcaagatattagtttggaaagaacttgac120
tatggctccatgacagaagctgagaaacagatgcttgtttctgaagtgaatttgcttcgt180
gaactgaaacatccaaacatcgttcgttactatgatcggattattgaccggaccaataca240
acactgtacattgtaatggaatattgtgaaggaggggatctggctagtgtaattacaaag300
ggaaccaaggaaaggcaatacttagatgaagagtttgttcttcgagtgatgactcagttg360
actctggccctgaaggaatgccacagacgaagtgatggtggtcataccgtattgcatcgg420
gatctgaaaccagccaatgttttcctggatggcaagcaaaacgtcaagcttggagacttt480
gggctagctagaatattaaaccatgacacgagttttgcaaaaacatttgttggcacacct540
tattacatgtctcctgaacaaatgaatcgcatgtcctacaatgagaaatcagatatctgg600
tcattgggctgcttgctgtatgagttatgtgcattaatgcctccatttacagcttttagc660
cagaaagaactcgctgggaaaatcagagaaggcaaattcaggcgaattccataccgttac720
tctgatgaattgaatgaaattattacgaggatgttaaacttaaaggattaccatcgacct780
tctgttgaagaaattcttgagaaccctttaatagcagatttggttgcagacgagcaaaga840
agaaatcttgagagaagagggcgacaattaggagagccagaaaaatcgcaggattccagc900
cctgtattgagtgagctgaaactgaaggaaattcagttacaggagcgagagcgagctctc960
aaagcaagagaagaaagattggagcagaaagaacaggagctttgtgttcgtgagagacta1020
gcagaggacaaactggctagagcagaaaatctgttgaagaactacagcttgctaaaggaa1080
cggaagttcctgtctctggcaagtaatccagaacttcttaatcttccatcctcagtaatt1140
aagaagaaagttcatttcagtggggaaagtaaagagaacatcatgaggagtgagaattct1200
gagagtcagctcacatctaagtccaagtgcaaggacctgaagaaaaggcttcacgctgcc1260
cagctgcgggctcaagccctgtcagatattgagaaaaattaccaactgaaaagcagacag1320
atcctgggcatgcgctag1338
<210>2
<211>445
<212>prt
<213>人工序列(artificialsequence)
<400>2
metproserargalagluasptyrgluvalleutyrthrileglythr
151015
glysertyrglyargcysglnlysileargarglysseraspglylys
202530
ileleuvaltrplysgluleuasptyrglysermetthrglualaglu
354045
lysglnmetleuvalsergluvalasnleuleuarggluleulyshis
505560
proasnilevalargtyrtyraspargileileaspargthrasnthr
65707580
thrleutyrilevalmetglutyrcysgluglyglyaspleualaser
859095
valilethrlysglythrlysgluargglntyrleuaspglugluphe
100105110
valleuargvalmetthrglnleuthrleualaleulysglucyshis
115120125
argargseraspglyglyhisthrvalleuhisargaspleulyspro
130135140
alaasnvalpheleuaspglylysglnasnvallysleuglyaspphe
145150155160
glyleualaargileleuasnhisaspthrserphealalysthrphe
165170175
valglythrprotyrtyrmetserprogluglnmetasnargmetser
180185190
tyrasnglulysseraspiletrpserleuglycysleuleutyrglu
195200205
leucysalaleumetproprophethralapheserglnlysgluleu
210215220
alaglylysilearggluglylyspheargargileprotyrargtyr
225230235240
seraspgluleuasngluileilethrargmetleuasnleulysasp
245250255
tyrhisargproservalglugluileleugluasnproleuileala
260265270
aspleuvalalaaspgluglnargargasnleugluargargglyarg
275280285
glnleuglygluproglulysserglnaspserserprovalleuser
290295300
gluleulysleulysgluileglnleuglngluarggluargalaleu
305310315320
lysalaargglugluargleugluglnlysgluglngluleucysval
325330335
arggluargleualagluasplysleualaargalagluasnleuleu
340345350
lysasntyrserleuleulysgluarglyspheleuserleualaser
355360365
asnprogluleuleuasnleuproserservalilelyslyslysval
370375380
hispheserglygluserlysgluasnilemetargsergluasnser
385390395400
gluserglnleuthrserlysserlyscyslysaspleulyslysarg
405410415
leuhisalaalaglnleuargalaglnalaleuseraspileglulys
420425430
asntyrglnleulysserargglnileleuglymetarg
435440445
<210>3
<211>33
<212>dna
<213>人工序列(artificialsequence)
<400>3
aaaggatccatgccttcccgggctgaggactat33
<210>4
<211>31
<212>dna
<213>人工序列(artificialsequence)
<400>4
aaagtcgacctagcgcatgcccaggatctgt31
- 还没有人留言评论。精彩留言会获得点赞!