二羟基嘧啶化合物及其应用的制作方法
本发明涉及药学领域,更具体地,涉及一种二羟基嘧啶化合物以及在制备抗流感病毒的药物中的应用。
背景技术:
流行性感冒(流感)是一种由流感病毒引起的急性呼吸道传染疾病,一直以来都严重影响人类的生命健康,并带来巨大的经济和社会负担。根据世界卫生组织的数据,季节性流感的流行每年都会造成300-500万例严重病例,并导致25-50万人死亡,流感世界范围的大流行更是会带来灾难性的后果。此外,禽流感是由禽流感病毒引起的一种鸟类病毒性传染病,一般情况下被感染的宿主没有明显的症状,禽流感病毒也可以感染家禽、人和一些哺乳动物。
目前,流感疫苗是预防和控制流感传播的最有效手段,接种疫苗主要是通过诱导产生血凝素抗体来起到保护作用。虽然灭活疫苗和减毒活疫苗都能有效的预防流感和其相关并发症,但其保护作用取决于疫苗病毒株和流行的病毒株之间的抗原匹配程度,以及接种者的年龄和身体健康状况。在现有条件下,要准确预测即将流行的流感病毒株是非常困难的。
由于病毒的抗原漂移,流感疫苗的成分每年都要根据世界卫生组织和美国疾病防治中心的流感监测数据进行调整,这给疫苗的生产带来很大的困难。而临床目前用于治疗流感病毒感染的药物主要为m2离子通道抑制剂和神经氨酸酶抑制剂这两类。临床上应用的m2离子通道抑制剂包括两种药物:金刚烷胺和金刚乙烷。该类药物很早就用来预防和治疗流感,m2离子通道抑制剂只对a型流感病毒有效,对b型流感病毒无效。目前,该类药物的耐药性问题已经非常严重,该类药物已不再作为流感防治的一线药物使用。神经氨酸酶抑制剂是根据流感病毒神经氨酸酶的晶体结构信息,通过合理药物设计开发出抗流感病毒药物,与m2离子通道抑制剂只对a型流感有效不同,神经氨酸酶对a型流感病毒和b型流感病毒感染都有效,但是随着流感病毒的变异以及药物滥用,使得神经氨酸酶的耐药性问题日益严重。
针对流感病毒日益严重的耐药性威胁以及目前仅有少数几种治疗药物的状况,开发新型抗流感病毒药物变得十分迫切和必要。
技术实现要素:
针对现有技术中的缺陷,根据本发明的一个方面,提供了一种二羟基嘧啶化合物,所述二羟基嘧啶化合物的结构通式为:
在上述二羟基嘧啶化合物中,r1为芳基或杂环;r2为c1-c4的烷基、c1-c4的烷基芳基、c1-c4的烷基杂环;x、y各自为介于0-3之间的任意自然数。
在上述二羟基嘧啶化合物中,r1为含有吸电子取代基或供电子取代基的芳基、五元杂环或六元杂环,r2为甲基、乙基、丙基、异丙基、叔丁基、苄基、乙基芳基或丙基芳基。
在上述二羟基嘧啶化合物中,所述含有取代基的芳基为含有吸电子取代基或供电子取代基的芳基,其中,所述吸电子取代基为卤素原子、硝基或三氟甲基,所述供电子取代基为c1-c3的烷氧基或烷基、氨基、羟基、巯基,杂环为吡咯环、噻吩环、呋喃环、咪唑环、噻唑环、恶唑环、哌啶环、哌嗪环、吗啉环或吡嗪环;r2为甲基、乙基、丙基、异丙基、叔丁基或苄基。
在上述二羟基嘧啶化合物中,r1为含有吸电子取代基的芳基;r2为甲基、乙基、叔丁基或苄基;x为2或3,y为介于0-2之间的任意自然数。
根据本发明的另一方面,还提供了二羟基嘧啶化合物在制备抗流感病毒的药物中的应用。
在上述应用中,所述抗流感病毒的药物包括所述二羟基嘧啶化合物、所述二羟基嘧啶化合物在药学上可接受的盐、酯、水合物或它们的组合以及辅料。
在上述应用中,所述二羟基嘧啶化合物在药学上可接受的盐包括有机盐或无机盐,其中,所述有机盐选自甲磺酸盐、甲酸盐、苯磺酸盐、对甲基苯磺酸盐、萘磺酸盐、乳酸盐、乙酸盐或苯甲酸盐中的一种或多种,所述无机盐选自盐酸盐、氢溴酸盐、硫酸盐或磷酸盐中的一种或多种。
在上述应用中,所述抗流感病毒的药物的剂型选自片剂、胶囊剂、丸剂、栓剂、气雾剂、口服液体制剂、颗粒剂、散剂、注射剂、糖浆剂、酒剂、酊剂、露剂、膜剂或它们的组合。
在上述应用中,所述抗流感病毒的药物的给药方式包括:口服、注射、植入、外用、喷雾、吸入或它们的组合。
本发明提供的二羟基嘧啶类化合物对流感病毒活性有较好的抑制作用,能显著降低流感病毒的毒性,且细胞毒性较低,从而可以将这类化合物用于制备抗流感病毒药物。
附图说明
为了更清楚地说明本发明实施例或现有技术中的技术方案,下面将对实施例中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图仅仅是本发明的一些实施例,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他的附图。
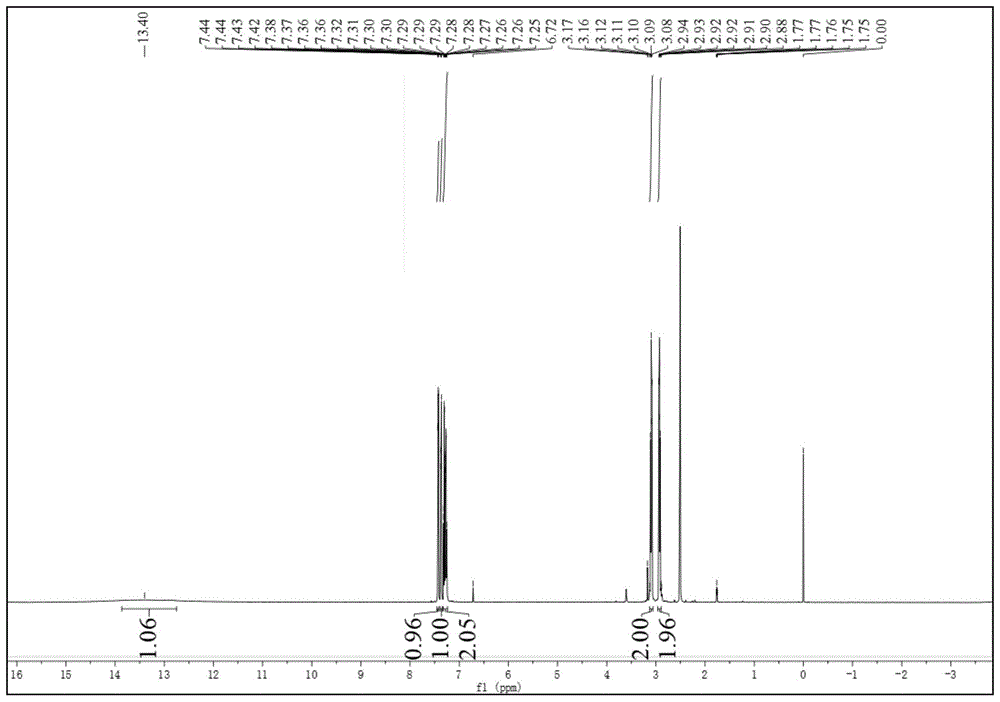
图1为化合物af-1-24的氢核磁谱图。
图2为化合物af-1-24的碳核磁谱图。
图3为化合物af-1-24的质谱谱图。
图4为化合物af-1-24的ec50值。
图5为利巴韦林的ec50值。
具体实施方式
下面将结合本发明实施例中的附图,对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员所获得的所有其他实施例,都属于本发明保护的范围。
本发明挑选化合物af-1-24的合成过程作为具体实施例,来对本发明二羟基嘧啶衍生物的具体合成路线进行说明,但实施例的选择并不意味着本发明的制备方法的任何限制。
化合物af-1-24的具体合成过程如下:
1、取100ml干燥的单口烧瓶,将2-氯-苯基乙酸乙酯(1g,0.0054mmol溶于10ml甲醇,之后将体系置于冰浴下,缓慢的加入氢化铝锂(0.41g,0.0108mmol),加入完毕后继续搅拌1h反应,反应完毕后加入少量的水进行淬灭,之后减压除去甲醇加入并向体系中加入15ml乙酸乙酯萃取,之后用饱和食盐水洗涤,收集萃取相,无水硫酸钠干燥过夜,干燥结束后减压除去溶剂得到无色油状物,即化合物a,无需纯化直接用于下一步反应。
2、取100ml干燥的圆底烧瓶,将化合物a(0.8g,0.0051mmol)溶于10ml吡啶,之后加入二氯亚砜(1.21g,0.010mmol),体系置于室温下搅拌反应4h,反应结束后减压除去吡啶后加入20ml乙酸乙酯稀释,之后用饱和食盐水洗涤,收集有机相,无水硫酸钠干燥过夜,干燥结束后,粗产品经过硅胶柱纯化得760mg化合物b,产率为85%。1h-nmr(600mhz,dmso-d6)δ7.42(dd,j=7.7,1.6hz,1h),7.36(dd,j=7.5,1.9hz,1h),7.30-7.23(m,2h),3.06(dd,j=9.2,6.7hz,2h),2.82-2.70(m,2h)。
3、取100ml干燥的圆底烧瓶,将化合物b(760mg,0.043mmol)溶于10ml乙腈,之后依次加入三甲基甲硅烷基氰化物(860mg,0.086mmol)以及四丁基氟化铵(2.27g,0.086mmol),之后室温搅拌反应24h,后反应结束后,减压除去乙腈,体系用乙酸乙酯稀释并用饱和食盐水洗涤,收集有机相,无水硫酸钠干燥。粗产品硅胶柱纯化得430mg无色油状物,即化合物c,产率60%。1h-nmr(600mhz,dmso-d6)δ7.42(dd,j=7.7,1.6hz,1h),7.36(dd,j=7.5,1.9hz,1h),7.30-7.23(m,2h),2.90(dd,j=9.2,6.7hz,2h),2.82-2.72(m,2h)。
4、取100ml干燥的单口烧瓶,将化合物c(1g,0.006mmol)溶于10ml无水乙醇中,加入50%的羟胺水溶液(0.44g,0.013mmol),将体系置于80℃加热回流5h。tlc检测原料反应完全后旋干乙醇得无色透明油状物,即化合物d,直接进行下一步反应。
5、取10ml干燥的单口烧瓶,将上一部反应所得的化合物d溶于10ml甲醇,加入丁炔酸二甲酯dmad(0.94g,0.007mmol),体系于60℃下加热反应1h。tlc检测原料反应完全后停止反应,减压除去甲醇,粗产品经过硅胶柱纯化得淡黄色透明油状物2.0g,将其溶于15ml的二甲苯中,体系于135℃加热回流反应12h,反应期有白色的固体不断地析出。反应结束后,停止加热,体系冷却至室温后加入20ml甲基叔丁基醚继续搅拌20min,之后过滤,抽滤并用50ml甲基叔丁基醚洗涤滤饼,烘干滤饼得1.08g白色固体,即化合物e,产率60%。1h-nmr(600mhz,dmso-d6)δ12.81(s,1h),10.22(s,1h),7.42(dd,j=7.7,1.6hz,1h),7.36(dd,j=7.5,1.9hz,1h),7.30-7.23(m,2h),3.82(s,3h),3.06(dd,j=9.2,6.7hz,2h),2.82-2.72(m,2h)。
6、将上一步所得的化合物e置于15mlthf中搅拌,体系呈白色浑浊状态,之后加入氢氧化锂(1.36g,0.032mmol)及适量水,体系变澄清,体系于60℃加热回流反应3h,之后体系又变回浑浊状态,将反应体系冷却至室温后,用1mhcl将ph调至2-3,体系由浑浊先变澄清再出现大量的白色固体,之后抽滤后用水洗涤滤饼,之后烘干滤饼,得0.93g白色固体,,即化合物af-1-24,产率95%。1h-nmr(600mhz,dmso-d6)δ13.40(s,1h),7.43(dd,j=7.8,1.5hz,1h),7.37(dd,j=7.5,1.8hz,1h),7.28(dtd,j=22.1,7.4,1.6hz,2h),3.09(dd,j=9.1,6.6hz,2h),2.96-2.89(m,2h);13c-nmr(101mhz,dmso-d6)δ167.64,159.57,151.89,150.58,137.73,133.39,131.27,129.72,128.87,127.85,123.02,32.25,30.89。esi-ms:[m+h]+295.46,found:295.32。
抗流感病毒化合物细胞水平抑制活性以及细胞毒性测定:
(1)抗流感化合物细胞水平的抗流感病毒活性检测
a)mdck细胞的复苏
将在液氮中冻存的mdck细胞在37℃水浴锅中解冻后,加入到盛有12ml培养基的培养皿中,培养基成分为dmem+10%胎牛血清+1%青霉素和链霉素,37℃,5%co2培养。
b)influenza(h1n1)-gluc病毒的扩增
购买发育良好的9-11日龄鸡胚,于尿囊腔接种,33℃-35℃孵卵箱中培养,孵育24h后检视,弃去死胎,48h后收获。收获前,将鸡胚置于4℃冰箱中过夜。收获的病毒放置于-80℃冰箱中。
c)病毒滴度测定
mdck细胞按照3×105个/ml接种于96孔板中,37℃,5%co2培养18h后,第一列3孔加入10倍稀释的病毒100μl,第二列3孔加入20倍稀释的病毒100μl,直到第九列3孔,第十列作为空白对照,培养24小时后取上清,加入腔肠素进行数据测定,gluciferase读值在100000-200000之间最为合适。
d)化合物的配制
将化合物af-1-24溶解在95%二甲基亚砜中,配制10mm储液,用培养基dmem+10%fbs(胎牛血清)+1%ps将上述化合物配制成100μm,40μm,4μm进行初步筛选。
e)将mdck细胞按照3×105个/ml接种于96孔板中,为防止培养基蒸发引起的边缘效应,96孔板外围加入200μlpbs缓冲液,37℃,5%co2培养18h后,每板可以测定6种化合物,将100μl细胞中的培养基吸走,在96孔板的第2列bcd行3孔细胞中加入50μl100μm的第一种化合物,第三列bcd行3孔中加入50μl40μm的化合物,第四列bcd行3个孔加入50μl4μm的化合物,第五列bcd行3孔加入50μl100μm第二种化合物,以此类推加到96孔板的第9列的3个孔,efg3行9列加入另3种化合物,第11列6个孔设为病毒对照和细胞对照。
f)抑制剂处理2h后,用培养基将influenza(h1n1)-gluc病毒稀释30倍,然后每孔加入50μl病毒,总体积变为100μl,因此,抑制剂的浓度变为配制浓度的1/2,37℃,5%co2培养24小时。
g)细胞培养24h后,取细胞上清30微升于白色酶标板中,加入30μl腔肠素,于微孔板检测仪中读取数值。
g)对20μm条件下抑制率50%以上的抑制剂进行确切的ec50测定,其方法如下:
将100μlmdck细胞按3×105个/ml接种于96孔板中,外围用200μlpbs封闭,防止边缘效应,37℃,5%co2培养箱中培养24h。
将筛选出的化合物10mm储液用培养基2倍梯度稀释成200μm-0.78μm9个浓度。
将96孔板中的细胞上清吸走后,加入50μl上述浓度的抑制剂,同时设置病毒对照和细胞对照。
加入抑制剂2h后,将influenza-(h1n1)-gluc病毒稀释30倍,加入50μl于96孔板中,37℃,5%co2培养24h。
取细胞上清30μl于白色酶标板中,加入30μl腔肠素,立刻于微孔板检测仪中读取数值,并用graphpadprism中作图计算ec50值,计算得到化合物的ec50为11.24μm,化合物af-1-24的ec50值见附图4。
(2)抗流感化合物细胞水平的抗流感病毒毒性检测
a)将抗流感化合物溶解在95%二甲基亚砜中,配制10mm储液,用培养基dmem+10%fbs+1%ps将上述化合物配制成100μm进行cc50细胞毒性测定。
b)将mdck细胞按照3×105个/ml接种于96孔板中,为防止培养基蒸发引起的边缘效应,96孔板外围加入200μlpbs缓冲液,37℃,5%co2培养18h后,每板可以测定两种化合物。将第一列100μl细胞中的培养基吸走,在96孔板的第2列bcd行3孔细胞中加入50μl100μm的第一种化合物,第三列bcd行3孔中同样加入50μl100μm的化合物,第四列bcd行3个孔同样加入50μl100μm的化合物,以此类推加到96孔板的第9列的3个孔,efg3行9列加入另一种化合物,第11列6个孔设为细胞对照。
c)细胞培养24h后,将孔内的培养液和药倒出,用pbs清洗2遍。每孔加入mtt溶液100ul。37℃,5%co2中孵育4h。加入100μldmso(100%)溶解结晶。10min后,结晶药物充分溶解,用酶联免疫检测仪(jk-mr-5033a,上海精学科学仪器有限公司)在492nm处测量各孔吸光值。并用graphpadprism作图计算cc50值,计算得到化合物af-1-24的cc50大于100μm。
同时以上市药物利巴韦林作为对照,按照测定化合物af-1-24的ec50的相同的方法测定利巴韦林的ec50为11μm,测试结果见附图5。
由以上数据可知,二羟基嘧啶类化合物对流感病毒活性有较好的抑制作用,能显著降低流感病毒的毒性,且细胞毒性较低,与上市药物利巴韦林的抑制效果相近,从而可以将这类化合物用于制备抗流感病毒药物。
为了清楚和易于理解的目的,通过举例说明和实施例详细地描述了上述发明。可以在附随的权利要求的范围内进行改变和修改,这对本领域的技术人员来说是很明显的。因此,可以理解,上面的说明书旨在用于说明而不是用于限制。因此,本发明的范围不应参考上述说明书来确定,而应当参照下面所附权利要求以及这些权利要求所享有的等同原则所确定的全部范围确定。
- 还没有人留言评论。精彩留言会获得点赞!