庚烯二酸二甲酯类化合物及其制备方法和应用与流程
本发明涉及医药领域,具体涉及庚烯二酸二甲酯类化合物及其制备方法和应用。
背景技术:
公开该背景技术部分的信息仅仅旨在增加对本发明的总体背景的理解,而不必然被视为承认或以任何形式暗示该信息构成已经成为本领域一般技术人员所公知的现有技术。
氧化应激是指高度活化的分子对dna、脂类或蛋白质造成损伤的细胞毒性过程。环境中各种氧化物和有毒物质,如空气和水污染、重金属、病原体、药物和电离辐射均可诱导氧化应激反应。其特点为胞内活性氧(ros)的增高,多种疾病如心脑血管疾病、糖尿病及其并发症、慢性阻塞性肺病、神经退行性疾病等均与细胞内过量的ros有关。nrf2(核因子e2相关因子2)信号通路是细胞内调节氧化还原平衡的主要信号通路,激活nrf2信号通路可以上调细胞内抗氧化蛋白和解毒酶的表达量,有效清除细胞内过量ros,nrf2信号通路一直被认为是细胞抵抗氧化损伤,重建氧化还原平衡,保持健康状态的核心通路。nrf2激动剂在糖尿病、心脑血管疾病等慢性病的防治方面确实发挥了积极作用。天然产物已成为nrf2激动剂发现的主要来源。
香青兰(dracocephalummoldavical.)是唇形科青兰属一年生草本植物,又名摩眼子、山薄荷、蓝秋花、玉米草等,为蒙古族和维吾尔族习用药,用于补脑安神,镇咳止喘,强心利尿。维医用于治疗冠心病及血液质旺盛(高血压)等疾病,几百余年的实践证明,疗效确切。其单方制剂“益心巴迪然吉布亚颗粒”治疗冠心病具有良好的疗效。香青兰主要分布于黑龙江、吉林、辽宁、内蒙古、甘肃、山西、青海、新疆等地区,新疆南部有栽培,药材资源丰富,已报道香青兰全草含有挥发油、萜类、黄酮类、氨基酸及微量元素等。但发明人发现,现阶段对香青兰全草的研究仍然有限。
技术实现要素:
本发明对香青兰地上全草进行了系统分离,提供了一种庚烯二酸二甲酯类化合物及其制备方法,以及提供了该类化合物在制备抗氧化的药物中的应用,以及在制备用于防护h2o2诱导的细胞氧化损伤的药物中应用,以及在制备诱导nrf2和/或其下游基因表达的药物或生化试剂中的应用。
具体地,本发明具有如下所述的技术方案:
在本发明的第一方面,本发明提供了一种庚烯二酸二甲酯类化合物,其具有式(x)所示结构:
其中,r选自-h或-or1;r1为h或
在本发明的实施方式中,所述庚烯二酸二甲酯类化合物选自以下结构:
其中,化合物i和ii互为异构体,化合物iv和v互为异构体。
其中,化合物ⅰ为(2e,4z)-6-羟基-4-(2-甲氧-2-氧代亚乙基)-庚-2-烯二酸二甲酯;化合物ii为(2z,4z)-6-羟基-4-(2-甲氧-2-氧代亚乙基)-庚-2-烯二酸二甲酯;化合物iii为(2e,4z,5z)-4-(2-甲氧-2-氧代亚乙基)-庚-2,5-二烯二酸二甲酯;化合物iv为(2e,4z)-6-o-阿魏酰基-4-(2-甲氧-2-氧代亚乙基)-庚-2-烯二酸二甲酯;化合物v为(2z,4z)-6--o-阿魏酰基-4-(2-甲氧-2-氧代亚乙基)-庚-2-烯二酸二甲酯。
在本发明的第二方面,本发明提供了制备上述庚烯二酸二甲酯类化合物的方法,其中,上述庚烯二酸二甲酯类化合物提取自香青兰,优选提取自香青兰地上全草。
在本发明的实施方式中,所述庚烯二酸二甲酯类化合物的制备方法包括:粉碎香青兰以乙醇回流提取得香青兰提取物;香青兰提取物以水混悬后经大孔树脂分离,得浓缩物后经柱色谱分离。
在本发明的一些实施方式中,所述庚烯二酸二甲酯类化合物的制备方法包括:粉碎香青兰地上全草,以20-95%乙醇回流提取至少一次,每次乙醇用量为待提取的香青兰地上全草质量的3-8倍,每次提取时间0.5-1.5小时,合并提取液后浓缩至干得香青兰提取物,加香青兰提取物质量0.5-1.5倍的水混悬,经大孔树脂分离,以水洗脱5-10个柱体积,后依次使用20%、40%、60%和95%乙醇洗脱,每次洗脱2-6个柱体积,合并40%乙醇洗脱液和60%乙醇洗脱液,浓缩后用硅胶柱色谱分离,用二氯甲烷/甲醇以体积比100:0-0:100依次洗脱,合并二氯甲烷/甲醇以100:10体积比洗脱的部分,浓缩至干,上样至sephadexlh-20柱,以100%甲醇洗脱,以硅胶薄层跟踪各洗脱部分,相同洗脱液合并,得到庚烯二酸二甲酯类化合物。
在本发明的一些实施方式中,所述庚烯二酸二甲酯类化合物的制备方法包括:取粉碎的香青兰地上全草,用60%的乙醇回流提取3次,每次乙醇的用量均为待提取的香青兰地上全草质量的5倍,每次提取时间为1小时,合并提取液后浓缩至干,得香青兰提取物,然后加等质量水混悬,经dm130大孔树脂分离,用水洗脱8个柱体积,后续依次用20%、40%、60%和95%乙醇洗脱,每种浓度乙醇均洗脱4个柱体积,将40%乙醇洗脱液和60%乙醇洗脱液合并,减压浓缩,浓缩物用硅胶柱色谱进一步分离,用体积比100:0-0:100的二氯甲烷:甲醇依次洗脱,硅胶薄层跟踪各洗脱部分,合并二氯甲烷:甲醇以体积比100:10的洗脱部分,浓缩至干,上样至sephadexlh-20柱,用100%甲醇洗脱,硅胶薄层跟踪各洗脱部分,相同洗脱液合并,分别得到庚烯二酸二甲酯类化合物ⅰ-ⅴ。
在本发明的第三方面,本发明提供了一种组合物或药物制剂,组合物或药物制剂包含本发明上述第一方面中所述的庚烯二酸二甲酯类化合物或其药学上可接受的盐,或者包含本发明上述第一方面中所述的庚烯二酸二甲酯类化合物的香青兰提取物或浓缩液,以及可以包括至少一种药学上可接受的辅料或载体。
在本发明的实施方式中,所述含有本发明上述第一方面中所述的庚烯二酸二甲酯类化合物的香青兰提取物或浓缩液可在本发明上述第二方面中所述的制备方法中获取,此处所述的提取液或浓缩液可以是分离了具体化合物的、也可以是同时含有本发明上述第一方面中所述的所有化合物的,即所述含有本发明上述第一方面中所述的庚烯二酸二甲酯类化合物的香青兰提取物或浓缩液可以同时含有本发明的化合物i-v中的一种或多种(比如二种、三种、四种或五种)。
本发明所述的药物组合物通常安全、无毒且为生物学上所需要的,因此,本发明中所述药学上可接受的载体或赋形剂是无毒且安全的,而且其与本发明所述化合物的组合也是无毒且安全的。本发明所述的药学上可接受的载体和赋形剂通常为本领域人员所熟知的,或者可由本领域技术人员根据实际情况能够确定的。
本发明化合物的药物组合物或药物制剂,本领域技术人员可根据实际情况有选择的以以下任意方式施与:口服、喷雾吸入、直肠给药、鼻腔给药、阴道给药、局部给药、非肠道给药如皮下、静脉、肌内、腹膜内、鞘内、心室内、胸骨内或颅内注射或输入,或借助一种外植的储器用药,其中优选口服、肌注、腹膜内或静脉内用药方式。
本发明化合物或含有这些化合物的药物组合物或药物制剂可以单位剂量形式给药。给药剂型可以是液体剂型、固体剂型。液体剂型可以是真溶液类、胶体类、微粒剂型、乳剂剂型、混旋剂型。其他剂型例如片剂、胶囊、滴丸、气雾剂、丸剂、粉剂、溶液剂、混悬剂、乳剂、颗粒剂、栓剂、冻干粉针剂、包合物、填埋剂、贴剂、擦剂等。
本发明的药物组合或药物制剂中还可以含有常用的载体,这里所述可药用载体包括但不局限于:离子交换剂,氧化铝,硬脂酸铝,卵磷脂,血清蛋白如人血清蛋白,缓冲物质如磷酸盐,甘油,山梨酯,山梨酸钾,饱和植物脂肪酸的部分甘油酯混合物,水,盐或电解质如硫酸鱼精蛋白,磷酸氢二钠,磷酸氢钾,氯化钠,锌盐,胶态氧化硅,三硅酸镁,聚乙烯吡咯烷酮,纤维素物质,聚乙二醇,羧甲基纤维素钠,聚丙烯酸酯,蜂蜡,羊毛酯等。载体在药物组合物中的含量可以是1重量%-98重量%,通常大约占到80重量%。为方便起见,局部麻醉剂,防腐剂,缓冲剂等可直接溶于载体中。
口服片剂和胶囊可以含有赋形剂如粘合剂,如糖浆,阿拉伯胶,山梨醇,黄芪胶,或聚乙烯吡咯烷酮,填充剂,如乳糖,蔗糖,玉米淀粉,磷酸钙,山梨醇,氨基乙酸,润滑剂,如硬脂酸镁,滑石,聚乙二醇,硅土,崩解剂,如马铃薯淀粉,或可接受的增润剂,如月桂醇钠硫酸盐。片剂可以用制药学上公知的方法包衣。
口服液可以制成水和油的悬浮液,溶液,乳浊液,糖浆,也可以制成干品,用前补充水或其它合适的媒质。这种液体制剂可以包含常规的添加剂,如悬浮剂,山梨醇,纤维素甲醚,葡萄糖糖浆,凝胶,羟乙基纤维素,羧甲基纤维素,硬脂酸铝凝胶,氢化的食用油脂,乳化剂,如卵磷脂,山梨聚糖单油酸盐,阿拉伯树胶;或非水载体(可能包含可食用油),如杏仁油,油脂如甘油,乙二醇,或乙醇;防腐剂,如对羟基苯甲酸甲酯或丙酯,山梨酸。如需要可添加调味剂或着色剂。
栓剂可包含常规的栓剂基质,如可可黄油或其它甘油酯。
对于胃肠外投药,液态剂型通常由化合物和一种消毒的载体制成。载体首选水。依照所选载体和药物浓度的不同,化合物既可溶于载体中也可制成悬浮溶液,在制成注射用溶液时先将化合物溶于水中,过滤消毒后装入封口瓶或安瓿中。
必须认识到,本发明化合物的最佳给药剂量和间隔是由化合物性质和诸如给药的形式、路径和不为以及所治疗的特定哺乳动物等外部条件决定的,而这一最佳给药剂量可用常规的技术确定。同时也必须认识到,最佳的疗程,即同时化合物在额定的时间内每日的剂量,可用本领域内公知的方法确定。
在本发明的第四方面,本发明还提供了上述第一方面中所述的庚烯二酸二甲酯类化合物或其药学上可接受的盐,或者包含上述庚烯二酸二甲酯类化合物的香青兰提取物或浓缩液,或者上述第三方面中所述的组合物或药物制剂在制备抗氧化的药物中的应用。
以及,本发明还提供了上述第一方面中所述的庚烯二酸二甲酯类化合物或其药学上可接受的盐,或者包含上述庚烯二酸二甲酯类化合物的香青兰提取物或浓缩液,或者上述第三方面中所述的组合物或药物制剂在制备用于防护h2o2诱导的细胞氧化损伤的药物中应用;优选地,所述细胞为beas-2b细胞。
以及,本发明还提供了上述第一方面中所述的庚烯二酸二甲酯类化合物或其药学上可接受的盐,或者包含上述庚烯二酸二甲酯类化合物的香青兰提取物或浓缩液,或者上述第三方面中所述的组合物或药物制剂在制备诱导nrf2和/或其下游基因表达的药物或生化试剂中的应用;优选地,所述nrf2下游基因选自nqo1和gclm。
以及,本发明还提供了上述第一方面中所述的庚烯二酸二甲酯类化合物或其药学上可接受的盐,或者包含上述庚烯二酸二甲酯类化合物的香青兰提取物或浓缩液,或者上述第三方面中所述的组合物或药物制剂在制备nrf2信号通路激动剂药物或生化试剂中的应用。
在本发明的实施方式中,本发明所述的化合物i、ii、iii、iv、v能够诱导nrf2及下游基因nqo1和gclm的表达。在本发明的一些实施方式中,本发明化合物i-v诱导nrf2及下游基因nqo1和gclm表达的作用在0-50μm的浓度下呈浓度依赖性,随着化合物浓度的升高,nrf2及下游基因nqo1和gclm的表达量逐渐升高,尤其在12.5-50μm的浓度下,这种诱导表达作用对浓度的依赖性最为明显,nrf2及下游基因nqo1和gclm的表达量的提升显著,在25-50μm的浓度下,nrf2及下游基因nqo1和gclm的表达量仍有提升,但在该浓度范围下,随浓度的增长,表达量对浓度的依赖性趋缓,表达量的增长速度减慢。
在本发明的实施方式中,本发明的化合物i、ii、iii、iv、v表现出对h2o2引起的细胞损伤的保护作用。在一些实施方式中,本发明的化合物i-v在不低于25μm的浓度下对200μmh2o2引起的细胞损伤表现出保护作用,尤其化合物ii和化合物v的保护作用更强。
附图说明
构成本申请的一部分的说明书附图用来提供对本申请的进一步理解,本申请的示意性实施例及其说明用于解释本申请,并不构成对本申请的不当限定。以下,结合附图来详细说明本发明的实施方案,其中:
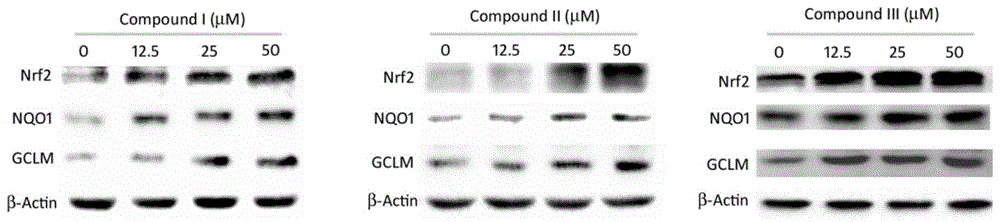
图1示出了实施例2中化合物i-iii诱导nrf2及下游基因nqo1和gclm的表达情况。
图2示出了实施例2中化合物iv和v诱导nrf2及下游基因nqo1和gclm的表达情况。
图3示出了实施例3中化合物i-v对h2o2引起的细胞损伤的保护作用。
具体实施方式
下面结合具体实施例,进一步阐述本发明。应理解,这些实施例仅用于说明本发明而不用于限制本发明的范围。下列实施例中未注明具体条件的实验方法,通常按照常规条件或按照制造厂商所建议的条件。
除非另行定义,文中所使用的所有专业与科学用语与本领域熟练人员所熟悉的意义相同。本发明所使用的试剂或原料均可通过常规途径购买获得,如无特殊说明,本发明所使用的试剂或原料均按照本领域常规方式使用或者按照产品说明书使用。此外,任何与所记载内容相似或均等的方法及材料皆可应用于本发明方法中。文中所述的较佳实施方法与材料仅作示范之用。
实施例1庚烯二酸二甲酯类化合物ⅰ-ⅴ的制备
称取粉碎的香青兰地上全草1000g,用60%的乙醇回流提取3次,每次乙醇的用量均为5000g,每次提取时间为1小时,合并提取液后浓缩至干,得香青兰提取物200g,然后加水200g混悬,经dm130大孔树脂分离,用水洗脱8个柱体积,后续依次用20%、40%、60%和95%乙醇洗脱,均洗脱4个柱体积,将40%和60%洗脱液合并,减压浓缩,浓缩物用硅胶柱色谱进一步分离,用体积比100:0-0:100的二氯甲烷:甲醇依次洗脱,硅胶薄层跟踪各洗脱部分,二氯甲烷:甲醇为100:10洗脱部分合并,浓缩至干,上样至sephadexlh-20柱,用100%甲醇洗脱,硅胶薄层跟踪各洗脱部分,相同洗脱液合并,分别得到化合物i、ii、iii、iv、v。其1hnmr和13cnmr数据如表1、2所示。
表1化合物i-iii的1hnmr(600mhz)和13cnmr(150mhz)数据
a在cdcl3中测定b在cd3od中测定
表2化合物iv和v的1hnmr(600mhz)和13cnmr(150mhz)数据
化合物ⅰ-ⅴ的波谱数据如下:
化合物ⅰ:灰黄色无定形粉末;
化合物ⅱ:灰黄色无定形粉末;
化合物ⅲ:灰黄色油状物;uv(meoh)λmax(logε)280(3.00),220(1.40)nm;ir(kbr)νmax2954,1725,1436,1173cm–1;1hand13cnmr见表1;hresimsm/z255.0863[m+h]+(calcd.forc12h15o6,255.0869).
化合物ⅳ:灰黄色油状物;
化合物ⅴ:灰黄色油状物;
实施例1制得的化合物ⅰ-ⅴ用作实施例2和3的样品。
实施例2:本发明的化合物诱导nrf2及其下游基因的表达
实验材料:人肺上皮beas-2b细胞株购自美国atcc;nrf2、nqo1、gclm和β-actin抗体购自santacruz公司;
实验方法:(1)细胞处理:细胞以1×106个细胞每孔的密度接种于6孔板,加化合物ⅰ-ⅲ的dmso溶液处理16小时。(2)细胞裂解:细胞处理完成后,以预冷的pbs洗两次除去残留药物,加入sds细胞裂解液100μl/孔,细胞刮刀收集细胞裂解液,煮沸3分钟,超声。(3)westernblot:采用聚丙烯酰胺凝胶电泳,转膜至硝酸纤维素薄膜,5%脱脂牛奶封闭1小时,1:1000加入一抗室温孵育2小时,洗3次,每次20分钟,加二抗1:5000室温孵育2小时,洗3次,每次20分钟,化学发光检测蛋白条带。
实验结果:当化合物i-v的浓度大于0时,细胞株nrf2及下游基因nqo1和gclm表达水平开始增加,本发明的化合物i-v表现出对nrf2及下游基因nqo1和gclm表达的诱导作用。并且本实施例的结果还发现,在0-50μm的浓度下,化合物i-v对于所述细胞株nrf2及下游基因nqo1和gclm表达水平均呈剂量依赖性诱导作用,特别是在12.5-50μm的浓度下,表达量的提升尤为显著,当化合物浓度在25-50μm时,这种表达水平的提升趋缓,如图1、图2所示。
实施例3:本发明的化合物对h2o2引起的细胞损伤的保护作用
beas-2b细胞以每孔10000的密度接种于96孔板,生长过夜后,将细胞分为5个处理组,对照组、h2o2处理组、h2o2加化合物ⅰ处理组、h2o2加化合物ⅱ处理组和h2o2加化合物ⅲ处理组,h2o2的浓度采用200μm,化合物i-v均采用25μm。细胞加化合物i-v预处理4小时后,加入200μmh2o2共培养24小时,每孔加入5mg/mlmtt溶液10μl,继续孵育4小时,之后,细胞用dmso溶液裂解,在570nm读取吸光度。每个处理组均设3个重复孔,实验进行3次重复。
实验结果:化合物i-v对h2o2引起的细胞损伤均表现出保护作用,其中,相同作用浓度下,化合物ii和化合物v的保护作用更强,结果如图3所示。
以上所述仅为本发明的优选实施例而已,并不用于限制本发明,尽管参照前述实施例对本发明进行了详细的说明,对于本领域的技术人员来说,其依然可以对前述各实施例所记载的技术方案进行修改,或者对其中部分技术特征进行等同替换。凡在本发明的精神和原则之内,所作的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!